Как из ацетилена получить воду – Урок №19. Получение и применение ацетилена.
alexxlab | 30.10.2019 | 0 | Разное
Ацетилен получение – Справочник химика 21
Опубликована работа [126] по сравнительной оценке различных методов производства ацетилена. Авторы этой работы на основании анализа большого фактического зарубежного и отечественного материала подвергают сомнению правильность вывода о том, что карбидный метод производства ацетилена по экономическим показателям уступает методам производства ацетилена из углеводородного сырья. На основании данных предприятий, действующих в СССР, авторы делают заключение, что по всем показателям (капиталовложения, себестоимость и энергозатраты) ацетилен, полученный окислительным пиролизом природного газа и особенно электрокрекингом, уступает ацетилену, полученному из карбида кальция (табл. V. 10). [c.169]Ацетилен, полученный нз 200 г карбида с массовой долей примесей 20%, вовлекли в реакцию гидратации. Какая масса уксусного альдегида образовалась, если массовая доля выхода ацетилена составила 75% от теоретического Ответ. 82,5 г.
В качестве флегматизаторов иногда используют и горючие вещества. В частности, ацетилен, полученный электрокрекингом метана или высокотемпературным пиролизом углеводородных газов, содержит примеси метана, пропана, бутана и других углеводородов, которые являются хорошими флегматизаторами и препятствуют термическому разложению и взрывному распаду ацетилена более эффективно, чем, например, азот. Ацетилен, флегматизированный данными углеводородами, можно сжимать до высоких давлений и нагревать до высоких температур, не опасаясь его разложения и взрыва. [c.45]
При рациональном использовании побочных продуктов ацетилен, полученный из углеводородных газов, будет дешевле карбидного. [c.275]
Рассчитайте массу бромной воды (массовая доля Вга 3,2%), которая обесцвечивается ацетиленом, полученным из карбида кальция массой 40 г. Карбид содержит посторонние примеси, массовая доля которых равна 4%, [c.180]
По некоторым данным, самой низкой себестоимостью обладает ацетилен, полученный путем частичного сжигания метана в случае [c.116]
Ацетилен, полученный из карбида кальция, подвергли гидратации и получили 176 г ацетальдегида. Сколько граммов карбида потребовалось для этого, если содержание примесей в нем составляет 25% Ответ. 341,33 г. [c.338]
Ацетилен, полученный в результате окислительного пиролиза метана, используется для производства различных ценных веществ ацетальдегида (стр. 136), винилацетата (стр. 163), хлористого винила (стр. 89), акрилонитрила (стр. 175). [c.72]
Содержание (в мг м ) примесей в ацетилене, полученном из карбида, до и после очистки [c.204]
Катализатор может дезактивироваться вследствие того, что образующийся ацетальдегид восстанавливает двухвалентную ртуть до одновалентной, а затем и до металлической, окисляясь до уксусной кислоты. Дезактивацию катализатора ускоряют также примеси, содержащиеся в ацетилене, полученном карбидным методом (НаЗ, РН3, АзИд, N1-13 и т. д.). Для предотвращения этого явления (и снижения выхода побочных продуктов) образующийся ацетальдегид отдувают из реакционного объема ацетиленом, подаваемым в некотором избытке. Кроме того, ацетилен тщательно очищают от примесей и в реакционную массу вводят окислители (соли трехвалентного железа, марганца и т. д.), регенерирующие активную форму катализатора
Этиловый спирт брожения или ацетилен, полученный из карбида кальция (1900—1910 гг.) [c.25]
Ацетилен, полученный из 200 г карбида с массовой долей примесей 20%, вовлекли в реакцию гидратации. Какая масса [c.309]
Образование амидов из кислот и аминов с помощью алкокси ацетиленов получение пептидов. Описано применение алкокси-ацетиленов для превращения смесей кислот и аминов в амиды [20]. [c.164]
Гидратация ацетилена в ацетальдегид (ацетилен, полученный из карбида кальция, не содержащий сернистых и фосфористых соединений) можно употреблять большой избыток ацетилена и поддерживать достаточно высокую температуру серной кислоты во избежание полимеризации образовавшегося ацетальдегида он должен удаляться из сферы действия серной кислоты гидратация ацетилена в газовой фазе водяным паром при высокой температуре не находит широкого применения [c.120]
Разработан метод определения сероводорода в ацетилене, полученном из карбида [673]. Смесь, содержащую также Nj, Н3Р, АзНз и другие компоненты, хроматографируют на колонке с 3% трикрезилфосфата на хромосорбе, газ-носитель — водород или гелий, температура 30° С применяют пламенно-ионизационный детектор. [c.148]
В 1939 г. опубликована работа [22] по исследованию микро-приМесей, находящихся в ацетилене, полученном карбидным способом. Оказалось, что около 95% всех серосодержащих продуктов, выделенных из ацетилена при низкой температуре,, приходится на ДВС. Содержание ДВС зависит от температуры гашения карбида и колеблется от 100—270 мг/м (мокрый генератор, 100°) до 1000—2700 мг/м (сухой генератор, 60—70 [23]). Появление две в ацетилене можно, вероятно, связать с присутствием примеси сульфида кальция в техническом карбиде [24, 25],
Ключевым соединением также является карбид бария и симметрично меченый ацетилен, полученный на его основе. [c.137]
Ацетилен, полученный из природного газа. [c.313]
Ацетилен, полученный из карбида кальция, всегда содержит ядовитые примеси сероводород и фосфористый водород. Поэтому все опыты с ацетиленом нужно проводить в вытяжном шкафу. [c.88]
Ацетилен, полученный из карбида, дороже этилена, полученного в качестве побочного продукта при крекинге мазута или средних масел однако ацетилен, полученный при пиролизе метана или остаточных заводских газов, в отдельных случаях может быть дешевле. [c.391]
Плазмохимический реактор рассматривается нами как объект автоматического управления. Известно, что для описания объекта автоматического управления необходимо установить связи между его выходами и входами. Эти связи для плазмохимического реактора можно выявить, воспользовавшись математической моделью процесса конверсии метана в ацетилен, полученной в работе [15]. В этой работе была рассмотрена следующая система обыкновенных нелинейных дифференциальных уравнений первого порядка, которая в определенных приближениях моделирует плазмохимический процесс конверсии метана в ацетилен в водородной плазменной струе [c.53]
Ацетилен, полученный из карбида, имеет ч
www.chem21.info
химические свойства, получение, применение, меры предосторожности
Ацетилен (или по международной номенклатуре – этин) – это непредельный углеводород, принадлежащий к классу алкинов. Химическая формула ацетилена – C2h3. Атомы углерода в молекуле соединены тройной связью. Он является первым в своем гомологическом ряду. Представляет собой бесцветный газ. Очень огнеопасен.
Получение
Все методы промышленного получения ацетилена сходятся к двум типам: гидролиз карбида кальция и пиролиз различных углеводородов. Последний требует меньших энергозатрат, но чистота продукта довольно низкая. У карбидного метода – наоборот.
Суть пиролиза заключается в том, что метан, этан или другой легкий углеводород при нагреве до высоких температур (от 1000 °C) превращается в ацетилен с выделением водорода. Нагрев может осуществятся электрическим разрядом, плазмой или сжиганием части сырья. Но проблема состоит в том, что в результате реакции пиролиза может образовываться не только ацетилен, но и еще множество разных продуктов, от которых необходимо впоследствии избавляться.
2Ch5 → C2h3 + 3h3
Карбидный метод основан на реакции взаимодействия карбида кальция с водой. Карбид кальция получают из его оксида, сплавляя с коксом в электропечах. Отсюда и такой высокий расход энергии. Зато чистота ацетилена, получаемого таким способом, крайне высока (99,9 %).
CaC2 + h3O → C2h3 + Ca(OH)2
В лаборатории ацетилен также можно получить дегидрогалогенированием дигалогенпроизводных алканов с помощью спиртового раствора щелочи.
Ch3Cl-Ch3Cl + 2KOH → C2h3 + 2KCl + 2h3O
Физические свойства ацетилена
Ацетилен – это газ без цвета и запаха. Хотя примеси могут давать ему чесночный запах. Практически не растворим в воде, немного растворим в ацетоне. При температуре -83,8 °C сжижается.
Химические свойства ацетилена
Исходя из тройной связи ацетилена, для него будут характерны реакции присоединения и реакции полимеризации. Атомы водорода в молекуле ацетилена могут замещаться другими атомами или группами. Поэтому можно сказать, что ацетилен проявляет кислотные свойства. Разберем химические свойства ацетилена на конкретных реакциях.
Реакции присоединения:
- Гидрирование. Осуществляется при высокой температуре и в присутствии катализатора (Ni, Pt, Pd). На палладиевом катализаторе возможно неполное гидрирование.
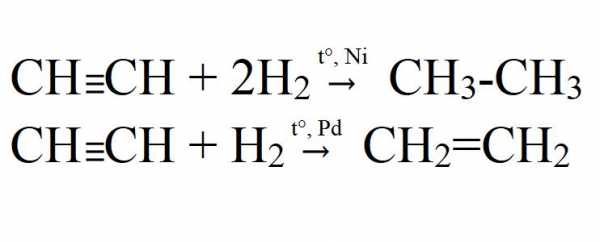
- Галогенирование. Может быть как частичным, так и полным. Идет легко даже без катализаторов или нагревания. На свету хлорирование идет с взрывом. При этом ацетилен полностью распадается до углерода.
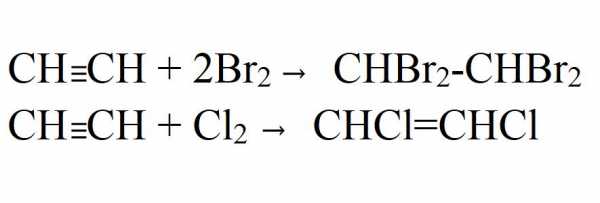
- Присоединение к уксусной кислоте и этиловому спирту. Реакции идут только в присутствии катализаторов.
- Присоединение синильной кислоты.
CH≡CH + HCN → Ch3=CH-CN
Реакции замещения:
- Взаимодействие ацетилена с металл-органическими соединениями.
CH≡CH + 2C2H5MgBr → 2C2H6 + BrMgC≡CMgBr
- Взаимодействие с металлическим натрием. Необходима температура 150 °C или предварительное растворение натрия в аммиаке.
2CH≡CH + 2Na → 2CH≡CNa + h3
- Взаимодействие с комплексными солями меди и серебра.
- Взаимодействие с амидом натрия.
CH≡CH + 2NaNh3 → NaC≡CNa + 2Nh4
Реакции полимеризации:
- Димеризация. При этой реакции две молекулы ацетилена объединяются в одну. Необходим катализатор – соль одновалентной меди.
- Тримеризация. В этой реакции три молекулы ацетилена образуют бензол. Необходим нагрев до 70 °C, давление и катализатор.
- Тетрамеризация. В результате реакции получается восьмичленный цикл – циклооктатетраен. Для этой реакции также требуется небольшой нагрев, давление и соответствующий катализатор. Обычно это комплексные соединения двухвалентного никеля.
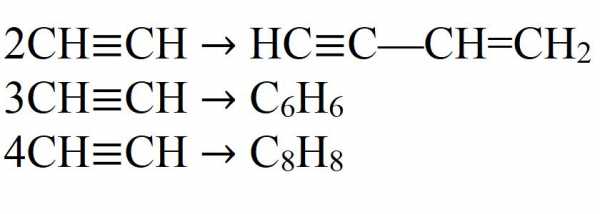
Это далеко не все химические свойства ацетилена.
Применение
Структурная формула ацетилена указывает нам на довольно прочную связь между атомами углерода. При ее разрыве, например при горении, выделяется очень много энергии. По этой причине ацетиленовое пламя обладает рекордно высокой температурой – около 4000 °C. Его используют в горелках для сварки и резки металла, а также в ракетных двигателях.
Пламя горения ацетилена имеет также очень высокую яркость, поэтому его часто используют в осветительных приборах. Используется он и во взрывотехнике. Правда, там применяется не сам ацетилен, а его соли.
Как видно из разнообразных химический свойств, ацетилен может применяться как сырье для синтеза других важных веществ: растворителей, лаков, полимеров, синтетических волокон, пластмасс, органического стекла, взрывчатых веществ и уксусной кислоты.
Безопасность
Как уже говорилось, ацетилен – огнеопасное вещество. С кислородом или воздухом он способен образовывать крайне легковоспламеняющиеся смеси. Чтобы вызвать взрыв, достаточно одной искры от статического электричества, нагрева до 500 °C или небольшого давления. При температуре 335 °C чистый ацетилен самовоспламеняется.
Из-за этого ацетилен хранят в баллонах под давлением, которые наполнены пористым веществом (пемза, активированный уголь, асбест). Таким образом, ацетилен распределяется по порам, уменьшая риск взрыва. Часто эти поры пропитывают ацетоном, из-за чего образуется раствор ацетилена. Иногда ацетилен разбавляют другими, более инертными газами (азот, метан, пропан).
Этот газ обладает и токсичным действием. При его вдыхании начнется интоксикация организма. Признаками отравления являются тошнота, рвота, шум в ушах, головокружение. Большие концентрации могут приводить даже к потере сознания.
www.nastroy.net
Ацетилен Этим способы получения – Справочник химика 21
Гидратация ацетиленов. Ацетилен и его гомологи при действии воды в присутствии катализатора (солей двухвалентной ртути) превращаются Б оксосоединения. При этом только ацетилен образует альдегид, а именно ацетальдегид (реакция Кучерова). Этот способ является одним из главных промышленных способов получения ацетальдегида [c.135] Сырьем для производства аммиака является смесь азота и водо рода. Эту смесь получают разными способами. Наиболее распространенные из них газификация твердого и жидкого топлив с последующей конверсией окиси углерода, конверсия метана и других углеводородных газов, комплексная переработка природного газа в ацетилен и синтез-газ, фракционное разделение горючих газов, в частности коксового, методом глубокого охлаждения, разделение воздуха на азот и кислород с применением для этого глубокого холода и электрохимический способ получения водорода и кислорода.
Кроме этого способа получения спирта, в настоящее время разработаны и другие промышленные методы. Одним из них является получение винного спирта из ацетилена. Сущность метода заключается в том, что ацетилен, получаемый действием воды на карбид кальция, пропускают через воду, в которой растворено немного ртутных солей (катализатор). В результате в воде образуется ацетальдегид по равенству [c.300]
Не умаляя большого практического значения способов получения молекулярного водорода методом конверсии водяным паром и двуокисью углерода и мономолекулярной дегидрогенизацией на активных катализаторах, следует отметить, что способ, связанный с получением водорода в результате полимолекулярных превращений углеводородов в настоящее время представляется все более и более перспективным. Это связано с тем, что водород получают здесь наряду с другими целевыми продуктами, в том числе с такими продуктами крупнотоннажного производства, как термическая сажа, пирографит и др., вместе с ароматическими углеводородами, ацетиленом и Т. д. Основным сырьем для получения водорода по этому способу может служить метан, являющийся главным компонентом природного газа, а также другие газообразные, жидкие и твердые парафиновые углеводороды, входящие в состав нефтей, т. е. все то же природное сырье, проблема рациональной переработки которого еще не решена полностью. Поэтому последнее обстоятельство делает любые работы, связанные с исследованием полимолекулярной дегидрогенизации углеводородов в ходе их поликонденсации при кок-сообразовании, весьма актуальными. [c.164]
Выбор способа очистки диацетилена зависит от метода получения и цели его использования. Диацетилен, образующийся при пиролизе природного газа, достаточно хорошо очищается с помощью низкотемпературной перегонки. Этим способом очистки пользуются как в лабораторной, так и промышленной практике. Очищенный таким образом диацетилен обладает степенью-чистоты, требуемой при физико-химических исследованиях [Ю] Этим же способом пользуется в промышленности для выделения диацетилена и винилацетилена из смеси их с ацетиленом 150]. ]Метод селективного растворения для выделения ацетилена, его-гомологов и диацетилена из газовой смеси [50, 62, 63] в настоящее время широко применяется на заводах. В качестве растворителей для этого используются метанол, диметилформамид, N-ме-тилпирролидон, ацетон, керосиновые фракции нефти и др. При этом, однако, необходимо учитывать возможность взаимодействия диацетилена с растворителем, как это имеет место в случае К-метилпирролидона-2 [382—384]. При пропускании диацетилена через N метилпирролидон-2 при охлаждении образуется устойчивый кристаллический комплекс, в котором молекулярное-отношение диацетилена к метилпцрролидону равно 1 1. Этот комплекс при нагревании до 30 50° С распадается с образованием диацетилена, что было использовано для выделения его в чистом виде из смеси с моноацетиленами. Так, исходная газовая смесь, полученная при электродуговом крекинге углеводородов, содержала ацетилена — 38,4 мол. %, метилацетилена — 16,4 мол. % и диацетилена — 45,1 мол.%. После пропускания этой смеси через К-метилпирролидоп-2 при 0° С до образования кристаллов отходящий газ имел следующий состав ацетилена — 55,7 мол.%, метилацетилена —42,2 мол.7о и диацетилена — 2,1 од.7о- При нагревании кристаллического комплекса до 40″ С образуется газ, содержащий 96,1 мол. % диацетилена. Повторная обработка дает совершенно чистый диацетилен. [c.57]
Полученный этим способом ацетилен имеет неприятный запах, сообщаемый ему примесями в техническом карбиде кальция. Чистый ацетилен почти без запаха. [c.204]
Ход урока. Учитель, указав на два способа получения ацетилена — карбидный и из природного газа, рассматривает первый способ, обращая внимание на экономическую сторону. Затем отмечает, что ацетилен, получаемый из природного газа, дешевле ацетилена, получаемого по карбидному способу. Почему На этот вопрос отвечают сами учащиеся. После этого учитель предлагает им самостоятельно разобраться в получении ацетилена вторым способом. [c.170]
Промышленный катализ тоже не обходится без соединений ртути. Один из способов получения уксусной кислоты и этилового спирта основан на реакции, открытой русским ученым М. Г. Кучеровым. Сырьем служит ацетилен. В присутствии катализаторов — солей двухвалентной ртути — он реагирует с водяным паром и превраш а-ется в уксусный альдегид. Окисляя это вещество, получа- ют уксусную кислоту, восстанавливая — спирт. Те н е соли помогают получать из нафталина фталевую кислоту — важный продукт основного органического синтеза. [c.247]
Исходным сырьем для получения уксусной кислоты по этому способу фактически являются уголь (С) и известь (СаО), так как из них в электрических печах получают карбид кальция ( aQ), а из последнего действием воды — необходимый для синтеза уксусной кислоты ацетилен. Этим способом в настоящее время получают основное количество уксусной кислоты. [c.165]
Органические вещества при действии жара обыкновенно дают ацетилен. Так, если пары обыкновенного спирта пропускать чрез накаленную трубку, то получается С Н в значительном количестве. Если из пламени свечи вытянуть аспиратором воздух, то там открывается ацетилен. Если светильный газ зажечь так, чтобы он горел в нижней части горелки, получается та ше ацетилен. Он образуется также чрез непосредственное соединение углерода и водорода так, если будем пропускать чрез два угля, помещенных в пространстве, наполненном водородом, гальванический ток, то при этом образуется светящаяся дуга, которая происходит от раскаленных частей угля. Эти частицы способны соединяться с водородом, причем образуется один только продукт С № уголь при этом как бы горит в водороде. Все эти способы получения ацетилена при действии жара показывают, что он есть продукт весьма прочный и, кроме последнего случая получения, всегда смешан с другими углеродистыми водородами. Чтобы получить ацетилен в отдельности, пользуются его способностью соединяться даже с металлами и металлическими солями. Так, если взять раствор азотносеребряной соли в аммиаке, то из ацетилена, смешан[ного] с друг[ими] продукт[ами], выделяется гремучий порошок ( Ag ), который, растворяясь в соляной кислоте, отделяет газ состава С Н . [c.374]
План развития народного хозяйства в СССР предусматривает значительное увеличение производства ацетилена в ближайшие годы, главным образом за счет применения методов, основанных на использовании углеводородного сырья. В качестве побочных продуктов при этом способе получения ацетилена образуется ряд так называемых высших ацетиленов , это главным образом, диацетилен, винилацетилен и метилацетилен. При этом количество диацетилена оказывается в 1,5—2 раза большим, чем количество винилацетилена и метилацетилена вместе взятых. [c.7]
Наиболее распространены акриловые реагенты, получаемые гидролизом полиакрилонптрила или полиакриламида — продуктов полимеризации нитрила акриловой кислоты. Промышленное значение имеют три способа получения этого мономера дегидратация этиленциангидрина, получаемого- взаимодействием окиси этилена с синильной кислотой (стадии / и // на рис. 34) присоединение синильной кислоты к ацетилену в присутствии катализатора и совместно
www.chem21.info
С2Н2 ацетилен. Свойства ацетилена. Получение ацетилена.
С2Н2 ацетилен. Свойства ацетилена. Получение ацетилена. 4.88/5 (97.50%) проголосовало 8
Свойства ацетилена.
В качестве горючего газа при кислородной резке наибольшее распространение получил ацетилен, который является химическим соединением углерода с водородом (С2Н2). При нормальных температуре и давлении ацетилен находится в газообразном состоянии.Химически чистый ацетилен является бесцветным газом со слабым эфирным запахом и слегка сладковатым вкусом. Технический ацетилен, применяемый для кислородной резки, вследствие присутствия в нем некоторых примесей (сероводорода, аммиака, фосфористого водорода и др.) отличается резким неприятным запахом и является вредным для организма человека.
При давлении свыше 2 кг/см2 ацетилен в больших объемах приобретает свойства взрывчатого газа и при соприкосновении с накаленной поверхностью или от электрической искры взрывается, при этом температура достигает 3000°С, а давление увеличивается более чем в 10 раз.
С кислородом и воздухом ацетилен образует взрывоопасные смеси, которые от огня взрываются. Ацетилено — воздушная смесь является взрывоопасной при наличии от 2,3 до 81% ацетилена в воздухе. Еще более опасной является ацетилено — кислородная смесь, которая от огня взрывается при содержании в кислороде от 2,3 до 93% ацетилена, при этом скорость распространения взрывной волны достигает 3000 м/сек, поэтому особенно тщательно нужно следить за плотностью всех ацетиленовых приборов, трубопроводов и пр.
Также читайте: Какие свойства кислорода. Вес 1 м3 кислорода. Вес жидкого кислорода. Способы получения кислорода.
Взрывчатость ацетилена сильно понижается при размещении его в капиллярных (очень тонких) каналах. Этим свойством ацетилена пользуются при наполнении баллонов под давлением — ацетиленовые баллоны заполняют специальной пористой массой.
Реакция ацетилена с ацетоном.
Ацетилен хорошо растворяется во многих жидкостях, особенно в ацетоне. В одном объеме ацетона при 15°С и нормальном давлении растворяется 23 объема ацетилена, а при повышенном давлении — пропорционально больше. Это свойство ацетилена также используют при наполнении баллонов. Растворимость ацетилена в ацетоне в значительной степени зависит от температуры: с повышением температуры растворимость уменьшается, а с понижением резко возрастает.
Способность растворенного ацетилена к взрыву понижается.
Реакция сгорания ацетилена.
Ацетилен при сгорании в смеси с чистым кислородом дает пламя с температурой 3050 — 3150°С, а при сгорании в смеси с воздухом 2350°С.
Полное сгорание ацетилена.
Для полного сгорания 1 м3 ацетилена требуется 2,5 м3 кислорода или 12,5 м3 воздуха.
Ацетилен легче кислорода и воздуха. Удельный вес ацетилена при 0°С и 760 мм рт. ст. 1,17 кг/м3.
При длительном взаимодействии с красной медью и серебром ацетилен дает соединения, которые при нагревании или при сильном ударе взрываются. Поэтому при изготовлении ацетиленовой аппаратуры и арматуры запрещено применение серебряных припоев и красной меди в чистом виде. Допускаются лишь технические медные сплавы, содержащие не более 70% меди.
Получение ацетилена.
Основным промышленным способом получения ацетилена является разложение карбида кальция водой. Карбид кальция представляет собой химическое соединение кальция с углеродом (СаС2) и является твердым веществом темно-серого или серого цвета.
Технический карбид кальция получается сплавлением негашеной извести с углем (коксом или антрацитом). Шихта, состоящая из смеси угля и извести в определенной пропорции, погружается в электрическую дуговую печь, где под влиянием тепла электрической дуги расплавляется с образованием карбида кальция.
Расплавленный карбид выливают из печи в формы — изложницы, в которых он застывает. Застывший карбид кальция затем дробят, сортируют на куски определенных размеров и упаковывают в специальные барабаны для хранения и транспортировки. Барабаны для упаковки карбида кальция делают из листового железа толщиной не менее 0,5—0,6 мм с герметически закрывающейся крышкой. На цилиндрической поверхности барабанов для повышения их прочности накатаны гофры. Барабан вмещает 50— 130 кг карбида кальция.
Карбидные барабаны следует открывать очень осторожно, так как по тем или иным причинам внутрь барабана может проникнуть влага и образоваться взрывоопасная ацетилено-воздушная смесь. Лучше всего покрыть крышку барабана слоем тавота и снимать ее специальным ножом. Ни в коем случае нельзя прибегать к ударам молотка.
Категорически запрещается при раскупорке карбидных барабанов применять пламя или же вырубать крышку барабана зубилом.
Разложение ацетилена.
При действии воды карбид кальция разлагается, образуя ацетилен и гашеную известь. Реакция протекает по уравнению
CaC2 + 2H2O = C2H2 + Ca(OH)2
и сопровождается значительным выделением тепла.
Карбид кальция при соприкосновении с атмосферным воздухом, содержащим пары воды, разлагается с выделением ацетилена. Из 1 кг карбида кальция обычно получается от 230 до 300 л ацетилена.
Для разложения 1 кг карбида кальция теоретически требуется 0,56 л воды. Реакция разложения карбида протекает с выделением большого количества тепла, поэтому недостаток воды может привести к значительному перегреву и даже воспламенению ацетилена в месте разложения карбида. Во избежание этого процесс разложения карбида ведут всегда с избыточным количеством воды, которая используется для охлаждения. Практически на 1 кг карбида кальция берется от 5 до 20 л воды.
Статья оказалась полезной?! Поделись с друзьями в социальных сетях!!!
mechanicinfo.ru
Получение ацетилена из карбида и его очистка
Основными недостатками карбидного метода получения ацетилена являются большой расход электроэнергии при производстве карбида кальция и значительное количество потребляемого сырья (известняка и кокса), перерабатываемого в несколько стадий. Достоинство этого метода состоит в получении концентрированного ацетилена, очистка которого от небольших примесей не представляет затруднений. При методах термического расщепления углеводородов используется меньшее количество сырья, которое превращается в ацетилен в одну стадию, но ацетилен получается разбавленным и требуется сложная система его очистки и концентрирования. Однако при этом побочно получаются смеси водорода с метаном или окисью углерода, утилизация которых снижает-себестоимость ацетилена. [c.107]Процесс получения ацети.пена ведут в специальных генераторах, куда непрерывно подается карбид кальция. Полученный ацетилен подвергают очистке от примесей (НзЗ, РН3 и др.) промыванием каким-либо окислителем. Из карбида кальция получают ацетилен и в лабораториях. [c.295]
Делаются попытки усовершенствовать производство карбида кальция, однако это связано с большим расходом электроэнергии и сырья, высокими капиталовложениями и себестоимостью кроме того, подобные установки технологически трудноуправляемы. Было предложено, например, для получения необходимого тепла сжигать (в присутствии кислорода) часть кокса для уменьшения расхода электроэнергии. При этом образуется много окиси углерода, использование которой в процессе также может снизить себестоимость ацетилена. В настоящее время, однако, большую часть ацетилена получают старым методом (из карбида кальция). Карбид кальция обладает тем преимуществом, что из него получается ацетилен 97— 98%-ной концентрации, поэтому дальнейшая его очистка очень проста его легко транспортировать. Ацетилен же, полученный из ме-. тана (и других углеводородов), требует трудоемкой операции выделения его из газовых смесей и транспортирования в резервуарах под давлением. Критерием выбора конкретного процесса получения ацетилена из метана (или его гомологов) служат его основные характеристики (термодинамика, кинетика, механизм реакции). [c.99]
Содержание (в мг м ) примесей в ацетилене, полученном из карбида, до и после очистки [c.204]
Вследствие легкости окисления альдегидов дальнейшее превращение в уксусную кислоту не представляет существенных затруднений. Другой необходимой предпосылкой для возникновения этого производства явилась разработка в 90-х годах XIX в. технического способа получения из кокса и извести карбида кальция, из которого легко при действии воды образуется ацетилен. Таким образом, синтез уксусной кислоты включает в себя четыре стадии а) получение карбида кальция, б) получение из карбида ацетилена и очистка его от примесей, в) получение уксусного альдегида (реакция Кучерова), г) получение уксусной кислоты он является ярким примером синтеза органического соединения, исходя из углерода и неорганических веществ — извести, воды и кислорода с использованием солей ртути и марганца. [c.272]
В ацетилене, полученном из карбида кальция, содержание вредных примесей невелико, и он легко очищается при обработке раствором гипохлорита кальция или другими реагентами с последующей осушкой хлоридом кальция или вымораживанием. При использовании ацетилена, полученного из природного газа, он подвергается более сложной очистке [6] с применением жидких (например, диметилформамида) или твердых сорбентов (активированных углей). [c.169]
Методика работы. Целью работы является получение уксусного альдегида из ацетилена по методу Кучерова с катализатором из серной кислоты с добавкой окиси ртути. Ацетилен, необходимый для опыта, берут из баллона или получают разложением карбида кальция водой. В обоих случаях ацетилен очищается от фосфорного и мышьяковистого водорода щелочным раствором перманганата калия, щелочным раствором гидросульфита натрия от сероводорода —подкисленным раствором медного купороса. При применении ацетилена из баллона необходима кроме того очистка от ацетона пропусканием через [c.122]
Ацетилен, полученный из карбида, имеет чистоту 99,5% и содержит примеси газов МНз, РНз, h3S. Если ацетилен идет на химическую переработку, то его очищают хромовой кислотой. При этом РНз и h3S окисляются в серную и фосфорную кислоты. Применяют для очистки также хлорную воду и ги-похлорит натрия. [c.246]
Разложение таблеток карбида бария производится в стеклянном аппарате 10%-ным водным раствором серной кислоты. Смесь газов собирается в металлическом газометре и для очистки пропускается через систему предварительно вакуумированных металлических ловушек, охлаждаемых жидким азотом. Ацетилен конденсируется на стенках ловушек и при испарении может быть собран в газгольдер с ртутным затвором. Представляет интерес вариант получения карбида бария с вакуумной отгонкой избытка металлического магния. Последующее разложение карбида бария не сопровождается образованием значительных количеств водорода, отпадает необходимость очистки ацетилена и в результате повышается его выход. [c.141]
Оба способа имеют свои преимущества и недостатки. Карбидный ацетилен дорог (на получение карбида кальция расходуется много электроэнергии), но легче поддается очистке. Метан — очень дешевое сырье, однако и его пиролиз требует немалых энергетических затрат, а кроме тоге , в ходе пиролиза образуется сложная смесь веществ, выделить из которой чистый ацетилен нелегко. В настоящее время доля карбидного ацетилена в мировом производстве составляет более половины. [c.309]
При получении дивинила через ацетилен — ацетальдегид регулируется сброс сточных вод от промывки ацетилена, получаемого из карбида кальция, и очистка их от известкового шлама. Для выделения шлама из отработанной воды при производстве ацетилена применяют трехъярусные отстойники. По имеющимся опытным данным, из сточных вод от промывки ацетилена в течение 30 мин. выпадает около 90% взвешенных веществ. За [c.31]
Получение ацетилена. Ацетилен получают разложением карбида кальция водой или пользуются готовым ацетиленом из баллона после предварительной очистки. [c.211]
Встречается в воздухе в производстве удобрений, серной и азотной кислот, при применении А. в холодильном деле, при получении его и аммониевых солей из аммиачной воды, в газовом производстве при очистке воды, керосина и некоторых минеральных масел, в производстве соды по методу Сольве, в производстве клея, нитроклетчатки, искусственного шелка, карбида кальция, красителей (индиго, амарант), лаков, в красильня
www.chem21.info
Ацетилен промышленные способы получения – Справочник химика 21
Гидратация ацетиленов. Ацетилен и его гомологи при действии воды в присутствии катализатора (солей двухвалентной ртути) превращаются Б оксосоединения. При этом только ацетилен образует альдегид, а именно ацетальдегид (реакция Кучерова). Этот способ является одним из главных промышленных способов получения ацетальдегида [c.135]Крекинг углеводородов при высоких температурах. При температуре выше 1000° все предельные углеводороды распадаются на углерод и водород. Этот процесс используется как дешевый метод получения водорода и газовой сажи. В определенных условиях удается изолировать промежуточные продукты расщепления, в частности ацетилен. Разложение метана с образованием ацетилена является самым дешевым промышленным способом получения последнего (стр. 92). [c.58]
Ацетилен получают в промышленности из карбида кальция, который образуется из угля и извести в электрических печах ( 4.2). В последние десятилетия приобретает все большее значение еще один промышленный способ получения ацетилена — пиролиз метана (природного газа) [c.309]
Повидимому, хлористый винил образуется в результате прямого замещения, а не вследствие отщепления хлористого водорода от первоначально образовавшегося дихлорэтана. Доказательством служит то, что хлористый винил получается в условиях, при которых хлористый водород не отщепляется от дихлорэтана. Другие промышленные способы получения хлористого винила (пиролиз дихлорэтана и присоединение хлористого водорода к ацетилену) описаны ниже. [c.149]
Для промышленного получения ацетальдегида применяются два способа. По одному из них исходным веществом является этиловый спирт, который окисляют в ацетальдегид бихроматом, и серной кислотой или, еще лучше, воздухом в присутствии нагретых металлов (меднохромовый катализатор). Однако основным способом получения ацетальдегида является присоединение воды к ацетилену (стр. 80) в присутствии солей ртути. [c.213]
Многие способы получения сложных эфиров описаны ранее присоединение карбоновых кислот к ацетилену (см. разд. 1.4.3), реакция Тищенко (см. разд. 4.2.4), этерификация (см. разд. 6.1.2), ацилирование спиртов ангидридами и галогенангидридами карбоновых кислот и кетенами (см. разд. 6.1.3.2), ацилирование енольных форм кетонов кетеном (см. разд. 6.1.3.2). Сравнительно недавно предложен интересный промышленный синтез винил-ацетата из этилена [c.372]
Выдающийся вклад в разработку многочисленных промышленных технологических процессов на основе ацетилена внес В Реппе Разработанные им способы получения разнообразных органических продуктов сделали ацетилен в 30-50-е годы XX столетия основным сырьевым источником промышленности органического синтеза На основе ацетилена получают в больших количествах уксусный альдегид, уксусную кислоту, уксусный ангидрид, этилацетат, хлористый винил, винилацетат, акрилонитрил, акрилаты, хлоропрен и др (см выше) [c.326]
Промышленный катализ тоже не обходится без соединений ртути. Один из способов получения уксусной кислоты и этилового спирта основан на реакции, открытой русским ученым М. Г. Кучеровым. Сырьем служит ацетилен. В присутствии катализаторов — солей двухвалентной ртути — он реагирует с водяным паром и превраш а-ется в уксусный альдегид. Окисляя это вещество, получа- ют уксусную кислоту, восстанавливая — спирт. Те н е соли помогают получать из нафталина фталевую кислоту — важный продукт основного органического синтеза. [c.247]
Существует два метода синтеза этанола, одного из органических продуктов, который получают в огромных количествах промышленным путем. Этилен для процесса гидратации изготовляют каталитическим гидрированием ацетилена (гл. 15) или получают крекингом нефти. Любой химический продукт, который можно легко синтезировать из ацетилена, обходится очень дешево, потому что сам ацетилен может быть получен в неограниченных количествах из карбида кальция ). Второй способ получения этанола состоит в брожении углеводов зерна, картофеля и плодов. [c.206]
Способы получения. Наибольшее промышленное значение из алкинов имеет ацетилен, получаемый в технике разложением карбида кальция водой или термической деструкцией углеводородов. [c.49]
Промышленный катализ тоже не обходится без соединений ртути. Один из способов получения уксусной кислоты и этилового спирта основан на реакции, открытой русским ученым М. Г. Кучеровым. Сырьем служит ацетилен. В присутствии катализаторов — солей двухвалентной ртути — он реагирует с водяным паром и превращается в уксусный альдегид. Окисляя это вещество, получают уксусную кислоту, восстанавливая — спирт. [c.209]
Кроме этого способа получения спирта, в настоящее время разработаны и другие промышленные методы. Одним из них является получение винного спирта из ацетилена. Сущность метода заключается в том, что ацетилен, получаемый действием воды на карбид кальция, пропускают через воду, в которой растворено немного ртутных солей (катализатор). В результате в воде образуется ацетальдегид по равенству [c.300]
Бутиндиол при этом можно получать с выходом до 71%. Однако промышленное значение приобрел способ Реппе [23], заключающийся в конденсации формальдегида (в виде формалина) с ацетиленом под небольшим давлением в присутствии катализатора — ацетиленида меди, осажденного на силикагеле [79—84]. Этот способ осуществляется в промышленном масштабе [50, 85] при непрерывном процессе и дает высокий выход бутиндиола. Он может служить и надежным препаративным способом получения бутиндиола в автоклаве с применением не разбавляемого азотом ацетилена [86]. Выход конечного продукта при этом достигает 80%. Поиски путей упрощения технологии и повышения безопасности атого способа привели советских ученых к возможности проведения реакции при атмосферном давлении на менее взрывоопасном мелкодисперсном катализаторе 188, 89] или в органических растворителях [89, 90]. Изучены также кинетика и механизм реакции [c.19]
Этот способ применяют как в лабораториях, так и в промышленности, где он освоен еще в прошлом веке. Карбидный ацетилен послужил сырьем для промышленности органического синтеза в странах, богатых углем (Германия, Англия). Однако получение его требует больших затрат электроэнергии, вследствие чего карбидный ацетилен дорог и в последнее время он вытесняется другими способами получения ацетилена. [c.83]
Ацетилен стал доступен в конце XIX в., после того как был получен в промышленных условиях карбид кальция, явившийся сырьем для производства ацетилена. Использование дешевого природного газа и продуктов переработки нефти стало новым мощным стимулом для получения ацетилена и последующего развития на ег
www.chem21.info
Ацетилен, получение и очистка – Справочник химика 21
Содержание (в мг м ) примесей в ацетилене, полученном из карбида, до и после очистки [c.204]Процесс получения ацети.пена ведут в специальных генераторах, куда непрерывно подается карбид кальция. Полученный ацетилен подвергают очистке от примесей (НзЗ, РН3 и др.) промыванием каким-либо окислителем. Из карбида кальция получают ацетилен и в лабораториях. [c.295]
В ацетилене, полученном из карбида кальция, содержание вредных примесей невелико, и он легко очищается при обработке раствором гипохлорита кальция или другими реагентами с последующей осушкой хлоридом кальция или вымораживанием. При использовании ацетилена, полученного из природного газа, он подвергается более сложной очистке [6] с применением жидких (например, диметилформамида) или твердых сорбентов (активированных углей). [c.169]
Делаются попытки усовершенствовать производство карбида кальция, однако это связано с большим расходом электроэнергии и сырья, высокими капиталовложениями и себестоимостью кроме того, подобные установки технологически трудноуправляемы. Было предложено, например, для получения необходимого тепла сжигать (в присутствии кислорода) часть кокса для уменьшения расхода электроэнергии. При этом образуется много окиси углерода, использование которой в процессе также может снизить себестоимость ацетилена. В настоящее время, однако, большую часть ацетилена получают старым методом (из карбида кальция). Карбид кальция обладает тем преимуществом, что из него получается ацетилен 97— 98%-ной концентрации, поэтому дальнейшая его очистка очень проста его легко транспортировать. Ацетилен же, полученный из ме-. тана (и других углеводородов), требует трудоемкой операции выделения его из газовых смесей и транспортирования в резервуарах под давлением. Критерием выбора конкретного процесса получения ацетилена из метана (или его гомологов) служат его основные характеристики (термодинамика, кинетика, механизм реакции). [c.99]
Процесс получения ацетилена из углеводородного сырья протекает в одну стадию, менее энергоемок, требует меньших капитальных затрат и, в целом, на 20% экономичнее карбидного процесса. Однако в этом методе ацетилен разбавлен водородом, а это требует более сложной системы его выделения из синтез-газа и очистки. [c.246]
После очистки в циклоне от следов ртути газообразные продукты реакции охлаждали сперва до 60°, что приводило к конденсации некоторой части ацетальдегида. Затем газ промывали жидкостью, вытекавшей из последнего скруббера, и получали 7%-ный водный раствор ацетальдегида. Последние следы ацетальдегида удаляли из газов промывкой их водой при 40° полученный при этом слабый раствор применяли для орошения предыдущего скруббера. Водный раствор ацетальдегида, содержащий следы ацетона и уксусной кислоты, а также высшие продукты конденсации, такие, как кротоновый альдегид, очищали ректификацией под давлением 3 ата. В качестве побочной фракции собирали ацетон, который концентрировали в отдельных колоннах. Выход товарного ацетальдегида составлял 93%, считая на ацетилен. [c.299]
Каким бы способом пи получался ацетилен, в результате образуется газ, содержащий сравнительно немного ацетилена (8—14%). В табл. III.2 приведены составы газов, получающихся при различных процессах. Поэтому выделение, очистка и концентрирование ацетилена занимают в технологической схеме получения ацетилена из метана большое место. В настоящее время существует довольно много способов выделения ацетилена из газов. [c.121]
В последнее время имеется стремление в производстве химических продуктов использовать не концентрированный, а разбавленный ацетилен. Сырой газ после очистки от сажи и гомологов ацетилена направляется на химический синтез, а затем уже выделяется продукт. Это целесообразно в том случае, если получающийся продукт выделить значительно легче, чем ацетилен, и это может компенсировать увеличение объема реакционно аппаратуры, вызываемое проведением реакции при меньшем парциальном давле ии ацетилена. В настоящее время такая схема разрабатывается применительно к получению ацетона, ацетальдегида, хлорвинила. [c.123]
К химическим методам очистки газообразного сырья относится и удаление из него ацетилена гидрированием. Ацетилен попадает в газовое сырье главным образом нри получении этилена пиролизом. В зависимости от условий последнего (сырья, концентрации водяного пара в нем, температуры и времени пребывания в печи) в продуктах пиролиза содержится большее [c.150]
Реакция сильно эндотермична и технические методы получения ацетилена различаются по способам подвода тепла, например посредством вольтовой дуги, путем сжигания части метана непосредственно в реакционном пространстве и др. Аналогичным путем, но при несколько более низких температурах, ацетилен может быть получен из высших углеводородов—пропана, бутана пл(г легких нефтяных погонов. Реакция получения ацетилена нз углеводородов протекает сложно и сопровождается образованием большого количества побочных продуктов—этилена, углерода в виде сажи, гомологов ацетилена. Разработанные методы разделения газовой смеси на отдельные компоненты с последующей тщательной очисткой позволяют выделить ацетилен в достаточно чистом виде. [c.94]
В настоящее время основным сырьем в производстве аммиака являются природный газ, попутные газы нефтедобычи, жидкие углеводороды и коксовый газ. Доля аммиака, получаемого из твердого топлива и электролитического водорода, все более снижается. При современных методах получения аммиака все большее значение приобретают процессы очистки газа. Из технологических газов на разных стадиях получения аммиака удаляют такие примеси, как сернистые соединения, двуокись и окись углерода, ацетилен, окислы азота, кислород и др. Эти примеси, содержащиеся в газе в различных концентрациях, по-разному влияют на процесс. Например, сернистые соединения оказывают сильное влияние на все катализаторы, применяемые в синтезе аммиака серосодержащие соединения, присутствующие в исходном углеводородном сырье, ухудшают работу катализаторов конверсии метана, что приводит к повышению температуры процесса и увеличению расхода кислорода. При использовании наиболее экономичного способа производства аммиака, который основан на методе бескислородной каталитической конверсии метана в трубчатых печах, содержание сернистых соединений в природном газе не должно превышать 1 мг/м . [c.7]
Получение и очистка исходного этилена. Материалом для производства этилена на одном из заводов Германии является этан или ацетилен. Этан подвергают дегидрированию в специальных печах в присутствии кислорода воздуха приблизительно при 800
www.chem21.info

