Ниобий металл или неметалл: Месторождения ниобия — Интернет-энциклопедии Красноярского края
alexxlab | 04.11.2021 | 0 | Разное
Месторождения ниобия — Интернет-энциклопедии Красноярского края
Основные области применения ниобия — ракетостроение, космическая и авиационная техника, атомная энергетика, радиотехника, электроника и химическая промышленность.
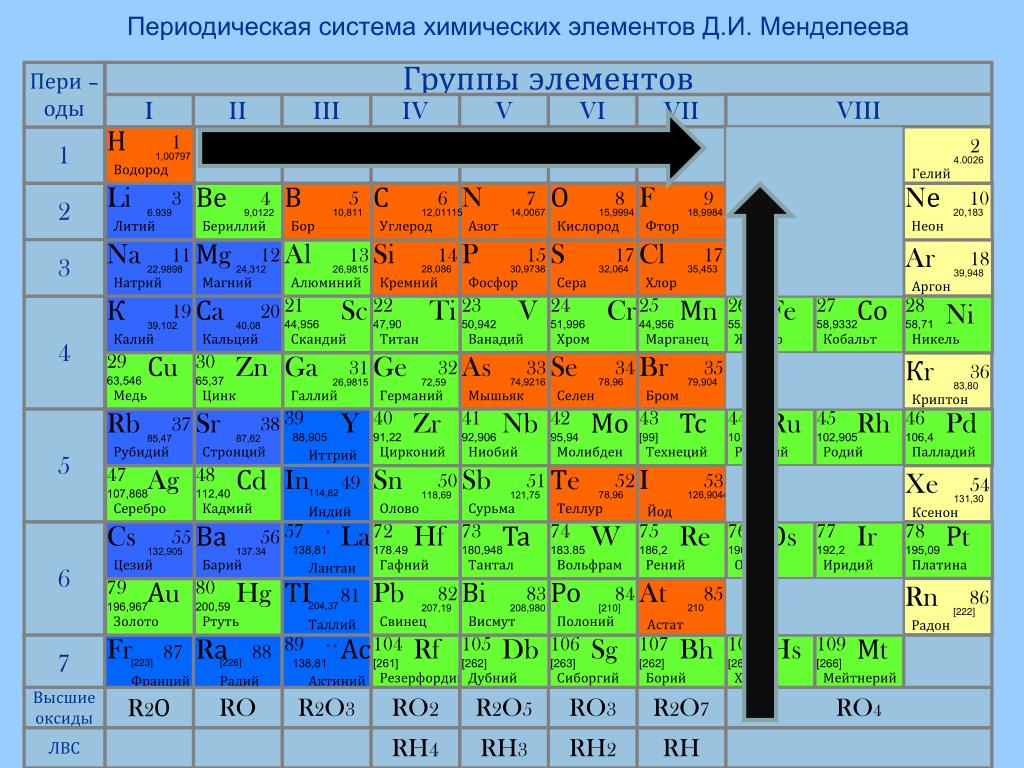
Ниобий (Nb) — редкий блестящий металл серебристо-серого цвета. Элемент таблицы Менделеева с атомным номером 41. Не встречается в природе в чистом виде. Обладает такими ценными свойствами, как тугоплавкость, коррозионная стойкость, малое сечение захвата тепловых нейтронов, способность образовывать сверхпроводящие и жаропрочные свойства, низкая работа выхода электронов, хорошие обрабатываемость давлением на холоде и свариваемость.
На территории Красноярского края расположены три месторождения ниобиевых руд — Татарское в Мотыгинском районе, уникальное Чуктуконское редкометальное месторождение в Нижнем Приангарье и ниобий-редкие земли на Кийском рудопроявлении в районе Енисейска.
Прогнозные ресурсы Татарского месторождения — 73 тыс. тонн пятиокиси ниобия. Ресурсы Чуктуконского месторождения оцениваются в 1 357 тыс. тонн. По Кийскому рудопроявлению нет утвержденных запасов. Чуктуконское месторождения является объектом первоочередного изучения, однако здесь не решен вопрос по обогащению руд.
- Связанные материалы
- Мотыгинский район
- Город Енисейск
Элемент № 41 был открыт дважды. В 1801 г. английский ученый Чарльз Хатчет исследовал образец минерала, присланного в Британский музей из Америки. Из этого минерала он выделил окисел не известного прежде элемента. Новый элемент Хатчет назвал колумбием, отмечая тем самым его заокеанское происхождение. А черный минерал получил название «колумбит».
В 1801 г. английский ученый Чарльз Хатчет исследовал образец минерала, присланного в Британский музей из Америки. Из этого минерала он выделил окисел не известного прежде элемента. Новый элемент Хатчет назвал колумбием, отмечая тем самым его заокеанское происхождение. А черный минерал получил название «колумбит».
Через год шведский химик Экеберг выделил из колумбита окисел еще одного нового элемента, названного танталом. Сходство соединений колумбия и тантала было так велико, что в течение 40 лет большинство химиков считало, что тантал и колумбий — один и тот же элемент.
В 1844 г. немецкий химик Генрих Розе исследовал образцы колумбита, найденные в Баварии. Он вновь обнаружил окислы двух металлов. Один из них был окислом известного уже тантала. Окислы были похожи, и, подчеркивая их сходство, Розе назвал элемент, образующий второй окисел, ниобием — по имени Ниобы, дочери мифологического мученика Тантала.
Металлический ниобий был впервые получен лишь в 1866 г. шведским ученым Бломстрандом при восстановлении хлорида ниобия водородом. В конце XIX в. были найдены еще два способа получения этого элемента. Сначала Муассан получил его в электропечи, восстанавливая окись ниобия углеродом, а затем Гольдшмидт сумел восстановить тот же элемент алюминием.
шведским ученым Бломстрандом при восстановлении хлорида ниобия водородом. В конце XIX в. были найдены еще два способа получения этого элемента. Сначала Муассан получил его в электропечи, восстанавливая окись ниобия углеродом, а затем Гольдшмидт сумел восстановить тот же элемент алюминием.
Называть элемент № 41 в разных странах продолжали по-разному: в Англии и США — колумбием, в остальных странах — ниобием. В 1950 г. по решению Международного союза чистой и прикладной химии было повсеместно узаконено название элемента «ниобий», а за основным минералом ниобия так и закрепилось наименование «колумбит». Его формула (Fe, Mn) (Nb, Ta) 2О6.
В земной коре ниобия содержится 18 грамм на одну тонну. Ниобий никогда не встречается в самородном состоянии. Близкие химические свойства ниобия и тантала обусловливают совместное их нахождение в одних и тех же минералах и участие в общих геологических процессах.
Элементарный ниобий — чрезвычайно тугоплавкий (2 468 °C) и высококипящий (4 927 °C) металл, очень стойкий во многих агрессивных средах. На него не действует ни одна кислота, за исключением плавиковой. Кислоты-окислители «пассивируют» ниобий, покрывая его защитной окисной пленкой. Химическая активность ниобия повышается при высоких температурах.
Ниобий активно реагирует со многими неметаллами, с ним образуют соединения галогены, азот, водород, углерод, сера, однако самыми важными его соединениями являются соединения с другими металлами. Ниобий является одним из первых технически важных сверхпроводящих материалов, его сплавы и соединения используются для изготовления сверхпроводящих соленоидов, а также некоторых других важных технических устройств.
Ниобий обладает хорошей теплопроводностью и не взаимодействует с ураном при температуре до 1 100 °C, что обуславливает его востребованность в атомной промышленности.
- Из минералов уже известных месторождений можно выплавить более 1,5 млн тонн металлического ниобия
Металлический ниобий получают из рудных концентратов путем их вскрытия, разделения ниобия и тантала, получения их чистых химических соединений, восстановления и рафинирования металлического ниобия и его сплавов.
Широкое применение ниобий нашел в черной и цветной металлургии. Сталь, легированная ниобием, обладает хорошей коррозионной стойкостью, не теряя при этом своей пластичности.
Хромо-марганцевой стали ниобий придает высокую износоустойчивость. Ниобием легируют и многие цветные металлы. Так, алюминий, легко растворяющийся в щелочах, не реагирует с ними, если в него добавлено всего 0,05 % ниобия. А медь, известную своей мягкостью, и многие ее сплавы ниобий словно закаляет. Он также увеличивает прочность таких металлов, как титан, молибден, цирконий, и одновременно повышает их жаростойкость и жаропрочность.
Свойства и возможности ниобия используются в авиационном и космическом строительстве, машиностроении, радиотехнической и химической промышленности, ядерной энергетике.
Ниобий подходит для изготовления контейнеров для хранения радиоактивных отходов или установок по их использованию. В химической промышленности из ниобийсодержащих сплавов и реже из листового ниобия иногда делают аппаратуру для производства высокочистых кислот.
В химической промышленности из ниобийсодержащих сплавов и реже из листового ниобия иногда делают аппаратуру для производства высокочистых кислот.
Из ниобийсодержащих сплавов и чистого ниобия сделаны некоторые детали ракет и бортовой аппаратуры искусственных спутников Земли.
Внешний вид и комплекс свойств ниобия используется в ювелирном деле и при производстве корпусов ручных часов: сплав ниобия с рением не только внешне похож на металлический иридий, но почти так же износостоек.
Ниобий применяют в криотронах — сверхпроводящих элементах вычислительных машин. Также ниобий использован в ускоряющих структурах большого адронного коллайдера.В медицине высокая коррозионная стойкость ниобия используется при производстве нитей.
Дата последнего изменения: 19.12.2014
- Горная энциклопедия. В 5 т.
 — М.: Советская энциклопедия, 1984—1991.
— М.: Советская энциклопедия, 1984—1991.
НИОБИЙ — СВОЙСТВА, ПРИМЕНЕНИЕ И СПЛАВЫ НИОБИЯ
Химические элементы ниобий и тантал неразрывно связаны между собой еще со времени открытия. Их взаимосвязь проявляется даже мифологически: название первого, происходит от имени Ниоба, которая в древнегреческой мифологии была дочерью царя Тантала. Генрих Розе приложил свою «легкую руку» к тому, чтобы наименование Nb крепко закрепилось в научных кругах и таблице Менделеева. Исследования немецкого химика в области изучения свойств минерала колумбита позволили выделить окислы двух металлов (1844 год). Первый относился к уже известному тогда танталу, второй оказался оксидом нового элемента — ниобия.
Что на сегодня известно о Nb
Ниобий – химический элемент, занимает место в V группе таблицы Менделеева, атомный номер – 41, атомная масса 92,9. Как и многие металлы, он характеризуется серо-стальным блеском.
Тугоплавкость считается самым важным физическим свойством металла, именно благодаря ей ниобий стал востребованным во многих областях промышленности. Плавится и кипит при температурах 2468 и 4927 0С, соответственно. Плотность вещества при комнатных условиях оценивается как 8.57 грамм в кубическом сантиметре. Металл обладает парамагнитностью. Имеет ОЦК кристаллическую решетку с радиусом 3.294 ангстрем.
Химические свойства ниобия и танталу также достаточно близки. Металлы отличаются высокой устойчивостью к воздействию отрицательных температур и большинства агрессивных сред. Например, заметное окисление Nb на воздухе наблюдается только при нагреве вещества свыше 200 0С. Список кислот, не воздействующих на ниобий, достаточно широк и включает:
- соляную;
- серную;
- хлорную;
- фосфорную.

Также металл устойчив к водным растворам аммиака. Уникальное свойство элемента образовывать диэлектрическую оксидную пленку в составе кислых электролитов нашло применение в изготовлении миниатюрных высокоемкостных конденсаторов, где элемент заменяет более дорогостоящий тантал.
Производство ниобия
Несмотря на то, что запасы Nb-содержащих руд превосходят аналоги для тантала, первые характеризуются очень скудным содержанием элемента. Как правило, концентраты содержат пятиокись ниобия – Nb2O5, процентное вхождение которое определяется типом руды:
- пирохлоровая – до 37%;
- лопаритовая — 8%;
- колумбитовая – от 30 до 60%.
Обычно, руда ниобия проходит цикл термического восстановления с участием алюминия или кремния. Результат процесса – соединения феррониобий и ферротанталониобий. Металлический ниобий добывают из аналогичного сырья, но сама технология более сложная и состоит из трех стадий:
- Добыча руды, его содержащей, переработка до состояния концентратов их вскрытие.

- Получение химических соединений Nb и Та с привлечением методов порошковой металлургии.
- Рафинирование позволяет получать металлический ниобий высокой пробы.
Так выглядит феррониобий
На сегодня, наиболее развиты такие методики получения Nb, как алюмино-, натрие- и карботермическая. Различными оказываются и прекурсоры для высокотемпературного восстановления ниобия. При натриетермическом способе – это K2NbF7, тогда как в алюминотермической методике используется пятиокись ниобия. Карботермическая технология подразумевает смешивание оксида Nb с сажей в высокотемпературной водородной среде, чтобы получить карбид ниобия. На следующем этапе, водородная среда заменяется вакуумом, и при тех же температурах, смешав карбид ниобия с его оксидом, получают сам металл.
Фольга из ниобия
Бестигельная электроннолучевая зонная плавка дает возможность вести производство монокристаллов Nb. Методами порошковой металлургии, пользуются для получения сначала сплавов, а после и чистого металла ниобий. Поэтому ничего удивительного, что «куплю ниобий» — частое содержание объявлений, публикуемых на страницах интернета. Ведь в таких ситуациях, вполне можно использовать вторичное сырье, а не руду или концентрат из нее.
Поэтому ничего удивительного, что «куплю ниобий» — частое содержание объявлений, публикуемых на страницах интернета. Ведь в таких ситуациях, вполне можно использовать вторичное сырье, а не руду или концентрат из нее.
Среди форм выпускаемого металла распространен ниобий в слитках. Они предназначены на изготовление сплавов на базе металла и прочих полуфабрикатов. Альтернативно выпускается штабик ниобия, классифицируемый соответственно чистоте химического состава. Наименьшее содержание примесей соответствует марке НБШ-00. Штабик ниобия НБШ-0 отличается повышенным вхождением железа, кремния тантала и титана. Наиболее легированная марка штабика ниобия — НБШ-1.
Альтернативная форма выпуска – прокат ниобия. В частности, большинство организаций предпочитает покупать листовой металл, пруток, проволоку. Еще одна разновидность проката ниобий фольга.
Магнитные и другие сплавы с Nb
Сплавы ниобия
Феррониобий представляет собой соединение, базовый состав которого определяют элементы: железо с одной стороны, а также смесь ниобия с танталом – с другой. Источником для соединения выступает техническая пятиокись ниобия из которой вещество производят электропечным алюминотермическим способом. Суммарное содержание Nb и Ta в сплаве составляет 40 – 65% и зависит от конкретной марки феррониобия, детальная информация по которым сведена в ГОСТ 16773-2003. Остальные составляющие соединения:
Источником для соединения выступает техническая пятиокись ниобия из которой вещество производят электропечным алюминотермическим способом. Суммарное содержание Nb и Ta в сплаве составляет 40 – 65% и зависит от конкретной марки феррониобия, детальная информация по которым сведена в ГОСТ 16773-2003. Остальные составляющие соединения:
- углерод;
- кремний;
- алюминий;
- титан;
- сера;
- фосфор.
Наибольшим содержанием, кроме ниобия с танталом, в сплаве представлены Si и Al. При этом, феррониобий с минимальным процентным вхождением Nb и Ta, характеризуется высоким вхождением кремния до 20%. Напротив, в сплаве с максимальным содержанием ниобия и тантала, среди легирующих добавок преобладает алюминий.
Свое применение феррониобий нашел сталеплавильной – производство конструкционной стали и литейной отраслях индустрии, а также в изготовлении электронных покрытий. Основной производитель соединения Вишневогорский металлургический завод «Северный ниобий». Предприятие расположено в Челябинской области, вблизи одноименного населенного пункта. В сферу деятельности ООО «Северный ниобий» также входит изготовление ферросплавов других металлов, включая молибден, вольфрам и титан.
Основной производитель соединения Вишневогорский металлургический завод «Северный ниобий». Предприятие расположено в Челябинской области, вблизи одноименного населенного пункта. В сферу деятельности ООО «Северный ниобий» также входит изготовление ферросплавов других металлов, включая молибден, вольфрам и титан.
Альтернативой соединения феррониобий, оказывается деформируемый сплав 5ВМЦ, где легирующими металлами выступают: цирконий, молибден и вольфрам. Применение 5ВМЦ, в основном, ограничено изготовлением полуфабрикатов.
Окислы металла
Наибольшее распространение среди этого вида соединений получила пятиокись ниобия. Это неорганическое вещество представлено белым кристаллическим порошком, обладающим кремовым оттенком и нерастворимым в воде, большинстве кислот. Пентаоксид ниобия характеризуется химической формулой Nb2O5 и подразделяется на три марки, в зависимости от чистоты: 99 – 97% исходного вещества.
Основные свойства пятиокиси ниобия:
- аморфные способности;
- повышенная прочность;
- тугоплавкость – температура плавления 1490 0С;
- окисляется при нагревании;
- реагирует с хлором, восстанавливается водородом.

Пятиокись ниобия получают разнообразными методиками, среди которых присутствуют: сжигание Nb в кислороде и проколка различных форм ниобия:
- нитрида на воздухе;
- более низкого оксида;
- NbC;
- Гидрида.
Основная сфера использования пятиокиси ниобия – производство высоколегированных марок сталей, изготовление сплавов.
Изделия из ниобия
Ассортимент продукции, как и формы выпускаемого металла достаточно разнообразны. Популярность элемента ниобий применение и производство его, обусловлены следующими свойствами элемента:
- тугоплавкость;
- устойчивость к разным видам коррозии;
- малая эффективность от столкновения с нейтронами;
- образование сплавов с жаропрочными и сверхпроводящими качествами;
- легкость сваривания;
- сохранение работоспособности при отрицательных температурах;
- геттерные свойства.

Аноды из ниобия
Среди отраслей, эксплуатирующих металл, следует выделить технику для авиации и космонавтики, где на базе Nb выпускают детали самолетов, ракет. Дополнительно, ниобий востребован радиотехникой, где из него изготавливают сдлелующее:
- детали электрических конденсаторов;
- элементы радарных установок;
- аноды из фольги, катоды, сетки для работы внутри мощных генераторных ламп.
Чтобы изготовить оболочки для урановых и плутониевых тепловыделяющих элементов, в атомной энергетике также применяют ниобий и его сплавы. Из соединения изготавливают контейнеры, трубы для транспортировки жидких металлов.
Альтернативная сфера, где цена продукции определяется не только содержанием элемента – монеты из ниобия и тантала. Так металл используют Австрийский монетный двор и Национальный банк Латвии, где активно развита чеканка ниобиевых монет в сочетании с серебром. Уже выпущено шесть разновидностей, общий вид которых: сердцевина – ниобий различных цветов и внешнее кольцо – серебро 900-й пробы.
Niobium – Энциклопедия Нового Света
Из энциклопедии Нового Света
Прыжки к: навигация, поиск
Предыдущий (Ninian Smart)
Nex , атомный номер 41) — редкий мягкий металл серого цвета. Он был обнаружен в разновидности колумбита (ныне называемого ниобитом) и сначала был назван в честь этого минерала. Он используется в сплавах для изготовления специальных сталей и прочных сварных соединений. При экстремально низких температурах он действует как сверхпроводник.
Содержание
- 1 Возникновение
- 2 История
- 3 Примечательные характеристики
- 3.1 Изотопы
- 4 соединения
- 5 приложений
- 6 Меры предосторожности
- 7 См. также
- 8 Сноски
- 9 Каталожные номера
- 10 Внешние ссылки
- 11 кредитов
Встречаемость
Металлический ниобий
Этот элемент никогда не встречается в свободном виде, но встречается в минералах колумбите ((Fe,Mn)(Nb,Ta) 2 O 6 ), колумбит-танталит или колтан ((Fe,Mn)(Ta,Nb) 2 O 6 ), пирохлор ((Na,Ca) 2 Nb 2 O 6 OH,F) и эвксенита ((Y,Ca,Ce,U,Th)(Nb,Ta,Ti) 2 O 6 ). Минералы, содержащие ниобий, часто также содержат тантал. Обнаружены крупные месторождения ниобия, связанные с карбонатитами (углеродисто-силикатными изверженными породами) и входящие в состав пирохлора. Бразилия и Канада являются основными производителями ниобиевых минеральных концентратов, а обширные запасы руды также находятся в Нигерии, Демократической Республике Конго и России.
Минералы, содержащие ниобий, часто также содержат тантал. Обнаружены крупные месторождения ниобия, связанные с карбонатитами (углеродисто-силикатными изверженными породами) и входящие в состав пирохлора. Бразилия и Канада являются основными производителями ниобиевых минеральных концентратов, а обширные запасы руды также находятся в Нигерии, Демократической Республике Конго и России.
История
Ниобий (в греческой мифологии: Ниоба, дочь Тантала) был обнаружен Чарльзом Хэтчеттом в 1801 году. Хэтчетт обнаружил ниобий в колумбитовой руде, отправленной в Англию в 1750-х годах Джоном Уинтропом, первым губернатором Коннектикута. Хэтчетт назвал этот элемент колумбием (символ Cb).
Примерно в то же время существовала значительная путаница в отношении разницы между этим элементом и близким к нему танталом. Эта путаница не была разрешена до 1846 года Генрихом Роузом и Жаном Шарлем Галиссаром де Мариньяком, которые заново открыли этот элемент. Роуз не знал о работе Хэтчетта и дал этому элементу другое название — ниобий. В 1864 году Кристиан Бломстранд первым получил чистый металл, восстановив хлорид ниобия нагреванием в атмосфере водорода.
В 1864 году Кристиан Бломстранд первым получил чистый металл, восстановив хлорид ниобия нагреванием в атмосфере водорода.
Международный союз теоретической и прикладной химии (IUPAC) официально принял слово «ниобий» в качестве названия 41-го элемента в 1950 году, после 100 лет споров. Это был своего рода компромисс; IUPAC принял вольфрам вместо вольфрама из уважения к использованию в Северной Америке; и ниобий вместо колумбия из уважения к европейскому использованию. Не все согласились, и хотя многие ведущие химические общества и правительственные организации называют его официальным названием IUPAC, многие ведущие металлурги, металлургические общества и большинство ведущих американских коммерческих производителей по-прежнему называют этот металл первоначальным «колумбием».
Примечательные характеристики
Ниобий является переходным металлом, который находится в периоде 5 периодической таблицы, между цирконием и молибденом. Он также находится в группе 5 (бывшая группа 5В), между ванадием и танталом.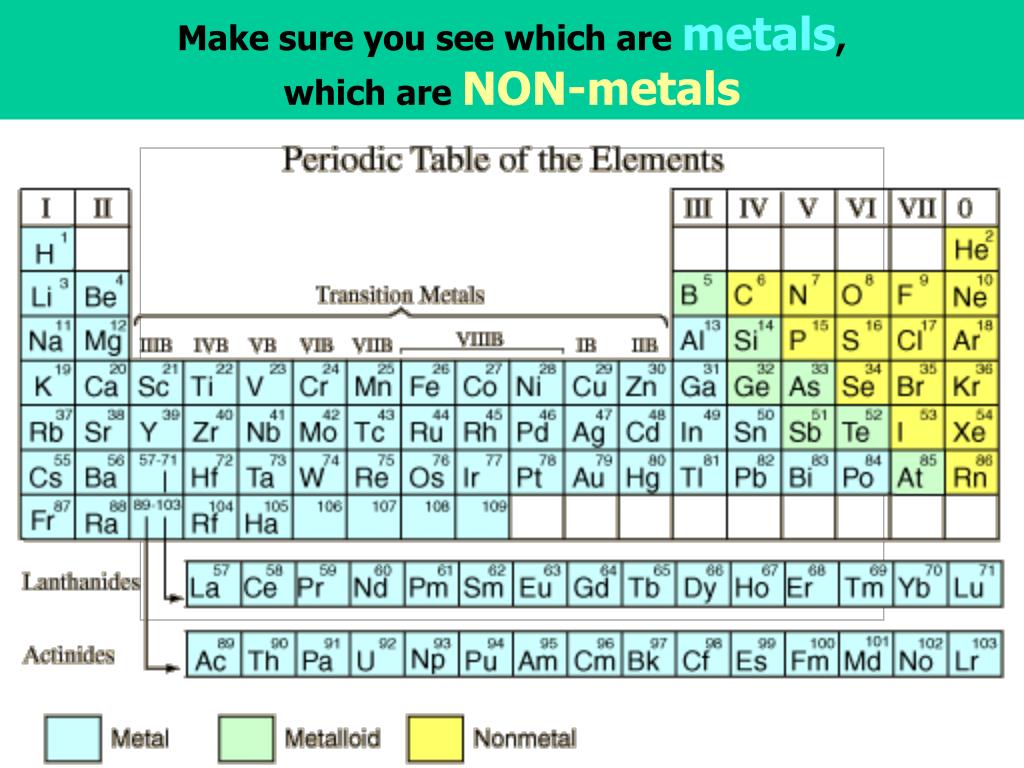 Его химические свойства почти идентичны свойствам тантала.
Его химические свойства почти идентичны свойствам тантала.
Этот блестящий серый пластичный металл приобретает голубоватый оттенок при длительном воздействии воздуха при комнатной температуре. Когда он обрабатывается даже при умеренных температурах, он должен быть помещен в защитную атмосферу. Металл начинает окисляться на воздухе при 200° С. Наиболее распространены его степени окисления +3 и +5, хотя известны и другие.
Изотопы
Встречающийся в природе ниобий состоит из одного стабильного изотопа: Nb-93. Наиболее стабильными радиоизотопами являются Nb-92 с периодом полураспада 34,7 млн лет; Nb-94 с периодом полураспада 20 300 лет; и Nb-91 с периодом полураспада 680 лет. Существует также метасостояние на 0,031 мегаэлектронвольт с периодом полураспада 16,13 года. Были охарактеризованы многие другие радиоизотопы с массовыми числами от 81 до 113. Большинство из них имеют период полураспада менее двух часов, за исключением Nb-9.5 (35 дней), Nb-96 (23,4 часа) и Nb-90 (14,6 часа).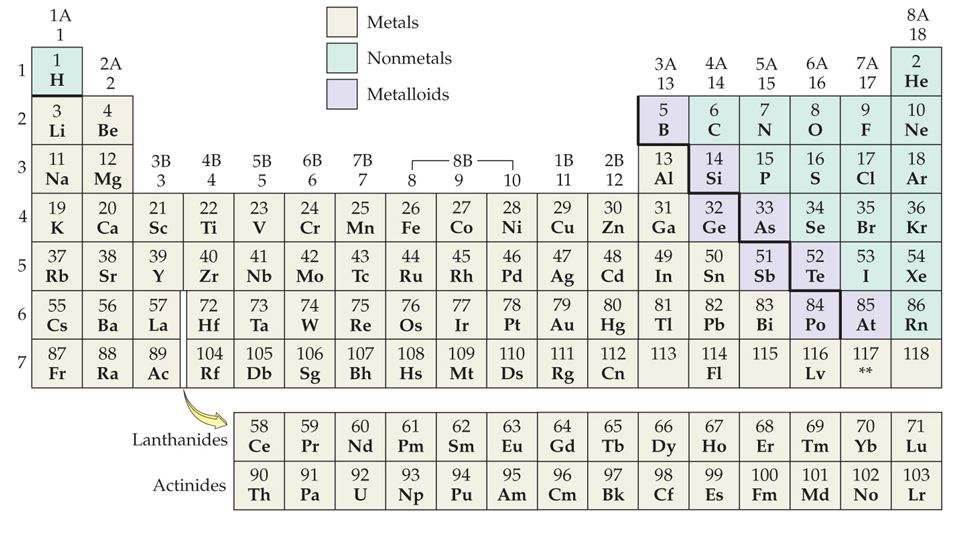
Соединения
- Карбид ниобия (NbC и Nb 2 C): Это чрезвычайно твердый, тугоплавкий керамический материал. Он имеет вид коричнево-серого металлического порошка с пурпурным блеском и обладает высокой устойчивостью к коррозии. Он обычно обрабатывается спеканием и является частой добавкой в твердые сплавы. В коммерческих целях он используется в насадках для режущих инструментов. Кроме того, это часто преднамеренный продукт в микролегированных сталях, и его можно использовать в огнеупорных покрытиях для ядерных реакторов.
- Хлорид ниобия(V) или Пентахлорид ниобия (NbCl 5 ): желтое кристаллическое твердое вещество, часто используемое в качестве исходного материала в химии ниобия. Его получают нагреванием металлического ниобия в хлоре. Часто загрязненный небольшими количествами оксихлорида ниобия (V) (NbOCl 3 ), он может быть очищен возгонкой. Это полезно для некоторых реакций в органической химии.

- Ниобий-олово (Nb 3 Sn): это металлическое химическое соединение ниобия (Nb) и олова (Sn), используемое в промышленности в качестве сверхпроводника II типа. Обычно он используется при 4,2 К, температуре кипения жидкого гелия. Он дороже, чем ниобий-титан (NbTi), но может выдерживать значения напряженности магнитного поля до 30 тесла (Тл), тогда как NbTi может выдерживать только примерно до 10 Тл. некоторые нержавеющие стали и сплав других цветных металлов. Эти сплавы прочны и часто используются в строительстве трубопроводов.
- Металл имеет низкое сечение захвата тепловых нейтронов и поэтому находит применение в атомной промышленности.
- Этот металл также используется в стержнях для дуговой сварки некоторых стабилизированных марок нержавеющей стали.
- Значительные количества ниобия в виде феррониобия высокой чистоты и никеля-ниобия используются в жаропрочных сплавах на основе никеля, кобальта и железа для таких применений, как компоненты реактивных двигателей, ракетные подузлы, а также жаростойкое и сжигающее оборудование.
 Этот металл использовался в усовершенствованных системах планера, таких как те, которые использовались в программе Gemini.
Этот металл использовался в усовершенствованных системах планера, таких как те, которые использовались в программе Gemini. - Ниобий рассматривается как альтернатива танталу в конденсаторах.
- Поскольку металлический ниобий и некоторые сплавы ниобия физиологически инертны (и, следовательно, гипоаллергенны), они используются в ювелирных изделиях и медицинских устройствах. Металлический ниобий, обработанный гидроксидом натрия, образует пористый слой, способствующий остеоинтеграции. [1]
- Наряду с титаном, танталом и алюминием, ниобий также можно подвергать электрическому нагреву и анодировать в широкий спектр цветов с помощью процесса, известного как реактивное анодирование металлов. Это делает его очень привлекательным для использования в ювелирных изделиях.
- Ниобий также добавляют в стекло для достижения более высокого показателя преломления, свойства, используемого в оптической промышленности для изготовления более тонких корректирующих стекол.

- При криогенных температурах ниобий становится сверхпроводником. При атмосферном давлении он имеет самую высокую критическую температуру среди элементарных сверхпроводников: 9,3 Кельвина (К). Кроме того, это один из трех элементарных сверхпроводников II типа (остальные — ванадий и технеций), что означает, что он остается сверхпроводником при воздействии сильных магнитных полей. Сплавы ниобий-олово и ниобий-титан используются в качестве проводов для сверхпроводящих магнитов, способных создавать чрезвычайно сильные магнитные поля. Ниобий также используется в чистом виде для изготовления сверхпроводящих ускоряющих структур для ускорителей частиц.
Меры предосторожности
Биологическая роль ниобия неизвестна. Пыль металла раздражает глаза и кожу, а также может быть пожароопасной. Ниобийсодержащие соединения относительно редко встречаются у большинства людей, но многие из них очень токсичны, и с ними следует обращаться осторожно.
См. также
- Химический элемент
- Металл
- Периодическая таблица
- Переходный металл
Сноски
- ↑ Годли, Реут и Дэвид Старосветски и Ирена Готман (2004).
 Костеподобное образование апатита на металлическом ниобии, обработанном водным раствором NaOH. Journal of Materials Science: Materials in Medicine 15: 1073–1077.
Костеподобное образование апатита на металлическом ниобии, обработанном водным раствором NaOH. Journal of Materials Science: Materials in Medicine 15: 1073–1077.
Ссылки
Ссылки ISBN поддерживают NWE за счет реферальных сборов
- Andrade, C.K.Z.; Роша, Р. О.; Русовский, Д.; и Годой, М.Н. 2005. «Исследования нуклеофильных добавок, опосредованных пентахлоридом ниобия, к энантиочистому циклическому N-ацилиминий-иону, полученному из ( S )-яблочной кислоты». Дж. Браз. хим. соц. 16: 535–539. Интернет-статья (файл .PDF). Проверено 7 августа 2007 г.
- Чанг, Раймонд. 2006. Химия (девятое изд.). Нью-Йорк: McGraw-Hill Science/Engineering/Math. ISBN 0073221031
- Коттон, Ф. Альберт и Уилкинсон, Джеффри. 1980. Передовая неорганическая химия (4-е изд.). Нью-Йорк: Уайли. ISBN 0-471-02775-8
- Fairbrother, F. 1967. Химия ниобия и тантала. Нью-Йорк: Издательство Elsevier. ASIN B0006BQA7U
- Гринвуд, Н.
 Н. и Эрншоу, А. 1998. Химия элементов (2-е издание). Оксфорд, Великобритания; Берлингтон, Массачусетс: Баттерворт-Хайнеманн, Elsevier Science. ISBN 0750633654. Онлайн-версия доступна по адресу [1]. По состоянию на 25 ноября 2006 г.
Н. и Эрншоу, А. 1998. Химия элементов (2-е издание). Оксфорд, Великобритания; Берлингтон, Массачусетс: Баттерворт-Хайнеманн, Elsevier Science. ISBN 0750633654. Онлайн-версия доступна по адресу [1]. По состоянию на 25 ноября 2006 г. - Ниобий Лос-Аламосская национальная лаборатория. По состоянию на 25 ноября 2006 г.
Внешние ссылки
Все ссылки получены 5 декабря 2018 г.
- WebElements.com – ниобий.
- Международный исследовательский центр тантала-ниобия.
- Ниобий для ускорителей частиц.
Кредиты
Энциклопедия Нового Света авторов и редакторов переписали и дополнили статью Википедии в соответствии со стандартами New World Encyclopedia . Эта статья соответствует условиям лицензии Creative Commons CC-by-sa 3.0 (CC-by-sa), которая может использоваться и распространяться с надлежащим указанием авторства. Упоминание должно быть выполнено в соответствии с условиями этой лицензии, которая может ссылаться как на авторов New World Encyclopedia , так и на самоотверженных добровольных участников Фонда Викимедиа. Чтобы процитировать эту статью, щелкните здесь, чтобы просмотреть список допустимых форматов цитирования. История более ранних вкладов википедистов доступна исследователям здесь:
Чтобы процитировать эту статью, щелкните здесь, чтобы просмотреть список допустимых форматов цитирования. История более ранних вкладов википедистов доступна исследователям здесь:
- Ниобий история
- Карбид ниобия история
- Ниобий(V)_хлорид история
- Ниобий-олово история
История этой статьи с момента ее импорта в New World Encyclopedia :
- История «Ниобия»
Примечание. На использование отдельных изображений могут распространяться некоторые ограничения, которые лицензируются отдельно.
Ниобий Цена, местонахождение, добыча и использование
Ниобий цена, возникновение, добыча и использование Ниобий [ˈnioːp] (в честь Ниобы, дочери тантала) представляет собой химический элемент с символом элемента Nb и атомным номером 41. Это один из переходных металлов. , в периодической таблице он находится в 5-м периоде и 5-й подгруппе (группа 5) или группе ванадия.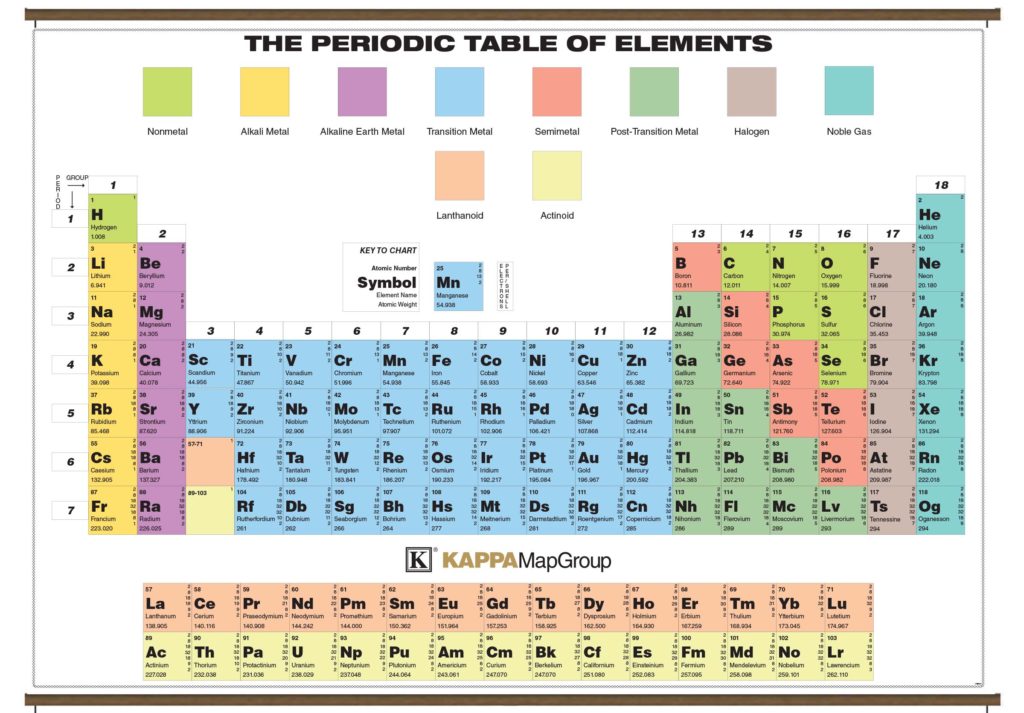
В англо-саксонской языковой зоне до сих пор многие металлурги, поставщики материалов и в частном порядке используют давно устаревшее обозначение columbium и аббревиатуру Cb .
Редко встречающийся тяжелый металл серого цвета и легко ковкий. Ниобий можно извлечь из минералов колумбита, колтана (колумбит-танталит) и лопарита. Он в основном используется в металлургии для изготовления специальных сталей и улучшения свариваемости.
Ниобий был открыт Чарльзом Хэтчеттом в 1801 году. Он нашел его в колумбитовой руде (первая находка в русле реки в Колумбии), которая была отправлена в Англию Джоном Уинтропом около 1700 года. Хэтчетт назвал элемент Колумбий . До середины 19 в. считалось, что колумбий и тантал, открытые в 1802 г., — один и тот же элемент, так как в минералах они почти всегда встречаются вместе (парагенезис).
Только в 1844 году берлинский профессор Генрих Розе показал, что ниобий и танталовая кислота — разные вещества. Не зная о работе Хэтчетта и его названии, он назвал вновь открытый элемент из-за его сходства с танталом в честь Ниобы, дочери Тантала.
Не зная о работе Хэтчетта и его названии, он назвал вновь открытый элемент из-за его сходства с танталом в честь Ниобы, дочери Тантала.
Только после 100 лет дебатов Международный союз теоретической и прикладной химии (IUPAC) в 1950 году выдвинул ниобий в качестве официального названия элемента.
В 1864 году Кристиану Вильгельму Бломстранду удалось получить металлический ниобий путем восстановления хлорида ниобия водородом при нагревании. В 1866 году Шарль Мариньяк подтвердил, что тантал является отдельным элементом.
В 1907 году Вернер фон Болтон получил очень чистый ниобий путем восстановления гептафторниобата натрием.
распространенность
Ниобий – редкий элемент с долей 1,8 · 10 в земной коре −3 %. Это не выглядит достойно. Из-за схожих ионных радиусов ниобий и тантал всегда являются братьями и сестрами. Наиболее важными минералами являются колумбит (Fe, Mn) (Nb, Ta) 2 O 6 , который также известен как ниобит или танталит в зависимости от содержания ниобия или тантала, а также пирохлор (NaCaNb 2 O 6 F).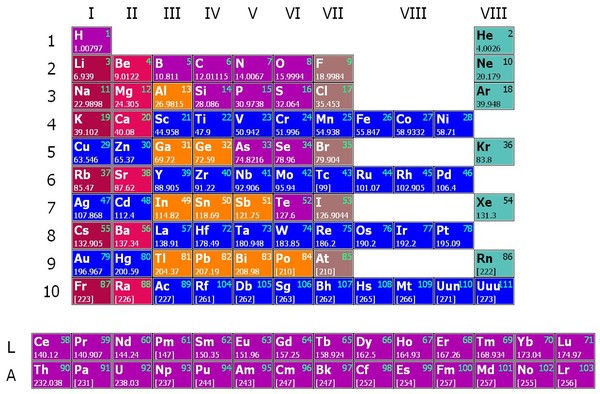
Другие в основном редкие минералы:
- Эвксенит [(Y, Ca, Ce, U, Th) (Nb, Ta, Ti) 2 O 6 ].
- Olmsteadit (KFe 2 (Nb, Ta) [O | PO 4 ] 2 · H 2 O) и
- Самарскит ((Y, He) 4 [(Nb, Ta) 2 O 7 ] 3 )
Экономический интерес представляют месторождения ниобия в карбонатитах, где в выветрелых почвах накопился пирохлор. Годовой объем производства в 2006 г. составил почти 60 000 т, 90% которых было добыто в Бразилии. В последние годы производство значительно увеличилось. Бразилия и Канада являются основными производителями ниобийсодержащих минеральных концентратов. Крупные рудные месторождения также расположены в Нигерии, Демократической Республике Конго и России.
Добыча и представление
Поскольку ниобий и тантал всегда встречаются вместе, ниобиевые и танталовые руды сначала перевариваются вместе, а затем разделяются фракционной кристаллизацией или разной растворимостью в органических растворителях. Первый такой промышленный процесс разделения был разработан Галиссаром де Мариньяком в 1866 г.
Первый такой промышленный процесс разделения был разработан Галиссаром де Мариньяком в 1866 г.
Сначала руды подвергают воздействию смеси концентрированной серной и плавиковой кислоты при температуре 50–80 °С. легко растворим.
Дикалиевые соли этих фторидов могут быть образованы путем их превращения в водную фазу и добавления фторида калия. Только фторид тантала мало растворим в воде и выпадает в осадок. Таким образом, легко растворимый фторид ниобия можно отделить от тантала. Однако в настоящее время широко распространено разделение экстракцией метилизобутилкетоном. Третья возможность разделения – фракционная перегонка хлоридов NbCl 5 и TaCl 5 . Их можно получить путем взаимодействия руды, кокса и хлора при высоких температурах.
Пентаоксид ниобия сначала получают из выделенного фторида ниобия путем взаимодействия с кислородом. Его либо сначала превращают в карбид ниобия с углеродом, а затем восстанавливают до металла с помощью дополнительного пятиокиси ниобия при 2000 ° C в вакууме, либо получают непосредственно алюминотермическим способом. Таким образом производится большая часть ниобия для сталелитейной промышленности с добавлением оксида железа для получения железо-ниобиевого сплава (60% ниобия). Если в качестве исходного материала для восстановления используются галогениды, это делается с использованием натрия в качестве восстановителя.
Таким образом производится большая часть ниобия для сталелитейной промышленности с добавлением оксида железа для получения железо-ниобиевого сплава (60% ниобия). Если в качестве исходного материала для восстановления используются галогениды, это делается с использованием натрия в качестве восстановителя.
Свойства
Ниобий — пластичный тяжелый металл с серым блеском. Известны степени окисления -3, -1, 0, +1, +2, +3, +4, +5. Как и в случае с ванадием, который в периодической таблице находится выше ниобия, уровень +5 является наиболее стабильным. Химическое поведение ниобия почти идентично поведению тантала, который находится непосредственно под ниобием в периодической таблице.
В результате образования пассивного слоя (защитного слоя) ниобий очень устойчив к воздействию воздуха. Поэтому большинство кислот не воздействуют на него при комнатной температуре. Только плавиковая кислота, особенно в смеси с азотной кислотой и горячей концентрированной серной кислотой, быстро разъедает металлический ниобий. Ниобий также нестабилен в горячих щелочах, так как они растворяют пассивный слой. При температуре выше 200°С начинает окисляться в присутствии кислорода. Сварочная обработка ниобия должна проходить в атмосфере защитного газа из-за его нестабильности на воздухе.
Ниобий также нестабилен в горячих щелочах, так как они растворяют пассивный слой. При температуре выше 200°С начинает окисляться в присутствии кислорода. Сварочная обработка ниобия должна проходить в атмосфере защитного газа из-за его нестабильности на воздухе.
Добавление вольфрама и молибдена к ниобию повышает его жаростойкость, а к алюминию – прочность.
Высокая температура перехода ниобия 9,25 К, ниже которой он является сверхпроводником, и его способность легко поглощать газы замечательны. Один грамм ниобия может поглотить 100 см³ водорода при комнатной температуре, что ранее использовалось в технологии электронных ламп.
Применение
Ниобий используется в качестве легирующей добавки для нержавеющих сталей, специальных нержавеющих сталей (например, трубы для производства соляной кислоты) и сплавов цветных металлов, так как материалы, легированные ниобием, характеризуются повышенной механической прочностью. Даже в концентрациях от 0,01 до 0,1 мас. % ниобий в сочетании с термомеханической прокаткой позволяет значительно повысить прочность и ударную вязкость стали. Первые попытки использования ниобия в качестве легирующего элемента (замена вольфрама) были предприняты в США в 1925. Очищенные таким образом стали часто используются в строительстве трубопроводов. В качестве сильного карбидообразователя ниобий также добавляют в сварочные материалы для связывания углерода.
% ниобий в сочетании с термомеханической прокаткой позволяет значительно повысить прочность и ударную вязкость стали. Первые попытки использования ниобия в качестве легирующего элемента (замена вольфрама) были предприняты в США в 1925. Очищенные таким образом стали часто используются в строительстве трубопроводов. В качестве сильного карбидообразователя ниобий также добавляют в сварочные материалы для связывания углерода.
Другие области применения включают:
- Применение в ядерных технологиях из-за низкого сечения захвата тепловых нейтронов.
- Производство стабилизированных ниобием сварочных электродов в качестве сварочных присадок для нержавеющих сталей, специальных нержавеющих сталей и сплавов на основе никеля
- Из-за своего голубоватого цвета используется для прокалывания украшений и изготовления украшений.
- В случае монет с ниобием (биметаллические монеты) цвет ниобиевой сердцевины может сильно различаться из-за физических процессов (например, монеты номиналом 25 евро из Австрии).

- Значительные количества феррониобия и ниобия никеля используются в металлургической промышленности для производства суперсплавов (сплавы на основе никеля, кобальта и железа). Из него изготавливают статические детали для стационарных и летающих газовых турбин, детали ракет и термостойкие детали для печного строительства.
- Ниобий используется в качестве материала анода в ниобиевых электролитических конденсаторах. Оксид ниобия, оксид ниобия (V), обладает высокой диэлектрической прочностью. Он наносится на поверхность ниобиевого анода в так называемом процессе формовки и служит диэлектриком в этом конденсаторе. Ниобиевые электролитические конденсаторы конкурируют с более популярными танталовыми электролитическими конденсаторами.
- Стеклянные колбы галогенных ламп снаружи с z. B. ниобия часть теплового излучения вольфрамовой нити отражается обратно внутрь. В результате можно достичь более высокой рабочей температуры и, следовательно, большей светоотдачи при меньшем потреблении энергии.

- В качестве катализатора (например, при производстве соляной кислоты и при производстве спиртов из бутадиена),
- В виде ниобата калия (химическое соединение калия, ниобия и кислорода), который используется в качестве монокристалла в лазерной технике и для нелинейных оптических систем
- Использование в качестве электродного материала для натриевых ламп высокого давления
- Сверхпроводимость: При температурах ниже 9,5 К чистый ниобий является сверхпроводником II типа. Сплавы ниобия (с N, O, Sn, AlGe, Ge) относятся к трем чистым элементам: ниобию, ванадию и технецию, а также к веществам типа II. , номер 3 Sn) и 23,2 К (ниобий германий, Nb 3 Ge). Сверхпроводящие объемные резонаторы из ниобия используются в ускорителях частиц (включая XFEL и FLASH в DESY в Гамбурге). Для создания сильных магнитных полей до 20 Тесла используются сверхпроводящие магниты с проводами из ниобия-олова и ниобия-титана. Например, для экспериментального термоядерного реактора ИТЭР используется 600 тонн ниобия-олова и 250 тонн ниобия-титана.
 Сверхпроводящие магниты LHC также изготовлены из ниобиевых сплавов.
Сверхпроводящие магниты LHC также изготовлены из ниобиевых сплавов.
инструкции по технике безопасности
Хотя ниобий считается нетоксичным, металлическая ниобиевая пыль раздражает глаза и кожу. Ниобиевая пыль легко воспламеняется.
Физиологический механизм действия ниобия неизвестен.
| Общий | ||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Название, условное обозначение, атомный номер | Ниобий, Nb, 41 | |||||||||||||||||||||||||||||||||||||||||||||
| Серия | Переходные металлы | |||||||||||||||||||||||||||||||||||||||||||||
| Группа, точка, блок | 5, 5, д | |||||||||||||||||||||||||||||||||||||||||||||
| Внешний вид | серый металлик | |||||||||||||||||||||||||||||||||||||||||||||
| Номер CAS | 7440-03-1 | |||||||||||||||||||||||||||||||||||||||||||||
| Массовая доля земной оболочки | 19 частей на миллион | |||||||||||||||||||||||||||||||||||||||||||||
| Атомный | ||||||||||||||||||||||||||||||||||||||||||||||
| атомная масса | 92, | и | ||||||||||||||||||||||||||||||||||||||||||||
| Атомный радиус (расчетный) | 145 (164) м. | |||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 137 вечера | |||||||||||||||||||||||||||||||||||||||||||||
| электронная конфигурация | [Кр] 4d 4 5s 1 | |||||||||||||||||||||||||||||||||||||||||||||
| 1. ионизация | 652,1 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||
| 2. ионизация | 1380 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||
| 3. ионизация | 2416 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||
| 4. ионизация | 3700 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||
| 5. ионизация | 4877 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||
| Физически | ||||||||||||||||||||||||||||||||||||||||||||||
| Физическое состояние | фиксированный | |||||||||||||||||||||||||||||||||||||||||||||
| кристаллическая структура | кубический объемно-центрированный | |||||||||||||||||||||||||||||||||||||||||||||
| плотность | 8,57 г/см 3 (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||
| Твердость по шкале Мооса | 6,0 | |||||||||||||||||||||||||||||||||||||||||||||
| магнетизм | парамагнитный ( = 2,3 10 −4 ) | |||||||||||||||||||||||||||||||||||||||||||||
| температура плавления | 2750 К (2477°С) | |||||||||||||||||||||||||||||||||||||||||||||
| точка кипения | 5017 К (4744°С) | |||||||||||||||||||||||||||||||||||||||||||||
| Молярный объем | 10,83 · 10 −6 м 3 / моль | |||||||||||||||||||||||||||||||||||||||||||||
| Теплота парообразования | 690 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||
| теплота плавления | 26,8 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||
| скорость звука | 3480 м/с при 293,15 К | |||||||||||||||||||||||||||||||||||||||||||||
| Электропроводность | 6,58 · 10 6 А / (В · м) | |||||||||||||||||||||||||||||||||||||||||||||
| теплопроводность | 54 Вт/(м·К) | |||||||||||||||||||||||||||||||||||||||||||||
| Химическая промышленность | ||||||||||||||||||||||||||||||||||||||||||||||
| степени окисления | 2, 5 | |||||||||||||||||||||||||||||||||||||||||||||
| нормальный потенциал | −1,1 В (Nb 2+ + 2 e – → Nb) | |||||||||||||||||||||||||||||||||||||||||||||
| электроотрицательность | 1,6 (шкала Полинга) | |||||||||||||||||||||||||||||||||||||||||||||
| изотоп | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| ЯМР свойства | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| инструкции по технике безопасности | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||


 — М.: Советская энциклопедия, 1984—1991.
— М.: Советская энциклопедия, 1984—1991.



 Костеподобное образование апатита на металлическом ниобии, обработанном водным раствором NaOH. Journal of Materials Science: Materials in Medicine 15: 1073–1077.
Костеподобное образование апатита на металлическом ниобии, обработанном водным раствором NaOH. Journal of Materials Science: Materials in Medicine 15: 1073–1077.  Н. и Эрншоу, А. 1998. Химия элементов (2-е издание). Оксфорд, Великобритания; Берлингтон, Массачусетс: Баттерворт-Хайнеманн, Elsevier Science. ISBN 0750633654. Онлайн-версия доступна по адресу [1]. По состоянию на 25 ноября 2006 г.
Н. и Эрншоу, А. 1998. Химия элементов (2-е издание). Оксфорд, Великобритания; Берлингтон, Массачусетс: Баттерворт-Хайнеманн, Elsevier Science. ISBN 0750633654. Онлайн-версия доступна по адресу [1]. По состоянию на 25 ноября 2006 г.

 Сверхпроводящие магниты LHC также изготовлены из ниобиевых сплавов.
Сверхпроводящие магниты LHC также изготовлены из ниобиевых сплавов. }
} }
}