Анодная защита металла от коррозии – Электрохимическая защита
alexxlab | 25.09.2019 | 0 | Разное
катодная защита от коррозии, анодная, протекторная, электрохимическая
Комплексная защита металла от коррозийных процессов основывается на:
- понижении коррозионных процессов путем наложения внешнего тока;
- ослаблении агрессивных свойств среды;
- увеличении химического сопротивления металлических конструкций;
- изоляции поверхностей от агрессивной среды.
В первых двух случаях в технологическую среду вводятся особые химические соединения – ингибиторы, или может быть использована электрохимическая защита. Эти методы позволяют при необходимости формировать новые защитные системы, которые минимизируют коррозию изделия при перемене условий эксплуатации.
Два последних метода, по большей части, относятся к химической защите и осуществляются на этапе проектирования, еще до начала эксплуатации готовых изделий или конструкций. Это может быть как подбор необходимых материалов, так и обработка изделий гальваническими или другими сберегающими составами (герметики, клеи). Чаще всего эти способы применяются при изготовлении строительных конструкций, металлических каркасов и арматуры.
Электрохимическая защита
Предохранение металла от коррозии путем наложения внешнего постоянного электрического тока, при котором радикально меняется электродный потенциал материала и изменяется скорость его коррозии, называется электрохимической защитой. Она надежно оберегает поверхности от коррозии, предотвращая разрушение подземных резервуаров, трубопроводов, днищ судов, газгольдеров, гидротехнических сооружений, газопроводов и т. п. Используется такой метод в тех случаях, когда коррозийный потенциал находится в зоне интенсивного распада или при пассивации, то есть когда происходит активное разрушение металлоконструкций.
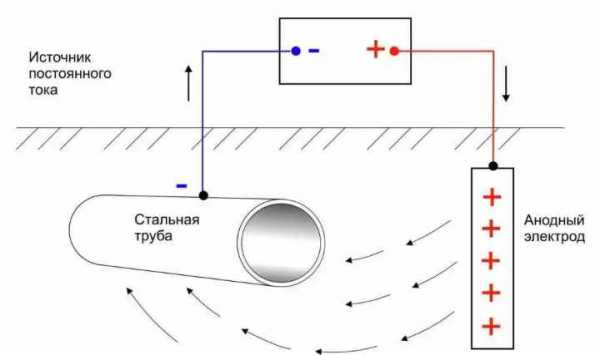
Принцип действия электрохимической защиты
К металлической конструкции извне подключается источник постоянного электрического тока. На поверхности изделия электрический ток формирует катодную поляризацию электродов, в результате чего совершается обмен, и анодные участки трансформируются в катодные. Вследствие этого, под воздействием коррозионной среды происходит разрушение анода, а не исходного материала. Такого рода защита подразделяется на катодную и анодную, зависит это от того в какую сторону (отрицательную или положительную) сдвигается потенциал металла.
Катодная защита от коррозии
Для повышения устойчивости металлических деталей при соприкосновении с какой-либо агрессивной средой или при эксплуатации с воздействием морской воды или почвы, применяется катодная защита от коррозии. При этом катодная поляризация сохраняемого металла достигается формированием микрогальванической пары с другим металлом (алюминий, цинк, магний), понижением скорости катодного процесса (деаэрация электролита) или наложением электротока от внешнего источника.
Такой прием, как правило, применяется для сохранения черных металлов, потому что из них изготавливается большая часть объектов размещающихся в почве и воде – например, пирсы, свайные сооружения, трубопроводы. Широкое применение данный метод нашел и в машиностроении, при профилактике коррозийных процессов новых и находящихся в эксплуатации машин, при обработке кузова автомобиля, полостей лонжеронов, узлов шасси и т. п. Следует заметить, что этим же способом производится эффективная защита днища автомобиля, которое наиболее часто подвергается воздействию агрессивных сред.
Катодная защита, при многих достоинствах, все же имеет и недостатки. Один из них – переизбыток защиты, такое явление отмечается при сильном смещении потенциала сохраняемого изделия в отрицательную сторону. В результате – хрупкость металла, коррозионное растрескивание материала и разрушение всех предохраняющих покрытий. Ее разновидностью является защита протекторная. При ее использовании к сберегаемому изделию присоединяется металл с отрицательным потенциалом (протектор), который впоследствии, сохраняя объект, разрушается.
Анодная защита
Анодная защита от коррозии металла применяется для изделий, изготовленных из высоколегированных железистых сплавов, углеродистой и кислотоупорной стали, расположенных в коррозионных средах с хорошей электропроводностью. При этом способе потенциал металла сдвигается в положительную сторону до того времени, пока не достигнет стабильного (пассивного) состояния.
Анодная электрохимическая установка включает в себя: источник тока, катод, электрод сравнения и сохраняемый объект.
Для того чтобы защита была максимально эффективной для какого-либо конкретного предмета, необходимо соблюсти определенные правила:
- свести к минимуму количество трещин, щелей и воздушных карманов;
- качество сварных швов и соединений металлоконструкций должно быть максимальным;
- катод и электрод сравнения должны быть помещены в раствор и находиться там постоянно.
Оставить комментарий
Как защитить металлы от коррозии? Виды и способы +Видео
 Как нам известно, что под воздействием окружающей среды портятся любые материалы и металлические изделия и стройматериалы не являются исключением, поэтому рассмотри лучшие методы защиты металла от коррозии.
Как нам известно, что под воздействием окружающей среды портятся любые материалы и металлические изделия и стройматериалы не являются исключением, поэтому рассмотри лучшие методы защиты металла от коррозии.
Коррозию невозможно убрать полностью, но снизить ее воздействие при этом увеличив срок эксплуатации изделий из металла вполне возможно.
Очень важным фактором является обработка металлических изделий и конструкций от коррозии, потому что данная процедура значительно увеличит их срок эксплуатации.
Виды антикоррозийной защиты
Защиту от коррозии условно подразделяют на два вида:
- когда ее применяют до начала использования конструкции или изделия и
- когда изделие или конструкция уже пребывают в использовании.
Первый вид способствует высокой сопротивляемости «химическому» воздействию. Изолирует прямой контакт с агрессивными средами (поверхностная изоляция).
Второй вид способствует снижению агрессивной окружающей среды (это будет зависеть от условий использования).

Применение электромагнитных полей, например, «наложение» внешних электрических токов, регулирование плотности и другие методики.
Использование видов защиты от коррозии выбирается индивидуально для каждого изделия и конструкции.
Так же это зависит от следующих факторов:
- Вид металла;
- Условия эксплуатации;
- Трудность проведения обработки антикоррозийными составами;
- Экономическая целесообразность;
- Производственные возможности.
Подробности о методах защиты
Все методики можно разделить:
- на активные (которые постоянно воздействуют на металл),
- пассивные (многоразового применения),
- технологические (применяют на этапе производства образцов).
Активные методики
Катодная защита от коррозии
Такую методику используют в тех случаях, если среда, контактирующая с металлом, является электропроводящей. На материал подают большой «минусовой» потенциал, данная процедура позволяет предотвращать его окисление.
Протекторная защита от коррозии
Является катодной поляризацией. Экземпляр связывают с контактом с материалом, который больше всего подвержен окислению в этой токопроводящей среде (проектором). Он как бы является своеобразным громоотводом, то есть принимает весь негатив агрессивных веществ на себя.
Но такого рода протектор требует периодической замены.
Анодная защита от коррозии
Этот вариант применяют очень редко, и он заключается в поддержке «инертности» материала по отношению к окружающей среде.
Пассивные
Создание защитной плёнки

Популярная и низко затратная методика предотвращения коррозии. Чтобы создать поверхностный слой применяют специальные вещества. Данные вещества должны быть не активными по отношению к агрессивным химическим соединениям, быть не электропроводными и иметь хорошую адгезию.
Все вещества для обработки металла перед применением находиться в жидком или аэрозольном состоянии, от этого будет зависеть способ нанесения.
Чтобы обработать металл используют лакокрасочные составы, разные полимеры или мастики.
Металлоконструкция в «желобах» для защиты
Используют для трубопроводов и инженерных систем. В качестве изолятора в этом случае, выступает воздушная прослойка, которая находится между внутренними стенками канала и металлом.
Фосфатирование
Так же металлы обрабатывают специальными окислителями. Такие окислители вступают с основой в реакцию и в результате на ее поверхности образуются отложения малорастворимых химических соединений.
Такой способ защиты от влаги считается очень эффективным.
Покрытие металла устойчивыми материалами

В этом случае, изделия из металла «хромируют», «оцинковывают» серебрят и тому подобное. Так же в качестве защиты металла выступает бетон, стекло, керамика, цементные растворы и так далее.
Пассивация

Данная манипуляция состоит в том, чтобы достаточно резко снизить химическую активность металла. В этом случае, поверхность металла обрабатывают специальными реактивами.
Уменьшение агрессивности среды — применения веществ, которые снижают коррозийные процессы (ингибиторы).
Осушение воздуха — это химическая очистка воздуха от различных вредных примесей и применение других методик, которые применимы в быту.
Гидрофобизация грунта – это засыпка в него специальных веществ для снижения агрессивности почвы.
Обработка ядохимикатами – применяют в тех случаях, когда существует вероятность развития биокоррозии.
Технологический способ защиты
Легирование – на основе металла изготавливают сплав устойчивый к агрессивным воздействиям.
Но такой способ можно реализовать только на промышленных производствах.
И так как вы поняли по вышеперечисленной информации не каждую методику антикоррозийной обработки можно использовать в бытовых условиях.
То есть получается возможности «частника» очень ограничены. В этой статье мы описали несколько способов антикоррозийной обработки металлов и надеемся, что данная информация была вам полезной. Желаем вам удачи и терпения!
ТОП 9 магазинов, где я выгодно закупаюсь
ТОП 7 по товарам и мебели для дома:
7 лучших строительных и мебельных магазинов!
- Akson.ru- это интернет-гипермаркет строительных и отделочных материалов!
- homex.ru- HomeX.ru предлагает большой выбор качественных отделочных, материалов, света и сантехники от лучших производителей с быстрой доставкой по Москве и России.
- Instrumtorg.ru – это интернет – магазин строительного, автомобильного, крепежного, режущего и другого инструмента, необходимого каждому мастеру.
- Qpstol.ru – “Купистол” стремится предоставить лучший сервис своим клиентам. 5 звёзд на ЯндексМаркет.
- Lifemebel.ru- гипермаркет мебели с оборотом более 50 000 000 в месяц!
- Ezakaz.ru- Представленная на сайте мебель изготавливается на собственной фабрике в Москве, а так же проверенными производителями из Китая, Индонезии, Малайзии и Тайваня.”
- Mebelion.ru- – крупнейший интернет-магазин по продаже мебели, светильников, интерьерного декора и других товаров для красивого и уютного дома.
domsdelat.ru
АНОДНАЯ ЗАЩИТА – это… Что такое АНОДНАЯ ЗАЩИТА?
- АНОДНАЯ ЗАЩИТА
см. Электрохимическая защита.
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
- АННУЛЕНЫ
- АНОДНОЕ ОКСИДИРОВАНИЕ
Смотреть что такое “АНОДНАЯ ЗАЩИТА” в других словарях:
анодная защита — Электрохимическая защита металла, способного пассивироваться анодной поляризацией, осуществляемая от внешнего источника тока или посредством соединения с металлом, имеющим более положительный потенциал, чем у защищаемого металла. [ГОСТ 5272 68]… … Справочник технического переводчика
анодная защита — [anodic protection] электро химическая защита металлов от коррозии, при которой защищаемое изделие является анодом; направлена на прекращение работы локальных анодных участков смещением потенциала в анодную область пассивного состояния… … Энциклопедический словарь по металлургии
Анодная защита — 122. Анодная защита Электрохимическая защита металла, способного пассивироваться анодной поляризацией, осуществляемая от внешнего источника тока или посредством соединения с металлом, имеющим более положительный потенциал, чем у защищаемого… … Словарь-справочник терминов нормативно-технической документации
Анодная защита — Anodic protection Анодная защита. (1) Метод снижения скорости коррозии металла путем поляризации его в пассивную область, где уровень растворения низок. (2) Наложение внешнего электрического потенциала, для того чтобы защитить металл от… … Словарь металлургических терминов
анодная защита — anodinė apsauga statusas T sritis chemija apibrėžtis Vienas metalų apsaugos nuo korozijos būdų: korozinis potencialas didinamas anodine poliarizacija iki pasyviosios būsenos potencialo. atitikmenys: angl. anodic protection rus. анодная защита … Chemijos terminų aiškinamasis žodynas
Защита от коррозии — (антикоррозионная защита) – способы и средства, предотвращающие или уменьшающие коррозию бетонных или железобетонных конструкций, арматуры. [Терминологический словарь по бетону и железобетону. ФГУП «НИЦ «Строительство» НИИЖБ им. А. А.… … Энциклопедия терминов, определений и пояснений строительных материалов
ЗАЩИТА ОТ КОРРОЗИИ — конструкционных материалов в агрессивных средах основана на: 1) повышении коррозионной стойкости самого материала; 2) снижении агрессивности среды; 3) предотвращении контакта материала со средой с помощью изолирующего покрытия; 4) регулировании… … Химическая энциклопедия
защита осушением — [induced current protection] способ защиты металлов от коррозии, заключающийся в помещении изделия в замкнутый герметический закрытый объем со средой осушеного воздуха или инертного газа; Смотри также: Защита металлов электрохимическая защита … Энциклопедический словарь по металлургии
Защита металлов — [metal protection] совокупность способов (процессов) противокоррозийной защиты металлов и сплавов в разных средах, а также проблемы теории и практики борьбы с коррозией: Смотри также: электрохимическая защита протекторная защита защита осушением… … Энциклопедический словарь по металлургии
Анодная зона — участок подземного металлического сооружения, на котором это сооружение имеет положительный электрический потенциал по отношению к окружающей среде. Источник: snip id 5429: Руководство по проектированию и защите от коррозии подземных… … Словарь-справочник терминов нормативно-технической документации
dic.academic.ru
Защита металлов от коррозии анодное окисление
Наиболее распространена защита алюминия и его сплавов от коррозии электрохимическим оксидированием, при котором окисление достигается действием электрического тока (см. работу 5 этого раздела). Алюминиевые изделия помещают в электролит в качестве анода, поэтому метод обработки носит название — анодное окисление, или анодирование. При анодировании на алюминии и его сплавах получают пленки толщиной 5—20 мк, а в специальных случаях до 200—300 мк. Анодирование применяется не только для защиты от коррозии и улучшения адгезии (сцепления) с лакокрасочными покрытиями, но и для декоративной отделки поверхности металла, получения на ней фотоизображений, повышения стойкости против истирания, получения поверхностного электро- и теплоизоляционного слоя и слоя высокой твердости. Твердость анодной окисной пленки на чистом алюминии 1500 кг/мм , т. е. выше, чем твердость закаленной инструментальной стали. С помощью анодных пленок алюминия изготовляют алюминиевые выпрямители и конденсаторы. В последнее время анодная окисная пленка используется как подслой для лучшего сцепления алюминия с гальваническими покрытиями (хромом, никелем, серебром и др.). [c.146]Защитные покрытия на неорганической основе. Многие металлические предметы (детали приборов и оружия, измерительные инструменты ИТ. п.) защищать от коррозии лакокрасочными покрытиями нельзя. Защита таких деталей от коррозии осуществляется покрытием их тончайшей окисной пленкой. Этот метод защиты металлов от коррозии называется оксидированием, а образующиеся при этом окисные пленки — оксидными. Оксидирование различных деталей осуществляется различными приемами 1) обработкой горячим раствором щелочи и селитры, 2) анодным окислением в растворе щелочи или в расплаве нитрата и нитрита натрия, 3) обработкой в атмосфере водяного пара и 4) обработкой в кислых электролитах. [c.315]
Ниобий несколько менее стоек к коррозии, чем тантал, и, подобно последнему, подвержен водородному охрупчиванию, если гальванический контакт или внешняя э. д. с. делают его катодным, а также при экспозиции в горячем водороде. Металл подвергается анодному окислению в кислых электролитах с образованием анодной окисной пленки, характеризующейся большой диэлектрической постоянной и высоким анодным потенциалом пробоя. Последнее свойство в сочетании с хорошей электропроводностью металла позволило использовать ниобий в качестве подложки для платиновых металлов при изготовлении анодов катодной защиты наложенным током, а также при производстве конденсаторов. [c.181]
Подготовленный таким методом висмутовый электрод сравнения непригоден для анодной защиты металлов от коррозии, когда требуется непрерывное длительное измерение потенциала защищаемого объекта. Чтобы получить стабильный в течение длительного времени потенциал висмутового электрода сравнения, нами предложен электрод, на поверхность которого нанесен объемный поверхностный слой оксидов методом электролитического или химического окисления. [c.97]
Электрохимическое анодное окисление позволяет получать пленки различной твердости, эластичности, пористости и толщины (до 0,8 мл1). Такие пленки служат хорошей защитой от коррозии и электрического пробоя, улучшают некоторые механические и физико-химические свойства металла. Свойства пленок зависят от состава электролита и условий их нанесения. [c.394]
На ход процесса коррозии большое влияние оказывают окис-ные пленки, образующиеся на поверхности металла. Так, например, алюминий в атмосферных условиях устойчивее железа, хотя обладает более высоким отрицательным электродным потенциалом. Объясняется это тем, что на воздухе алюминий легко окисляется, покрываясь плотной плёнкой окиси, предохраняющей затем металл от дальнейшего окисления. Пленка же окиси железа рыхлая и не изолирует поверхность металла от соприкосновения с воздухом. Процесс коррозии при этом распространяется в глубь металла. С образованием защитных окис-ных пленок связано пассивирование металлов. Это явление заключается в том, что некоторые довольно активные металлы (Сг, А1 и др.) теряют свою активность после обработки концентрированной азотной кислотой или после анодного окисления. Наиболее распространенными способами защиты металлов от коррозии является нанесение на их поверхность изолирующих пленок. [c.284]
При катодном покрытии (например, 5п на железе) очень важна герметичность. Пока слой защищающего металла не нарушен, металл хорошо сохраняется. Но при обнажении металла хотя бы в одном месте начнет энергично разрушаться защищаемый металл (Ре под слоем олова). Для защиты от коррозии на поверхности металла искусственно создают окисные, окисно-хроматные, фосфатные, сульфидные и другие пленки обработкой изделий специальными химическими составами. Широко применяют анодное окисление путем электролиза в кислой среде в присутствии окислителей. Скорость кислотной коррозии уменьшают введением в кислоту замедлителей (ингибиторов) коррозии. Коррозионная стойкость железа повышается введением легирующих добавок (нержавеющие стали содержат добавки Сг, N1 и других металлов). [c.285]
Защита от коррозии путем воздействия на анодные или катодные участки поверхности обеспечивается противокоррозионными пигментами. В зависимости от механизма действия различают пигменты-ингибиторы и пигменты-пассиваторы. Анодное ингибирование достигается пигментами, обладающими способностью принимать электроны или увеличивать pH среды и вследствие химических процессов окисления или гидратации образовывать на анодных участках защитные пленки. Результатом их действия является смещение электродных потенциалов металлов в более положительную сторону, в том числе в область пассивного состояния, в которой коррозии металла не происходит. Приведенные ниже данные показывают сдвиг стационарного потенциала стали в воде под влиянием добавок пигментов [c.164]
Пассивация анодов имеет большое практическое значение создание нерастворимых (инертных) анодов для проведения процессов разряда анионов, реакций окисления веществ образование оксидных пленок с целью защиты металлов от коррозии. При проведении анодного процесса с растворением металла пассивирование анода — вредное явление, которое необходимо ослабить и устранить. [c.318]
Покрытие более благородным металлом (анодная защита) может оказаться целесообразным в тех случаях, когда окисление основного металла ведет к замедлению коррозии за счет пассивации, связанной
www.chem21.info
Анодная защита металлов от коррозии
Анодная защита металлов от коррозии [c.71]Б. Определение параметров проектируемых систем электрохимической защиты. Основными параметрами систем электрохимической (протекторной, катодной или анодной) защиты металлов от коррозии являются [c.9]
АНОДНАЯ ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ [c.1]
Анодная защита металлов от коррозии.— М. Хи-мия, 1983.— 184 с., ил. [c.2]
В книге обобщен многолетний опыт исследования, разработки и внедрения анодной защиты металлов от коррозии. Значительная часть экспериментального материала выполнена в головной лаборатории анодной электрохимической защиты металлов от коррозии Минхимпрома. [c.7]
Подготовленный таким методом висмутовый электрод сравнения непригоден для анодной защиты металлов от коррозии, когда требуется непрерывное длительное измерение потенциала защищаемого объекта. Чтобы получить стабильный в течение длительного времени потенциал висмутового электрода сравнения, нами предложен электрод, на поверхность которого нанесен объемный поверхностный слой оксидов методом электролитического или химического окисления. [c.97]
Регулятор потенциала предназначен для анодной защиты металлов от коррозии как в промышленных, так и в лабораторных условиях. Прибор можно использовать для длительного электросинтеза органических соединений и металлографического правления. [c.111]
В чем сущность анодной защиты металла от коррозии [c.190]
Таким образом, имеется принципиальная возможность катодной и анодной защиты металлов от коррозии. Однако, как будет показано ниже, величины защитных потенциалов значительно отличаются от теоретических значений. Во многих случаях при Е1 коррозия не предотвращается, а усугубляется. [c.43]
Анодная электрохимическая защита металлов от коррозии [c.321]
Анодная электрохимическая защита металлов от коррозии— сравнительно новый и очень специфический метод. Он основан на переходе металла из активного состояния в пассивное вследствие смещения его потенциала при анодной поляризации от внешнего источника тока. [c.69]
Теоретически полная защита металла от коррозии при катодной поляризации возможна тогда, когда металлу будет сообщен потенциал более отрицательный, чем термодинамический потенциал металла. Величина защитного эффекта при некотором смещении потенциала Дф определяется катодной и анодной поляризуемостью Дф/Дг системы. Катодная защита эффективна тогда, когда металл обладает большой катодной поляризуемостью и малой анодной, т. е. для смещения потенциала системы до потенциала защиты фз нужны относительно небольшие токи. Во всех случаях электрохимическая защита эффективна в средах с достаточно высокой электропроводностью. Как правило, ее широко применяют для защиты от коррозии в морской воде, в почвах, в грунтовых водах и т. п. [c.141]
Известно, что в крепких растворах едкого натра пу-.. тем анодной обработки получают весьма прочные оксидные пленки, которые используют для защиты металла от коррозии. Оксидная пленка состоит из различных окислов железа. [c.43]
Совершенствование метода анодной электрохимической защиты металлов от коррозии обусловило ряд новых требований к инженерным решениям аппаратуры, особенно к средствам контроля и регулирования потенциала,— высокая надежность [c.116]
ПРОМЫШЛЕННОЕ ПРИМЕНЕНИЕ АНОДНОЙ ЭЛЕКТРОХИМИЧЕСКОЙ ЗАЩИТЫ МЕТАЛЛОВ ОТ КОРРОЗИИ [c.136]
Изложенные в этой книге материалы показывают, что анодная электрохимическая защита металлов от коррозии сформировалась как самостоятельное направление в науке о коррозии. [c.171]
Защита металлов от коррозии в нейтральных электролитах может быть осуществлена как ингибиторами, так и пассиваторами. При этом под ингибиторами следует понимать любое соединение, которое подавляет коррозию, вне зависимости от того, на какую электрохимическую реакцию оно влияет. К пассиваторам будем относить лишь те соединения, которые уменьшают скорость коррозии благодаря преимущественному торможению анодной реакции. В согласии с этими определениями ингибитор может и не являться пассиватором, но любой пассиватор будет ингибитором. [c.9]
Многочисленные известные, а также все вновь появляющиеся методы защиты металлов от коррозии могут быть рассмотрены на основе характера оказываемого ими торможения на ту или иную стадию электрохимической коррозии или изменения ими степени термодинамической нестабильности системы. В этом случае в соответствии с основным выражением электрохимической коррозии (1) методы защиты металлов можно классифицировать следующим образом (см. табл. 2). В качестве способов защиты находят практическое применение как методы, базирующиеся на уменьшении степени термодинамической нестабильности, так и методы, основанные на торможении кинетики катодных и анодных процессов, и в несколько меньшей степени — методы, действие которых обусловлено увеличением общего омического сопротивления коррозионной системы. [c.10]
Электрохимической называется защита металла от коррозии, осуществляемая принудительной анодной или катодной поляризацией. [c.228]
Электрохимическая защита металла от коррозии происходит за счет катодной поляризации металла до потенциала, при котором замедляется процесс ионизации (рис. 9.9). Анодному процессу растворения металла и сопровождающему его катодному процессу соответствуют равновесные потенциалы д и Е . Коррозионный потенциал ор при этом соответствует точке пересечения поляризационных кривых. Если при катодной поляризации будет достигнута плотность катодного тока, равная то потенциал металла снизится до величины В этих условиях металл будет частично защищен от коррозии, так как скорость растворения уменьшится до величины, соответствующей плотности тока /кор. Если же плотность катодного тока возрастает до /защ, то потенциал металла понизится до величины и на его поверхности будет протекать только катодный процесс. [c.281]
К настоящему времени доказано [4—6], что растворение металлов (электрохимический процесс) — результат протекания сопряженных и независимых катодной и анодной реакций, скорость которых, согласно законам электрохимической кинетики, определяется общим значением потенциала на границе металл — раствор, составом раствора и условиями диффузии компонентов или продуктов реакции в растворе. Скорость окислительной и восстановительной реакций выражается через плотность анодного и катодного токов. Электрохимические принципы защиты металлов от коррозии [7, 8] вытекают из анализа коррозионных диаграмм (рис. 1), на которых представлены в зависимости от потенциала истинные скорости возможных в системе металл — раствор анодных и катодных реакций. Защита металла от коррозии достигается либо электрохимической защитой — искусственным поддержанием потенциала вблизи равновесного потенциала анодной реакции ф [c.9]
В последние годы особенно интенсивно предпринимались шаги к внедрению анодной защиты металлов от коррозии в промышленность как в Советском Союзе, так и за рубежом. Впервые в Советском Союзе промышленная проверка анодной за-Ш.ИТЫ теплообменников для 76—907о-ной серной кислоты была осуществлена в 1964 г., поскольку сернокислотные среды наиболее часто применяются в промышленных системах анодной защиты. [c.136]
Электрохимическая защита металлов от коррозии основана на уменьшении скорости коррозии металлических конструкций вутём их катодной и анодной поляризации. Наиболее распространена так называемая катодная защита металла, которая мсшет осуществляться присоединением защищаемой металлической конструкции к отрицательному полюсу внешнего источника постоянного тока или к металлу, имеющему более отрицательный потенциал (протекторная. защита). [c.36]
Для защиты металлов от коррозии в щелях возможно применять ингибиторы. Однако следует учитывать, что пополнение концентрации ингибиторов в щели затруднено и поэтому требуется введение в раствор повышенной концентрации ингибиторов. В циркуляционных и перемешиваемых системах, где доступ ингибитора в щель несколько увеличивается, разница в требуемой концентрации не так велика, как в спокойных, неперемешиваемых электролитах. Эффективное средство подавления коррозии металлов в узких зазорах — это применение смесей анодных ингибиторов, один из которых должен обладать окислительными свойствами. [c.14]
Частичная или полная защита металла от коррозии превращением его в катод, используя или гальванический, или внешний ток. Противоположно Anodi prote tion —Анодной защите. [c.914]
Как известно, для защиты металла от коррозии при отсутствии напряжений успешно применяется электрохимическая защита. Она производится с помощью протектора, изготовленного из значительно менее благородного металла, т. е. имеющего значительно более отрицательный электродный потенциал, чем металл защищаемого объекта или анодных покрытий (см. VI—8), или при помощи катодной поляризации защищаемого объекта от внешнего источника тока. Благодаря электрохимической защите местные коррозионные пары на металле должны перестать работать и весь защищаемый объект должен сделаться катодным. Основы электрохимической защиты разработаны и описаны Г. В. Акимовым [1, 2] и Н. Д. Томашевым [151]. [c.179]
В книге содержатся теоретические и инженерные сведения об исполь зовании искусственно наведенной пассивности в практике защиты металлов от коррозии. Изложены общие представления об анодной защите металлов, коррозионно-электрохимическом поведении углеродистой и нержавеющих сталей, титана и анодной защите их в различных электропроводящих средах. Большое внимание уделено аппаратурному оформлению метода като дам, электродам сравнения, средствам регулирования и контроля потенциала, автоматическим системам. Описан новый вариаит защиты — анодная защита с дополнительным катодным протектором. Приведены примеры промышленного применения анодной защиты, показаны эффективность и экономичность этого вида зашиты. [c.2]
При защите металлов от коррозии наиболее эффективен метод, который тормозит основную контролирующую стадию данного электрохимического процесса, т. е. когда основной фактор защиты данного метода совпадает с контролирующим фактором данного коррозионного процесса. При одновременном применении нескольких методов защиты металла от коррозии, как привило, легче достичь более полной защиты, если все эти методы действуют преимущественно на основную контролирующую стадию электрохимического коррозионного процесса. Например, при уменьшении коррозии металла добавлением анодных ингибиторов (пассиваторов) усиление эффекта защиты достигается также введением катодных присадок в сплав или дополнительной анодной поляризацией, т. е. рядом методов, тормозящих анодный процесс. Наоборот, одновременное применение нескольких методов, действующих на различные контролирующие стадии электрохимической коррозии, будет, как правило, менее эффективным, а иногда и вредным. Например, если ограничение коррозии металла достигнуто методами, тормозящими анодный процесс (легирование стали хромом, добавкой окислителей или анодных ингибиторов в раствор), то нерационально одновременно применять методы, тормозящие катодный процесс (устранение катодных включений в сплаве, уменьше- [c.48]
В работе Пальмера не было достаточно изучено влияние pH. Полная защита металла от коррозии только хроматами часто требует очень высоких концентраций этого замедлителя коррозии, в отдельных случаях до 10 000 мг/л. В замкнутых системах охлаждения, в тех случаях, когда высокая концентрация хроматов надежно предотвращает язвенную коррозию и образование наростов ржавчины, нет особой надобности заменять хроматирование дианод-ным методом. Однако в большинстве случаев это не имеет места и применение дианодного метода в таких системах дает большой положительный эффект. Дианодный метод пригоден и при наличии трубок из адмиралтейской латуни, а также для защиты и других металлов. Если вследствие наличия неплотностей в систему проникает h3S, то эффективность ди-анодного метода надает, так как сероводород разрушает хроматы. [c.104]
Обзорная статья И. Л. Розенфельда посвящена подведению итогов в области развития теории защиты металлов от коррозии ингибиторами и синтезу новых летучих ингибиторов коррозии. РассА1атривается новый принцип создания ингибиторов коррозии, заключающийся не в торможении анодного процесса, а в ускорении катодного, приводящего, благодаря наличию аномальной зависимости скорости растворения металла от потенциала, к переводу металла в пассивное состояние. В обзоре рассмотрены такие вопросы, как механизм защиты металлов летучими ингибиторами, адсорбция, методы исследования упругости паров, электрохимия летучих ингибиторов и т. д. Описываются свойства синтезированных соединений и методы их использования в качестве универсальных летучих ингибиторов. [c.7]
Металлические покрытия широко применяются для защиты металлов от коррозии во многих отраслях промышленности. Их различают по способу нанесения 1) погружение в расплавленный металл 2) диффузионный 3) распыление 4) механотерми-ческий (плакирование) 5) гальванический, а также по механизму электрохимической защиты [1]. В последнем случае различают анодные и катодные покрытия. [c.169]
Катодная защита внещним током — защита металла от коррозии с помощью постоянного тока от внешнего источника. При этом защищаемый металл присоединяют к отрицательному полюсу внешнего источника (т. е. в качестве катода), а к положительному полюсу присоединяют дополнительный электрод, поляризуемый анодно. [c.198]
mash-xxl.info
Методы защиты от коррозии
Методы защиты от коррозии можно объединить в следующие группы:
1) нанесение защитных покрытий и пленок;
2) изменение электрохимического потенциала защищаемого материала по отношению к среде на границе фаз;
3) модификация коррозионной среды.
Борьба с коррозией с применением защитных покрытий является наиболее распространенным способом. В качестве защитных применяют металлические и неметаллические покрытия.
Металлические покрытия могут быть выполнены из металла более или менее благородного, чем подложка. В связи с этим они делятся на две группы: катодные и анодные покрытия.
К катодным покрытиям относятся те покрытия, электрохимический потенциал которых в данных условиях больший, чем у защищаемого металла. На алюминий почти всегда наносят катодные покрытия. Покрытия из благородных металлов на стали имеют такой же характер. Катодные покрытия защищают металл только благодаря его изоляции от атакующей среды. Поэтому свою роль они выполняют только при наличии полной сплошности. Если в катодном покрытии образуется щель, то в условиях коррозии она становится катодом, а открытая часть защищаемого металла – анодным элементом. Анодная поверхность при этом значительно меньше, чем катодная. Электрохимическое разрушение металла концентрируется на небольшой поверхности. Учитывая опасности, кроющиеся в возможных несплошностях катодных покрытий, их делают сравнительно большой толщины.
Анодные покрытия – это покрытия, выполненные из металла, у которого электродный потенциал меньше, чем у защищаемого металла. Для железа, работающего в малокислых или нейтральных растворах, анодными покрытиями являются цинк, алюминий. Защитные свойства анодных покрытий состоят не только в механической изоляции металла от коррозионной среды. Они заключаются еще и в электрохимическом воздействии. В случае нарушения покрытия и образования коррозионного элемента, защищаемый металл, являющийся катодом, не разрушается. Небольшие несплошности в анодных покрытиях не опасны.
Металлические покрытия наносят электроосаждением, погружением в расплавленные металлы, металлизацией напылением, химическим осаждением солей, диффузией и т. д. В последнее время все большее распространение получает нанесение покрытий в вакууме.
Неметаллические покрытия применяются в случае возникновения химической реакции металла в соответствующих средах. К ним, в частности, относят оксидные алюминиевые покрытия, полученные в ходе специального электролитического процесса. Фосфатные покрытия применяются в большинстве случаев с дополнительными защитными средами, как, например, краски, лаки и т. п. Фосфатирование стали состоит в погружении изделия в разбавленный раствор фосфорной кислоты и кислых фосфатов цинка или магния. В результате реакции образуется нерастворимый фосфат железа, который в ходе процесса плотно покрывает поверхность металла. К этой же группе относят керамические покрытия и стекловидные эмали. Эти покрытия достаточно стойки к воздействию минеральных и органических кислот. Их недостатком является повышенная хрупкость и низкая стойкость в условиях резких перепадов температуры.
К органическим покрытиям относятся разнообразные лакокрасочные материалы.
Знание механизма коррозии позволило создать методы коррозионной защиты путем наложения на металл такого потенциала, при котором он становится термодинамически устойчивым. К таким методам относятся катодная защита и уменьшение агрессивности среды, окружающей металлоконструкцию.
Катодная защита состоит в присоединении к защищаемой конструкции анода-протектора с более отрицательным электрохимическим потенциалом. Протектор (лат. protector – покровитель, защитник) и служит таким анодом, препятствующим разрушению защищаемого сплава; сам протектор при коррозии постепенно разрушается.
Протектором может являться любой металл, имеющий по отношению к данному сплаву более отрицательный потенциал. Однако разница в потенциалах не должна быть слишком большой, чтобы при электрохимическом процессе не происходило быстрого разрушения протектора.
Протекторы представляют собой обычно небольшие пластинки, присоединяемые к защищаемой детали заклепками или болтами. Катодную или протекторную защиту широко применяют при защите от морской и подземной коррозии металлоконструкций, коммуникаций, трубопроводов, сосудов и т. д. В качестве анодов-протекторов для защиты стальных изделий обычно применяют сплавы магния или цинка. Защита может также осуществляться присоединением защищаемого металла к отрицательному полюсу постоянного тока.
Для уменьшения агрессивности окружающей среды в нее вводят добавки, называемые ингибиторами коррозии, которые или способствуют пассивации металла, или значительно снижают скорость его коррозии. Условием использования ингибиторов является эксплуатация изделия в замкнутой среде постоянного состава.
Различают анодные и катодные ингибиторы. В качестве анодных ингибиторов коррозии используют различные вещества, образующие нерастворимые соединения на анодных участках. Одним из таких пассиваторов является хромпик К2Сr207, вводимый в количестве 2 – 3 г/л в раствор охлаждающей жидкости.
Катодные ингибиторы тормозят катодный процесс. К их числу относятся различные травильные присадки, добавляемые в количестве 1 – 2 % в кислоты для снятия окалины без разрушения основного металла.
Летучие ингибиторы, такие как нитрат натрия NaNO2, применяют для пропитки бумаги, в которую заворачивают детали, подлежащие хранению или транспортировке. Испаряясь, они насыщают окружающее детали пространство, создавая защитную газовую среду. Летучие ингибиторы отличаются высокой эффективностью. Стальные изделия, завернутые в бумагу, обработанную NaNO2, в условиях относительной влажности 85 % не ржавеют в течение 5 лет. Преимуществом летучих ингибиторов является отказ от применения защитных покрытий, удобство расконсервации и постоянная готовность деталей к немедленному использованию без дополнительной обработки.
uas.su
Защита металлов от коррозии
Для защиты металлов от коррозии применяют различные методы и их комбинации:
1. Создание рациональных форм конструкций машин и механизмов, в которых не должно быть мест скопления грязи и влаги – очагов коррозии.
2. Легирование металлов – введение в сплавы добавок повышающих коррозионную стойкость. Например, нержавеющие стали содержат 12-20% хрома и добавки других металлов (Ni, Mn, Ti, Co, Nb, Mo), которые позволяют создавать сплавы, устойчивые в различных коррозионных средах. На поверхности таких сплавов формируется защитная пленка, обладающая высокой адгезией к металлу, коэффициентом объемного расширения таким же, как у металла, высокой химической стойкостью.
Другим примером коррозионностойкого сплава является латунь – двойной или многокомпонентный сплав на основе меди с легирующим компонентом – цинком. В латуни различных марок вводят добавки – Sn, Ni, Pb, Mn, Fe. Из латуней изготовляют очень ответственные детали морских судов, электромашин, вкладыши подшипников, детали часовых механизмов, теплотехническую и химическую аппаратура.
3. Изоляция поверхности металлаот агрессивной средыдостигается нанесением на нее различных покрытий.
Покрытия бывают металлические и неметаллические, которые в свою очередь подразделяются на химические и лакокрасочные.
Металлические покрытия получают в результате лужения (нанесения слоя олова) никелирования, хромирования, оцинкования. Металлические покрытия подразделяют на катодные и анодные.
Катодные покрытия – это покрытия менее активным металлом, нарушение которого приводит к анодному растворению основного металла. Так луженое железо при нарушении защитного оловянного покрытия подвергается анодному растворению, поскольку железо является более активным металлом.
Анодные покрытия – покрытия более активным металлом, нарушение которого ведет к его постепенному растворению. Например, оцинкованное железо в нейтральной среде:
А(–): Zn –2ē = Zn2+
К(+): O2 + H2O + 4ē = 4OH–
Zn + O2 + 2OH– = Zn(OH)2
Неметаллические химические покрытия наносятся методом фосфатирования и оксидирования.
• Фосфатирование – формирование на поверхности чугуна, углеродистой стали, кадмия, цинка, меди, алюминия слоя малорастворимых фосфатов железа, цинка или марганца действием препарата МАЖЕФ (сокращение от – марганец, железо, фосфор).
• Оксидирование – формирование оксидных пленок на поверхности металлических изделий. Это покрытие может использоваться и как декоративное. Наносится химическим и электрохимическим путем. Поверхность железа подвергается обработке в щелочных растворах, при этом постепенно формируется защитная оксидная пленка: Fe → Na2FeO2 → Na2Fe2O4 → Fe3O4.
Лакокрасочные покрытия (ЛКП). К лакокрасочным материалам относятся эмали, лаки, краски, шпаклевки, грунтовки. Их наносят на металл слоями. Например, на кузов автомобиля, который предварительно обработан фосфатирующим составом наносят грунтовку, которая обеспечивает высокую адгезию (сцепление) покрытия с подложкой и защиту металла от электрохимической коррозии. Затем грунтованную поверхность шпаклюют. Шпаклевкой выравнивают поверхность, удаляют дефекты, трещины, царапины, поры. После высыхания слоя шпаклевки наносят слои эмали, лака. Это несколько упрощенная схема дает представление о составе и строении ЛКП.
4. Электрохимическая защита основана на том, что можно изменить скорость коррозии металла, сдвигая его потенциал пропусканием внешнего тока. Рассмотрим катодную и анодную защиту.
Катодная защитаможет осуществляться двумя способами:
1)Наложение катодного тока, т.е. подключение защищаемого изделия в качестве катода к внешнему источнику тока. При этом анодом служат инертные вспомогательные электроды. Таким способом защищают буровые платформы, подземные трубопроводы.
2) Протекторная защита – защита изделия посредством контакта с более активным металлом (более электроотрицательным), который является анодом. Электрохимическое растворение протектора обеспечивает протекание катодного тока через защищаемый металл. Металл-протектор (магний, цинк, алюминий и их сплавы) постепенно полностью растворяется. Такой вид защиты очень эффективен. Его используют для защиты днищ морских судов, трубопроводов и др.
Анодная защита эффективна для металлов с незавершенными d-электронными слоями (Fе, Ni, Cr, Mo, Ti, Zr) которые при смещении их потенциала от потенциала коррозии в анодную сторону переходят в пассивное состояние. При этом ток растворения металла падает в десятки раз. Перевод металла в пассивное состояние осуществляется током большой плотности. Поддержание металла в пассивном состоянии требует наложения незначительного по величине тока. Например, пассивация нержавеющей стали в 66%-ном растворе H2SO4 при t = 24°С осуществляется током 6 А/м2, а поддержание этого состояния – 10–3А/м2. Токи анодной защиты обычно меньше токов катодной защиты. Это делает анодную защиту весьма эффективной.
5. Изменение свойств коррозионной среды. Скорость разрушения металла можно уменьшить путем удаления или снижения концентрации веществ, вызывающих коррозию, или внедрения в среду замедлителей коррозии – ингибиторов.
Ингибиторная защита – введение в агрессивную среду ингибиторов (органических или неорганических веществ, небольшие количества которых резко снижают скорость коррозии металла, предотвращая его разрушение).
Этот метод отличается высокой экономичностью, легким внедрением в производство, не требует дополнительно специального оборудования.
Ингибиторы используются для защиты металлов в водно-солевых, кислотных, щелочных, в водно-органических и органических средах, при коррозии в атмосферных условиях, почве и т.д.
Введение ингибитора в агрессивную среду вызывает изменение кинетики электродных реакций. Эффективность и механизм действия ингибитора, зависит от природы металла, строения ингибитора, свойств агрессивной среды, условий протекания процесса коррозии (температура, гидродинамика).
Выбор способа защиты определяется условиями работы металла и экономикой.
Электролиз
Электрохимический процесс, в котором электрическая энергия превращается в химическую – электролиз, который проводится в электролизере.
Электролизер – электрохимическая система, состоящая из электродов и электрохимической ванны с раствором или расплавом электролита. Электродами называются проводники с электронной проводимостью, находящиеся в контакте с ионным проводником. Для протекания процесса электроды соединяют с источником постоянного тока при помощи проводов. Катод электролизера соединяется с отрицательным полюсом источника тока, на нем проходит восстановление ионов электролита избытком электронов от источника тока. Анод соединен с положительным полюсом, на нем проходят процессы окисления.
Похожие статьи:
poznayka.org

