Аргон формула газ: Аргон (Ar) – Ingas
alexxlab | 21.06.2023 | 0 | Разное
Argon | SIAD
Навигационная цепочка
Argon header
Контакты generico
Контакты
+7.495.7213026
Ссылка на страницу
Argon
- ТЕХНИЧЕСКИЕ СВОЙСТВА
- ПРИМЕНЕНИЕ
- БЕЗОПАСНОСТЬ
- ПРОИЗВОДСТВО
- СПОСОБЫ ПОСТАВКИ
Аргон – благородный газ, который составляет 0,93 процента атмосферы Земли.
Благородные газы – группа редких газов, которая включает аргон, гелий, криптон, неон, ксенон и, иногда, радон. Они показывают большую стабильность и чрезвычайно низкие степени реакции.
Технические Свойства
Продукт: аргон
Химическая формула : Ar
Уровень чистоты: ≥ 99.996%
Относительная плотность (воздух = 1): 1.38
Вид: бесцветный газ
Запах : газ без запаха
Точка воспламенения в воздухе: негорючий
Прочие свойства: нетоксичный, не коррозийный; показывает низкую тепловую проводимость и небольшую растворимость в воде.
Технические свойства
Аргон используется для нескольких типов применения, которые перечислены ниже.
Производство алюминия
В алюминиевой промышленности аргон используется:
- Для замены воздуха или азота, создавая благоприятную инертную атмосферу
- Чтобы помочь в удалении нежелательных растворимых газов во время дегазации
- Чтобы удалить растворённый водород и макрочастицы из литого алюминия.
Обработка и производство cтали
В сталелитейной промышленности аргон используется:
- Чтобы заместить газ или пар и предотвратить окисление
- Чтобы получить постоянную температуру и однородный состав при перемешивании литой стали
- Чтобы помочь в удалении нежелательных растворимых газов во время дегазации
- Как транспортирующий газ, чтобы определить состав образца путём газовой хроматографии
- Чтобы прогнать угарный газ и уменьшить потери хрома при аргонокислородном обезуглероживании (A.
 O.D.) Используется при очистке нержавеющей стали.
O.D.) Используется при очистке нержавеющей стали.
Производство металлопрордукции
При производстве металлопрордукции аргон используется:
- Для создания инертного газового щита при сварке
- Для создания безкислородной и безазотной среды при отжиге и прокате металлов и сплавов
- Для промывки литых металлов, чтобы устранить пористость отливков.
Производство полупроводников
В производстве полупроводников аргон используется:
- Для создания защитной атмосферы и среды, передающей высокую температуру, для выращивания германиевых и кремниевых кристаллов.
Освещение
В освещении аргон используется:
- Для заполнения ламп накаливания и флуоресцентных ламп
- Для создания синего света в лампах неонового типа.
Хоть он и не является токсичным, аргон в высоких концентрациях может вызвать удушье. Кроме того, контакт с жидким аргоном может причинить холодные и морозные ожоги. Чтобы избежать этих вредных последствий, производители и клиенты должны следовать строгим правилам безопасности при хранении газа и при обращении с ним, а также сверяться с нашим посвящённым аргону Информационным листком по безопасности материалов.
Чтобы избежать этих вредных последствий, производители и клиенты должны следовать строгим правилам безопасности при хранении газа и при обращении с ним, а также сверяться с нашим посвящённым аргону Информационным листком по безопасности материалов.
Побочный продукт производства кислорода и азота, аргон, добывается для коммерческих целей посредством технологии разделения воздуха. Этот процесс состоит из разделения компонентов, содержавшихся в воздухе:
- азот (78 %)
- кислород (21 %)
- аргон (0,9 %)
- другие газы (0,1 %).
Существующие сегодня промышленные установки представляют собой эволюцию процесса Клода-Линде, названного так по именам двух ученых, французского и немецкого, которые внесли вклад в его разработку; для охлаждения воздуха они первоначально применяли изоэнтальпическое расширение, только со снижением давления, и, позже изоэнтропическое расширение, с производством энергии.
Установка состоит из двух колонн, одна над другой, работающих при различных давлениях с газовым потоком (восходящим) и жидкостным потоком (нисходящим), в равновесии между газообразным и жидкостным состояниями. Когда поток достигает вершины колонны, там увеличивается концентрация азота, а ближе к основанию увеличивается концентрация кислорода.
Когда поток достигает вершины колонны, там увеличивается концентрация азота, а ближе к основанию увеличивается концентрация кислорода.
Аргон получают в третьей фракционирующей ректификационной колонне, в которой процесс дистилляции повторяется на смеси аргона и кислорода, взятой из промежуточной точки верхней колонны.
Существующие установки для разделения воздуха достигли высокой степени автоматизации, и управление ими осуществляется через компьютер; система управления руководит полным циклом производства и последующей стадией распределения продукта до места хранения или использования.
На заводе в Озио-Сопра (Osio Sopra), лучшем из существующих в Италии предприятий в сфере промышленных газов и самом крупном промышленном производстве SIAD, новая установка для разделения воздуха T 1000, запущенная в сентябре 1997 года, заменила собой часть старых заводов, выдавая производительность равную 1300 тонн кислорода в день.
Завод был разработан компанией SIAD MACCHINE IMPIANTI.
Варианты поставки аргона и услуги, доступные клиентам SIAD, включают:
- Транспортировку в баллонах, блоках баллонов или резервуарах
- Проектирование и установку систем распределения газа
- Поставку оборудования для правильного использования газа
- Помощь и техническое консультирование по транспортировке, распределению и применению газа.
Аргон может также поставляться:
- со степенью чистоты 5.0 – 5.5 – 5.8
- в специальных и калибровочных смесях с различным составом, по запросу.
Способы поставки
Аргон: температура, состояния, сварка
Аргон (обозначается как Ar) — наиболее часто встречающийся в воздухе инертный газ. Он отличается полной химической инертностью. Это свойство позволяет широко применять газ в таких областях, как сварка, упаковка, производство материалов высокой чистоты, а также для тушения пожаров.
История открытия
Предыстория открытия Ar началась в 1785 году. Выдающийся ученый и естествоиспытатель из Великобритании Генри Кэвендиш исследовал состав воздуха. Он подвергал азот окислению и взвешивал получившиеся окислы. По окончании опыта в сосуде оставался газ. Кэвендиш определил его объем в 0,8% от начального объема воздуха. Состав этого газа ученый определить не смог. Спустя столетие к проблеме вернулись сэры Джон Рэлей и Уильям Рэмзи. В ходе проведенных опытов они обнаружили, что азот, выделенный из воздуха, имеет большую плотность, нежели азот, получаемый в ходе реакции разложения нитрита аммония. в 1884 году им удалось выделить из воздуха некий газ, более плотный, чем азот. Это вещество имело одноатомную молекулярную структуру и было крайне инертным – т.е. не реагировало с другими веществами. На заседании Королевского Общества новому газу было присвоено название «аргон», что в переводе с древнегреческого значило «спокойный, ленивый»
Выдающийся ученый и естествоиспытатель из Великобритании Генри Кэвендиш исследовал состав воздуха. Он подвергал азот окислению и взвешивал получившиеся окислы. По окончании опыта в сосуде оставался газ. Кэвендиш определил его объем в 0,8% от начального объема воздуха. Состав этого газа ученый определить не смог. Спустя столетие к проблеме вернулись сэры Джон Рэлей и Уильям Рэмзи. В ходе проведенных опытов они обнаружили, что азот, выделенный из воздуха, имеет большую плотность, нежели азот, получаемый в ходе реакции разложения нитрита аммония. в 1884 году им удалось выделить из воздуха некий газ, более плотный, чем азот. Это вещество имело одноатомную молекулярную структуру и было крайне инертным – т.е. не реагировало с другими веществами. На заседании Королевского Общества новому газу было присвоено название «аргон», что в переводе с древнегреческого значило «спокойный, ленивый»
Аргон в природе
Ввиду практически полной инертности Ar представлен в естественной среде исключительно в несвязанном виде. Его процентная доля в различных частях Земли равна приблизительно:
Его процентная доля в различных частях Земли равна приблизительно:
- земная кора – 0,00012%;
- морская вода – 0,00045%;
- атмосфера – 0,926%.
Доля Ar в воздухе выше, чем суммарная доля всех остальных инертных газов. Основным источником для его добычи служит наша атмосфера. В коре Земли аргон содержится также в виде радиоактивного изотопа Аргон-40 и появляется в ходе реакции распада изотопов Калия. Современная наука вместе с остальными инертными газообразными элементами относит Ar к VIII группе периодической системы.
Как добывают аргон
Благодаря значительному с промышленной точки зрения содержанию аргона в воздухе его получают в качестве дополнительного продукта криогенной ректификации O2 и N2. Технология основана на том факте, что температура кипения (или сжижения) Ar лежит между температурами N2 и O2. Перед началом процесса воздух подвергается тщательной очистке от пыли в многоступенчатых фильтрах, осушается от водяных паров, а далее мощными компрессорами сжимается до тех пор, пока не перейдет в жидкое состояние.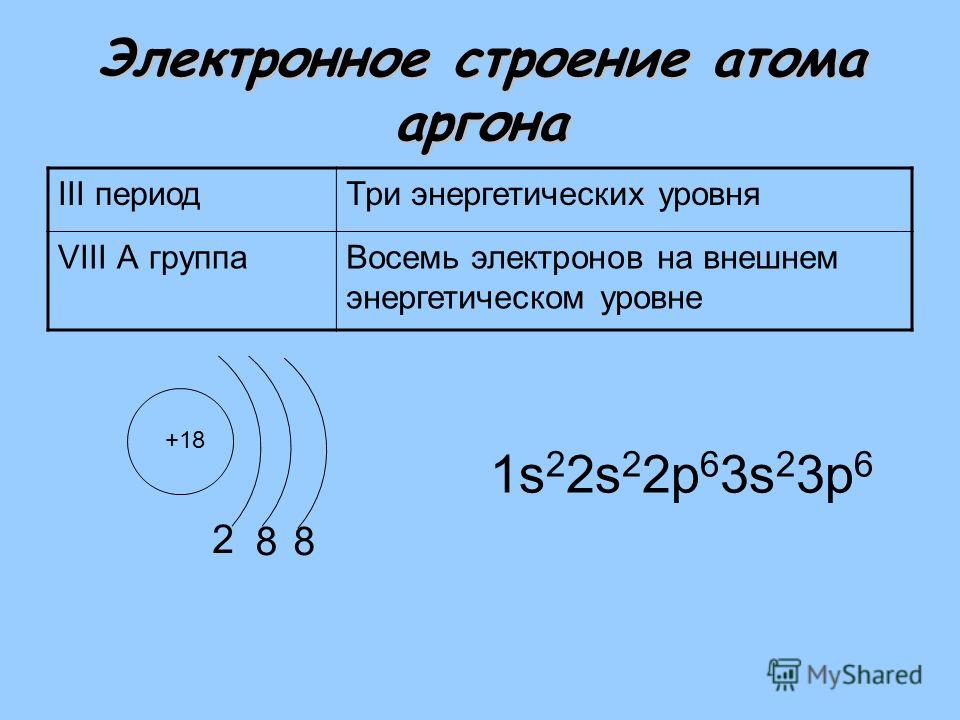 Жидкость перегоняют в ректификационной колонне, чтобы разделить ее на отдельные вещества. Первым испаряется азот при -195 °С, его пары собираются на соответствующей тарелке ректификатора и отводятся в отдельный резервуар. Следующим по высоте (и при температуре кипения -185 °С) отбирается аргонная фракция, содержащая 12% Ar, менее полпроцента азота и кислород. Она подается в следующую ректификационную колонну, в которой процентная доля Ar доводится до 85, оставшееся приходится на кислород со следами азота. Такое вещество называется сырым аргоном, исходным материалом для получения очищенного газа.
Жидкость перегоняют в ректификационной колонне, чтобы разделить ее на отдельные вещества. Первым испаряется азот при -195 °С, его пары собираются на соответствующей тарелке ректификатора и отводятся в отдельный резервуар. Следующим по высоте (и при температуре кипения -185 °С) отбирается аргонная фракция, содержащая 12% Ar, менее полпроцента азота и кислород. Она подается в следующую ректификационную колонну, в которой процентная доля Ar доводится до 85, оставшееся приходится на кислород со следами азота. Такое вещество называется сырым аргоном, исходным материалом для получения очищенного газа.
В промышленности применяется несколько методов очистки сырого аргона от примесей.
Водород, добавляемый в состав сырья, окисляется на катализаторе и нагреве до 500 °С, таким образом, из состава смеси выводится кислород. Образовавшийся на катализаторе водяной пары удаляют при посредстве влагоотделителя. Газ после этого осушают. Аргон с оставшимся в нем азотом вновь ректифицируют. Применяются и альтернативные методы получения Ar. Во время синтеза аммиака из азота и водорода в химических реакторах Ar получают как сопутствующий продукт производства. Технологический компонент это синтеза – продувочный газ – содержит до 20% Ar. Из этого газа и извлекают самый спокойный элемент. Стоимость производства, складывающаяся в основном из затрат на охлаждение и нагрев компонентов, делится между аммиаком и аргоном, и получается существенно ниже. Качество газа, получаемого любым методом, определяется технологией очистки его от небольших количеств остаточного N2, O2, водяных паров и H2. Аппарат, получающий ионные пучки аргона[/caption]
Применяются и альтернативные методы получения Ar. Во время синтеза аммиака из азота и водорода в химических реакторах Ar получают как сопутствующий продукт производства. Технологический компонент это синтеза – продувочный газ – содержит до 20% Ar. Из этого газа и извлекают самый спокойный элемент. Стоимость производства, складывающаяся в основном из затрат на охлаждение и нагрев компонентов, делится между аммиаком и аргоном, и получается существенно ниже. Качество газа, получаемого любым методом, определяется технологией очистки его от небольших количеств остаточного N2, O2, водяных паров и H2. Аппарат, получающий ионные пучки аргона[/caption]
Общая характеристика Ar
Ar входит в группу инертных газов. Заряд его ядра – 18, под таким же номером элемент располагается в таблице Менделеева. Из всех участников VIIIA группы он является наиболее часто встречающимся в природе. Объемная доля Ar в атмосфере -0,93%, массовая доля составляет 1,28%.Элемент является газом без цвета, вкуса и запаха. Химически не активен – аргон не вступает в реакцию и практически не соединяется ни с какими элементами или веществами, за исключением CU(Ar)O, и гидрофторида аргона. Весьма плохо растворим водой, чуть большая растворимость наблюдается при взаимодействии с органическими растворителям.
Химически не активен – аргон не вступает в реакцию и практически не соединяется ни с какими элементами или веществами, за исключением CU(Ar)O, и гидрофторида аргона. Весьма плохо растворим водой, чуть большая растворимость наблюдается при взаимодействии с органическими растворителям.
Виды аргона
Говоря о видах, или сортах Ar, надо понимать, что это одно и то же химическое вещество. Виды различаются по степени очистки от примесей.
- Высший сорт. Содержание Ar не менее 99,99% . Этот сорт особо высокой чистоты применяется для ответственных сварочных работ, таких, как сварка материалов, химически активных в нагретом состоянии: некоторые цветные сплавы, прежде всего титановые, нержавеющая сталь и др. Используется также для сварки высоконагруженных изделий из конструкционной стали.
- Первый сорт. Содержание Ar не менее 99,98%, Применяется при сварке сплавов на основе алюминия с другими металлами и сплавами, для менее активных цветных металлов.
- Второй сорт.
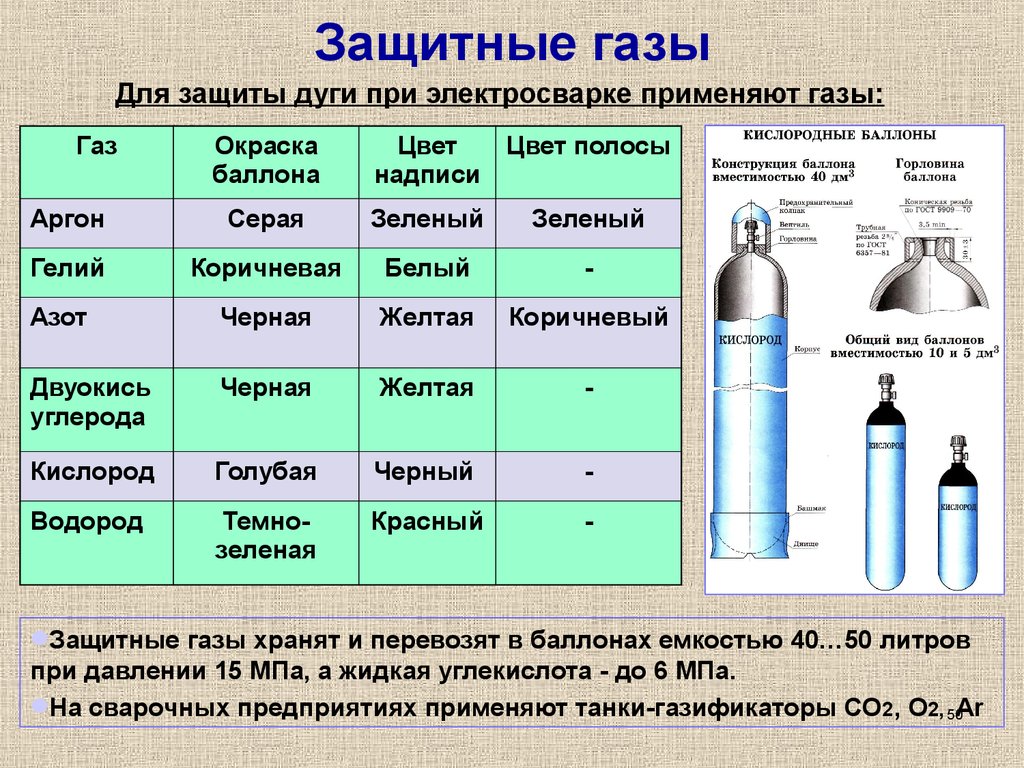 Содержание Ar не менее 99,95%. Используется при сваривании деталей из жаростойких стальных сплавов, алюминия и конструкционных сталей. Применение чистого Ar в этих случаях нежелательно, поскольку приводит к повышенной пористости материала шва и не позволяет защитить сварочную ванну от повышенной влажности и других загрязнений. Во избежание возникновения такого дефекта в состав смеси защитных газов добавляют углекислый газ и кислород, связывающие выделяющийся при сварке водород и другие примеси. Образующиеся в ходе этих реакций шлаки всплывают на поверхность сварочной ванны и после застывания удаляются вместе с окалиной.
Содержание Ar не менее 99,95%. Используется при сваривании деталей из жаростойких стальных сплавов, алюминия и конструкционных сталей. Применение чистого Ar в этих случаях нежелательно, поскольку приводит к повышенной пористости материала шва и не позволяет защитить сварочную ванну от повышенной влажности и других загрязнений. Во избежание возникновения такого дефекта в состав смеси защитных газов добавляют углекислый газ и кислород, связывающие выделяющийся при сварке водород и другие примеси. Образующиеся в ходе этих реакций шлаки всплывают на поверхность сварочной ванны и после застывания удаляются вместе с окалиной.
Физические и химические свойства
Свойства аргона типичны для члена VIII группы. При обычной температуре Ar пребывает в газообразном состоянии. Молекула включает в себя единственный атома, химическая формула весьма простая: Ar. Температура кипения весьма низка : -185,8 °С при атмосферном уровне давления. Растворимость в воде низкая – всего 3,29 мл на 100 мл жидкости Плотность аргона при нормальных условиях составляет 1,78 кг/м3. Молярная теплоемкость газа- 20,7 Дж/Кмоль. Газ практически полностью инертен. На сегодняшний день ученым удалось получить лишь два его соединения – CU(Ar)O, и гидрофторид аргона. Соединения существуют лишь при сверхнизких температурах. Предполагается, что Ar может входить в состав неустойчивых в нормальном состоянии молекул эксимерного типа. Такие молекулы могут существовать лишь в возбужденном состоянии, например, в ходе электроразряда высокой интенсивности. Такие соединения возможны с ртутью, кислородом и фтором. Электроотрицательность по шкале Полинга равна 4,3.
Молекула включает в себя единственный атома, химическая формула весьма простая: Ar. Температура кипения весьма низка : -185,8 °С при атмосферном уровне давления. Растворимость в воде низкая – всего 3,29 мл на 100 мл жидкости Плотность аргона при нормальных условиях составляет 1,78 кг/м3. Молярная теплоемкость газа- 20,7 Дж/Кмоль. Газ практически полностью инертен. На сегодняшний день ученым удалось получить лишь два его соединения – CU(Ar)O, и гидрофторид аргона. Соединения существуют лишь при сверхнизких температурах. Предполагается, что Ar может входить в состав неустойчивых в нормальном состоянии молекул эксимерного типа. Такие молекулы могут существовать лишь в возбужденном состоянии, например, в ходе электроразряда высокой интенсивности. Такие соединения возможны с ртутью, кислородом и фтором. Электроотрицательность по шкале Полинга равна 4,3.
Как степень окисления, так и электродный потенциал имеют нулевое значение, что характерно для инертного газа.
Ионный радиус составляет 154, радиус ковалентности – 106 Пм. Ионизационный порог- 1519 кдж/моль
Ионизационный порог- 1519 кдж/моль
Атомная и молекулярная масса
Такие важные параметры, как атомная и молекулярная массы, показывают, насколько масса молекулы вещества и масса его атома соответственно превышают значение, равное одной двенадцатой доле массы атома водорода. Ввиду того, что молекула Ar состоит из единственного атома, молекулярная и атомная масса аргона идентичны и составляют 39,984.
Изотопы
В природных условиях Ar встречается в качестве трех устойчивых изотопов
- 36Ar– процентная доля этого изотопа составляет 0,337% в ядре 18 протонов и 18 нейтронов;
- 38Ar- его доля всего 0,063%, в ядре 18 протонов и 20 нейтронов;
- 40Ar – наиболее распространен, его доля составляет 99,6%, в ядре так же 18 протонов, но уже 22 нейтрона.
Искусственным путем удавалось получать изотопы с массовым индексом от 32 до 55, наиболее стабильным из них оказался  Большая процентная доля 40Ar среди изотопов, встречающихся в природе, вызвана постоянным образованием его в ходе реакции распада изотопа калий-40. На 1000 кг калия в ходе таких реакций за год образуется не более 3100 атомов 40Ar. Но, поскольку эти реакции идут постоянно в течение сотен миллионов лет, изотоп накопился в природе в существенных объемах. Доминирование тяжелого изотопа в природе обуславливает тот факт, что атомный вес Ar превышает атомный вес калия, находящегося в таблице следом за ним. При создании Периодической системы такого противоречия не было, поскольку аргон был обнаружен и свойства его были исследованы значительно позже, в первом десятилетии XX века. Первоначально Ar был помещен в первую группу таблицы, восьмая группа была выделена позднее.
Большая процентная доля 40Ar среди изотопов, встречающихся в природе, вызвана постоянным образованием его в ходе реакции распада изотопа калий-40. На 1000 кг калия в ходе таких реакций за год образуется не более 3100 атомов 40Ar. Но, поскольку эти реакции идут постоянно в течение сотен миллионов лет, изотоп накопился в природе в существенных объемах. Доминирование тяжелого изотопа в природе обуславливает тот факт, что атомный вес Ar превышает атомный вес калия, находящегося в таблице следом за ним. При создании Периодической системы такого противоречия не было, поскольку аргон был обнаружен и свойства его были исследованы значительно позже, в первом десятилетии XX века. Первоначально Ar был помещен в первую группу таблицы, восьмая группа была выделена позднее.
Ионы
Как и другие инертные газы (такие, как He и Ne), Ar подвержен ионизации. При возбуждении атомов и сообщении им высоких энергий возникают молекулярные ионы Ar2+.
Молекула и атом
Для инертных газов эти понятия идентичны, поскольку эти элементы не желают вступать в химическую связь даже с себе подобными. Молекула включает в себя один атом, химическая формула газа не отличается от обозначения элемента: Ar.
Молекула включает в себя один атом, химическая формула газа не отличается от обозначения элемента: Ar.
Молярная масса
Молярная масса аргона составляет 39,95 г/моль. Существуют несколько методов ее вычисления:- С применением относительной атомной массы M и коэффициента пропорциональности к, выражающего соотношение между относительной массой и молярной. Этот коэффициент является универсальной константой и равен для всех элементов. Молярная масса M выражается как произведение коэффициента пропорциональности на относительную массу.
- С использованием молярного объема. Потребуется найти объем, занимаемый при обычных условиях некоторой массой газа, далее рассчитать массу 22,4 литров вещества при таких же условиях.
- С применением уравнения Менделеева-Клапейрона, моделирующего идеальный газ.
pV = mRT / M,
проведя преобразования, получим выражение для молярной массы:
M=mRT/pV
где
- p – давление в паскалях,
- V –объем в кубометрах
- m – масса в граммах,
- Т – температура в Кельвинах,
- R – константа, значение которой 8,314 Дж/(моль×К).

Область применения
Шире всего аргон применяется при сварочных работах. Он используется для создания защитной атмосферы вокруг сварочной ванны, вытесняя из рабочей зоны O2 и N2, содержащиеся в атмосфере. Особенно важно это для сварки цветных металлов, многие из которых, к примеру, Ti, отличаются высокой химической активностью в нагретом состоянии. Незаменим инертный газ также для неразъемного соединения нержавеющих и высоколегированных сплавов. Также широко применяется при монтаже высоконагруженных строительных конструкций, таких, как каркасы высотных зданий, фермы мостов и многих других. Здесь его применение обеспечивает высокое качество, однородность и долговечность ответственных соединений. В строительной индустрии аргонная сварка доминирует среди других методов.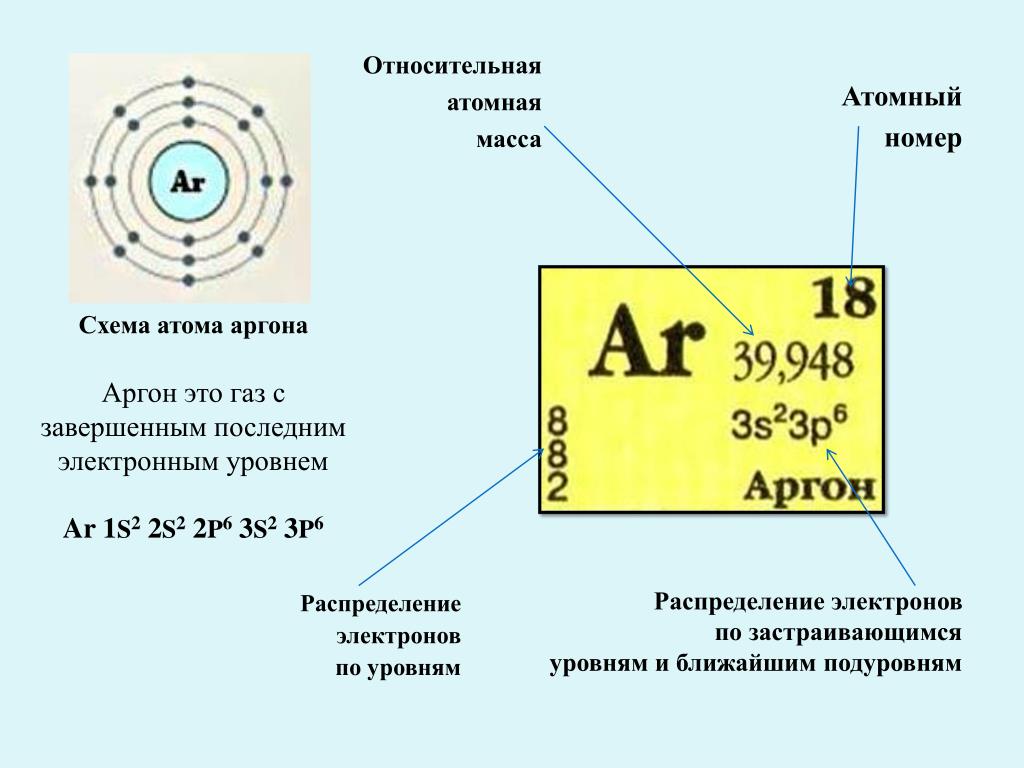
Используется метод также в атомной промышленности, в транспортном машиностроении и в аэрокосмической отрасли.
В домохозяйствах аргонная сварка распространена не так широко. Это объясняется:
- высокой стоимостью оборудования и расходных материалов;
- необходимостью достаточной квалификации сварщика;
- меньшими нагрузками, испытываемыми домашними конструкциями;
- более низкими требованиями к прочности и долговечности сварных соединений.
Если в домохозяйстве возникает эпизодическая потребность в таких сварочных работах, то дешевле, быстрее и надежнее пригласить сварщика-специалиста. Характерным свойством Ar является его более высокая плотность по сравнению с воздухом. Поэтому максимальная эффективность аргонной сварки достигается при нижнем сварочном положении. В этом случае инертный раз растекается по поверхности детали и образует защитное облако значительной протяженности, позволяя вести сварку, как большими токами, так и на большой скорости. При сварке в наклонном и верхнем положении приходится учитывать «проваливание» аргона сквозь воздух. Чтобы компенсировать это явление, либо увеличивают подачу газа, либо проводят работы в герметичном помещении, заполненным инертным газом. В обоих случаях себестоимость работ возрастает.
Поэтому максимальная эффективность аргонной сварки достигается при нижнем сварочном положении. В этом случае инертный раз растекается по поверхности детали и образует защитное облако значительной протяженности, позволяя вести сварку, как большими токами, так и на большой скорости. При сварке в наклонном и верхнем положении приходится учитывать «проваливание» аргона сквозь воздух. Чтобы компенсировать это явление, либо увеличивают подачу газа, либо проводят работы в герметичном помещении, заполненным инертным газом. В обоих случаях себестоимость работ возрастает.
Поскольку потенциал ионизации Ar невысок, его использование обеспечивает идеальные геометрических характеристик сварочного шва, прежде всего, профиля. Возбужденная электродуга в аргоновой атмосфере также отличается высокой стабильностью своих параметров. С другой стороны, низкое значение потенциала ионизации обуславливает и более низкое напряжение розжига и поддержания дуги. Это сокращает ее тепловыделение и усложняет провар толстых листов металла. Более высокая температура дуги в аргоновой атмосфере существенно повышает проплав сварочного шва. Это позволяет проводить сварку за один проход при условии точного соблюдения параметров зазора между заготовками.
Более высокая температура дуги в аргоновой атмосфере существенно повышает проплав сварочного шва. Это позволяет проводить сварку за один проход при условии точного соблюдения параметров зазора между заготовками.
В случае применения TIG-метода сварочных работ аргоновая атмосфера защищает от коррозионного влияния не только зону сварки, но и окончание неплавкого электрода.
В ряде специфических случаев в состав защитной газовой смеси добавляют гелий.
Кроме применения при сварочных работах, аргон используется:
- Как плазмоообразующее веществона установках плазменного раскроя металла.
- Для создания инертной среды в упаковках пищевых продуктов. Он вытесняет из пакетов и контейнеров кислород воздуха и водяные пары, пагубно влияющие на срок годности продуктов.
 Продукты в защитной атмосфере хранятся в несколько раз дольше, чем в обычной упаковке. Применяется этот метод и для упаковки медицинских изделий и препаратов, позволяя сохранить их в должной стерильности и химической чистоте.
Продукты в защитной атмосфере хранятся в несколько раз дольше, чем в обычной упаковке. Применяется этот метод и для упаковки медицинских изделий и препаратов, позволяя сохранить их в должной стерильности и химической чистоте. - В качестве активного агента в противопожарных установках. Аргон вытесняет кислород (или другой газ) из очага горения, прекращая его.
- Для создания защитной среды в технологических установках при обработке полупроводниковых устройств, создании микросхем и других электронных компонентов или материалов высоких степеней чистоты.
- Наполнитель электроламп.
- В рекламных люминесцентных трубках.
Зависимость давления аргона в баллоне от температуры
По мере нагрева давление газообразного вещества в замкнутом объеме повышается. В таблице приведены примерные значения давления в баллоне в зависимости от температуры окружающего воздуха.
| T, °C | P, Мегапаскаль |
| -40 | 10,45 |
| -30 | 11,33 |
| -20 | 12,21 |
| -10 | 12,92 |
| 0 | 13,74 |
| +10 | 14,62 |
| +20 | 15,33 |
| +30 | 16,03 |
Следует учитывать, что баллонное давление изменяется не мгновенно, а по мере его прогрева или охлаждения.
Техника безопасности при работе с аргоном
Сам по себе не являясь ядовитым, аргон при неправильном использовании может нанести серьезный вред здоровью или даже создать угрозу жизни. Аргон замещает кислород воздуха и создает смесь, непригодную для дыхания. Человек может пострадать или даже погибнуть от удушья. Сжиженный аргон имеет очень низкую температуру и при контакте с незащищенной кожей приводит к тяжелым обморожениям. Во избежание неприятных последствий при работе с газом следует неукоснительно соблюдать следующие правила:
- При работе в атмосфере аргона обязательно использовать изолирующий противогаз.
- При работе на полуавтоматах с подачей аргона обеспечить вентиляцию рабочей зоны.
- Использовать газоанализатор, содержание кислорода в воздухе должно быть не ниже 19%.
- Спецодежда должна полностью закрывать коду, быть чистой и целой.
Перед началом работы также следует осмотреть баллоны, шланги и запорную арматуру на предмет отсутствия механических повреждений и утечек газа.
Формула газа аргона. Структура, свойства, использование, примеры вопросов
Аргон — химический элемент с атомным номером 18. Он принадлежит к 18-й группе периодической таблицы и является третьим по величине газом аргоном. Газ, используемый в люминесцентных лампах, представляет собой одноатомный аргон. Он имеет молекулярную формулу Ar. Аргон — негорючий газ, не имеющий цвета и запаха и имеющий более высокую плотность, чем воздух. Когда он подвергается сильному нагреванию или огню, материал сильно разрывается. Аргон — первый обнаруженный нобелевский газ. Его признали английский физик лорд Рэлей и шотландский ученый Уильям Рамсей в 189 г.4. Аргон происходит от греческого слова «аргос», что означает «ленивый» или «неактивный». Он имеет место с респектабельным газом и составляет около 0,93% земного воздуха. Это третий по распространенности газ в воздухе.
Формула газа аргона
Его химическая формула – Ar. Он имеет молекулярную массу 39,948 г/моль. Это стабильный газ, он не имеет цепной структуры. Однако существует газовая структура аргона, показывающая орбиты,
Однако существует газовая структура аргона, показывающая орбиты,
Наличие аргона
Мировой климат устанавливается на уровне около 0,934% по объему и 1,288% по массе. Кроме того, воздух является важным современным источником дезинфицирующих аргоновых изделий. С помощью фракционирования предприятия отделяют аргон от воздуха, и чаще всего криогенная частичная очистка представляет собой взаимодействие, при котором образуются другие чистые газы, такие как азот, неон, ксенон и кислород. Морская вода содержит 0,45 частей на миллион аргона, а окружающая среда содержит около 1,2 частей на миллион аргона.
Производство аргона
Механическим путем производят частичную очистку жидкого воздуха. Аргон — это инертный защитный газ, который мы по большей части используем при сварке и других современных циклах, требующих высокой температуры, при которой нормальные безжизненные вещества становятся чувствительными, как в графитовых электрических нагревателях, которые используют его, чтобы предотвратить потребление графита.
Свойства газообразного аргона
Аргон как элемент обладает набором свойств, которые отличают его от других элементов периодической таблицы и даже от других благородных газов. Эти свойства включают его атомные свойства, физические свойства и химические свойства.
Атомные свойства аргона
Атомные свойства аргона относятся к свойствам одного атома аргона. These include:
- Atomic number: 18
- Atomic mass: 39.948
- Number of electrons: 18
- Valency (Oxidation states): 0
- Common Isotopes: Argon-36, Argon-38, Argon-40
Физические свойства газообразного аргона
- Температура плавления аргона составляет -189 °С, а температура кипения -185,7 °С. Это означает, что он существует в виде газа при стандартных условиях.
- Газообразный аргон бесцветен, не имеет вкуса и запаха
- Как неметалл, агрон имеет очень низкую металличность и является плохим проводником тепла и электричества
- Плотность аргона составляет 0,00178 г на кубический сантиметр
- Аргон в 2,5 раза более растворим в воде, чем азот, и имеет одинаковую растворимость в воде с кислородом.

Химические свойства газообразного аргона
- Известно, что аргон химически неактивен. В некоторых редких случаях и в экстремальных условиях он образует слабые, сложные структуры.
- Поскольку этот элемент не проявляет никакой химической активности, его называют инертным газом.
Использование аргона
- Он используется при сварке для предотвращения горения графита.
- Используется в люминесцентных лампах и других газоразрядных лампах.
- Аргоноплазменная коагуляция использует проводящую электричество аргоновую плазму в качестве среды для подачи высокочастотного тока для коагуляции тканей. Бесконтактная функция обеспечивает быструю коагуляцию с минимальными манипуляциями и травмами ткани-мишени.
Примеры вопросов
Вопрос 1. Является ли аргон металлом или неметаллом?
Ответ:
Аргон является неметаллическим элементом.
Он находится в группе 18 (VIIIa) периодической таблицы элементов, которую также называют группой благородных газов.
Вопрос 2: Какова химическая формула аргона?
Ответ:
Аргон (Ar) — химический элемент, относящийся к группе 18 (благородные газы) периодической таблицы. Это самый распространенный и широко используемый благородный газ на планете.
Вопрос 3: Каковы 5 применений аргона?
Ответ:
Пять видов использования аргона в человеческом обществе включают следующее:
- Внутренние лампочки
- Производство полупроводников
- Медицина 3 лазеры 94 334
- 4 0033 Геологическое датирование
Вопрос 4: Вреден ли аргон для человека?
Ответ:
Аргон естественным образом присутствует в окружающей среде и обычно считается нетоксичным.
Однако воздействие высоких концентраций аргона может снизить доступность кислорода в воздухе и, таким образом, вызвать удушье. Жидкий аргон также очень холодный и может вызвать обморожение при контакте.
Вопрос 5: Как рассчитать молярную массу аргона?
Ответ:
Масса аргона (Ar) составляет 39,948 г/моль. Формула расчета молярной массы заключается в делении массы конкретного химического элемента или химического соединения (г) на количество вещества (моль). В результате молярная масса аргона (Ar) становится равной 39,948 г/моль.
Вопрос 6: Используется ли аргон в медицине?
Ответ:
Аргон также использовался как надежный инструмент в клинической практике. Аргоноплазменная коагуляция (APC) — это бесконтактная стратегия, в которой используется часто повторяющееся ощущение аргоновой плазмы для закрытия окружающих тканей и контроля дренирования вокруг важных мест посредством коагуляции.
Газовая смесь, состоящая из гелия и аргона, имеет плотность 0,670…
Последние каналы
- Общая химия
Химия
- Общая химия
- Органическая химия
- Аналитическая химия
- GOB Химия
- Биохимия
Биология
Биология
Общая биология биология
Математика
- Колледж Алгебра
- Тригонометрия
- Предварительное исчисление
Физика
- Физика
Бизнес
- Микроэкономика
- Макроэкономика
- Финансовый учет
Социальные науки
- Психология
Начните печатать, затем используйте стрелки вверх, чтобы выбрать вариант из списка, и используйте стрелки вниз, чтобы выбрать вариант из списка.


