Аргон молярная масса: Молярная масса аргона
alexxlab | 26.05.2023 | 0 | Разное
АРГОН (Ar)
Основные параметры и свойства Аргона
Свойства атома Аргона |
|
|
Название |
Аргон / Argon |
|
Символ |
Ar |
|
Номер |
18 |
|
Атомная масса (молярная масса) |
39,948 (1) а. е. м. (г/моль) |
|
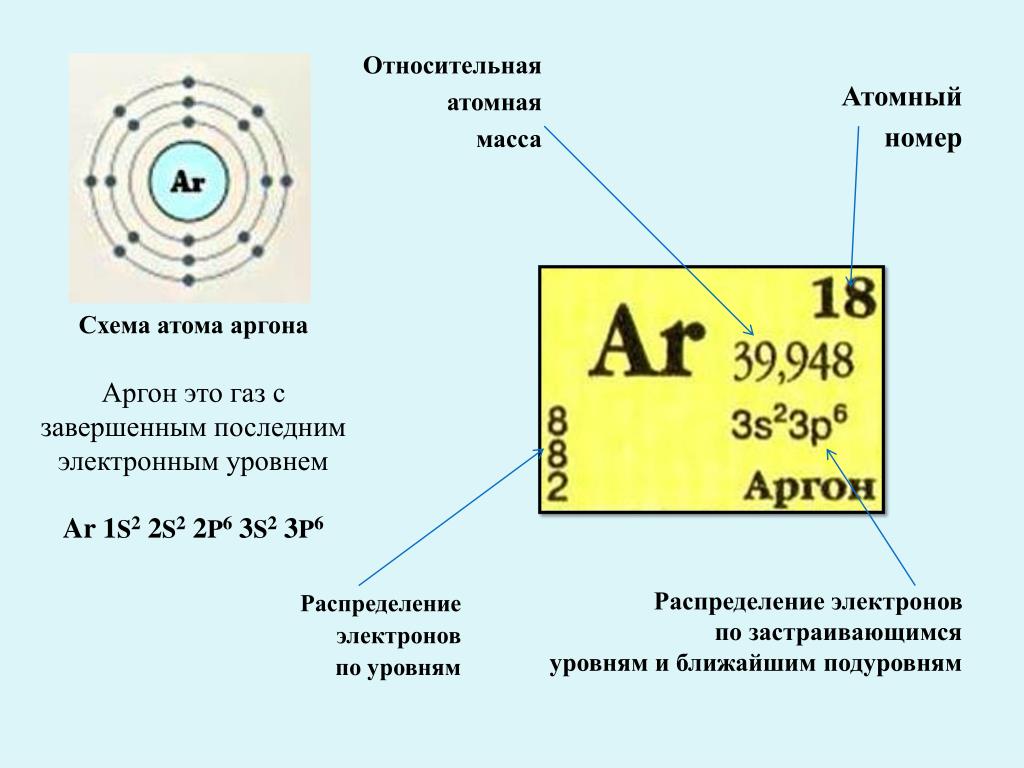
Электронная конфигурация |
[Ne] 3s2 3p6 |
|
Радиус атома |
? (71) пм |
Химические свойства Аргона |
|
|
Ковалентный радиус |
106 пм |
|
Радиус иона |
154 пм |
|
Электроотрицательность |
4,3 (шкала Полинга) |
|
Электродный потенциал |
0 |
|
Степени окисления |
0 |
|
Энергия ионизации (первый электрон) |
1519,6 (15,76) кДж/моль (эВ) |
Термодинамические свойства простого вещества |
|
|
Плотность (при н. |
1,784·10−3 г/см3 |
|
Плотность при т. п. |
1,40 г/см3 |
|
Температура плавления |
83,8 К (-189,35 °C) |
|
Температура кипения |
87,3 К (-185,85 °C) |
|
Уд. теплота плавления |
7,05 ккал/кг кДж/моль |
|
Уд. теплота испарения |
6,45 кДж/моль кДж/моль |
|
Молярная теплоёмкость |
20,79 Дж/(K·моль) |
|
Молярный объём |
24,2 см3/моль |
Кристаллическая решётка простого вещества |
|
|
Структура решётки |
кубическая гранецентрированая |
|
Параметры решётки |
5,260 Å |
|
Температура Дебая |
85 K |
Прочие характеристики Аргона |
|
|
Теплопроводность |
(300 K) 0,0164 вт/м×град Вт/(м·К) |
Задачи по термодинамике
Репетиторы ❯ ЕГЭ и ГИА ❯ Задачи по термодинамике
Автор: Андрей Алексеевич
●
12. 11.2020
11.2020
Раздел: ЕГЭ и ГИА
Разбираем две задачи из ЕГЭ по физике прошлых лет. Задание №26.
Задача №1В сосуде содержится 0,1 моль аргона. Среднеквадратичная скорость его молекул равна 400 м/с. Чему равна внутренняя энергия этой порции аргона?
Решение
Молярная масса аргона M=40 г/моль. Все инертные газы являются одноатомными, аргон — инертный газ, следовательно, одноатомный. Внутренняя энергия одноатомного газа равна:
U = RT = pV
Запишем основное уравнение МКТ газа:
Найдём внутреннюю энергию аргона:
Ответ: 320.
Задача №2
В сосуде содержится 0,1 моль гелия. Среднеквадратичная скорость его молекул равна 400 м/с. Чему равна внутренняя энергия этой порции гелия?
Решение
Молярная масса гелия M = 4 г/моль.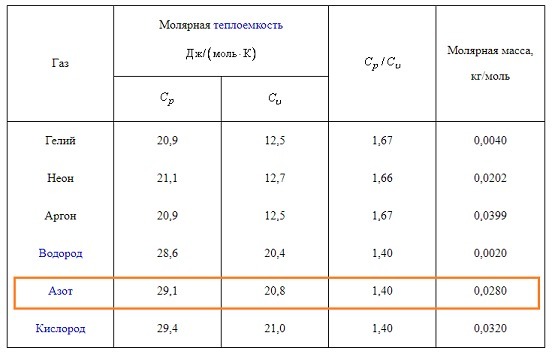 Все инертные газы являются одноатомными, гелий — инертный газ, следовательно, одноатомный. Внутренняя энергия одноатомного газа равна:
Все инертные газы являются одноатомными, гелий — инертный газ, следовательно, одноатомный. Внутренняя энергия одноатомного газа равна:
U = RT = pV
Запишем основное уравнение МКТ газа:
Найдем внутреннюю энергию гелия:
Ответ: 32.
© blog.tutoronline.ru, при полном или частичном копировании материала ссылка на первоисточник обязательна.
Физика
Курсы физики для студентов нефизических специальностей
Математика
Курсы по математике 9 класс
Алгебра 8 класс
Информатика и ИКТ
Курсы по информатике для студентов
Английский язык
Подготовка к ЕГЭ по английскому
Программирование
Основы программирования на С++
Информатика и ИКТ
Курс подготовки к ОГЭ по дисциплине «Информатика» для учащихся базовой школы (9 класс)
Математика
Курсы по геометрии 7 класс
Как найти молярную массу аргона?
Ответить
Проверено 267,9 тыс. + просмотров
+ просмотров
Молярная масса Ar не является целым числом, а атомный номер Ar равен 18.
Полный ответ:
Итак, в вопросе задан вопрос, как мы будем определять или вычислять молярную массу аргона.
С тех пор, как мы изучаем периодическую таблицу, мы очень хорошо знакомы с двумя терминами, относящимися к элементу, атомным номером и молярной массой элемента.
Атомный номер — это уникальный номер элемента, который является идентификатором элемента. Никакие два элемента не будут иметь одинаковый атомный номер. Атомный номер дает количество протонов и количество электронов, присутствующих в элементах, поскольку атомный номер будет равен количеству протонов и количеству электронов в элементе.
Здесь нас интересует элемент Ar, атомный номер которого равен 18. Таким образом, количество присутствующих протонов и электронов также равно 18.
Теперь мы обсудим молярную массу или атомный вес элемента. {40}}. $ и мы берем среднюю массу этих изотопов, чтобы получить молярную массу Ar, и мы получим значение 39.948.
{40}}. $ и мы берем среднюю массу этих изотопов, чтобы получить молярную массу Ar, и мы получим значение 39.948.
Примечание: Мы также можем найти значение атомной массы, если количество нейтронов и протонов присутствует в атоме, оно будет примерно равно атомной массе, поскольку многие атомы существуют как комбинация их изотопов в реальном мире. .
Если число молей аргона в взятой пробе и масса пробы известны, то мы можем найти молярную массу аргона, изменив уравнение:
$\text{No}\text{.}\,\text {из}\,\text{моль}\,\text{=}\dfrac{\text{данные}\,\text{масса}}{\text{Молярная}\,\text{масса}}$
$\text{Молярная}\,\text{масса=}\dfrac{\text{Данная}\,\text{масса}}{\text{Нет}\text{.}\,\text{из}\ ,\text{моль}}$
Молярная масса также называется молекулярной массой, формулой грамма молекулярной массы и т. д.
Единицей молекулярной массы является $\text{г/моль}$
Дата последнего обновления: 17 мая 2023 г.
•
Всего просмотров: 267. 9k
9k
•
Просмотров сегодня: 7.28k
Недавно обновленные страницы
В Индии по случаю бракосочетания фейерверк 12 класс химия JEE_Main
Щелочноземельные металлы Ba, Sr, Ca и Mg могут быть отнесены к 12 классу химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал 12 класс химии JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 класс 12 химии JEE_Main
Какой элемент обладает наибольшим атомным радиусом А 11 класс химии JEE_Main
Фосфин получают из следующей руды Кальций 12 класса химии JEE_Main
В Индии по случаю бракосочетания фейерверк 12 класса химии JEE_Main
Щелочноземельные металлы Ba, Sr, Ca и Mg могут быть отнесены к 12 классу химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал 12 класс химии JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 класс 12 химии JEE_Main
Какой элемент обладает наибольшим атомным радиусом А Химический класс 11 JEE_Main
Фосфин получают из следующей руды А Кальций 12 химического класса JEE_Main
Актуальные сомнения
Молекулярная масса вещества
Молекулярная масса вещества, также называемая молярной массой , M, представляет собой массу 1 моля этого вещества, выраженную в M граммах.
В системе СИ единицей измерения М является [кг/кмоль], в английской системе единицей измерения является [фунт/фунт-моль], а в системе СГ единицей измерения М является [г/моль]. Молекулярная масса представлена одним и тем же числом во всех системах единиц независимо от используемой системы. По этой причине во многих случаях единица молекулярной массы не упоминается; однако следует понимать, что это не безразмерный параметр.
Молекулярная масса чистого соединения определяется по его химической формуле и атомным массам его элементов. Атомные массы элементов, обнаруженных в органических веществах: C = 12,011, H = 1,008, S = 32,065, O = 15,999 и N = 14,007.
Пример: Молекулярная масса этанола (C
Для расчета молекулярной массы этанола суммируется молекулярная масса каждого атома в молекуле:
M этанол = 2*12,011[кг/кмоль] + 6*1,008[кг/кмоль] + 1*15,999 [кг/кмоль] = 46,069 [кг/кмоль]
См. также Физические данные для углеводородов, Физические данные для спиртов и карбоновых кислот кислоты, Физические данные для органических соединений азота и Физические данные для органических соединений серы 9
также Физические данные для углеводородов, Физические данные для спиртов и карбоновых кислот кислоты, Физические данные для органических соединений азота и Физические данные для органических соединений серы 9
 011
011 461
461 179
179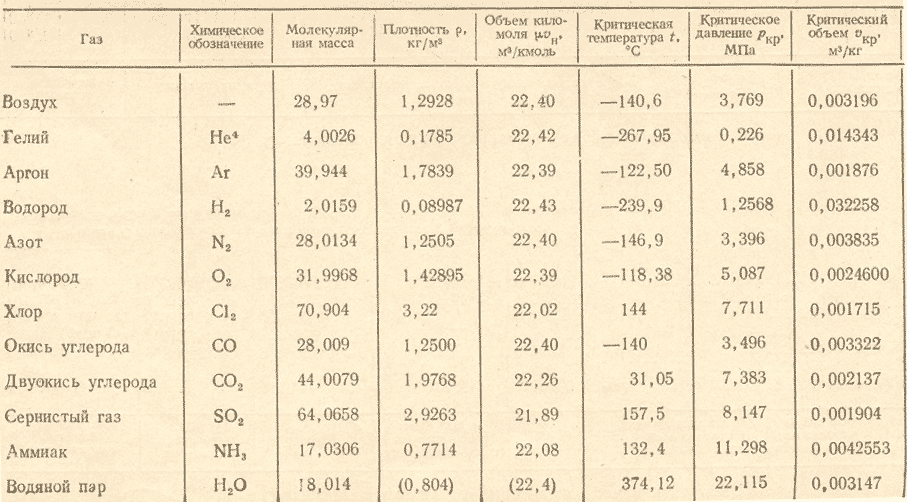


 у.)
у.)