Аргон плотность: Аргон – это газ: плотность, формула, масса в баллоне, применение в сварке
alexxlab | 11.04.2023 | 0 | Разное
Аргон – свойства, характеристики – сайт АО «ГРАСИС»
Запрос на оборудование
В атмосфере содержится около 0,9% аргона. Аргон, который, как и азот, представляет собой нейтральный бесцветный газ, существует в природе только в составе атмосферного воздуха. Он не пригоден для поддержания жизни, однако незаменим в некоторых технологических процессах благодаря высокому уровню химической инертности и относительной простоте извлечения.
| Внешний вид простого вещества | |
|---|---|
| Инертный газ без цвета, вкуса и запаха | |
| Свойства атома | |
| Имя, символ, номер | Аргон / Argon (Ar), 18 |
| Атомная масса (молярная масса) | 39,948 а. е. м. (г/моль) |
| Электронная конфигурация | [Ne] 3s2 3p6 |
| Радиус атома | 71пм |
| Химические свойства | |
| Ковалентный радиус | |
| Радиус иона | 154 пм |
| Электроотрицательность | 4,3 (шкала Полинга) |
| Электродный потенциал | 0 |
| Степени окисления | 0 |
| Энергия ионизации (первый электрон) | 1519,6(15,75) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
Плотность (при н. у.) у.) | (при 186 °C) 1,40 г/см3 |
| Температура плавления | 83,8 K |
| Температура кипения | 87,3 K |
| Теплота испарения | 6,52 кДж/моль |
| Молярная теплоёмкость | 20,79 Дж/(K·моль) |
| Молярный объём | 24,2 см3/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированая |
| Параметры решётки | 5,260 A |
| Температура Дебая | 85 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 0,0177 Вт/(м·К) |
История открытия
История открытия аргона начинается в 1785 году, когда английский физик и химик Генри Кавендиш, изучая состав воздуха, решил установить, весь ли азот воздуха окисляется.
В течение многих недель он подвергал воздействию электрического разряда смесь воздуха с кислородом в U-образных трубках, в результате чего в них образовывались все новые порции бурых окислов азота, которые исследователь периодически растворял в щёлочи. Через некоторое время образование окислов прекращалось, но, после связывания оставшегося кислорода, оставался газовый пузырь, объём которого не уменьшался при длительном воздействии электрических разрядов в присутствии кислорода. Кавендиш оценил объём оставшегося газового пузыря в 1/120 от первоначального объёма воздуха. Разгадать загадку пузыря Кавендиш не смог, поэтому прекратил свое исследование, и даже не опубликовал его результатов. Только спустя много лет английский физик Джеймс Максвелл собрал и опубликовал неизданные рукописи и лабораторные записки Кавендиша.
Через некоторое время образование окислов прекращалось, но, после связывания оставшегося кислорода, оставался газовый пузырь, объём которого не уменьшался при длительном воздействии электрических разрядов в присутствии кислорода. Кавендиш оценил объём оставшегося газового пузыря в 1/120 от первоначального объёма воздуха. Разгадать загадку пузыря Кавендиш не смог, поэтому прекратил свое исследование, и даже не опубликовал его результатов. Только спустя много лет английский физик Джеймс Максвелл собрал и опубликовал неизданные рукописи и лабораторные записки Кавендиша.
Дальнейшая история открытия аргона связана с именем Рэлея, который несколько лет посвятил исследованиям плотности газов, особенно азота. Оказалось, что литр азота, полученного из воздуха, весил больше литра «химического» азота (полученного путём разложения какого-либо азотистого соединения, например, закиси азота, окиси азота, аммиака, мочевины или селитры) на 1,6 мг (вес первого был равен 1,2521, а второго 1,2505 г. ). Эта разница была не так уж мала, чтобы можно было её отнести на счет ошибки опыта. К тому же она постоянно повторялась независимо от источника получения химического азота.
). Эта разница была не так уж мала, чтобы можно было её отнести на счет ошибки опыта. К тому же она постоянно повторялась независимо от источника получения химического азота.
Не придя к разгадке, осенью 1892 года Рэлей в журнале «Nature» опубликовал письмо к учёным, с просьбой дать объяснение тому факту, что в зависимости от способа выделения азота он получал разные величины плотности. Письмо прочли многие учёные, однако никто не был в состоянии ответить на поставленный в нём вопрос.
У известного уже в то время английского химика Уильяма Рамзая также не было готового ответа, но он предложил Рэлею свое сотрудничество. Интуиция побудила Рамзая предположить, что азот воздуха содержит примеси неизвестного и более тяжелого газа, а Дьюар обратил внимание Рэлея на описание старинных опытов Кавендиша (которые уже были к этому времени опубликованы).
Пытаясь выделить из воздуха скрытую составную часть, каждый из учёных пошел своим путём. Рэлей повторил опыт Кавендиша в увеличенном масштабе и на более высоком техническом уровне.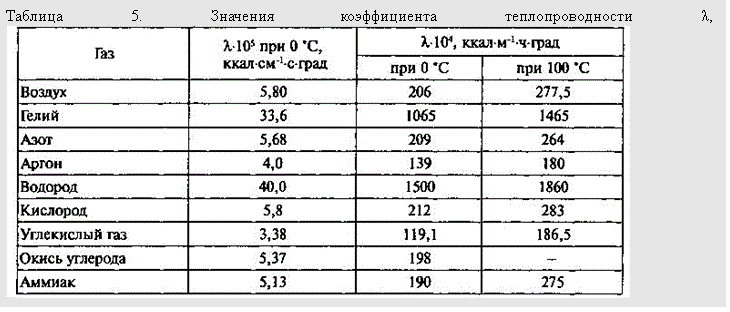 Трансформатор под напряжением 6000 вольт посылал в 50-литровый колокол, заполненный азотом, сноп электрических искр. Специальная турбина создавала в колоколе фонтан брызг раствора щёлочи, поглощающих окислы азота и примесь углекислоты. Оставшийся газ Рэлей высушил, и пропустил через фарфоровую трубку с нагретыми медными опилками, задерживающими остатки кислорода. Опыт длился несколько дней.
Трансформатор под напряжением 6000 вольт посылал в 50-литровый колокол, заполненный азотом, сноп электрических искр. Специальная турбина создавала в колоколе фонтан брызг раствора щёлочи, поглощающих окислы азота и примесь углекислоты. Оставшийся газ Рэлей высушил, и пропустил через фарфоровую трубку с нагретыми медными опилками, задерживающими остатки кислорода. Опыт длился несколько дней.
Рамзай воспользовался открытой им способностью нагретого металлического магния поглощать азот, образуя твёрдый нитрид магния. Многократно пропускал он несколько литров азота через собранный им прибор. Через 10 дней объём газа перестал уменьшаться, следовательно, весь азот оказался связанным. Одновременно путём соединения с медью был удален кислород, присутствовавший в качестве примеси к азоту. Этим способом Рамзаю в первом же опыте удалось выделить около 100 см³ нового газа.
Итак, был открыт новый элемент. Стало известно, что он тяжелее азота почти в полтора раза и составляет 1/80 часть объёма воздуха. Рамзай при помощи акустических измерений нашёл, что молекула нового газа состоит из одного атома — до этого подобные газы в устойчивом состоянии не встречались. Отсюда следовал очень важный вывод — раз молекула одноатомна, то, очевидно, новый газ представляет собой не сложное химическое соединение, а простое вещество.
Рамзай при помощи акустических измерений нашёл, что молекула нового газа состоит из одного атома — до этого подобные газы в устойчивом состоянии не встречались. Отсюда следовал очень важный вывод — раз молекула одноатомна, то, очевидно, новый газ представляет собой не сложное химическое соединение, а простое вещество.
Много времени затратили Рамзай и Рэлей на изучение его реакционной способности по отношению ко многим химически активным веществам. Но, как и следовало ожидать, пришли к выводу: их газ совершенно недеятелен. Это было ошеломляюще — до той поры не было известно ни одного настолько инертного вещества.
Большую роль в изучении нового газа сыграл спектральный анализ. Спектр выделенного из воздуха газа с его характерными оранжевыми, синими и зелёными линиями резко отличался от спектров уже известных газов. Уильям Крукс, один из виднейших спектроскопистов того времени, насчитал в его спектре почти 200 линий. Уровень развития спектрального анализа на то время не дал возможности определить, одному или нескольким элементам принадлежал наблюдаемый спектр.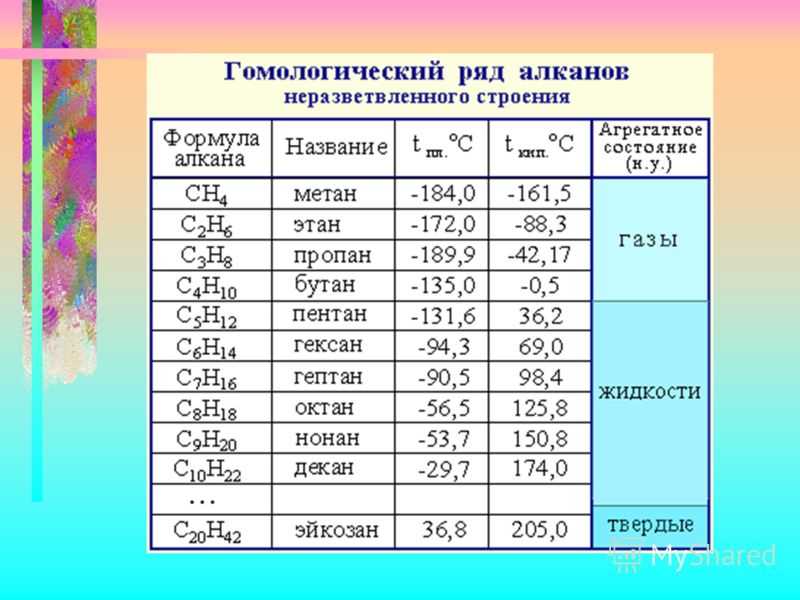 Несколько лет спустя выяснилось, что Рамзай и Рэлей держали в своих руках не одного незнакомца, а нескольких — целую плеяду инертных газов.
Несколько лет спустя выяснилось, что Рамзай и Рэлей держали в своих руках не одного незнакомца, а нескольких — целую плеяду инертных газов.
7 августа 1894 года в Оксфорде, на собрании Британской ассоциации физиков, химиков и естествоиспытателей, было сделано сообщение об открытии нового элемента, который был назван аргоном. В своём докладе Рэлей утверждал, что в каждом кубическом метре воздуха присутствует около 15 г открытого газа (1,288 вес. %). Слишком невероятен был тот факт, что несколько поколений ученых не заметили составной части воздуха, да еще и в количестве целого процента! В считанные дни десятки естествоиспытателей из разных стран проверили опыты Рамзая и Рэлея. Сомнений не оставалось: воздух содержит аргон.
Через 10 лет, в 1904 году, Рэлей за исследования плотностей наиболее распространённых газов и открытие аргона получает Нобелевскую премию по физике, а Рамзай за открытие в атмосфере различных инертных газов — Нобелевскую премию по химии.
Основное применение
Пищевая отрасль
В контролируемой среде аргон может во многих процессах использоваться в качестве замены для азота. Высокая растворимость (в два раза превышающая растворимость азота) и определенные молекулярные характеристики обеспечивают его особые свойства при хранении овощей. При определенных условиях он способен замедлять метаболические реакции и значительно сокращать газообмен.
Высокая растворимость (в два раза превышающая растворимость азота) и определенные молекулярные характеристики обеспечивают его особые свойства при хранении овощей. При определенных условиях он способен замедлять метаболические реакции и значительно сокращать газообмен.
Производство стекла, цемента и извести
При использовании для заполнения ограждений с двойным глазурованием аргон обеспечивает превосходную тепловую изоляцию.
Металлургия
Аргон используется для предупреждения контакта и последующего взаимодействия между расплавленным металлом и окружающей атмосферой.
Использование аргона позволяет оптимизировать такие производственные процессы как перемешивание расплавленных веществ, продувка поддонов реакторов для предупреждения повторного окисления стали и обработка стали узкого применения в вакуумных дегазаторах, включая вакуумно-кислородное обезуглероживание, окислительно-восстановительных процессы и процессы открытого сжигания. Однако наибольшую популярность аргон приобрел в процессах аргоно-кислородного обезуглероживания нерафинированной высокохромистой стали, позволяя минимизировать окисление хрома.
Лабораторные исследования и анализы
В чистом виде и в соединениях с другими газами аргон используется для проведения промышленных и медицинских анализов и испытаний в рамках контроля качества.
В частности аргон выполняет функцию газовой плазмы в эмиссионной спектрометрии индуктивно-связанной плазмой (ICP), газовой подушки в атомно-абсорбционной спектроскопии в графитной печи (GFAAS) и газа-носителя в газовой хроматографии с использованием различных газоанализаторов.
В соединении с метаном аргон используется в счетчиках Гейгера и детекторах рентгеновского флуоресцентного анализа (XRF), где он выполняет функцию гасящего газа.
Сварка, резка и нанесение покрытия
Аргон используется в качестве защитной среды в процессах дуговой сварки, при поддуве защитного газа и при плазменной резке.
Аргон предупреждает окисление сварных швов и позволяет сократить объем дыма, сбрасываемого в процессе сварки.
Электроника
Сверхчистый аргон служит в качестве газа-носителя для химически активных молекул, а также в качестве инертного газа для защиты полупроводников от посторонних примесей (например, аргон обеспечивает необходимую среду для выращивания кристаллов силикона и германия).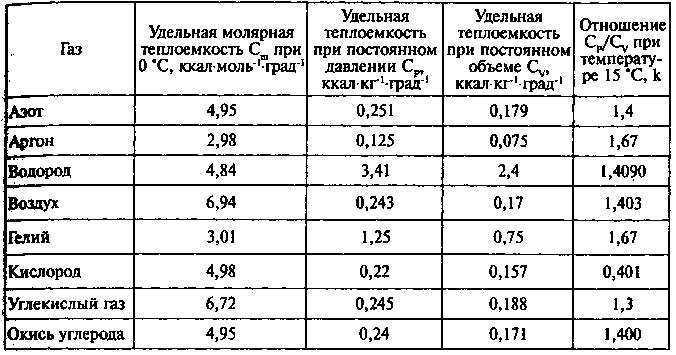
В ионном состоянии аргон используется в процессах металлизации напылением, ионной имплантации, нормализации и травления при производстве полупроводников и высокоэффективном производстве материалов.
Автомобильная и транспортная отрасль
Затаренный герметизированный аргон служит для наполнения подушек безопасности в автомобилях.
Ключевые свойства аргона для широкого применения в промышленности
14.04.2022
Инертные газы не вступают в реакцию с другими веществами, не участвуют в синтезе химических соединений, не поддерживают процессы горения. И тем не менее, такие газы широко применяются в промышленности, где их физико-химические свойства максимально востребованы и актуальны. Один из таких газов – аргон. Его задействуют в сварочных операциях, раскрое металла, химических реакциях, на пищевых производствах, при сборке электроники и т. д.
Свойства и характеристики газа аргона
Важнейшее отличительное качество аргона – его инертность, то есть неспособность вступать в любые химические реакции. Этот газ тяжелее воздуха, практически не растворяется в воде, при нормальных условиях бесцветный, не имеет вкуса и запаха, не подвержен горению, отличается низкой теплопроводностью. Аргон не ядовит, его доля в воздушной массе составляет 0,9 % объема. Газ имеет плотность 1,784 кг/м3, температура кипения в ректификационной установке -185,8 °C. Благодаря доступности получения и низкой стоимости потребность заказать аргон с доставкой возникает у множества промышленных предприятий, строительных компаний и научно-исследовательских центров.
Этот газ тяжелее воздуха, практически не растворяется в воде, при нормальных условиях бесцветный, не имеет вкуса и запаха, не подвержен горению, отличается низкой теплопроводностью. Аргон не ядовит, его доля в воздушной массе составляет 0,9 % объема. Газ имеет плотность 1,784 кг/м3, температура кипения в ректификационной установке -185,8 °C. Благодаря доступности получения и низкой стоимости потребность заказать аргон с доставкой возникает у множества промышленных предприятий, строительных компаний и научно-исследовательских центров.
Применение аргона в различных отраслях
Аргон востребован во многих отраслях промышленности, в народном хозяйстве и даже в быту. Его применение распространено в следующих сферах:
- пищевое производство – при помощи газа из резервуаров вытесняют кислород и воду для долгого хранения продукции, добавка в виде аргона также применяется в производстве упаковки продовольственных товаров;
- металлообработка – аргон создает защитную среду, благодаря которой металлы и сплавы не вступают в реакцию с кислородом во время сварки, также газ используют при плазменном раскрое и резке;
- изготовление осветительного оборудования – с применением аргона люминесцентные лампы и лампы накаливания становятся более долговечными и эффективными;
- сборка стеклопакетов – газом заполняют светопрозрачные конструкции для лучшей тепло- и звукоизоляции окон;
- медицина – аргон задействуют в методах щадящей хирургии, при остановке кровотечений;
- химическая отрасль – используя аргон, специалисты анализируют чистоту веществ, обрабатывают металлы и расплавы.

Как лучше приобретать аргон?
Потребителям доступен аргон двух видов: в сжиженном и газообразном состоянии, в зависимости от сферы применения и условий эксплуатации. Наиболее выгодный вариант покупки – обмен баллонов с аргоном. Обменивая старые баллоны, клиент сразу же получает аттестованные заполненные емкости, готовые к эксплуатации. В случае если заказчик впервые приобретает газ, ему необходимо купить новую заполненную емкость, также готовую к использованию. В дальнейшем баллон используют для обмена. При необходимости у компании-поставщика технических газов можно приобрести дополнительное газобаллонное оборудование, например горелки.
Аргон | Газовая энциклопедия Air Liquide
- Молекула
- Характеристики
- Приложения
- Безопасность и совместимость
- Узнать больше
Нажмите и перетащите, чтобы переместить трехмерную молекулу
Объемы жидкости/газа
Расчет объема или массы количества газа или жидкости
Жидкая фаза
При температуре кипения при 1,013 бар
м³ (Объем)
кг (масса)
Газовая фаза
В стандартных условиях (1,013 бар, 15°C)
м³ (Объем)
кг (масса)
Физические свойства
Загрузить набор данных (XLSX – 98,38 КБ)
- Общие свойства
- Твердая фаза
- Жидкая фаза
- Газовая фаза
Давление (бар)
| Скрытая теплота плавления (при температуре плавления) | 29,588 кДж/кг |
| Температура плавления | – 189,37 °С |
| Температура кипения | – 185,85 °С |
| Скрытая теплота парообразования (при температуре кипения) | 161,14 кДж/кг |
| Плотность жидкости (при температуре кипения) | 1395,4 кг/м 3 |
| Коэффициент сжимаемости Z | 9.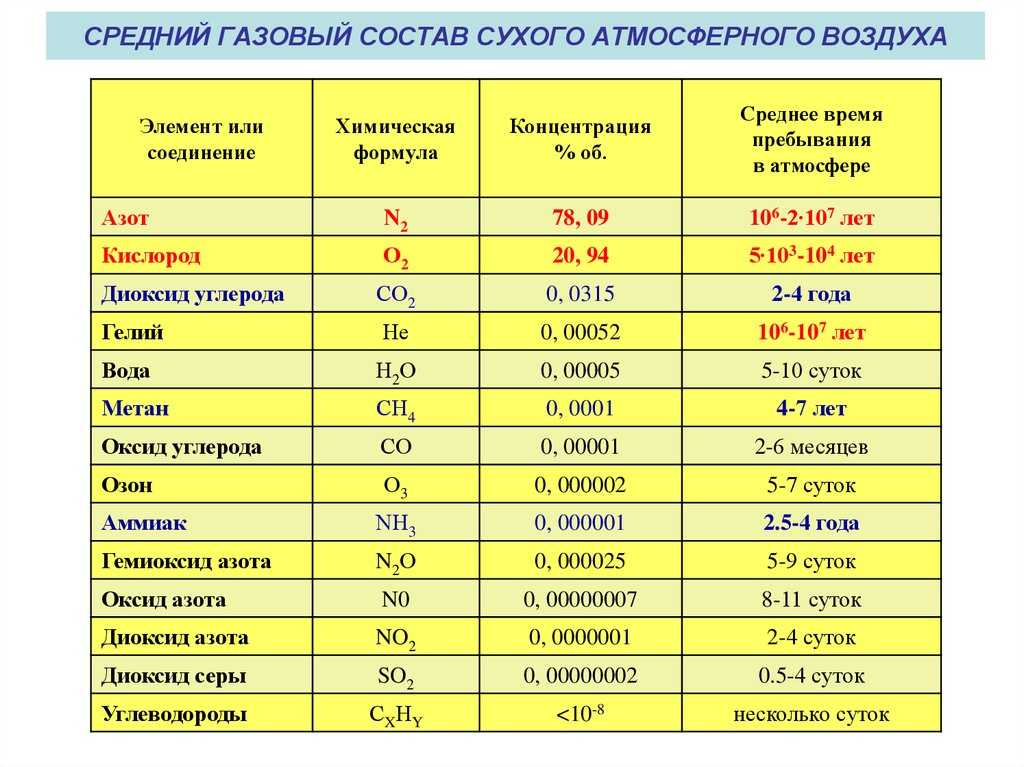 9906E-1 9906E-1 |
| Отношение Cp/Cv γ | 1.6702 |
| Плотность газа (при температуре кипения) | 5,772 кг/м 3 |
| Плотность газа | 1,7835 кг/м 3 |
| Эквивалент газ/(жидкость при температуре кипения) | 782 об/об |
| Теплоемкость Cp | 5.2185E-1 кДж/(кг.К) |
| Теплоемкость Cv | 3.1243E-1 кДж/(кг.К) |
| Удельный вес | 1,38 |
| Удельный объем | 5.607E-1 м 3 /кг |
| Теплопроводность | 16,483 мВт/(м.К) |
| Вязкость | 2.1017E-4 По |
| Коэффициент сжимаемости Z | 9.9925E-1 |
| Отношение Cp/Cv γ | 1,6698 |
| Плотность газа | 1,6903 кг/м 3 |
| Эквивалент газ/(жидкость при температуре кипения) | 825,53 об/об |
| Теплоемкость Cp | 5. 2165E-1 кДж/(кг.К) 2165E-1 кДж/(кг.К) |
| Теплоемкость Cv | 3.1241E-1 кДж/(кг.К) |
| Растворимость в воде | 3.025E-5 моль/моль |
| Удельный вес | 1,38 |
| Удельный объем | 5.916E-1 м 3 /кг |
| Теплопроводность | 17,245 мВт/(м.К) |
| Вязкость | 2.1987E-4 По |
| Коэффициент сжимаемости Z | 9.9937E-1 |
| Отношение Cp/Cv γ | 1,6696 |
| Плотность газа | 1,6335 кг/м 3 |
| Эквивалент газ/(жидкость при температуре кипения) | 854,24 об/об |
| Теплоемкость Cp | 5.2155E-1 кДж/(кг.К) |
| Теплоемкость Cv | 3.1238E-1 кДж/(кг.К) |
| Растворимость в воде | 2. 519E-5 моль/моль 519E-5 моль/моль |
| Удельный вес | 1,38 |
| Удельный объем | 6.122E-1 м 3 /кг |
| Теплопроводность | 17,746 мВт/(м.К) |
| Вязкость | 2.2624E-4 По |
Применение
Примеры использования этой молекулы в промышленности и здравоохранении
Авиация
Аргон используется при сварке и термообработке, а также в качестве защитной атмосферы.
Автомобильная промышленность
Аргон используется в чистом виде или в смесях для дуговой, плазменной и лазерной сварки. Аргон защищает сварные швы от воздуха, а также снижает выбросы дыма в большинстве процессов дуговой сварки. Аргон используется для надувания автомобильных подушек безопасности.
Напитки
Аргон используется для инертизации вина для предотвращения окисления в процессе виноделия.
Электронные компоненты
Аргон используется в процессах плазменного травления. Аргон используется в процессах PVD (физическое осаждение из паровой фазы). Он также используется для вытягивания кристаллов кремниевых слитков.
Аргон используется в процессах PVD (физическое осаждение из паровой фазы). Он также используется для вытягивания кристаллов кремниевых слитков.
Пищевые продукты
Аргон позволяет продлить срок хранения пищевых продуктов в модифицированной атмосфере.
Стекло
Аргон предотвращает коррозию вольфрамовой нити накаливания в лампочке и, как следствие, почернение колбы при инертизации атмосферы. Аргон используется для повышения теплоизоляционных характеристик стеклопакетов.
Больничная помощь
Жидкий аргон используется в хирургии
Лаборатории и исследовательские центры
Аргон используется для анализа в исследовательских лабораториях и контроля качества в промышленности и здравоохранении: плазменный газ для плазменно-эмиссионной спектрометрии, защитный газ в графитовой печи атомной абсорбции спектрометрия, газ-носитель в газовой хроматографии для различных детекторов. В смеси с метаном аргон используется в счетчике Гейгера и в рентгенофлуоресцентном детекторе в качестве гасящего газа.
Производство металлов
Аргон используется для защиты жидкого металла от реакций с соединениями, присутствующими в окружающем воздухе, такими как кислород. Он также используется по тем же причинам во многих сварочных процессах.
Металл
Аргон используется для перемешивания и инертизации в сталеплавильном производстве и во время аргоно-кислородного обезуглероживания (AOD) нержавеющей стали.
Безопасность и совместимость
- Основные опасности
- Совместимость материалов
GHS04
Газ под давлением
Запах
нет
Металлы
| Алюминий | Удовлетворительно |
| Латунь | Удовлетворительно |
| Монель | Нет данных |
| Медь | Нет данных |
| Ферритная сталь | Удовлетворительно |
| Нержавеющая сталь | Удовлетворительно |
| Цинк | Нет данных |
| Титан | Нет данных |
Пластик
| Политетрафторэтилен | Удовлетворительно |
| Полихлортрифторэтилен | Удовлетворительно |
| Поливинилиденфторид | Удовлетворительно |
| Поливинилхлорид | Удовлетворительно |
| Этилентетрафторэтилен | Нет данных |
| Поликарбонат | Нет данных |
| Полиамид | Удовлетворительно |
| Полипропилен | Удовлетворительно |
Эластомеры
| Бутилкаучук (изобутен-изопрен) | Удовлетворительно |
| Нитриловый каучук | Удовлетворительно |
| Хлоропрен | Удовлетворительно |
| Хлорфторуглероды | Нет данных |
| Силикон | Удовлетворительно |
| Перфторэластомеры | Удовлетворительно |
| Фторэластомеры | Удовлетворительно |
| Неопрен | Нет данных |
| Полиуретан | Удовлетворительно |
| Этилен-пропилен | Удовлетворительно |
Смазочные материалы
| Смазка на углеводородной основе | Удовлетворительно |
| Смазка на основе фторуглерода | Удовлетворительно |
Совместимость материалов
Рекомендации: Компания Air Liquide собрала данные о совместимости газов с материалами, чтобы помочь вам определить, какие материалы использовать для газовой системы. Хотя информация была собрана из источников, которые Air Liquide считает надежными (Международные стандарты: Совместимость материалов баллонов и клапанов с содержанием газа; Часть 1 — Металлические материалы: ISO11114-1 (март 2012 г.), Часть 2 — Неметаллические материалы: ISO11114-2 (апрель 2013 г.), ее следует использовать с особой осторожностью и инженерной оценкой. Такие необработанные данные не могут охватывать все условия концентрации, температуры, влажности, примесей и аэрации. Поэтому рекомендуется использовать эту таблицу только для определения возможных материалов для применения при высоком давлении и температуре окружающей среды.Для подтверждения выбора материала для данного применения необходимо провести обширные исследования и испытания в конкретных условиях использования.Обратитесь в региональную группу Air Liquide для получения экспертных услуг.
Хотя информация была собрана из источников, которые Air Liquide считает надежными (Международные стандарты: Совместимость материалов баллонов и клапанов с содержанием газа; Часть 1 — Металлические материалы: ISO11114-1 (март 2012 г.), Часть 2 — Неметаллические материалы: ISO11114-2 (апрель 2013 г.), ее следует использовать с особой осторожностью и инженерной оценкой. Такие необработанные данные не могут охватывать все условия концентрации, температуры, влажности, примесей и аэрации. Поэтому рекомендуется использовать эту таблицу только для определения возможных материалов для применения при высоком давлении и температуре окружающей среды.Для подтверждения выбора материала для данного применения необходимо провести обширные исследования и испытания в конкретных условиях использования.Обратитесь в региональную группу Air Liquide для получения экспертных услуг.
Подробнее
Дополнительная информация
Аргон был открыт в 1894 году сэром Уильямом Рамзи и лордом Джоном Рэлеем. Название аргон происходит от греческого «αργόν» (аргос), что означает «ленивый» в связи с его химической неактивностью. Аргон существует только в атмосфере. Воздух содержит около 0,9 % аргона, нейтрального и бесцветного газа. Аргон широко используется в промышленности из-за его высокой химической инертности. Аргон получают воздушной криогенной перегонкой.
Название аргон происходит от греческого «αργόν» (аргос), что означает «ленивый» в связи с его химической неактивностью. Аргон существует только в атмосфере. Воздух содержит около 0,9 % аргона, нейтрального и бесцветного газа. Аргон широко используется в промышленности из-за его высокой химической инертности. Аргон получают воздушной криогенной перегонкой.
☢️ Плотность аргона (Ar) [& г/см3, кг/м3, Использование, Источники …
Все имеет массу и объем, а значит и плотность. Поэтому ожидается, что мельчайшая частица материи, такая как атом аргона, тоже имеет его. Но какова плотность атома Ar?
Примечание. Узнайте больше о плотности здесь.
В случае аргона плотность составляет 0,0017824 г/см³. Однако есть интересные факты об Аргоне, о которых мало кто знает. Также проверьте преобразование кг/м³…
Аргон Данные
Аргон Плотность г/см³
0,0017824 г/см³
кг/м³
1,7824 кг/м³
Состояние при 20 °C
Газ
Используется в осветительных приборах 9004.
 21 Его часто используют для наполнения ламп накаливания. Некоторые смешиваются с криптоном в люминесцентных лампах. Кристаллы в полупроводниковой промышленности выращивают в атмосфере аргона.
21 Его часто используют для наполнения ламп накаливания. Некоторые смешиваются с криптоном в люминесцентных лампах. Кристаллы в полупроводниковой промышленности выращивают в атмосфере аргона.Атомная масса
39 948
Узнайте больше об атомной массе.
Источники
Постоянно выбрасывается в воздух при распаде радиоактивного калия-40. Чистый вид получают фракционной перегонкой жидкого воздуха.
Атомный номер
18
Узнайте больше об атомном номере.
Атомный символ
Ar
Название Происхождение
Греческий: argos (неактивный).
Открытие
Открыто: сэром Уильямом Рэмси, бароном Рэлеем
Год: 1894
Место: Шотландия
Описание
Бесцветный благородный газ без запаха и вкуса. Это третий по распространенности элемент в земной атмосфере и составляет около 1%.
Это третий по распространенности элемент в земной атмосфере и составляет около 1%.
Хотите узнать больше деталей и данных об аргоне (Ar)? Проверьте мой полный список элементов.
Цитирование
Сульфид аммония: формула, молярная…
Пожалуйста, включите JavaScript
Сульфид аммония: формула, молярная масса и раствор
эссе, вы также должны указать, где и как вы нашли эту информацию.
Это придает достоверность вашей статье и иногда требуется в высших учебных заведениях.
Чтобы облегчить себе жизнь (и цитирование), просто скопируйте и вставьте приведенную ниже информацию в свое задание или эссе:
Luz, Gelson. «Плотность аргона (Ar) [& г/см3, кг/м3, Использование, Источники…» Материалы. Gelsonluz.com. дд мммм. гггг.
Теперь замените дд, мммм и гггг на день, месяц и год, когда вы просматривали эту страницу. Также замените URL-адрес фактическим URL-адресом этой страницы (< и > остаются, хорошо?). Этот формат цитирования основан на MLA.
Этот формат цитирования основан на MLA.
Видео
У вас возникли проблемы с пониманием основ атомарных элементов? В этом видео вы узнаете:
- Что такое элемент
- Что такое вещество
- Как выглядят элементы
- Как небольшое количество атомов может соединяться и образовывать совершенно разные вещества
Цветная периодическая таблица
Нужна редактируемая периодическая таблица для редактирования? Может быть, добавить школьный логотип, рабочую команду или что-нибудь еще, чтобы ваша газета выглядела круто?
Наряду с основной информацией об атоме / элементе (например, плотность аргона и все другие атомные данные) он также содержит информацию с цветовой кодировкой о: состоянии (газ, жидкость или твердое тело при комнатной температуре), деталях групп / серий и многом другом. ..
Как насчет стимула поделиться этим постом? (Вы поможете другим коллегам найти этот блог)
Загрузите и наслаждайтесь этой полной и цветной периодической таблицей, которую вы можете редактировать и наслаждаться.

