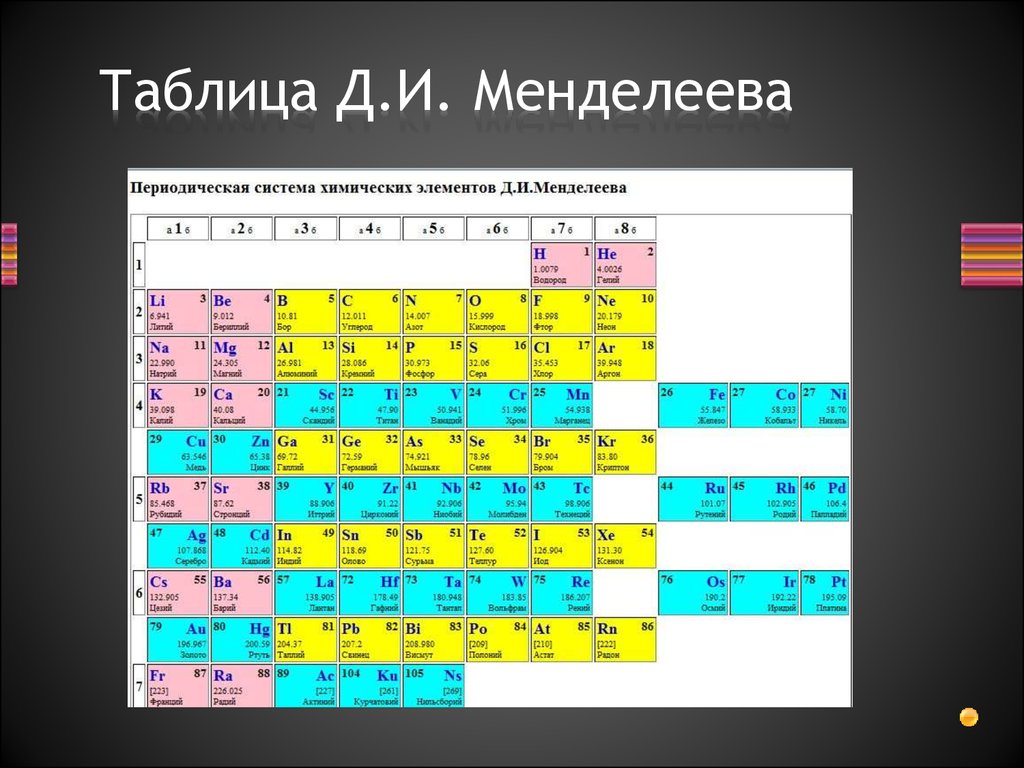
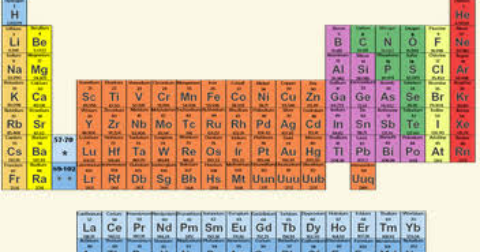
Атомная масса цинка: Молярная масса цинка (Zn), формула и примеры
alexxlab | 16.01.2023 | 0 | Разное
ICSC 0349 – СУЛЬФАТ ЦИНКА ДЕСЯТИВОДНЫЙ
ICSC 0349 – СУЛЬФАТ ЦИНКА ДЕСЯТИВОДНЫЙ« back to the search result list(ru)
Chinese – ZHEnglish – ENFinnish – FIFrench – FRHebrew – HEHungarian – HUItalian – ITJapanese – JAKorean – KOPersian – FAPolish – PLPortuguese – PTRussian – RUSpanish – ES
| СУЛЬФАТ ЦИНКА ДЕСЯТИВОДНЫЙ | ICSC: 0349 (Октябрь 2001) |
| CAS #: 7446-20-0 |
| EINECS #: 231-793-3 |
| ОСОБЫЕ ОПАСНОСТИ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ТУШЕНИЕ ПОЖАРА | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Не горючее. |
В случае возникновения пожара в рабочей зоне, использовать надлежащие средства пожаротушения. |
| НЕ ДОПУСКАТЬ ОБРАЗОВАНИЕ ПЫЛИ! | |||
|---|---|---|---|
| СИМПТОМЫ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ПЕРВАЯ ПОМОЩЬ | |
| Вдыхание | Кашель. Боли в горле. Сбивчивое дыхание. | Применять местную вытяжку или средства защиты органов дыхания. | Свежий воздух, покой. Может потребоваться искусственное дыхание. |
| Кожа | Покраснение. | Защитные перчатки. | Снять загрязненную одежду. Промыть кожу большим количеством воды или принять душ. |
| Глаза | Покраснение. Боль. Потеря зрения. | Использовать защитные очки. |
Прежде всего промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно сделать без затруднений), затем обратится за медицинской помощью. |
| Проглатывание | Боль в животе. Диарея. Тошнота. Рвота. | Не принимать пищу, напитки и не курить во время работы. | Прополоскать рот. Дать выпить один или два стакана воды. Обратиться за медицинской помощью . |
| ЛИКВИДАЦИЯ УТЕЧЕК | |
|---|---|
Индивидуальная защита: Респиратор с сажевым фильтром, подходящий для концентрации вещества в воздухе. НЕ допускать попадания этого химического вещества в окружающую среду. Смести просыпанное вещество в закрытые контейнеры. Тщательно собрать оставшееся. Затем хранить и утилизировать в соответствии с местными правилами. Затем хранить и утилизировать в соответствии с местными правилами. |
Согласно критериям СГС ООН Транспортировка |
| ХРАНЕНИЕ | |
| Хорошо закрывать. Хранить в местах не имеющих сливов или доступа к канализации | |
| УПАКОВКА | |
| СУЛЬФАТ ЦИНКА ДЕСЯТИВОДНЫЙ | ICSC: 0349 |
| ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА | |
|---|---|
|
Агрегатное Состояние; Внешний Вид
Физические опасности
Химические опасности
|
Формула: ZnSO4. 7H2O |
| ВОЗДЕЙСТВИЕ НА ОРГАНИЗМ И ЭФФЕКТЫ ОТ ВОЗДЕЙСТВИЯ | |
|---|---|
|
Пути воздействия
Эффекты от кратковременного воздействия
|
Риск вдыхания
Эффекты от длительного или повторяющегося воздействия
|
| Предельно-допустимые концентрации |
|---|
|
MAK: (вдыхаемая фракция): 0.1 mg/m3; категория ограничения пикового воздействия: I(4). MAK: (ингаляционная фракция): 2 mg/m3; категория ограничения пикового воздействия: I(2). MAK: группа риска для беременности: C |
| ОКРУЖАЮЩАЯ СРЕДА |
|---|
| Вещество очень токсично для водных организмов. |
| ПРИМЕЧАНИЯ |
|---|
| См. карту ICSC 1698. |
| ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ |
|---|
|
Классификация ЕС Символ: Xn, N; R: 22-41-50/53; S: (2)-22-26-39-46-60-61 |
| (ru) | Ни МОТ, ни ВОЗ, ни Европейский Союз не несут ответственности за качество и точность перевода или за возможное использование данной информации. © Версия на русском языке, 2018 |
Изотопы цинка | Производственное объединение «Электрохимический завод»
Цинк природного происхождения имеет пять стабильных изотопов:
64Zn (цинк-64), 66Zn (цинк-65), 67Zn (цинк-67), 68Zn (цинк-68) и 70Zn (цинк-70).
Цинк-64 является наиболее обильным (48,6 % природного содержания ). Известны двадцать пять радиоизотопов цинка, наиболее долгоживущие из них – 65Zn (период полураспада 244,26 дней) и 72Zn (период полураспада 46,5 часа). Все остальные радиоактивные изотопы имеют периоды полураспада менее 14 часов, и большинство из них имеют периоды полураспада менее 1 секунды.
| ИЗОТОП | ПРИРОДНОЕ СОДЕРЖАНИЕ, % | СТЕПЕНЬ ОБОГАЩЕНИЯ, % | ХИМИЧЕСКИЕ ФОРМЫ |
| 64Zn обедн. | 48,17 | < 1 | металл (Zn) оксид (ZnO) порошок, таблетки ацетат (Zn(CH3COO)2 ×H2O) |
| 64Zn | 48,17 | 99,90 | |
| 66Zn | 27,73 | 99,00 | |
| 67Zn | 4,04 | 78,00 | |
| 68Zn | 18,45 | 99,00 | |
| 70Zn | 0,61 | 99,50 |
Основные сферы использования: атомная энергетика, научные исследования, медицина.
| По данным открытых источников | |
| ИЗОТОП | ОБЛАСТИ ПРИМЕНЕНИЯ |
| цинк, обедненный по 64Zn | – добавка в форме окиси или ацетата в водяной теплоноситель энергетических ядерных реакторов для предотвращения коррозии конструкционных материалов и снижения дозовой нагрузки на персонал АЭС |
| 64Zn | – регистрация малых потоков нейтронов, определение нейтронных спектров реакторов |
| 66 Zn | – получение генератора для производства радиоизотопа 68Ga (галий-68) для использования в медицине |
| 67Zn | – определение потребностей человека в цинке, выявление нарушений обмена веществ, заболеваний печени, алкоголизма; – получение радиоизотопа 67Ga (галий-67) для использования в медицине; – исследование с использованием мёссбауэровской спектроскопии радиационной стойкости сплавов Cu–Fe; – исследование влияния добавок магнитных изотопов на радиационно-оптические свойства веществ в аморфном виде; – изучение распределения металлов в организме животных |
| 68Zn | – получение радиоизотопа 67Ga (галий-67) на циклотроне для диагностики системных злокачественных новообразований первичных и метастатических опухолей лёгких и мягких тканей |
| 70Zn | – исследование миграции элементов в почве, растительности и других природных средах методом изотопных индикаторов |
Цинк-67, цинк-68 и цинк-70 применяются для получения терапевтического изотопа 67Cu (медь-67). | |
► К таблице выпускаемых изотопов
Использование цинка, обедненного по изотопу 64Zn, в атомной энергетике
Особый интерес представляет цинк, обедненный по изотопу 64Zn, используемый в качестве добавки в системах охлаждения ядерных реакторов. Добавление цинка снижает количество радиоактивного 60Со, образующегося в результате облучения потоком нейтронов природного кобальта, который в свою очередь содержится в конструкционных материалах оборудования. Присутствие 60Со способствует накоплению радиоактивного излучения в системах охлаждения, и, как следствие, приводит к увеличению мощности дозы облучения, получаемой персоналом. Если вводится природный цинк, а в природной смеси изотопов на долю 64Zn приходится 48,6 %, под облучением потоком нейтронов 64Zn образует радиоактивный 65Zn, который только увеличивает мощность дозы облучения. Если удалить из природной смеси изотопы 64Zn, можно значительно сократить дозовую нагрузку ремонтного персонала, уменьшить количество радиоактивных отходов, увеличить срок службы реактора.
Если удалить из природной смеси изотопы 64Zn, можно значительно сократить дозовую нагрузку ремонтного персонала, уменьшить количество радиоактивных отходов, увеличить срок службы реактора.
Рассчитайте относительную атомную массу сульфата цинка.\\[\\left[ {Zn = 65;{\\text{ }}S = 32;{\text{ }}O = 16} \\right]\\ ]
Ответить
Проверено
216.6k+ views
Подсказка: Атом состоит из ядра с нейтронами и протонами, которые окружены электронами на орбитах. Количество протонов (атомный номер) можно считать равным общему количеству электронов в нейтральном атоме (обозначается как Z). Принимая во внимание, что сумма количества нейтронов и количества протонов равна массовому числу атома или атомной массы (обозначается как M).
Полный ответ:
– Шкала относительной атомной массы теперь основана на изотопе углерода, то есть на углероде-12. Таким образом, мы можем сказать, что относительная атомная масса равна средней массе всех атомов, присутствующих в элементе, по сравнению с 1/12 массы атома C-12.
– Из-за присутствия большего количества нейтронов (по сравнению с протонами) в ядре относительная атомная масса обычно как минимум вдвое превышает атомный номер. Следует также отметить, что числовая разница между атомным номером и относительной атомной массой увеличивается с увеличением атомного номера.
– В настоящем вопросе нам не даются различные изотопные массы и процентное содержание элементов, поэтому мы грубо рассчитаем относительную атомную массу сульфата цинка, добавив атомную массу каждого атома следующим образом:
– Сульфат цинка имеет химическая формула $ZnS{O_4}$, которая содержит 1 атом \[Zn\], 1 атом \[S\] и 4 атома \[O\].
Относительная атомная масса = $(1 \times 65) + (1 \times 32) + (4 \times 16) = 161$
Отсюда относительная атомная масса сульфата цинка 161,
Примечание:
Чтобы рассчитать точную относительную атомную массу, необходимо учитывать разные массы изотопов одного и того же элемента, а также их процентное содержание в элементе.
Недавно обновленные страницы
В Индии по случаю бракосочетания фейерверк 12 класса химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть организованы 12 класса химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал 12 класс химия JEE_Main
Что из нижеперечисленного является истинным пероксидом A rmSrmOrm2 класс 12 по химии JEE_Main
Какой элемент обладает наибольшим атомным радиусом A класс 11 по химии JEE_Main
Фосфин получают из следующей руды A Кальций класса 12 по химии JEE_Main
В Индии на по случаю брака фейерверк 12 класс химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть организованы 12 класс химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал 12 класс химии JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 класс 12 по химии JEE_Main
Какой элемент обладает наибольшим атомным радиусом A класс 11 по химии JEE_Main
Фосфин получают из следующей руды A Кальций класс 12 по химии JEE_Main 6 Актуальные сомнения Студенты также читают Атомная масса и молекулярная масса Разница между атомной массой и атомным весом Атомная масса элементов|Атомная масса первых 30 элементов атомного числа и массового числа Атомного числа и массового числа, изотопы и изобаров Экстракция цинка Размер атомного и атомного радиуса Цинк фосфат Гидроксид Zinc Рассчитайте массу цинка, образующегося при пропускании тока силой 0,2 ампера через
камеру на 45 минут. Возьмем молярную массу цинка 65,4 грамма на моль и заряд в один фарадей.
90,65 умножить на 10 по четырем кулонам. Ответ дайте в граммах с точностью до трех знаков после запятой. В этой задаче ток в ячейке вызывает восстановление двух ионов цинка с образованием
твердый цинк. Мы сможем решить эту проблему, если сможем определить, сколько электронов отреагировало на
образуют в клетке металлический цинк. Мы можем использовать эту формулу для расчета общего заряда, где 𝑄 — общий заряд,
𝐼 — ток, а 𝑡 — время, измеряемое в секундах. Отсюда мы можем определить количество электронов, доставленных в клетку, а затем
определите массу образовавшегося цинка. Эта проблема дала нам ток 0,2 ампера. И проблема говорит, что ток проходил через ячейку в течение 45 минут. Теперь нам нужно знать, скольким электронам эквивалентен этот общий заряд, чтобы мы могли
рассчитать количество образовавшегося цинка. Мы можем вычислить это, используя эту формулу, которая говорит нам, что заряд равен
количество заряженных частиц, умноженное на постоянную Фарадея. Мы хотим найти количество, поэтому нам нужно изменить это уравнение, чтобы изолировать
𝑛. Мы можем сделать это, если разделим обе части уравнения на 𝐹, что дает нам это
уравнение. Давайте быстро поменяем это уравнение так, чтобы 𝑛 было в левой части. Теперь мы можем подключить заряд, который мы рассчитали для 𝑄. И подставим постоянную Фарадея вместо 𝐹, которая дана в задаче
9,65 умножить на 10 до четырех кулонов заряда на моль заряженных частиц. Единицы кулонов сокращаются, и мы получаем около 0,0055958 молей электронов. Теперь нам нужно выяснить, сколько цинка образуется при таком количестве электронов.
реагируют с ионами цинка. Из нашего уравнения реакции мы видим, что каждые два моля электронов образуют один
моль твердого цинка. Итак, количество цинка вдвое меньше количества электронов. Итак, нам нужно вычислить половину от 0,0055958, что составляет около 0,0027979 молей. Последнее, что нам нужно сделать, это преобразовать это количество цинка в массу
цинк. Мы можем сделать это, умножив количество цинка на молярную массу цинка. Подставим сумму, которую мы только что вычислили. И молярная масса была дана в задаче; это 65,4 грамма на моль. Единицы молей сокращаются, и мы получаем примерно 0,182984 грамма. Вопрос.
 ячейке в течение периода времени с учетом тока
ячейке в течение периода времени с учетом тока Стенограмма видео
 Но нам нужно выразить это время в секундах, чтобы включить его в наше уравнение. В одной минуте 60 секунд, поэтому мы можем преобразовать минуты в секунды, если
умножьте на 60. Это дает нам 2700 секунд. Мы можем пойти дальше и подключить это к нашей проблеме. Один ампер эквивалентен одному кулону в секунду. Мы можем заменить эти единицы. Итак, теперь секунды отменяются. Общий заряд составляет 540 кулонов.
Но нам нужно выразить это время в секундах, чтобы включить его в наше уравнение. В одной минуте 60 секунд, поэтому мы можем преобразовать минуты в секунды, если
умножьте на 60. Это дает нам 2700 секунд. Мы можем пойти дальше и подключить это к нашей проблеме. Один ампер эквивалентен одному кулону в секунду. Мы можем заменить эти единицы. Итак, теперь секунды отменяются. Общий заряд составляет 540 кулонов.