Что такое электрохимическая и химическая коррозия – 2. Химическая и электрохимическая коррозия. Виды коррозии, встречающиеся в судовой практике.
alexxlab | 23.02.2020 | 0 | Разное
Электрохимическая коррозия и химическая: определение и защита
Больше всего металлы боятся коррозии. Она способна привести в негодность самые прочные конструкции. Огромные мосты, линии электропередач, километровые трубопроводы становятся беспомощными перед разрушающим процессом. Чтобы повреждения не допустить, металл защищают. Но важно понимать, что бывает несколько видов окисления. Электрохимическая коррозия, химическая или газовая – все они похожи по следствиям, но эффективными методами защиты от каждого вида будут свои индивидуальные мероприятия, зависящие от многих факторов.
Коррозия электрохимического плана наиболее часто поражает металлы. Это связано с тем, что они, как правило, неустойчивы термодинамически в среде, которая их окружает, а последняя чаще представляет обычный электролит, то есть проводник. Поэтому за счет металла коррозионная среда стремится к восстановлению путем переноса частиц через электрический ток.

Суть, причины и признаки химической коррозии
Для возникновения химической коррозии нужно не так уж много: металл и соответствующая коррозионная среда. Причины большой вероятности появления окисления – это неустойчивое термодинамическое состояние металла и стремление его перейти к более устойчивому состоянию. Словесной формулой это можно выразить следующим образом:
Исходный металл + среда окислительного характера = протеканию реакции = результату в виде ржавчины.
Основной признак химической коррозии – окислительная среда – не является электролитом как при электрохимической, то есть окислительно-восстановительные процессы имеют чисто химический подтекст. Химическая коррозия бывает двух видов:
- та, которая протекает в газовой среде, когда температура вокруг очень высока;
- второй вид химической коррозии связан с жидкостями.
Для идеальной защиты от коррозии необходимо проводить мероприятия комбинированной защиты, так как в реальности на металл воздействует одновременно и электрохимическое, и химическое окисление.
Отличия химической коррозии от электрохимической
Под процессом электрохимической коррозии понимают окислительно-восстановительную реакцию коррозионной среды за счет электронов металла, которые отнимаются у него под воздействием электрического потенциала, возникающего в электролите, коим является эта окислительная среда. Ионизация сопровождается разрушением той части, которая непосредственно контактирует со средой, а ржавчина, видимая невооруженным глазом, не что иное, как восстановленная коррозионная среда.
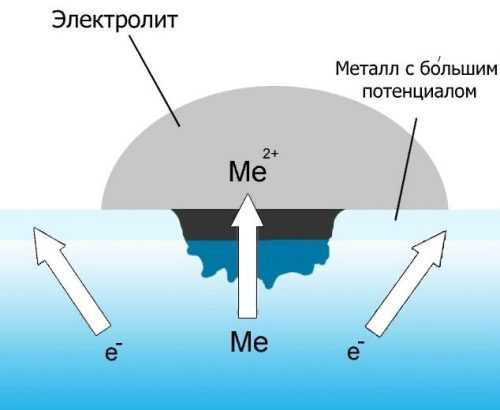
Если говорить о том, чем отличается коррозия химического плана от электрохимической, то здесь есть несколько принципиальных моментов:
- Сущностью электрохимической коррозии является процесс, протекающий в электролите, и это главное.
- В электрохимической обязательно присутствует электрический ток, чего нет при химическом окислении.
- Электрохимическая коррозия характеризуется не одномоментным переходом частиц от металла к окислительному компоненту, а определяется величиной потенциала. То есть, чем потенциал выше, тем больше скорость движения частиц и быстрее восстановительный процесс коррозионной среды. При химическом же процессе разрушение вещества сопровождается одновременным восстановлением коррозионной среды.
Выделяют следующие виды электрохимической коррозии:
- Межкристаллитная. Электрохимическое явление, когда у алюминия, никеля, иных элементов наблюдается разрушение зерна по его границе, и происходит это избирательно. В результате конструкция теряет свою прочность, ухудшаются свойства пластичности. Опасность в том, что этот электрохимический процесс визуально может быть незаметен.
- Питтинговая. Проявляется как поражение точечных участков на таких элементах, как медь, ее сплавы и другие. Размер отдельных участков, где проявляется коррозия, обычно не превышает 1.5 миллиметров. Электрохимический питтинг бывает поверхностного типа, а также открытый и закрытый.
- Щелевая. Опасный вид электрохимической коррозии, сопровождающийся быстрым усиленным разрушением областей, где есть микротрещины, зазоры либо щели. Коррозия может протекать при любом состоянии окружающей среды.
Протекторная защита от электрохимической коррозии
Как упоминалось выше, чем больше потенциал металла, тем быстрее происходит электрохимическая коррозия. Значит, снижая электрический потенциал, можно добиться наступления момента, когда процесс окисления станет невозможным. На этом принципе основана протекторная или, другими словами, электрохимическая защита металлических конструкций, газопроводов, корпусов морских судов. Берется такой металл, который ведет себя активнее, нежели основной защищаемый, и соединяется с последним токопроводящим проводником. Получается, что уже этот анод вступает в реакцию с коррозионной средой, а основной металл остается невредимым.
Анодную защиту нужно периодически возобновлять, ведь «жертвенный металл» в процессе эксплуатации также очень сильно разрушается, особенно если он не совсем правильно подобран для работы в конкретной среде.
Основные случаи, когда применение протекторной защиты будет оправдано:
- Недостаточно средств на проведение более дорогостоящих защитных мероприятий.
- Если защитой нужно обеспечить конструкции из металла небольших габаритов.
- Когда трубопроводы имеют дополнительную поверхностную изоляцию.
Такую защиту от электрохимической коррозии, как протекторная, применяют, в основном, к разным маркам стали. Здесь уместным будет использование протекторов на основе кадмия, алюминия, магния, хрома, цинка, но используется не чистый элемент, а сплавы.
Цинковые протекторы
Цинковые протекторы, кроме основы из цинка, содержат:
- до 0.15% кадмия при минимально возможном процентном соотношении в 0.025%;
- до 0.5% алюминия;
- примеси железа, свинца и меди, общей суммой не превышающие 0.005%.
Наиболее эффективное применение цинка выявлено в морской воде, где с помощью таких протекторов успешно работает защита, например, газовых или нефтяных магистралей. Плюс цинка еще в том, что он допустим к использованию со взрывоопасными веществами. Когда происходит растворение анода, не наблюдается выделения загрязняющих веществ, которые могут навредить экологии.
Применение цинковых протекторов в водоемах, где вода имеет пресный состав либо в грунте под землей сопровождается быстрым образованием на поверхности протектора таких соединений, как оксиды и гидроксиды, которые приводят к торможению электрохимического процесса окисления анода, и фактически прекращается защита основного металла от электрохимической коррозии.
Установка цинкового протектора на днище корабля:

Магниевые протекторы
В чистом виде магниевые протекторы нецелесообразно применять, что объясняется быстрым ржавлением этого металла. Поэтому коррозионные защитники на базе магния, кроме него, имеют:
- максимум 5%, минимум 2% цинка;
- максимум 7%, минимум 5% алюминия;
- небольшое содержание меди, никеля и свинца, не более десятых долей процента.
Протекторы из магния хороши, когда среда, в которой они применяются, имеет pH не выше 10.5, что соответствует грунтам обычного характера, водным объектам со слабосоленой акваторией либо попросту пресной воде. Для защиты подходят любые трубопроводы и металлоконструкции, находящиеся в описанных выше условиях. Применение магния в агрессивных соленых растворах сопровождается быстрым образованием плохо растворимой пленки на его поверхности.
В некоторых случаях магниевые протекторы влияют на металл таким образом, что последний становится более хрупким, и в теле конструкции могут образовываться трещины. Прежде чем применять магний для защиты от электрохимической коррозии конкретной марки стали, нужно провести дополнительные исследования, чтобы избежать негативных последствий.
Алюминиевые протекторы
Целевое назначение протекторов из алюминия – работать в качестве защиты от электрохимической коррозии в средах с водой проточной с соленым составом, например, в прибрежных морских водах. В составе сплава протектора из алюминия имеются:
- примеси индия, кадмия, кремния не более 0.02%;
- цинка – до 8%;
- магния – до 5%.
Благодаря этим дополнительным металлам нет возможности появления на протекторе жесткой, задерживающей растворение пленки. Допустимо применять алюминиевый протектор и в средах, подходящих для магниевого протектора.
Способы защиты металлов от химической коррозии
Так как химическая коррозия никоим образом не связана с потенциалом металла, и протекторы либо катоды ее не предотвратят, способы защиты от нее имеют свою специфику. Борьба с разрушением такого характера может проходить по трем основным направлениям:
- Метод конструкционного решения проблемы. Он связан с тем, чтобы использовать сплавы, которые имеют очень высокую устойчивость к коррозии, либо применять биметаллические композиции, где основной конструкционный металл покрыт тонким слоем устойчивого соединения (например, оцинковку).
- Метод улучшения среды, где будет эксплуатироваться изделие, путем изменения pH, нейтрализации агрессивных составляющих коррозионной среды.
- Метод пассивной защиты, наиболее известный тем, что доступ к поверхности конструкции в коррозионной среде блокируется пленкой из неактивного и не вступающего в реакцию материала. Это покрытие разного рода лакокрасочными компонентами для защиты от коррозии.
Если вы сталкивались с электрохимической коррозией, имеете профильное образование, ориентируетесь в вопросах защиты металла, получили практические навыки по организации протекторной защиты металлоконструкций либо применяли метод катодной защиты, поделитесь своими знаниями в комментариях.
wikimetall.ru
2.2 Электрохимическая коррозия металлов
Под электрохимической коррозией подразумевают процесс взаимодействия металлов с электролитами в виде водных растворов, реже с неводными электролитами, например, с некоторыми органическими электропроводными соединениями или безводными расплавами солей при повышенных температурах. Делится на электрокоррозию и гальванокоррозию. Из указанных разновидностей рассмотрим лишь гальванокоррозию.
2.2.1 Электрохимическая гальванокоррозия. Электрохимическая коррозия – наиболее распространенный вид коррозии металлов. Примером коррозионных процессов электрохимического характера является разрушение деталей машин, приборов и различных металлических конструкций в почвенных, грунтовых, речных и морских водах, в атмосфере под адсорбированными пленками влаги, в технических растворах.
Растворенный кислород и ионы водорода – важнейшие окислители, вызывающие электрохимическую коррозию металлов.
Рассмотрим схему этого процесса. Сложность его заключается в том, что на одной и той же поверхности происходят одновременно два процесса, противоположные по своему химическому смыслу: окисление металла и восстановление окислителя. Оба процесса должны протекать сопряженно, чтобы сохранялось равенство числа электронов, отдаваемых металлом и присоединяющихся к окислителю в единицу времени. Только в этом случае может наступить стационарное состояние.
Итак, процессы электрохимической коррозии протекают по законам электрохимической кинетики, когда общая реакция взаимодействия может быть разделена на следующие, в значительной степени самостоятельные, электродные процессы:
– анодный процесс – переход металла в раствор в виде ионов (в водных растворах, обычно гидратированных) с оставлением эквивалентного количества электронов в металле:
Ме 0 – nē → Ме n+
– катодный процесс – ассимиляция появившихся в металле избыточных электронов деполяризаторами.
Различают коррозию с водородной и кислородной (или окислительной) деполяризацией. При наличии в растворе газообразного кислорода и невозможностью протекания процесса коррозии с водородной деполяризацией основную роль деполяризатора исполняет кислород. Коррозионные процессы, у которых катодная деполяризация осуществляется растворенным в электролите кислородом, называют процессами коррозии металлов с кислородной деполяризацией. Это наиболее распространенный тип коррозии металла в воде, в нейтральных и даже в слабокислых солевых растворах, в морской воде, в земле, в атмосфере воздуха.
Общая схема кислородной деполяризации сводится к восстановлению молекулярного кислорода до иона гидроокисла:
В случае водородной деполяризации на катоде протекает процесс восстановления ионов водорода, находящихся в среде:
2Н++ 2ē + → Н2.
2.3Способы защиты от коррозии
Выбор того или иного способа определяется его эффективностью, а также экономической целесообразностью.
2.3.1 Легирование металла – эффективный (хотя обычно дорогой) метод повышения коррозионной стойкости металлов. При легировании в состав сплава обычно вводят компоненты, вызывающие пассивирование металла. В качестве таких компонентов применяются хром, никель, вольфрам и др.
Основное средство защиты металлов от газовой коррозии – легирование такими компонентами, которые улучшают свойства защитных пленок, образующихся при окислении металла. Для стали такими элементами являются хром, алюминий, кремний. Эти элементы при высоких температурах окисляются энергичнее, чем железо, и образуют при этом плотные защитные пленки оксидов.
2.3.2 Защитные покрытия. Слои, искусственно создаваемые на поверхности металлических изделий и сооружений для предохранения их от коррозии, называются защитными покрытиями. Выбор вида покрытия зависит от условий, в которых используется металл.
Широко распространенным способом защиты металлов от коррозии является покрытие их слоем других металлов. Покрывающие металлы сами корродируют с малой скоростью, так как покрываются плотной оксидной пленкой. В зависимости от величины электродного потенциала защищаемого металла и покрытия, различают катодные и анодные покрытия.
Катодное покрытие – металл покрытия менее активен, чем защищаемый металл. Например, олово хорошо покрывает железо и достаточно стойко против действия разбавленных растворов кислот. В случае механического повреждения такого покрытия возникает гальваническая пара, в которой электроны переходят от железа к олову; анодом здесь является железо, а катодом олово. В этом случае разрушается железо, а олово остается без изменений (рисунок 5).
Анодное покрытие – покрытие более активным металлом. Например, покрытие железа цинком (рисунок 4). При механическом повреждении цинкового покрытия возникает гальваническая пара, в которой железо служит катодом, а анодом – цинк. Электроны переходят от цинка к железу, цинк разрушается, а железо остается защищенным до тех пор, пока не разрушится весь цинк. На основании вышеизложенного можно сделать вывод о том, что более надежным является анодное покрытие.
а)б)
1 – раствор; 2 – покрытие; 3 – основной материал; 4 – пора
Рисунок 4 – Схема коррозии металла в кислом
растворе при нарушении анодного а) и катодного б) покрытия
К ряду покрытий, получаемых химической обработкой металла, относятся защитные покрытия, образующиеся непосредственно на поверхности металла. Образование на поверхности металлических изделий защитных оксидных пленок носит в технике общее название оксидирование.
Неметаллические защитные покрытия могут быть как неорганическими, так и органическими. Защитное действие этих покрытий сводится в основном к изоляции металла от окружающей среды. В качестве неорганических покрытий могут быть неорганические эмали, оксиды металлов, соединения хрома, фосфора и др. К органическим относятся лакокрасочные покрытия, покрытия смолами, пластмассами, полимерными пленками, резиной.
2.3.3 Электрохимические методы защиты. Методы электрохимической защиты основаны на изменении потенциала защищаемого металла и не связаны с изоляцией металла от коррозионной среды. К ним относятся катодная защита, называемая также электрозащитой, и протекторная (или анодная) защита.
Катодная защита заключается в том, что защищаемая конструкция А (рисунок 5), находящаяся в среде электролита (например, в почвенной воде), присоединяется к катоду внешнего источника электричества В. Защищаемая конструкция становится катодом. В ту же агрессивную среду помещают кусок старого металла Б (рельс, балка), присоединяемый к аноду внешнего источника электричества. В процессе коррозии этот кусок старого металла становится анодом и разрушается.
Протекторная защита отличается от катодной защиты тем, что для ее осуществления используется специальный анод – протектор, в качестве которого применяют металл более активный, чем металл защищаемой конструкции (алюминий, цинк). Протектор Б (рисунок 6) соединяют с защищаемой конструкцией А проводником электрического тока В. В процессе коррозии протектор служит анодом и разрушается, тем самым предохраняя от разрушения защищаемую конструкцию.
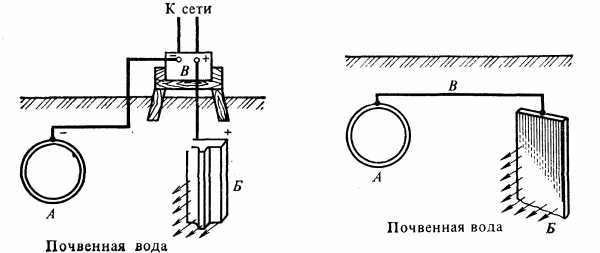
Рисунок 5 – Схема катодной Рисунок 6 – Схема анодной
защиты (протекторной) защиты
2.3.4 Изменение свойств коррозионной среды. Изменение свойств коррозионной среды пригодно для случаев, когда защищаемое изделие эксплуатируется в ограниченном объеме жидкости. Один из методов состоит в удалении из раствора, в котором эксплуатируется защищаемая деталь, растворенного кислорода (деаэрация). В качестве примера можно привести освобождение воды, идущей на питание паровых котлов, от растворенного в ней кислорода, что достигается, например, при фильтровании воды через слой железных стружек.
Для замедления коррозии металлических изделий в агрессивную среду вводят вещества, называемые ингибиторами (или замедлителями) коррозии. Это имеет большое значение в тех случаях, когда металл необходимо защищать от разъедания кислотами. В зависимости от вида коррозии, природы металла и раствора применяются различные ингибиторы, действие которых специфично.
2.3.5 Создание рациональных конструкций. Выбор материалов и их сочетаний для данной машины, конечно, диктуется технической и экономической целесообразностью, но должен обеспечивать ее коррозионную устойчивость. Конструктор должен предусмотреть рациональные формы машины, допускающие быструю очистку от грязи; машина не должна иметь мест скопления влаги, которая является возбудителем коррозии.
studfiles.net
Коррозия химическое и электрохимическое – Справочник химика 21
Различают два вида коррозии химическую и электрохимическую. Химическая коррозия — это непосредственное взаимодействие металла с токонепроводящей внешней средой. Например, окисление металла кислородом воздуха при высокт” температуре (газовая коррозия) или разрушение, происходящее при низких температурах в органических растворителях, нефти и т. п. Некоторые оксидные пленки защищают металлы в той или иной степени от даль-нейш его разрушения (АиОз, ZnO, MgO, N 0, СггОз), другие, напротив, способствуют развитию процесса коррозии (оксиды железа, щелочных и щелоч оземельных металлов). Электрохимическая коррозия — процесс разрушения металла в растворе электролита. Взаимодействие металла с растворами, способными проводить электрический ток, происходит не только при непосредственном погружении металлического изделия в раствор электролита, но даже при хранении в атмосферных условиях, так как на его поверхности образуется тонкая пленка влаги, В этом тонком слое [c.90]По характеру взаимодействия металла со средой различают два основных типа коррозии химическую и электрохимическую. [c.7]
Разрушение металлов под воздействием внешней среды называется коррозией. Ржавление — частный случай коррозии, когда разрушению подвергаются черные металлы, т. е. железо и его сплавы. В зависимости от характера внешней среды, с которой взаимодействует металл, различают два вида коррозии — химическую и электрохимическую. = [c.131]
Известно, что металлы и их сплавы разрушаются под воздействием воздуха, воды, различных других веществ Разрушение металлов (или их сплавов) под воздейст рием окружающих условий, при котором они теряют присущие им свойства, называется коррозией. Различают два основных типа коррозии химическую и электрохимическую. [c.322]
Принято различать коррозию химическую и электрохимическую. При химической коррозии металлы подвергаются действию различных газов, паров воды (при высокой температуре), а также действию жидкостей, не проводящих электрического тока. Электрохимическая коррозия происходит под действием растворов различных электролитов. [c.180]
Коррозия металла — разрушение его под воздействием окружающей среды — самопроизвольный и нежелательный процесс. Различают два вида коррозии химическую и электрохимическую. Химической коррозией называется разрушение металла окислением его в окружаюш,ей среде без возникновения электрического тока в системе. В этом случае происходит взаимодействие металла с составными частями среды — с газами и неэлектролитами. [c.177]
Коррозией называется разрушение металлов или сплавов в результате воздействия внешней среды. По механизму протекания коррозионного процесса различают два вида коррозии химическую и электрохимическую. [c.14]
Различают два вида коррозии — химическую и электрохимическую. Если окисление металла происходит как обычная химическая реакция (соединение железа с кислородом при высокой температуре с образованием окалины), то коррозию называют химической. [c.168]
По механизму протекания коррозионного разрушения различают два типа коррозии химическую и электрохимическую. [c.160]
Металлы подвергаются коррозии. Под коррозией понимают разрушение металла под воздействием окружающей среды. Это самопроизвольный окислительно-восстановительный процесс. По механизму протекания разрушения различают два типа коррозии химическую и электрохимическую. [c.233]
Коррозией называют процессы разрушения металлов при их контакте с внешней средой. Возможны два вида коррозии химическая и электрохимическая. [c.275]
Металлы подвергаются коррозии. Под коррозией понимают разрушение металла под воздействием окружающей среды. Различают два вида коррозии химическую и электрохимическую. [c.316]
Различают два процесса коррозии — химический и электрохимический. Первый наблюдается при взаимодействии металла со средой путем химических реакций. Наиболее распространенным примером химической коррозии является газовая коррозия, имеющая место, в частности, при контакте металлов с сернистым газом, сероводородом, углекислым газом и другими газами при повышенных температурах, [c.6]
По механизму протекания процесса различают два вида коррозии химическую и электрохимическую. [c.65]
Ход процесса коррозии и его механизм в з ачительной мере зависят от среды, в которой она протекает. Различают два основных вида коррозии—химическую и электрохимическую. [c.12]
Основной задачей в раскрытии механизма структурной коррозии, химической и электрохимической обработки металлов является дальнейшее совершенствование методики электрохимических исследований, которая должна обеспечить снятие потенциостатических кривых для отдельных структурных составляющих и физически неоднородных участков металла, т. е. методики, позволяющей поддержать заданный потенциал и одновременно определять дифференциальные токи (плотности анодных токов) на отдельных структурных составляющих и физически неоднородных участках металла, соответствующие данному потенциалу. [c.81]
Применение такой методики позволит более успешно раскрывать особенности структурной коррозии, химической и электрохимической обработки различных сталей и сплавов. [c.81]
Нижеописанные опыты мы распределили по видам коррозии — химической и электрохимической. [c.249]
Далее рассмотрим отдельные типы коррозии химическую и электрохимическую. [c.10]
Вопросы внутренней коррозии нами в настоящей главе не-рассматриваются. Внешняя коррозия происходит по внешней поверхности трубопроводов, резервуаров, аппаратов и других конструкций и разделяется по механизму действия на коррозию химическую и электрохимическую. [c.335]
Коррозия металлов представляет собой окислительно-восстановительный процесс. Металлы при этом окисляются, а вещества, с которыми они взаимодействуют, восстанавливаются. Различают коррозию химическую и электрохимическую.&ensp
www.chem21.info
Коррозия электрохимическая и химическая — Мегаобучалка
Разрушение металла под воздействием окружающей среды называют коррозией.
Коррозия помимо уничтожения металла отрицательно влияет на эксплуатационные характеристики деталей, содействуя всем видам разрушения.
Коррозия в зависимости от характера окружающей среды может быть химической и электрохимической.
Электрохимическая коррозия имеет место в водных растворах, а так же в обыкновенной атмосфере, где имеется влага.
Сущность этой коррозии в том, что ионы металла на поверхности детали, имея малую связь с глубинными ионами, легко отрываются от металла молекулами воды.
Металл, потеряв часть положительно заряженных частиц, ионов, заряжается отрицательно за счет избыточного количества оставшихся электронов. Одновременно слой воды, прилегающий к металлу, за счет ионов металла приобретает положительный заряд. Разность зарядов на границе металл – вода обуславливает скачок потенциала, который в процессе коррозии изменяется, увеличиваясь от растворения металла, и уменьшаясь от осаждения ионов из раствора на металле.
Если количество ионов переходящих в раствор и осаждающихся на металле одинаково, то скорости растворения и осаждения металла равны и процесс коррозии (разрушения металла) не происходит. Этому соответствует равновесный потенциал .
За нулевой потенциал принимают равновесный потенциал водородного иона в водном растворе при концентрации положительных ионов водорода, равной 1 моль ионов + на 1 литр.
Стандартные потенциалы других элементов измерены по отношению к водородному потенциалу.

Металлы, стандартный потенциал которых отрицательный – корродируют в воде, в которой растворен кислород тем активнее, чем отрицательней значение электрохимического потенциала.
Уходящие ионы металла, взаимодействуя с ионами , образуют гидроксиды, нерастворимые в воде, которые называют ржавчиной, а процесс их образования – ржавлением.
Схема ржавления железа:
;
Гидроксид железа в присутствии кислорода, растворенного в воде, превращается в . Так как это нерастворимое соединение, то равновесный потенциал не может быть достигнут и коррозия будет продолжаться до полного разрушения.
В зависимости от структуры коррозия имеет разное проявление: при однородном металле – коррозия происходит равномерно по всей поверхности. При неоднородном металле – коррозия избирательная и называется точечной. Это явление наиболее опасно, так как приводит к быстрой порче всего изделия. Избирательная коррозия создает очаги концентрации напряжений, что содействует разрушению.
Химическая коррозия может происходить за счет взаимодействия металла с газовой средой при отсутствии влаги. Продуктом коррозии являются оксиды металла. Образуется пленка на поверхности металла толщиной в 1…2 периода кристаллической решетки. Этот слой изолирует металл от кислорода и препятствует дальнейшему окислению, защищает от электрохимической коррозии в воде. При создании коррозионно-стойких сплавов – сплав должен иметь повышенное значение электрохимического потенциала и быть по возможности однофазным.
megaobuchalka.ru
Химическая и электрохимическая коррозия металлов
Презентация урока Химическая и электрохимическая коррозия металлов
Познавательная цель урока: дать учащимся понятие о коррозии металлов, её видах и способах защиты от коррозии. Показать химизм процесса.
Воспитательная цель урока: Показать отрицательное значение коррозии для промышленности, в частности автомобильной, указать на разрушающую роль коррозии и борьбу с ней.
Развивающая цель урока: оценить значение современных технологий изготовления легированных сплавов и других средств защиты от коррозии для современной автомобильной промышленности.
Тип урока: комбинированный.
Метод урока: рассказ, беседа, демонстрации, тестирование, самостоятельная работа, сообщения учащихся.
Актуализация знаний учащихся.
Тестирование.
Тест на тему: металлы. Физические и химические свойства металлов.
- Какой из ионов металлов по строению внешнего уровня будет похож на благородный газ?
а) Fe³+
б) Zn²+
в) Са²+
г) Li+
2. Какие из металлов легче взаимодействуют с водой?
а) Ag
б) Na
в) Zn
г) Cu
3. Расположите металлы по степени увеличения их химической активности.
а) Na
б) Fe
в) Ag
г) Cu
4. Какой из металлов имеет строение атома 1/8/2.
а) Al
б) Cu
в) Na
г) Mg
5. По какому принципу расположены металлы в ряду напряжения металлов.
а) по строению атома;
б) в порядке уменьшения химической активности;
в) в порядке увеличения химической активности;
г) в порядке увеличения атомных масс.
6. Какой из металлов в наибольшей степени обладает металлическим блеском?
а) Au
б) Cu
в) Al
г) Ag
Ответы:
- в, г
- б
- в, г, б, а
- в
- б
- г
За 6 правильных ответов – «5»
За 4 или5 ответов – «4»
За 3 ответа – «3»
За 1 или 2 ответа – «2»
Фронтальный опрос. (вопросы).
1. Где в периодической системе расположены металлы?
2. Какое количество электронов характерно для внешнего уровня металлов и о чем это говорит?
3. Перечислить, с какими веществами взаимодействуют металлы?
4. Перечислить, с какими неметаллами могут взаимодействовать металлы?
5. Написать на доске уравнение взаимодействия железа с кислородом и объяснить его.
6. Может ли оксид железа перейти в гидроксид Fe3. Как?
7. Написать уравнение реакции образования гидроксида железа 3.
Индивидуальный опрос.
1. Рассказать об электрохимическом ряде напряжений металлов.
Переход к изучению нового материала.
Мы повторили свойства металлов, а из жизненного опыта мы знаем, что металлы, приходя в соприкосновение с внешней средой, в той или иной мере, и с различной скоростью, подвергаются разрушению. Вот этим вопросом мы и займемся сегодня. Тема нашего урока «Химическая и электрохимическая коррозия металлов». Записываем тему.
Так что же такое коррозия? (Показ слайда №1)
Самопроизвольное разрушение металлических материалов, происходящее под химическим воздействием окружающей среды называют коррозией, (слайд №2) от латинского corrodere – разъедать. В основном этот процесс происходит под воздействием кислорода воздуха и воды. (Показ слайда №3)
Коррозия бывает двух видов – химическая (показ слайда №4) и электрохимическая. (показ слайда №5)
Химическая коррозия происходит под воздействием кислорода и воды. (показ слайда №6)
4Fe0+3O2 = 2Fe2O3
4Fe0+3O2+6h3O = 4Fe3+(OH)3↓
Электрохимическая коррозия (показ слайда №7) возникает в том случае, если во внешней среде находятся два соединенных друг с другом металла с различной химической активностью. (показ слайда №8).
Давайте рассмотрим, что же происходит с металлами при коррозии.
Если чистое железо имело степень окисления «0», то после коррозии степень окисления его становится «+3». О чем это говорит? Коррозия металлов это окислительно-восстановительный процесс, при котором атомы металлов окисляются. Окислителем выступает кислород О2, а также ионы водорода Н+, образующиеся при диссоциации воды.
При электрохимической коррозии между двумя металлами возникает гальванический элемент, (задается вопрос об аккумуляторе) в котором начинает окисляться более сильный и активный металл. Теперь рассмотрим результаты заложенных нами опытов. Выясняется, что есть вещества ускоряющие коррозию, например соль, или конкретно хлорид ионы Cl-. Есть вещества, замедляющие коррозию, например щелочь, вернее гидроксид ионы ОН-. При электрохимической коррозии разрушается более сильный металл, а у слабого коррозия замедляется или вовсе прекращается. В нашем случае корродирует железо, как более активный металл, чем медь. Но если соединить железо с цинком, то корродировать будет цинк, тем самым, защищая железо от разрушения.
Общая масса металлов, используемых в виде различных изделий в мировом хозяйстве, очень велика. Поэтому, несмотря на то, что скорость коррозии обычно мала, ежегодно из-за коррозии мировая потеря металла составляет 20 миллионов тонн. (показ слайда №9) Но еще большие убытки приносит не потеря металла, а порча изделий из него. Затраты на ремонт или замену деталей судов, автомобилей, приборов, аппаратуры химических производств во много раз превышают их стоимость. Существуют и косвенные потери: утечки нефти или газа из поврежденных коррозией трубопроводов, порчу продуктов питания, потерю здоровья, а иногда и жизни людей, и т.д. Поэтому на защиту от коррозии тратятся большие средства, ибо защита от коррозии – важнейшая проблема. Какие же меры и средства защиты от коррозии вы могли бы предложить? Предлагаются различные способы.
Резюме:
Для защиты от коррозии применяются:
1. Покрытие металлов красками, лаками, смазками, полимерными пленками. (показ слайда №10)
2. Механическая обработка: шлифовка, полировка.
3. Создание химически чистых металлов. (показ слайда №11)
4. Защитное покрытие одних металлов другими: хромирование, никелирование, анодирование. (показ слайда №12)
5. Оцинкование и лужение Fe, Cu.
6. Использование ингибиторов.
7. Создание сплавов (нержавеющая сталь).
8. Протекторная защита, когда возле труб находящихся в земле, располагаются куски активного металла, например Mg. С судов стоящих на рейде так же сбрасывают кусок магния, соединенным с днищем. (показ слайда №13)
Теперь давайте посмотрим, как обстоит дело с коррозией в автомобильной промышленности. Для этого двое учащихся подготовили сообщения. Зачитываются сообщения.
Закрепление.
- Что такое коррозия?
- О каких видах коррозии мы узнали?
- Как можно объяснить коррозию с точки зрения окисления – восстановления.
- Как влияет на коррозию окружающая среда.
- Как защитить металлы от коррозии?
Задание на дом.
Знаете ли вы что?
С того момента, как человек стал использовать железо в производстве транспортных средств и всевозможных металлоконструкций, коррозия, воздействие которой приводит к серьезным убыткам, начала привлекать внимание исследователей. Это произошло в 30-х годах 20 века, когда автомобильная промышленность развивалась весьма активно. Коррозия является достаточно сложным процессом. Но, даже не углубляясь в основы химии, можно понять его причины. С точки зрения обывателя, коррозия превращает железо в ржавчину. Этот процесс происходит в обязательном присутствии двух компонентов – воды и кислорода. Очевидно, что оба эти вещества в избытке находятся в атмосфере и полностью изолировать металл от их воздействия практически невозможно. Воду (вместе с растворенными в ней различными элементами) часто называют электролитом.На скорость протекания коррозии могут влиять и другие обстоятельства. К примеру, соль, а вернее, ионы хлора, равно как и примеси промышленных выбросов, является мощным ускорителем коррозии. А если учесть, что в зимний период дороги крупных городов нашей страны регулярно обрабатываются теми или иными реагентами на основе различных солей, то можно понять, почему в России так актуальна проблема антикоррозионной защиты автомобилей.Но не только присутствие тех или иных химических элементов влияет на скорость протекания коррозии. К примеру, она увеличивается при росте влажности или температуры, что накладывает ограничения на функционирование выхлопной системы, моторного отсека и плохо вентилируемых скрытых полостей.Коррозия автомобильного кузова имеет много специфических особенностей. Известно, что различные его участки корродируют с разной скоростью, т.к. при эксплуатации находятся в разных условиях. Одно из основных уязвимых мест — сварные швы, с помощью которых конструкция сохраняет свою форму. Именно там чаще всего и возникают очаги ржавчины. Дело в том, что в местах сварки всегда есть микротрещины, которые без труда заполняются влагой. В механизме щелевой коррозии важную роль играют вибрации автомобиля при езде, а также перепады температур в зимний период. В последнем случае влага, превращаясь в лед, увеличивает щель, т.к. в твердом состоянии занимает уже больший объем. Поэтому в следующий раз образовавшийся зазор заполнится большим количеством воды, которая, замерзнув, снова его увеличит. Такой, казалось бы, незатейливый циклический процесс, в конечном счете, приводит к серьезным последствиям. Следует также отметить, что коррозионная стойкость стали в местах швов существенно ниже из-за воздействия высокой температуры в момент сварки, как на саму сталь, так и на гальваническое покрытие в случае его наличия.Автомобильный кузов в силу своих конструктивных особенностей обладает большим количеством внутренних полостей. Мало того, что они скрыты от глаз автомобилиста (это часто приводит к позднему обнаружению ржавчины), так еще и плохо вентилируются. В результате там скапливается вода и прочие пагубные для металла вещества и образуется зона повышенной влажности. Так что коррозия в скрытых полостях протекает особенно быстро и, что самое опасное, незаметно.Еще одно уязвимое для коррозии место автомобильного кузова — поверхность днища. И это вполне очевидно, т.к. постоянное механическое воздействие щебня и песка вместе с водой и солью, в избытке летящих из-под колес, в состоянии «пробить» даже надежные защитные покрытия.Работа двигателя и выхлопной системы автомобиля также может спровоцировать появление ржавчины, т.к. функционирование данных узлов связано с существенным повышением температуры.Таким образом, современный автомобиль, обладая сложной конструкцией кузова, весьма сильно подвержен воздействию коррозии. Причем, с точки зрения защиты, разные его компоненты требуют индивидуального подхода, что заметно усложняет процедуру антикоррозионной обработки.
У владельцев многих иномарок существует мнение, что их автомобилям не нужна дополнительная антикоррозионная обработка, т.к. на конвейере уже обо всем позаботился производитель. А если данный автомобиль оснащен оцинкованным кузовом, то это мнение переходит в настоящую убежденность. Но, как оказывается, реальность несколько отличается от ожиданий. Но обо всем по порядку.Помимо оцинковки, набирающей популярность в развитых странах, для защиты от коррозии применяют различные методы грунтования. При производстве отечественных автомобилей чаще используется так называемый анафорезный метод. В развитом мире он уже давно устарел морально, т.к. демонстрировал низкие показатели антикоррозионной стойкости. Тем не менее, в нашей стране его применяют весьма активно.Катафорезный метод грунтования более эффективен. Но как показала реальная эксплуатация, без дополнительной антикоррозионной обработки подобные кузова также довольно быстро пасуют перед ржавчиной. Данный метод используется в России все активнее. К примеру, новые вазовские модели, а также многие иномарки обрабатываются именно таким образом.Наконец, наиболее действенный способ заводской борьбы с коррозией — оцинковка. В автомобильной промышленности принята толщина цинкового покрытия 6-9 мкм. На опытной пластине с такой толщиной гальванического цинка при ее размещении в станции натурных испытаний (напр. промышленной зоне большого города) первые признаки коррозии проявляются в среднем уже через 9-12 месяцев. Это объясняется наличием микропор в цинковом покрытии, через которые влага воздуха вместе со всеми примесями проникает до металла, и процесс прошел. Чем толще цинковое покрытие, тем меньше вероятность, что микропоры «совпадают», и тем надежнее защита. Каждый дополнительный мкм цинкового покрытия увеличивает вес автомобиля и тем самым расход топлива. Поэтому найден компромисс — 6-9 мкм цинкового покрытия, что значительно уменьшает коррозионную стойкость автомобиля и не столь уж увеличивает расход топлива. Действительно, оцинкованные кузова «живут» гораздо дольше. Но не так долго, как это принято думать. Срок их жизни, во-первых, зависит от толщины гальванического покрытия, типа (двустороннее или одностороннее), а главное – от наличия в процессе эксплуатации его повреждений. Последних избежать практически невозможно, т.к. они появляются во время точечной сварки, когда не только «сгорает» тонкий слой цинка, но и оголенная сталь образует в месте сварки гальванический элемент с цинком, тем самым, ускоряя начало коррозии. Поэтому даже оцинкованные кузова по прошествии нескольких лет эксплуатации страдают от коррозии в случае отсутствия дополнительной поддержки антикоррозионных материалов.
infourok.ru
Специфика протекания электрохимической коррозии металлоизделий
От латинского слова corrosio, означающего «разъедание», образовано всем известное понятие коррозии, означающим самопроизвольное разрушение материала при взаимодействии с контактирующей с ним средой. Влиянию коррозии подвержены не только металлы, но и полимеры (старение полимеров), керамика и даже деревянные материалы.
Контактирующая с веществами окружающая среда вносит свою специфику во взаимодействие с ними, по типу взаимодействия выделяют многочисленные разновидности процессов разрушения, включая электрохимическую коррозию металлоконструкций или химическую коррозию.
Реакции корродирования обусловлены возникновением окислительно-восстановительных реакций вещества с контактирующей с ним средой, необходимых для перехода вещества в наиболее устойчивое термодинамическое состояние.
Классификация процессов корродирования
Многообразие сред и условий протекания коррозионных процессов не позволяет создать всеобъемлющую и единую систему классификации встречающихся коррозий.
Основными критериями разделения коррозионных разновидностей в настоящее время являются:
- Степень агрессивности среды, в которой происходит процесс коррозионного разрушения;
- Условия протекания коррозионных реакций;
- Локальность коррозионных изменений, связанная с корродированием отдельных участков;
- Характер разрушений рабочей поверхности металлоконструкции;
- Механизм процесса корродирования, согласно которому принято выделять:
- химическую и
- электрохимическую коррозии.
Отличия химической коррозии от электрохимической
Коррозия химическая и электрохимическая принципиально отличаются друг от друга по виду взаимодействия вещества с контактирующей средой, длительности процесса и по конечному результату взаимодействия.
- Химическая коррозия происходит в обезвоженной среде, то есть при полном отсутствии влаги. Результатом коррозии химической для металлоконструкций являются образовавшиеся оксиды металлов. Оксиды создают пленку толщиной не более двух периодов кристаллической решетки, но этого оказывается достаточно, чтобы изолировать основной металл от кислорода контактирующей среды и воспрепятствовать дальнейшему окислению.
- Реакции электрохимической коррозии обязательно происходят в электролитной среде и относятся к анодно-катодным взаимодействиям. Это могут быть водные растворы, а также иная среда, содержащая влагу, например, обыкновенная атмосфера. Ионы металла поверхностного слоя материала, имеющие положительный заряд, отрываются молекулами воды, в результате основной металл обретает избыточное количество оставшихся электронов и заряжается отрицательно. Слой воды, граничащий с металлом, за счет приобретенных ионов, отданных металлом, заряжается положительно. Граничный слой воды с металлом приобретает скачок потенциала, обусловленный разностью зарядов. Примером электрохимических реакций корродирования являются разрушающие факторы для металлоконструкций, эксплуатируемых в воде или в сырой атмосфере, при воздействии охлаждающих эмульсий и жидкостей, используемых при мехобработке металлов, образование накипи при использовании магниевых анодов в электрических бойлерах.
Немного подробнее об электрохимическом корродировании металлоконструкций

Коррозия авто
Электрохимическая коррозия металлов – самый распространенный вид коррозионного разрушения, представляющий собой разрушение металлов в электролитных средах, с созданием в системе направленного движения электронов и ионов.
На поверхности и в граничном со средой слое металла одновременно происходят анодная и катодная реакции, в ходе которых происходят:
- Анодное окисление метала;
- Катодное восстановление водорода или кислорода.
Это важно! Не следует относить к электрохимической коррозии корродирование однородных материалов, например, всем известное ржавление железа. Для протекания электрохимических коррозионных разрушений всегда необходимо присутствие электролита. Ими могут оказаться дождевая вода, конденсат, с которыми происходит соприкосновение структурных элементов материала или двух различных контактирующих веществ, имеющих различные по величине окислительно-восстановительные потенциалы.
Основные методы защиты металлов от электрохимических коррозионных разрушений
Защита металлоконструкций базируется на целенаправленных воздействиях, частично снижающих или полностью предотвращающих активность факторов, провоцирующих развитие коррозионных процессов. Защитные мероприятия однозначно разделены на три категории:
- Воздействие на конструкционный материал, которое на практике чаще всего выражается нанесением защитных и изолирующих покрытий;
- Воздействие на контактирующую с металлоконструкцией среду, на практике это методы ингибирования воды или ее деаэрации;
- Комбинированные мероприятия.
 Наиболее доступные и широко применяемые из методов защиты:
Наиболее доступные и широко применяемые из методов защиты:
- Легирование металла, основанное на внедрении в сплав компонентов на основе вольфрама, хрома или никеля, провоцирующих образование устойчивых оксидных пленок, тем самым вызывающих пассивность конструкционного металла к коррозионному разрушению;
- Покрытия конструкционного металла;
- Электрохимическая защита от коррозии, базирующаяся на использовании торможения коррозионных реакций путем присоединения к защищаемой металлоконструкции элементов с более высоким значением отрицательного потенциала электрода;
- Подщелачивание коррозионной среды или ее деаэрация с целью снижения концентрации водородных ионов.
stroitel5.ru
Химическая и электрохимическая коррозия
Навигация:
Главная → Все категории → Горные работы для отчистки вод
Химическая и электрохимическая коррозия
Коррозия считается химической, если после разрыва металлической связи атомы металла непосредственно соединяются химической связью с теми атомами или группами атомов, которые входят в состав окислителей, отнимающих валентные электроны у металла. Химическая коррозия возможна в любой коррозионной среде, но чаще всего она наблюдается в случаях, когда среда не является электролитом. Скорость ее определяется, как правило, диффузией частиц металла, и окислителя через поверхностную пленку продуктов коррозии, иногда — растворением или испарением этой пленки, ее растрескиванием, изредка — конвективной доставкой окислителя из внешней среды.
Коррозия считается электрохимической, если при выходе из металлической решетки образующийся катион вступает в связь не с окислителем, а с другими компонентами коррозионной среды. Окислителю же передаются электроны, освобождающиеся при образовании катиона. Такой процесс возможен в тех случаях, когда в окружающей среде существуют два типа реагентов, из которых одни способны соединяться устойчивыми связями с катионом металла без участия его валентных электронов, а другие (окислители) могут присоединить валентные электроны металла, не удерживая около себя катионы.
При электрохимической коррозии удаление атома из металлической решетки (что составляет сущность любого коррозионного процесса) осуществляется в результате двух независимых, но сопряженных, связанных между собой электрическим балансом, электрохимических процессов: анодного (переход сольватируемых катионов металла в раствор) и катодного (связывание окислителем освобождающихся электронов). Следовательно, процесс электрохимической коррозии можно замедлить не только путем торможения анодного процесса, но и воздействия на скорость катодного.
Наиболее распространены два катодных процесса: разряд водородных ионов и восстановление растворенного кислорода. Их ча-cjo называют соответственно водородной и кислородной деполяризацией.
Анодный и катодный процессы с определенной вероятностью и в той или иной последовательности протекают в любых точках металлической поверхности, где катионы и электроны могут взаимодействовать с компонентами коррозионной среды. Если поверхность однородна, то катодные и анодные процессы равновероятны по всей ее площади. В таком идеальном случае коррозия называется гомогенно-електрохимичеекой, отмечая, таким образом, отсутствие какой-либо неоднородности в распределении вероятности электрохимических процессов в любой точке поверхности, что не исключает термодинамической гетерогенности взаимодействующих фаз.
В действительности на, металлических поверхностях существуют участки с различными условиями доставки реагирующих компонентов, с разным энергетическим состоянием атомов или с различными примесями. На таких участках возможно более энергичное протекание анодного или катодного процессов, и коррозия становится гетерогенно-электрохимической.
Проводимость металла очень высока, и при возникновении избыточного заряда электроны практически мгновенно перераспределяются, так что плотность заряда и электрический потенциал металла меняются одновременно по всей его поверхности независимо от того, в каких ее точках электроны освободились после ухода катионов, а в каких захватываются окислителем.
В частности это означает, что от мест, где преимущественно протекает анодная реакция, электроны перемещаются в металле к местам протекания катодной. Соответственно раствор вблизи анодных участков получает избыточный положительный заряд растворившихся катионов, а вблизи катодных заряжается отрицательно в результате захвата электронов растворенным окислителем.
В растворе эти заряды не перераспределяются так легко, как в металле. Поэтому с повышением скорости процесса потенциал раствора, находящегося в непосредственной близости от анодных участков, становится все более положительным, что затрудняет катодный процесс. Иначе это можно представить, как вызванное протеканием тока падение напряжения между прианодным и прика-тодным слоями раствора, с учетом которого потенциал металла по отношению к прианодному слою оказывается более отрицательным, а по отношению к прикатодному — более положительным, чем по отношению к объему раствора.
Когда такое падение напряжения велико, коррозионную систему удобнее представить в виде системы короткозамкнутых микро-или макрогальванических элементов. В остальных случаях при определении средней по площади- скорости растворения металла современная теория, наряду с вышеизложенной моделью, позволяет также представлять электрохимически гетерогенную поверхность как квазигомогенную. Тогда ей приписывают удельные анодные и катодные характеристики, равные интегрально усредненным ‘по площади значениям одноименных характеристик моделируемой на основе теории подобия гетерогенной поверхности. Графически их изображают на коррозионной диаграмме в виде анодных и катодных поляризационных кривых, которые отображают влияние электродного потенциала на усредненные по площади и выраженные в единицах плотности тока скорости выхода катионов и электронов с данной поверхности в данный электролит.
Похожие статьи:
Консервация металлических изделии
Навигация:
Главная → Все категории → Горные работы для отчистки вод
Статьи по теме:
Главная → Справочник → Статьи → Блог → Форум
stroy-spravka.ru

