Д1Ат свойства – 1Ҕ?
alexxlab | 20.05.2020 | 0 | Разное
Лист алюминиевый Д1АТ в Москве и Санкт-Петербурге по доступной цене
Алюминиевый лист Д1АТ по выгодной цене
Звоните и заказывайте!
+7 (499) 713-34-46 (Москва)
+7 (495) 798-73-38 (Владимир)
Алюминиевый лист Д1АТ (относится к дюралюминам) применяется тогда, когда важно максимально снизить вес конструкции, наделяя её определенной прочностью и жесткостью. Основными легирующими веществами становятся медь, магний и, в меньшей степени, марганец.
Механические свойства после термического упрочнения оказываются вполне сопоставимы с показателями низкоуглеродистых сталей. Литера «Т» в обозначении указывает на закалку и операцию естественного старения. Отжиг же качественно повышает пластичность и открывает новые возможности по формообразованию.
Сфера применения: авиационная и космическая промышленность, судостроение, машиностроение, изготовление железнодорожного транспорта. Зачастую находится место для применения дюралюминов в строительных и прочих сооружениях.
Цены на продукцию предоставляются по запросу. Отправьте нам заявку и мы вышлем Вам актуальные расценки на всю, интересующую Вас продукцию.
Ответим в течении 30 минут.
Характеристика и преимущества
Алюминиевый лист Д1АТ обладает всеми ключевыми преимуществами сплава на основе алюминия:
- Способность работать в условиях постоянного химического воздействия. У дюралюминия это выражено не так, как у чистого металла, но низкоуглеродистая сталь или оцинковка оказываются далеко позади. Кроме того, часто используется нанесение дополнительного покрытия из технического алюминия – на это указывает литера «А».
- Отсутствие проблем со всеми видами обработки: от механической резки до сварки. Особенное значение имеет пластичность, позволяющая придать сложную форму изделиям.
- Высокие показатели, как статической, так и усталостной прочности. Данный параметр является приоритетным и обуславливает выбор именно этой марки.
- Легкость. Вес отличается в разы от железных сплавов.
- Подверженность различным видам технологического воздействия на поверхность с целью оптимизации её свойств.
Д1АТ массово поставляется в виде именно листового проката. Это позволяет использовать его для изготовления корпусных высокопрочных конструкций.
mt-holding.ru
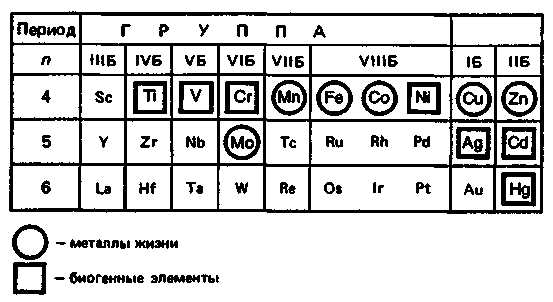
1. Общая характеристика d-элементов.
d–ЭЛЕМЕНТЫ И ИХ СОЕДИНЕНИЯ
 К
d-блоку
относятся 32 элемента периодической
системы. d-Элементы
входят в 4—7-й большие периоды. У атомов
IIIБ-группы
появляется первый электрон на d-орбитали.
В последующих Б-группах происходит
заполнение d-подуровня
до 10 электронов (отсюда название
К
d-блоку
относятся 32 элемента периодической
системы. d-Элементы
входят в 4—7-й большие периоды. У атомов
IIIБ-группы
появляется первый электрон на d-орбитали.
В последующих Б-группах происходит
заполнение d-подуровня
до 10 электронов (отсюда название
Особенностью элементов этих периодов является непропорционально медленное возрастание атомного радиуса с возрастанием числа электронов. Такое относительно медленное изменение радиусов объясняется так называемым лантаноидным сжатием вследствие проникновения ns-электронов под d-электронный слой. В результате наблюдается незначительное изменение атомных и химических свойств d-элементов с увеличением атомного номераю Сходство химических свойств проявляется в характерной особенности d-элементов образовывать комплексные соединения с разнообразными лигандами.
В ажным
свойствомd-элементов
является переменная валентность и,
соответственно, разнообразие степеней
окисления. Эта особенность связана
главным образом с незавершенностью
предвнешнего d-электронного
слоя (кроме элементов IБ-
и IIБ-групп).
Возможность существования d-элементов
в разных степенях окисления определяет
широкий диапазон окислительновосстановительных
свойств элементов. В низших степенях
окисления d-элементы
проявляют свойства металлов. С увеличением
атомного номера в группах Б металлические
свойства закономерно уменьшаются.
ажным
свойствомd-элементов
является переменная валентность и,
соответственно, разнообразие степеней
окисления. Эта особенность связана
главным образом с незавершенностью
предвнешнего d-электронного
слоя (кроме элементов IБ-
и IIБ-групп).
Возможность существования d-элементов
в разных степенях окисления определяет
широкий диапазон окислительновосстановительных
свойств элементов. В низших степенях
окисления d-элементы
проявляют свойства металлов. С увеличением
атомного номера в группах Б металлические
свойства закономерно уменьшаются.
В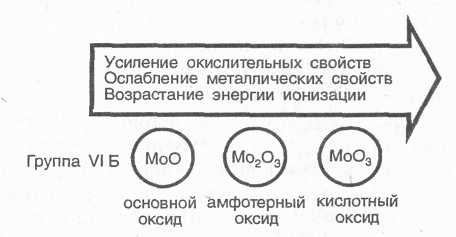 растворах кислородсодержащие анионыd-элементов
с высшей степенью окисления проявляют
кислотные и окислительные свойства.
Катионные формы низших степеней окисления
характеризуются основными и
восстановительными свойствами.
растворах кислородсодержащие анионыd-элементов
с высшей степенью окисления проявляют
кислотные и окислительные свойства.
Катионные формы низших степеней окисления
характеризуются основными и
восстановительными свойствами.
d-Элементы в промежуточной степени окисления проявляют амфотерные свойства. Эти закономерности можно рассмотреть на примере соединений молибдена:
С изменением свойств меняется окраска комплексов молибдена в различных степенях окисления (VI — II):
VI V IV III
[МоО3Сl2]2- [МоОСl5]2- [МоО2Сl4]4- [МоСl6]3-
бесцветный зеленый коричневый красный
В периоде с увеличением заряда ядра наблюдается уменьшение устойчивости соединений элементов в высших степенях окисления. Параллельно возрастают окислительно-восстановительные потенциалы этих соединений. Наибольшая окислительная способность наблюдается у феррат-ионов и перманганат-ионов. Следует отметить, что у d-элементов при нарастании относительной электроотрицательности усиливаются кислотные и неметаллические свойства.
С увеличением устойчивости соединений при движении сверху вниз в Б-группах одновременно уменьшаются их окислительные свойства.
Можно предположить, что в ходе биологической эволюции отбирались соединения элементов в промежуточных степенях окисления, которые характеризуются мягкими окислительно-восстановительными свойствами. Преимущества такого отбора очевидны: они способствуют плавному протеканию биохимических реакций. Уменьшение ОВ потенциала создает предпосылки для более тонкой «регулировки» биологических процессов, что обеспечивает выигрыш энергии. Функционирование организма становится менее энергоемким, а значит более экономичным по потреблению пищевых продуктов.
С точки зрения эволюции для организма становится оправданным существование d-элементов в низших степенях окисления. Известно, что ионы Мn2+, Fе2+ , Со2+ при физиологических условиях не являются сильными восстановителями, а ионы Сu2+ и Fе2+ практически не проявляют в организме восстановительных свойств. Дополнительное снижение реакционной способности происходит при взаимодействии этих ионов с биоорганическими лигандами.
Может показаться, что вышесказанному противоречит важная роль биоорганических комплексов молибдена(V) и (VI) в различных организмах. Однако и это согласуется с общей закономерностью. Несмотря на высшую степень окисления такие соединения проявляют слабые окислительные свойства.
Необходимо отметить высокие комплексообразующие способности d-элементов, которые обычно значительно выше, чем у s- и p-элементов. Это прежде всего объясняется возможностями d-элементов быть как донорами, так и акцепторами пары электронов, образующих координационное соединение.
В случае гидроксокомплекса хрома [Сr(ОН)6]3- ион металла является акцептором пары электронов. Гибридизация 3d24sp3-орбиталей хрома обеспечивает более устойчивое энергетическое состояние, чем при расположении электронов хрома на орбиталях гидроксогрупп.
Соединение [СrСl4]2- образуется, наоборот, в результате того, что неподеленные d-электроны металла занимают свободные d-орбитали лигандов, поскольку в данном случае энергия этих орбиталей ниже.
Свойства катиона Сr3+ показывают непостоянство координационных чисел d-элементов. Чаще всего, это четные числа от 4 до 8, реже встречаются числа 10 и 12. Необходимо отметить, что существуют не только одноядерные комплексы. Известны многочисленные ди-, три- и тетра-ядерные координационные соединения d-элементов.
Примером может служить биядерный комплекс кобальта [Со2(NН3)10(О2)](NО3)5, который может служить моделью переносчика кислорода.
Более 1/3 всех микроэлементов организма составляют d-элементы. В организмах они существуют в виде комплексных соединений или гидратированных ионов со среднем временем обмена гидратной оболочки от 10-1 до 10-10 с. Поэтому можно утверждать, что «свободные» ионы металлов в организме не существуют: это либо их гидраты, либо продукты гидролиза.
В биохимических реакциях d-элементы наиболее часто проявляют себя как металлы-комплексообразователи. Лигандами при этом выступают биологически активные вещества, как правило, органического характера или анионы неорганических кислот.
Б елковые
молекулы образуют сd-элементами
бионеорганические комплексы — кластеры
или биокластеры. Ион металла
(металл-комплексо-образователь)
располагается внутри полости кластера,
взаимодействуя с электроотрицательными
атомами связывающих групп белка:
гидроксильных (—ОН), сульфгидрильных
(—SН),
карбоксильных (—СООН) и аминогрупп
белков (Н2N–).
Для проникновения иона металла в полость
кластера необходимо, чтобы диаметр иона
был соизмерим с размером полости. Таким
образом, природа регулирует формирование
биокластеров с ионами d-элементов
определенных размеров.
елковые
молекулы образуют сd-элементами
бионеорганические комплексы — кластеры
или биокластеры. Ион металла
(металл-комплексо-образователь)
располагается внутри полости кластера,
взаимодействуя с электроотрицательными
атомами связывающих групп белка:
гидроксильных (—ОН), сульфгидрильных
(—SН),
карбоксильных (—СООН) и аминогрупп
белков (Н2N–).
Для проникновения иона металла в полость
кластера необходимо, чтобы диаметр иона
был соизмерим с размером полости. Таким
образом, природа регулирует формирование
биокластеров с ионами d-элементов
определенных размеров.
Наиболее известные металлоферменты: карбоангидраза, ксантиноксидаза, сукцинатдегидрогеназа, цитохромы, рубредоксин. Они представляют собой биокластеры, полости которых образуют центры связывания субстратов с ионами металла.
Биокластеры (белковые комплексы) выполняют различные функции.
Транспортные белковые комплексы доставляют к органам кислород и необходимые элементы. Координация металла идет через кислород карбоксильных групп и азот аминогрупп белка. При этом образуется устойчивое хелатное соединение.
Вкачестве координирующего металла выступаютd-элементы (кобальт, никель, железо). Пример железосодержащего транспортного белкового комплекса — трансферрин.
Другие биокластеры могут выполнять аккумуляторную (накопительную) роль — это железосодержащие белки: гемоглобин, миоглобин, ферритин. Они будут рассмотрены при описании свойства группы VIIIБ.
Элементы Zn, Fе, Со, Мо, Сu — жизненно необходимы, входят в состав металлоферментов. Они катализируют реакции, которые можно разделить на три группы:
Кислотно-основные взаимодействия. Участвует ион цинка, входящий в состав фермента карбоангидразы, катализирующего обратимую гидратацию СО2 в биосистемах.
Окислительно-восстановительные взаимодействия. Участвуют ионы Fе, Со, Сr, Мо. Железо входит в состав цито-хрома, в ходе процесса происходит перенос электрона:
Fе3+ → Fе2+ + е–
3. Перенос кислорода. Участвуют Fе, Сu. Железо входит в состав гемоглобина, медь — в состав гемоцианина. Предполагается, что эти элементы связываются с кислородом, но не окисляются им.
Соединения d-элементов избирательно поглощают свет с разными длинами волн. Это приводит к появлению окраски. Квантовая теория объясняет избирательность поглощения расщеплением d-подуровней ионов металлов под действием поля лигандов.
Хорошо известны следующие цветные реакции на d-элементы:
Мn2+ + S2- = МnS↓ (осадок телесного цвета)
Нg2+ + 2I– = НgI2 ↓(желтый или красный осадок)
К2Сr2О7 + Н2SО4 (конц.) = К2SО4 + Н2О + 2СrО3↓
(кристаллы оранжевого цвета)
Приведенные выше реакции используются в аналитической химии для качественного определения соответствующих ионов. Уравнение реакции с дихроматом показывает, что происходит при приготовлении «хромовой смеси» для мытья химической посуды. Эта смесь необходима для удаления как неорганических, так и органических отложений с поверхности химических склянок. Например, жировых загрязнений, которые всегда остаются на стекле после прикосновения пальцев.
Необходимо обратить внимание на то, что d-элементы в организме обеспечивают запуск большинства биохимических процессов, обеспечивающих нормальную жизнедеятельность.
studfiles.net
цена, характеристики, отзывы — spb.metalloprokat.ru
Лист дюралюминиевый плоский алюминиевый прокат. Листовой алюминий один из самых востребованных материалов в настоящее время.
Преимущества листов из алюминиевых сплавов:
малый вес;
устойчивость к любым неблагоприятным факторам, в том числе коррозии;
легкость обработки.
Лист дюралюминиевый 3 мм Д1АТ в наличии на складах в Екатеринбурге и Тюмени, осуществляем доставку.
Лист дюралюминиевый используется:
в производстве оконных и дверных блоков, перекрытий, каркасов;
в отделке фасадов зданий, витражей, в строительстве кровель и полов, ступеней;
незаменимый материал для сооружений, которые стоят рядом морем. Ведь алюминий не подвергается воздействию ультрафиолетовых лучей или перепадов температуры, дождей и морских бризов, для чего его можно и не обрабатывать.
Основные сферы применения дюралюминиевых листов:
машиностроение всех направлений;
фармацевтика;
пищевая отрасль;
химическая промышленность и ее отрасли;
строительство;
коммунальное хозяйство;
оформительское дело;
производство посуды.
Актуальную цену Вы можете уточнить у нашего менеджера.
Сплав Д1АТ (1110) – алюминиевый деформируемый сплав. Т на конце марки означает закаленный и естественно состаренный.
Применение сплава Д1АТ: для производства лопастей винтов, узлов креплений, строительных конструкций; профилей с площадью сечения до 200 см2 и диаметром описанной окружности до 350 мм, которые предназначены для использования в авиационной промышленности и специальных отраслях машиностроения; круглых тянутых и катаных труб для трубопроводов валов трансмиссий и тяг управления самолетов; прессованных крупногабаритных труб; специальных профилей методом холодного выдавливания и прессованием с последующим волочением.
Технологические свойства сплава Д1АТ:
Удельный вес: 2700 кг/м3;
Твердость материала: HB 10 -1 = 95 МПа;
Закалка дуралюмина Д1АТ: проводится при 495-510 С (все виды полуфабрикатов), старение при 20 С более 96 часов.
В своем химическом составе сплав Д1АТ содержит: Fe до 0,7; Si до 0,7; Mn 0,4 – 0,8; Ni до 0,1; Ti до 0,1; Al 91,6 – 95,4; Cu 3,8 – 4,8; Mg 0,4 – 0,8; Zn до 0,3.
Актуальную цену Вам подскажет наш менеджер.
Купить Лист 3 Д1АТ легко:
1. Вы отправляете заявку
2. Мы выставляем вам счет
3. Вы оплачиваете удобным для вас способом
4. Получаете свой товар
Что необходимо знать о компании Кин-Мет.
Поставляемый металлопрокат постоянно имеется в наличии, и хранится на складе порядка 2000 тонн.
Собственное производство профнастила.
Мы предлагаем отсрочку платежа до месяца.
Мы делаем все возможное для минимизации сроков обработки и доставки.
Осуществляем резку металла в размер и по вашим чертежам.
Предоставляем услугу ответственного хранения на крытом складе.
Мы предлагаем программу лояльности, позволяющую получать скидки на закупку, обработку или доставку металлопроката.
Преимущества работы с нами:
1. Товар в наличии на складе
2. Официальная гарантия
3. Высокое качество товаров
4. Оперативная доставка
5. Программа лояльности
Актуальную цену на Лист 3 сплав Д1АТ дюралюминиевый Вам подскажет наш менеджер.
Окончательная цена на продукцию формируется, исходя из условий поставки: кол-ва, условий оплаты и места отгрузки. Спросите у менеджера.
Данный прайс-лист носит исключительно информационный характер и ни при каких условиях не является публичной офертой, определяемой положениями ч. 2 ст. 437 Гражданского кодекса Российской Федерации.
spb.metalloprokat.ru
2. Антитела. Свойства антител – Вопрос 29. Антигены и антитела – Медицинская микробиология – Лекции 3 курс – Medkurs.ru
Антителами называются сывороточные белки, образующиеся в ответ на действие антигена. Они относятся к сывороточным глобулинам, поэтому называются иммуноглобулины (Ig). Через них реализуется гуморальный тип иммунного ответа.
Антитела обладают двумя свойствами:
специфичность, т. е. способность вступать во взаимодействие с антигеном, аналогичным тому, который индуцировал (вызвал) их образование;
гетерогенность по физико-химическому строению, по специфичности, по генетической детерминированности образования (по происхождению).
Все иммуноглобулины являются иммунными, т. е. образуются в результате иммунизации, контакта с антигенами. Тем не менее по происхождению они делятся на:
нормальные (анамнестические) антитела, которые обнаруживаются в любом организме как результат бытовой иммунизации;
инфекционные антитела, которые накапливаются в организме в период инфекционной болезни;
постинфекционные антитела, которые обнаруживаются в организме после перенесенного инфекционного заболевания;
поствакцинальные антитела, которые возникают после искусственной иммунизации.
Антитела (иммуноглобулины) всегда специфичны антигену, индуцировавшему их образование. Тем не менее противомикробные иммуноглобулины по специфичности делятся на те же группы, что и соответствующие микробные антигены:
группоспецифические;
видоспецифические;
вариантспецифические;
перекрестнореагирующие.
В настоящее время довольно часто методами биотехнологии и/или генной инженерии получают иммуноглобулины, продуцируемые одним клоном клеток. Они называются моноклональными антителами. Их продуценты — клетки-гибридомы, являющиеся потомками, полученными при скрещивании В-лимфоцита (плазматической клетки) с опухолевой клеткой. От плазматической клетки гибридома наследует способность к синтезу антител, а от опухолевой клетки — способность длительно культивироваться вне организма.
Помимо специфичности одним из основных свойств иммуноглобулинов является их гетерогенность, т. е. неоднородность популяции иммуноглобулинов по генетической детерминированности их образования и по физико-химическому строению.
Далее по теме:
www.medkurs.ru
A, B, C и D

Автоматическими выключателями называются приборы, отвечающие за защиту электроцепи от повреждений, связанных с воздействием на нее тока большой величины. Слишком сильный поток электронов способен вывести из строя бытовую технику, а также вызвать перегрев кабеля с последующим оплавлением и возгоранием изоляции. Если вовремя не обесточить линию, это может привести к пожару, Поэтому, в соответствии с требованиями ПУЭ (Правила устройства электроустановок), эксплуатация сети, в которой не установлены электрические автоматы защиты, запрещена. АВ обладают несколькими параметрами, один из которых – время токовая характеристика автоматического защитного выключателя. В этой статье мы расскажем, чем различаются автоматические выключатели категории A, B, C, D и для защиты каких сетей они используются.
Особенности работы автоматов защиты сети
К какому бы классу ни относился автоматический выключатель, его главная задача всегда одна – быстро определить появление чрезмерного тока, и обесточить сеть раньше, чем будет поврежден кабель и подключенные к линии устройства.

Токи, которые могут представлять опасность для сети, подразделяются на два вида:
- Токи перегрузки. Их появление чаще всего происходит из-за включения в сеть приборов, суммарная мощность которых превышает ту, что линия способна выдержать. Другая причина перегрузки – неисправность одного или нескольких устройств.
- Сверхтоки, вызванные КЗ. Короткое замыкание происходит при соединении между собой фазного и нейтрального проводников. В нормальном состоянии они подключены к нагрузке по отдельности.
Устройство и принцип работы автоматического выключателя – на видео:
Токи перегрузки
Величина их чаще всего незначительно превышает номинал автомата, поэтому прохождение такого электротока по цепи, если оно не затянулось слишком надолго, не вызывает повреждения линии. В связи с этим мгновенного обесточивания в таком случае не требуется, к тому же нередко величина потока электронов быстро приходит в норму. Каждый АВ рассчитан на определенное превышение силы электротока, при котором он срабатывает.
Время срабатывания защитного автоматического выключателя зависит от величины перегрузки: при небольшом превышении нормы оно может занять час и более, а при значительном – несколько секунд.
За отключение питания под воздействием мощной нагрузки отвечает тепловой расцепитель, основой которого является биметаллическая пластина.

Этот элемент нагревается под воздействием мощного тока, становится пластичным, изгибается и вызывает срабатывание автомата.
Токи короткого замыкания
Поток электронов, вызванный КЗ, значительно превосходит номинал устройства защиты, в результате чего последнее немедленно срабатывает, отключая питание. За обнаружение КЗ и немедленную реакцию аппарата отвечает электромагнитный расцепитель, представляющий собой соленоид с сердечником. Последний под воздействием сверхтока мгновенно воздействует на отключатель, вызывая его срабатывание. Этот процесс занимает доли секунды.
Однако существует один нюанс. Иногда ток перегрузки может также быть очень большим, но при этом не вызванным КЗ. Как же аппарат должен определить различие между ними?
На видео про селективность автоматических выключателей:
Здесь мы плавно переходим к основному вопросу, которому посвящен наш материал. Существует, как мы уже говорили, несколько классов АВ, различающихся по времятоковой характеристике. Наиболее распространенными из них, которые применяются в бытовых электросетях, являются устройства классов B, C и D. Автоматические выключатели, относящиеся к категории A, встречаются значительно реже. Они наиболее чувствительны и используются для защиты высокоточных аппаратов.
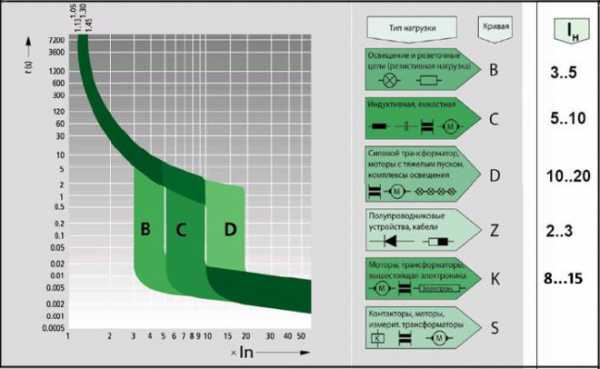
Между собой эти устройства различаются по току мгновенного расцепления. Его величина определяется кратностью тока, проходящего по цепи, к номиналу автомата.
Характеристики срабатывания защитных автоматических выключателей
Класс АВ, определяющийся этим параметром, обозначается латинским литером и проставляется на корпусной части автомата перед цифрой, соответствующей номинальному току.
В соответствии с классификацией, установленной ПУЭ, защитные автоматы подразделяются на несколько категорий.
Автоматы типа МА
Отличительная черта таких устройств – отсутствие в них теплового расцепителя. Аппараты этого класса устанавливают в цепях подключения электрических моторов и других мощных агрегатов.
Защиту от перегрузок в таких линиях обеспечивает реле максимального тока, автоматический выключатель только предохраняет сеть от повреждений в результате воздействия сверхтоков короткого замыкания.
Приборы класса А
Автоматы типа А, как было сказано, обладают самой высокой чувствительностью. Тепловой расцепитель в устройствах с времятоковой характеристикой А чаще всего срабатывает при превышении силой тока номинала АВ на 30%.

Катушка электромагнитного расцепления обесточивает сеть в течение примерно 0,05 сек, если электроток в цепи превышает номинальный на 100%. Если по какой-либо причине после увеличения силы потока электронов в два раза электромагнитный соленоид не сработал, биметаллический расцепитель отключает питание в течение 20 – 30 сек.
Автоматы, имеющие времятоковую характеристику А, включаются в линии, при работе которых недопустимы даже кратковременные перегрузки. К таковым относятся цепи с включенными в них полупроводниковыми элементами.
Защитные устройства класса B
Аппараты категории B обладают меньшей чувствительностью, чем относящиеся к типу A. Электромагнитный расцепитель в них срабатывает при превышении номинального тока на 200%, а время на срабатывание составляет 0,015 сек. Срабатывание биметаллической пластины в размыкателе с характеристикой B при аналогичном превышении номинала АВ занимает 4-5 сек.
Оборудование этого типа предназначено для установки в линиях, в которые включены розетки, приборы освещения и в других цепях, где пусковое повышение электротока отсутствует либо имеет минимальное значение.

Автоматы категории C
Устройства типа C наиболее распространены в бытовых сетях. Их перегрузочная способность еще выше, чем у ранее описанных. Для того, чтобы произошло срабатывание соленоида электромагнитного расцепления, установленного в таком приборе, нужно, чтобы проходящий через него поток электронов превысил номинальную величину в 5 раз. Срабатывание теплового расцепителя при пятикратном превышении номинала аппарата защиты происходит через 1,5 сек.
Установка автоматических выключателей с времятоковой характеристикой C, как мы и говорили, обычно производится в бытовых сетях. Они отлично справляются с ролью вводных устройств для защиты общей сети, в то время как для отдельных веток, к которым подключены группы розеток и осветительные приборы, хорошо подходят аппараты категории B.
Это позволит соблюсти селективность защитных автоматов (избирательность), и при КЗ в одной из веток не будет происходить обесточивания всего дома.
Автоматические выключатели категории Д
Эти устройства имеют наиболее высокую перегрузочную способность. Для срабатывания электромагнитной катушки, установленной в аппарате такого типа, нужно, чтобы номинал по электротоку защитного автомата был превышен как минимум в 10 раз.

Срабатывание теплового расцепителя в этом случае происходит через 0,4 сек.
Устройства с характеристикой D наиболее часто используются в общих сетях зданий и сооружений, где они играют подстраховочную роль. Их срабатывание происходит в том случае, если не произошло своевременного отключения электроэнергии автоматами защиты цепи в отдельных помещениях. Также их устанавливают в цепях с большой величиной пусковых токов, к которым подключены, например, электромоторы.
Защитные устройства категории K и Z
Автоматы этих типов распространены гораздо меньше, чем те, о которых было рассказано выше. Приборы типа K имеют большой разброс в величинах тока, необходимых для электромагнитного расцепления. Так, для цепи переменного тока этот показатель должен превышать номинальный в 12 раз, а для постоянного – в 18. Срабатывание электромагнитного соленоида происходит не более чем через 0,02 сек. Срабатывание теплового расцепителя в таком оборудовании может произойти при превышении величины номинального тока всего на 5%.
Этими особенностями обусловлено применение устройств типа K в цепях с исключительно индуктивной нагрузкой.
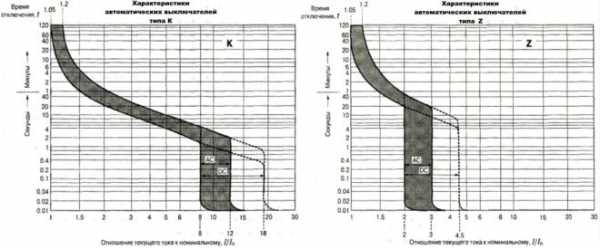
Приборы типа Z тоже имеют разные токи срабатывания соленоида электромагнитного расцепления, но разброс при этом не столь велик, как в АВ категории K. В цепях переменного тока для их отключения превышение токового номинала должно быть трехкратным, а в сетях постоянного – величина электротока должна быть в 4,5 раза больше номинальной.
Аппараты с характеристикой Z используются только в линиях, к которым подключены электронные устройства.
Наглядно про категории автоматов на видео:
Заключение
В этой статье мы рассмотрели время токовые характеристики защитных автоматов, классификацию этих устройств в соответствии с ПУЭ, а также разобрались, в каких цепях устанавливаются приборы различных категорий. Полученная информация поможет вам определить, какое защитное оборудование следует использовать в сети, исходя из того, какие устройства к ней подключены.
yaelectrik.ru
D-элементы и их соединения
1. Общая характеристика d-элементов
К d-блоку относятся 32 элемента периодической системы. d-Элементы входят в 4–7-й большие периоды. У атомов IIIБ-группы появляется первый электрон на d-орбитали. В последующих Б-группах происходит заполнение d-подуровня до 10 электронов (отсюда название d-элементы). Строение внешних электронных оболочек атомов d-блока описывается общей формулой (n-1)dansb, где а = 1–10, b = 1–2.
Особенностью элементов этих периодов является непропорционально медленное возрастание атомного радиуса с возрастанием числа электронов. Такое относительно медленное изменение радиусов объясняется так называемым лантаноидным сжатием вследствие проникновения ns-электронов под d-электронный слой. В результате наблюдается незначительное изменение атомных и химических свойств d-элементов с увеличением атомного номера. Сходство химических свойств проявляется в характерной особенности d-элементов образовывать комплексные соединения с разнообразными лигандами.
Важным свойством d-элементов является переменная валентность и, соответственно, разнообразие степеней окисления. Эта особенность связана главным образом с незавершенностью предвнешнего d-электронного слоя (кроме элементов IБ- и IIБ-групп). Возможность существования d-элементов в разных степенях окисления определяет широкий диапазон окислительно-восстановительных свойств элементов. В низших степенях окисления d-элементы проявляют свойства металлов. С увеличением атомного номера в группах Б металлические свойства закономерно уменьшаются.
В растворах кислородсодержащие анионы d-элементов с высшей степенью окисления проявляют кислотные и окислительные свойства. Катионные формы низших степеней окисления характеризуются основными и восстановительными свойствами.
d-элементы в промежуточной степени окисления проявляют амфотерные свойства. Эти закономерности можно рассмотреть на примере соединений молибдена:
С изменением свойств меняется окраска комплексов молибдена в различных степенях окисления (VI — II):
В периоде с увеличением заряда ядра наблюдается уменьшение устойчивости соединений элементов в высших степенях окисления. Параллельно возрастают окислительно-восстановительные потенциалы этих соединений. Наибольшая окислительная способность наблюдается у феррат-ионов и перманганат-ионов. Следует отметить, что у d-элементов при нарастании относительной электроотрицательности усиливаются кислотные и неметаллические свойства.
С увеличением устойчивости соединений при движении сверху вниз в Б-группах одновременно уменьшаются их окислительные свойства.
Можно предположить, что в ходе биологической эволюции отбирались соединения элементов в промежуточных степенях окисления, которые характеризуются мягкими окислительно-восстановительными свойствами. Преимущества такого отбора очевидны: они способствуют плавному протеканию биохимических реакций. Уменьшение ОВ потенциала создает предпосылки для более тонкой «регулировки» биологических процессов, что обеспечивает выигрыш энергии. Функционирование организма становится менее энергоемким, а значит более экономичным по потреблению пищевых продуктов.
С точки зрения эволюции для организма становится оправданным существование d-элементов в низших степенях окисления. Известно, что ионы Мn2+, Fе2+ , Со2+ при физиологических условиях не являются сильными восстановителями, а ионы Сu2+ и Fе2+ практически не проявляют в организме восстановительных свойств. Дополнительное снижение реакционной способности происходит при взаимодействии этих ионов с биоорганическими лигандами.
Может показаться, что вышесказанному противоречит важная роль биоорганических комплексов молибдена(V) и (VI) в различных организмах. Однако и это согласуется с общей закономерностью. Несмотря на высшую степень окисления такие соединения проявляют слабые окислительные свойства.
Необходимо отметить высокие комплексообразующие способности d-элементов, которые обычно значительно выше, чем у s- и p-элементов. Это прежде всего объясняется возможностями d-элементов быть как донорами, так и акцепторами пары электронов, образующих координационное соединение.
В случае гидроксокомплекса хрома [Сr(ОН)6]3- ион металла является акцептором пары электронов. Гибридизация 3d24sp3-орбиталей хрома обеспечивает более устойчивое энергетическое состояние, чем при расположении электронов хрома на орбиталях гидроксогрупп.
Соединение [СrСl4]2- образуется, наоборот, в результате того, что неподеленные d-электроны металла занимают свободные d-орбитали лигандов, поскольку в данном случае энергия этих орбиталей ниже.
Свойства катиона Сr3+ показывают непостоянство координационных чисел d-элементов. Чаще всего, это четные числа от 4 до 8, реже встречаются числа 10 и 12. Необходимо отметить, что существуют не только одноядерные комплексы. Известны многочисленные ди-, три- и тетра-ядерные координационные соединения d-элементов.
Примером может служить биядерный комплекс кобальта [Со2(NН3)10(О2)](NО3)5, который может служить моделью переносчика кислорода.
Более 1/3 всех микроэлементов организма составляют d-элементы. В организмах они существуют в виде комплексных соединений или гидратированных ионов со среднем временем обмена гидратной оболочки от 10-1 до 10-10 с. Поэтому можно утверждать, что «свободные» ионы металлов в организме не существуют: это либо их гидраты, либо продукты гидролиза.
В биохимических реакциях d-элементы наиболее часто проявляют себя как металлы-комплексообразователи. Лигандами при этом выступают биологически активные вещества, как правило, органического характера или анионы неорганических кислот.
Белковые молекулы образуют с d-элементами бионеорганические комплексы — кластеры или биокластеры. Ион металла (металл-комплексо-образователь) располагается внутри полости кластера, взаимодействуя с электроотрицательными атомами связывающих групп белка: гидроксильных (–ОН), сульфгидрильных (–SН), карбоксильных (–СООН) и аминогрупп белков (Н2N–). Для проникновения иона металла в полость кластера необходимо, чтобы диаметр иона был соизмерим с размером полости. Таким образом, природа регулирует формирование биокластеров с ионами d-элементов определенных размеров.
Наиболее известные металлоферменты: карбоангидраза, ксантиноксидаза, сукцинатдегидрогеназа, цитохромы, рубредоксин. Они представляют собой биокластеры, полости которых образуют центры связывания субстратов с ионами металла.
Биокластеры (белковые комплексы) выполняют различные функции.
Транспортные белковые комплексы доставляют к органам кислород и необходимые элементы. Координация металла идет через кислород карбоксильных групп и азот аминогрупп белка. При этом образуется устойчивое хелатное соединение.
В качестве координирующего металла выступают d-элементы (кобальт, никель, железо). Пример железосодержащего транспортного белкового комплекса — трансферрин.
Другие биокластеры могут выполнять аккумуляторную (накопительную) роль — это железосодержащие белки: гемоглобин, миоглобин, ферритин. Они будут рассмотрены при описании свойства группы VIIIБ.
Элементы Zn, Fе, Со, Мо, Сu — жизненно необходимы, входят в состав металлоферментов. Они катализируют реакции, которые можно разделить на три группы:
Кислотно-основные взаимодействия. Участвует ион цинка, входящий в состав фермента карбоангидразы, катализирующего обратимую гидратацию СО2 в биосистемах.
Окислительно-восстановительные взаимодействия. Участвуют ионы Fе, Со, Сr, Мо. Железо входит в состав цито-хрома, в ходе процесса происходит перенос электрона:
Fе3+ > Fе2+ + е–
3. Перенос кислорода. Участвуют Fе, Сu. Железо входит в состав гемоглобина, медь — в состав гемоцианина. Предполагается, что эти элементы связываются с кислородом, но не окисляются им.
Соединения d-элементов избирательно поглощают свет с разными длинами волн. Это приводит к появлению окраски. Квантовая теория объясняет избирательность поглощения расщеплением d-подуровней ионов металлов под действием поля лигандов.
Хорошо известны следующие цветные реакции на d-элементы:
Мn2+ + S2- = МnSv (осадок телесного цвета)
Нg2+ + 2I– = НgI2 v(желтый или красный осадок)
К2Сr2О7 + Н2SО4 (конц.) = К2SО4 + Н2О + 2СrО3v
(кристаллы оранжевого цвета)
Приведенные выше реакции используются в аналитической химии для качественного определения соответствующих ионов. Уравнение реакции с дихроматом показывает, что происходит при приготовлении «хромовой смеси» для мытья химической посуды. Эта смесь необходима для удаления как неорганических, так и органических отложений с поверхности химических склянок. Например, жировых загрязнений, которые всегда остаются на стекле после прикосновения пальцев.
Необходимо обратить внимание на то, что d-элементы в организме обеспечивают запуск большинства биохимических процессов, обеспечивающих нормальную жизнедеятельность.
studfiles.net
1.Физико-химические свойства антител.
Антитела – белки, относящиеся к иммуноглобулинам, которые синтезируются лимфоидными и плазматическими клетками в ответ на попадание в организм антигена, обладающими способностью специфически связываться с ним. Антитела составляют более 30% белков сыворотки крови, обеспечивают специфичность гуморального иммунитета благодаря способности связываться только с тем антигеном, который стимулировал их синтез. По своей природе антитела относятся к иммуноглобулинам (Ig) с разными физико-химическими и биологическим свойствами. В зависимости от них различают иммуноглобулины классов IgM, IgG, IgA, IgЕ, IgD. У сельскохозяйственных животных обнаружены только IgM, IgG, IgA.
Свойства антител зависят от структуры. Первые данные о ней получены Портером (Porter, 1959) и Эдельманом (Еdеlmаn, 1962) при изучении воздействия фермента папаина, меркаптоэтанола и мочевины на гетерогенные иммуноглобулины кролика. Было установлено, что папаин делит молекулы антител на 3 фрагмента, два из которых идентичны друг другу и способны связывать атигены, 3-ий фрагмент легко кристаллизовался и не обладал антительной активностью. Два первых фрагмента получили обозначение Fаb (англ. Fragment antigen binding,т. е. фрагмент, связывающий антиген), 3-ий обозначили как Fc (англ. Frаgmеnt crystalline, т.е. фрагмент кристаллический).
При фракционировании иммуноглобулинов после воздействия меркаптоэтанола и мочевины были получены полипептидные цепи молекулярной массой 55-77 кДа, которые стали называть тяжелыми (Н-цепи, англ. heavy – тяжелый) и легкие полипептидные цепи молекулярной массой 20-25 кДа (L-цепи, light – легкий). Антительной активностью обе разновидности цепей не обладали.
Характерным свойством иммуноглобулинов является их специфичность, т.е. они взаимодействуют только с теми антигенами, которые индуцировали их образование. Специфичность данной реакции обусловлена N- концевой последовательностью L и H-цепей. Антиген, связывающий центр молекулы иммуноглобулина называется антидетерминантой. Важное значение в связывании антигена имеет 3 участка в вариабельных областях L и H-цепей, обозначаемые CDR-1, CDR-2, CDR-3.
3.Антигенные свойства иммуноглобулинов послужили теми фенотипическими признаками, изучение которых позволило установить закономерности генетической регуляции биосинтеза иммуноглобулинов. Сама молекула иммуноглобулина способна выступать в роли антигена в тех случаях, когда иммуноглобулины одного вида вводятся в особь другого.
Антигенные свойства иммуноглобулинов определяются различными антигенными детерминантами, расположены в белковой части молекулы. Антитела обладают 2 свойствами: специфичностью, т е вступать во взаимодействие с антигеном, аналогичным, тому, который индуцировал их образование. Все иммуноглобулины являются иммунными, т е образуются в результате иммунизации, контакта с антигенами. Тем не менее по происхождению они делятся на: нормальные антитела, которые обнаруживаются в любом организме; инфекционные антитела, накапливаются в организме в период инфекционной болезни; постинфекционные антител, после переноса заболевания. Антитела всегда специфичны антигену, индуцировавшему их образование. По специфичности делятся на: группоспецифические; видоспецифические; вариантспецифические. Гетерогенность, т е неоднородность популяции иммуноглобулинов по генетической детерминированности их образования и по физико-химическому строению.
studfiles.net

