Диаграмма состояния системы железо углерод – Диаграмма состояния железо-углерод
alexxlab | 04.05.2020 | 0 | Разное
ИЗУЧЕНИЕ ДИАГРАММЫ СОСТОЯНИЯ СИСТЕМЫ ЖЕЛЕЗО-УГЛЕРОД (ЦЕМЕНТИТ)
В технике наиболее широко применяются железоуглеродистые сплавы, поэтому самое большое значение среди диаграмм состояния имеет диаграмма состояния железо-углерод (цементит).
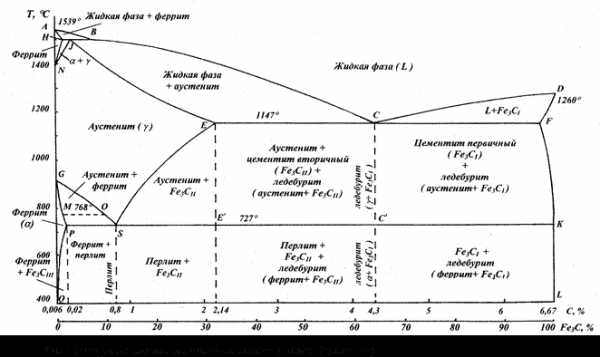
Имеется два варианта диаграммы состояния Fe-C: стабильная и метастабильная. Диаграмма состояния, показанная на рис.1, является диаграммой метастабильного равновесия, характеризующего превращения в системе железо-карбид железа. Стабильная диаграмма состояния характеризует превращения в система железо-графит. Особенностью диаграммы является двойная шкала по оси абсцисс, отражающая содержание углерода и цементита.
Структурный фазовый состав системы, указанный по диаграмме, соответствует действительному составу только при бесконечно медленных изменениях температуры. В зависимости от скорости изменения температуры линии фазовых превращений сдвигаются на некоторую величину переохлаждения или перенагрева, необходимую для переструктурирования системы при данной скорости изменения температуры.
В зависимости от температуры и содержания углерода железоуглеродистые сплавы образуют ряд структурных составляющих (фаз).
ФЕРРИТ (сокращенно обозначают Ф или a)- твердый раствор внедрения углерода в a-железе, имеет объемно-центрированную кубическую (ОЦК) кристаллическую решетку. Максимальная растворимость углерода в феррите при 727°С составляет 0,02% С, при комнатной температуре предельная растворимость С всего 0,006%. Феррит ниже точки Кюри (линия МО при 758°С) магнитен, на диаграмме занимает области GPQ и AHJ (низкотемпературный и высокотемпературный феррит, соответственно).
АУСТЕНИТ (сокращенно А или g)- твердый раствор внедрения углерода в g-железе, имеет гранецентрированную кубическую (ГЦК) решетку. Предел растворимость углерода в g-железе при температуре 1147°С равна 2,14%. Аустенит немагнитен, на диаграмме состояния занимает область AESG. Он имеет твердость НВ 160 при пластичности 40-50%.
ЦЕМЕНТИТ (Fе 3С или Ц)- химическое соединение железа с углеродом Fе3С (карбид железа), содержит 6,67% С. Цементит метастабилен: при высоких температурах распадается на более стабильные железо и чистый графит, поэтому температуру его плавления точно установить на сегодня невозможно, наиболее совершенный эксперимент с лазерным нагревом дал значение 1260°С.
Цементит обладает высокой твердостью >НВ 800 и очень низкой пластичностью, ниже 210°С магнитен.
В зависимости от условий образования различают цементит первичный Fе3СI который образуется из жидкого расплава при его затвердевании; вторичный Fе3СII, образующийся при распаде аустенита; третичный Fе3СIII– при выделении углерода из феррита.
ГРАФИТ- представляет собой чистый углерод, он мягок, обладает низкой прочностью и электропроводностью. В чугунах и графитизированной стали содержится в виде включений. Форма графитовых включений оказывает влияние на механические и технологические свойства железоуглеродистых сплавов.
ПЕРЛИТ – эвтектоидная механическая смесь феррита и цементита, содержащая 0,83%С, образуется при 727°С в результате распада аустенита в процессе его охлаждения:
g-Fe(C) — a-Fe(C) + Fe3C
Перлит чаще всего бывает пластинчатым, но может быть и зернистым. Это определяет его механические свойства: пластинчатый перлит имеет прочность sв= 800-900 МПа, пластичность d <16%, твердость НВ 180-220; у зернистого sв = 800 Мпа, d =15%, НВ 160-200.
 |
ЛЕДЕБУРИТ – механическая смесь (эвтектика) аустенита и цементита, образующаяся из жидкого расплава при 1147°С и при содержании 4,3%С. Твердость НВ 600-700, хрупок. При температурах ниже эвтектоидной (727°С) аустенит превращается в перлит, поэтому ниже прямой ЕК ледебурит представляет собой механическую смесь перлита и цементита. Перлит и ледебурит, а также более мелкозернистые сорбит, троостит рассматриваются чаще как двухфазные структурные составляющие.
Кроме этого, в железоуглеродистых сплавах обычно имеются еще различные неметаллические включения – химические соединения железа с кислородом, азотом, серой, фосфором и др.
Превращения в сплавах железо-цементит. Точка А – температура плавления чистого железа (0% С), точка D – плавление цементита. В точке С образуется эвтектика (ледебурит) . Точка Е показывает максимальную растворимость углерода в аустените при 1147°С, она принята границей деления железоуглеродистых сплавов на стали (до 2,14%С) и чугуны (содержание углерода выше 2,14%).
Линия ABCD – линия ликвидус (выше ликвидуса существует только жидкая фаза) показывает начало первичной кристаллизации: по линии АВ из жидкости начинает кристаллизовываться высокотемпературный феррит, по линии ВС – аустенит, а по линии CD кристаллизуется первичный цементит. В области ABJH существует жидкий раствор и кристаллы феррита, в области BCEJ – жидкая фаза + аустенит, а в CDF – жидкость + первичный цементит.
Линия AHJECF – линия солидус (ниже солидуса существует только твердая фаза) показывает конец первичной кристаллизации. Она также является началом вторичной кристаллизации (перекристаллизации), характерной для твердой фазы. Прямая ECF называется линией эвтектических превращений.
Аллотропия (полиморфизм) железа определяет превращения в сталях при их охлаждении от аустенитного состояния. Точка G диаграммы соответствует температуре аллотропического превращения чистого железа (911°С). С повышением содержания углерода до 0,8% температура аллотропического превращения аустенита в феррит, постепенно снижаясь, достигает 727°С. Линия GS – начало, линия GP – конец превращения аустенита в феррит, поэтому область GPQ характеризует феррит.
В точке S (с концентрацией 0,8%С и температурой 727°С) протекает реакция распада аустенита, продуктом которой является эвтектоидная смесь, называемая перлитом. Поэтому прямая PSK называется прямой эвтектоидных превращений. В области GSP существует аустенит и феррит, а в области QPS – перлит + феррит.
Таблица 1. Характерные точки диаграммы состояния системы железо – цементит
| Обозначение точки на диаграмме | Температура, °С | Содержание углерода, % | Обозначение точки на диаграмме | Температура, °С | Содержание углерода, % | |
| А | J | 0,16 | ||||
| В | 0,51 | К | 6,67 | |||
| С | 4,3 | L | 6,67 | |||
| С’ | 4,3 | М | 0,018 | |||
| D | 6,67 | N | ||||
| Е | 2,14 | 0,75 | ||||
| Е’ | 2,14 | Р | 0,02 | |||
| F | 6,5 | Q | 0,006 | |||
| G | S | 0,8 | ||||
| Н | 0,10 |
Точки аллотропических переходов называют также критическими точками и обозначают буквой А с индексом r, если точка находится на кривой охлаждения, и с – на кривой нагрева. При индексах r и с ставится цифра, указывающая положение рассматриваемой точки на линиях.
Линия GS поэтому называют также линией верхних критических точек А
Линия SE является линией ограниченной растворимости углерода в аустените: со снижением температуры растворимость падает с 2,14% до 0,8%. В связи с этим в сплавах при охлаждении избыточный углерод выпадает из аустенита в виде карбида железа Fе3С. Поэтому в области SEE’ существуют аустенит и вторичный цементит. Кривая SE также является геометрическим местом точек Acm и Arm . В области 0,8 SE’ 2,14 существуют перлит и цементит.
В чугунах и первичный аустенит, и аустенит в составе эвтектики к концу кристаллизации содержат максимально возможное содержание углерода (2,14% С). Со снижением температуры до 1147°С и ниже линии SE избыточный углерод выпадает из аустенита в виде вторичного цементита. Поэтому в области ЕСС’E’ существуют аустенит + ледебурит + вторичный цементит, а в oбласти CFKC’ – ледебурит + вторичный цементит. По прямой PSK в чугунах аустенит характеризуется перлитным превращением. Отсюда в области 2,14 Е’С’ 4,3 существуют перлит + ледебурит + вторичный цементит, а в области 4,3 С’К 6,67 – ледебурит + первичный цементит.
Следует отметить, что линия GPSK является концом вторичной кристаллизации железоуглеродистых сплавов.
Структура различных классов сталей и чугунов. В зависимости от содержания углерода стали делят на доэвтектоидные (С < 0,8%) (их также можно назвать конструкционными), эвтектоидные (С = 0,8%) и заэвтектоидные (С > 0,8%), последние две группы относят к инструментальным сталям.
Технически чистое железо содержит углерод не более 0,01%. Его структура – почти чистый феррит (рис. 2а.).
Структура дозвтектоидных сталей состоит из феррита (светлые участки) и перлита (рис. 2б). Перлит, представляющий собой мелкодисперсную двухфазную смесь, при травлении разъедается кислотой неравномерно по глубине (рис. 2г). При рассматривании в металлографический микроскоп более глубокие “язвы” в перлите оказываются в тени, и в сравнению с другими однородными фазами, отсвечивающими по всей площади, перлит кажется темнее.
Структура эвтектоидной стали – перлит (рис. 2в), а заэвтектоидных – перлит и цементит (светлые участки в виде сетки или игл) (рис. 2д).
 |
В зависимости от содержания углерода чугуны делятся на доэв-тектические (2.14% < С < 4.3), эвтектические (С = 4.3%) и заэвтектические (С > 4.3%).
У чугунов без графита излом имеет матово-белый цвет, поэтому их называют белыми чугунами в противоположность серым чугунам, у которых часть углерода выделилась в виде включений графита. В белых чугунах весь углерод связан в твердых растворах и химических соединениях. Структура доэвтектических белых чугунов состоит из перлита, ледебурита и цементита (рис. 2е). Структура эвтектического чугуна – ледебурит (рис. 2ж), заэвтектических чугунов – ледебурит + первичный цементит (рис. 2з).
Правила определения количественного соотношения фаз. Имея диаграмму состояния, можно проследить за фазовыми превращениями любого сплава и указать состав и количественное соотношение фаз при любой температуре. Это осуществляется с помощью довольно простых правил, применение которых рассмотрим на примере.
Задача: Пусть требуется определить фазовый состав железоуглеродистой системы с содержанием углерода 2% при: а)комнатной температуре; б)при 800°С.
Решение: а)С химической точки зрения в железоуглеродистых сплавах при комнатной температуре имеются только две фазы: феррита и цементита (карбида железа Fе3С), в то время как при 800°С кроме феррита и цементита может существовать еще фаза аустенита.
При комнатной температуре, когда отсутствует аустенит, фазовый состав сплава можно определить прямо по второй шкале абсцисс: так 2%С соответствует содержанию карбида железа 30%. остальное феррит (70%).
Подобный метод решения вопроса по координатам точек на диаграмме называется правилом определения фаз (правило концентраций).
б) В случае других температур вторая шкала абсцисс не отражает действительного соотношения фаз и не должна применяться.
В данном случае применяем правило отрезков. Оно позволяет на основе диаграмм состояния определять для любого сплава при любой температуре относительное количество присутствующих в нем фаз или структурных элементов и определять количественный состав каждого из них, т. е. производить не только качественный, но и количественный анализ сплавов. Для этого, согласно правилу отрезков, через определенную точку (рис. 3), отвечающую данному сплаву, проводят на уровне заданной температуры (800°С) горизонталь (так называемую коноду)
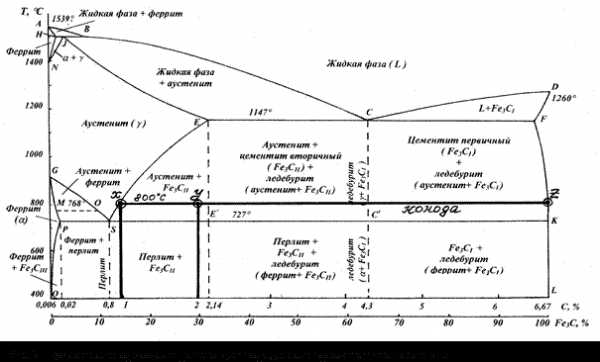 |
до пересечения ее с линиями фазовых и структурных превращений и делаем соответствующий анализ.
При 800°С сплав с данной концентрацией попадает в область CEE’ (точка y). По начерченной нами коноде, опуская перпендикуляр из точки x пересечения ее с линией аустенитного превращения (линия SE) находим, что предел растворимости углерода в аустените при 800°С приблизительно равна 1%. Таким образом, содержание аустенитной фазы будет уменьшаться со 100% при содержании углерода 1% до 0% при содержании углерода 6,67%, когда весь сплав будет состоять только из цементита. При промежуточном содержании С фазовый состав линейно изменяется: постепенно падает содержание аустенита со 100% до нуля, а концентрация цементита растет с 0 до 100%.
Для определения содержания цементита СЦсогласно правилу отрезков используем выражение:
(1)
где xy и xz – длины отрезков, определяемые по шкале содержания углерода. Учитывая что xy=2-1=1, xz= 6,67-1=5,67 находим содержание цементита:
Длины отрезков, соответствующие фазам, следует брать в направлении, обратном расположению фаз на диаграмме.
Содержание аустенита находим из:
СA = 100% – СЦ (2)
Вычислим:
СA = 100-17,64=82,36%
Указания по выполнению работы:
1. Самостоятельно проработать, т.е. сделать конспект прилагаемого теоретического материала, а также указанной ниже литературы, и уяснить учебные вопросы по данной теме. В конспекте аккуратно нарисовать диаграмму состояния системы “железо-цементит” с подробным указанием характерных температур и наличия фаз. Рекомендуется штриховкой цветными карандашами обозначить границы существования структурных составляющих.
Нарисовать характерный вид структуры различных железоуглеродистых сплавов при различных содержаниях С с указанием фаз.
2. Решить следующие задачи:
а) Пользуясь диаграммой состояния (обозначая линии построения цветными карандашами или пастой) определить температуры перехода в полностью жидкое и полностью твердое состояния для системы Fe-C с указанным по варианту содержанием углерода. Результаты записать.
б) Определить фазовый состав системы Fe – С в равновесном (отожженном) состоянии с заданным содержанием углерода при комнатной и указанной по варианту температурах. Графические построения и ход расчета, а также полученные результаты должны быть отражены в отчете по работе.
Контрольные вопросы: 1. Что такое диаграмма состояния 2. Что такое фазовые превращения и чем они обусловлены? 3. Границы содержания углерода для сталей и чугунов. 4. Состав и структура отдельных фаз в диаграмме состояния “железо-углерод”: феррита, аустенита, цементита, перлита и ледебурита. 5. Почему диаграмма состояния “железо-углерод” ограничивается по оси абсцисс содержанием углерода 6,67%? 6. В каком качестве находится углерод в различных структурных составляющих железных сплавов ? 7. Как определить по диаграмме состояния фазовый состав равновесной системы? 8. Какие эвтектические и эвтектоидные превращения имеют место на диаграмме состояния системы Fe – С ?
Задания по вариантам. Решить задачи по диаграмме состояния при данных условиях:
| Вариант | |||||||||||||||
| а) Содерж. С,% | 0,2 | 0,6 | 0,8 | 1,0 | 1,4 | 1,8 | 2,0 | 2,2 | 2,6 | 3,0 | 3,6 | 4,0 | 4,3 | 5,0 | 6,0 |
| б) Содерж. С,% температура ,°С | 6,5 | 4,5 | 2,5 | 1,5 | 4,0 | 3,5 | 3,0 | 2,0 | 5,5 | 4,8 | 5,0 | 2,0 | 6,0 | 3,6 | 1,5 |
Похожие статьи:
poznayka.org
Диаграмма состояния системы железо – углерод. – 13 Сентября 2011 – Технологии
1. Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
2. Феррит (Ф, α) – твердый раствор внедрения углерода в α-железе (от латинского слова ferrum – железо).
Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727 °С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539 °С) с предельной растворимостью углерода 0,1 % при температуре 1499 °С (точка J).
Свойства феррита близки к свойствам железа.
Он мягок (твердость –130 НВ, временное сопротивление – σв = 300 МПа) и пластичен (относительное удлинение – δ =50 %), магнитен до 768 °С.
3. Аустенит (А, γ) – твердый раствор внедрения углерода в γ-железо (по имени английского ученого Р. Аустена).
Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ-железе 2,14 % при температуре 1147 °С (точка Е).
Аустенит имеет твердость 200…250 НВ, пластичен (относительное удлинение – δ =40…50 %), парамагнитен.
При растворении в аустените других элементов могут изменяться свойства и температурные границы существования.
4. Цементит – характеристика дана выше.
В железоуглеродистых сплавах присутствуют фазы – цементит первичный, цементит вторичный, цементит третичный.
Химические и физические свойства этих фаз одинаковы.
Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений.
Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов.
Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита).
Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
5. Графит – характеристика дана выше.
Поскольку углерод в сплавах с железом встречается в виде цементита и графита, существуют две диаграммы состояния, описывающие условия равновесия фаз в системах железо – цементит и железо – графит.
Первая диаграмма (Fе — Fе3С) называется цементитной (метастабильная), вторая (Fе – С)- графитной (стабильная).
Оба варианта диаграммы приводятся вместе в одной системе координат – температура – содержание углерода (рис. 1).
Диаграмма состояния системы железо – углерод построена по результатам многочисленных исследований, проведенных учеными разных стран.
Особое место среди них занимают работы Д.К. Чернова.
Он открыл существование критических точек в стали, определил их зависимость от содержания углерода, заложил основы для построения диаграммы состояния железоуглеродистых сплавов в ее нижней, наиболее важной части.
Буквенное обозначение узловых точек в диаграмме является общепринятым как в России, так и за рубежом.
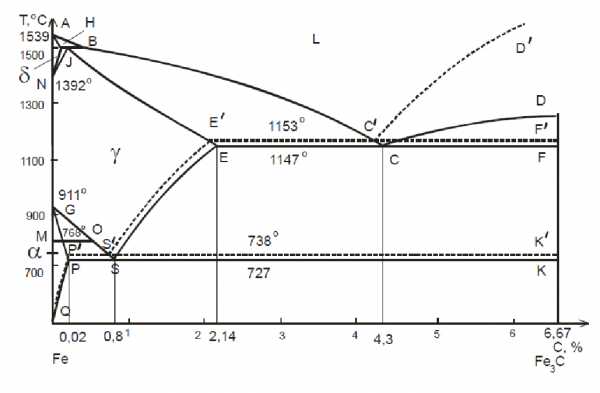
Рис. 1. Общий вид диаграммы состояния системы железо – углерод
СИСТЕМА ЖЕЛЕЗО — ЦЕМЕНТИТ (Fe — Fе3С)
Диаграмма состояния системы железо – цементит изображена на рис. 2.
Данные о точках диаграммы приведены в табл. 1.
Имеющиеся во всех областях диаграммы фазы видны на рис. 2.
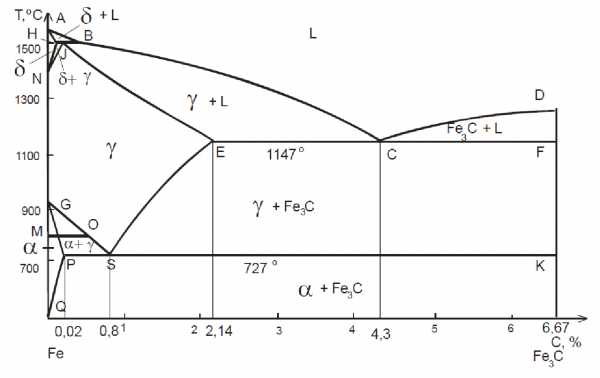
Рис. 2. Диаграмма состояния системы железо – цементит
Ликвидус по всей диаграмме проходит по линиям АВ, ВС, СD; солидус – по линиям АН, НJ, JЕ, ЕСF.
Сплавы железа с углеродом обычно делят на стали и чугуны.
Условной границей для такого деления является 2,14 % С (точка E).
Сплавы, содержащие углерода менее 2,14 %, относятся к сталям, более 2,14 % – к чугунам.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, обозначаются буквой А.
В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс с (от слова chauffage – нагрев) при нагреве и индекс r (от слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
Таким образом, например, нагрев доэвтектоидной стали выше соответствующей точки на линии СS обозначается как нагрев выше точки АС3.
При охлаждении же этой стали первое превращение должно быть обозначено как Аr3, второе (на линии РSК) – как Аr1.
Таблица 1.Узловые точки диаграммы состояния системы Fе — Fе3С.
Обозначение точки | t,°С | С,% | Значение точки |
А | 1539 | 0 | Плавление (кристаллизация) чистого железа |
N | 1392 | 0 | Полиморфное превращение δ↔ γ в чистом железе |
G | 911 | 0 | Полиморфное превращение α↔ γ в чистом железе |
Н | 1499 | 0,1 | δ-твердый раствор, предельно насыщенный углеродом. Участвует в перитектическом превращении |
J (I) | 1499 | 0,16 | Аустенит, возникающий в результате перитектического превращения |
В | 1499 | 0,51 | Жидкая фаза, участвующая в перитектическом превращении |
D | 1260 | 6,67 | Предполагаемая температура плавления Fе3С |
Е | 1147 | 2,14 | Аустенит, предельно насыщенный углеродом |
С | 1147 | 4,3 | Жидкая фаза, испытывающая эвтектическое превращение |
F | 1147 | 6,67 | – |
P | 727 | 0,02 | Феррит, предельно насыщенный углеродом |
S | 727 | 0,8 | Аустенит, испытывающий эвтектоидное превращение |
K | 727 | 6,67 | – |
Q | 20 | 0,006 | Феррит, предельно насыщенный углеродом |
Прежде чем перейти к непосредственному разбору на конкретных примерах процессов фазовых превращений, совершающихся в различных сплавах при их охлаждении и нагреве, необходимо сделать следующие замечания.
*Всякая диаграмма состояния показывает условия равновесного сосуществования фаз во взятой системе компонентов.
*Составы фаз при любой температуре удовлетворяют значениям, определяемым по сопряженным кривым только при условии установившегося физико-химического равновесия и при наличии плоской границы раздела фаз, т. е. при бесконечно большом радиусе кривизны этой поверхности.
*Если же поверхности раздела контактирующих фаз имеют иной (меньший) радиус кривизны, то создаются иные условия равновесия, в связи с чем изменяется взаимный ход соответствующей сопряженной пары кривых…
lmx.ucoz.ru
Диаграмма состояния системы железо – углерод (Fe-C) :: Диаграммы сплавов
Начало изучения диаграммы состояния системы железо – углерод связано с открытием критических точек в стали Д. К. Черновым в 1868 г.
Для точки A приняты значения 0,16% (по массе), или 0,74% (ат.), для точки В — значения 0,51% (по массе), или 2,33% (ат.). По данным термического анализа , линия ликвидус δ-фазы АВ — почти прямая, точке В соответствует 2,47% (ат.), предельная растворимость углерода в δ-Feсоставляет 0,5 % (эт.). Температура перитектической горизонтали равна 1496±2°С, точке 1 отвечает 0,18 % (но массе), или 0,83 % (эт.). Предельная растворимость углерода в γ-Fe при 1147°С составляет 2,14% (по массе), или 9,2% (ат.) ; при 1150°С 2,02% (по массе), или 8,7 % (ат.). Возможно, цементит испытывает инконгруэнтное разложение при 1250—1300° С. Температура эвтектической горизонтали ECF принята равной 1147°С, эвтектике (точке С) соответствует 4,30%(по массе), или 17,28 % (ат.) С .
Превращение у↔а (A3, кривая GS), исследованное многими авторами, также подтверждено последующими работами. Кристаллическая структура. Феррит имеет о. ц. к. структуру a-Fe. Период решетки a-Feравен 0,2862 им при 20 °С и линейно возрастает до 0,2899 нм при 910 °С . При 769 °С (точка Кюри) ферромагнитное a-Feпереходит в «немагнитное α-Fe» (точнее, в упорядоченное антиферромагнитное β-Fe) . Вследствие малой растворимости углерода в a-Fe[0,02 % (по массе)] период решетки Тk-феррита практически такие же, как и чистого a-Fe. Атомы углерода в феррите занимают преимущественно октапоры. Выше 1392 °С γ-Fe превращается в парамагнитную δ-фазу, существующую при 1392—1536 °С. Период решетки о. ц. к. δ-Fe равен 0,2925 нм при 1392 °С и линейно растет до 0,2935 нм при 1536 °С . Температурная зависимость периода решетки для α-(β-) и γ-Fe различны. Период решетки δ-феррита с повышением температуры увеличивается сильнее, чем α (β)-фазы и, по-видимому, растет с увеличением содержания углерода. Карбид Fe7C3 получен только при высоких давлениях. Он имеет гексагональную структуру типа Сr7С3. Периоды решетки а=0,6882 нм, с= 0,4540 нм. Установлено существование метастабильного карбида Fe2C
markmet.ru
Диаграмма состояния сплавов железо-углерод — WiKi
Диагра́мма фа́зового равнове́сия (диаграмма состоя́ния) желе́зо—углеро́д (иногда эту диаграмму называют «диаграмма железо—цементит») — графическое отображение фазового состояния сплавов железа с углеродом в зависимости от их химического состава и температуры.
Диаграмма состояния
Железо образует с углеродом химическое соединение Fe3C цементит. Так как на практике применяют металлические сплавы на основе железа с содержанием углерода до 5 %, практически интересна часть диаграммы состояния от чистого железа до цементита[1]. Поскольку цементит — метастабильная фаза, то и соответствующая диаграмма называется метастабильной (сплошные линии на рисунке).
Для серых чугунов и графитизированных сталей рассматривают стабильную часть диаграммы железо—графит (Fe—Гр), поскольку именно графит является в этом случае стабильной фазой. Цементит выделяется из расплава намного быстрее графита и во многих сталях и белых чугунах может существовать достаточно долго, несмотря на метастабильность. В серых чугунах графит существует обязательно.
На рисунке тонкими пунктирными линиями показаны линии стабильного равновесия (то есть с участием графита), там где они отличаются от линий метастабильного равновесия (с участием цементита), а соответствующие точки обозначены штрихом. Обозначения фаз и точек на этой диаграмме приведены согласно неофициальному международному соглашению.
Фазы диаграммы железо-углерод
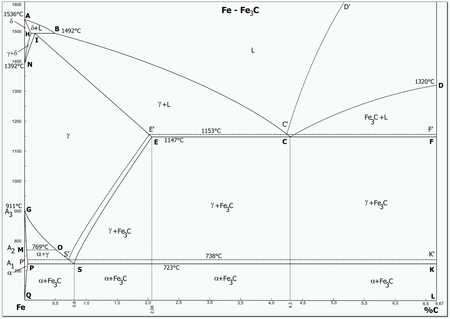 Часть диаграммы состояния сплавов железо-цементит
Часть диаграммы состояния сплавов железо-цементитВ системе железо — углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях[источник не указан 785 дней] с образованием однородной жидкой фазы.
Феррит — Твёрдый раствор внедрения углерода в α-железе с объёмно-центрированной кубической решёткой.
Феррит имеет переменную, зависящую от температуры предельную растворимость углерода: минимальную — 0,006 % при комнатной температуре (точка Q), максимальную — 0,02 % при температуре 700 °C (точка P). Атомы углерода располагаются в центре грани или (что кристаллогеометрически эквивалентно) на середине рёбер куба, а также в дефектах решетки[2].
При температуре выше 1392 °C существует высокотемпературный феррит с предельной растворимостью углерода около 0,1 % при температуре около 1500 °C (точка H).
Свойства феррита близки к свойствам чистого железа. Он мягок (твёрдость по Бринеллю — 130 НВ) и пластичен, ферромагнитен (при отсутствии углерода) до точки Кюри — 770 °C.
Аустенит (γ) — твёрдый раствор внедрения углерода в γ-железе с гранецентрированной кубической решёткой.
Атомы углерода занимают место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в аустените — 2,14 % при температуре 1147 °C (точка Е). Аустенит имеет твёрдость 200—250 НВ, пластичен, парамагнитен. При растворении других элементов в аустените или в феррите изменяются свойства и температурные границы их существования[3].
Цементит (Fe3C) — химическое соединение железа с углеродом (карбид железа), со сложной ромбической решёткой, содержит 6,67 % углерода. Он твёрдый (свыше 1000 HВ), и очень хрупкий. Цементит — метастабильная фаза и при длительном нагреве самопроизвольно разлагается с выделением графита.
В железоуглеродистых сплавах цементит как фаза может выделяться при различных условиях:
- цементит первичный (выделяется из жидкости),
- цементит вторичный (выделяется из аустенита),
- цементит третичный (из феррита),
- цементит эвтектический и
- эвтектоидный цементит.
Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зёрен аустенита (после эвтектоидного превращения они станут зёрнами перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зёрен[4].
Эвтектический цементит наблюдается лишь в белых чугунах. Эвтектоидный цементит имеет пластинчатую форму и является составной частью перлита. Цементит может при специальном сфероидизируюшем отжиге или закалке с высоким отпуском выделяться в виде мелких сфер. Влияние на механические свойства сплавов оказывает форма, размер, количество и расположение включений цементита, что позволяет на практике для каждого конкретного применения сплава добиваться оптимального сочетания твёрдости, прочности, стойкости к хрупкому разрушению и т. п.[5]
Графит — фаза состоящая только из углерода со слоистой гексагональной решёткой. Плотность графита (2,3 г/см3) много меньше плотности всех остальных фаз (около 7,5—7,8 г/см3) и это затрудняет и замедляет его образование, что и приводит к выделению цементита при более быстром охлаждении. Образование графита уменьшает усадку при кристаллизации, графит выполняет роль смазки при трении, уменьшая износ, способствует рассеянию энергии вибраций.
Графит имеет форму крупных крабовидных (изогнутых пластинчатых) включений (обычный серый чугун) или сфер (высокопрочный чугун).
Графит обязательно присутствует в серых чугунах и их разновидности — высокопрочных чугунах. Графит присутствует также и в некоторых марках стали — в так называемых графитизированных сталях.
Фазовые переходы
Линия ACD — это линия ликвидуса, показывающая температуры начала затвердевания (конца плавления) сталей и белых чугунов. При температурах выше линии ACD — жидкий сплав. Линия AECF — это линия солидуса, показывающая температуры конца затвердевания (начала плавления).
По линии ликвидуса АС (при температурах, отвечающих линии АС) из жидкого сплава кристаллизуется аустенит, а по линии ликвидуса CD — цементит, называемый первичным цементитом. В точке С при 1147 °С и содержании 4,3 % углерода из жидкого сплава одновременно кристаллизуется аустенит и цементит первичный, образуя эвтектику, называемую ледебуритом. При температурах, соответствующих линии солидуса AE, сплавы с содержанием углерода до 2,14 % окончательно затвердевают с образованием структуры аустенита. На линии солидуса EC (1147° С) сплавы с содержанием углерода от 2,14 до 4,3 % окончательно затвердевают с образованием эвтектики ледебурита. Так как при более высоких температурах из жидкого сплава выделялся аустенит, следовательно, такие сплавы после затвердевания будут иметь структуру аустенит + ледебурит.
На линии солидуса CF (1147 °С) сплавы с содержанием углерода от 4,3 до 6,67 % окончательно затвердевают также с образованием эвтектики ледебурита. Так как при более высоких температурах из жидкого сплава выделялся цементит (первичный), следовательно, такие сплавы после затвердевания будут иметь структуру — первичный цементит + ледебурит[6].
В области ACEA, между линией ликвидуса AC и солидуса AEC, будет жидкий сплав + кристаллы аустенита. В области CDF, между линией ликвидуса CD и солидуса CF, будет жидкий сплав + кристаллы цементита (первичного). Превращения, протекающие при затвердевании сплавов, называют первичной кристаллизацией. В результате первичной кристаллизации во всех сплавах с содержанием углерода до 2,14 % образуется однофазная структура — аустенит. Сплавы железа с углеродом, в которых в результате первичной кристаллизации в равновесных условиях получается аустенитная структура, называют сталями.
Сплавы с содержанием углерода более 2,14 %, в которых при кристаллизации образуется эвтектика ледебурит, называют чугунами. В рассматриваемой системе практически весь углерод находится в связанном состоянии, в виде цементита. Излом таких чугунов светлый, блестящий (белый излом), поэтому такие чугуны называют белыми[4].
В железоуглеродистых сплавах превращения происходят также и в твердом состоянии, называемые вторичной кристаллизацией и характеризуемые линиями GSE, PSK, PQ. Линия GS показывает начало превращения аустенита в феррит (при охлаждении). Следовательно, в области GSP будет структура аустенит + феррит.
Линия SE показывает, что с понижением температуры растворимость углерода в аустените уменьшается. Так, при 1147 °С в аустените может раствориться углерода 2,14 %, а при 727°С — 0,8 %. С понижением температуры в сталях с содержанием углерода от 0,8 до 2,14 % из аустенита выделяется избыточный углерод в виде цементита, называемого вторичным. Следовательно, ниже линии SE (до температуры 727°С) сталь имеет структуру: аустенит + цементит (вторичный). В чугунах с содержанием углерода от 2,14 до 4,3 % при 1147 °С, кроме ледебурита, есть аустенит, из которого при понижении температуры тоже будет выделяться вторичный цементит. Следовательно, ниже линии EC (до температуры 727 °С) белый чугун имеет структуру: ледебурит + аустенит + цементит вторичный.
Линия PSK (727° С) — это линия эвтектоидного превращения. На этой линии во всех железоуглеродистых сплавах аустенит распадается, образуя структуру, представляющую собой механическую смесь феррита и цементита и называемую перлитом. Ниже 727°С железоуглеродистые сплавы имеют следующие структуры.
- Стали, содержащие углерода менее 0,8 %, имеют структуру феррит + перлит и называются доэвтектоидными сталями.
- Сталь с содержанием углерода 0,8 % имеет структуру перлита и называется эвтектоидной сталью.
- Стали с содержанием углерода от 0,8 до 2,14 % имеют структуру цементит + перлит и называются заэвтектоидными сталями.
- Белые чугуны с содержанием углерода от 2,14 до 4,3 % имеют структуру перлит + вторичный цементит + ледебурит и называются доэвтектическими чугунами.
- Белый чугун с содержанием углерода 4,3 % имеет структуру ледебурита и называется эвтектическим чугуном.
- Белые чугуны с содержанием углерода от 4,3 до 6,67 % имеют структуру цементит первичный + ледебурит и называются заэвтектическими чугунами[5].
Линия PQ показывает, что с понижением температуры растворимость углерода в феррите уменьшается от 0,02 % при 727 °С до 0,006 % при комнатной температуре. При охлаждении ниже температуры 727° С из феррита выделяется избыточный углерод в виде цементита, называемого третичным. В большинстве сплавов железа с углеродом третичный цементит в структуре можно не учитывать из-за весьма малых его количеств. Однако в низкоуглеродистых сталях в условиях медленного охлаждения третичный цементит выделяется по границам зерен феррита (рис. 76). Эти выделения уменьшают пластические свойства стали, особенно способность к холодной штамповке[5].
См. также
Примечания
- ↑ Кузьмин, 1971, с. 91.
- ↑ Циммерман, 1982, с. 31.
- ↑ Циммерман, 1982, с. 33.
- ↑ 1 2 Кузьмин, 1971, с. 93.
- ↑ 1 2 3 Кузьмин, 1971, с. 95.
- ↑ Кузьмин, 1971, с. 92.
Литература
- Кузьмин Б. А., Самохоцкий А. И., Кузнецова Т. Н. Металлургия, металловедение и конструкционные материалы. — Москва: Высшая школа, 1971. — 352 с.
- Циммерман Р., Гюнтер К. Металлургия и материаловедение. — Справ. издание. Пер. с нем.. — Москва: Металлургия, 1982. — 480 с.
ru-wiki.org

