Диаграмма состояния железо углерод сплавов: Диаграмма железо-углерод | ООО КВАДРО
alexxlab | 03.10.1986 | 0 | Разное
Диаграмма состояния Fe-C (реферат) :: Рефераты по металлургии
Равновесное состояние железоуглеродистых сплавов в зависимости от содержания углерода и температуры описывает диаграмма состояния железо – углерод. На диаграмме состояния железоуглеродистых сплавов (рис. 1) на оси ординат отложена температура, на оси абсцисс – содержание в сплавах углерода до 6,67%, то есть до такого количества, при котором образуется цементит Fе3С. По диаграмме состояния системы железо – углерод судят о структуре медленно охлажденных сплавов, а также о возможности изменения их микроструктуры в результате термической обработки, определяющей эксплуатационные свойства. На диаграмме состояния Fe – Fе3С приняты международные обозначения. Сплошными линиями показана диаграмма состояния железо – цементит (метастабильная, так как возможен распад цементита), а пунктирными – диаграмма состояния железо – графит {стабильная).
Рассматриваемую диаграмму правильнее считать не железоуглеродистой (Fe – С), а железоцементитной (Fe – Fе3С), так как свободного углерода в сплавах не содержится. Но так как содержание углерода пропорционально содержанию цементита, то практически удобнее все изменения структуры сплавов связывать с различным содержанием углерода.
Но так как содержание углерода пропорционально содержанию цементита, то практически удобнее все изменения структуры сплавов связывать с различным содержанием углерода.
Компоненты системы железо и углерод – элементы полиморфные. Основной компонент системы – железо.
Углерод растворим в железе в жидком и твердом состояниях, а также может образовать химическое соединение – цементит Fе3С или присутствовать в сплавах в виде графита.
В системе железо-цементит (Fe – Fе3С) имеются следующие фазы: жидкий раствор. твердые растворы – феррит и аустенит, а также химическое соединение – цементит.
Феррит может иметь две модификации – высоко- и низкотемпературную. Высокотемпературная модификация d-Fe и низкотемпературная – a-Fe представляют собой твердые растворы углерода, соответственно, в d- и a- железе.
Предельное содержание углерода в a-Fe при 723°С -0,02%, а при 20°С – 0,006%. Низкотемпературный феррит a-Fe по свойствам близок к чистому железу и имеет довольно низкие механические свойства, например, при 0,06% С:
s = 250 МПа;
d – 50%;
y= 80%;
твердость – 80. ..90 НВ.
..90 НВ.
Аустенитg-Fe – твердый раствор углерода в g-железе. Предельная растворимость углерода в g-железе 2,14%. Он устойчив только при высоких температурах, а с некоторым примесями (Мn, Сг и др.) при обычных (даже низких) температурах. Аустенит обладает высокой пластичностью, низкими пределами текучести и прочности. Твердость аустенита 160…200 НВ.
Цементит Fе3С – химическое соединение железа с углеродом, содержащее 6,67% vглерода. Между атомами железа и углерода в цементите действуют металлическая и ковалентная связи. Температура плавления ~1250°С. Цементит является метастабильной фазой; область его гомогенности очень узкая и на диаграмме состояния он изображается вертикалью. Время его устойчивости уменьшается с повышением температуры: при низких температурах он существует бесконечно долго, а при температурах, превышающих 950°С, за несколько часов распадается на железо и графит. Цементит имеет точку Кюри (210°С) и обладает сравнительно высокими твердостью (800 НВ и выше) и хрупкостью.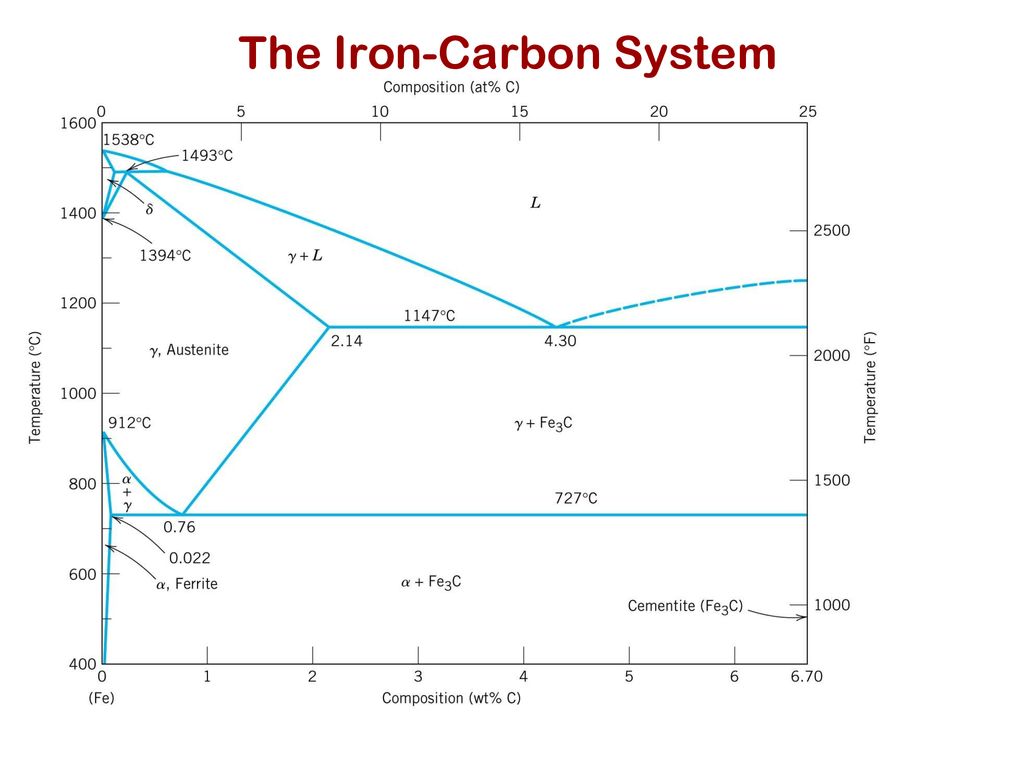 Прочность его i растяжение очень мала (s =40 МПа).
Прочность его i растяжение очень мала (s =40 МПа).
В системе железо – цементит имеются две тонкие механические смеси фаз – эвтектическая (ледебурит) и эвтектоидная (перлит).
Ледебурит является смесью двух фаз g-Fe + Fе3С, образующихся при 1130°С в сплавах, содержащих от 2,0 до 6,67%С, и наблюдается визуально как структурная составляющая железоуглеродистых сплавов, главным образом, чугунов. Ледебурит обладает достаточно высокими прочностью (НВ>600) и хрупкостью.
Перлит (до 2,0%С) представляет собой смесь a-Fe + Fе3С (в легированных сталях -карбидов), образующуюся при 723°С и содержании углерода 0,83% в процессе распада аустенита, и наблюдается визуально как структурная составляющая железоуглеродистых сплавов. Механические свойства перлита зависят от формы и дисперсности частичек цементита (прочность пластинчатого перлита несколько выше, чем зернистого):
s=800…900 МПа;
d< 16%;
НВ 180..,220.
Диаграмма состояния Fe – Fе3С (рис. 1) является комбинацией диаграмм простых типов. На ней имеются три горизонтали трехфазных равновесий: перитектического (1496°С), эвтектического (1147°С) и эвтектоидного (727°С).
1) является комбинацией диаграмм простых типов. На ней имеются три горизонтали трехфазных равновесий: перитектического (1496°С), эвтектического (1147°С) и эвтектоидного (727°С).
Все линии на диаграмме состояния соответствуют критическим точкам, то есть температурам, при которых происходят фазовые и структурные превращения в железоуглеродистых сплавах.
Линия ABCD – линия начала кристаллизации сплава (ликвидус), линия AHJECF – линия конца кристаллизации сплава (солидус).
В области диаграммы HJCE находится смесь двух фаз: жидкого раствора и аустенита, а в области CFD – жидкого раствора и цементита. В точке С при содержании 4,3%С и температуре 1130°С происходит одновременная кристаллизация аустенита и цементита и образуется их тонкая механическая смесь – ледебурит. Ледебурит присутствует во всех сплавах, содержащих от 2,0 до 6,67%С (чутуны).
Точка Е соответствует предельному насыщению железа углеродом (2,0%С).
В области диаграммы AGSF находится аустенит. При охлаждении сплавов аустенит распадается с выделением по линии GS феррита, а по линии SE – вторичного цементита. Линии GS и PS имеют большое практическое значение для установления режимов термической обработки сталей. Линию GS называют линией верхних критических точек, а линию PS –нижних критических точек.
Линии GS и PS имеют большое практическое значение для установления режимов термической обработки сталей. Линию GS называют линией верхних критических точек, а линию PS –нижних критических точек.
В области диаграммы GSP находится смесь двух фаз – феррита и распадющегося аустенита, а в области диаграммы SEE’ – смесь вторичного цементита и распадающегося аустенита.
В точке S при содержании 0,8%С и при температуре 723°С весь аустенит распадается и одновременно кристаллизуется тонкая механическая смесь феррита и цементита – перлит.
Линия PSK соответствует окончательному распаду аустенита и образованию перлита. В области ниже линии PSK никаких изменений структуры не происходит.
Структурные превращения в сплавах, находящихся в твердом состоянии, вызваны следующими причинами: изменением растворимости углерода в железе в зависимости от температуры сплава (QP и SE), полиморфизмом железа (PSK) и влиянием содержания растворенного углерода на температуру полиморфных превращений (растворение углерода в железе способствует расширению температурной области существования аустенита и сужению области феррита).
Диаграмма стабильного равновесия Fe – Fе3С, обозначенная на рис. 1 пунктиром, отображает возможность образования высокоуглеродистой фазы – графита – на всех этапах структурообразования в сплавах с повышенным содержанием углерода. Диаграмма состояния стабильной системы железо – графит отличается от метастабильной системы железо-цементит только в той части, где в фазовых равновесиях участвует высокоуглеродистая фаза (графит или цементит).
На диаграмме состояния различают две области: стали и чугуны. Условия принятого разграничения – возможность образования ледебурита (предельная растворимость углерода в аустените):
• стали – до 2,14% С, не содержат ледебурита;
• чугуны – более 2,14%С, содержат ледебурит.
В зависимости от содержания углерода (%) железоуглеродистые сплавы получили следующие названия:
• менее 0,83 – доэвтектоидные стали;
• 0,83 – эвтектоидные стали;
• 0,83…2 – заэвтектоидные стали;
• 2. ..4,3 – доэвтектические чугуны;
..4,3 – доэвтектические чугуны;
• 4,3…6,67 – заэвтектические чугуны.
АНАЛИЗ ДИАГРАММЫ СОСТОЯНИЯ ЖЕЛЕЗО – углерод
vk.com/club152685050 | vk.com/id446425943
Лабораторная работа 2
Цель работы – изучить диаграмму состояния Fe – C и структурные превращения железоуглеродистых сплавов.
Задание и порядок выполнения работы
1.Ознакомиться с основными теоретическими положениями.
2.Дать описание основных линий, точек, фаз и структурных составляющих диаграммы состояния железо – цементит.
3.Вычертить диаграмму состояния в масштабе с принятым обозначением точек, температур, концентраций углерода и обозначить структуры во всех областях диаграммы.
4.Научиться определять концентрации углерода в фазах при различных температурах и количественные соотношения фаз, используя правило отрезков.
5.Построить кривые охлаждения заданных сплавов с применением правила фаз, занести номера критических точек, числа степеней свободы, структуры на каждом участке кривой и превращения на горизонтальных участках.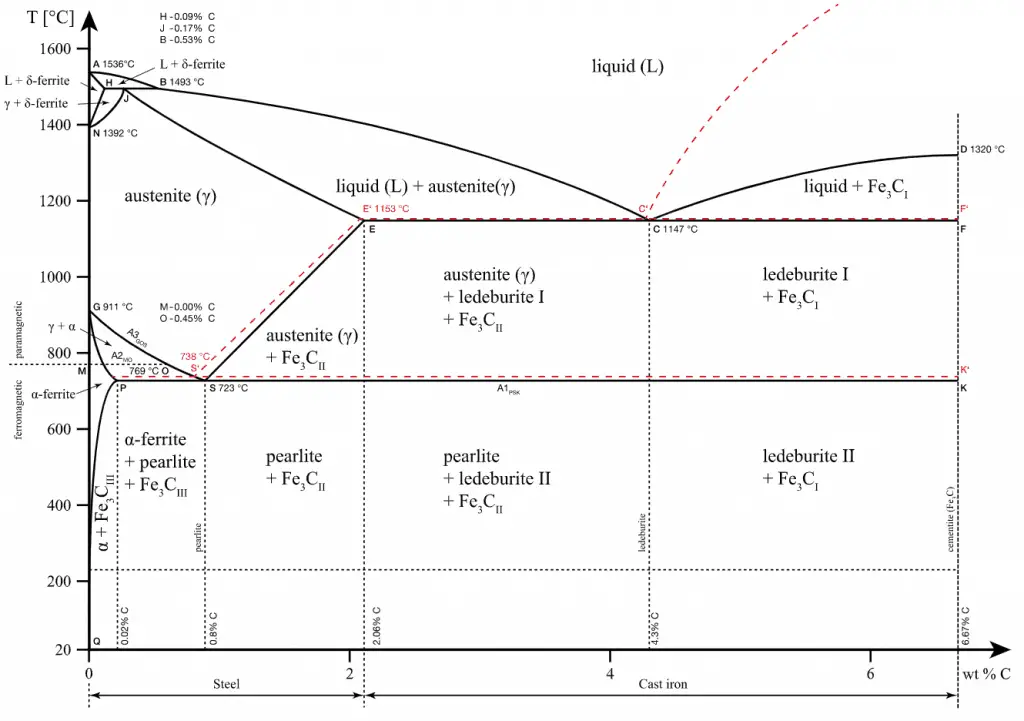
Основы теории Наиболее распространенными металлическими материалами являются
сплавы железа и углерода – стали и чугуны. В сталях содержится менее 2,14%С, а в чугунах – более 2,14%С. Диаграмма железо – углерод показывает фазовый состав и структуру железоуглеродистых сплавов (сталей и чугунов).
Рассмотрим компоненты системы железо – углерод и их взаимодействие. Компоненты – вещества, образующие систему:
1. Железо – металл сероватого цвета, температура плавления 1539 ºС, плотность 7,68 г/см3. Железо имеет четыре модификации: α, β, γ и δ.
При температурах ниже 911ºС кристаллическая решетка железа – объемно центрированный куб (ОЦК). Эту модификацию называют α-железо. До температуры 768 ºС (точка Кюри) α-железо магнитно, выше – немагнитно. Его называют β – немагнитным или β – железом.
При нагреве железа объемно центрированная кубическая решетка при 911 ºС перестраивается в гранецентрированную кубическую (ГЦК). Эта модификация существует до 1392 ºС и называется γ-железом.
Выше 1392 С и до температуры плавления вновь устойчивой является ОЦК решетка – δ-железо.
2. Углерод – неметаллический элемент, плотность 2,5 г/см3, температура плавления 3500 ºС. В железоуглеродистых сплавах в свободном виде углерод находится в форме графита.
Углерод растворим в железе в жидком и твердом состояниях, может образовывать химическое соединение – цементит.
14
vk.com/club152685050 | vk.com/id446425943
Практическое значение имеет часть диаграммы от железа до цементита (рис. 6), называется также диаграммой железо – цементит (Fе – Fe3C).
Фазы. Фаза – однородная часть системы, отделенная от других частей системы поверхностью раздела, при переходе через которую строение, состав и свойства изменяются скачкообразно. В системе железо – углерод различают следующие фазы: жидкий расплав, феррит, аустенит, цементит; рассмотрим подробнее.
а
б
Рис. 5. Кристаллические решетки:
а – феррита, б – аустенита.
1.Феррит – твердый раствор внедрения углерода
вα-железе (рис. 5,а).
5,а).
Атом углерода располагается в решетке феррита в центре грани куба, а также в вакансиях, на дислокациях и т.д. Феррит имеет переменную предельную растворимость углерода: при комнатной температуре (точка Q) – 0,006 %, максимальную – 0,02 %С при температуре 727oС (точка P). В высокотемпературном феррите максимальное содержание углерода (0,1%) наблюдается при температуре 1499°С (точка Н диаграммы).
Свойства феррита близки к свойствам железа. Он мягок и пластичен, магнитен до 768o С.
При 0,006 %С: в = 250 МПа, 0,2 = 120 МПа, = 50%, 80–100НВ.
2. Аустенит – твердый раствор углерода в – железе (рис. 5,б).
Атом углерода располагается в центре элементарной ячейки. Предельная растворимость углерода в -железе – 2,14% при температуре 1147 ºС (точка Е).
3. Цементит – химическое соединение железа с углеродом – карбид железа Fe3C.
Вцементите содержится 6,67% (концентрация углерода при изменении температуры остается неизменной, в отличие от твердых растворов). Имеет сложную ромбическую решетку. Цементит – неустойчивое химическое соединение и в определенных условиях распадается с образованием свободного углерода в виде графита.
Имеет сложную ромбическую решетку. Цементит – неустойчивое химическое соединение и в определенных условиях распадается с образованием свободного углерода в виде графита.
Цементит самая твердая и хрупкая составляющая железоуглеродистых сплавов (твердость ≈ 800 НВ, δ=0%).
Вжелезоуглеродистых сплавах присутствуют фазы: цементит первичный (ЦI), цементит вторичный (ЦII), цементит третичный (ЦIII). Химические и физические свойства этих фаз одинаковы. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
15
vk.com/club152685050 | vk.com/id446425943
4. Жидкий расплав. Углерод растворяется в железе в жидком состоянии, образуя однородный жидкий расплав.
Кристаллизация сплавов
ABCD – линия ликвидус, ниже которой происходит кристаллизация сплавов.
AHJECF – линия солидус, линия окончания кристаллизации.
При содержании углерода в сплаве менее 0,51% кристаллизация начинается с выделения -феррита; при 0,51 %С 4,3 с выделения аустенита; кристаллизация сплавов, содержащих 4,3 %С 6,67 начинается
свыделения из расплава кристалликов цементита первичного.
Всплавах, содержащих до 0,1% С, кристаллизация заканчивается при
температурах, соответствующих линии AH, с образованием -феррита. Сплавы, содержащие 0,1 %С 0,51 при температуре 1499 С
испытывают перитектическое превращение:
ЖB + ФН АJ
Линия HJB – линия перитектических превращений.
При содержании углерода от 0,1% до 0,16%, то есть между т. Н и т. J, недостаточно жидкости для реакции со всем имеющимся количеством феррита. Поэтому после окончания реакции остается избыточный феррит, который с понижением температуры вплоть до линии JN переходит в аустенит.
При содержании углерода от 0,16%, до 0,51%, то есть между т. J и В, количество феррита недостаточно для реакции со всем имеющимся количеством жидкости.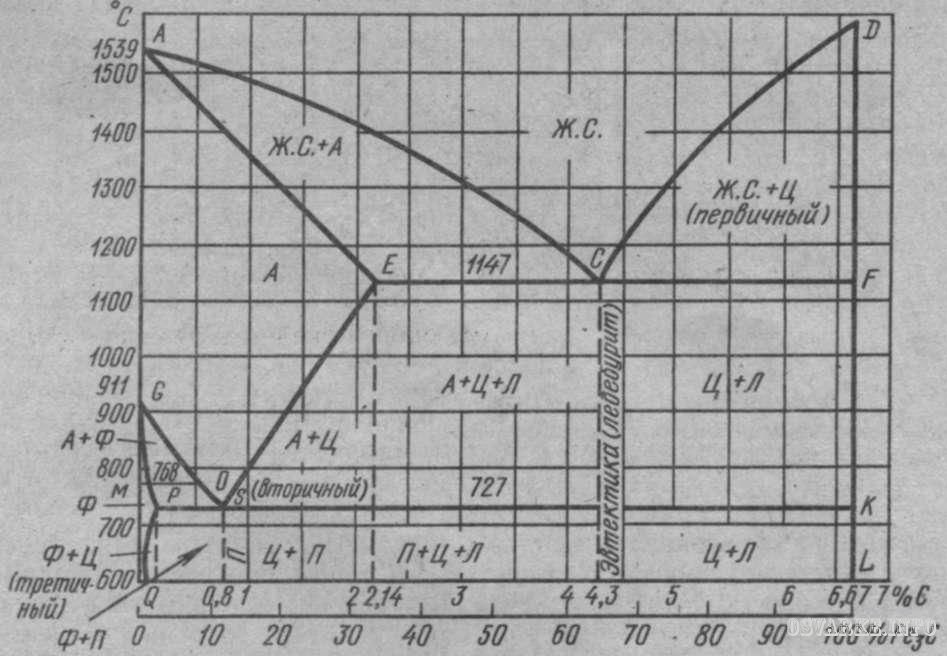 Поэтому после окончания реакции остается избыточная жидкость, которая с понижением температуры вплоть до линии солидус JE кристаллизуется в аустенит.
Поэтому после окончания реакции остается избыточная жидкость, которая с понижением температуры вплоть до линии солидус JE кристаллизуется в аустенит.
Сплавы, содержащие до 2,14%С, называются сталью, а более 2,14% С – чугуном. Принятое разграничение совпадает с предельной растворимостью углерода в аустените. Стали после затвердевания имеют аустенитную структуру, обладающую высокой пластичностью. Поэтому стали при повышенных температурах легко деформируются и в отличие от чугуна являются ковкими сплавами.
Особенность первичной кристаллизации сплавов, содержащих углерода более 2,14% заключается в том, что она заканчивается эвтектическим превращением при t = 1147 С:
ЖC АЕ+ЦF
Эвтектический сплав (4,3% С) затвердевает при постоянной температуре с образованием эвтектики – ледебурита – механической смеси аустенита и цементита.
16
vk.com/club152685050 | vk.com/id446425943
Рис. 6. Диаграмма состояния железо – углерод.
vk.com/club152685050 | vk.com/id446425943
В до- и заэвтектических чугунах первичная кристаллизация начинается с выделения избыточной фазы, соответственно аустенита или цементита.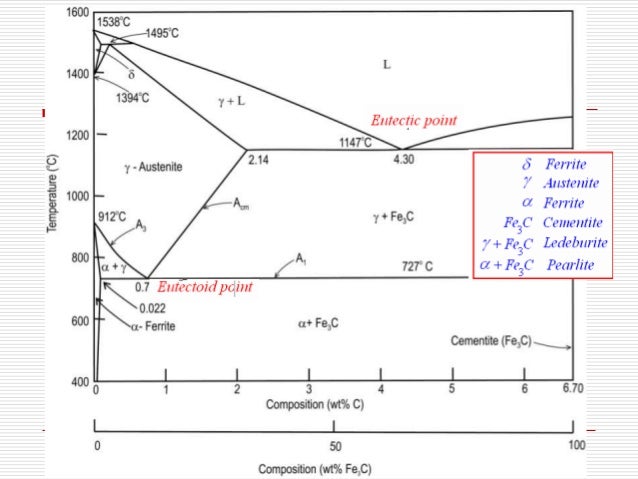
Ледебурит имеет сотовое (пластины цементита, проросшие разветвленными кристаллами аустенита) или пластинчатое (тонкие пластины цементита, разделенные аустенитом – образуется при быстром охлаждении) строение. Сотовое и пластинчатое строение нередко сочетается в одной колонии.
Ледебурит хрупок, тверд (700НВ) и плохо обрабатывается резанием.
По сравнению со сталями чугуны обладают значительно лучшими литейными свойствами (низкой температурой плавления, имеют меньшую усадку).
Фазовые и структурные изменения после затвердевания связаны с полиморфизмом железа, изменением растворимости углерода в
аустените и феррите с понижением температуры и эвтектоидным превращением.
В доэвтектоидных сплавах (%С 0,8%) ниже линии GOS -решетка аустенита перестраивается в -решетку, что и приводит к образованию феррита, линия GOS называется линией ферритных превращений. В температурной области PGS по границам зерен аустенита образуются зародыши феррита, они растут, поглощая зерна аустенита.
В температурной области PGS по границам зерен аустенита образуются зародыши феррита, они растут, поглощая зерна аустенита.
По мере выделения феррита состав аустенита изменяется по линии ферритных превращений, приближаясь к эвтектоидному. Этот состав достигается на линии PSK (727 ºС), где происходит эвтектоидное превращение. Эвтектоидное превращение заключается в распаде аустенита на механическую смесь феррита и цементита. Перлит – механическая смесь феррита и цементита. Линия PSK – линия эвтектоидных превращений.
АsФр+Цк
После окончательного охлаждения доэвтектоидные сплавы имеют структуру: феррит + перлит. Чем больше углерода, тем меньше феррита и больше перлита.
Сплавы с содержанием углерода менее 0,02% называются техническим железом. Ниже линии GP существует только феррит. С понижением температуры растворимость углерода в -железе уменьшается в соответствии с линией PQ – линией предельной растворимости углерода в – железе. Из феррита выделяется цементит третичный. Точка Р соответствует максимальной растворимости углерода в -железе – 0,02%.
Точка Р соответствует максимальной растворимости углерода в -железе – 0,02%.
Линия МО – линия магнитных превращений. Сталь при нагреве становится немагнитной, никаких структурных изменений при этом не происходит.
vk.com/club152685050 | vk.com/id446425943
В заэвтектоидных сталях (0,8 %С 2,14) вследствие уменьшения растворимости углерода в -железе с понижением температуры выделяется избыточная фаза – вторичный цементит. Превращение аустенита начинается в соответствии с линией ES – линией цементитных превращений (или предельной растворимости углерода в -железе).
По мере выделения цементита состав аустенита изменяется по линии ES, приближаясь к эвтектоидному. Этот состав достигается на линии PSK, где происходит эвтектоидное превращение аустенита в перлит.
После окончательного охлаждения заэвтектоидные сплавы имеют структуру: цементит + перлит.
Вэвтектоидной стали (0,8%С) весь аустенит переходит в перлит. Перлит чаще имеет пластинчатое строение, то есть состоит из чередующихся пластинок феррита и цементита. Толщина пластинок 7,3:1. После специальной обработки перлит может иметь зернистое строение.
Толщина пластинок 7,3:1. После специальной обработки перлит может иметь зернистое строение.
Перлит с пластинчатым цементитом обладает твердостью 200 – 230 НВ, пределом прочности 800 – 900 МПа, относительным удлинением 10%.
Вдоэвтектических чугунах ниже 1147 С происходит частичный распад аустенита – как первичных его кристаллов, выделившихся из жидкости, так и аустенита, входящего в состав ледебурита (вследствие уменьшения растворимости углерода в соответствии с линией SE).
При 727 С аустенит, обедненный углеродом до 0,8%, превращается в перлит. Таким образом, доэвтектические чугуны, после окончательного охлаждения имеют структуру перлит + цементит вторичный + ледебурит, где ледебурит – механическая смесь перлита и цементита. Эвтектический чугун состоит только из ледебурита (перлит + цементит). Заэвтектический чугун содержит углерода больше 4,3% и после затвердевания его структура – цементит + ледебурит.
Фазовый состав всех сплавов при температуре ниже 727 С одинаков; они состоят из феррита и цементита1. Однако свойства сталей и белых чугунов значительно различаются. Таким образом, основным фактором, определяющим свойства сплавов системы железо – цементит является их структура.
Однако свойства сталей и белых чугунов значительно различаются. Таким образом, основным фактором, определяющим свойства сплавов системы железо – цементит является их структура.
Построение кривых охлаждения При построении кривых охлаждения необходимо пользоваться правилом
фаз: с=k – f + 1,
где с – вариантность системы (число степеней свободы), k – число компонентов, f – число фаз.
Количество компонент в данной системе всегда равно 2 – это железо и углерод.
Количество фаз находят используя диаграмму (рис. 6).
1 Умножение содержания углерода на 15 дает содержание цементита в стали и чугуне, % по массе, а практически и по объему.
19
vk.com/club152685050 | vk.com/id446425943
Не следует путать фазы со структурными составляющими, так как последние могут быть однофазными и многофазными, а одна и та же фаза может входить в разные составляющие. Например, в доэвтектических чугунах при комнатной температуре цементит вторичный, цементит перлита и цементит ледебурита является одной и той же фазой. Структура этого чугуна – перлит + ледебурит + цементит, а фазовый состав – феррит + цементит. Рассуждения: перлит это двухфазная структурная составляющая, состоящая из феррита и цементита; ледебурит при комнатной температуре состоит из перлита и цементита, в свою очередь, перлит сам по себе тоже неоднороден и является смесью феррита и цементита; а структурная составляющая цементит – однофазна. Схематично эти рассуждения можно представить следующим образом:
Структура этого чугуна – перлит + ледебурит + цементит, а фазовый состав – феррит + цементит. Рассуждения: перлит это двухфазная структурная составляющая, состоящая из феррита и цементита; ледебурит при комнатной температуре состоит из перлита и цементита, в свою очередь, перлит сам по себе тоже неоднороден и является смесью феррита и цементита; а структурная составляющая цементит – однофазна. Схематично эти рассуждения можно представить следующим образом:
Зная количество фаз и количество компонент, можно определить число степеней свободы. На линиях эвтектического, эвтектоидного и перитектического превращений система Fе – Fе3С находится в трехфазном состоянии, которое согласно правилу фаз является для двухкомпонентных систем нонвариантной: C=2-3+1=0. Все превращения при С = 0 происходят при постоянных температурах, и на кривой охлаждения они характеризуются горизонтальным участком.
Вдвухфазных областях диаграммы системы являются моновариантным:
С= 2-2+1=1, в связи с чем превращения в сплавах в этих областях происходят в интервале температур. Выделение скрытой теплоты кристаллизации замедляет темп снижения температуры, поэтому участки кривых охлаждения в таких случаях будут пологими (с меньшим наклоном). Начало и конец превращений, когда изменяется вариантность системы, фиксируют на кривых охлаждения перегибами.
Выделение скрытой теплоты кристаллизации замедляет темп снижения температуры, поэтому участки кривых охлаждения в таких случаях будут пологими (с меньшим наклоном). Начало и конец превращений, когда изменяется вариантность системы, фиксируют на кривых охлаждения перегибами.
Воднофазных областях системы биварианты: C=2-1+1=2. При этом с изменением температуры никаких превращений не происходит, и на кривых охлаждения будут крутые участки (с большим наклоном).
Кривые охлаждения необходимо строить, начиная с жидкого состояния. На каждом участке кривой должны быть обозначены число степеней свободы (С = …) и структуру. На горизонтальных участках обозначают превращения, например, А→Ф+Ц.
На рис. 7 приведен пример построения кривой охлаждения заэвтектоидной стали содержащей 1,5%С.
Выше линии ликвидус сплав находится в жидком однофазном состоянии. В соответствии с правилом фаз (С=2-1+1=2, фаза – жидкий раствор) система в этой области бивариантна, фазовых превращений не
20
vk. com/club152685050 | vk.com/id446425943
com/club152685050 | vk.com/id446425943
происходит, и температура до точки 1 снижается достаточно интенсивно (крутой участок кривой охлаждения).
В точке 1 начинается процесс первичной кристаллизации, продолжающийся до точки 2, из жидкого раствора выпадают кристаллы аустенита. По мере охлаждения сплава от точки 1 до точки 2 концентрация компонентов в аустените изменяется согласно линии JЕ от точки J к точке 2, а в жидкости – согласно линии BC от точки 1 к точке 2 (рис. 3). Составы и количества фаз определяют по правилу отрезков. Например, в точке m состав жидкой фазы найдем проекцией точки n на ось концентраций, а состав твердой фазы – проекцией точки k.
2΄
Рис. 7. Диаграмма состояния Fe – C и кривая охлаждения для стали, содержащей 1,5%С.
Количество фаз определяют из соотношения отрезков:
Q |
|
| km | 100 %; | Q |
|
| mn | 100 % | |
ж | kn | тв | kn | |||||||
|
|
|
|
|
|
Процесс первичной кристаллизации в данном случае идет при понижении температуры, что согласуется с правилом фаз (С=2-2+1=1; фазы – жидкий раствор и аустенит). Таким образом, система в этой области моновариантна, в процессе превращения выделяется скрытая теплота кристаллизации, замедляющая снижение температуры, поэтому участок кривой охлаждения будет пологим. Первичная кристаллизация сплава заканчивается в точке 2.
Таким образом, система в этой области моновариантна, в процессе превращения выделяется скрытая теплота кристаллизации, замедляющая снижение температуры, поэтому участок кривой охлаждения будет пологим. Первичная кристаллизация сплава заканчивается в точке 2.
В интервале между точками 2 и 3 сплав охлаждается, не претерпевая никаких превращений. Система при этом бивариантна (C=2-1+1=2; фаза – аустенит), участок кривой охлаждения будет крутым.
При температуре, соответствующей точке 3, достигается предел насыщения аустенита углеродом. Ниже этой точки аустенит становится перенасыщенным. Избыточный углерод из зерен аустенита диффундирует к их границам и здесь выделяется в виде вторичного цементита. Процесс кристаллизации вторичного цементита, в соответствии с правилом фаз, протекает с понижением температуры сплава (С=2-2+1=1; фазы – аустенит и
21
vk.com/club152685050 | vk.com/id446425943
цементит). Таким образом, система моновариантна, выделяющаяся скрытая теплота кристаллизации замедляет снижение температуры, и участок кривой охлаждения будет пологим. Концентрация углерода в аустените при этом изменяется согласно линии ES от точки 3 к точке S и достигает эвтектоидной (0,8%С) при температуре 727 С (точка 4). При этой температуре и концентрации аустенит превращается в перлит (эвтектоидное превращение):
Концентрация углерода в аустените при этом изменяется согласно линии ES от точки 3 к точке S и достигает эвтектоидной (0,8%С) при температуре 727 С (точка 4). При этой температуре и концентрации аустенит превращается в перлит (эвтектоидное превращение):
Аs Фр+Цк
Согласно правилу фаз при эвтектоидном превращении система нонвариантна (С=2-3+1=0; фазы – аустенит, цементит, феррит), процесс идет при постоянной температуре, и на кривой охлаждения будет горизонтальный участок.
Ниже температуры 727°С в рассматриваемом сплаве практически не происходит превращений. По теоретическим данным, из феррита здесь выделяется третичный цементит, вследствие чего система будет моновариантной (С=2-2+1=1; фазы – феррит и цементит). Но феррит здесь содержится только в составе перлита, третичный цементит выделяется в незначительном количестве и металлографически не обнаруживается, так как сливается с цементитом перлита. Таким образом, в структуре стали данного состава при комнатной температуре наблюдаются зерна перлита, окаймленные тонкой сеткой вторичного цементита.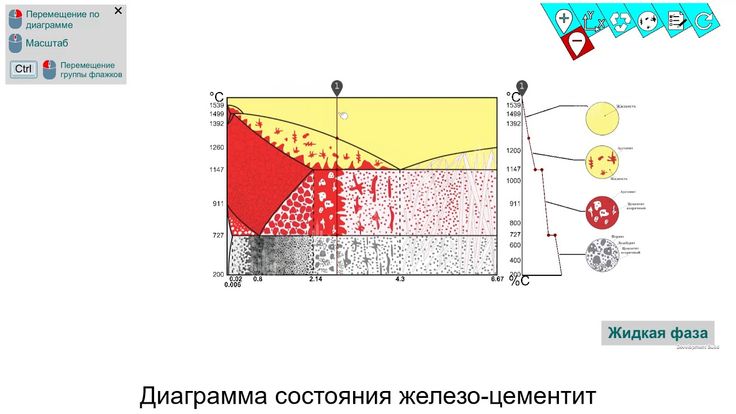
Превращения в сплавах в процессе нагрева происходят в обратной последовательности при некотором их перегреве выше температур равновесного состояния.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1.Как взаимодействует углерод с железом?
2.Какое максимальное процентное содержание углерода может быть в α-, γ-, δ-железе?
3.Укажите линии и точки диаграммы, приведите их названия.
4.Что представляет собой каждая из структурных составляющих: аустенит, феррит, цементит, перлит, ледебурит?
5.Что представляет собой перитектическое превращение?
6.Что представляет собой эвтектическое превращение и как оно протекает?
7.Что представляет собой эвтектоидное превращение и как оно протекает?
8.Какие фазы присутствует на линии PSK и каковы их составы? Какова вариантность системы на этой линии?
9.Какой цементит называется первичным, вторичным, третичным?
10.В чем причина выделения вторичного и третичного цементита по мере понижения температуры?
11.Расскажите и покажите, как определяется концентрация углерода в аустените при различных температурах в заэвтектоидных сталях и доэвтевктических чугунах.
12.Какое изменение происходит в ледебурите на линии РSК?
13.В чем причина выделения феррита в доэвтектоидных сталях ниже линии
GS?
22
vk.com/club152685050 | vk.com/id446425943
14.Какие фазы присутствуют в доэвтектических чугунах при комнатной температуре и какова при этом вариантность системы?
23
Основные определения и обозначения диаграммы железо цементит
Железо – металл переходной группы серебристо-серого цвета, с плотностью 7,8 т/м3, температурой плавления 1539 °С. При изменении температуры изменяется строение кристаллической решетки железа (Feδ(C)-1539…1392 °С, Feγ-1392…911 °С, Feα -911…768 °С, Feα- менее 768 °С).
Углерод – неметаллический элемент с плотностью 2,5 т/м3, температурой плавления 2500 °С. Углерод имеет две аллотропические формы: графита и алмаза.
Аустенит (А) — твердый раствор внедрения углерода в γ-железе; предельная растворимость углерода в γ-железе – 2,14% (σв=600 МПа, δ=30%, НВ 1800…2000).
Ледебурит (Л) — структурная составляющая (эвтектика) железоуглеродистых сплавов, главным образом чугунов, представляющая собой механическую смесь кристаллов аустенита и цементита, образующихся в сплавах, содержащих от 2,0 до 6,67% углерода (σв=1000 МПа, δ=1…2%, НВ4 500…5000).
Перлит (П) — структурная составляющая (эвтектоид) железоуглеродистых сплавов, представляющая собой механическую смесь чередующихся пластинок феррита и цементита, образующихся при распаде аустенита во всех сплавах системы с концентрацией углерода более 0,02% при t = 727°С (σв=600 МПа, δ=20%, НВ 2000).
Сталь — железоуглеродистый сплав, содержащий 0,02 – 2,14% углерода. По содержанию углерода и наличию структурных составляющих различают: доэвтектоидные (углерода 0,02 – 0,83%), эвтектоидные (углерода 0,83%), заэвтектоидные (углерода 0,83 – 2,14%) стали.
Феррит (Ф) — твердый раствор внедрения углерода в α-железе. Различают низкотемпературный α-феррит с растворимостью углерода до 0,02 % и высокотемпературный α-феррит с предельной растворимостью углерода 0,1% (σв=300 МПа, δ=40%, НВ800…1000).
Цементит Fe3C (Ц) — химическое соединение железа с углеродом (карбид железа) с концентрацией углерода 6,67% (σв = 20000 МПа, δ=0%, НВ8000).
Чугун — железоуглеродистый сплав, содержащий более 2,14% углерода. По содержанию углерода и наличию структурных составляющих различают чугуны: доэвтектические (углерода 2,14 – 4,3%), эвтектические (углерода 4,3%) и заэвтектические чугуны (углерода 4,3 – 6,67%).
Чугуны белые — чугуны, кристаллизующиеся подобно углеродистым сталям по метастабильной диаграмме состояния Fe – Fe3C (углерод находится в химически связанном состоянии в виде цементита; имеет белый блестящий излом).
Основными компонентами сталей и чугунов являются железо и углерод. Углерод может находиться в равновесии с жидкой фазой и с твердыми растворами на основе железа в виде цементита (метастабильное равновесие) или графита (стабильное равновесие) в зависимости от внешних условий. Это обстоятельство определяет два варианта диаграммы состояния «железо — углерод» (рисунок 1). Большее практическое значение имеет метастабильная диаграмма состояния. С помощью этой диаграммы объясняют не только превращения, происходящие в сталях и белых чугунах. Она является основой для выбора оптимальных режимов термообработки железоуглеродистых сплавов.
Большее практическое значение имеет метастабильная диаграмма состояния. С помощью этой диаграммы объясняют не только превращения, происходящие в сталях и белых чугунах. Она является основой для выбора оптимальных режимов термообработки железоуглеродистых сплавов.
Наряду с основными компонентами в этих сплавах имеются постоянные технологические примеси, которые могут оказывать существенное влияние на их свойства и формирование структуры.
В системе Fe — Fe3C различают следующие фазы: жидкий раствор, твердые растворы — феррит и аустенит, а также цементит (в том числе первичный, вторичный и третичный).
Рисунок 1 – Диаграмма состояния железо-цементит.
К структурным составляющим в системе Fe — Fe3C, наряду с перечисленными выше фазами, относятся ледебурит и перлит.
Составы и количества фаз в системе «железо-цементит» можно определить с помощью правили отрезков. Правилом отрезков, или правилом рычага, пользуются для определения процентного и весового состава жидкой и твердой фаз или двух различных твердых фаз (количество структурных составляющих и их концентраций). Для этого, например, из точки b (рисунок 2) проводят горизонталь до линий GP и GS. Проекция точки a на ось концентраций показывает содержание углерода в феррите, а содержание точки с — содержание углерода в аустените при определенной температуре. Для определения количественного соотношения аустенита и феррита необходимо составить обратно пропорциональное отношение отрезков: Qф/Qау=bc/ab, где Qф — количество феррита; Qay — количество аустенита для температуры, соответствующей точке b. Пусть в точке b масса всего сплава составляет 100 г, тогда Qф/(100 — Qф)=bc/ab. Подставляя значения отрезков bс и ab, взятые из диаграммы состояния, можно определить количество феррита, а затем и количество аустенита.
Для этого, например, из точки b (рисунок 2) проводят горизонталь до линий GP и GS. Проекция точки a на ось концентраций показывает содержание углерода в феррите, а содержание точки с — содержание углерода в аустените при определенной температуре. Для определения количественного соотношения аустенита и феррита необходимо составить обратно пропорциональное отношение отрезков: Qф/Qау=bc/ab, где Qф — количество феррита; Qay — количество аустенита для температуры, соответствующей точке b. Пусть в точке b масса всего сплава составляет 100 г, тогда Qф/(100 — Qф)=bc/ab. Подставляя значения отрезков bс и ab, взятые из диаграммы состояния, можно определить количество феррита, а затем и количество аустенита.
Рисунок 2 – Схема применения правила отрезков
Читайте также: Построение кривых охлаждения сплавов Железо-Цементит
заказ решения заданий по материаловедению.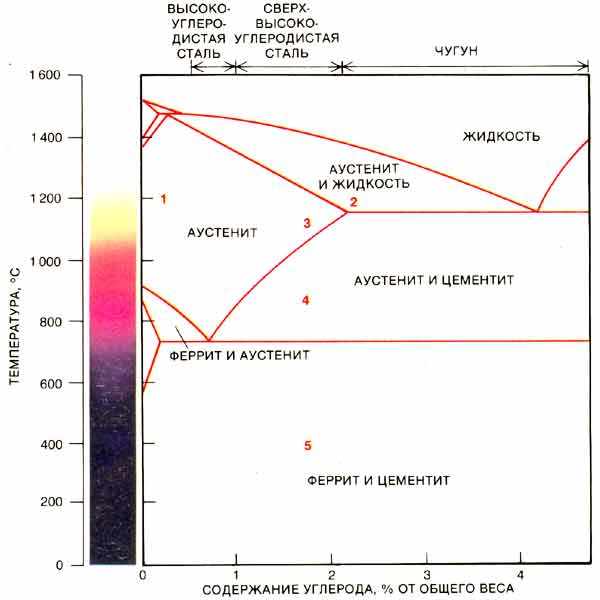 Решение предоставляется в печатном виде (в Word) с детальными комментариями. Решение предоставляется в печатном виде (в Word) с детальными комментариями. |
Диаграмма состояния “железо – углерод”
Диаграмма состояния железо-углерод (цементит) — это графическое отображение фазового состава и структуры сплавов в зависимости от концентрации углерода и температуры
- Жидкая фаза
- Перлит
Компоненты в системе «железо-углерод»
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит:
Железо
Железо – d-переходный металл серебристо-светлого цвета. Температура плавления – 1539° С. Удельный вес равен 7,86 г/см3. Наиболее существенной особенностью железа является его полиморфизм. В твердом состоянии железо может находиться в двух модификациях — α и γ. Полиморфные превращения происходят при температурах 911° С и 1392° С. При температуре ниже 911° С и выше 1392° С существует Feα (или α-Fе) с объемно-центрированной кубической решеткой. В интервале температур 911…1392° С устойчивым является Feγ (или γ-Fе) с гранецентрированной кубической решеткой. При превращении α→γ наблюдается уменьшение объема, так как решетка γ-Fе имеет более плотную упаковку атомов, чем решетка α-Fе. При охлаждении во время превращения γ→α наблюдается увеличение объема. В интервале температур 1392…1539° С высокотемпературное Feα называют Feδ. Высокотемпературная модификация Feα не представляет собой новой аллотропической формы.
Наиболее существенной особенностью железа является его полиморфизм. В твердом состоянии железо может находиться в двух модификациях — α и γ. Полиморфные превращения происходят при температурах 911° С и 1392° С. При температуре ниже 911° С и выше 1392° С существует Feα (или α-Fе) с объемно-центрированной кубической решеткой. В интервале температур 911…1392° С устойчивым является Feγ (или γ-Fе) с гранецентрированной кубической решеткой. При превращении α→γ наблюдается уменьшение объема, так как решетка γ-Fе имеет более плотную упаковку атомов, чем решетка α-Fе. При охлаждении во время превращения γ→α наблюдается увеличение объема. В интервале температур 1392…1539° С высокотемпературное Feα называют Feδ. Высокотемпературная модификация Feα не представляет собой новой аллотропической формы.
При температуре ниже 768° С железо ферромагнитно, а выше – парамагнитно. Точку 768° С, соответствующую магнитному превращению, т.е. переходу из ферромагнитного состояния в парамагнитное называют точкой Кюри.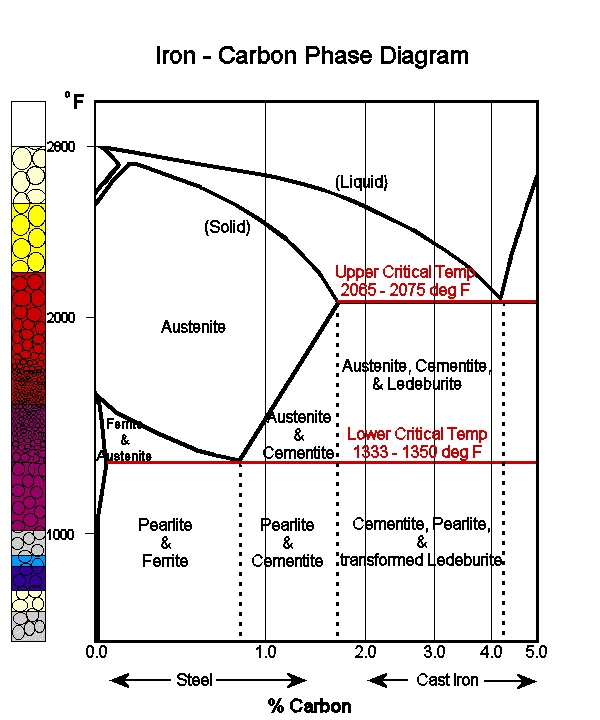 Модификация Feγ парамагнитна.
Модификация Feγ парамагнитна.
Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (временное сопротивление – σв=250 МПа, предел текучести – σт=120 МПа) и высокими характеристиками пластичности (относительное удлинение – δ=50 %, а относительное сужение – ψ=80 %). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна. Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.
Углерод
Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500° С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000° С).
В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
Цементит
Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Более точные исследования показали, что цементит может иметь переменную концентрацию углерода. Однако в дальнейшем, при разборе диаграммы состояния, сделаем допущение, что Fе3С имеет постоянный состав. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260° С. Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу. При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 210° С. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: например, азотом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Если графит является стабильной фазой, то цементит – это метастабильная фаза. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
Влияние химических элементов на свойства железоуглеродистых сплавов
Железоуглеродистый сплав кроме железа и углерода (постоянных компонентов) содержит полезные, вредные и постоянные (технологические) примеси, которые оказывают различные влияния на свойства конструкционных материалов.
Углерод в железоуглеродистом сплаве может находиться в виде карбида железа Fe3C (цементита) либо в виде графита.
Углерод является основным сплавляемым компонентом, который специально вводят для увеличения прочности, твердости и улучшения технологических и эксплуатационных свойств конструкционных материалов. Влияние углерода на свойства конструкционных материалов зависит от состояния или взаимодействия его с железом, т. е. от образования той или иной структуры железоуглеродистого сплава.
Если при взаимодействии углерода с железом образуется цементит, то сплав будет иметь высокие твердость, хрупкость и практически не будет поддаваться обработке резанием.
Если углерод, взаимодействуя с железом, образует структуры механических смесей (перлита или феррита), то сплав будет иметь высокие механические и технологические свойства.
Кремний и марганец в железоуглеродистых сплавах являются полезными примесями. Кремний в сплав попадает частично из руды, а основная масса — в процессе плавки при раскислении сплава.
Раскисление — это процесс удаления вредных включений оксида железа (FeO) путем введения раскислителей (марганца, кремния и различных ферросплавов). Раскислители, соединяясь с оксидом железа, образуют шлаки, которые подлежат удалению. Незначительная часть раскислителей остается в железоуглеродистом сплаве. Как правило, раскислению подлежит большинство сталей и чугунов.
Кремний полностью растворяется в основной структуре сплава с образованием твердого раствора, повышает предел текучести, уменьшает хрупкость. Высокое содержание кремния (1 … 2 %) придает стали упругость. Кроме того, кремний способствует преобразованию углерода из структуры цементита в свободный углерод в виде графита, уменьшая при этом твердость и хрупкость сплавов. Марганец попадает в сплав при переработке марганцевых руд, а также в процессе раскисления.
Марганец образует с железом твердый раствор, а также способствует образованию химического соединения, поэтому он повышает твердость, износостойкость, прочность. Высокое содержание марганца способствует образованию цементита, что приводит к повышению твердости и хрупкости сплава. Кроме того, марганец нейтрализует вредное влияние серы.
Высокое содержание марганца способствует образованию цементита, что приводит к повышению твердости и хрупкости сплава. Кроме того, марганец нейтрализует вредное влияние серы.
Сера и фосфор в железоуглеродистых сплавах являются вредными примесями.
Фосфор попадает в сплав из руды. Исходный чугун, как правило, имеет высокую массовую долю фосфора. Фосфор ограниченно растворяется в железе, а его избыточное содержание приводит к образованию фосфида железа — очень хрупкого соединения. Фосфор, растворяясь в железе, резко снижает его плотность и приводит к хрупкости в холодном состоянии. Это свойство называется хладноломкостью сплавов. Фосфор также приводит к повышению твердости и уменьшению прочности. Марганец, взаимодействуя с фосфором в процессе раскисления, удаляет его с образованием шлаков.
В отдельных случаях фосфор может быть полезен, так как улучшает обрабатываемость резанием, жидкотекучесть, а при наличии незначительного количества меди повышает коррозионную стойкость.
Сера попадает в сплав из руд, а также из топлива в процессе его горения. Не растворяясь в железе, сера образует с ним легкоплавкую и очень хрупкую механическую смесь (эвтектику) и делает сплав хрупким в районе температур красного каления (это свойство получило название красноломкости), поэтому железоуглеродистые сплавы с высоким содержанием серы не подвергаются горячей обработке давлением.
При высоком содержании в сплаве углерода наличие серы повышает его твердость и хрупкость, ухудшает литейные свойства, снижает жидкотекучесть, увеличивает усадку металла при охлаждении отливок и склонность к образованию микротрещин. Вредное влияние серы нейтрализуется марганцем. При введении в сплав незначительной массовой доли марганца образуется соединение с серой — сульфид марганца (MnS) вместо легкоплавкого сульфида железа (FeS). Сульфид марганца частично удаляется вместе со шлаком.
В железоуглеродистых сплавах могут находиться с очень низкой массовой долей различные газы: азот, водород и кислород. Эти химические элементы являются скрытыми примесями. Из-за сложности их химического анализа массовую долю этих элементов не определяют и в технических условиях не нормируют.
Эти химические элементы являются скрытыми примесями. Из-за сложности их химического анализа массовую долю этих элементов не определяют и в технических условиях не нормируют.
Кроме того, в незначительных количествах встречаются различные металлы (олово, цинк, сурьма, свинец, никель, медь, хром и др.) — случайные примеси. Эти группы металлов попадают как из руд, так и из перерабатываемого при металлургическом процессе стального лома.
Все перечисленные случайные примеси являются неизбежным следствием технологического процесса, т. е. специально не добавляются. В связи с этим получаемые стали с незначительной массовой долей никеля, меди, хрома и других металлов не рассматривают как легированные стали.
Кроме естественных, постоянных, скрытых и случайных химических элементов в железоуглеродистый сплав (особенно в сталь) вводят специальные химические элементы с целью изменения микроструктуры сплава, физико-химических и других свойств.
Специально вводимые в железоуглеродистый сплав химические элементы называют легирующими элементами, а сплавы, полученные на их основе, — легированными сплавами (сталями и чугунами).
В качестве легирующих элементов вводят алюминий, ванадий, вольфрам, молибден, медь, кобальт, кремний, никель, тантал, титан, хром и др.
Государственные стандарты строго регламентируют массовую долю полезных и вредных примесей в железоуглеродистых сплавах.
В сталях, как правило, содержание этих элементов, %, ограничивается следующими верхними пределами:
Марганец ………………………………………………………………………………… 0,8
Кремний ………………………………………………………………………………….. 0,5
Фосфор …………………………………………………………………………………… 0,05
Сера ………………………………………………………………………………………… 0,05
В чугунах по государственным стандартам допускается более высокая массовая доля, %, полезных и вредных примесей (в зависимости от групп и марок):
Марганец ……………………………………………………………………… 0,3 … 1,5
Кремний ………………………………………………………………………… 0,3 … 5,0
Фосфор …………………………………………………………………………. 0,20… 0,65
Сера ………………………………………………………………………………. 0,08 … 0,12
Фазы в системе «железо-углерод»
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Жидкая фаза
Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
Феррит
Феррит (Ф, α)- твердый раствор внедрения углерода в α-железе (от латинского слова ferrum – железо). Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727° С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539° С) с предельной растворимостью углерода 0,1 % при температуре 1499° С (точка J).
Свойства феррита близки к свойствам железа. Он мягок (твердость – 80 — 130 НВ, временное сопротивление – σв=300 МПа) и пластичен (относительное удлинение — δ=50 %), магнитен до 768° С.
Под микроскопом феррит выглядит как светлые полиэдрические зерна. В сталях может существовать в виде сетки (разной толщины, в зависимости от содержания углерода), зерен (малоуглеродистые стали), пластин или игл (видманштетт).
Аустенит в сталях
Аустенит (А, γ) – твердый раствор внедрения углерода в γ–железо (по имени английского ученого Р. Аустена). Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ -железе 2,14 % при температуре 1147° С (точка Е). Аустенит имеет твердость 180 НВ, пластичен (относительное удлинение – δ=40…50 %), парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования. Под микроскопом выглядит как светлые полиэдрические зерна с двойниками.
Аустена). Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ -железе 2,14 % при температуре 1147° С (точка Е). Аустенит имеет твердость 180 НВ, пластичен (относительное удлинение – δ=40…50 %), парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования. Под микроскопом выглядит как светлые полиэдрические зерна с двойниками.
Цементит – формы существования
В железоуглеродистых сплавах присутствуют фазы: цементит первичный, цементит вторичный, цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
Поскольку углерод в сплавах с железом встречается в виде цементита и графита, существуют две диаграммы состояния, описывающие условия равновесия фаз в системах железо — цементит и железо — графит. Первая диаграмма (Fе — Fе3С) называется цементитной (метастабильная), вторая (Fе — С) — графитной (стабильная). Оба варианта диаграммы приводятся вместе в одной системе координат: температура — содержание углерода. Диаграмма состояния системы железо — углерод построена по результатам многочисленных исследований, проведенных учеными ряда стран. Особое место среди них занимают работы Д.К. Чернова. Он открыл существование критических точек в стали, определил их зависимость от содержания углерода, заложил основы для построения диаграммы состояния железоуглеродистых сплавов в ее нижней, наиболее важной части.
Буквенное обозначение узловых точек в диаграмме является общепринятым как в России, так и за рубежом.
Диаграмма состояния железо-углерод
Имеющиеся во всех областях диаграммы фазы видны на рисунке. Значение всех линий указано в таблице.
Значение всех линий указано в таблице.
Ликвидус по всей диаграмме проходит по линиям АВ, ВС, СD; солидус — по линиям АН, НJ, JЕ, ЕСF. Сплавы железа с углеродом обычно делят на стали и чугуны. Условной границей для такого деления является 2,14 % С (точка E). Сплавы, содержащие углерода менее 2,14 %, относятся к сталям, более 2,14 % — к чугунам.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, имеют условные обозначения. Обозначаются буквой А. В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс с (от слова chauffage – нагрев) при нагреве и индекс r (от слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
Таким образом, например, нагрев доэвтектоидной стали выше соответствующей точки на линии GS обозначается как нагрев выше точки АС3. При охлаждении же этой стали первое превращение должно быть обозначено как Аr3, второе (на линии РSК) — как Аr1.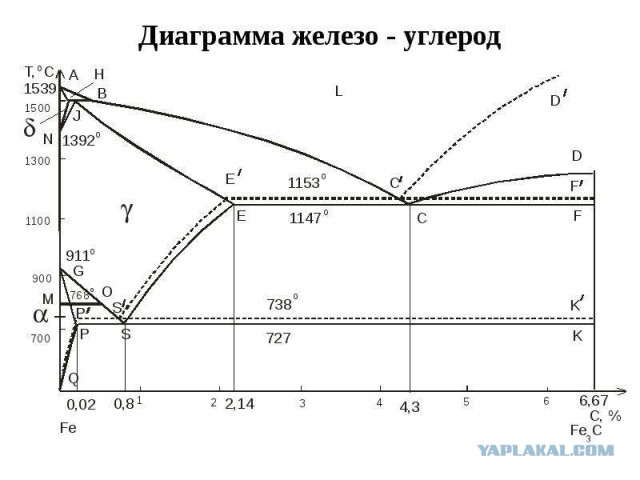
Химические соединения
Основные структуры, составляющие железоуглеродистых сплавов:
Феррит представляет собой твердый раствор углерода в α-Fe. При температуре 723°C максимальное содержание углерода составляет 0.02%.It не вытравит если никакие примеси.
Цементит-соединение, содержащее углерод железа fe3c-6,67% карбида углерода. Эвтектика является неотъемлемой частью смеси и самостоятельным структурным компонентом. За счет замещения атомами других металлов может образовываться твердый раствор, который неустойчив и разлагается при термической обработке. Цементит очень твердых(НВ 800) и хрупок.
Аустенит представляет собой твердый раствор углерода в γ-Fe. Атомы углерода вводятся в кристаллическую решетку, и степень насыщения может варьироваться в зависимости от температуры и impurities. It устойчив только при высоких температурах, а стабилен даже при нормальных низких температурах-примеси Mn, Cr. Аустенитная твердость HB 170… 220.
Микроструктура:
- а-гиперэвтектоидная сталь-феррит (светлая область) и перлит (темная область) с увеличением 500X, б-эвтектоидная сталь-перлит (1000′), в-эвтектоидная сталь-зацепляющийся перлит и цементит (200’).
 )
) - Растворимость углерода в феррите снижается с 727% при 0,02°с до 0,005% при комнатной температуре.
Другие структурные составляющие в системе «железо-углерод»
Кроме компонентов и фаз в системе сплавов «железо-углерод» присутствуют другие структурные составляющие — перлит и ледебурит
Перлит
Перлит — эвтектоид, механическая смесь феррита и цементита, полученная в результате распада аустенита при охлаждении сплавов ниже 727° С. При медленном охлаждении перлит присутствует во всех сплавах с концентрацией углерода от 0,02 до 6,67%. Под микроскопом перлит может выглядеть либо как пластины, либо как зерна — зернистый перлит. Его вид, также как и механические свойства, зависит от скорости охлаждения сплава и вида его термической обработки
Ледебурит в сталях
Ледебурит — эвтектика, механическая смесь аустенита и цементита, выделяющаяся из жидкости при охлаждении сплавов ниже 1147° С. Принципиальное отличие эвтектикой составляющей от эвтектоидной заключается в том, что первая выделяется из жидкости, а вторая из твердого раствора, в случае железоуглеродистых сплавов — из аустенита. Название данная структурная составляющая получила в честь имени немецкого ученого-металлурга Ледебура.
Название данная структурная составляющая получила в честь имени немецкого ученого-металлурга Ледебура.
Сплавы железа с углеродом
Железоуглеродистые сплавы могут содержать следующие структурные компоненты:
- Феррит (F) представляет собой твердый раствор, содержащий углерод и другие элементы в iron. It имеет объемно-центрированную кубическую решетку. Растворимость углерода в феррите очень мала, до 0,005% при комнатной температуре. При 727°C, самая высокая растворимость 0,02% феррита очень пластична, мягка и обрабатывается путем приложения давления в холодных условиях.
Аустенит (а) представляет собой твердый раствор углерода и других элементов G-iron. It присутствует только при высоких температурах. максимальная растворимость углерода в г-железе составляет 1147% при температуре 2,14°С и 727 ° с при 0,8%.Эта температура является нижним пределом присутствия аустенита в железоуглеродистом сплаве. Аустенит очень пластичен, но тверже феррита.
Значение линий диаграммы состояния системы железо-углерод
Значения линий на диаграмме железо-углерод
Всякая диаграмма состояния показывает условия равновесного сосуществования фаз во взятой системе компонентов.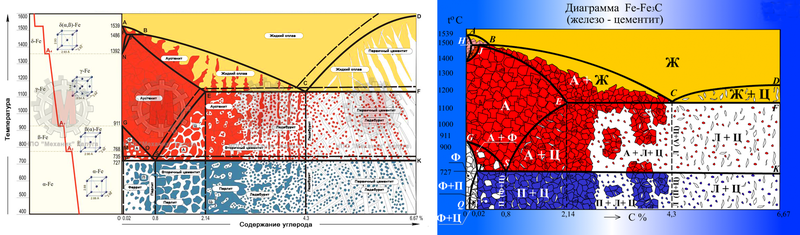
Полное физико-химическое равновесие между фазами может быть достигнуто только в специальных лабораторных условиях, а на практике некоторым приближением к этому состоянию может быть случай чрезвычайно медленного охлаждения или нагрева сплава с весьма длительными выдержками во времени при любых искомых температурах.
Сложный эфир уксусной кислоты — https://www.dcpt.ru
Диаграмма состояния системы железо-углерод – Технарь
Механические смеси состоят из нескольких компонентов, которые при затвердевании (кристаллизации) не взаимодействуют друг с другом. Каждая из фаз сохраняет свою кристаллическую решетку. Например, у сталей могут одновременно быть смеси феррита и аустенита, или перлита и цементита. Диаграммы состояния строятся на основе кривых нагрева и охлаждения. Рассмотрим сплав (рис. 1.25) медь- никель (Cu — Ni). Атомы Cu и Ni могут соединяться в любых пропорциях (0…100%), образуя твердый раствор, при этом атомы Ni могут замещать в кристаллической решетке Cu все атомы. По горизонтальной оси откладывается содержание компонентов в твердом растворе, а по вертикальной- температура. Точка 1083 °C показывает температуру плавления меди, а точка 1452 °C –никеля. Нижняя линия (солидус) –это граница твердого раствора. Ниже ее оба металла и смесь находятся в твердом состоянии (в кристаллическом виде). Выше верхней линии (ликвидуса) располагается область жидкого раствора обоих этих металлов и сплавов. В «чечевице» , очерченной нижней и верхней линиями , лежит область смеси кристаллов и более тугоплавкового металла с капельками более легкоплавкого.
По горизонтальной оси откладывается содержание компонентов в твердом растворе, а по вертикальной- температура. Точка 1083 °C показывает температуру плавления меди, а точка 1452 °C –никеля. Нижняя линия (солидус) –это граница твердого раствора. Ниже ее оба металла и смесь находятся в твердом состоянии (в кристаллическом виде). Выше верхней линии (ликвидуса) располагается область жидкого раствора обоих этих металлов и сплавов. В «чечевице» , очерченной нижней и верхней линиями , лежит область смеси кристаллов и более тугоплавкового металла с капельками более легкоплавкого.
В правой части рисунка 1.25 находятся кривые нагрева и охлаждения смеси (в данном случае представлена 50 % смесь) этих металлов. На основании таких кривых, полученных для различных смесей в интервале 0…100% и построена диаграмма состояний. На кривых нагрева и охлаждения видны горизонтальные линии: при разрушении кристаллов тепло подводится , но повышения температуры нет, т.к. это тепло расходуется на разрушение кристаллов; при кристаллизации, наоборот, выделяется тепло, поэтому температура сплава по времени не снижается.
Для компонентов (пример для смеси свинец–сурьма), неограниченно растворимых в жидком состоянии и совершенно нерастворимых в твердом состоянии, с образованием механической смеси (эвтектики), диаграмма представлена на рис. 1.26.
На первом участке диаграммы ниже линии температур 327…243 °C кристаллизуется свинец, а далее на участке температур 243…631 °C — сурьма. В точке С кристаллизуется свинец и сурьма, и жидкость без промежуточных фаз переходит в твердое состояние. Эта смесь называется эвтектикой. До нее будет доэвтектический сплав (Рb + Э), а после заэвтектический сплав (Sb + Э). В точке С самая низкая температура плавления ( 243 °C ) сплава.
Имеется связь характера диаграмм состояний со свойствами (электропроводность, твердость, прочность и т. д.). Так для первой группы сплавов –твердых растворов, с ростом концентрации компонента (например, Ni на рис. 1.25) механические свойства (твердость, прочность) увеличиваются, а для второй группы имеется точка экстремума, т. е. сначала механические характеристики повышаются, а далее снижаются.
е. сначала механические характеристики повышаются, а далее снижаются.
Структурные составляющие железо — углеродистых сплавов представлены в виде твердых растворов (рис. 1. 27) ( феррит и аустенит), химического соединения (цементит) и механических смесей (перлит, ледобурит,…).
Феррит это твердый раствор внедрение углерода в a—железо. Он очень мягкий и пластичный, хорошо проводит тепло и электричество, сильно магнитен. Углерода в нем очень мало ( около 0,002 % ). В микроструктурах металла цементит имеет белый цвет. Углерод замещает центральный атом объемно — центрированной кубической решетки (a — железо) или вакансии кристаллической решетки.
Фазовые превращения (рис. 1.28) происходят по мере изменения температуры. При нагреве до 768 °С a — железо теряет свои магнитные свойства, но кристаллическая решетка не меняется.
При 898 °С – эта решетка превращается в гранецентрированную кубическую решетку, называемую g — железом. Аустенит это твердый раствор внедрения углерода в y –железо. Он не магнитен, сравнительно мягкий, углерода содержится в нем максимально до 2 %.
Аустенит это твердый раствор внедрения углерода в y –железо. Он не магнитен, сравнительно мягкий, углерода содержится в нем максимально до 2 %.
При 1401 °С g — железо превращается в s — железо с объемно — центрированной решеткой, существующей до температуры плавления железа (1539 °С ).
Цементит — это химическое соединение (карбид железа Fe3C), содержащее 6,67 % углерода и имеющее высокую твердость и хрупкость, плохо проводящее электрический ток и тепло. Цементная сетка является светлой на микроструктурах сплава. Цементит является неустойчивым химическим соединением и при высоких температурах происходит его распад на железо и углерод:
Fe3 C ® Fe + C.
Ледебурит—это механическая смесь ( эвтектика ), состоящая из аустенита и цементита и содержащая 4,3 % углерода , образуется при температурах ниже 1147 °С, имеет высокую твердость и хрупкость.
Перлит – механическая смесь (эвтектоид), состоящая из тонких пластинок или зерен цементита и феррита, образуется в результате распада аустенита при температурах ниже 727 °С. Углерода в перлите 0,8 %.
Углерода в перлите 0,8 %.
На основе кривых охлаждения и нагрева сплавов Fe-C строится диаграмма состояний системы железо-углерод. На ней имеются линии: ликвидуса–АСД; солидуса — AECF. Выше линии ликвидуса металл находится в жидком состоянии, а ниже линии солидуса в твердом (кристаллическом) состоянии. Остальные линии отражают превращения в сплавах, происходящие после затвердевания. Ниже линии солидуса, при дальнейшем снижении температуры происходят структурные изменения, т.е. перекристаллизация уже в твердом состоянии (вторичная кристаллизация).
В точке S аустенит распадается на твердую однородную смесь кристаллов феррита и цемента — перлит. Сплав в точке S — эвтектоидный, при содержании углерода меньше 0,8% доэвтектоидный, а более 0,8% — заэвтектоидный. После 0,8% происходит распад аустенита с выпаданием из него вторичного цементита.
Точка А –это температура плавления чистого железа Fe, а точка Д — температура плавления цементита Fe3C. Точка Е ( 2,14 % С) делит сплав на две группы: стали и чугуны. Левее точки Е будут стали, а правее- чугуны.
Точка Е ( 2,14 % С) делит сплав на две группы: стали и чугуны. Левее точки Е будут стали, а правее- чугуны.
Температура плавления стали с увеличением количества углерода С в ней снижается, а чугунов после 4,3 % — увеличивается. Сразу после затвердевания структура сталей состоит из аустенита, а чугунов из смесей: аустенит + ледебурит ; цементит + ледебурит.
При охлаждении доэвтектоидных сталей (С < 0,8%, т.е. левее точки S) аустенит распадается, из него выделяется феррит.
В эвтектоидной точке С будет механическая смесь кристаллов аустенита и цементита — ледебурит. Правее точки С выделяется цементит. Сплавы чугунов левее точки С — доэвтектоидные, правее — заэвтектоидные.
Белые чугуны (белый оттенок на изломе). состоят из ледебурита и цементита Они твердые, хрупкие, трудно механически обрабатываются. Используются для передела в сталь.
Если углерод в сплаве находится в свободном состоянии, т.е. в виде графита, то это серые чугуны.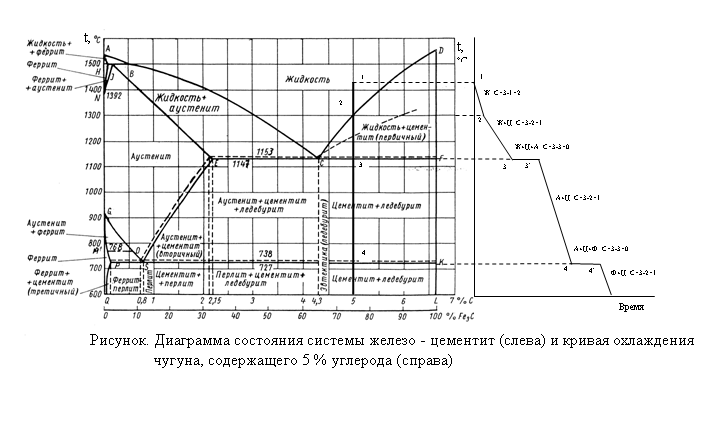
Диаграмма железо — углерод имеет большое практическое значение для инженеров. По ней можно определить температуру плавления и затвердевания сталей и чугунов, интервалы температур при обработке сталей давлением (ковка, штамповка,…) и термической обработке (закалка, отпуск,…), т.е. .она нужна металлургу, кузнецу и термисту.
Метки: доэвтектический сплавзаэвтектический сплавковкаЛедебуритледобуритмагнитенМеханические смесиперлитпрочностьсваркасвинец–сурьмаСтруктурные составляющие железотвердостьФазовые превращенияЦементитштамповкаэвтектоид
Диаграмма Железо-Цементит (метастабильная) и кривая охлаждения сплава Fe-C
- формат doc
- размер 31 КБ
- добавлен 23 июня 2009 г.
Рисунок в векторном формате. Диаграмма и кривая охлаждения на одном
рисунке (с общей шкалой температур) с подписанным составом фаз на
различных участках и с обозначенными превращениями фаз. Содержание
углерода 1,15 %. Температуры излома кривой подписаны соответственно
диаграмме. Автор: Бечин А. В. АГТУ (САФУ) и другие У/З (все, где
изучают материаловедение).
Содержание
углерода 1,15 %. Температуры излома кривой подписаны соответственно
диаграмме. Автор: Бечин А. В. АГТУ (САФУ) и другие У/З (все, где
изучают материаловедение).
Читать онлайн
Смотрите также
Лабораторная
- формат rtf
- размер 6.62 МБ
- добавлен 18 октября 2010 г.
1. Задание №1 Диаграмма Железо-цементит и ее составляющие. 2. Задание №2 Расшифровать марку сплава, влияние элементов, входящих в сплав, график термической обработки детали для получения заданных механических свойств 7ХГ2ВМ, 3. Задание №3 условия образования твердых растворов, механических смесей и химических соединений в металлических сплавах
Лабораторная
- формат doc
- размер 81.
 37 КБ
37 КБ - добавлен 19 февраля 2010 г.
Что такое твердость. Методика ее определения. Начертите диаграмму состояния железо-цементит с указанием во всех ее областях фаз и структурных составляющих. Рассмотрите формирование структуры при охлаждении из жидкого состояния сплава, содержащего 3,8% С. В произвольной точке этого сплава между линиями ликвидус и солидус, определите содержание C в фазах и их количество. Назначить режим обработки шестерни из стали 20 обеспечивающий твердость зуба H…
Лабораторная
- формат docx
- размер 1014.83 КБ
- добавлен 02 марта 2010 г.
Железо и его сплавы. Диаграмма состояния «железо-цементит». Критические точки и структурные составляющие. Технологические особенности производства изделий из полимерных материалов. Свободное литьё в формы. Оборудование и оснастка.
Критические точки и структурные составляющие. Технологические особенности производства изделий из полимерных материалов. Свободное литьё в формы. Оборудование и оснастка.
Контрольная работа
- формат rtf
- размер 12.39 МБ
- добавлен 31 мая 2011 г.
Тверской государственный технический университет, факультет ИДПО, 2 курс, СТМ. Контрольная работа по материаловедению, Вариант №1. Вычертите диаграмму состояния железо – цементит, укажите структурные составляющие во всех областях диаграммы, постройте кривую охлаждения (с применением правила фаз) для сплава, содержащего 0,35 % углерода Какова структура этого сплава при комнатной температуре и как такой сплав называется? Расшифруйте марку стали…
Лабораторная
- формат docx
- размер 935.
 16 КБ
16 КБ - добавлен 09 марта 2010 г.
Пользуясь диаграммой состояния железо-углерод (цементит). опишите процесс охлаждения сплава (от жидкого состояния до комнот-ной температуры) содержащего 3% углевода. Укажите причины возникновения трещин в отливках. Перечислите виды трещин. Назовите меры предупреждения трещин и коробления отливок. Опишите явления, происходящие в металле при нагреве перед обра-боткой давлением. Изложите понятие температурного интервала обработки металлов давлением…
- формат pdf
- размер 2.64 МБ
- добавлен 02 ноября 2009 г.
Учебное пособие. Основы теории сплавов. Диаграмма состояния двухкомпонентной системы с неограниченной растворимостью. Диаграмма состояния Железо- карбид железа(Fe-Fe3C).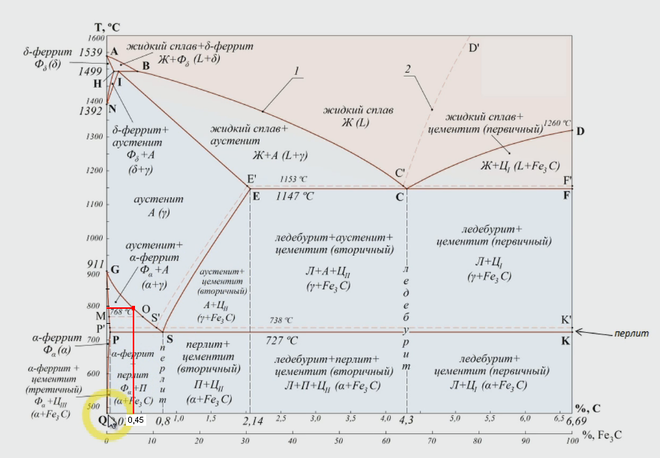 Кристализация и формирование структуры сплава. Отжиг. Закалка. Отпуск. и т. д.
Кристализация и формирование структуры сплава. Отжиг. Закалка. Отпуск. и т. д.
Курсовая работа
- формат docx
- размер 49.71 КБ
- добавлен 08 декабря 2011 г.
Сумской Государственный Университет, Сумы/Украина, Кафедра ПМ и ТКМ(материаловедения), 2010, 13 страниц. Описана диаграмма состояния двойных сплавов и диаграмма железо-цементит.
Статья
- формат doc
- размер 3.69 МБ
- добавлен 28 декабря 2011 г.
МГАКХиС, Москва, Засимова Т.В., 2011 г., 176 стр. Введение. Задачи курса. Строение и свойства типовых двухкомпонентных сплавов. Фазовые превращения в железоуглеродистых сплавах. Диаграмма железо-цементит. Основы термической обработки сталей. Фазовые превращения в сплавах железо-углерод в твердом состоянии. Фазовые превращения при нагреве стали. Вязкое и хрупкое разрушение. Этапы процесса хрупкого разрушения. Конструкционные стали. Цветные металл…
Строение и свойства типовых двухкомпонентных сплавов. Фазовые превращения в железоуглеродистых сплавах. Диаграмма железо-цементит. Основы термической обработки сталей. Фазовые превращения в сплавах железо-углерод в твердом состоянии. Фазовые превращения при нагреве стали. Вязкое и хрупкое разрушение. Этапы процесса хрупкого разрушения. Конструкционные стали. Цветные металл…
Практикум
- формат doc
- размер 240.5 КБ
- добавлен 30 января 2012 г.
Методические указания к лабораторной работе по материаловедению. – Омск: Изд-во СибАДИ, 2002. – 13 с. Рассмотрены структуры сталей и чугунов и их связь с диаграммой состояния железо–цементит. Показаны зависимости структур углеродистых материалов от их химического состава и температуры. Указаны области применения чугунов. Таблиц: 1 Иллюстраций: 8 Библиография: 2 названия Содержание Введение Краткие сведения о диаграмме состояния железо–цементит…
Указаны области применения чугунов. Таблиц: 1 Иллюстраций: 8 Библиография: 2 названия Содержание Введение Краткие сведения о диаграмме состояния железо–цементит…
Лабораторная
- формат gif, jpg
- размер 5.73 МБ
- добавлен 16 января 2010 г.
На диаграмме сплавов не указаны критические точки, по которым строилась кривая охлаждения сплава.rn
Что такое фазовая диаграмма железо-углерод?
Фазовая диаграмма железо-углерод
Фазовая диаграмма железо-углерод широко используется для понимания различных фаз стали и чугуна. И сталь, и чугун представляют собой смесь железа и углерода. Также оба сплава содержат небольшое количество микроэлементов.
График довольно сложный, но, поскольку мы ограничиваем наше исследование Fe3C, мы сосредоточимся только на 6,67 весовых процентах углерода.
Эта фазовая диаграмма железо-углерод построена с массовыми концентрациями углерода по оси X и температурной шкалой по оси Y.
На рис. показана диаграмма равновесия Fe-C, на которой изображены различные структуры (полученные при нагреве и охлаждении), фазы и микроскопические составляющие различных видов стали и чугуна. Основные структуры, значение различных линий и критические точки обсуждаются ниже.
Структуры на диаграмме Fe-C
Основными микроскопическими составляющими железа и стали являются следующие:
- Аустенит
- Феррит
- Цементит
- Перлит
1. Аустенит
Аустенит представляет собой твердый раствор свободного углерода (феррита) и железа в гамма-железе. При нагреве стали после достижения верхней критической температуры завершается формирование структуры аустенита, который является твердым, пластичным и немагнитным.
Способен растворять большое количество углерода. Он находится между критическими или переходными диапазонами при нагреве и охлаждении стали. Он образуется при содержании в стали углерода до 1,8% при 1130°С. При охлаждении ниже 723°С он начинает превращаться в перлит и феррит. Аустенитные стали не упрочняются обычными методами термической обработки и немагнитны.
Он образуется при содержании в стали углерода до 1,8% при 1130°С. При охлаждении ниже 723°С он начинает превращаться в перлит и феррит. Аустенитные стали не упрочняются обычными методами термической обработки и немагнитны.
2. Феррит
Феррит содержит очень мало углерода или совсем не содержит углерода в железе. Это название, данное кристаллам чистого железа, которые являются мягкими и пластичными. Медленное охлаждение низкоуглеродистой стали ниже критической температуры приводит к образованию ферритной структуры. Феррит не затвердевает при быстром охлаждении. Он очень мягкий и очень магнитный.
3. Цементит
Цементит представляет собой химическое соединение углерода с железом и известен как карбид железа (Fe3C). Чугун с содержанием углерода 6,67% имеет полную структуру цементита. Свободный цементит содержится во всех сталях, содержащих более 0,83% углерода. Он увеличивается с увеличением процентного содержания углерода, как это отражено на диаграмме равновесия Fe-C. Это очень тяжело.
Это очень тяжело.
Считается, что твердость и хрупкость чугуна обусловлены наличием цементита. Это снижает прочность на растяжение. Он образуется, когда углерод образует определенные соединения с железом в виде карбидов железа, чрезвычайно твердых по своей природе. Хрупкость и твердость чугуна в основном определяются наличием в нем цементита. Магнитен ниже 200°C.
4. Перлит
Перлит представляет собой эвтектоидный сплав феррита и цементита. Это происходит, в частности, в средне- и низкоуглеродистых сталях в виде механической смеси феррита и цементита в соотношении 87:13. Его твердость увеличивается с увеличением доли перлита в железном материале.
Перлит относительно прочен, тверд и пластичен, в то время как феррит слаб, мягок и пластичен. Он состоит из чередующихся светлых и темных пластин.
Эти слои попеременно состоят из феррита и цементита. При рассмотрении под микроскопом поверхность выглядит как жемчужина, поэтому ее называют перлитной. Твердые стали представляют собой смесь перлита и цементита, а мягкие стали — смеси феррита и перлита.
По мере увеличения содержания углерода выше 0,2 % при температуре, при которой феррит впервые отделяется от аустенитной капли, до тех пор, пока при 0,8 % углерода или выше не будет отслоения свободного феррита от аустенита. Эта сталь называется эвтектоидной, и по составу она имеет перлитную структуру.
При нагревании и охлаждении железа с различным процентным содержанием углерода (до 6%) следующие фазы, изображающие линии, расскажут о структуре железа, о том, как оно заряжается.
Значимость превращений Строки
1. Линия ABCD
Линия ABCD говорит о том, что над этой линией завершено плавление при нагревании железа. Расплавленный металл находится исключительно в ликвидусной форме. Ниже этой линии и выше линии AHJECF металл частично твердый и частично жидкий.
Твердый металл известен как аустенит. Таким образом, линия ABCD представляет температуры, при которых плавление считается завершенным. За этой линией металл находится полностью в расплавленном состоянии.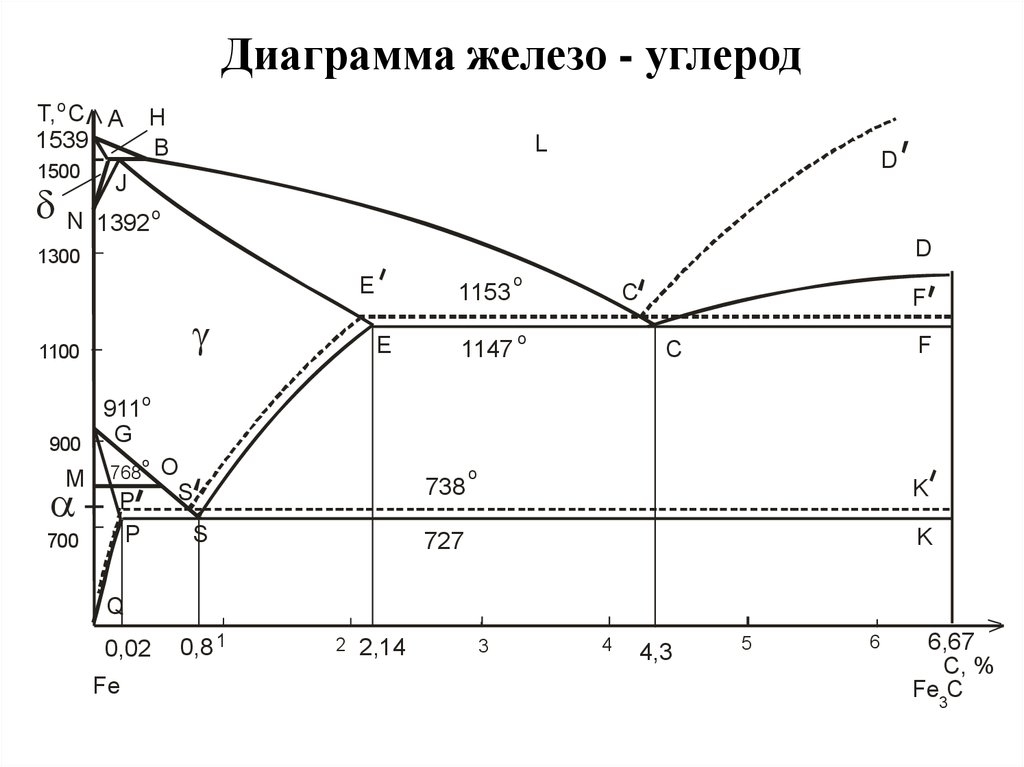 Это не горизонтальная линия, температура плавления зависит от содержания углерода.
Это не горизонтальная линия, температура плавления зависит от содержания углерода.
2. Строка AHJECF
Эта строка говорит нам о том, что металл начинает плавиться при этой температуре. Эта линия не горизонтальна, и, следовательно, температуры плавления будут меняться в зависимости от содержания углерода. Ниже этой линии и выше линии GSEC металл находится в твердом состоянии и имеет аустенитную структуру.
3. Линия PSK
Эта линия проходит при температуре около 723°C, является горизонтальной линией и известна как линия более низкой критической температуры, поскольку на этой линии начинается превращение стали. % углерода на это не влияет, т.е. сталь с разным % углерода будет трансформироваться при одной и той же температуре.
Диапазон выше линии до GSE известен как диапазон трансформации. Эта линия говорит нам, что сталь с содержанием углерода от 0,8% до 0,8% начнет превращаться из феррита и перлита в аустенит при нагреве.
4. Строка ECF
Это строка при температуре 1130°C, которая говорит, что для чугуна с % C от 2% до 4,3%. Ниже этой линии и выше линии SK чугун будет содержать аустенит + ледебурит и цементит + ледебурит.
Ниже этой линии и выше линии SK чугун будет содержать аустенит + ледебурит и цементит + ледебурит.
Часто задаваемые вопросы.
Что такое диаграмма железо-углерод?
Диаграмма Fe-C (также называемая фазой железа-углерода или диаграммой равновесия) представляет собой графическое изображение соответствующих состояний микроструктуры сплава железо-углерод (Fe-C) в зависимости от температуры и содержания углерода. Чтобы объяснить эту диаграмму, необходимо сделать введение о металлических конструкциях и чистом железе.
Как читать диаграмму железо-углерод?
Почему диаграмма железо-углерод называется диаграммой равновесия?
Карбид железа называют метастабильной фазой. Таким образом, диаграмма железо-карбид железа, хотя технически представляет собой метастабильные условия, может рассматриваться как представляющая изменения равновесия в условиях относительно медленного нагрева и охлаждения.
Какие фазы представлены на диаграмме состояния железа и углерода?
Для фазовой диаграммы железо-углерод интересующими фазовыми полями являются феррит, цементит, аустенит, феррит + цементит, феррит + аустенит и аустенит + цементит.
Что такое диаграмма равновесия углерода?
Диаграмма равновесия железо-углерод (также называемая фазовой диаграммой железо-углерод) представляет собой графическое представление соответствующих состояний микроструктуры сплава железо-углерод (Fe-C) в зависимости от температуры и содержания углерода.
Каково процентное содержание углерода в эвтектоидной стали?
Сталь, содержащая 0,8% С, известна как эвтектоидная сталь. Равновесная микроструктура эвтектоидной стали, полученной при комнатной температуре, представляет собой перлит.
Что такое мягкая сталь?
Мягкая сталь представляет собой черный металл, изготовленный из железа и углерода. Это недорогой материал со свойствами, подходящими для большинства общетехнических применений. Низкоуглеродистая мягкая сталь обладает хорошими магнитными свойствами благодаря высокому содержанию железа; поэтому он определяется как «ферромагнитный».
Из чего сделана сталь? Сталь
, сплав железа и углерода, в котором содержание углерода колеблется до 2 процентов (при более высоком содержании углерода материал определяется как чугун). На сегодняшний день это наиболее широко используемый материал для строительства инфраструктуры и промышленности в мире, он используется для изготовления всего, от швейных иголок до нефтяных танкеров.
На сегодняшний день это наиболее широко используемый материал для строительства инфраструктуры и промышленности в мире, он используется для изготовления всего, от швейных иголок до нефтяных танкеров.
Какое значение имеет температура a0 на диаграмме карбида железа?
Линия A1 является линией эвтектоидной температуры и является самой низкой температурой, при которой f.c.c. железо может существовать в равновесных условиях. Чуть выше линии A1 микроструктура состоит примерно из 25 процентов аустенита и 75 процентов феррита.
Что такое критическая температура на диаграмме железо-углерод?
Таким образом, это температура, соответствующая границе раздела фаз гамма + альфа/гамма для доэвтектоидной стали, и она является функцией содержания углерода в стали, поскольку она уменьшается от 9от 10°С при 0 % С до 727°С при 0,76 % С. Ее также называют верхней критической температурой доэвтектоидных сталей.
Что такое эвтектоидная температура на диаграмме железо-углерод?
Эвтектоидная реакция описывает фазовое превращение одного твердого вещества в два разных твердых тела. В системе Fe-C существует эвтектоидная точка примерно при 0,8 мас.% С, 723°С. Фаза чуть выше температуры эвтектоида для простых углеродистых сталей известна как аустенит или гамма.
В системе Fe-C существует эвтектоидная точка примерно при 0,8 мас.% С, 723°С. Фаза чуть выше температуры эвтектоида для простых углеродистых сталей известна как аустенит или гамма.
Какое значение имеет диаграмма железо-углерод?
Фазовая диаграмма железо-углерод широко используется для понимания различных фаз стали и чугуна. И сталь, и чугун представляют собой смесь железа и углерода. Также оба сплава содержат небольшое количество микроэлементов.
Является ли углерод FCC?
Углерод более растворим в ГЦК-фазе, занимающей область «γ» на фазовой диаграмме, чем в ОЦК-фазе. Процент углерода определяет тип сплава железа, который образуется при охлаждении из фазы ГЦК или из жидкого железа: альфа-железо, углеродистая сталь (перлит) или чугун.
Как узнать, это BCC или FCC?
Наиболее прямое различие между кристаллами ГЦК и ОЦК заключается в расположении атомов. В гранецентрированной кубической структуре атом находится во всех 8 угловых положениях и в центре всех 6 граней. Объемно-центрированная кубическая структура имеет атом во всех 8 угловых положениях и еще один в центре куба.
Объемно-центрированная кубическая структура имеет атом во всех 8 угловых положениях и еще один в центре куба.
Является ли сталь BCC или FCC?
Альфа-фаза называется ферритом. Феррит является обычным компонентом сталей и имеет объемно-центрированную кубическую (ОЦК) структуру [которая менее плотно упакована, чем ГЦК].
Что такое железо-углеродное равновесие?
В равновесных условиях в железоуглеродистых сплавах, содержащих до 0,8 % углерода, образуется доэвтектоидный феррит. Реакция протекает при 910°С в чистом железе, а между 910°С и 723°С в сплавах железа с углеродом.
Что такое перлит на диаграмме железо-углерод?
Перлит представляет собой эвтектоидную смесь цементита и феррита. Диаграмма равновесия железо-углерод: Фазовая диаграмма Fe-Fe3C не является истинным равновесием, поскольку карбид железа представляет собой нестабильную фазу, которая после длительной термообработки разлагается на железо и углерод (форма графита).
Что такое феррит на диаграмме железо-углерод?
Феррит известен как твердый раствор α. Это твердый раствор внедрения небольшого количества углерода, растворенного в α (ОЦК) железе. Максимальная растворимость составляет 0,025 % С при 723°С, а растворяется только 0,008 % С при комнатной температуре. Это самая мягкая структура, которая представлена на диаграмме.
Это твердый раствор внедрения небольшого количества углерода, растворенного в α (ОЦК) железе. Максимальная растворимость составляет 0,025 % С при 723°С, а растворяется только 0,008 % С при комнатной температуре. Это самая мягкая структура, которая представлена на диаграмме.
Какая фаза почти чистого железа?
Чистое железо (α-железо или «феррит») претерпевает изменение кристаллической структуры при нагревании выше 910 ° C, образуя γ-железо или «аустенит».
Почему линия ACM круче, чем линия A3?
Линия Acm намного круче, чем линия A3, что хотя и означает, что количество доэвтектоидного цементита в товарных сталях очень мало, но это также означает, что для растворения этого цементита для полного растворения необходимо проводить слишком высокие температуры. гомогенизация аустенита.
Фазовые диаграммы системы железо-углерод
Сплав представляет собой смесь двух или более материалов, по крайней мере один из которых является металлом. Сплавы могут иметь микроструктуру, состоящую из твердых растворов, где вторичные атомы вводятся в кристаллическую решетку в качестве заместителей или внедрений. Сплав также может представлять собой смесь металлических фаз (два или более растворов, образующих микроструктуру различных кристаллов внутри металла).
Сплавы могут иметь микроструктуру, состоящую из твердых растворов, где вторичные атомы вводятся в кристаллическую решетку в качестве заместителей или внедрений. Сплав также может представлять собой смесь металлических фаз (два или более растворов, образующих микроструктуру различных кристаллов внутри металла).
Но все сплавы могут существовать в разных фазах. Фазы – это физически однородные состояния сплава. Фаза имеет точный химический состав — определенное расположение и связи между атомами, и эта структура атомов придает разные свойства разным фазам. Фазовые диаграммы представляют собой графическое представление фаз, присутствующих в сплаве при различных условиях температуры, давления или химического состава.
Фазовая диаграмма системы железо-углерод
Простейшие ферросплавы известны как стали , и состоят из железа (Fe) , легированного углеродом (C) (от 0,1% до 1%, в зависимости от тип).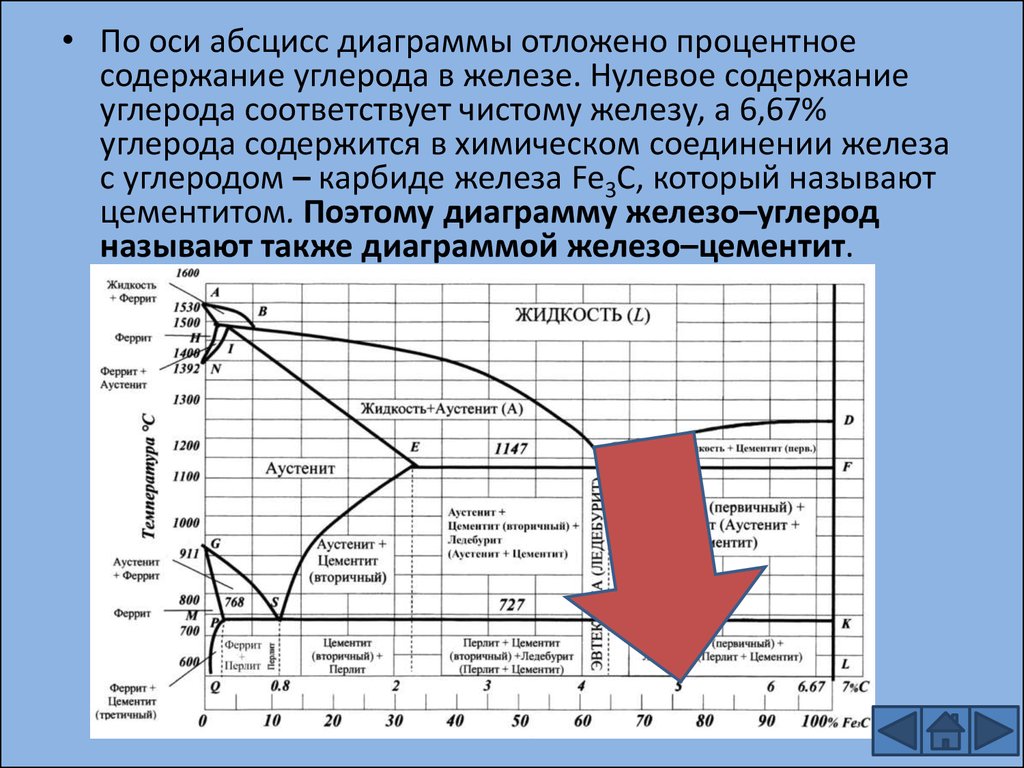 Добавление небольшого количества неметаллического углерода к железу меняет его большую пластичность на большую прочность . Из-за своей очень высокой прочности, но все же значительной ударной вязкости, а также способности сильно изменяться при термической обработке сталь является одним из наиболее полезных и распространенных ферросплавов в современном использовании. На рисунке показан железо-карбид железа (Fe-Fe 3 В) фазовая диаграмма. Процент присутствующего углерода и температура определяют фазу сплава железа с углеродом, его физические характеристики и механические свойства. Процент углерода определяет тип сплава железа: железо, сталь или чугун. На рисунке показана фазовая диаграмма железо-карбид железа (Fe-Fe3C). Процент присутствующего углерода и температура определяют фазу сплава железа с углеродом, его физические характеристики и механические свойства. Процентное содержание углерода определяет тип ферросплава: железо, сталь или чугун.
Добавление небольшого количества неметаллического углерода к железу меняет его большую пластичность на большую прочность . Из-за своей очень высокой прочности, но все же значительной ударной вязкости, а также способности сильно изменяться при термической обработке сталь является одним из наиболее полезных и распространенных ферросплавов в современном использовании. На рисунке показан железо-карбид железа (Fe-Fe 3 В) фазовая диаграмма. Процент присутствующего углерода и температура определяют фазу сплава железа с углеродом, его физические характеристики и механические свойства. Процент углерода определяет тип сплава железа: железо, сталь или чугун. На рисунке показана фазовая диаграмма железо-карбид железа (Fe-Fe3C). Процент присутствующего углерода и температура определяют фазу сплава железа с углеродом, его физические характеристики и механические свойства. Процентное содержание углерода определяет тип ферросплава: железо, сталь или чугун.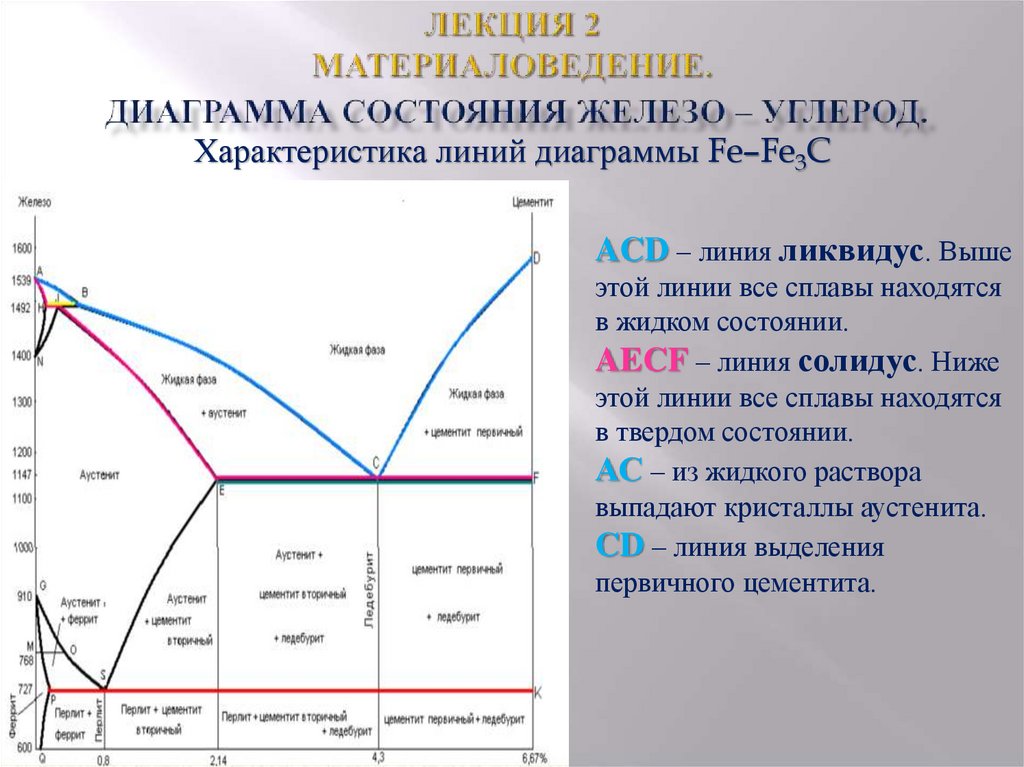 Источник: wikipedia.org Лэппле, Фолькер – Wärmebehandlung des Stahls Grundlagen. Лицензия: CC BY-SA 4.0
Источник: wikipedia.org Лэппле, Фолькер – Wärmebehandlung des Stahls Grundlagen. Лицензия: CC BY-SA 4.0
Общие фазы в сталях и чугунах
Термическая обработка сталей требует понимания как равновесных фаз, так и метастабильных фаз, возникающих при нагревании и/или охлаждении. Для сталей стабильные равновесные фазы включают:
- Феррит . Феррит или α-феррит представляет собой объемно-центрированную фазу кубической структуры железа, которая существует при температурах ниже 912°C при низких концентрациях углерода в железе. α-феррит может растворять только до 0,02% углерода при 727°C. Это связано с конфигурацией решетки железа, которая образует кристаллическую структуру ОЦК. Первичной фазой низкоуглеродистой или мягкой стали и большинства чугунов при комнатной температуре является ферромагнитное α-Fe.
- Аустенит . Аустенит, также известный как гамма-фазное железо (γ-Fe), представляет собой немагнитную фазу железа с гранецентрированной кубической структурой.
 Аустенит в железоуглеродистых сплавах обычно присутствует только при температуре выше критической эвтектоидной температуры (723°С) и ниже 1500°С, в зависимости от содержания углерода. Однако его можно поддерживать при комнатной температуре за счет добавок в сплав, таких как никель или марганец. Углерод играет важную роль в термообработке, так как расширяет температурный диапазон стабильности аустенита. Более высокое содержание углерода снижает температуру, необходимую для аустенизации стали, так что атомы железа перестраиваются, образуя структуру решетки ГЦК. Аустенит присутствует в наиболее часто используемом типе нержавеющей стали, которая очень хорошо известна своими коррозионная стойкость.
Аустенит в железоуглеродистых сплавах обычно присутствует только при температуре выше критической эвтектоидной температуры (723°С) и ниже 1500°С, в зависимости от содержания углерода. Однако его можно поддерживать при комнатной температуре за счет добавок в сплав, таких как никель или марганец. Углерод играет важную роль в термообработке, так как расширяет температурный диапазон стабильности аустенита. Более высокое содержание углерода снижает температуру, необходимую для аустенизации стали, так что атомы железа перестраиваются, образуя структуру решетки ГЦК. Аустенит присутствует в наиболее часто используемом типе нержавеющей стали, которая очень хорошо известна своими коррозионная стойкость. - Графит . Добавление небольшого количества неметаллического углерода к железу меняет его большую пластичность на большую прочность .
- Цементит . Цементит (Fe 3 C) является метастабильным соединением, и при некоторых обстоятельствах он может диссоциировать или разлагаться с образованием α-феррита и графита в соответствии с реакцией: Fe 3 C → 3Fe(α) + C (графит).
 Цементит в чистом виде является керамическим, твердым и хрупким, что делает его пригодным для упрочнения сталей. Его механические свойства зависят от его микроструктуры, которая зависит от того, как он смешивается с ферритом.
Цементит в чистом виде является керамическим, твердым и хрупким, что делает его пригодным для упрочнения сталей. Его механические свойства зависят от его микроструктуры, которая зависит от того, как он смешивается с ферритом.
Метастабильные фазы:
- Перлит . В металлургии перлит представляет собой слоистую металлическую структуру из двух фаз, состоящую из чередующихся слоев феррита (87,5 мас.%) и цементита (12,5 мас.%), встречающегося в некоторых сталях и чугунах. Он назван в честь своего сходства с перламутром.
- Мартенсит . Мартенсит представляет собой очень твердую метастабильную структуру с объемно-центрированной тетрагональной (ОЦТ) кристаллической структурой. Мартенсит образуется в сталях, когда скорость охлаждения аустенита настолько высока, что атомы углерода не успевают диффундировать из кристаллической структуры в достаточно больших количествах для образования цементита (Fe 3 С).
- Бейнит .
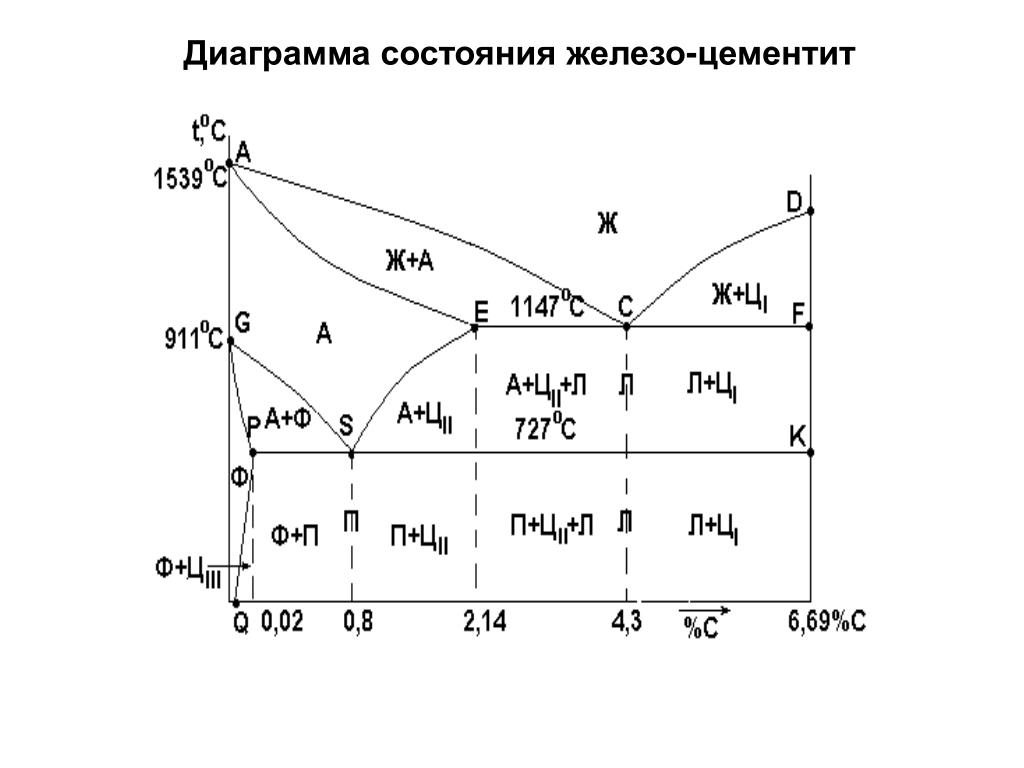 Бейнит представляет собой пластинчатую микроструктуру, которая образуется в сталях из аустенита, когда скорость охлаждения недостаточно высока для образования мартенсита, но все же достаточно высока, так что углерод не успевает диффундировать с образованием перлита. Бейнитные стали, как правило, прочнее и тверже, чем перлитные стали, однако они демонстрируют желаемое сочетание прочности и пластичности.
Бейнит представляет собой пластинчатую микроструктуру, которая образуется в сталях из аустенита, когда скорость охлаждения недостаточно высока для образования мартенсита, но все же достаточно высока, так что углерод не успевает диффундировать с образованием перлита. Бейнитные стали, как правило, прочнее и тверже, чем перлитные стали, однако они демонстрируют желаемое сочетание прочности и пластичности.
Критическая температура стали
Критическая температура стали определяет фазовый переход между двумя фазами стали. Как 9Сталь 0159 нагревается выше критической температуры , около 1335°F (724°С), она претерпевает фазовый переход, рекристаллизуясь в виде аустенита. Существует два типа критической температуры:
- Нижняя критическая температура (Ac1). Температура, при которой аустенит начинает превращаться из феррита.
- Верхняя критическая температура (Ac3). Температура, при которой аустенит полностью превращается из феррита.

Система Fe-C имеет эвтектоидную точку при приблизительно 0,8 мас.% C, 723°C. Фаза выше температуры эвтектоида для простых углеродистых сталей известна как аустенит или гамма.
Ссылки:
Материаловедение:
Министерство энергетики США, Материаловедение. Справочник по основам Министерства энергетики, том 1 и 2. Январь 1993 г.
Министерство энергетики США, материаловедение. Справочник по основам Министерства энергетики, том 2 и 2. Январь 1993 г.
Уильям Д. Каллистер, Дэвид Г. Ретвиш. Материаловедение и инженерия: введение 9издание, Wiley; 9 издание (4 декабря 2013 г.), ISBN-13: 978-1118324578.
Эберхарт, Марк (2003). Почему все ломается: Понимание мира, между прочим, разваливается. Гармония. ISBN 978-1-4000-4760-4.
Гаскелл, Дэвид Р. (1995). Введение в термодинамику материалов (4-е изд.). Издательство Тейлор и Фрэнсис. ISBN 978-1-56032-992-3.
Гонсалес-Виньяс, В. и Манчини, Х.Л. (2004). Введение в материаловедение. Издательство Принстонского университета. ISBN 978-0-691-07097-1.
и Манчини, Х.Л. (2004). Введение в материаловедение. Издательство Принстонского университета. ISBN 978-0-691-07097-1.
Эшби, Майкл; Хью Шерклифф; Дэвид Себон (2007). Материалы: инженерия, наука, обработка и дизайн (1-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-7506-8391-3.
Дж. Р. Ламарш, А. Дж. Баратта, Введение в ядерную технику, 3-е изд., Prentice-Hall, 2001, ISBN: 0-201-82498-1.
See above:
Materials Science
The Iron-Carbon Phase Diagram – IspatGuru
The Iron-Carbon Phase Diagram
- satyendra
- March 11, 2013
- 5 Comments
- bcc, цементит, критическая температура, ГЦК, феррит, термообработка сталей, мартенсит, микроструктура, перлит, фаза, фазовая диаграмма,
Фазовая диаграмма железо-углерод
Фазовые диаграммы являются очень важным инструментом в изучении сплавов для решения многих практических задач в металлургии. Эти диаграммы определяют области устойчивости фазы, которая может существовать в системе сплавов в условиях постоянного атмосферного давления. Для двойной системы координатами этих диаграмм являются температура и состав. Взаимоотношения между фазами, температурой и составом в системе сплава обычно представляются фазовой диаграммой только в равновесных условиях. Такие условия возникают при малых скоростях нагрева и охлаждения сплавов, когда кинетика превращений не играет существенной роли.
Для двойной системы координатами этих диаграмм являются температура и состав. Взаимоотношения между фазами, температурой и составом в системе сплава обычно представляются фазовой диаграммой только в равновесных условиях. Такие условия возникают при малых скоростях нагрева и охлаждения сплавов, когда кинетика превращений не играет существенной роли.
В своей простейшей форме железо и стали представляют собой сплавы железа (Fe) и углерода (C). Существует три типа ферросплавов. Эти сплавы состоят из (i) железа с содержанием углерода менее 0,0008 % при комнатной температуре, (ii) сталей с содержанием углерода от 0,008 % до 2,14 % (обычно менее 1 %) и микроструктуры, состоящей из феррита и цементита. ) и (iii) чугун с содержанием углерода от 2,14 % до 6,7 % (обычно менее 4,5 %). Изучение состава и структуры железа и стали начинается с фазовой диаграммы железо-углерод (Fe-C) (рис. 1). Фазовая диаграмма Fe-C также используется в качестве основы для понимания процессов термообработки.
Многие из основных характеристик системы Fe-C влияют на поведение даже самых сложных сплавов железа и стали. Например, фазы, обнаруженные в простой бинарной системе Fe-C, сохраняются в сложных сталях, но необходимо изучить влияние легирующих элементов на формирование и свойства этих фаз. Диаграмма Fe-C представляет собой ценную основу, на которой можно построить знания как о простых углеродистых, так и о легированных сталях.
Например, фазы, обнаруженные в простой бинарной системе Fe-C, сохраняются в сложных сталях, но необходимо изучить влияние легирующих элементов на формирование и свойства этих фаз. Диаграмма Fe-C представляет собой ценную основу, на которой можно построить знания как о простых углеродистых, так и о легированных сталях.
Рис. 1 Фазовая диаграмма железо-углерод
C — примесь внедрения в Fe. Он образует твердый раствор с альфа-, гамма- и дельта-фазами железа. Максимальная растворимость C в альфа-железе составляет 0,025% при 727°C. Объемно-центрированное кубическое (ОЦК) железо имеет относительно небольшие промежуточные положения. Максимальная растворимость C в гранецентрированном кубическом (ГЦК) гамма-железе составляет 2,14 % при 1148 °C. ГЦК-железо имеет более крупные промежуточные положения. Механические свойства железоуглеродистых сплавов (железо и стали) зависят от их микроструктуры, то есть от того, как смешаны различные фазы.
Фазовая диаграмма железо-углерод на рис. 2 фактически показывает две диаграммы, а именно (i) стабильную диаграмму железо-графит (красные линии), (ii) и метастабильную диаграмму Fe-Fe3C. Цементит метастабилен, и истинное равновесие должно быть между железом и графитом (С). Хотя графит широко встречается в чугунах, обычно трудно получить эту равновесную фазу в сталях. Для развития стабильного состояния обычно требуется очень много времени, особенно при низких температурах и низком содержании углерода. Следовательно, диаграмма нормального равновесия, которая обычно используется, представляет собой диаграмму метастабильного Fe-Fe3C, поскольку она имеет отношение к поведению большинства сталей на практике.
2 фактически показывает две диаграммы, а именно (i) стабильную диаграмму железо-графит (красные линии), (ii) и метастабильную диаграмму Fe-Fe3C. Цементит метастабилен, и истинное равновесие должно быть между железом и графитом (С). Хотя графит широко встречается в чугунах, обычно трудно получить эту равновесную фазу в сталях. Для развития стабильного состояния обычно требуется очень много времени, особенно при низких температурах и низком содержании углерода. Следовательно, диаграмма нормального равновесия, которая обычно используется, представляет собой диаграмму метастабильного Fe-Fe3C, поскольку она имеет отношение к поведению большинства сталей на практике.
Детали стабильных и метастабильных фазовых диаграмм системы Fe-C, особенно на стороне, богатой железом, известны намного лучше, чем любые другие бинарные системы с аналогичной сложностью. Однако все еще существуют значительные области, в которых фазовая диаграмма не установлена, например, в диапазонах температур, составов и давлений, не связанных непосредственно с производством чугуна и стали.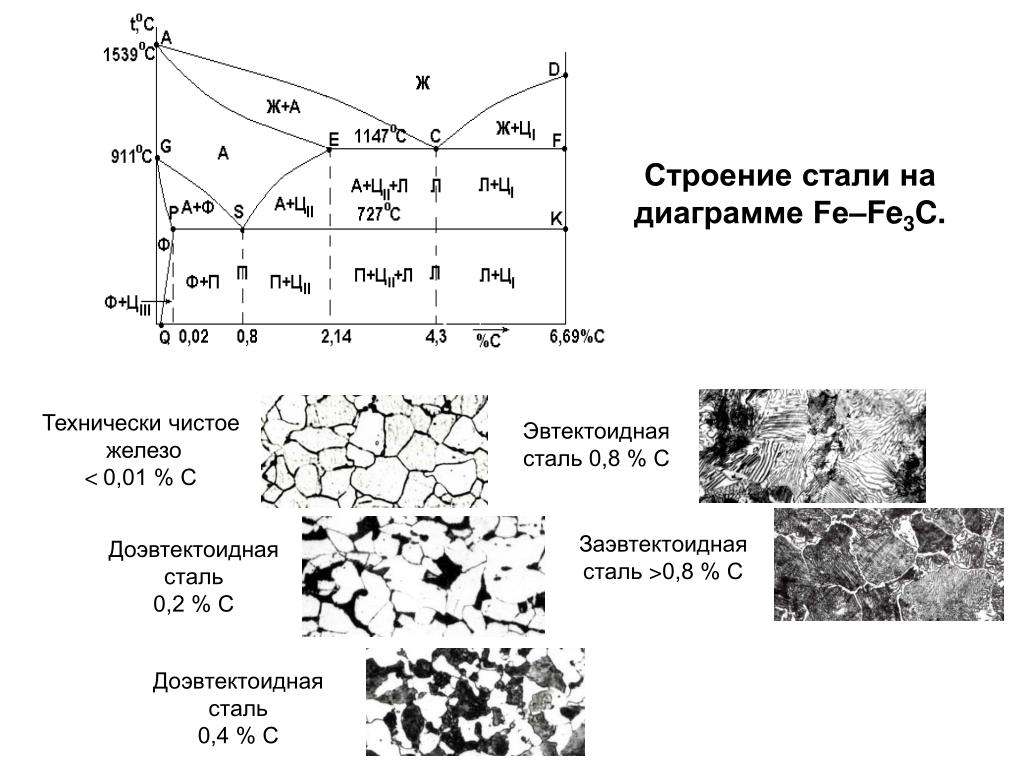
Рис. 2 Диаграмма железо-углерод, показывающая стабильные и метастабильные фазы
В системе железо-углерод присутствуют некоторые важные металлургические фазы и микрокомпоненты. В системе Fe–Fe3C углерод является примесью внедрения в Fe. Он образует твердый раствор с альфа (альфа-феррит), гамма (аустенит) и дельта (дельта-феррит) фазами железа. Это важные фазы на фазовой диаграмме Fe – Fe3C. Между однофазными полями обнаруживаются области со смесями двух фаз, таких как феррит и цементит, аустенит и цементит, феррит и аустенит. При самых высоких температурах можно обнаружить поле жидкой фазы, а под ним находятся поля двух фаз: жидкость и аустенит, жидкость и цементит и жидкость и феррит. При термообработке сталей всегда избегают жидкой фазы. В точке эвтектики (4,26 % С) жидкий сплав при охлаждении непосредственно превращается в аустенит и цементит без какого-либо двухфазного поля. Точно так же в эвтектоидной точке (0,76 % C) аустенитная фаза при охлаждении напрямую превращается в феррит и цементит без какого-либо двухфазного поля. Некоторым важным границам в однофазных полях даны специальные названия, облегчающие понимание диаграммы.
Некоторым важным границам в однофазных полях даны специальные названия, облегчающие понимание диаграммы.
Основными фазами железа и стали в равновесии являются следующие фазы.
- Феррит или фаза альфа-железа — это стабильная форма железа при комнатной температуре. Это относительно мягкая низкотемпературная фаза и стабильная равновесная фаза. Он превращается в ГЦК-аустенит (гамма-фаза) при 910 °C. Феррит является обычным компонентом сталей и имеет ОЦК-структуру, которая менее плотно упакована, чем ГЦК-структура. Он мягкий и довольно пластичный. Он обладает магнитными свойствами при температуре ниже 768°C. Обладает низкой прочностью и хорошей ударной вязкостью.
- Фаза аустенита или гамма-железа. Аустенит представляет собой высокотемпературную фазу. Это твердый раствор C в FCC-железе. Следовательно, он имеет структуру FCC, которая представляет собой плотноупакованную структуру. Это немагнитная и пластичная фаза. Он превращается в дельта-феррит ОЦК при 1394 °C.
 Он нестабилен ниже температуры эвтектики (727 °C), если его не охладить быстро. Аустенит обладает хорошей прочностью и ударной вязкостью.
Он нестабилен ниже температуры эвтектики (727 °C), если его не охладить быстро. Аустенит обладает хорошей прочностью и ударной вязкостью. - Дельта-ферритовая фаза – твердый раствор C в ОЦК-железе. Он стабилен только при температуре выше 1394°С. Плавится при 1538°С. Обладает парамагнитными свойствами.
- Цементит – Fe3C или карбид железа. Это интерметаллическое соединение Fe и C. Он имеет сложную орторомбическую структуру и является метастабильной фазой. Это тяжелая, хрупкая фаза. Он имеет низкую прочность на растяжение, хорошую прочность на сжатие и низкую ударную вязкость. Разлагается (очень медленно, в течение нескольких лет) на альфа-феррит и С (графит) в интервале температур от 650 до 700°С. максимальное значение 2,14 % при 1148°С. Такая высокая растворимость углерода в аустените чрезвычайно важна при термообработке, когда обработка на твердый раствор в аустените с последующей быстрой закалкой до комнатной температуры позволяет образовать пересыщенный твердый раствор углерода в железе.
 Ферритная фаза ограничена максимальной растворимостью углерода 0,025 % при 727°C. Поскольку диапазон содержания углерода в обычных сталях составляет от 0,05 % до 1,5 %, феррит обычно связан с цементитом в той или иной форме. Точно так же дельта-фаза очень ограничена и находится в диапазоне температур между 1394 град С и 1538 град С/ полностью исчезает, когда содержание углерода достигает 0,5 %.
Ферритная фаза ограничена максимальной растворимостью углерода 0,025 % при 727°C. Поскольку диапазон содержания углерода в обычных сталях составляет от 0,05 % до 1,5 %, феррит обычно связан с цементитом в той или иной форме. Точно так же дельта-фаза очень ограничена и находится в диапазоне температур между 1394 град С и 1538 град С/ полностью исчезает, когда содержание углерода достигает 0,5 %.Сплав эвтектоидного состава (0,76% C) при медленном охлаждении образует перлит, представляющий собой слоистую структуру из двух фаз, а именно альфа-феррита и цементита. Перлит представляет собой смесь феррито-цементитной фазы. Он имеет характерный внешний вид и может рассматриваться как микроструктурная единица или микрокомпонент. Он представляет собой совокупность чередующихся пластинок феррита и цементита, которая после длительной выдержки ниже 727°С вырождается (сфероидизируется или укрупняется) в частицы цементита, диспергированные с ферритовой матрицей. Является эвтектоидом и имеет ОЦК-структуру.
 Это частично растворимый раствор Fe и C. Механически перлит имеет промежуточные свойства по сравнению с мягким, пластичным ферритом и твердым, хрупким цементитом. Обладает высокой прочностью и низкой вязкостью.
Это частично растворимый раствор Fe и C. Механически перлит имеет промежуточные свойства по сравнению с мягким, пластичным ферритом и твердым, хрупким цементитом. Обладает высокой прочностью и низкой вязкостью.Гипоэвтектоидные сплавы содержат доэвтектоидный феррит (образованный при температуре выше эвтектоидной) вместе с эвтектоидным перлитом, который содержит эвтектоидный феррит и цементит. Заэвтектоидные сплавы содержат проэвтектоидный цементит (образуется выше температуры эвтектоида вместе с перлитом, содержащим эвтектоидный феррит и цементит). из этих микроструктур приведены ниже.
- Бейнит – фаза между перлитом и мартенситом. Это твердый метастабильный микрокомпонент, состоящий из непластинчатой смеси феррита и цементита в очень мелком масштабе. Верхний бейнит образуется при более высоких температурах и имеет перистый вид. Нижний бейнит образуется при более низких температурах и имеет игольчатый вид. Твердость бейнита увеличивается с понижением температуры его образования.
 Обладает хорошей прочностью и жесткостью.
Обладает хорошей прочностью и жесткостью. - Мартенсит – это очень твердая форма кристаллической структуры стали. Он назван в честь немецкого металлурга Адольфа Мартенса. Он образуется при быстром охлаждении, твердый и хрупкий. Это объемно-центрированная тетрагональная (BCT) форма железа, в которой растворено некоторое количество углерода. Он образуется во время закалки, когда гранецентрированная кубическая решетка аустенита искажается в объемноцентрированную тетрагональную структуру без потери содержащихся в ней атомов углерода на цементит и феррит. Это пересыщенный раствор атомов С в феррите. Это твердая метастабильная фаза. Он имеет решетчатую морфологию, когда С составляет менее 0,6 %, пластинчатую морфологию, когда С составляет более 1 %, и смесь промежуточных форм. Он имеет высокую прочность и твердость и низкую ударную вязкость.
- Сорбит/троостит. Структуры нижней стадии перлита с очень мелкими чешуйками называются сорбитом и трооститом. Возрастающим скоростям охлаждения соответствуют структуры превращения перлитной стадии.
 Однако это меняет структурное соотношение и формирование перлита в зависимости от расстояния между чешуйками. Структура не видна под оптическим микроскопом.
Однако это меняет структурное соотношение и формирование перлита в зависимости от расстояния между чешуйками. Структура не видна под оптическим микроскопом. - Видманштеттеновый феррит – получается при быстром охлаждении доэвтектоидной простой углеродистой стали до температуры выше температуры A3. Из-за быстрого охлаждения у кристаллов феррита остается мало времени для зарождения не только на границе зерен, но и внутри крупных аустенитных зерен. Они быстро растут в некотором предпочтительном направлении кристалла внутри зерна и, таким образом, становятся удлиненными. Структура либо в виде игл (реек), либо в виде пластин, которые имеют тенденцию выстраиваться в одном направлении в пределах одного зерна.
На диаграмме железо-C есть много температур и критических точек, которые важны как с базовой, так и с практической точки зрения. Это температуры, когда при охлаждении или нагревании в них происходят как фазовые, так и магнитные превращения. Температуры, при которых происходят превращения в твердом состоянии, называются критическими температурами, или критическими точками.
 Основные температуры и критические точки приведены ниже.
Основные температуры и критические точки приведены ниже.- Температура A0 – это температура Кюри, при которой магнитное превращение цементита в немагнитное происходит при нагревании. В структуре могут образовываться дефекты, такие как дислокации, разломы и вакансии. Цементит является металлическим и ферромагнитным с температурой Кюри около 210 градусов C. При сплавлении металлические растворы замещают места железа; более мелкие атомы, такие как бор, заменяют углерод в междоузлиях.
- A1 температура – это температура (727°С), при которой происходит эвтектоидное превращение. При этой температуре перлит превращается в аустенит при нагреве и наоборот
- Температура А2 – называется температурой Кюри феррита (768 град С), при которой ферромагнитный феррит при нагревании превращается в парамагнитный. При этой температуре микроструктура не меняется.
- Температура A3 – это температура, при которой феррит только начинает формироваться из аустенита при охлаждении доэвтектоидной стали или последние следы свободного феррита превращаются в аустенит при нагреве.
 Таким образом, это температура, соответствующая границе раздела фаз гамма + альфа/гамма для доэвтектоидной стали, и она является функцией содержания углерода в стали, так как она уменьшается от 9от 10°С при 0 % С до 727°С при 0,76 % С. Ее также называют верхней критической температурой доэвтектоидных сталей. Температурный интервал между температурами А1 и А3 называется критическим диапазоном, в котором аустенит находится в равновесии с ферритом.
Таким образом, это температура, соответствующая границе раздела фаз гамма + альфа/гамма для доэвтектоидной стали, и она является функцией содержания углерода в стали, так как она уменьшается от 9от 10°С при 0 % С до 727°С при 0,76 % С. Ее также называют верхней критической температурой доэвтектоидных сталей. Температурный интервал между температурами А1 и А3 называется критическим диапазоном, в котором аустенит находится в равновесии с ферритом. - Температура Acm – это температура в заэвтектоидной стали, при которой доэвтектоидный цементит только начинает формироваться (при охлаждении) из аустенита. Он представляет собой температуру границы раздела фаз гамма/гамма + Fe3C и является функцией углерода. Линия Acm показывает, что растворимость углерода в твердом состоянии в аустените очень быстро снижается с максимума 2,14 % при 1148°C до максимума 0,76 % при 727°C из-за большей стабильности цементита при более низких температурах. Дополнительный углерод выделяется из аустенита в виде доэвтектоидного цементита в заэвтектоидных сталях (также называемого вторичным цементитом в чугунах).
 Отделение цементита от аустенита (при охлаждении) также сопровождается выделением тепла.
Отделение цементита от аустенита (при охлаждении) также сопровождается выделением тепла. - Температура A4 – это температура, при которой аустенит превращается в дельта-железо. Самое низкое значение этой температуры составляет 1394°С, что соответствует чистому железу. Эта температура увеличивается по мере увеличения процентного содержания углерода.
- Ms температура – это температура, при которой начинается превращение аустенита в мартенсит при охлаждении.
- Температура Mf – это температура, при которой заканчивается образование мартенсита при охлаждении. Все изменения, кроме образования мартенсита, происходят при более низких температурах при охлаждении, чем при нагреве, и зависят от скорости изменения температуры.
Превращение аустенита в феррит – В равновесных условиях в железоуглеродистых сплавах, содержащих до 0,76 % углерода, образуется доэвтектоидный феррит. Реакция протекает при 910°С в чистом железе, а между 910°С и 727°С в сплавах железа с углеродом.
 Однако при закалке из аустенитного состояния до температур ниже эвтектоидной температуры феррит может образовываться вплоть до температур 600°С. При понижении температуры превращения наблюдаются выраженные морфологические изменения, которые обычно относятся к доэвтектоидным формам. и заэвтектоидные фазы, хотя в каждом случае существуют вариации из-за точной кристаллографии вовлеченных фаз. Например, те же принципы применимы к образованию цементита из аустенита, но морфологически отличить феррит от цементита нетрудно.
Однако при закалке из аустенитного состояния до температур ниже эвтектоидной температуры феррит может образовываться вплоть до температур 600°С. При понижении температуры превращения наблюдаются выраженные морфологические изменения, которые обычно относятся к доэвтектоидным формам. и заэвтектоидные фазы, хотя в каждом случае существуют вариации из-за точной кристаллографии вовлеченных фаз. Например, те же принципы применимы к образованию цементита из аустенита, но морфологически отличить феррит от цементита нетрудно.Превращение аустенита в цементит – Существуют различные морфологии цементита, которые образуются при постепенно более низких температурах превращения. Начальное развитие аллотриоморфов границ зерен очень похоже на развитие феррита, и рост боковых пластин или видманштеттовского цементита происходит по той же схеме. Аллотриоморф имеет форму, не отражающую его внутреннюю кристаллическую симметрию. Это связано с тем, что он имеет тенденцию образовываться на поверхности аустенитных зерен, образуя таким образом слои, которые повторяют контуры границ зерен.
 Пластинки цементита имеют более строго кристаллографическую форму, несмотря на то, что ориентационная связь с аустенитом более сложная. Как и в случае с ферритом, большинство боковых пластин происходит из аллотриоморфов границ зерен, но в реакции цементита больше боковых пластин зарождается на границах двойников в аустените.
Пластинки цементита имеют более строго кристаллографическую форму, несмотря на то, что ориентационная связь с аустенитом более сложная. Как и в случае с ферритом, большинство боковых пластин происходит из аллотриоморфов границ зерен, но в реакции цементита больше боковых пластин зарождается на границах двойников в аустените.Реакция аустенита и перлита – Перлит является наиболее известной микроструктурой на фазовой диаграмме железо-углерод. Он был обнаружен Сорби более века назад, который правильно предположил, что это пластинчатая смесь железа и карбида железа. Это очень распространенный компонент самых разных сталей, где он вносит существенный вклад в прочность. Пластинчатые эвтектоидные структуры такого типа широко распространены в металлургии сталей. Эти структуры имеют много общего с реакциями клеточной преципитации. Оба типа реакций происходят путем зародышеобразования и роста и, следовательно, контролируются диффузией. Зародыши перлита встречаются на границах аустенитных зерен, но ясно, что они также могут быть связаны как с доэвтектоидным ферритом, так и с цементитом.
 В промышленных сталях перлитные конкреции могут образовываться на включениях.
В промышленных сталях перлитные конкреции могут образовываться на включениях.Фазовая диаграмма железоуглеродистых сплавов | Сталь | Металлургия
РЕКЛАМА:
Фазовая диаграмма представляет собой диаграмму, показывающую количество и характер фаз, присутствующих в данном сплаве при любой температуре и составе в условиях равновесия. На рис. 1.13 показаны различные составляющие стали.
Есть четыре основных фазы стали, а именно, феррит, цементит, аустенит и перлит. Было замечено, что различные другие элементы, помимо углерода и железа, которые присутствуют в сталях в виде примесей или легирующих элементов, не оказывают заметного влияния на диаграмму состава железа и углерода, показанную на рис. 1.13. Однако их присутствие изменяет положение граничных линий.
РЕКЛАМА:
Эти четыре этапа описаны ниже:
1. Феррит:
Твердый раствор углерода до 0,025% в растворителе а-железо. Эта фаза обозначена на схеме GSP.
Феррит ϒ-фаза превращается в феррит из-за медленного охлаждения твердых сплавов. Феррит обычно не содержит углерода, но содержит много других элементов, таких как Mn, Si, Cr в твердом растворе.
ϒ-фаза превращается в феррит из-за медленного охлаждения твердых сплавов. Феррит обычно не содержит углерода, но содержит много других элементов, таких как Mn, Si, Cr в твердом растворе.мягкий, слабый и пластичный.
ОБЪЯВЛЕНИЯ:
Твердость феррита составляет от 50 до 100 по Бринеллю. Феррит наиболее известен своей высокой пластичностью.
2. Цементит:
Это прерывистое соединение, состоящее из определенного расположения атомов железа и углерода в решетке, причем относительное количество каждого из атомов, присутствующих в данном образце, соответствует формуле Fe 3 C. Эта фаза образуется за счет медленного охлаждение твердых сплавов в зоне ЭСК. По химическому составу представляет собой соединение углерода и карбида железа Fe 9.0179 3 С.
Другие элементы, которые могут присутствовать в стали, также находятся в форме карбидов. В такой стали цементит очень твердый и имеет твердость порядка 1400 единиц по Бринеллю.
 В отожженной стали (т. е. в контролируемо охлажденной стали) цементит находится в виде сфероидов (округлых частиц) или параллельных пластин (пластинчатых слоев) или в виде покрытия перлитных зерен. Цементит довольно хрупок, но тверд и прочен.
В отожженной стали (т. е. в контролируемо охлажденной стали) цементит находится в виде сфероидов (округлых частиц) или параллельных пластин (пластинчатых слоев) или в виде покрытия перлитных зерен. Цементит довольно хрупок, но тверд и прочен.ОБЪЯВЛЕНИЙ:
Феррит и цементит имеют тенденцию образовывать слоистую структуру, называемую перлитом.
Количество перлита в простой углеродистой стали (углерод от 0,1 до 1,5%) увеличивается с увеличением содержания углерода. При содержании углерода 0,83% все зерна будут перлитными. Углерод при избытке 0,83% образует свободный цементит по границам зерен, вызывая снижение предела прочности при растяжении из-за локальной хрупкости.
3. Аустенит:
Твердый раствор углерода до 1,7% в гамма-железе. Аустенит получают нагреванием углеродистой-железо-стали выше диапазона GSF. Образование аустенита происходит за счет межфазной реакции феррита и цементита. Сначала образуются зародыши аустенита, а затем они продолжают расти за счет дальнейшей реакции феррита и цементита.
 Скорость образования аустенита увеличивается при повышении температуры.
Скорость образования аустенита увеличивается при повышении температуры.РЕКЛАМА:
Диаграмма железо-углерод показывает, какая из трех фаз стали задана при заданной температуре и концентрации углерода, когда сплав охлаждается или нагревается достаточно медленно, чтобы он оставался в состоянии равновесия.
4. Перлит:
Железо при комнатной температуре имеет объемно-центрированную кубическую решетку (a-железо), а при нагревании выше 910°C принимает гранецентрированно-кубическую решетку (ϒ-железо, также называемое аустенитом). Эти две аллотропные формы железа имеют разные физические свойства (например, коэффициенты расширения).
Переход из одной аллотропной формы в другую называется превращением или реакцией. Энергия затрачивается на переход от ϒ к α-железу, и кривая охлаждения показывает термическую задержку при температуре, при которой происходит событие.
РЕКЛАМА:
Для чистого железа превращение происходит при 910°C, но с добавлением углерода оно происходит в диапазоне температур, предельные значения которых известны как критические точки — (A 3 более высокая температура, т.
Углерод е. та, при которой начинается превращение при охлаждении , и А 1 — нижняя точка (723° для всех марок железа/стали). При 0,8% углерода A 3 сливается с A 1 и поднимается как на более низком, так и на верхнем уровнях углерода.
е. та, при которой начинается превращение при охлаждении , и А 1 — нижняя точка (723° для всех марок железа/стали). При 0,8% углерода A 3 сливается с A 1 и поднимается как на более низком, так и на верхнем уровнях углерода.имеет разную растворимость в аустените и феррите. При 1130°C аустенит может содержать до 1,7% углерода, когда весь углерод находится в растворе. Углерод растворен в междоузлиях, то есть атом углерода не заменяет атом железа, образуя часть куба, а прижимается между атомами железа. В случае объемно-центрированной кубической структуры (для феррита) пространство между атомами железа недостаточно, и атом углерода выбрасывается со своего места. Вот какая реакция происходит в А 3 точка.
В точке A 3 b.c.c. Ферритное зерно начинает зарождаться на краю аустенитного зерна, создавая границу между двумя составляющими. По мере снижения температуры между пределами A 3 и A 1 граница продвигается все дальше и дальше вглубь аустенитного зерна.
 Когда углерод выбрасывается из решетки феррита, он диффундирует в тело аустенитного зерна и остается в растворе.
Когда углерод выбрасывается из решетки феррита, он диффундирует в тело аустенитного зерна и остается в растворе.Таким образом, непреобразованный аустенит постепенно обогащается углеродом до предела 0,8%. При дальнейшем охлаждении до предела А 1 оставшийся аустенит полностью превращается в феррит, и практически весь углерод выбрасывается из раствора с образованием слоев цементита, которые располагаются между ферритом.
Если кусок простой углеродистой стали (углерод до 1,5% и без легирующих элементов) нагреть в печи с постоянной скоростью, то его температура будет повышаться с одинаковой скоростью до тех пор, пока не будет достигнута температура, при которой это повышение останавливается на короткое время. время или температура может даже упасть, хотя температура печи продолжает расти. В этот момент тепло используется для перегруппировки атомов железа, что, в свою очередь, вызывает образование твердого раствора, называемого аустенитом.
Температура, при которой перлит превращается в аустенит, называется нижней критической температурой нагрева (около 723°C).
 Феррит или цементит превращаются в аустенит при более высокой температуре, известной как верхняя критическая точка нагрева (которая зависит от содержания углерода в стали).
Феррит или цементит превращаются в аустенит при более высокой температуре, известной как верхняя критическая точка нагрева (которая зависит от содержания углерода в стали).Аналогично, при равномерном охлаждении температура падает равномерно до тех пор, пока не будет достигнута температура, при которой охлаждение начинается медленнее (известная как верхняя критическая температура охлаждения и на 30°C меньше верхней критической точки нагрева).
В этот момент аустенит начинает разрушаться с образованием феррита или цементита, в зависимости от содержания углерода в стали. Это изменение продолжается до тех пор, пока не будет достигнута нижняя критическая точка охлаждения (695°С), когда весь оставшийся аустенит превращается в перлит.
Диаграмма железо-углерод ничего не говорит об агрегатном состоянии присутствующих фаз. Другими словами, такая информация, как относительные размеры или формы феррита и цементита, не может быть получена, когда оба они присутствуют в определенном температурном диапазоне.
 Эту информацию можно получить только при микроскопическом исследовании полированной и протравленной поверхности металла.
Эту информацию можно получить только при микроскопическом исследовании полированной и протравленной поверхности металла.Диаграмма железо-углерод также помогает определить фазовые превращения, происходящие при медленном охлаждении стального образца определенного состава от высокой температуры. Рассмотрим случай образца стали с содержанием углерода 0,5 %. В области GSEN металл полностью аустенитный и будет оставаться в этом состоянии до тех пор, пока не охладится и не пересечет линию GS, когда по границам зерен аустенита начнет формироваться феррит.
Количество феррита будет увеличиваться по мере снижения температуры от линии GS до линии PS. При температуре 723°C весь оставшийся аустенит будет иметь содержание углерода 0,80% и будет трансформироваться при постоянной температуре в чередующиеся пластины феррита и цементита (эта пластинчатая пластинчатая структура известна как перлит). При всех температурах ниже 723°C мы все еще имеем смесь феррита и перлита.
Далее рассмотрим, какие изменения происходят при охлаждении эвтектоидной стали (сталь с 0,8% углерода).
 В этом случае ничего не происходит до тех пор, пока не будет достигнута температура 723°С, когда весь металл при постоянной температуре переходит в перлит.
В этом случае ничего не происходит до тех пор, пока не будет достигнута температура 723°С, когда весь металл при постоянной температуре переходит в перлит.Если охлаждать стальную деталь с содержанием углерода 1,2 %, то сначала по границам зерен выделяется цементит при температуре, соответствующей линии SE. Это продолжается до тех пор, пока не будет достигнута температура 723°C, когда весь оставшийся материал превратится в перлит. Ниже температуры 723°C дальнейшего изменения в структуре не происходит.
Способность стали к закалке зависит от разницы в растворимости углерода аустенита и феррита и склонности избыточного углерода осаждаться в форме цементита, когда аустенит превращается в феррит. Расстояние между частицами цементита зависит от скорости охлаждения и их формы.
Если скорость охлаждения стали при пересечении температурной линии 723°С высокая, то частицы цементита, выпавшие в осадок, будут очень маленькими и близко расположенными, а если скорость медленная, то частицы выпавшего цементита будут более крупными и более удаленными друг от друга.
 .
.Форма частиц цементита может быть пластинчатой, сфероидальной или игольчатой. Ламеллярная структура, известная как перлит, состоит из чередующихся пластин цементита и феррита. Является ли перлит крупным или мелким, зависит от относительного расстояния между цементитными пластинами.
Сфероидальная структура состоит из примерно сферических глобул цементита в матрице феррита. Этот тип структуры известен как сфероидит, в котором глобулы относительно большие. Игольчатая структура, также известная как структура Видманштеттена, состоит из заштрихованной игольчатой структуры ферритовых игл в очень тонком перлите.
Что происходит, когда образец из углеродистой стали с содержанием углерода 0,5 % охлаждают выше температурной линии 723°C, показанной ниже:
Более сложные изменения, происходящие при очень быстром охлаждении аустенита, приводящие к очень твердым структурам, можно объяснить диаграммой время-температура-превращение (3T) или так называемыми S-кривыми из-за их формы (также известными как изотермические превращения).
 ).
).Указано, что при нагреве стали выше линии GS карбид железа в железе разлагается; все железо превратится в у-железо, а весь углерод перейдет в раствор (результирующая структура известна как аустенит). Когда аустенитную сталь резко охлаждают до температуры ниже 723°C и выдерживают при этой температуре в течение разного времени, образуются разные типы структур разной твердости.
Трансформация для разных температур начинается и заканчивается в разное время. S-кривые или ST-кривые представляют собой графики на полулогарифмической бумаге, которые показывают время, когда начинается и заканчивается результирующее превращение, когда аустенитная сталь быстро закаливается до определенной температуры. На рис. 1.15 показана такая кривая.
Можно отметить, что если превращение происходит при температуре около 723°C (A 1 ), полученная структура будет крупноперлитной, а сталь будет относительно мягкой. По мере снижения температуры превращения перлит становится мельче, а сталь тверже.

Эта тенденция продолжается до тех пор, пока не будет достигнута температура около 565°С (А 0 ), ниже которой до температуры 150°С (А 0 ’) образуется новая структура, известная как бейнит. Он состоит из тонкой комбинации карбида железа и феррита. Структура вблизи температуры А 0 напоминает перлит, а вблизи А 0 ‘ более тонкая и твердая, имеет более игольчатую структуру видманштеттенового типа.
Если температура превращения ниже 150°C, то образуется структура, известная как мартенсит. Аустенит в основном состоит из дельта-железа и имеет гранецентрированную кубическую форму, тогда как железо при низких температурах имеет объемно-центрированную кубическую форму.
Таким образом, обычное превращение дельта-железа в альфа-железо при охлаждении требует значительной перестройки атомов железа, для достижения которой требуется время. Если закаливать материал с очень высокой скоростью, то металл не успевает перестроиться и образуется переохлажденное дельта-железо.

Переохлаждение железа из аустенитной формы делает атомы менее подвижными и увеличивает время, необходимое для нормальной дельта-альфа-перегруппировки, и подвергает материал очень большим внутренним напряжениям из-за присутствия избыточного углерода. Конечным результатом является образование искаженной формы феррита с тетрагональным мартенситом. Образовавшийся пересыщенный твердый раствор углерода в объемно-центрированном тетрагональном искаженном феррите очень твердый и хрупкий и известен как мартенсит.
На рис. 1.16 показано образование феррита, перлита и цементита при изменении содержания углерода до 1,2% и изменении механических свойств.
Главная ›› Металлургия ›› Промышленность ›› Металлы ›› Сталь ›› Железоуглеродистые сплавы
Фазовая диаграмма железо-углерод – Edelstahl härten
Углерод является наиболее важным легирующим элементом в железе. По этой причине даже самые незначительные изменения в содержании углерода могут привести к значительным изменениям в характеристиках материала.
 Тем не менее, значение фазовой диаграммы железо—углерод быстро уменьшается, если материал быстро охлаждается или нагревается. Диаграмма также менее информативна, если увеличивается доля других легирующих элементов .
Тем не менее, значение фазовой диаграммы железо—углерод быстро уменьшается, если материал быстро охлаждается или нагревается. Диаграмма также менее информативна, если увеличивается доля других легирующих элементов .Углерод встречается в двух различных формах: во-первых, в связанной форме и, во-вторых, в виде элементарного углерода в форме графита. Вот почему фазовая диаграмма железо-углерод появляется в двух формах . Стабильная система с диаграммой Fe-Graphite и метастабильная с диаграммой Fe-Fe 3 C-диаграмма. Обе системы можно представить на одной диаграмме, хотя на практике в основном используется метастабильная система Fe-Fe 3 C.
Как представлены фазы на фазовой диаграмме железо-углерод?По оси x диаграммы отложен массовый процент углерода. Температура отложена по оси Y. Чтобы сделать диаграмму более наглядной, показано только технически интересное содержание углерода от 0 до 6,67%.
 Сплавы, содержащие углерода более 6,67 %, образуют фазу 100 % цементита
Сплавы, содержащие углерода более 6,67 %, образуют фазу 100 % цементита Поля фаз ограничены линиями, представляющими точки излома, сдвинутые на другие температуры. Для лучшего понимания соответствующие точки обозначены буквами . Обратите внимание, что на некоторых диаграммах точка I обозначена как J. Одной из наиболее важных линий является линия ликвидуса , представленная ломаной ABCD. Выше этой линии сплав находится в жидкой форме. Полилиния AHIECF называется линией солидуса . Ниже этой линии сплав полностью тверд. Если температура находится между ними, сплав имеет кашицеобразную консистенцию. Сплав состоит из остаточного расплава, δ-железа, γ-железа и цементита (Fe 3 С). Пропорции текучие и меняются в зависимости от температуры. Как только при охлаждении сплава температура падает ниже линии ликвидуса, начинается первичная кристаллизация из расплава.
Железо имеет различные аллотропные модификации .
Какое металлографическое обозначение? Таким образом, в зависимости от содержания углерода и температуры образуются разные фазы. Интеркаляционные смешанные кристаллы, образованные δ-, γ- и α-твердыми растворами железа, обладают различной растворимостью углерода. Вариации вызваны различными пространственными решетками и постоянными решетки.
Таким образом, в зависимости от содержания углерода и температуры образуются разные фазы. Интеркаляционные смешанные кристаллы, образованные δ-, γ- и α-твердыми растворами железа, обладают различной растворимостью углерода. Вариации вызваны различными пространственными решетками и постоянными решетки.В металлографии смешанные кристаллы называются δ-ферритом, аустенитом для γ-смешанных кристаллов и ферритом для α-смешанных кристаллов. Here is an overview of the carbon content of the individual phases :
Designation
Max C-content
Metallographic designation
Δ-SOLID раствор
0,10 % BEI 1493 ° C
Δ-Ferrite
γ-Solid Solution 9000
γ-Solid Solution 9000
06060601101010101010101010110110101011011101105051050505.
9000
9000
9000
. Austenite
α-solid solution
0,02 % bei 723° C
Ferrite
Cementite (Fe 3 C) is an iron-carbon compound что также является фазой. Тем не менее, цементит является промежуточная фаза , которую не следует путать со смешанными кристаллами железа. Химический состав цементита всегда одинаков, хотя он встречается в трех различных формах :
- Первичный цементит: первичная кристаллизация из расплава (соответствует линии CD)
- Вторичный цементит: выделение из аустенита (соответствует линии ES)
- Третичный цементит: выделение из феррита (соответствует линии PQ)
Вторичный цементит присутствует при содержании углерода от 2,06 до 4,3 % C, но не показан на диаграмме.
 Это связано с тем, что его нельзя обнаружить металлографически.
Это связано с тем, что его нельзя обнаружить металлографически.In addition to the phases, phase mixtures also occur:
Какие изотермические реакции показаны на фазовой диаграмме железо-углерод?Designation
Consists of
Area of existence
Perlite
88 % Феррит / 12 % цементит
0,02 % – 6,67 % BEI T ≤ 723 ° C
ledeburite I
Austenite I
%.
 cementite
cementite2,06 % – 6,67 % bei 723° C ≤ 1147° C
Ledeburite II
51,4 % Perlite / 48,6 % cementite
2 ,06 % – 6,67 % при T ≤ 723°C
Три изотермические реакции показаны на фазовой диаграмме железо-углерод. Линия HIB представляет собой перитектику, линия ECF — эвтектику, а левая PSK — эвтектоидную реакцию.
При нагреве или охлаждении стали на линиях происходят превращения. Они отмечены точками останова. Вот наиболее важные из них:
- На линии P-S-K аустенит распадается на перлит , если содержание углерода менее 0,02 % (А 1 ).
- Феррит теряет ферромагнетизм на линии M-O при нагревании выше 769°C (A 2 )
- Если температура падает ниже линии G-O-S во время охлаждения, образуется низкоуглеродистый феррит .
 В ходе этого процесса аустенит накапливается с выделяющимся углеродом до тех пор, пока температура не поднимется до 723°С и не достигнет эвтектоидной концентрации (А 3 ).
В ходе этого процесса аустенит накапливается с выделяющимся углеродом до тех пор, пока температура не поднимется до 723°С и не достигнет эвтектоидной концентрации (А 3 ).
Фазовая диаграмма железо-углерод помогает лучше понять поведение чугуна и стали. Сталь, например, легко формуется в диапазоне аустенита и поэтому может быть кована. С другой стороны, чугун имеет более высокую долю углерода, который присутствует в форме графита и ледебурита. Это значительно ограничивает пластичность.
По этой причине диаграмма железо-углерод становится важным инструментом для оценки стали и чугуна .
Фазовая диаграмма Fe-C — химия твердого тела @Aalto
Перейти к концу метаданных
Фазовые диаграммы — одна из самых важных диаграмм в материаловедении. Такие диаграммы несут в себе массу полезной информации: температуры плавления каждого из материалов, взаимный предел их растворимости друг в друге в различном диапазоне температур, какая микроструктура будет у сплава при определенной концентрации и температуре и многое другое.
 . На фазовых диаграммах ось абсцисс (горизонтальная линия) представляет весовой процент (мас.%) или атомный процент (ат.%) концентрации одного материала в другом. Как правило, концентрация вещества B постепенно увеличивается слева направо, и на правом конце оси концентрации она составляет 100 %, поэтому это чистый материал B. Ось ординат (вертикальная линия) представляет диапазон температур (обычно диапазон от 0 до o °С, чуть выше температуры плавления каждого из материалов, представленных на диаграмме).
. На фазовых диаграммах ось абсцисс (горизонтальная линия) представляет весовой процент (мас.%) или атомный процент (ат.%) концентрации одного материала в другом. Как правило, концентрация вещества B постепенно увеличивается слева направо, и на правом конце оси концентрации она составляет 100 %, поэтому это чистый материал B. Ось ординат (вертикальная линия) представляет диапазон температур (обычно диапазон от 0 до o °С, чуть выше температуры плавления каждого из материалов, представленных на диаграмме).Из всех фазовых диаграмм фазовая диаграмма железо-углерод является самой важной, так как с помощью этой диаграммы можно получать различные стали и чугуны, которые играют решающую роль в любой технологически развитой цивилизации.
Рисунок 1. Пример бинарной фазовой диаграммы для произвольных материалов A и B (Рисунок: Никита Бобров).
Типичная бинарная (система из двух материалов) фазовая диаграмма показана на Рисунок 1 .
 Как правило, он состоит из различных областей: область α + β показывает случай, когда присутствуют как α-, так и β-фазы материалов A и B соответственно. Обычно существует определенный предел растворимости материала А в В (и наоборот) и выше этого предела растворимости для материала В в кристаллической структуре материала А уже нет места и он начинает образовывать отдельные зернистые включения, полностью состоящие из материала B (т.е. состоящий из β-фазы). Область α показывает случай, когда предел растворимости еще не достигнут и материал B в той или иной форме включен в кристаллическую структуру материала A (то же самое относится и к области β). L или жидкая область показывает случай, когда оба материала A и B присутствуют в жидкой фазе. Области α + L показывают случай, когда α-фаза материала A присутствует с некоторым кристаллическим включением или концентрацией материала B и отдельным включением чистого материала B в жидкой фазе (то же самое, но наоборот относится к β + L область).
Как правило, он состоит из различных областей: область α + β показывает случай, когда присутствуют как α-, так и β-фазы материалов A и B соответственно. Обычно существует определенный предел растворимости материала А в В (и наоборот) и выше этого предела растворимости для материала В в кристаллической структуре материала А уже нет места и он начинает образовывать отдельные зернистые включения, полностью состоящие из материала B (т.е. состоящий из β-фазы). Область α показывает случай, когда предел растворимости еще не достигнут и материал B в той или иной форме включен в кристаллическую структуру материала A (то же самое относится и к области β). L или жидкая область показывает случай, когда оба материала A и B присутствуют в жидкой фазе. Области α + L показывают случай, когда α-фаза материала A присутствует с некоторым кристаллическим включением или концентрацией материала B и отдельным включением чистого материала B в жидкой фазе (то же самое, но наоборот относится к β + L область).
Линии AB и DE называются линии solvus (эти линии показывают максимальный предел растворимости для каждого из материалов при определенной температуре), линии BF и DG называются линиями solidus (эти линии показывают максимальную концентрацию материала В в материале А, в котором еще присутствует только твердая фаза, присутствует при определенной температуре и наоборот), а линии FC и CG называются ликвидус линии (эти линии показывают максимальную температуру, при которой оба материала начинают находиться в жидкой фазе при определенной концентрации) [1, с.312-313] . Точка C на фазовой диаграмме называется эвтектической точкой (или инвариантной точкой), а линия BD называется эвтектической изотермой .
 Именно в этот момент при температуре
\(Т_С\)
и концентрация
\(с_С\)
происходит важная реакция: обе α- и β-фазы материалов А и В сразу переходят в жидкое состояние без промежуточного перехода через α + L или β + L регионов. Диаграммы состояния, обладающие таким прямолинейным переходом из твердой в жидкую (или другую твердую) фазу обеих составляющих сплава, называются эвтектическими фазовыми диаграммами [2, с.298-301] . Точки F и G показывают температуры плавления материалов A и B соответственно, а точки B и D показывают максимально возможную температуру, необходимую для этого предела растворимости (и D ). быть достигнуто) материала B в материале A и наоборот.
Именно в этот момент при температуре
\(Т_С\)
и концентрация
\(с_С\)
происходит важная реакция: обе α- и β-фазы материалов А и В сразу переходят в жидкое состояние без промежуточного перехода через α + L или β + L регионов. Диаграммы состояния, обладающие таким прямолинейным переходом из твердой в жидкую (или другую твердую) фазу обеих составляющих сплава, называются эвтектическими фазовыми диаграммами [2, с.298-301] . Точки F и G показывают температуры плавления материалов A и B соответственно, а точки B и D показывают максимально возможную температуру, необходимую для этого предела растворимости (и D ). быть достигнуто) материала B в материале A и наоборот.Рис. 2. Построение зубчатой линии на бинарной фазовой диаграмме для двух произвольных материалов А и В (рис.
 : Никита Бобров).
: Никита Бобров).Представьте, что у нас есть некий сплав, который состоит из двух материалов A и B при определенной концентрации c и температуре T . Если он состоит более чем из одной фазы (например, α и β), мы хотели бы знать фактическое количество фаз α и β материалов A и B, присутствующих в сплаве, и атомную концентрацию составляющего материала в этих фазах. (фаза α имеет определенную концентрацию материала B, а фаза β имеет в ней определенную концентрацию материала A). Чтобы получить эту информацию, так называемые 9Необходимо построить соединительную линию 0820 . Она проходит через точку М (точка, в которой в данный момент находится сплав) параллельно оси концентрации до пересечения с линиями, составляющими границу областей фаз, присутствующих в данный момент в сплаве ( линии сольвуса, ликвидуса или солидуса). В частности, точка \(с_\альфа\) – концентрация вещества B в фазе α и \( с_\бета \) – концентрация вещества B в фазе β ( Рисунок 2 ).
 Для получения массовых процентов (или атомных процентов) количества фаз α и β, присутствующих в сплаве, можно использовать так называемое правило рычага , которое следует формулам:
Для получения массовых процентов (или атомных процентов) количества фаз α и β, присутствующих в сплаве, можно использовать так называемое правило рычага , которое следует формулам:\[W_\alpha=\frac{|c_\beta-c|}{|c_\alpha-c_\beta|}; \] \[ W_\beta=\frac{|c_\alpha-c|}{|c_\alpha-c_\beta|}; \]
, где \(W_\альфа\) а также \(W_\бета\) – весовые проценты относительных количеств α- и β-фаз, присутствующих в сплаве в точке M соответственно и \(с\) – это общая концентрация материала В, присутствующего в сплаве в точке M (см. Рисунок 2 ).
По тем же формулам можно рассчитать относительные концентрации и количества любых двух фаз, присутствующих в сплаве при данной температуре и составе (например, α + L , β + L и т. д.) [1, с. .314-316] . Рисунок 3. Бинарная фазовая диаграмма железо-углерод (карбид железа)
На рисунке 3 показана часть диаграммы состояния железо-углерод.
 На первый взгляд это может показаться очень перегруженным и трудным для интерпретации, однако, как вы увидите дальше, это совсем не так. Чистое железо (крайняя левая вертикальная линия на рис. 3 ) при комнатной температуре имеет стабильную форму, называемую α-ферритом , которая имеет объемно-центрированную кубическую кристаллическую структуру. При нагревании до 911 o С (точка G ) железо переходит в γ-фазу, называемую аустенит , который имеет гранецентрированную кубическую кристаллическую структуру. При последующем нагреве при 1392 o C (точка N ) железо переходит в фазу δ-феррита (имеющую объемно-центрированную кристаллическую структуру), которая затем плавится в жидкую фазу при 1536 o C (точка А ). Углерод при смешивании с железом ниже предела растворимости ведет себя как примесь внедрения, присутствуя в структуре железа, увеличивает его твердость, но делает более хрупким.
На первый взгляд это может показаться очень перегруженным и трудным для интерпретации, однако, как вы увидите дальше, это совсем не так. Чистое железо (крайняя левая вертикальная линия на рис. 3 ) при комнатной температуре имеет стабильную форму, называемую α-ферритом , которая имеет объемно-центрированную кубическую кристаллическую структуру. При нагревании до 911 o С (точка G ) железо переходит в γ-фазу, называемую аустенит , который имеет гранецентрированную кубическую кристаллическую структуру. При последующем нагреве при 1392 o C (точка N ) железо переходит в фазу δ-феррита (имеющую объемно-центрированную кристаллическую структуру), которая затем плавится в жидкую фазу при 1536 o C (точка А ). Углерод при смешивании с железом ниже предела растворимости ведет себя как примесь внедрения, присутствуя в структуре железа, увеличивает его твердость, но делает более хрупким. При превышении 6,67 мас.% состава углерода в железе сплав переходит в соединение карбид железа \( Fe_3C \)
который также называют цементитом (он показан вертикальной линией FK справа от Рисунок 3 ), поэтому технически правильнее называть такую диаграмму фазовой диаграммой железо-карбид железа. Сплав железа, содержащий от 0 до 2,06% углерода по весу, называется сталью, а тот, который содержит от 2,06 до 6,67%, называется чугуном, однако в большинстве практических случаев концентрация углерода в сплавах железа не превышает 1% по весу. Железо-железный карбид эвтектическая фазовая диаграмма с точкой эвтектики S при температуре 723 o C и содержании углерода 0,8 мас.% (есть еще одна эвтектическая точка C при температуре 1147 o C и концентрации углерода 90,793 мас. %). , однако это не будет обсуждаться на этой странице). [1, с.562-565] .
При превышении 6,67 мас.% состава углерода в железе сплав переходит в соединение карбид железа \( Fe_3C \)
который также называют цементитом (он показан вертикальной линией FK справа от Рисунок 3 ), поэтому технически правильнее называть такую диаграмму фазовой диаграммой железо-карбид железа. Сплав железа, содержащий от 0 до 2,06% углерода по весу, называется сталью, а тот, который содержит от 2,06 до 6,67%, называется чугуном, однако в большинстве практических случаев концентрация углерода в сплавах железа не превышает 1% по весу. Железо-железный карбид эвтектическая фазовая диаграмма с точкой эвтектики S при температуре 723 o C и содержании углерода 0,8 мас.% (есть еще одна эвтектическая точка C при температуре 1147 o C и концентрации углерода 90,793 мас. %). , однако это не будет обсуждаться на этой странице). [1, с.562-565] .
Эвтектоидный состав
Рис. 4. Схема фазового превращения железоуглеродистого сплава эвтектоидного состава : CC BY-SA 4.0, модифицированный Никитой Бобровым).
На рис. 4 показано фазовое превращение сплава эвтектоидного состава [3, с.146-147] . Он начинается в точке и при содержании 0,8 мас.% и около 900 o °С. Поскольку эта точка находится в области γ-аустенитной фазы, сплав полностью состоит из γ-аустенита, который, как схематически показано на включении в Рисунок 4 . При медленном охлаждении сплав движется вдоль \(хх’\) оси и при прохождении через точку эвтектики γ-фазное железо (аустенит) претерпевает переход в α-феррит, а часть углерода, содержащегося в сплаве, образует цементит в виде очень тонких «полос», образующих колонии различного размера и форма. В каждой из этих колоний цементит имеет одинаковую ориентацию, меняющуюся от колонии к колонии – такая структура называется перлит (структура перлита схематично показана во включении рис.
 4 в точке б ) [4] . Относительная толщина «полосок» α-феррита по отношению к «полоскам» цементита составляет приблизительно 8:1. Для оценки относительного количества цементита и феррита, присутствующих в сплаве, и содержания в них углерода необходимо построить соответствующую линию, которая пересекает линии QP и KF диаграммы.
4 в точке б ) [4] . Относительная толщина «полосок» α-феррита по отношению к «полоскам» цементита составляет приблизительно 8:1. Для оценки относительного количества цементита и феррита, присутствующих в сплаве, и содержания в них углерода необходимо построить соответствующую линию, которая пересекает линии QP и KF диаграммы.Доэвтектоидный состав
Рис. 5. Схемы фазового превращения железоуглеродистого сплава доэвтектоидного состава : CC BY-SA 4.0, модифицированный Никитой Бобровым).
В случае, когда концентрация углерода в сплаве меньше эвтектоидной, его называют доэвтектоидным ( гипо- означает под эвтектоид) состав [5, с.10-12] . Типичный пример превращения сплава, содержащего углерод доэвтектоидного состава, показан на рис. 5 . В точке f (приблизительно при 1100 o C, см.
 включение в Рисунок 5 ) сплав будет состоять только из аустенитной фазы с концентрацией углерода около 0,04 мас.%. При медленном охлаждении сплав будет следовать
\(гг’\)
ось на фазовой диаграмме. Сразу после прохождения линии GS в точке g включения фазы α-феррита начнут формироваться между границами зерен γ-аустенита (см. включение в Рисунок 5 ). Относительные количества и концентрации каждой из фаз можно рассчитать, построив соответствующую связующую линию, которая будет пересекать линии GP (составляющие точки
\(с_\альфа\)
) и GS (подчеркивая
\(с_\гамма\)
). По мере дальнейшего охлаждения сплава непосредственно перед пересечением изотермы эвтектики (линия ПК ) в точке h включения α-феррита будут увеличены (занимая все пространство между границами зерен γ-аустенита) и будут иметь концентрацию углерода 0,02 мас.
включение в Рисунок 5 ) сплав будет состоять только из аустенитной фазы с концентрацией углерода около 0,04 мас.%. При медленном охлаждении сплав будет следовать
\(гг’\)
ось на фазовой диаграмме. Сразу после прохождения линии GS в точке g включения фазы α-феррита начнут формироваться между границами зерен γ-аустенита (см. включение в Рисунок 5 ). Относительные количества и концентрации каждой из фаз можно рассчитать, построив соответствующую связующую линию, которая будет пересекать линии GP (составляющие точки
\(с_\альфа\)
) и GS (подчеркивая
\(с_\гамма\)
). По мере дальнейшего охлаждения сплава непосредственно перед пересечением изотермы эвтектики (линия ПК ) в точке h включения α-феррита будут увеличены (занимая все пространство между границами зерен γ-аустенита) и будут иметь концентрацию углерода 0,02 мас. % (точка P ), в то время как γ-аустенитная фаза будет иметь эвтектическую концентрацию углерода 0,8% по весу (точка S ), как видно на включении Рисунок 5 . Поскольку зерна γ-аустенитной фазы имеют эвтектическую концентрацию, они будут испытывать такой же переход, как и в сплаве эвтектоидного состава, т. е. перейдут в структуру перлита (см. включение в пункте j в рис 5 ). Фаза α-феррита, расположенная между зернами перлита, называется доэвтектоидным α-ферритом ( про- означает уже образовавшуюся до того, как пересечет изотерму эвтектики), а α-феррит, присутствующий внутри зерен перлита называется эвтектоидным α-ферритом , так как он образуется при пересечении эвтектической изотермы (мы разделяем их только потому, что они занимают разное место в микроструктуре доэвтектоидного сплава, но обе эти фазы α-феррита имеют одинаковую концентрацию углерода в них, что можно рассчитать, построив соответствующую связующую линию, которая будет пересекать линии PQ и FK ) [2, стр.
% (точка P ), в то время как γ-аустенитная фаза будет иметь эвтектическую концентрацию углерода 0,8% по весу (точка S ), как видно на включении Рисунок 5 . Поскольку зерна γ-аустенитной фазы имеют эвтектическую концентрацию, они будут испытывать такой же переход, как и в сплаве эвтектоидного состава, т. е. перейдут в структуру перлита (см. включение в пункте j в рис 5 ). Фаза α-феррита, расположенная между зернами перлита, называется доэвтектоидным α-ферритом ( про- означает уже образовавшуюся до того, как пересечет изотерму эвтектики), а α-феррит, присутствующий внутри зерен перлита называется эвтектоидным α-ферритом , так как он образуется при пересечении эвтектической изотермы (мы разделяем их только потому, что они занимают разное место в микроструктуре доэвтектоидного сплава, но обе эти фазы α-феррита имеют одинаковую концентрацию углерода в них, что можно рассчитать, построив соответствующую связующую линию, которая будет пересекать линии PQ и FK ) [2, стр. 324-326] .
324-326] .Заэвтектоидный состав
Рис. 6. Схемы фазового превращения железоуглеродистого сплава заэвтектоидного состава : CC BY-SA 4.0, модифицированный Никитой Бобровым).
В случае, когда концентрация углерода в сплаве выше эвтектоидного, его называют заэвтектоидным ( гипер- означает над эвтектоидным) состава [5, с.13-15] . Заэвтектоидный сплав будет претерпевать почти те же фазовые превращения, что и доэвтектоидный сплав, с той лишь разницей, что вместо α-ферритной фазы между границами зерен γ-аустенита образуется цементитная фаза ( \( Fe_3C \) ) сформируется. А именно, если посмотреть на пример фазового превращения заэвтектоидного сплава в рис. 6 , оно сначала начнется в точке ч , состоящей исключительно из γ-аустенита при температуре около 1100 o °С и 0,13 мас.% концентрации углерода. При медленном охлаждении сплав будет следовать \(зз’\) линии на фазовой диаграмме.
 После пересечения линии SE сплав войдет в γ+
\( Fe_3C \)
область и цементит (
\( Fe_3C \)
) начнет формироваться между границами зерен γ-аустенита (см. схематические включения в точке k на рис. 6 ). При дальнейшем охлаждении в точке l включения цементита будут увеличиваться, охватывая все пространство между границами зерен γ-аустенита. В этой точке (и в любой другой точке диаграммы) цементит будет иметь состав углерода 6,67 мас.%, а γ-аустенит будет иметь эвтектоидный состав углерода 0,8 мас.% (правильная связующая линия 9).0804 SK или другими словами эвтектическая изотерма). После пересечения изотермы эвтектики γ-аустенит эвтектоидного состава образует перлит (как в эвтектоидном сплаве). Цементит, находящийся между границами зерен перлита, называется доэвтектоидным цементитом (тот, который уже образовался до пересечения эвтектической изотермы), а тот, что присутствует в микроструктуре перлита, называется эвтектоидным цементитом (см.
После пересечения линии SE сплав войдет в γ+
\( Fe_3C \)
область и цементит (
\( Fe_3C \)
) начнет формироваться между границами зерен γ-аустенита (см. схематические включения в точке k на рис. 6 ). При дальнейшем охлаждении в точке l включения цементита будут увеличиваться, охватывая все пространство между границами зерен γ-аустенита. В этой точке (и в любой другой точке диаграммы) цементит будет иметь состав углерода 6,67 мас.%, а γ-аустенит будет иметь эвтектоидный состав углерода 0,8 мас.% (правильная связующая линия 9).0804 SK или другими словами эвтектическая изотерма). После пересечения изотермы эвтектики γ-аустенит эвтектоидного состава образует перлит (как в эвтектоидном сплаве). Цементит, находящийся между границами зерен перлита, называется доэвтектоидным цементитом (тот, который уже образовался до пересечения эвтектической изотермы), а тот, что присутствует в микроструктуре перлита, называется эвтектоидным цементитом (см. схема включения в точке м в Рисунок 6 ) [2, с.327-328] .
схема включения в точке м в Рисунок 6 ) [2, с.327-328] .Механические свойства железоуглеродистых сплавов
Микроструктура различных сплавов и их состав оказывают непосредственное влияние на их механические свойства. В целом, как уже упоминалось, более высокая концентрация углерода в железе увеличивает его твердость, но делает его более хрупким. Сплавы доэвтектоидного состава являются одними из самых мягких и пластичных, так как доэвтектоидный α-феррит, внедренный между зернами перлита, сравнительно мягок и способствует неразрушающему пластическому и упругому удлинению образца при приложении нагрузки. Заэвтектоидные железоуглеродистые сплавы значительно тверже и менее пластичны, чем сплавы доэвтектоидного состава, так как доэвтектоидный цементит, присутствующий между границами зерен перлита, представляет собой очень прочный и хрупкий материал, не выдерживающий высокого удлинения при приложении внешней силы и разрушения в хрупкий способ.
 Железоуглеродистые сплавы эвтектоидного состава полностью состоят из зерен перлита и имеют промежуточную вязкость и пластичность между доэвтектоидными и заэвтектоидными сплавами [6] [7] .
Железоуглеродистые сплавы эвтектоидного состава полностью состоят из зерен перлита и имеют промежуточную вязкость и пластичность между доэвтектоидными и заэвтектоидными сплавами [6] [7] .Из всех железоуглеродистых сплавов чугуны обладают наибольшей твердостью и наиболее хрупкими. Их очень трудно сварить (из-за высокого содержания углерода) и обычно при больших нагрузках они хрупко разрушаются. Чугуны используются во многих отраслях промышленности: головки и блоки двигателей, станки, поворотные кулаки, шестерни, компоненты автомобильных тормозов, клапаны, насосы, горные буры и многие другие. Чугуны используются даже в повседневных целях, например, для изготовления заборов и даже сковородок. Способность чугунной посуды выдерживать высокие температуры делает ее хорошим выбором для изготовления сковородок, а способность долго отдавать тепло делает ее очень удобной для томления и тушения. Также из-за высокой твердости на них очень сложно оставить царапины простыми половниками и ложками, что продлевает их службу в качестве посуды для приготовления пищи.
 Однако, как и все другие ферросплавы, чугуны подвержены ржавчине, а значит, кухонная утварь, изготовленная из него, нуждается в надлежащем уходе и хранении.
Однако, как и все другие ферросплавы, чугуны подвержены ржавчине, а значит, кухонная утварь, изготовленная из него, нуждается в надлежащем уходе и хранении.В реальных применениях стали содержат другие элементы (кроме углерода) в своем сплаве, такие как Ni , W , Mo , Cr , V и многие другие. Таким образом, могут существовать многомерные фазовые диаграммы. Кроме того, в условиях реального производства обычно равновесное охлаждение невозможно, так как оно требует много времени и энергии. Более того, во многих случаях неравновесное охлаждение полезно для большого количества приложений. На самом деле большинство сталей производится в неравновесной среде [2, с.329-330]
. Имеются многочисленные фазовые диаграммы, показывающие зависимость скорости охлаждения от конечной микроструктуры сплава и, следовательно, от его конечных физико-механических свойств [2, с.
 356-378] .
356-378] .[1] 1 2 3 Р. Аббасчян, Лара Аббашян, Роберт Э. Рид-Хилл, Принципы физической металлургии, Cengage Learning, США, 2008
[2] 1 2 3 4 5 Уильям Д. Каллистер-младший, Дэвид Г. Ретвиш, Материаловедение и инженерия: введение, Wiley, США, 2014
[3] 1 Дэниел А. Брандт, Дж. К. Уорнер, Основы металлургии, издательство Goodheart-Wilcox, США, 2004
[4] 1 Эмбери Дж. Д., Фишер Р. М., Структура и свойства вытянутого перлита, Acta Metallurgica, 1966 , 14, 147-159 (10.1016/0001-6160(66)-3)
[5] 1 2 Дж.

- Бейнит – фаза между перлитом и мартенситом. Это твердый метастабильный микрокомпонент, состоящий из непластинчатой смеси феррита и цементита в очень мелком масштабе. Верхний бейнит образуется при более высоких температурах и имеет перистый вид. Нижний бейнит образуется при более низких температурах и имеет игольчатый вид. Твердость бейнита увеличивается с понижением температуры его образования.

