Для чего используется карбид кальция: Карбид кальция
alexxlab | 29.02.1988 | 0 | Разное
Карбид кальция: хранение, получение, реакция
При щелочной реакции углерода с металлами могут получится различные карбиды. За счет соединения определенных химических элементов получаются соединения, которые характеризуются высокой прочностью. Довольно большое распространение получил вариант исполнения, который получил название карбид кальция. Его стали применять в самых различных областях промышленности.
Карбид кальция
Содержание
Внешний вид и характеристики технического карбида кальция
Впервые рассматриваемый состав был получен в 1862 году. Проводимая процедура касалась отделения кальция от извести, в результате чего получился бледно-серый состав без признаков, свойственных металлам. В результате опыта был получен карбид, который в последствии стал активно использоваться при выпуске различной продукции.
В начале 20 века карбид кальция стали использовать для производства ацетилена в больших объемах. Именно поэтому стали вести активные исследования для выявления более производительной технологии.
Технические характеристики материала определяют его широкое распространение. Внешний вид вещества характеризуется светло-серым цветом, выпускаются карбиды в виде камня или порошка.
Физические свойства
При выборе практически любого материала следует уделять больше всего внимания физическим свойствам. У рассматриваемого они следующие:
- Соединение имеет кристаллическую структуру.
- Показатель температуры плавления составляет 2300 °С. Стоит учитывать, что подобная цифра свойственна только чистому составу. Добавление в состав различных примесей приводит к тому, что температура плавления существенно падает.
Чистый карбид кальция
Стоит учитывать, что карбид кальция в большинстве случаев находится в твердом состоянии. Кроме этого, цвет может варьироваться от серого до коричневого цвета. Физические свойства карбида кальция определяют его широкое применение в самых различных отраслях промышленности.
Химические свойства
Немаловажное значение имеют и химические свойства. Они также учитываются при применении материала. К основным характеристикам можно отнести следующие качества:
Они также учитываются при применении материала. К основным характеристикам можно отнести следующие качества:
- Карбид кальция характеризуется тем, что хорошо впитывает влагу. Стоит учитывать, подобная процедура проявляется яркой химической реакцией, связанной с разложением вещества.
- При работе с рассматриваемым материалом стоит учитывать, что образующаяся пыль оказывает раздражительный эффект на слизистые органы. Кроме этого, подобная реакция может проявится при попадании кристаллов или пыли на поверхность кожи. Именно поэтому при работе с рассматриваемым соединением следует использовать респиратор и некоторые другие средства защиты.
- Кристаллы активное реагируют на воздействие других веществ зачастую только при нагреве. При этом может образоваться карбонат кальция.
- В некоторых случаях проводится соединение кристаллического вещества с азотом, в результате чего получается цианамид кальция.
- При нагреве может проходить реакция с мышьяком и хлором, а также фосфором.

Карбонат кальция
Считается, что наиболее важным химическим качеством является податливость к разложению при воздействии воды.
Получение
Как ранее было отмечено, карбид кальция активно применяется при получении самых различных материалов. Именно поэтому процесс получения карбида кальция постоянно совершенствовался. К особенностям применяемых технологий можно отнести нижеприведенные моменты:
- В качестве сырья применяется негашеная известь. В большинстве случаев вещество получается из извести, но в домашних условиях провести подобную процедуру сложно.
- Известь смешивается с измельченном коксом для получения однородной массы.
- В промышленности карбид кальция получают по схеме, которая предусматривает нагрев вещества до высокой температуры. Для этого применяются электронные печи. Рекомендуемая температура плавления составляет 1900 ⁰С.
- После нагрева вещества до столь высокой температуры оно переходит в жидкое состояние. Для работы подготавливаются специальные формы.

При рассмотрении того, как из углерода получить карбид кальция отметим, что по установленным стандартам в состав должно входить не менее 80% основного вещества. На долю примесей должно приходится не более 25%, в число которых также входит углерод. Производство оксида кальция также приводит к выделению тепловой энергии, что стоит учитывать.
Транспортировка и хранение
Порошок карбида кальция при воздействии влаги практически моментально разлагается. При этом образуется ацетилен, который при большой концентрации горюч и взрывоопасный. Именно поэтому нужно уделять довольно много внимания хранению карбида кальция, для чего часто применяют бидоны и специальные барабаны. К другим особенностям хранения отнесем следующие моменты:
- Выделяющийся ацетилен легче воздуха, поэтому скапливается вверху.
 Стоит учитывать, что он обладает наркотическими действиями, может самовоспламеняться.
Стоит учитывать, что он обладает наркотическими действиями, может самовоспламеняться. - При производстве большого объема вещества особое внимание уделяется технике безопасности. Для фасовки применяются специальные упаковки.
- Для открытия упаковки следует использовать инструменты, которые не становятся причиной образования искр.
- Если вещество попадает на кожу или слизистую оболочку, то его нужно сразу удалить. При этом пострадавшая поверхность обрабатывается специальным кремом или другим защитно-заживляющим веществом.
- По установленным правилам, транспортировка может проводится исключительно при применении крытого транспортного средства. При этом проводить доставку по воздуху запрещается.
Контейнер для транспортировки
Установленные правила также запрещают хранить карбид кальция вместе с другими химическими веществами и источниками тепла. Это связано с тем, что образующиеся газы могут вступать в химическую реакцию с другими химическими веществами и возгораться.
Применение карбида кальция
Как ранее было отмечено, карбид кальция встречается в самых различных областях промышленности, зачастую поставляют для проведения промышленного синтеза. Свойства карбида кальция и реакция, протекающая при его соединении с различными веществами, определяют использование вещества в нижеприведенных случаях:
- Многие синтетически компоненты, входящих в состав современных материалов, производят на основе рассматриваемого компонента.
- Применяется для получения цианамида кальция. Подобный компонент используется для получения различных химических удобрений. Именно поэтому сырье применяется для регулирования скорости роста растений.
- Цианамид кальция также получают при соединении вещества с азотом.
- В некоторых случаях проводится восстановление металлов щелочной группы.
- Можно использовать рассматриваемое соединение в процессе газовой сварки.
При рассмотрении карбида кальция и области применения стоит учитывать, что подобное вещество чаще всего применяют для получения ацетилена. Подобный синтез карбида кальция разработал немецкий ученый. Среди особенностей подобного способа применения отметим следующие моменты:
Подобный синтез карбида кальция разработал немецкий ученый. Среди особенностей подобного способа применения отметим следующие моменты:
- Ацетилен из карбида получают при оказании воздействия водой на используемое сырье.
- В результате прохождения химической реакции образуется требующийся газ, гашеная известь выпадает в осадок.
- Стоит учитывать, что при смешивании компонентов выделяется большое количество тепла. Поэтому работа должна проводится с учетом техники безопасности.
- В зависимости от вида применяемой технологии переработки сырья с 1 килограмма выходит около 290 литров газа.
- Скорость протекания процедуры зависит от чистоты применяемого сырья, температуры и количества воды.
Получение ацетилена из карбида кальция
Как показывает практика, при использовании чистого карбида на протекание химической реакции отводится около 20 литров волы на 1 килограмм сырья. Подобное количество воды требуется для того чтобы снизить температуру реакции, за счет чего обеспечиваются оптимальные условия для работы.
Техника безопасности
При проведении различных химических реакций для производства материалов должна соблюдаться техника безопасности. Как ранее было отмечено, выделяемые вещества могут быть взрывоопасными. Техника безопасности при взаимодействии с различными химическими веществами заключается в следующем:
- Для хранения и обработки требуется герметичное место. В обычном гараже проводить работы не рекомендуется.
- Нельзя допускать огонь к самому сырью, а также образующимся газам.
- Даже мелкие частицы могут привести к поражению кожных покровов. Именно поэтому работа должна проводится в респираторе и защитной одежде.
- Генераторы ацетилена размещают исключительно в хорошо изолированных помещениях.
- Если сырье применялось при проведении сварочных работ, то следует образующийся шлак утилизировать в специальных местах.
- При перемещении металлических и иных емкостей они должны быть надежно закреплены, столкновение и падение не допускается.
 Это может привести к появлению искр, которые станут причиной взрыва вещества.
Это может привести к появлению искр, которые станут причиной взрыва вещества.
Горение карбида кальция
Вышеприведенная информация определяет то, что работы с рассматриваемым сырьем не рекомендуется проводить в гараже или домашней мастерской. Несоблюдении технологии, отсутствии требующего оснащения и многие другие причины могут привести к возникновению искры и воспламенению веществ.
Карбид кальция реакция с водой
Рассматриваемое сырье чаще всего применяется для соединения с водой, в результате чего получается ацетилен. Взаимодействие карбида кальция с водой становится причиной появления газа с неприятным запахом и достаточно большим количеством различных примесей. В чистом виде получить подобное вещество можно только при его многоэтапной очистке.
Реакция карбида кальция с водой может быть проведена опытным путем. К особенностям подобной процедуры отнесем следующие моменты:
- В качестве емкости применяется 1,5-литровая бутылка.
- После ее заполнения водой добавляется несколько кусочков кристаллического материала.

- Протекание реакции приводит к появлению избыточного давления.
- После того как карбид кальция больше не вступает в реакцию, на бутылку помещается горящая бумага. В результате взаимодействия между карбидом кальция и водой образуется газ, который взрывается. При рассматриваемом опыте образуется огненное облако.
Подобный опыт довольно опасен и должен быть проведен с соблюдением техники безопасности.
В заключение отметим, что рассматриваемый компонент в последнее время часто применяется для проведения самых различных опытов. Соединение обладает большим количеством свойств, которые должны учитываться. Выделение тепла и газов становится причиной, по которой проводить опыты рекомендуется только в промышленности.
Карбид кальция — свойства, получение и применение
Содержание
- История получения
- Получение
- Физические свойства
- Химические свойства
- Внешний вид и характеристики технического карбида кальция
- Область применения карбида кальция
- Физиологическое действие
Карбид кальция — CaC2 — в чистом виде белое кристаллическое вещество. Бинарное неорганическое соединение кальция с углеродом.
Бинарное неорганическое соединение кальция с углеродом.
История получения
Впервые получен в 1861 году Фридрихом Вёлером нагреванием сплава цинка и кальция с углём.
Получение
В настоящее время получают прокаливанием в электрических печах (температура 1900—1950 °C) смеси оксида кальция с коксом.
Полученный таким образом технический продукт имеет чисто-черный цвет вследствие загрязнения углём и другими красящими примесями. Он содержит также примеси фосфида и сульфида кальция, вследствие чего такой карбид кальция и полученный из него ацетилен имеют неприятный запах.
Физические свойства
- Бесцветные тетрагональные кристаллы.
- Плотность: 2,2 (+20 °C, г/см3).
- Удельная теплоёмкость при постоянном давлении (в Дж/г·K): 0,92 (+20—325 °C).
- Стандартная энтальпия образования ΔfH (298 К, кДж/моль): −62,8 (т).
- Стандартная энергия Гиббса образования ΔfG (298 К, кДж/моль): −67,8 (т).

- Стандартная энтропия образования S (298 К, Дж/моль·K): 70,3 (т).
- Стандартная мольная теплоёмкость Cp (298 К, Дж/моль·K): 62,34 (т).
- Энтальпия плавления ΔHпл (кДж/моль): 32,2.
- Карбид кальция имеет резкий чесночный запах.
Химические свойства
При взаимодействии c водой карбид кальция гидролизуется с образованием ацетилена и гидроксида кальция (гашёной извести):
Представленная выше реакция является экзотермической. Следует иметь в виду, что реакция карбида кальция с водой протекает очень бурно. При нарушении правил техники безопасности при проведении этой реакции возможно получение травм и ожогов.
Внешний вид и характеристики технического карбида кальция
Карбид кальция получают сплавлением в электрических печах кокса и негашеной извести. Расплавленный карбид кальция выпускается из печи в специальные формы — изложницы, в которых он затвердевает. Застывший карбид кальция дробится и сортируется на куски определённых размеров.
Технический карбид кальция представляет собой твёрдое кристаллическое вещество. По внешнему виду карбид кальция представляет собой твёрдое вещество тёмно-серого или коричневого цвета. Он даёт кристаллический излом серого цвета с различными оттенками в зависимости от чистоты. Карбид кальция жадно поглощает воду. При взаимодействии с водой даже на холоде карбид кальция разлагается с бурным выделением ацетилена и большого количества тепла. Из за содержания примесей при добавлении воды выделяется неприятный запах. Разложение карбида кальция происходит и под влиянием атмосферной влаги.
По ГОСТ 1460-56 установлены следующие размеры (грануляция) кусков карбида кальция: 2×8; 8×15; 15×25; 25×80. Технический карбид кальция содержит до 80 % химически чистого карбида кальция, остальное составляют примеси — негашеная известь, углерод, кремнекислота и другое.
Область применения карбида кальция
Карбид кальция используют при проведении автогенных работ и освещения, а также в производстве ацетиленовой сажи и продуктов органического синтеза, из которых главным является синтетический каучук.
Карбид кальция применяют в производстве цианамида кальция, из которого получают удобрения, цианистые соединения. Карбид кальция используют для получения карбидно-карбамидного регулятора роста растений, изготовления порошкового карбидного реагента.
Из 1 кг технического карбида получается от 235 до 285 л ацетилена в зависимости от его сорта и грануляции: чем чище и крупнее карбид кальция, тем большее количество ацетилена он даёт при разложении.
Для разложения 1 кг карбида кальция теоретически требуется 0,56 л воды. Практически берут от 5 до 20 л воды с целью лучшего охлаждения ацетилена и обеспечения безопасности при работе. Скорость разложения карбида кальция водой зависит от его чистоты, грануляции, температуры и чистоты воды. Чем чище карбид кальция, меньше размер его кусков, выше температура и чище вода, тем больше скорость.
Физиологическое действие
- Среди всех неорганических производных кальция CaC2 очень ядовит.
- По степени воздействия на организм человека карбид кальция относится к 1-му классу опасности согласно ГОСТ 12.
 1.007.
1.007. - Попадание карбида кальция внутрь организма также является опасным.
- Пыль карбида кальция оказывает раздражающее действие на кожу, слизистые оболочки органов дыхания.
- Карбид кальция CaC2 чрезвычайно опасен для окружающей среды.
Разработать технологию получения карбида кальция в печах мощностью 100 МВА
Министерство образования и науки РФ
ФГБОУ ВПО «Сибирский государственный индустриальный университет»
Институт металлургии и материаловедения
Кафедра металлургии цветных металлов и химической технологии
Курсовая работа
По дисциплине «Технология электротермических производств»
Разработать технологию получения карбида кальция в печах мощностью 100 МВА.
Руководитель работы
Исполнитель – студент
группы МХТ-08
Копылова М.
Отчет защищен с оценкой __________________ «______» _________г
Члены комиссии ____________________
_____________________
_____________________
Новокузнецк 2012
Содержание
Введение…………………………………………………………
- Общая часть………….……………………………………………………
……6
1.1 Применение карбида кальция в промышленности………………………6
1.2 Физические и химические
свойства карбида кальция………………
1.3 Приготовление шихты для
1.4 Схема производства карбида………………………………………….…13
2. Расчет материального и теплового баланса плавки карбида кальция…….16
2.1 Материальный баланс плавки карбида кальция……………….………..16
2.1.1 Расчет количества восстановителя…………..………………….
2.1.2 Расчет количества и состава продуктов плавки …………………21
2.1.3 Расчет количества и состава газовой фазы………………..………22
2.2 Расчет теплового баланса плавки карбида
кальция……………………24
2.2.1 Цель и методы расчета теплового баланса……………………….24
2.2.2 Расчет статей прихода тепла………………………………………25
2.2.3 Расчет расходов тепла………………………………………………25
2.3 Расчет расхода электроэнергии…………………………………………
3. Технология переработки мелочи извести и угля в полых электродах ……30
4. Технология очистки печных газов………………………………………….32
Заключение………………..
Список использованной литературы………………..
Введение
Карбид кальция (CaC2) представляет собой твердое
кристаллическое вещество. Химически
чистый карбид кальция бесцветен, цвет
технического продукта, содержащего 20-25%
примесей (в основном – негашеной извести),
изменяется от светло-бурого до черного.
Химически
чистый карбид кальция бесцветен, цвет
технического продукта, содержащего 20-25%
примесей (в основном – негашеной извести),
изменяется от светло-бурого до черного.
Температура плавления
карбида кальция равняется 2160
Вещество бурно реагирует с водой, с разбавленными минеральными кислотами и водными растворами щелочей с выделением ацетилена и значительного количества тепла.
С водородом (Н2) выше 2200°C карбид кальция образует ацетилен и СаН2, с азотом (N2
) и аммиаком (NH3) при нагревании – цианамид (CaCN2). Окисляется на воздухе выше 700°C, взаимодействует с хлором (Cl2) и хлористым водородом (HCl) выше 250°C.Карбид кальция – сильный восстановитель, восстанавливает при нагревании почти все оксиды металлов до карбидов или свободных металлов.
По степени воздействия
на организм карбид кальция относится к веществам 1-го класса опасности.
Получают карбид кальция
преимущественно
Технический карбид кальция
широко применяют в технике, главным
образом для промышленного
Схема производства и потребления карбида кальция.
1. Общая часть
Общая часть
Карбид кальция применяется
Важнейшим
соединением, получаемым из 
Другое направление, по которому используется карбид кальция, основано на его способности при разложении водою выделять ацетилен. Последний в свою очередь имеет большое применение в промышленности, во-первых, для получения ряда органических соединений, например искусственного каучука, и, во-вторых, в качестве горючего газа для получения высоких температур.
В первые годы развития карбидной промышленности карбидом кальция пользовались исключительно для получения ацетилена, который применялся для целей освещения. Еще Деви в 1863 г. было известно свойство карбида кальция разлагаться водой с выделением ацетилена и способность последнего при сгорании на воздухе давать светящееся пламя. В целях улучшения смешивания ацетилена с воздухом для получения более яркого пламени последнему придают плоскую форму, для чего сжигание ацетилена производится в специальных горелках.
В дальнейшем ацетилен нашел
применение в ряде других областей,
главнейшей из которых является автогенная
сварка и резка металлов, основанная на
способности ацетилена при сжигании в
струе кислорода давать пламя, температура
которого достигает 3000—3150°.
В последние годы, помимо использования ацетилена для производства автогенных работ, он нашел другую чрезвычайно большую область применения, а именно, для получения из него ряда новых органических продуктов, которые в свою очередь находят широкое применение в различных областях современной промышленности. Можно указать на ряд синтетических продуктов, получаемых из ацетилена. Важнейшими из них являются химические соединения ацетилена с хлором. Эти соединения жидкости, превосходно растворяющие жиры, масла, смолу и другие органические соединения. Они хорошо растворяют также серу, фосфор и ряд неорганических солей. Поэтому они с успехом заменяют бензин и сероуглерод при экстракции жиров и имеют преимущество перед последними в том отношении, что являются негорючими, т. е. неогнеопасными продуктами.
Из ацетилена путем
присоединения к нему воды получается ацетальдегид,
а из последнего синтетическая уксусная
кислота, ацетон, искусственные смолы
и этиловый или винный спирт. Особый интерес
представляет возможность получения этим
способом уксусной кислоты.
Особый интерес
представляет возможность получения этим
способом уксусной кислоты.
Одной из важнейших областей применения ацетилена является использование его в качестве сырья для получения синтетического каучука [1].
1.2 Физические и химические свойства карбида кальция
Карбиды – соединения углерода с металлами, а также с бором и кремнием. Эти соединения обладают удивительным разнообразием физических и химических свойств. Так, карбид золота Au2C2 взрывается уже при попытке пересыпать его с листочка фильтровальной бумаги, на котором он был высушен. С другой стороны, карбиды некоторых элементов (например, бора и тантала) не разлагаются даже при температуре белого каления и настолько химически инертны, что на них не действует царская водка, а по твердости они приближаются к алмазу!
Карбид кальция,
или, как его обычно называют,
«карбид» представляет собой
продукт, сплавления извести с углеродом. Впервые карбид
кальция был получен в 1863г. ученым Деви.
В 1892г. карбид кальция был получен другим
ученым Муассаном в электропечи при температуре
около 3000°. Это открытие легло в основу
современного способа промышленного получения
карбида кальция путем плавления извести
с антрацитом или коксом в электропечах.
ученым Деви.
В 1892г. карбид кальция был получен другим
ученым Муассаном в электропечи при температуре
около 3000°. Это открытие легло в основу
современного способа промышленного получения
карбида кальция путем плавления извести
с антрацитом или коксом в электропечах.
В химически чистом
виде карбид кальция
Карбид кальция,
только что полученный из печи, имеет серый,
коричнево-желтый или черный цвет в зависимости
от степени его чистоты. Свежий излом карбида
кальция имеет блестящую поверхность,
которая на воздухе теряет свой блеск
вследствие поглощения влаги, причем происходит
выделение ацетилена и выветривание поверхности,
принимающей при этом серовато-белый цвет
[1].
Удельная масса
технического карбида кальция
находится в зависимости от
содержания в нем чистого
Температура плавления
карбида кальция также  Наиболее низкую температуру плавления,
а именно 1630°, имеет смесь, состоящая и»
70% карбида кальция и около 30% окиси кальция.
При дальнейшем увеличении содержания
окиси кальция температура плавления
опять поднимается. Чистый карбид кальция
СаС имеет температуру плавления 2300°.
Температура (расплавленного карбида
кальция при выпуске из печи равна 1900—2000°.
Наиболее низкую температуру плавления,
а именно 1630°, имеет смесь, состоящая и»
70% карбида кальция и около 30% окиси кальция.
При дальнейшем увеличении содержания
окиси кальция температура плавления
опять поднимается. Чистый карбид кальция
СаС имеет температуру плавления 2300°.
Температура (расплавленного карбида
кальция при выпуске из печи равна 1900—2000°.
Из химических свойств карбида кальция отмечаются следующие. Сухой водород не реагирует с карбидом кальция ни на холоде, ни при высокой температуре. В сухом кислороде при высокой температуре карбид кальция сгорает с оАзот реагирует с карбидом кальция при температуре 1000°, образуя цианамид кальция. На этой реакции и основано производство цианамида кальция из карбида кальция.
Хлор действует на карбид кальция лишь при нагревании. Пары серы при температуре 500° дают с карбидом кальция соединения, так же как фосфор и мышьяк.
Рисунок 1 – Зависимость удельного веса карбида кальция от его чистоты
Наиболее важным для
промышленности химическим свойством карбида
кальция является его способность разлагаться
водой с выделением ацетилена. Это разложение
происходит также при недостаточном количестве
воды, например под действием влаги атмосферного
воздуха. Поэтому нельзя хранить карбид
открытым, а необходимо хранить его в герметически
закрытой таре.
Это разложение
происходит также при недостаточном количестве
воды, например под действием влаги атмосферного
воздуха. Поэтому нельзя хранить карбид
открытым, а необходимо хранить его в герметически
закрытой таре.
Технический карбид кальция, получаемый в электропечи, не является чистым карбидом СаС3, а содержит ряд примесей, попадающих в него из сырых материалов, которыми пользуются для производства.
Состав технического карбида кальция [1]:
Карбид кальция СаС2 85,5%
Известь или окись кальция СаО 8,3%
Окись магния МgO 0,4%
Окись железа и алюминия Fе2O3+Al2O3 0,2%
Кремнекислота SiO2 3,2%
Сера S 0,3%
Углерод С 2,2%
Итого 100,1%
Качество карбида
кальция определяется количеством ацетилена,
которое может быть получено при разложении
водой 1кг продукта. Количество
выделяемого ацетилена при разложении
одного и того же количества карбида кальция
зависит от процентного содержания в нем
чистого карбида кальция. Теоретически
при разложении 1кг химически чистого карбида
кальция водой должно получиться 406,25г
ацетилена, что при 0° и 760мм ртутного столба
соответствует объему в 348,7л. Число литров ацетилена,
выделяемое 1кг карбида кальция, определяющее
качество последнего, называется литражом.
Теоретически
при разложении 1кг химически чистого карбида
кальция водой должно получиться 406,25г
ацетилена, что при 0° и 760мм ртутного столба
соответствует объему в 348,7л. Число литров ацетилена,
выделяемое 1кг карбида кальция, определяющее
качество последнего, называется литражом.
Рисунок 2 – Зависимость температуры плавления кальция от содержания извести СаО
Существующим у нас стандартом предусматривается для карбида кальция литраж при 20°С и 760мм ртутного столба для сорта «А» (СаС2 = 78-86%) от 250 до 300 и для сорта «Б» (СаС2 = 70-76%) от 230 до 280.
Для приготовления смеси
или шихты сырых материалов последние
сперва дробятся до определенной величины
кусков, отвешиваются в определенных количествах и смешиваются. Величина
кусков, на которые дробятся материалы,
зависит от их качества и физических свойств.
Практикой установлено, что лучшее сплавление
шихты в электропечи получается тогда,
когда известь берется в кусках величиной
50—100 мм, а антрацит 25—50 мм. Величина кусков антрацита
зависит от того, насколько он легко реагирует
в электропечи с известью. При работе с
антрацитом, обладающим хорошей реакционной
способностью, для приготовления шихты
могут быть взяты куски большого размера
и, наоборот, если антрацит плохо сплавляется
с известью, то он берется в кусках небольшой
величины, так как в противном случае он
не успеет прореагировать с известью и
выходит из печи вместе с расплавленным
карбидом.
Величина кусков антрацита
зависит от того, насколько он легко реагирует
в электропечи с известью. При работе с
антрацитом, обладающим хорошей реакционной
способностью, для приготовления шихты
могут быть взяты куски большого размера
и, наоборот, если антрацит плохо сплавляется
с известью, то он берется в кусках небольшой
величины, так как в противном случае он
не успеет прореагировать с известью и
выходит из печи вместе с расплавленным
карбидом.
свойства и применение. Получение ацетилена :: SYL.ru
Поливаем обильно. Осенняя подкормка для увеличения плодородия почвы
Кекс с кабачком. Готовим ароматную выпечку с лаймом
Яркие пятна на чистом лице: тренд обещает стать главным в этом сезоне
Как вписать в комфортный осенний образ балетки – хит этого сезона
Положительное восприятие: почему именно принт в горох самый привлекательный
Гусиные лапки – главный принт осени: тенденции и секреты использования в образе
Белый – лучший выбор: какие цвета заставят выглядеть наряд женщины за 50 дороже
Бульон поможет превратить картофельное пюре в шедевр
Как продлить молодость: Высоцкая рассказала о домашних бьюти-процедурах
Футболки с рукавами ¾: одежда, визуально уменьшающая широкую спину
Автор Злата Усачева
Карбиды – это группа неорганических соединений углерода с металлами, а также с кремнием или бором (поскольку эти элементы проявляют металлические свойства). Карбид кальция – одно из наиболее востребованных веществ этой группы. О свойствах и применении соединения читайте ниже.
Карбид кальция – одно из наиболее востребованных веществ этой группы. О свойствах и применении соединения читайте ниже.
История получения
Карбид кальция – соединение, получившее широкое применение в современной промышленности. В 1862 году немецкий химик Фридрих Велер впервые синтезировал молекулу этого вещества. Получение карбида кальция он осуществил следующим образом. Ученый приготовил расплав кальция с цинком, а затем нагрел его с углем. В результате получился карбид. Химическая формула соединения – CaC2.Промышленный способ получения карбида предложил ученый Муассан в 1892 году. Другие названия вещества – ацетиленид кальция, или углеродистый кальций. Кристаллическая решетка соединения выглядит следующим образом:
Физические свойства
По своим физическим свойствам карбид кальция является кристаллическим веществом с температурой плавления 2300 оС. Эта цифра является справедливой лишь для чистого соединения. Карбид, содержащий примеси, может иметь другие показатели температуры плавления. Основное агрегатное состояние вещества – твердое, а цвет варьирует от серого до коричневого.
Основное агрегатное состояние вещества – твердое, а цвет варьирует от серого до коричневого.
Химические свойства
Карбид кальция хорошо впитывает воду. Этот процесс сопровождается химической реакцией разложения. Важно, что карбидная пыль обладает раздражающим действием на слизистые оболочки, кожу и органы дыхания. Поэтому во время работы с соединением необходимо использовать противогазы либо противопылевые респираторы. С кислородом карбид кальция взаимодействует при высокой температуре с образованием карбоната кальция. Реакция с азотом приводит к синтезу цианамида кальция. Также при высоких температурах карбид кальция вступает в реакции соединения с хлором, фосфором, мышьяком. Но все-таки одним из важнейших свойств соединения считается разложение водой.
Получение
Производство карбида кальция заключается в следующем. Негашеную известь и предварительно измельченный кокс смешивают. Полученную смесь подвергают расплавлению в электрических печах. Кокс и оксид кальция берутся в равных по массе частях. Процесс происходит при температуре 1900 оС. Расплав выходит из печи и в дальнейшем разливается по специальным формам. Затем уже затвердевший карбид кальция дробят и сортируют по размеру кусков. Гранулы вещества разделяются на четыре фракции в соответствии с их размерами: 25×80, 15×25, 8×15, 2×8, которые определяются ГОСТом 1460-56. По своему составу технический карбид кальция содержит 75-80% основного вещества. На долю примесей, таких, как углерод, известь и других, приходится до 25% от общей массы полученной смеси. Кроме того, содержащийся в техническом карбиде сульфид и фосфид кальция обусловливают довольно неприятный его запах. Представим реакцию получения СаС2: СаО + 3С → СаС2 + СО↑. Образование ацетиленида кальция сопровождается поглощением тепла. Поэтому логично предположить, что реакция его разложения, напротив, идет с выделением энергии.
Процесс происходит при температуре 1900 оС. Расплав выходит из печи и в дальнейшем разливается по специальным формам. Затем уже затвердевший карбид кальция дробят и сортируют по размеру кусков. Гранулы вещества разделяются на четыре фракции в соответствии с их размерами: 25×80, 15×25, 8×15, 2×8, которые определяются ГОСТом 1460-56. По своему составу технический карбид кальция содержит 75-80% основного вещества. На долю примесей, таких, как углерод, известь и других, приходится до 25% от общей массы полученной смеси. Кроме того, содержащийся в техническом карбиде сульфид и фосфид кальция обусловливают довольно неприятный его запах. Представим реакцию получения СаС2: СаО + 3С → СаС2 + СО↑. Образование ацетиленида кальция сопровождается поглощением тепла. Поэтому логично предположить, что реакция его разложения, напротив, идет с выделением энергии.
Транспортировка и хранение
По причине того, что влага моментально разлагает карбид с выделением большого количества тепла и образованием взрывоопасного газа ацетилена, хранить вещество необходимо в герметично закупоренных барабанах или бидонах. Следует помнить, что ацетилен легче воздуха и способен скапливаться в верхних зонах помещения. Этот газ, помимо наркотического действия, обладает способностью к самовоспламенению. Поэтому использовать карбид кальция необходимо с большой осторожностью. Расфасовке на производстве уделяется особое внимание. Готовое вещество помещается в специальные барабаны (тара, напоминающая консервные банки). Такая упаковка требует аккуратного вскрытия. При этом должен использоваться инструмент, не приводящий к образованию искр (молоток или специальный нож). В случае попадания карбида на кожу или слизистые оболочки необходимо немедленно промыть пораженный участок водой и обработать место вазелином или жирным кремом. Транспортировка соединения осуществляется с использованием только крытых видов транспорта. Воздушная доставка карбида запрещена. Помещения, где хранится СаС2, должны быть хорошо проветриваемыми. Также не разрешается хранить карбид совместно с другими химическими веществами. Это может привести к нежелательным, а, возможно, и опасным, реакциям.
Следует помнить, что ацетилен легче воздуха и способен скапливаться в верхних зонах помещения. Этот газ, помимо наркотического действия, обладает способностью к самовоспламенению. Поэтому использовать карбид кальция необходимо с большой осторожностью. Расфасовке на производстве уделяется особое внимание. Готовое вещество помещается в специальные барабаны (тара, напоминающая консервные банки). Такая упаковка требует аккуратного вскрытия. При этом должен использоваться инструмент, не приводящий к образованию искр (молоток или специальный нож). В случае попадания карбида на кожу или слизистые оболочки необходимо немедленно промыть пораженный участок водой и обработать место вазелином или жирным кремом. Транспортировка соединения осуществляется с использованием только крытых видов транспорта. Воздушная доставка карбида запрещена. Помещения, где хранится СаС2, должны быть хорошо проветриваемыми. Также не разрешается хранить карбид совместно с другими химическими веществами. Это может привести к нежелательным, а, возможно, и опасным, реакциям. Срок хранения карбида составляет полгода.
Срок хранения карбида составляет полгода.
Применение
Область применения карбида кальция чрезвычайно широка. В первую очередь это промышленный синтез. Карбид кальция используется для производства синтетического каучука, уксусной кислоты, ацетона, этилена, винилхлорида, стирола. Также он находит применение в получении цианамида кальция. Это вещество ценно своим использованием в синтезе различных удобрений и цианистых веществ. В сельском хозяйстве любому агроному известно такое название, как карбидно-карбамидный регулятор. Он применяется для регуляции роста растений. А для его получения также используется карбид кальция. Кроме того, это соединение находит применение в процессе производства цианамида кальция. Эта реакция основана на нагревании карбида кальция с азотом. Восстановление щелочных металлов также не обходится без применения описываемого нами вещества. Карбид кальция применяется и в процессе газосварки. Например, широко используются карбидные лампы. Принцип их работы основан на взаимодействии в специальной емкости карбида с водой и сгорании на выходе из аппарата конечного вещества реакции – ацетилена.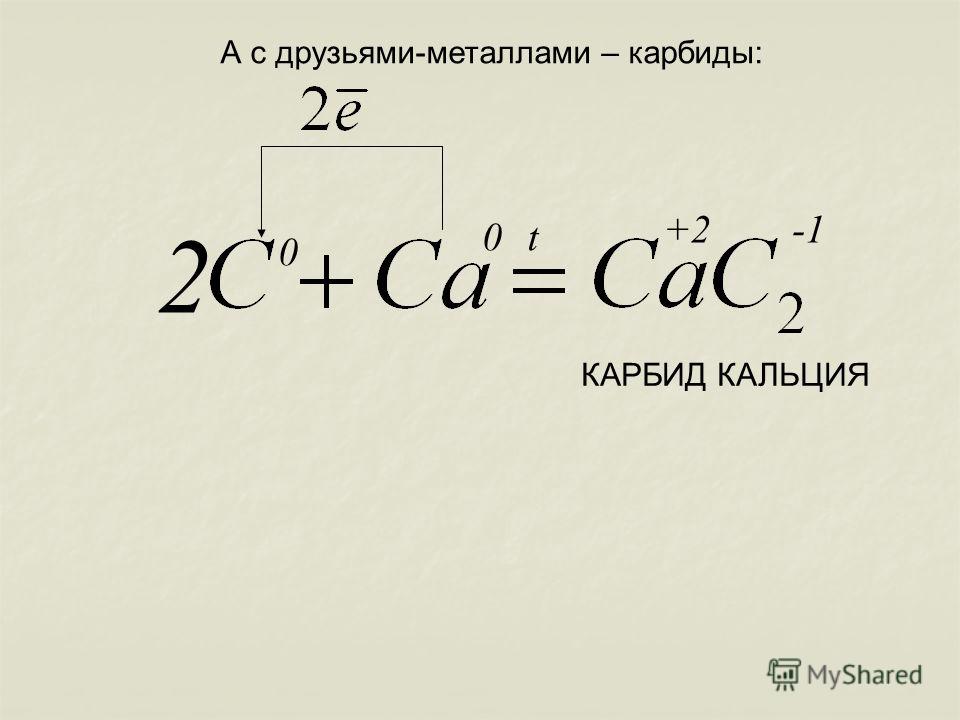 Посмотрите на фото карбидной лампы.
Посмотрите на фото карбидной лампы.
Производство ацетилена
Одной из важнейших областей применения карбида кальция является его использование в получении ацетилена. Заслуга в открытии этого способа также принадлежит немецкому ученому-химику Фридриху Велеру. В основе этого промышленного процесса лежит реакция разложения карбида под воздействием воды. СаС2 + 2 Н2О → С2Н2 + Са(ОН)2↓.На выходе образуется газ ацетилен и гашеная известь, выпадающая в осадок. Процесс сопровождается выделением большого количества тепла. Объем газа на выходе зависит от того, насколько чистый используется для реакции карбид кальция. Ацетилен, образующийся в результате, может иметь различный объем – 1 кг исходного вещества может дать от 235 до 290 литров газа. Что касается скорости протекания реакции, то она зависит как от малого процента примесей в карбиде кальция, так и от температуры воды, а также ее чистоты. Если рассматривать теоретическую реакцию производства ацетилена из карбида, то в ней на 1 кг карбида достаточно 560 мл воды. Однако на практике объем воды для проведения реакции увеличивается. На 1 кг карбида кальция в условиях промышленного синтеза требуется от 5 до 20 литров воды. Такое количество необходимо для того, чтобы ацетилен лучше охлаждался, а также для обеспечения оптимальной безопасности при работе. Ниже изображен немецкий химик Фридрих Велер.
Однако на практике объем воды для проведения реакции увеличивается. На 1 кг карбида кальция в условиях промышленного синтеза требуется от 5 до 20 литров воды. Такое количество необходимо для того, чтобы ацетилен лучше охлаждался, а также для обеспечения оптимальной безопасности при работе. Ниже изображен немецкий химик Фридрих Велер.
Лабораторный опыт получения ацетилена
Многим из школьных уроков химии знакома реакция взаимодействия карбида с водой. Обычно этот опыт позволяет продемонстрировать реакцию получения ацетилена, а также физические и химические его свойства. Процесс выделения газа при этом происходит достаточно бурно, поэтому трубка, отводящая ацетилен из колбы с действующими веществами, помещается в чашу с водой. Это обеспечивает менее активное и стремительное движение газа. Кроме того, в лабораторных условиях можно использовать и другой способ, чтобы сделать не слишком бурной реакцию разложения такого соединения, как карбид. Ацетилен при этом идет равномерно и спокойно. Для этого вместо воды необходимо взять насыщенный раствор поваренной соли. Также в лаборатории при проведении этой реакции следует осторожно добавлять воду в карбид, помещенный в объемную колбу, а не наоборот.
Для этого вместо воды необходимо взять насыщенный раствор поваренной соли. Также в лаборатории при проведении этой реакции следует осторожно добавлять воду в карбид, помещенный в объемную колбу, а не наоборот.
Похожие статьи
- Алкины: получение и применение
- Получение аммиака в промышленности. Получение аммиака в лаборатории
- Ацетилен: химические свойства, получение, применение, меры предосторожности
- Гашеная известь: свойства, получение, применение
- Все о кристаллизации. Как сделать кристалл в домашних условиях?
- Ацетон: формула, особенности свойств, применение
- Оксид кальция: свойства, получение, применение
Также читайте
Карбид кальция — свойства, получение и применение
Карбид кальция — CaC2 — в чистом виде белое кристаллическое вещество. Бинарное неорганическое соединение кальция с углеродом.
Бинарное неорганическое соединение кальция с углеродом.
| Карбид кальция | |
| Общие | |
| Систематическое наименование | Кальция карбид |
| Традиционные названия | Ацетиленид кальция; углеродистый кальций |
| Хим. формула | CaC2 |
| Рац. формула | CaC2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 64,0994 (±0,004) г/моль |
| Плотность | 2,22 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 2160 °C |
| • кипения | 2300 °C |
| Структура | |
| Координационная геометрия | 6 |
| Кристаллическая структура | Тетрагональная |
| Классификация | |
| Рег. номер CAS | 75-20-7 |
| PubChem | 6352 |
Рег. номер EINECS номер EINECS | 200-848-3 |
| SMILES | [C-]#[C-].[Ca+2] |
| InChI | 1S/C2.Ca/c1-2;/q-2;+2 UIXRSLJINYRGFQ-UHFFFAOYSA-N |
| RTECS | EV9400000 |
| ChemSpider | 6112 |
| Безопасность | |
| NFPA 704 | |
Физические свойства
- Бесцветные тетрагональные кристаллы.
- Плотность: 2,2 (+20 °C, г/см3).
- Удельная теплоёмкость при постоянном давлении (в Дж/г·K): 0,92 (+20—325 °C).
- Стандартная энтальпия образования ΔH (298 К, кДж/моль): −62,8 (т).
- Стандартная энергия Гиббса образования ΔG (298 К, кДж/моль): −67,8 (т).
- Стандартная энтропия образования S (298 К, Дж/моль·K): 70,3 (т).
- Стандартная мольная теплоёмкость Cp (298 К, Дж/моль·K): 62,34 (т).
- Энтальпия плавления ΔHпл (кДж/моль): 32,2[1].
Внешний вид и характеристики технического карбида кальция
Карбид кальция получают сплавлением в электрических печах кокса и негашеной извести. Расплавленный карбид кальция выпускается из печи в специальные формы — изложницы, в которых он затвердевает. Застывший карбид кальция дробится и сортируется на куски определённых размеров.
Расплавленный карбид кальция выпускается из печи в специальные формы — изложницы, в которых он затвердевает. Застывший карбид кальция дробится и сортируется на куски определённых размеров.
Технический карбид кальция представляет собой твёрдое кристаллическое вещество. По внешнему виду карбид кальция представляет собой твёрдое вещество тёмно-серого или коричневого цвета. Он даёт кристаллический излом серого цвета с различными оттенками в зависимости от чистоты. Карбид кальция жадно поглощает воду. При взаимодействии с водой даже на холоде карбид кальция разлагается с бурным выделением ацетилена и большого количества тепла. Разложение карбида кальция происходит и под влиянием атмосферной влаги.
По ГОСТ 1460-56 установлены следующие размеры (грануляция) кусков карбида кальция: 2×8; 8×15; 15×25; 25×80. Технический карбид кальция содержит до 80 % химически чистого карбида кальция, остальное составляют примеси — негашеная известь, углерод, кремнекислота и другое[3].
Лабораторный опыт получения ацетилена
Многим из школьных уроков химии знакома реакция взаимодействия карбида с водой. Обычно этот опыт позволяет продемонстрировать реакцию получения ацетилена, а также физические и химические его свойства. Процесс выделения газа при этом происходит достаточно бурно, поэтому трубка, отводящая ацетилен из колбы с действующими веществами, помещается в чашу с водой. Это обеспечивает менее активное и стремительное движение газа. Кроме того, в лабораторных условиях можно использовать и другой способ, чтобы сделать не слишком бурной реакцию разложения такого соединения, как карбид. Ацетилен при этом идет равномерно и спокойно. Для этого вместо воды необходимо взять насыщенный раствор поваренной соли. Также в лаборатории при проведении этой реакции следует осторожно добавлять воду в карбид, помещенный в объемную колбу, а не наоборот.
Обычно этот опыт позволяет продемонстрировать реакцию получения ацетилена, а также физические и химические его свойства. Процесс выделения газа при этом происходит достаточно бурно, поэтому трубка, отводящая ацетилен из колбы с действующими веществами, помещается в чашу с водой. Это обеспечивает менее активное и стремительное движение газа. Кроме того, в лабораторных условиях можно использовать и другой способ, чтобы сделать не слишком бурной реакцию разложения такого соединения, как карбид. Ацетилен при этом идет равномерно и спокойно. Для этого вместо воды необходимо взять насыщенный раствор поваренной соли. Также в лаборатории при проведении этой реакции следует осторожно добавлять воду в карбид, помещенный в объемную колбу, а не наоборот.
Ваша корзина пуста, для оформления заказа выберите товар в каталоге
Поиск по каталогу
Доставка продукции осуществляется компанией ХИМОПТТОРГ во все регионы Центральной России:
- Белгородская область
- Липецкая область
- Курская область
- Тамбовская область
- Воронежская область
Область применения карбида кальция
Карбид кальция используют при проведении автогенных работ и освещения, а также в производстве ацетиленовой сажи и продуктов органического синтеза, из которых главным является синтетический каучук.
Карбид кальция применяют в производстве цианамида кальция, из которого получают удобрения, цианистые соединения. Карбид кальция используют для получения карбидно-карбамидного регулятора роста растений, изготовления порошкового карбидного реагента.
Из 1 кг технического карбида получается от 235 до 285 л ацетилена в зависимости от его сорта и грануляции: чем чище и крупнее карбид кальция, тем большее количество ацетилена он даёт при разложении.
Для разложения 1 кг карбида кальция теоретически требуется 0,56 л воды. Практически берут от 5 до 20 л воды с целью лучшего охлаждения ацетилена и обеспечения безопасности при работе. Скорость разложения карбида кальция водой зависит от его чистоты, грануляции, температуры и чистоты воды. Чем чище карбид кальция, меньше размер его кусков, выше температура и чище вода, тем больше скорость[3].
Химические свойства
Карбид кальция хорошо впитывает воду. Этот процесс сопровождается химической реакцией разложения. Важно, что карбидная пыль обладает раздражающим действием на слизистые оболочки, кожу и органы дыхания. Поэтому во время работы с соединением необходимо использовать противогазы либо противопылевые респираторы. С кислородом карбид кальция взаимодействует при высокой температуре с образованием карбоната кальция. Реакция с азотом приводит к синтезу цианамида кальция. Также при высоких температурах карбид кальция вступает в реакции соединения с хлором, фосфором, мышьяком. Но все-таки одним из важнейших свойств соединения считается разложение водой.
Поэтому во время работы с соединением необходимо использовать противогазы либо противопылевые респираторы. С кислородом карбид кальция взаимодействует при высокой температуре с образованием карбоната кальция. Реакция с азотом приводит к синтезу цианамида кальция. Также при высоких температурах карбид кальция вступает в реакции соединения с хлором, фосфором, мышьяком. Но все-таки одним из важнейших свойств соединения считается разложение водой.
Отрывок, характеризующий Карбид кальция
Курган, на который вошел Пьер, был то знаменитое (потом известное у русских под именем курганной батареи, или батареи Раевского, а у французов под именем la grande redoute, la fatale redoute, la redoute du centre [большого редута, рокового редута, центрального редута] место, вокруг которого положены десятки тысяч людей и которое французы считали важнейшим пунктом позиции. Редут этот состоял из кургана, на котором с трех сторон были выкопаны канавы. В окопанном канавами место стояли десять стрелявших пушек, высунутых в отверстие валов. В линию с курганом стояли с обеих сторон пушки, тоже беспрестанно стрелявшие. Немного позади пушек стояли пехотные войска. Входя на этот курган, Пьер никак не думал, что это окопанное небольшими канавами место, на котором стояло и стреляло несколько пушек, было самое важное место в сражении. Пьеру, напротив, казалось, что это место (именно потому, что он находился на нем) было одно из самых незначительных мест сражения. Войдя на курган, Пьер сел в конце канавы, окружающей батарею, и с бессознательно радостной улыбкой смотрел на то, что делалось вокруг него. Изредка Пьер все с той же улыбкой вставал и, стараясь не помешать солдатам, заряжавшим и накатывавшим орудия, беспрестанно пробегавшим мимо него с сумками и зарядами, прохаживался по батарее. Пушки с этой батареи беспрестанно одна за другой стреляли, оглушая своими звуками и застилая всю окрестность пороховым дымом. В противность той жуткости, которая чувствовалась между пехотными солдатами прикрытия, здесь, на батарее, где небольшое количество людей, занятых делом, бело ограничено, отделено от других канавой, – здесь чувствовалось одинаковое и общее всем, как бы семейное оживление.
В линию с курганом стояли с обеих сторон пушки, тоже беспрестанно стрелявшие. Немного позади пушек стояли пехотные войска. Входя на этот курган, Пьер никак не думал, что это окопанное небольшими канавами место, на котором стояло и стреляло несколько пушек, было самое важное место в сражении. Пьеру, напротив, казалось, что это место (именно потому, что он находился на нем) было одно из самых незначительных мест сражения. Войдя на курган, Пьер сел в конце канавы, окружающей батарею, и с бессознательно радостной улыбкой смотрел на то, что делалось вокруг него. Изредка Пьер все с той же улыбкой вставал и, стараясь не помешать солдатам, заряжавшим и накатывавшим орудия, беспрестанно пробегавшим мимо него с сумками и зарядами, прохаживался по батарее. Пушки с этой батареи беспрестанно одна за другой стреляли, оглушая своими звуками и застилая всю окрестность пороховым дымом. В противность той жуткости, которая чувствовалась между пехотными солдатами прикрытия, здесь, на батарее, где небольшое количество людей, занятых делом, бело ограничено, отделено от других канавой, – здесь чувствовалось одинаковое и общее всем, как бы семейное оживление. Появление невоенной фигуры Пьера в белой шляпе сначала неприятно поразило этих людей. Солдаты, проходя мимо его, удивленно и даже испуганно косились на его фигуру. Старший артиллерийский офицер, высокий, с длинными ногами, рябой человек, как будто для того, чтобы посмотреть на действие крайнего орудия, подошел к Пьеру и любопытно посмотрел на него. Молоденький круглолицый офицерик, еще совершенный ребенок, очевидно, только что выпущенный из корпуса, распоряжаясь весьма старательно порученными ему двумя пушками, строго обратился к Пьеру. – Господин, позвольте вас попросить с дороги, – сказал он ему, – здесь нельзя. Солдаты неодобрительно покачивали головами, глядя на Пьера. Но когда все убедились, что этот человек в белой шляпе не только не делал ничего дурного, но или смирно сидел на откосе вала, или с робкой улыбкой, учтиво сторонясь перед солдатами, прохаживался по батарее под выстрелами так же спокойно, как по бульвару, тогда понемногу чувство недоброжелательного недоуменья к нему стало переходить в ласковое и шутливое участие, подобное тому, которое солдаты имеют к своим животным: собакам, петухам, козлам и вообще животным, живущим при воинских командах.
Появление невоенной фигуры Пьера в белой шляпе сначала неприятно поразило этих людей. Солдаты, проходя мимо его, удивленно и даже испуганно косились на его фигуру. Старший артиллерийский офицер, высокий, с длинными ногами, рябой человек, как будто для того, чтобы посмотреть на действие крайнего орудия, подошел к Пьеру и любопытно посмотрел на него. Молоденький круглолицый офицерик, еще совершенный ребенок, очевидно, только что выпущенный из корпуса, распоряжаясь весьма старательно порученными ему двумя пушками, строго обратился к Пьеру. – Господин, позвольте вас попросить с дороги, – сказал он ему, – здесь нельзя. Солдаты неодобрительно покачивали головами, глядя на Пьера. Но когда все убедились, что этот человек в белой шляпе не только не делал ничего дурного, но или смирно сидел на откосе вала, или с робкой улыбкой, учтиво сторонясь перед солдатами, прохаживался по батарее под выстрелами так же спокойно, как по бульвару, тогда понемногу чувство недоброжелательного недоуменья к нему стало переходить в ласковое и шутливое участие, подобное тому, которое солдаты имеют к своим животным: собакам, петухам, козлам и вообще животным, живущим при воинских командах. Солдаты эти сейчас же мысленно приняли Пьера в свою семью, присвоили себе и дали ему прозвище. «Наш барин» прозвали его и про него ласково смеялись между собой. Одно ядро взрыло землю в двух шагах от Пьера. Он, обчищая взбрызнутую ядром землю с платья, с улыбкой оглянулся вокруг себя. – И как это вы не боитесь, барин, право! – обратился к Пьеру краснорожий широкий солдат, оскаливая крепкие белые зубы. – А ты разве боишься? – спросил Пьер. – А то как же? – отвечал солдат. – Ведь она не помилует. Она шмякнет, так кишки вон. Нельзя не бояться, – сказал он, смеясь. Несколько солдат с веселыми и ласковыми лицами остановились подле Пьера. Они как будто не ожидали того, чтобы он говорил, как все, и это открытие обрадовало их. – Наше дело солдатское. А вот барин, так удивительно. Вот так барин! – По местам! – крикнул молоденький офицер на собравшихся вокруг Пьера солдат. Молоденький офицер этот, видимо, исполнял свою должность в первый или во второй раз и потому с особенной отчетливостью и форменностью обращался и с солдатами и с начальником.
Солдаты эти сейчас же мысленно приняли Пьера в свою семью, присвоили себе и дали ему прозвище. «Наш барин» прозвали его и про него ласково смеялись между собой. Одно ядро взрыло землю в двух шагах от Пьера. Он, обчищая взбрызнутую ядром землю с платья, с улыбкой оглянулся вокруг себя. – И как это вы не боитесь, барин, право! – обратился к Пьеру краснорожий широкий солдат, оскаливая крепкие белые зубы. – А ты разве боишься? – спросил Пьер. – А то как же? – отвечал солдат. – Ведь она не помилует. Она шмякнет, так кишки вон. Нельзя не бояться, – сказал он, смеясь. Несколько солдат с веселыми и ласковыми лицами остановились подле Пьера. Они как будто не ожидали того, чтобы он говорил, как все, и это открытие обрадовало их. – Наше дело солдатское. А вот барин, так удивительно. Вот так барин! – По местам! – крикнул молоденький офицер на собравшихся вокруг Пьера солдат. Молоденький офицер этот, видимо, исполнял свою должность в первый или во второй раз и потому с особенной отчетливостью и форменностью обращался и с солдатами и с начальником. Перекатная пальба пушек и ружей усиливалась по всему полю, в особенности влево, там, где были флеши Багратиона, но из за дыма выстрелов с того места, где был Пьер, нельзя было почти ничего видеть. Притом, наблюдения за тем, как бы семейным (отделенным от всех других) кружком людей, находившихся на батарее, поглощали все внимание Пьера. Первое его бессознательно радостное возбуждение, произведенное видом и звуками поля сражения, заменилось теперь, в особенности после вида этого одиноко лежащего солдата на лугу, другим чувством. Сидя теперь на откосе канавы, он наблюдал окружавшие его лица. К десяти часам уже человек двадцать унесли с батареи; два орудия были разбиты, чаще и чаще на батарею попадали снаряды и залетали, жужжа и свистя, дальние пули. Но люди, бывшие на батарее, как будто не замечали этого; со всех сторон слышался веселый говор и шутки. – Чиненка! – кричал солдат на приближающуюся, летевшую со свистом гранату. – Не сюда! К пехотным! – с хохотом прибавлял другой, заметив, что граната перелетела и попала в ряды прикрытия.
Перекатная пальба пушек и ружей усиливалась по всему полю, в особенности влево, там, где были флеши Багратиона, но из за дыма выстрелов с того места, где был Пьер, нельзя было почти ничего видеть. Притом, наблюдения за тем, как бы семейным (отделенным от всех других) кружком людей, находившихся на батарее, поглощали все внимание Пьера. Первое его бессознательно радостное возбуждение, произведенное видом и звуками поля сражения, заменилось теперь, в особенности после вида этого одиноко лежащего солдата на лугу, другим чувством. Сидя теперь на откосе канавы, он наблюдал окружавшие его лица. К десяти часам уже человек двадцать унесли с батареи; два орудия были разбиты, чаще и чаще на батарею попадали снаряды и залетали, жужжа и свистя, дальние пули. Но люди, бывшие на батарее, как будто не замечали этого; со всех сторон слышался веселый говор и шутки. – Чиненка! – кричал солдат на приближающуюся, летевшую со свистом гранату. – Не сюда! К пехотным! – с хохотом прибавлял другой, заметив, что граната перелетела и попала в ряды прикрытия. – Что, знакомая? – смеялся другой солдат на присевшего мужика под пролетевшим ядром. Несколько солдат собрались у вала, разглядывая то, что делалось впереди. – И цепь сняли, видишь, назад прошли, – говорили они, указывая через вал. – Свое дело гляди, – крикнул на них старый унтер офицер. – Назад прошли, значит, назади дело есть. – И унтер офицер, взяв за плечо одного из солдат, толкнул его коленкой. Послышался хохот.
– Что, знакомая? – смеялся другой солдат на присевшего мужика под пролетевшим ядром. Несколько солдат собрались у вала, разглядывая то, что делалось впереди. – И цепь сняли, видишь, назад прошли, – говорили они, указывая через вал. – Свое дело гляди, – крикнул на них старый унтер офицер. – Назад прошли, значит, назади дело есть. – И унтер офицер, взяв за плечо одного из солдат, толкнул его коленкой. Послышался хохот.
КАРБИДЫ
КАРБИДЫ
(от латинского carbo – уголь) – соединения углерода с металлами, а также с бором и кремнием. Эти соединения обладают удивительным разнообразием физических и химических свойств. Так, карбид золота Au2C2 взрывается уже при попытке пересыпать его с листочка фильтровальной бумаги, на котором он был высушен. С другой стороны, карбиды некоторых элементов (например, бора и тантала) не разлагаются даже при температуре белого каления и настолько химически инертны, что на них не действует царская водка, а по твердости они приближаются к алмазу!
Также по теме:
ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ
Впервые необычное соединение металла с углеродом (К2С2) получил в 1809 знаменитый английский химик Гемфри Дэви. В 1863 французский химик Марселен Бертло изучил свойства другого карбида – очень неустойчивого и легко взрывающегося карбида одновалентной меди Cu2C2. В 1878 немецкий металлург Ф.Мюллер, растворив образцы стали в разбавленной серной кислоте, выделил карбид железа Fe3C. Но только в конце 19 в. французский химик Анри Муассан, прославившийся получением фтора, синтезировал многие из этих необычных соединений и изучил их свойства. Он получал карбиды, нагревая до очень высокой температуры смеси древесного угля с разными металлами, их оксидами или карбонатами. Для этого он использовал жар вольтовой дуги в электрической печи собственной конструкции.
В 1863 французский химик Марселен Бертло изучил свойства другого карбида – очень неустойчивого и легко взрывающегося карбида одновалентной меди Cu2C2. В 1878 немецкий металлург Ф.Мюллер, растворив образцы стали в разбавленной серной кислоте, выделил карбид железа Fe3C. Но только в конце 19 в. французский химик Анри Муассан, прославившийся получением фтора, синтезировал многие из этих необычных соединений и изучил их свойства. Он получал карбиды, нагревая до очень высокой температуры смеси древесного угля с разными металлами, их оксидами или карбонатами. Для этого он использовал жар вольтовой дуги в электрической печи собственной конструкции.
Карбиды, как оказалось, можно получить не только в лаборатории. Еще до работ Муассана австрийский ученый Э.Вайнсхенк в 1889 открыл в метеоритах минерал когенит, представляющий собой смешанный карбид железа, кобальта и никеля состава (FeNiCo)3C. А сам Муассан в 1904 обнаружил в метеорите, привезенном из каньона Диабло в штате Аризона, темно-зеленый минерал, представляющий собой карбид кремния SiC. Этот минерал в честь ученого назвали муассанитом.
Этот минерал в честь ученого назвали муассанитом.
Также по теме:
УГЛЕРОД
Раньше карбиды классифицировали по их устойчивости к действию воды и кислот, а также по тому, какие газы выделяются при их разложении. Современная классификация учитывает тип химической связи между атомами в карбидах – именно от этого зависят в основном физические и химические свойства. В соответствии с этой классификацией, карбиды можно разделить на три группы, которые довольно сильно отличаются по своим свойствам.
К первой группе относятся так называемые солеобразные карбиды с ионной связью. Эти карбиды образуют щелочные и щелочноземельные металлы, алюминий, редкоземельные элементы, а также актиноиды. Их состав иногда соответствует типичным валентностям металлов (Al4C3), а иногда – нет (Ве2С). Многие ионные карбиды можно получить непосредственно из элементов (Са + 2С ® СаС2) или восстановлением оксидов углеродом (СаО + 3С ® СаС2 + СО). Ионный характер связи приводит к высокой температуре плавления; например, карбид кальция СаС2 плавится при 2300°С, карбид тория ThC2 – при 2655°С. Водой или разбавленными кислотами ионные карбиды легко разлагаются – гидролизуются. При этом образуются различные углеводороды и гидроксид металла. Самый известный пример – получение ацетилена гидролизом карбида кальция: СаС2 + 2Н2О ® Ca(OH)2 + С2Н2. Ацетилен выделяется также при гидролизе Na2C2, К2С2 и др. Поэтому такие карбиды можно рассматривать как производные ацетилена, в которых атомы водорода замещены атомами металла. При этом катионы металла и анионы С2–2 размещаются в соответствующих узлах кристаллической решетки. Солеобразный характер этих карбидов подтверждается возможностью их электролиза в расплавленном состоянии. Интересно отметить, что чистый карбид кальция – бесцветные кристаллы, хотя увидеть их непросто, так как обычный технический продукт имеет цвет от бурого до черного.
Водой или разбавленными кислотами ионные карбиды легко разлагаются – гидролизуются. При этом образуются различные углеводороды и гидроксид металла. Самый известный пример – получение ацетилена гидролизом карбида кальция: СаС2 + 2Н2О ® Ca(OH)2 + С2Н2. Ацетилен выделяется также при гидролизе Na2C2, К2С2 и др. Поэтому такие карбиды можно рассматривать как производные ацетилена, в которых атомы водорода замещены атомами металла. При этом катионы металла и анионы С2–2 размещаются в соответствующих узлах кристаллической решетки. Солеобразный характер этих карбидов подтверждается возможностью их электролиза в расплавленном состоянии. Интересно отметить, что чистый карбид кальция – бесцветные кристаллы, хотя увидеть их непросто, так как обычный технический продукт имеет цвет от бурого до черного.
Взаимодействие карбидов щелочных металлов с водой протекает исключительно бурно. Так, если карбид калия просто облить водой, произойдет бурная реакция, которая сопровождается взрывом такой силы, что выделяющийся ацетилен сразу же разлагается с выделением угля. Чтобы провести реакцию К2С2 + 2Н2О ® 2КОН + С2Н2, надо медленно пропускать над карбидом водяной пар.
Чтобы провести реакцию К2С2 + 2Н2О ® 2КОН + С2Н2, надо медленно пропускать над карбидом водяной пар.
В ряде случаев карбиды ионного типа образуются непосредственно при пропускании ацетилена через растворы солей металлов. Так карбиды серебра, меди(I), золота и ртути, которые чаще называют ацетиленидами. Ацетилениды щелочных металлов можно получить действием ацетилена на свободные металлы. В сухом виде ацетилениды тяжелых металлов легко разлагаются со взрывом. Гидролиз ионных карбидов других металлов показывает, что они «происходят» из других углеводородов. Например, при гидролизе карбида алюминия выделяется метан: Al4C3 + 12h3O ® 4Al(OH)3 + 3Ch5 (так же гидролизуется карбид бериллия Ве2С), а при гидролизе карбида магния получается метилацетилен: Mg2C3 + 4h3O ® 2Mg(OH)2+ НС≡С–СН3. Интересно, что карбид магния другого состава, MgC2, дает при гидролизе только ацетилен. Иногда при гидролизе ионных карбидов углеводороды выделяются совместно с водородом, который частично гидрирует непредельные углеводороды. С выделением почти равных количеств водорода и метана разлагается карбид марганца: Mn3C + 6h3O ® 3Mn(OH)2 + Ch5 + h3. Карбиды редкоземельных металлов и тория при разложении разбавленными кислотами выделяют не чистый ацетилен, а его смесь с метаном, этиленом и другими углеводородами. Например, при гидролизе карбида церия СеС2 получается смесь ацетилена с метаном в соотношении 4:1, а также немного этилена и жидких и твердых углеводородов (состав продуктов зависит от условий проведения реакции). Еще больше жидких и твердых углеводородов дает при гидролизе карбид урана.
С выделением почти равных количеств водорода и метана разлагается карбид марганца: Mn3C + 6h3O ® 3Mn(OH)2 + Ch5 + h3. Карбиды редкоземельных металлов и тория при разложении разбавленными кислотами выделяют не чистый ацетилен, а его смесь с метаном, этиленом и другими углеводородами. Например, при гидролизе карбида церия СеС2 получается смесь ацетилена с метаном в соотношении 4:1, а также немного этилена и жидких и твердых углеводородов (состав продуктов зависит от условий проведения реакции). Еще больше жидких и твердых углеводородов дает при гидролизе карбид урана.
Выделение углеводородов при гидролизе карбидов позволило Д.И.Менделееву выдвинуть так называемую карбидную теорию происхождения нефти в глубинах Земли из неорганических веществ. По представлению Менделеева, в глубинах земного шара должны быть расплавленные металлы, в основном железо, которое с углеродом дает карбид. Во время горообразования в земной коре образуются трещины, по которым в глубины проникает вода. Воздействуя на карбид железа и карбиды других металлов, вода (в виде пара) образует углеводороды, например: 2FeC + 3h3O ® Fe2O3 + C2h5. Газообразные углеводороды по тем же трещинам поднимаются ближе к поверхности, где скапливаются в пористых пластах. Однако когда в 60-е гг. 20 в. был подробно изучен состав углеводородов нефти, оказалось, что смесь «искусственных углеводородов», образующихся при гидролизе карбидов, по своему составу резко отличается от природной смеси. Кроме того, все нефти, полученные неорганическим путем, оптически неактивны, тогда как природная нефть оптически активна. На основании этих, а также ряда других фактов неорганическая теория происхождения нефти была подвергнута критике, и в настоящее время многие ученые полагают, что нефть имеет биологическое происхождение.
Газообразные углеводороды по тем же трещинам поднимаются ближе к поверхности, где скапливаются в пористых пластах. Однако когда в 60-е гг. 20 в. был подробно изучен состав углеводородов нефти, оказалось, что смесь «искусственных углеводородов», образующихся при гидролизе карбидов, по своему составу резко отличается от природной смеси. Кроме того, все нефти, полученные неорганическим путем, оптически неактивны, тогда как природная нефть оптически активна. На основании этих, а также ряда других фактов неорганическая теория происхождения нефти была подвергнута критике, и в настоящее время многие ученые полагают, что нефть имеет биологическое происхождение.
Ко второй группе относятся карбиды, которые образуют переходные металлы IV–VII групп, а также кобальт, железо и никель. Это металлоподобные соединения с другой структурой. В них атомы углерода, имеющие небольшие размеры, не связаны друг с другом и располагаются в пустотах между атомами металлов. Различная упаковка атомов металла в кристаллической решетке приводит к разному составу карбидов даже для одного и того же металла; например, хром образует карбиды состава Cr3C2, Cr4C, Cr7C3 и др. Эти карбиды (их называют карбидами внедрения) часто отличаются большой твердостью и очень высокими температурами плавления. Например, карбиды тантала и гафния TaC и HfC – наиболее тугоплавкие из известных веществ (плавятся при 3985 и 3890°С соответственно).
Эти карбиды (их называют карбидами внедрения) часто отличаются большой твердостью и очень высокими температурами плавления. Например, карбиды тантала и гафния TaC и HfC – наиболее тугоплавкие из известных веществ (плавятся при 3985 и 3890°С соответственно).
Металлоподобные карбиды обладают высокой электропроводностью и очень высокой химической стойкостью к агрессивным средам (многие из них не растворяются даже в царской водке). Они используются для упрочнения чугуна и стали (карбиды железа, хрома, вольфрама, молибдена), а также для производства очень твердых сплавов, которые применяют для обработки металлов резанием (карбиды WC, TiC, TaC, VC, Cr3C2). Например, твердые наконечники резцов, сверл делают из победита – спеченного порошка карбида вольфрама WC с добавкой металлического кобальта. Очень важную роль играет карбид железа Fe3C (цементит) – твердые кристаллы, входящие в структуру чугуна и стали.
Карбид вольфрама WC используют также для изготовления буровых коронок, деталей аппаратуры для производства синтетических алмазов, для нанесения износостойких покрытий на поверхности металлов. Карбид титана интересен ярким проявлением нестехиометрии: состав этого соединения выражается формулой TiCх
Карбид титана интересен ярким проявлением нестехиометрии: состав этого соединения выражается формулой TiCх
, где
х
колеблется в пределах от 0,49 до 1 (
см
. СТЕХИОМЕТРИЯ). Это вещество, как и карбид вольфрама, используют как компонент жаропрочных, жаростойких и твердых сплавов, для получения износостойких покрытий, для изготовления тугоплавких тиглей, в которых можно плавить почти любые металлы (сам карбид плавится при 3257°С). Карбидом титана выкладывают внутренние стенки высокотемпературных печей.
К третьей группе относятся ковалентные карбиды. Их образуют кремний и бор – соседи углерода по периодической таблице, близкие к нему как по размеру атомов, так и по электроотрицательности. Карбид кремния SiC (техническое название – карборунд) в чистом виде – бесцветные кристаллы, но примеси часто окрашивают его в различные цвета, вплоть до черного. По своей структуре это соединение аналогично алмазу; решетку карбида кремния можно получить, если в немного расширенной решетке алмаза заменить половину атомов углерода на атомы кремния. Это вещество обладает очень высокой твердостью; помимо этого оно имеет свойства полупроводника. Из него делают шлифовальные бруски и круги, огнеупорные материалы для печей и литейных машин, нагревательные элементы для электропечей, полупроводниковые диоды.
Это вещество обладает очень высокой твердостью; помимо этого оно имеет свойства полупроводника. Из него делают шлифовальные бруски и круги, огнеупорные материалы для печей и литейных машин, нагревательные элементы для электропечей, полупроводниковые диоды.
Бор образует по два карбида с точно известной структурой – В4С и В13С2. Наибольшее значение имеет первый из них – черные блестящие кристаллы, которые по твердости уступают лишь алмазу и нитриду бора BN. Этот карбид применяют для изготовления абразивных и шлифовальных материалов и в качестве полупроводника. Карбид, обогащенный изотопом 10В, используется как поглотитель нейтронов в ядерных реакторах.
Илья Леенсон
Способ получения карбида кальция
Изобретение может быть использовано в химической промышленности и охране окружающей среды. Твердые бытовые отходы, например бумагу, картон, дерево, кожу, пластмассу, текстиль, подвергают пиролизу. Продукты пиролиза с содержанием летучих 4-10 масс.% и зольностью не выше 6 масс. % используют в качестве углеродистого восстановителя при плавлении извести в электротермической печи. Плавление ведут в режиме печи сопротивления при удельной плотности тока на электроде 1,5-2,0 А/см2 с использованием полых электродов. Расплав охлаждают в печи и извлекают. Содержание СаС2 – 85 масс.%, литраж – до 316 л/кг. Изобретение позволяет улучшить экологию путем утилизации твердых бытовых отходов и исключения образования в процессе плавления хлорорганических соединений. Сокращается продолжительность процесса. 1 з.п. ф-лы.
% используют в качестве углеродистого восстановителя при плавлении извести в электротермической печи. Плавление ведут в режиме печи сопротивления при удельной плотности тока на электроде 1,5-2,0 А/см2 с использованием полых электродов. Расплав охлаждают в печи и извлекают. Содержание СаС2 – 85 масс.%, литраж – до 316 л/кг. Изобретение позволяет улучшить экологию путем утилизации твердых бытовых отходов и исключения образования в процессе плавления хлорорганических соединений. Сокращается продолжительность процесса. 1 з.п. ф-лы.
Изобретение относится к химической технологии, в частности к получению карбида кальция.
Известен способ получения карбида кальция, включающий плавление шихты, состоящей из оксида кальция (извести) и углеродистого восстановителя (кокса, антрацита) (Кузнецов Л.А. Производство карбида кальция. М.: 1954, с.77-78).
Недостатком способа является использование дорогостоящих и дефицитных углеродистых материалов (металлургического кокса и антрацита), а также длительность процесса из-за незначительной поверхности контакта реагирующих элементов.
Известен способ получения карбида кальция (патент РФ № 2129093, кл. С 01 В 31/32, заявл. 1,1.03.97), согласно которому коксозольный остаток термической переработки окисленных бурых углей состава, масс.%: СаО – 4.75, С – 34.5, Fe2О3 – 6.6, SiO2 – 5.0, Mg – 3.3, Al2О3 – 1.6, S – 0.1, остальное 0,5, смешивают с 12,9-28,3% от массы смеси карбоната кальция в виде известняка, подвергают высокотемпературной плавке при 2000-2100°С, охлаждают, разделяют СаС2 и ферросилиций, получают СаС2 с литражом 275-285 л/кг и содержанием ферросилиция 0,1-0,2 масс.%. Использование отходов угледобычи позволяет снизить себестоимость карбида кальция на 30%.
Недостатками способа являются технологические сложности при эксплуатации производства и ухудшение технико-экономических и экологических показателей процесса, обусловленные значительным содержанием примесей (железа, кремния, магния).
Известен также способ получения карбида кальция (а. с. № 350753, Кл. С 01 В 31/30, заявл. 15.06.70) путем взаимодействия извести с углеводородами (с коксом или без него), согласно которому в качестве углеводородов используют жидкие или твердые парафиновые, ароматические, высокомолекулярные соединения гибридного или гетероциклического строения, а также их технические смеси, например, мазут или сырой антрацит. Углеводородное сырье подают в реакционное пространство электродуговой печи через полые электроды. При взаимодействии углеводородов с накаленной до 2000-2500°C поверхностью расплава последние расщепляются с выделением углерода, что позволяет интенсифицировать процесс по сравнению, например, с использованием в качестве углеродистого восстановителя антрацита или кокса.
с. № 350753, Кл. С 01 В 31/30, заявл. 15.06.70) путем взаимодействия извести с углеводородами (с коксом или без него), согласно которому в качестве углеводородов используют жидкие или твердые парафиновые, ароматические, высокомолекулярные соединения гибридного или гетероциклического строения, а также их технические смеси, например, мазут или сырой антрацит. Углеводородное сырье подают в реакционное пространство электродуговой печи через полые электроды. При взаимодействии углеводородов с накаленной до 2000-2500°C поверхностью расплава последние расщепляются с выделением углерода, что позволяет интенсифицировать процесс по сравнению, например, с использованием в качестве углеродистого восстановителя антрацита или кокса.
Недостатком способа являются большие энергетические затраты, обусловленные высокотемпературным расщеплением углеводородов (2500°С), а также невозможность использования побочных продуктов технологического процесса (смесь сажи, водорода, ацетилена), что ухудшает экологию процесса.
Кроме того, в процессе используется плавление карбида кальция в дуговом режиме работы карбидной печи, что определяет удельную плотность электрического тока в электроде 5-7 А/см2 (Электротермические процессы химической технологии. Л.: Химия, Ленинградское отделение, 1984, с.212) Это ведет к значительным возгонам карбонатной составляющей шихтовых материалов, что также ухудшает экономические и экологические показатели процесса.
Наиболее близким к заявляемому способу получения карбида кальция (прототипом) является способ производства карбида кальция, описанный в заявке DE № 4241245 (кл. С 01 В 31/32, 1994), заключающийся в использовании при получении карбида кальция реакции обмена содержащего углерод соединения с оксидом кальция в электродуговой печи. В качестве содержащего углерод соединения используют измельченные отходы пластмасс, которые в присутствии тонкодисперсного оксида кальция (массовое соотношение оксида кальция к отходам пластмасс составляет 1:0,5-3) обрабатывают во вращающейся трубчатой печи. Процесс получения исходного материала (шихты) для производства карбида кальция идет в две стадии: сначала проводят пиролиз при 400-800°С, а затем кальцинирование при 1000-1300°С образовавшегося на первой стадии продукта, представляющего собой смесь оксида кальция и пиролизного кокса. После охлаждения до 500°С мелкие фракции (менее 3 мм) смеси карбида кальция с коксом отделяют, а крупные (более 3 мм) подают в закрытую карбидную печь как исходный материал для получения карбида кальция. Полученный карбид кальция содержит 82% СаС2.
Процесс получения исходного материала (шихты) для производства карбида кальция идет в две стадии: сначала проводят пиролиз при 400-800°С, а затем кальцинирование при 1000-1300°С образовавшегося на первой стадии продукта, представляющего собой смесь оксида кальция и пиролизного кокса. После охлаждения до 500°С мелкие фракции (менее 3 мм) смеси карбида кальция с коксом отделяют, а крупные (более 3 мм) подают в закрытую карбидную печь как исходный материал для получения карбида кальция. Полученный карбид кальция содержит 82% СаС2.
Известный способ дает возможность утилизации пластмассовых отходов и открывает малозатратный углеродистый компонент для процесса производства карбида кальция, однако он малоэффективен применительно к технологии получения карбида кальция, так как осуществляется в несколько стадий, что существенно влияет на продолжительность технологического процесса и качество целевого продукта. Кроме того, в среде, создаваемой в трубчатой печи, будет в качестве восстановителя образовываться сажа – вещество с пониженной активностью как восстановитель в системе взаимодействия СаО:С, а на второй стадии – прокаливание смеси оксида кальция и пиролизного кокса при температуре 1000-1300°С – будет происходить графитизация углерода, то есть снижение его восстановительной активности в процессе получения карбида кальция, что отрицательно скажется на интенсивности процесса. В заявке DE № 4241245 не указана температура, при которой проводился процесс плавления карбида кальция, но известно, что получение даже самого низкоплавкого карбида кальция не может быть осуществлено при температуре ниже 1750°С. Карбид кальция, полученный по известному способу и содержащий 82% СаС2, плавится при температуре не ниже 1900°С (см. рис. XIV.8 “Диаграмма плавкости системы СаО-СаС2 / Электротермические процессы химической технологии”. Химия, Ленинградское отделение, 1984 г., с.327). Приведенный в заявке DE № 4241245 диапазон температур 1000-1300°С относится к температуре кальцинации (просто прокалки) смеси оксида кальция и пиролизного кокса с целью получения более качественной шихты для производства карбида кальция. Следует также отметить, что значительное содержание в шихте углеродистых материалов (в способе-прототипе массовое соотношение оксида кальция к отходам пластмасс составляет 1:0,5-3,0) кроме необоснованного расхода сырья и энергии на его переработку, ведет к значительным газопылевым выбросам в системе, что негативно сказывается на экологии окружающей среды.
В заявке DE № 4241245 не указана температура, при которой проводился процесс плавления карбида кальция, но известно, что получение даже самого низкоплавкого карбида кальция не может быть осуществлено при температуре ниже 1750°С. Карбид кальция, полученный по известному способу и содержащий 82% СаС2, плавится при температуре не ниже 1900°С (см. рис. XIV.8 “Диаграмма плавкости системы СаО-СаС2 / Электротермические процессы химической технологии”. Химия, Ленинградское отделение, 1984 г., с.327). Приведенный в заявке DE № 4241245 диапазон температур 1000-1300°С относится к температуре кальцинации (просто прокалки) смеси оксида кальция и пиролизного кокса с целью получения более качественной шихты для производства карбида кальция. Следует также отметить, что значительное содержание в шихте углеродистых материалов (в способе-прототипе массовое соотношение оксида кальция к отходам пластмасс составляет 1:0,5-3,0) кроме необоснованного расхода сырья и энергии на его переработку, ведет к значительным газопылевым выбросам в системе, что негативно сказывается на экологии окружающей среды.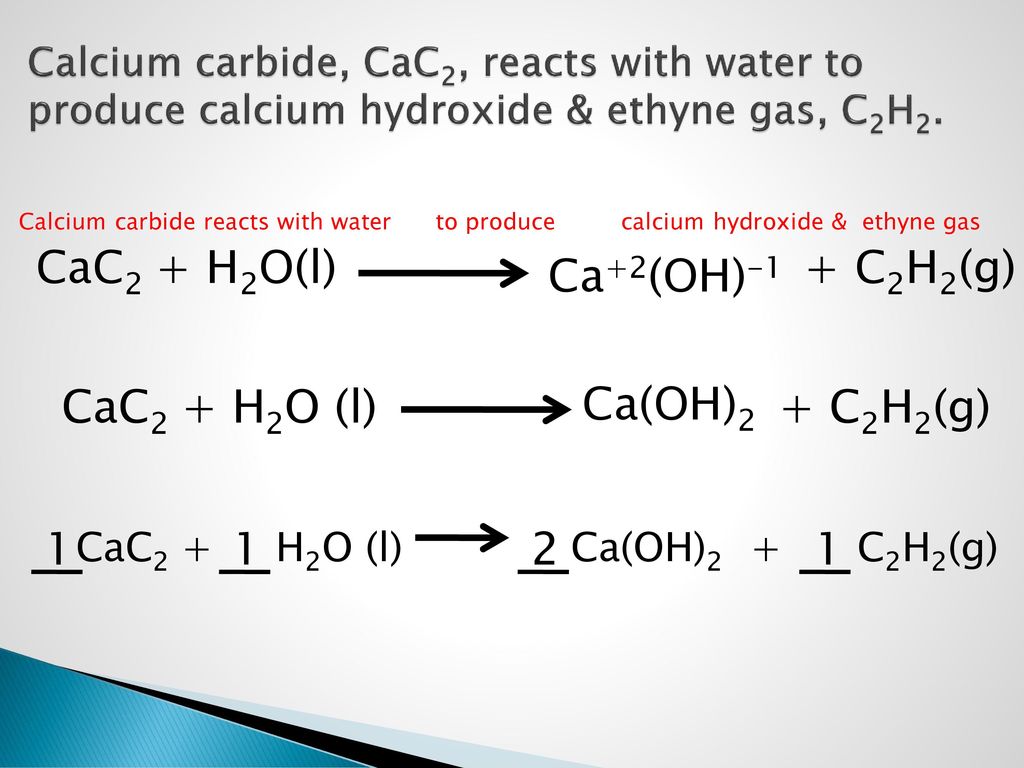
Задачей предлагаемого изобретения является повышение эффективности способа за счет сокращения продолжительности процесса, увеличения выхода целевого продукта высокого качества и расширения сырьевой базы, а также его экологичности.
Поставленная задача достигается тем, что в способе получения карбида кальция путем плавления в электротермической печи извести и углеродистого восстановителя, в качестве которого используют продукты пиролиза твердых бытовых отходов, согласно изобретению берут продукты пиролиза с содержанием летучих 4-10 масс.% и зольностью не выше 6 масс.% и плавление ведут в режиме печи сопротивления при удельной плотности тока на электроде 1,5-2,0 А/см2 с использованием полых электродов, при этом берут отходы бумаги, картона, дерева, кожи, пластмасс, текстиля.
Заявляемый способ получения карбида кальция является эффективным и экологичным, так как пиролиз некомпостируемых твердых бытовых отходов (ТБО) проводится в закрытой емкости с косвенным обогревом при температуре до 800°С с получением активного углеродистого восстановителя, который содержит летучих 4-10 масс. %, разлагаемых при нагреве в результате непосредственного контакта с расплавом карбида кальция (температура 1800-2000°С) и насыщающих оксид кальция молекулярным углеродом в зоне твердофазных процессов в ванне карбидной печи, что приводит к возрастанию интенсивности процесса в зоне плавления, исключает разбавление пиролизного газа и определяет незначительные (по сравнению с процессом сжигания) объемы газопылевых выбросов. Кроме того, в предлагаемом способе используется двухкомпонентная шихта: оксид кальция и углеродистый восстановитель подаются в карбидную печь раздельно и это позволяет строго выдерживать оптимальное соотношение оксида кальция к углеродистому восстановителю в пределах 1:0,65-0,85, что значительно улучшает качество получаемого карбида кальция.
%, разлагаемых при нагреве в результате непосредственного контакта с расплавом карбида кальция (температура 1800-2000°С) и насыщающих оксид кальция молекулярным углеродом в зоне твердофазных процессов в ванне карбидной печи, что приводит к возрастанию интенсивности процесса в зоне плавления, исключает разбавление пиролизного газа и определяет незначительные (по сравнению с процессом сжигания) объемы газопылевых выбросов. Кроме того, в предлагаемом способе используется двухкомпонентная шихта: оксид кальция и углеродистый восстановитель подаются в карбидную печь раздельно и это позволяет строго выдерживать оптимальное соотношение оксида кальция к углеродистому восстановителю в пределах 1:0,65-0,85, что значительно улучшает качество получаемого карбида кальция.
Углеродистый восстановитель получают следующим образом. Готовят шихту из следующих фракций ТБО в соотношениях компонентов в соответствии с морфологическим составом ТБО (мас.%): бумага, картон – 58; дерево – 6,5; кожа – 4,3; пластические массы – 19,6; текстиль – 11. Шихту подвергают термическому нагреву в закрытой емкости до температуры 800°C и выдерживают при этой температуре 2 часа. Выделяющуюся в процессе термообработки шихты газопаровую фазу или сжигают «на свечу» или утилизируют как теплоноситель. Коксовый остаток, используемый далее в процессе получения карбида кальция в качестве углеродистого восстановителя, охлаждают и анализируют. Получаемый углеродистый восстановитель имеет состав (мас.%): углерод – Собщий – 90-94, в том числе летучие – 4-10; содержание металлов СаО – 0,28-0,6; Al – 0,1-0,96; Mg – 0,05-0,096; Fe – 0,09-0,91; Si – 0,13-2,94; Cr – 0,003-0,038; Ti – 0,01-0,025; Cu – 0,0001-0,015; Zn – 0,001-0,003; Ni – 0,002; Cd<0,001; Pb – 0,003; P<0,03; Mn – 0,001.
Шихту подвергают термическому нагреву в закрытой емкости до температуры 800°C и выдерживают при этой температуре 2 часа. Выделяющуюся в процессе термообработки шихты газопаровую фазу или сжигают «на свечу» или утилизируют как теплоноситель. Коксовый остаток, используемый далее в процессе получения карбида кальция в качестве углеродистого восстановителя, охлаждают и анализируют. Получаемый углеродистый восстановитель имеет состав (мас.%): углерод – Собщий – 90-94, в том числе летучие – 4-10; содержание металлов СаО – 0,28-0,6; Al – 0,1-0,96; Mg – 0,05-0,096; Fe – 0,09-0,91; Si – 0,13-2,94; Cr – 0,003-0,038; Ti – 0,01-0,025; Cu – 0,0001-0,015; Zn – 0,001-0,003; Ni – 0,002; Cd<0,001; Pb – 0,003; P<0,03; Mn – 0,001.
Выход продукта – 35-38%. Продукт различной грануляции, легко размалываемый.
Поскольку углеродистый восстановитель, полученный в процессе пиролиза ТБО, имеет малую прочность, легко истирается в транспортных системах при подаче его в ванну карбидной печи, наиболее рационально его использование по следующей технологии.
Первое – раздельная подача компонентов шихты для выплавки карбида кальция в ванну печи. Известковый компонент шихты грануляцией 12-25 мм подают в ванну, мелкодисперсный углеродистый восстановитель, размолотый до грануляции минус 3 мм, подают непосредственно в зону расплава карбида кальция через полый электрод.
Второе – режим плавки с учетом возможности выноса мелкодисперсного компонента шихты мягкий, при малой плотности тока на электроде в пределах 1,5-2,0 А/см2 и при низком рабочем напряжении 45-50 вольт, т.е бездуговой режим плавления в режиме печи сопротивления.
Пример
Готовят шихту из 960 г извести грануляцией 10-15 мм, загружают ее в ванну лабораторной карбидной печи мощностью 40 кВт. Печь работает при следующих электрических характеристиках: напряжение – 40 вольт, плотность тока в электроде 1,5-2 А/см2. Для запуска печи на под насыпают низколитражную мелочь карбида кальция. После разогрева печи (через 15 минут) через отверстие по центру полого угольного электрода подают в расплав углеродистый восстановитель в количестве 650 г грануляцией минус 3 мм, при этом между жидкой фазой, представляющей расплав СаС2-СаО, и твердым углеродом происходит реакция карбидообразования при температурах 1800-2200°C. Известь растворяется в расплаве и взаимодействует с углеродистым восстановителем. Реакционные газы, проходя через слой извести, насыщают ее углеродом и это способствует более активному растворению извести в расплаве СаС2-СаО. Взаимодействие расплава СаС2-СаО с углеродистым восстановителем приводит к обогащению жидкой ванны карбидом до соотношения, отвечающего температуре и давлению СО в печи. Остаточное содержание летучих пиролизуется в зоне высоких температур при подаче восстановителя непосредственно в зону расплава, продукт пиролиза дополнительно насыщает известковую составляющую углеродом.
Известь растворяется в расплаве и взаимодействует с углеродистым восстановителем. Реакционные газы, проходя через слой извести, насыщают ее углеродом и это способствует более активному растворению извести в расплаве СаС2-СаО. Взаимодействие расплава СаС2-СаО с углеродистым восстановителем приводит к обогащению жидкой ванны карбидом до соотношения, отвечающего температуре и давлению СО в печи. Остаточное содержание летучих пиролизуется в зоне высоких температур при подаче восстановителя непосредственно в зону расплава, продукт пиролиза дополнительно насыщает известковую составляющую углеродом.
Срабатывание шихтовых материалов постоянно компенсируют раздельной подачей компонентов: извести в объем ванны, углеродистого восстановителя в зону расплава через отверстие в электроде. По конструктивным особенностям используемой лабораторной карбидной печи плавку ведут «на блок». Расплав охлаждают в печи, извлекают, анализируют. Вес выплавленного карбида кальция – 1,2 кг. Получают продукт с содержанием СаС2 – 85% (литраж 316 л/кг).
Получают продукт с содержанием СаС2 – 85% (литраж 316 л/кг).
Удельный расход сырья (на 1 кг условного карбида кальция):
известь – 960 г,
углеродистый восстановитель – 650 г.
Содержание примесей в карбиде кальция: РН3 – менее 0,003%;
Н2S – менее 0,015%.
Остаточное содержание летучих в углеродистом восстановителе свыше 10% ухудшает процесс получения карбида кальция, т.к. при плавлении карбида кальция возрастает интенсивность выделения летучих, нарушается работоспособность элементов конструкции печи, реакционные газы процесса засоряются непрореагировавшими сажистыми включениями, что осложняет работу элементов печи (снижается электрическое сопротивление изоляции и возникают пробои в электроизоляции) и осложняет работу узла газоочистки реакционных газов.
Снижение содержания летучих в углеродистом восстановителе менее 4% массовых нежелательно, т.к. резко снижается интенсивность плавления карбида кальция за счет сокращения зоны твердофазных процессов в ванне печи, где имеет место нагрев шихты и насыщение окиси кальция углеродом, что определяет интенсивность процесса в зоне плавления.
Низкая зольность, не выше 6 масс.%, углеродистого восстановителя исключает необходимость дополнительных затрат энергии и сырья, расходуемых при производстве карбида кальция, на побочные нецелевые реакции, снижает величину возгонов в процессе плавления соединений элементов, содержащихся в золе, имеющих более низкие температуры плавления и разложения, чем карбид кальция.
Предлагаемый способ позволяет исключить образование больших объемов реакционных газов (водорода, ацетилена), смешанных с сажей, не подлежащих использованию и тем самым улучшить экологичность процесса. Остатки хлора, которые в основной массе отогнаны из углеродистого восстановителя при пиролизе твердых бытовых отходов, связываются в прочное соединение CaCl2, которое имеет температуру плавления ниже температуры плавления СаС2 и поэтому выводится из процесса без разложения, что исключает образование в процессе плавления карбида кальция опасных хлорорганических соединений (диоксинов, фуранов).
Таким образом, заявляемый способ получения карбида кальция является более эффективным и экологичным по сравнению со способом-прототипом, так как проходит в одну стадию, позволяет получать карбид кальция более высокого качества с содержанием СаС2 85 масс.% (литраж до 316 л/кг) и при этом вовлечь в переработку продукты пиролиза твердых бытовых отходов (бумаги, картона, дерева, кожи, пластмасс, текстиля), которые в настоящее время практически не утилизируются, что значительно улучшает общую экологическую обстановку окружающей среды.
1. Способ получения карбида кальция путем плавления в электротермической печи извести и углеродистого восстановителя, в качестве которого используют продукты пиролиза твердых бытовых отходов, отличающийся тем, что берут продукты пиролиза с содержанием летучих 4-10 мас.% и зольностью не выше 6 мас.% и плавление ведут в режиме печи сопротивления при удельной плотности тока на электроде 1,5-2,0 А/см2 с использованием полых электродов.
2. Способ по п.1, отличающийся тем, что используют отходы бумаги, картона, дерева, кожи, пластмасс, текстиля.
Карбид кальция – структура, производство, применение и часто задаваемые вопросы
Карбид кальция, также называемый ацетилидом кальция, представляет собой химическое соединение, имеющее химическую формулу CaC2. В основном он используется в промышленности для производства цианамида кальция и ацетилена.
Это чистый материал бесцветного, а, однако, куски технического соединения карбида кальция имеют либо коричневый, либо серый цвет и состоят примерно на 80–85 % из СаС2 (остальное — СаО — оксид кальция), Са3Р2 ( фосфид кальция), Ca3N2 (нитрид кальция), CaS (сульфид кальция), SiC (карбид кремния) и др.). При наличии следов влаги карбид кальция технический издает неприятный запах, напоминающий запах чеснока.
Примечание. Применение карбида кальция включает производство газообразного ацетилена и производство ацетилена в карбидных лампах; производство химикатов для удобрений; а также в сталелитейном производстве.
Структура CaC2
Рассмотрим структуру карбида кальция.
(изображение скоро будет загружено)
Производство карбида кальция
Карбид кальция промышленно производится в электродуговой печи со смесью кокса и извести, примерно при 2200 °C (3,990°F). Это эндотермическая реакция, которая требует высокой температуры для удаления монооксида углерода при 110 килокалориях (460 кДж) на моль. С момента своего изобретения в 1892 году этот метод не изменился.
CaO + 3C → CaC2 + CO
Высокая температура, необходимая для этой реакции, практически недостижима при традиционном сжигании. Итак, эту реакцию проводят в электродуговой печи с использованием графитовых электродов. Полученный карбидный продукт по весу будет содержать около 80% карбида кальция. Кроме того, карбид подвергается дальнейшему дроблению с образованием небольших кусков, размер которых может достигать 50 мм, а примеси концентрируются в более мелких фракциях.
Содержание CaC2 в этом продукте определяют путем измерения количества образовавшегося ацетилена при гидролизе. Например, немецкие и британские стандарты содержания более крупных фракций составляют 295 л/кг и 300 л/кг соответственно (при давлении 101 кПа и температуре 20 °C (68 °F)). Примеси карбида включают фосфид, который при гидролизе дает фосфин.
В химии эта реакция не была важной частью промышленной революции и стала возможной в Соединенных Штатах в результате чрезмерного количества недорогой гидроэлектроэнергии, которая производилась на Ниагарском водопаде до конца 20-го века.
Производство цианамида кальция
Соединение карбида кальция реагирует с азотом при более высоких температурах с образованием цианамида кальция. Это представлено с помощью приведенного ниже уравнения.
CaC2 + N2 → CaCN2 + C
Обычно в качестве удобрения можно использовать термин нитролим, представляющий собой цианамид кальция. Он также гидролизуется до цианамида, h3NCN.
Он также гидролизуется до цианамида, h3NCN.
Сталеплавильное производство
Рассмотрим использование цианамида кальция в сталеплавильном производстве, как указано ниже:
Карбид кальция можно использовать при десульфурации железа (чугун, чугун и сталь).
Возможно использование в качестве мощного раскислителя на объектах внепечной обработки.
Его можно использовать в качестве топлива в сталеплавильном производстве, чтобы увеличить долю брака до жидкого чугуна, в зависимости от экономики.
Карбидные лампы
Карбид кальция можно использовать в карбидных лампах. Капание воды на карбид приводит к образованию газообразного ацетилена, который, в свою очередь, горит и излучает свет. Хотя эти лампы давали более устойчивый и яркий свет, чем свечи, они были настолько опасны в угольных шахтах, что горючий газ метан делал их серьезной опасностью.
Присутствие горючих газов в угольных шахтах привело к появлению шахтерских ламп безопасности, таких как лампа Дэви, где проволочная сетка снижает риск воспламенения метана. Тем не менее карбидные лампы широко использовались в медных, оловянных и сланцевых рудниках, где метан не считался серьезной опасностью. Большинство ламп горняков теперь заменены электрическими лампами.
Но, тем не менее, карбидные лампы используются для добычи полезных ископаемых в нескольких менее богатых странах. Примером могут служить серебряные рудники недалеко от Потоси в Боливии. В настоящее время они также используются несколькими спелеологами, исследующими пещеры и другие подземные области, хотя в этом использовании их все чаще заменяют светодиодными лампами.
Использование карбида кальция (CaC2)
Карбид кальция используется в производстве поливинилхлорида в виде ацетилена, который является производным карбида кальция и используется в качестве сырья для производства ПВХ.

Карбид кальция также используется в производстве ацетилена и гидроксида кальция.
Может использоваться для удаления серы из железа. Удаление серы из любого материала называется десульфурацией.
Мы можем использовать его для производства цианамида кальция.
Это соединение также можно использовать в качестве агента созревания, такого как этилен.
Может использоваться в лампах, таких как карбидные лампы. Раньше его использовали в качестве автомобильных фар.
Он также используется в качестве раскислителя, что означает, что он помогает удалять кислород при производстве стали.
Он также используется в бамбуковых пушках и пушках большого взрыва.

Объем рынка карбида кальция, рост, тенденции
Объем мирового рынка карбида кальция оценивался в 14,78 млрд долларов США в 2021 году. Прогнозируется, что рынок вырастет с 15,30 млрд долларов США в 2022 году до 21,02 млрд долларов США в 2029 году, демонстрируя среднегодовой темп роста 4,6% в течение прогнозируемого периода. Глобальная пандемия COVID-19 была беспрецедентной и ошеломляющей: спрос на карбид кальция во всех регионах превысил ожидаемый по сравнению с допандемическим уровнем. Согласно нашему анализу, мировой рынок продемонстрировал рост на 1,5% в 2020 году по сравнению с 2019 годом..
Карбид кальция, также известный как CaC₂, в основном используется для производства ацетилена, цианамида кальция, карбидных ламп и игрушечных пушек. Он также используется для кондиционирования шлака, десульфурации и вдувания в печь при производстве стали. В текущем сценарии он широко используется для производства газообразного ацетилена, который, в свою очередь, используется для производства поливинилхлорида или ПВХ. Производство ПВХ с использованием CaC₂ считается осуществимым методом, поскольку он не требует использования нефти или природного газа и имеет такие преимущества, как более низкая молекулярная масса и лучшие пластифицирующие свойства, чем ПВХ на нефтяной основе. Текущие тенденции на рынке — это растущий спрос на пластмассовые изделия на основе ПВХ, а также растущая химическая, сталелитейная и сельскохозяйственная промышленность.
Производство ПВХ с использованием CaC₂ считается осуществимым методом, поскольку он не требует использования нефти или природного газа и имеет такие преимущества, как более низкая молекулярная масса и лучшие пластифицирующие свойства, чем ПВХ на нефтяной основе. Текущие тенденции на рынке — это растущий спрос на пластмассовые изделия на основе ПВХ, а также растущая химическая, сталелитейная и сельскохозяйственная промышленность.
ВОЗДЕЙСТВИЕ COVID-19
Снижение спроса на ПВХ подорвало рынок на фоне пандемии COVID-19
Китай является крупным производителем и поставщиком сырья по всему миру. Распространение COVID-19 оказало жизненно важное влияние на цепочку поставок. Продукт находит широкое применение в производстве газообразного ацетилена, что, вероятно, повлияет на рынок карбида кальция. Этот фактор связан с общенациональным карантином в Китае, что привело к значительному сокращению производственных мощностей, неблагоприятной рабочей ситуации, отсутствию транспорта и снижению экспортной активности.
Кроме того, спрос на ПВХ также снижается, что влияет на спрос на карбид кальция. Снижение спроса на ПВХ можно объяснить остановкой заводов, сокращением строительных работ и замедлением цепочки поставок. Более того, пандемия также вызвала разрыв в цепочке экспорта и импорта, что привело к высоким экспортным ценам. Все вышеперечисленные факторы прямо или косвенно влияют на рост рынка ацетилида кальция.
ПОСЛЕДНИЕ ТЕНДЕНЦИИ
Запросите бесплатный образец , чтобы узнать больше об этом отчете.
Заметная тенденция роста спроса на ацетилен в различных областях применения
Рост коммерческого применения ацетилена повысил спрос на карбид кальция. Применения ацетилена включают питьевое освещение, сварку и резку металлов, производство химикатов, производство пластмасс и другие. ПВХ и ПВДФ производятся из производных ацетилена, таких как метан и этилен. Пластмассы являются очень экономичными и простыми в производстве продуктами, которые находят применение в различных отраслях промышленности. Этот растущий спрос на пластмассы еще больше поддерживает рост рынка. Кроме того, ацетилен используется для синтеза различных химических веществ. Постепенный рост химической промышленности будет способствовать дальнейшему росту рынка.
Этот растущий спрос на пластмассы еще больше поддерживает рост рынка. Кроме того, ацетилен используется для синтеза различных химических веществ. Постепенный рост химической промышленности будет способствовать дальнейшему росту рынка.
ДВИЖУЩИЕ ФАКТОРЫ
Растущий спрос на ацетилен и его производные для развития рынка полимеры и многое другое. Рост производства ацетилена и его производных эффективно повлиял на рост рынка карбида кальция.
Ацетилен также используется в различных отраслях промышленности, таких как фармацевтика, производство пластмасс, красителей и каучука. Производные ацетилена используются в различных потребительских товарах, таких как лаки для волос, косметика, солнцезащитные средства и лосьоны. Также эти производные служат сырьем для производства полиуретановых волокон и синтетического каучука. В настоящее время ацетилен в основном используется в производстве ПВХ в Китае, доминирующей стране в производстве и потреблении ацетилена. Следовательно, ожидается, что растущий спрос на ацетилен и его производные будет стимулировать потребление продукта в течение отчетного периода.
Следовательно, ожидается, что растущий спрос на ацетилен и его производные будет стимулировать потребление продукта в течение отчетного периода.
Увеличение производства стали для стимулирования роста рынка
CaC 2 используется в качестве десульфурирующего и восстановительного агента в сталелитейной промышленности. Кроме того, он также используется в качестве модулирующего агента при производстве доменного графита в чугуне и в качестве компонента чистового шлака при рафинировании черных и цветных металлов. В некоторых промышленных процессах карбид кальция также используется в качестве осушителя. Это увеличение связано с устойчивостью спроса на сталь, улучшением инвестиций и инфраструктурных программ. Следовательно, ожидается, что увеличение производства стали во всем мире из-за спроса на нее будет способствовать росту рынка.
ОГРАНИЧИВАЮЩИЕ ФАКТОРЫ
Вредное воздействие карбида кальция на здоровье для ограничения роста рынка
Карбид кальция может нанести вред здоровью потребителя при длительном воздействии. Кроме того, он используется для обработки пищевых продуктов, что чрезвычайно опасно, поскольку содержит частицы фосфора и мышьяка и при растворении в воде образует газообразный ацетилен. Мышьяк и ацетилен могут воздействовать на различные органы человеческого тела и вызывать различные проблемы со здоровьем, такие как головокружение, головная боль, сонливость, нарушения настроения, судороги и длительная гипоксия. Растущее осознание его воздействия на здоровье может снизить спрос на него, тем самым сдерживая рост рынка.
Кроме того, он используется для обработки пищевых продуктов, что чрезвычайно опасно, поскольку содержит частицы фосфора и мышьяка и при растворении в воде образует газообразный ацетилен. Мышьяк и ацетилен могут воздействовать на различные органы человеческого тела и вызывать различные проблемы со здоровьем, такие как головокружение, головная боль, сонливость, нарушения настроения, судороги и длительная гипоксия. Растущее осознание его воздействия на здоровье может снизить спрос на него, тем самым сдерживая рост рынка.
Сегментация
По приложениям. растет из нескольких приложений, таких как синтез растворителей и органических соединений, необходимых в фармацевтической промышленности и производстве красителей, кислородно-ацетиленовая сварка и производство пластмасс и синтетического каучука. Этот фактор привел к увеличению производства газообразного ацетилена, что, как ожидается, приведет к увеличению потребления продукта.
Газообразный ацетилен станет свидетелем высокого спроса в производстве поливинилхлорида, предпочтительного пластика для изготовления труб и фитингов, пленок и листов, а также проводов и кабелей. Использование газообразного ацетилена является предпочтительным сырьем для производства ПВХ, поскольку позволяет избежать зависимости от нефти и природного газа.
Использование газообразного ацетилена является предпочтительным сырьем для производства ПВХ, поскольку позволяет избежать зависимости от нефти и природного газа.
Растущее предпочтение цианамида кальция в сельском хозяйстве для производства удобрений приводит к росту продаж продукции во всем мире. Растущий спрос на восстановители и осушители со стороны химической промышленности создаст возможности для роста рынка. Кроме того, растущее использование продукта для десульфурации железа и в качестве топлива в сталеплавильном производстве будет стимулировать рынок в течение рассматриваемого периода. Ожидается, что другой сегмент будет расти из-за увеличения использования карбида кальция в игрушечных пушках, карбидных лампах и для созревания фруктов.
Согласно анализу конечных пользователей
Сегмент химикатов, демонстрирующий значительный среднегодовой темп роста в течение прогнозируемого периода , смолы, полимеры, цианамид кальция и другие органические химические вещества. Ожидается, что растущий спрос на ацетилен и его производные со стороны фармацевтической и пластмассовой промышленности, а также на цианамид кальция со стороны сельскохозяйственной отрасли будет стимулировать развитие этого сегмента. Кроме того, ожидается, что растущая химическая промышленность поддержит рост химического сегмента.
Ожидается, что растущий спрос на ацетилен и его производные со стороны фармацевтической и пластмассовой промышленности, а также на цианамид кальция со стороны сельскохозяйственной отрасли будет стимулировать развитие этого сегмента. Кроме того, ожидается, что растущая химическая промышленность поддержит рост химического сегмента.
Аналогичным образом ожидается, что сегмент производства стали придаст импульс рынку в течение прогнозируемого периода благодаря CaC 2 в качестве десульфурирующего и восстановительного агента и топлива в сталелитейной промышленности. Растущий спрос на десульфураторы и восстановители со стороны сталелитейной промышленности будет стимулировать рынок во всем мире.
РЕГИОНАЛЬНЫЕ ИНСАЙТЫ
Объем рынка карбида кальция в Азиатско-Тихоокеанском регионе, 2021 г. (млрд долларов США)
Чтобы получить дополнительную информацию о региональном анализе этого рынка, запросите бесплатный образец
Азиатско-Тихоокеанский регион составил 14,16 млрд долларов США в 2021 году. Ожидается, что в этом регионе будет наблюдаться самый высокий рост рынка в течение прогнозируемого периода. Процветающая химическая и сталелитейная промышленность в регионе является ключевым двигателем рынка. Китай, Индия и Япония являются ключевыми странами, вносящими вклад в рост рынка в регионе благодаря росту производства ПВХ в этих странах.
Ожидается, что в этом регионе будет наблюдаться самый высокий рост рынка в течение прогнозируемого периода. Процветающая химическая и сталелитейная промышленность в регионе является ключевым двигателем рынка. Китай, Индия и Япония являются ключевыми странами, вносящими вклад в рост рынка в регионе благодаря росту производства ПВХ в этих странах.
На Северную Америку придется значительная доля в 2021 году, и ожидается, что она останется ключевым регионом в течение прогнозируемого периода из-за увеличения спроса со стороны химической, сталелитейной и промышленной отраслей. Однако ожидается, что спрос в регионе Северной Америки будет расти при относительно более низком среднегодовом темпе роста, поскольку процессы производства ПВХ на основе природного газа и нефти были заменены методом преобразования карбида кальция в ПВХ.
Принимая во внимание, что в Европе ожидается значительный рост рынка. Растущий спрос на цианамид кальция со стороны сельскохозяйственной отрасли будет способствовать росту рынка в регионе. Кроме того, использование CaC 2 для десульфурации железа и в качестве топлива в сталеплавильном производстве и расширяющейся сталелитейной промышленности является другими ключевыми факторами, стимулирующими рост рынка ацетилида кальция в Европе.
Кроме того, использование CaC 2 для десульфурации железа и в качестве топлива в сталеплавильном производстве и расширяющейся сталелитейной промышленности является другими ключевыми факторами, стимулирующими рост рынка ацетилида кальция в Европе.
Прогнозируется, что в остальном мире темпы роста будут ниже, чем в других регионах, из-за предпочтения процессов производства ацетилена на основе нефти.
КЛЮЧЕВЫЕ ИГРОКИ ОТРАСЛИ
Ключевые производители укрепляют свои позиции, предлагая новые решения для химической промышленности
Основные производители этого рынка расположены в Китае, что приводит к фрагментации рынка. Производители, расположенные в Северной Америке и Европе, стремятся расширить свое присутствие в Китае и других странах Азиатско-Тихоокеанского региона, чтобы укрепить свои позиции на рынке и стимулировать рост бизнеса организации. Эти основные игроки на рынке добились прочного присутствия в регионах, мощного портфеля продуктов и каналов сбыта.
KC Group сохраняет сильное присутствие на внутреннем рынке. Компания приняла стратегии поддержания хороших отношений с потребителями, сохранения и расширения своего присутствия на местном рынке и предоставления качественных продуктов.
СПИСОК ОСНОВНЫХ КОМПАНИЙ:
- Carbide Industries LLC (США)
- APH – Regency Power Group (Индия)
- MCB Industries Bhd. (Малайзия)
- KC Group (Индия)
- DCM Shriram Ltd. (Индия)
- Alzchem (Германия)
- Denka Company Limited (Япония)
- American Elements (США)
- IN Mongolia BaiIMAICAICIAICA.
- Lonza (Switzerland)
- Mil-Spec Industries Corporation (U.S.)
- Xiahuayuan Xuguang Chemical (China)
- PT Emdeki Utama Tbk (Indonesia)
REPORT COVERAGE
Инфографическое представление рынка карбида кальция
Просмотреть полную инфографику
Чтобы получить информацию о различных сегментах, поделитесь с нами своими запросами. Кроме того, он дает представление о тенденциях мирового рынка карбида кальция и освещает важные события в отрасли. В дополнение к факторам, указанным выше, отчет включает в себя различные факторы, которые способствовали росту рынка в последние годы.
Кроме того, он дает представление о тенденциях мирового рынка карбида кальция и освещает важные события в отрасли. В дополнение к факторам, указанным выше, отчет включает в себя различные факторы, которые способствовали росту рынка в последние годы.
Report Scope & Segmentation
ATTRIBUTE | DETAILS |
Study Period | 2018 -2029 |
Базовый год | 2021 |
Estimated Year | 2022 |
Forecast Period | 2022-2029 |
Исторический период | 2018-2020 |
| 02 Unit | Value (USD Billion), Volume (Million Ton) |
Segmentation | Application, End-user, Geography |
по применению |
|
By End-user |
|
По географическому признаку | |
Рынок карбида кальция | Глобальный отраслевой отчет, 2031 г.

1. Резюме
1.1. Обзор рынка карбида кальция
1.2. Ключевые тенденции рынка
1.3. Текущий рынок и будущий потенциал
1.4. Колесо возможностей роста TMR
2. Обзор рынка
2.1. Сегментация рынка
2.2. Индикаторы рынка
2.3. Определения рынка
2.4. Динамика рынка
2.4.1. Драйверы
2.4.2. Ограничения
2.4.3. Возможности
2.5. Анализ пяти сил Портера
2.6. Анализ цепочки создания стоимости
2.6.1. Список потенциальных клиентов
3. Анализ воздействия COVID-19
4. Перспективы производства карбида кальция на рынке
5. Анализ динамики цен на рынке карбида кальция, 2019–2030 гг.
5.1. По конечному использованию
5.2. По регионам
6. Анализ и прогноз мирового рынка карбида кальция по конечному использованию, 2019–2030 гг.
6.1. Введение и определения
6.2. Прогноз объема мирового рынка карбида кальция (тонн) и стоимости (млн долларов США) по конечному использованию, 2019–2030 гг.
6.2.1. Производство стали
6.2.2. Агрохимия
6.2.3. Фармацевтическая
6.2.4. Изготовление металла
6.2.5. Строительный материал
6.2.6. Энергия и мощность
6.2.7. Прочее
6.3. Привлекательность мирового рынка карбида кальция по конечному использованию
7. Анализ и прогноз мирового рынка карбида кальция по приложениям, 2019–2030 гг.
7.1. Введение и определения
7.2. Прогноз объема мирового рынка карбида кальция (тонн) и стоимости (млн долларов США) по приложениям, 2019–2030 гг.
7.2.1. Десульфурирующий агент
7.2.2. Ацетилен Газ
7.2.3. Восстанавливающий агент
7. 2.4. Цианамид кальция
2.4. Цианамид кальция
7.2.5. Химический промежуточный продукт
7.2.6. Прочее
7.3. Привлекательность мирового рынка карбида кальция по приложениям
8. Анализ и прогноз мирового рынка карбида кальция по регионам, 2019 г.–2030
8.1. Основные выводы
8.2. Прогноз объема мирового рынка карбида кальция (тонн) и стоимости (млн долл. США) по регионам, 2019–2030 гг.
8.2.1. Северная Америка
8.2.2. Европа
8.2.3. Азиатско-Тихоокеанский регион
8.2.4. Латинская Америка
8.2.5. Ближний Восток и Африка
8.3. Привлекательность мирового рынка карбида кальция по регионам
9. Анализ и прогноз рынка карбида кальция в Северной Америке, 2019 г.–2030
9.1. Основные выводы
9.2. Прогноз объема рынка карбида кальция в Северной Америке (тонн) и стоимости (млн долларов США) по конечному использованию, 2019–2030 гг.
9.3. Прогноз объема рынка карбида кальция в Северной Америке (тонн) и стоимости (млн долларов США) по приложениям, 2019–2030 гг.
9.4. Прогноз объема рынка карбида кальция в Северной Америке (тонн) и стоимости (млн долларов США) по странам, 2019–2030 гг.
9.4.1. Прогноз объема рынка карбида кальция в США (тонн) и стоимости (млн долларов США) по конечному использованию, 2019 г.–2030
9.4.2. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) по заявкам, 2019–2030 гг.
9.4.3. Прогноз объема рынка карбида кальция в Канаде (тонн) и стоимости (млн долларов США) по конечному использованию, 2019–2030 гг.
9.4.4. Прогноз объема рынка карбида кальция в Канаде (тонн) и стоимости (млн долларов США) по заявкам, 2019–2030 гг.
9.5. Анализ привлекательности рынка карбида кальция в Северной Америке
10. Анализ и прогноз рынка карбида кальция в Европе, 2019 г.–2030
10. 1. Основные выводы
1. Основные выводы
10.2. Объем европейского рынка карбида кальция (тонн) и стоимость (млн долл. США) Прогноз по конечному использованию, 2019–2030 гг.
10.3. Прогноз объема европейского рынка карбида кальция (тонн) и стоимости (млн долларов США) по заявкам, 2019–2030
10.4. Прогноз объема европейского рынка карбида кальция (тонн) и стоимости (млн долларов США) по странам и субрегионам, 2019–2030 гг.
10.4.1. Прогноз объема рынка карбида кальция в Германии (тонн) и стоимости (млн долларов США) по конечному использованию, 2019 г.–2030
10.4.2. Прогноз объема рынка карбида кальция в Германии (тонн) и стоимости (млн долларов США) по заявкам, 2019–2030 гг.
10.4.3. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) по конечному использованию, 2019–2030 гг.
10.4.4. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) по приложениям, 2019–2030 гг.
10. 4.5. Прогноз объема рынка карбида кальция в Великобритании (тонн) и стоимости (млн долларов США) по конечному использованию, 2019 г.–2030
4.5. Прогноз объема рынка карбида кальция в Великобритании (тонн) и стоимости (млн долларов США) по конечному использованию, 2019 г.–2030
10.4.6. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) в Великобритании по заявкам, 2019–2030 гг.
10.4.7. Объем рынка карбида кальция в Италии (тонны) и стоимость (млн долларов США) Прогноз по конечному использованию, 2019–2030 гг.
10.4.8. Прогноз объема рынка карбида кальция в Италии (тонн) и стоимости (млн долларов США) по приложениям, 2019–2030 гг.
10.4.9. Прогноз объема рынка карбида кальция в Испании (тонн) и стоимости (млн долл. США) по конечному использованию, 2019–2030 гг.
10.4.10. Прогноз объема рынка карбида кальция в Испании (тонн) и стоимости (млн долларов США) по приложениям, 2019–2030 гг.
10.4.11. Объем рынка карбида кальция в России и СНГ (тонн) и стоимость (млн долл. США) Прогноз по конечному использованию, 2019–2030 гг.
10.4.12. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) в России и СНГ по заявкам, 2019–2030 гг.
10.4.13. Прогноз объема рынка карбида кальция в остальной Европе (тонн) и стоимости (млн долларов США) по конечному использованию, 2019 г.–2030
10.4.14. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долл. США) в остальной Европе по приложениям, 2019–2030 гг.
10.5. Анализ привлекательности европейского рынка карбида кальция
11. Анализ и прогноз рынка карбида кальция в Азиатско-Тихоокеанском регионе, 2019–2030 гг.
11.1. Основные выводы
11.2. Прогноз объема рынка карбида кальция в Азиатско-Тихоокеанском регионе (тонн) и стоимости (млн долл. США) по конечному использованию, 2019–2030 гг.
11.3. Прогноз объема рынка карбида кальция в Азиатско-Тихоокеанском регионе (тонн) и стоимости (млн долларов США) по заявкам, 2019 г.–2030
11. 4. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) в Азиатско-Тихоокеанском регионе по странам и субрегионам, 2019–2030 гг.
4. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) в Азиатско-Тихоокеанском регионе по странам и субрегионам, 2019–2030 гг.
11.4.1. Прогноз объема рынка карбида кальция в Китае (тонн) и стоимости (млн долларов США) по конечному использованию, 2019–2030 гг.
11.4.2. Прогноз объема рынка карбида кальция в Китае (тонн) и стоимости (млн долларов США) по заявкам, 2019–2030 гг.
11.4.3. Прогноз объема рынка карбида кальция в Японии (тонн) и стоимости (млн долларов США) по конечному использованию, 2019 г.–2030
11.4.4. Объем рынка карбида кальция в Японии (тонны) и стоимость (млн долларов США) Прогноз по приложениям, 2019–2030 гг.
11.4.5. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) по конечному использованию, 2019–2030 гг.
11.4.6. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) по приложениям, 2019–2030 гг.
11. 4.7. Прогноз объема рынка карбида кальция в странах АСЕАН (тонн) и стоимости (млн долл. США) по конечному использованию, 2019–2030 гг.
4.7. Прогноз объема рынка карбида кальция в странах АСЕАН (тонн) и стоимости (млн долл. США) по конечному использованию, 2019–2030 гг.
11.4.8. Прогноз объема рынка карбида кальция в АСЕАН (тонн) и стоимости (млн долларов США) по приложениям, 2019–2030 гг.
11.4.9. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долл. США) в Азиатско-Тихоокеанском регионе по конечному использованию, 2019–2030 гг.
11.4.10. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) в остальной части Азиатско-Тихоокеанского региона по заявкам, 2019–2030 гг.
11.5. Анализ привлекательности рынка карбида кальция в Азиатско-Тихоокеанском регионе
12. Анализ и прогноз рынка карбида кальция в Латинской Америке, 2019–2030 гг.
12.1. Основные выводы
12.2. Объем рынка карбида кальция в Латинской Америке (тонн) и стоимость (млн долл. США) Прогноз по конечному использованию, 2019–2030 гг.
12.3. Объем рынка карбида кальция в Латинской Америке (тонны) и стоимость (млн долл. США) Прогноз по заявкам, 2019–2030 гг.
12.4. Прогноз объема рынка карбида кальция в Латинской Америке (тонн) и стоимости (млн долларов США) по странам и субрегионам, 2019 г.–2030
12.4.1. Объем рынка карбида кальция Бразилии (тонны) и стоимость (млн долларов США) Прогноз по конечному использованию, 2019–2030 гг.
12.4.2. Объем рынка карбида кальция Бразилии (тонны) и стоимость (млн долларов США) Прогноз по заявкам, 2019–2030
12.4.3. Объем рынка карбида кальция в Мексике (тонны) и стоимость (млн долл. США) Прогноз по конечному использованию, 2019–2030 гг.
12.4.4. Прогноз объема рынка карбида кальция в Мексике (тонн) и стоимости (млн долларов США) по приложениям, 2019 г.–2030
12.4.5. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долл. США) в Латинской Америке по конечному использованию, 2019–2030 гг.
12.4.6. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долл. США) в Латинской Америке по заявкам, 2019–2030 гг.
12.5. Анализ привлекательности рынка карбида кальция в Латинской Америке
13. Анализ и прогноз рынка карбида кальция на Ближнем Востоке и в Африке, 2019–2030 гг.
13.1. Основные выводы
13.2. Ближний Восток и Африка Объем рынка карбида кальция (тонн) и стоимость (млн долларов США) Прогноз по конечному использованию, 2019–2030
13.3. Ближний Восток и Африка Объем рынка карбида кальция (тонн) и стоимость (млн долларов США) Прогноз по приложениям, 2019–2030
13.4. Ближний Восток и Африка Объем рынка карбида кальция (тонн) и стоимость (млн долларов США) Прогноз по странам и субрегионам, 2019–2030
13.4.1. Прогноз объема рынка карбида кальция GCC (тонн) и стоимости (млн долларов США) по конечному использованию, 2019 г.–2030
13.4.2. Объем рынка карбида кальция GCC (тонн) и стоимость (млн долларов США) Прогноз по заявкам, 2019–2030
Объем рынка карбида кальция GCC (тонн) и стоимость (млн долларов США) Прогноз по заявкам, 2019–2030
13.4.3. Южная Африка nada Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долл. США) по конечному использованию, 2019–2030 гг.
13.4.4. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долл. США) в Южной Африке по заявкам, 2019–2030 гг.
13.4.5. Прогноз объема рынка карбида кальция (тонн) и стоимости (млн долларов США) на Ближнем Востоке и в Африке по конечному использованию, 2019 г.–2030
13.4.6. Прогноз объема рынка карбида кальция на Ближнем Востоке и в Африке (тонн) и стоимости (млн долл. США) по заявкам, 2019–2030 гг.
13.5. Анализ привлекательности рынка карбида кальция на Ближнем Востоке и в Африке
14. Конкурентная среда
14.1. Анализ доли рынка компании на мировом рынке карбида кальция, 2019 г.
14.2. Профили компании (подробности — обзор, финансовые показатели, последние изменения и стратегия)
14. 2.1. ALMAMET GMBH
2.1. ALMAMET GMBH
14.2.1.1. Описание компании
14.2.1.2. Обзор бизнеса
14.2.1.3. Финансовый обзор
14.2.1.4. Стратегический обзор
14.2.2. Rexarc International, Inc.
14.2.2.1. Описание компании
14.2.2.2. Обзор бизнеса
14.2.2.3. Финансовый обзор
14.2.2.4. Стратегический обзор
14.2.3. Donau Chemie AG
14.2.3.1. Описание компании
14.2.3.2. Обзор бизнеса
14.2.3.3. Финансовый обзор
14.2.3.4. Стратегический обзор
14.2.4. Bisley & Company Pty Ltd
14.2.4.1. Описание компании
14.2.4.2. Обзор бизнеса
14.2.5. SMS group GmbH
14.2.5.1. Описание компании
Описание компании
14.2.5.2. Обзор бизнеса
14.2.5.3. Финансовый обзор
14.2.5.4. Стратегический обзор
14.2.6. Xiahuayuan Xuguang Chemical Co., Ltd
14.2.6.1. Описание компании
14.2.6.2. Обзор бизнеса
14.2.6.3. Финансовый обзор
14.2.6.4. Стратегический обзор
14.2.7. SHERWIN INDUSTRIES
14.2.7.1. Описание компании
14.2.7.2. Обзор бизнеса
14.2.7.3. Финансовый обзор
14.2.7.4. Стратегический обзор
14.2.8. MCB INDUSTRIES SDN. BHD
14.2.8.1. Описание компании
14.2.8.2. Обзор бизнеса
14.2.8.3. Финансовый обзор
14.2.8.4. Стратегический обзор
14.2.9. Denka Company Limited
14. 2.9.1. Описание компании
2.9.1. Описание компании
14.2.9.2. Обзор бизнеса
14.2.9.3. Финансовый обзор
14.2.9.4. Стратегический обзор
14.2.10. KC GROUP
14.2.10.1. Описание компании
14.2.10.2. Обзор бизнеса
14.2.10.3. Финансовый обзор
14.2.10.4. Стратегический обзор
14.2.11. Lonza
14.2.11.1. Описание компании
14.2.11.2. Обзор бизнеса
14.2.11.3. Финансовый обзор
14.2.11.4. Стратегический обзор
15. Первичные исследования: ключевые идеи
16. Приложение
Список таблиц
Таблица 1. Прогноз объема мирового рынка карбида кальция (тонн) по конечному использованию, 2019–2030 гг.
Таблица 2. Стоимость мирового рынка карбида кальция (млн долл. США) Прогноз по конечному использованию, 2019–2030
США) Прогноз по конечному использованию, 2019–2030
Таблица 3. Прогноз объема мирового рынка карбида кальция (тонн) по применению, 2019–2030 гг.
Таблица 4. Прогноз стоимости мирового рынка карбида кальция (млн долл. США) по применению , 2019–2030
Таблица 5. Прогноз объема мирового рынка карбида кальция (тонн) по регионам, 2019 г.–2030
Таблица 6. Прогноз стоимости мирового рынка карбида кальция (млн долл. США) по регионам, 2019–2030 гг.
Таблица 8. Прогноз рыночной стоимости карбида кальция в Северной Америке (млн долл. США) по конечному использованию, 2019–2030 гг. 10: Прогноз рыночной стоимости карбида кальция в Северной Америке (млн долларов США) по приложениям, 2019 г.–2030
Таблица 11. Прогноз объема рынка карбида кальция в Северной Америке (тонн) по странам, 2019–2030 гг.
Таблица 13. Прогноз объема рынка карбида кальция в США (тонн) по конечному использованию, 2019–2030 гг.
: Прогноз объема рынка карбида кальция в США (тонн) по приложениям, 2019 г. –2030
–2030
Таблица 16. Прогноз рыночной стоимости карбида кальция в США (млн долл. США) по потреблению, 2019–2030 гг.
Таблица 18. Прогноз рыночной стоимости карбида кальция в Канаде (млн долл. США) по конечному использованию, 2019–2030 гг.
Прогноз рыночной стоимости карбида кальция (млн долларов США) по заявкам, 2019 г.–2030
Таблица 21: Прогноз объема европейского рынка карбида кальция (тонн) по конечному использованию, 2019–2030
Таблица 22: Прогноз стоимости европейского рынка карбида кальция (млн долл. США) по конечному использованию, 2019–2030
Таблица 23: Прогноз объема европейского рынка карбида кальция (тонн) по применению, 2019–2030 гг.
Таблица 24: Прогноз стоимости европейского рынка карбида кальция (млн долл. США) по применению, 2019–2030 гг. Прогноз объема рынка карбида кальция (тонн) по странам и субрегионам, 2019 г.–2030
Таблица 26: Прогноз стоимости рынка карбида кальция в Европе (млн долл. США) по странам и субрегионам, 2019–2030
Таблица 27: Прогноз объема рынка карбида кальция в Германии (тонн) по конечному использованию, 2019 –2030
Таблица 28. Прогноз рыночной стоимости карбида кальция в Германии (млн долл. США) по конечному использованию, 2019–2030 гг.
Прогноз рыночной стоимости карбида кальция в Германии (млн долл. США) по конечному использованию, 2019–2030 гг.
Таблица 30. Прогноз рыночной стоимости карбида кальция в Германии (млн долл. США) по приложениям, 2019 г.–2030
Таблица 31. Прогноз объема рынка карбида кальция в Великобритании (тонн) по конечному использованию, 2019–2030 гг.
Таблица 33. Прогноз объема рынка карбида кальция в Великобритании (тонн) по заявкам, 2019–2030 гг. Прогноз объема рынка карбида кальция (тонн) по конечному использованию, 2019–2030 гг.
Таблица 36. Прогноз рыночной стоимости карбида кальция во Франции (млн долл. США) по конечному использованию, 2019–2030 гг.
: Прогноз рыночной стоимости карбида кальция во Франции (млн долл. США) по заявкам, 2019–2030 гг.
Прогноз рыночной стоимости (млн долл. США) по конечному использованию, 2019–2030 гг.
Таблица 41. Прогноз объема рынка карбида кальция в Италии (тонн) по заявкам, 2019–2030 гг. Прогноз объема рынка карбида кальция (тонн) по конечному использованию, 2019–2030 гг.
Таблица 44. Прогноз рыночной стоимости карбида кальция в Испании (млн долл. США) по конечному использованию, 2019–2030 гг. Прогноз объема рынка (тонн) по заявкам, 2019–2030 гг.
Таблица 46: Прогноз стоимости рынка карбида кальция в Испании (млн долл. США) в разбивке по областям применения, 2019–2030 гг.
Таблица 48. Прогноз рыночной стоимости карбида кальция в России и СНГ (млн долл. США) по конечному использованию, 2019–2030 гг.
Таблица 50. Прогноз рыночной стоимости карбида кальция в России и СНГ (млн долл. США) по областям применения, 2019 г.–2030
Таблица 51. Прогноз объема рынка карбида кальция в остальной Европе (тонн) по конечному использованию, 2019–2030 гг.
Таблица 52. Прогноз рыночной стоимости карбида кальция в остальной Европе (млн долл. США) по конечному использованию , 2019–2030
Таблица 53: Прогноз объема рынка карбида кальция в остальной Европе (тонн) по применению, 2019–2030 гг.
Таблица 54: Прогноз стоимости рынка карбида кальция в остальной Европе (млн долл. США) по применению, 2019 –2030
США) по применению, 2019 –2030
Таблица 55. Прогноз объема рынка карбида кальция в Азиатско-Тихоокеанском регионе (тонны) по конечному использованию, 2019 г.–2030
Таблица 56. Прогноз рыночной стоимости карбида кальция в Азиатско-Тихоокеанском регионе (млн долл. США) по конечному использованию, 2019–2030 гг.
Таблица 58: Прогноз стоимости рынка карбида кальция в Азиатско-Тихоокеанском регионе (млн долл. США) по приложениям, 2019–2030 гг.
Таблица 60. Прогноз рыночной стоимости карбида кальция в Азиатско-Тихоокеанском регионе (млн долл. США) по странам и субрегионам, 2019 г.–2030
Таблица 61. Прогноз объема рынка карбида кальция в Китае (тонн) по конечному использованию, 2019–2030 гг.
Таблица 63. Прогноз объема рынка карбида кальция в Китае (тонн) по заявкам, 2019–2030 гг. Прогноз объема рынка карбида кальция (тонн) по конечному использованию, 2019–2030 гг.
Таблица 66. Прогноз стоимости рынка карбида кальция в Японии (млн долл. США) по конечному использованию, 2019–2030 гг.
США) по конечному использованию, 2019–2030 гг.
: Прогноз рыночной стоимости карбида кальция в Японии (млн долл. США) по заявкам, 2019–2030 гг.
Прогноз рыночной стоимости (млн долл. США) по конечному использованию, 2019–2030 гг.
Таблица 71. Прогноз объема рынка карбида кальция в Индии (тонн) по заявкам, 2019–2030 гг.
Прогноз объема рынка карбида кальция (тонн) по конечному использованию, 2019–2030 гг.
Прогноз объема рынка (тонн) по заявкам, 2019–2030 гг.
Таблица 76: Прогноз рыночной стоимости карбида кальция в странах АСЕАН (млн долл. США) по приложениям, 2019–2030 гг.
Таблица 78. Прогноз рыночной стоимости карбида кальция в остальной части Азиатско-Тихоокеанского региона (млн долл. США) по конечному использованию, 2019–2030 гг. 2030
Таблица 80. Прогноз рыночной стоимости карбида кальция в остальных странах Азиатско-Тихоокеанского региона (млн долл. США) по заявкам, 2019 г.–2030
Таблица 81: Прогноз объема рынка карбида кальция в Латинской Америке (тонн) по конечному использованию, 2019–2030 гг.
Таблица 82: Прогноз рыночной стоимости карбида кальция в Латинской Америке (млн долл. США) по конечному использованию, 2019 –2030
Таблица 83. Прогноз объема рынка карбида кальция в Латинской Америке (тонн) по заявкам, 2019–2030 гг.
Таблица 85. Прогноз объема рынка карбида кальция в Латинской Америке (тонн) по странам и субрегионам, 2019 г.–2030
Таблица 86. Прогноз рыночной стоимости карбида кальция в Латинской Америке (млн долл. США) по странам и субрегионам, 2019–2030 гг. 2019–2030
Таблица 88. Прогноз рыночной стоимости карбида кальция в Бразилии (млн долл. США) по конечному использованию, 2019–2030 гг.
Таблица 90. Прогноз рыночной стоимости карбида кальция в Бразилии (млн долл. США) по приложениям, 2019 г.–2030
Таблица 91. Прогноз объема рынка карбида кальция в Мексике (тонн) по конечному использованию, 2019–2030 гг.
Таблица 93. Прогноз объема рынка карбида кальция в Мексике (тонн) по заявкам, 2019–2030 гг. Прогноз объема рынка карбида кальция в Латинской Америке (тонн) по конечному использованию, 2019 г.–2030
Прогноз объема рынка карбида кальция в Латинской Америке (тонн) по конечному использованию, 2019 г.–2030
Таблица 96. Прогноз рыночной стоимости карбида кальция в остальной части Латинской Америки (млн долл. США) по конечному использованию, 2019–2030 гг.
, 2019–2030
Таблица 98. Прогноз рыночной стоимости карбида кальция в остальной части Латинской Америки (млн долл. США) по приложениям, 2019–2030 гг.
-использование, 2019–2030 гг.
Таблица 100. Прогноз рыночной стоимости карбида кальция на Ближнем Востоке и в Африке (млн долл. США) по конечному использованию, 2019 г.–2030
Таблица 101. Прогноз объема рынка карбида кальция на Ближнем Востоке и в Африке (тонн) по заявкам, 2019–2030 гг.
–2030
Таблица 103. Прогноз объема рынка карбида кальция на Ближнем Востоке и в Африке (тонн) по странам и субрегионам, 2019–2030 гг.
по странам и субрегионам, 2019 г.–2030
Таблица 105: Прогноз объема рынка карбида кальция GCC (тонн) по конечному использованию, 2019–2030 гг.
Таблица 106: Прогноз рыночной стоимости карбида кальция GCC (млн долл. США) по конечному использованию, 2019–2030 гг.
Таблица 107. Прогноз объема рынка карбида кальция в странах Персидского залива (тонн) по заявкам, 2019–2030 гг.
Прогноз объема рынка карбида кальция в Африке (тонн) по конечному использованию, 2019 г.–2030
Таблица 110. Прогноз рыночной стоимости карбида кальция в Южной Африке (млн долл. США) по конечному использованию, 2019–2030 гг.
Таблица 112. Прогноз рыночной стоимости карбида кальция в Южной Африке (млн долл. США) по потреблению, 2019–2030 гг.
Таблица 113. –2030
Таблица 114. Прогноз рыночной стоимости карбида кальция в остальной части Ближнего Востока и Африки (млн долл. США) по конечному использованию, 2019 г.–2030
Таблица 115: Прогноз объема рынка карбида кальция в остальной части Ближнего Востока и Африки (тонн) по приложениям, 2019–2030
Таблица 116: Прогноз рыночной стоимости карбида кальция в остальной части Ближнего Востока и Африки (млн долл. США), по областям применения, 2019–2030 гг.
США), по областям применения, 2019–2030 гг.
Список рисунков
Рисунок 1. Динамика мировых цен на карбид кальция по областям применения, 2019–2030 гг. 2019–2030 гг. (долл. США/т)
Рисунок 3. Объемная доля мирового рынка карбида кальция по конечному использованию, 2019, 2025 и 2030 гг.
Рисунок 4. Привлекательность мирового рынка карбида кальция по конечному использованию
Применение, 2019, 2025 и 2030 гг. Рыночная привлекательность по регионам
Рисунок 9. Объемная доля рынка карбида кальция в Северной Америке по конечному использованию, 2019, 2025 и 2030 гг.
Рисунок 10. Привлекательность рынка карбида кальция в Северной Америке по конечному использованию Доля в объемах по приложениям, 2019, 2025 и 2030 гг.0003
Рисунок 14. Привлекательность рынка карбида кальция в Северной Америке по странам
Рисунок 15. Объемная доля европейского рынка карбида кальция по конечному использованию, 2019, 2025 и 2030 годы -use
Рисунок 17. Объемная доля европейского рынка карбида кальция по приложениям, 2019, 2025 и 2030 гг.
Объемная доля европейского рынка карбида кальция по приложениям, 2019, 2025 и 2030 гг.
Рисунок 18. Привлекательность европейского рынка карбида кальция по приложениям и субрегион, 2019 г., 2025 и 2030
Рисунок 20. Привлекательность европейского рынка карбида кальция по странам и субрегионам
Рисунок 21. Объемная доля рынка карбида кальция в Азиатско-Тихоокеанском регионе по конечному использованию, 2019, 2025 и 2030 годы
Рисунок 22 : Привлекательность рынка карбида кальция в Азиатско-Тихоокеанском регионе по конечному использованию
Рисунок 23. Объемная доля рынка карбида кальция в Азиатско-Тихоокеанском регионе по применению, 2019, 2025 и 2030 годы0003
Рисунок 25. Объемная доля рынка карбида кальция в Азиатско-Тихоокеанском регионе по странам и субрегионам, 2019, 2025 и 2030 гг. Доля рынка карбида кальция в Америке по конечному использованию, 2019, 2025 и 2030 гг.
Рисунок 28. Привлекательность рынка карбида кальция в Латинской Америке по конечному использованию 2019, 2025 и 2030
Рисунок 30. Привлекательность рынка карбида кальция в Латинской Америке по приложениям
Привлекательность рынка карбида кальция в Латинской Америке по приложениям
Рисунок 31. Объемная доля рынка карбида кальция в Латинской Америке по странам и субрегионам, 2019, 2025 и 2030 годы
Рисунок 32: Привлекательность рынка карбида кальция в Латинской Америке по странам и субрегионам
Рисунок 33. Объемная доля рынка карбида кальция на Ближнем Востоке и в Африке по конечному использованию, 2019, 2025 и 2030 годы
Рисунок 34. Карбид кальция на Ближнем Востоке и в Африке Рыночная привлекательность по конечному использованию
Рисунок 35. Объемная доля рынка карбида кальция на Ближнем Востоке и в Африке по приложениям, 2019, 2025 и 2030 гг.
Рисунок 36. Привлекательность рынка карбида кальция на Ближнем Востоке и в Африке по приложениям Объемная доля рынка карбида по странам и субрегионам, 2019, 2025 и 2030 гг.
Рисунок 38. Привлекательность рынка карбида кальция на Ближнем Востоке и в Африке по странам и субрегионам по компаниям, 2019 г.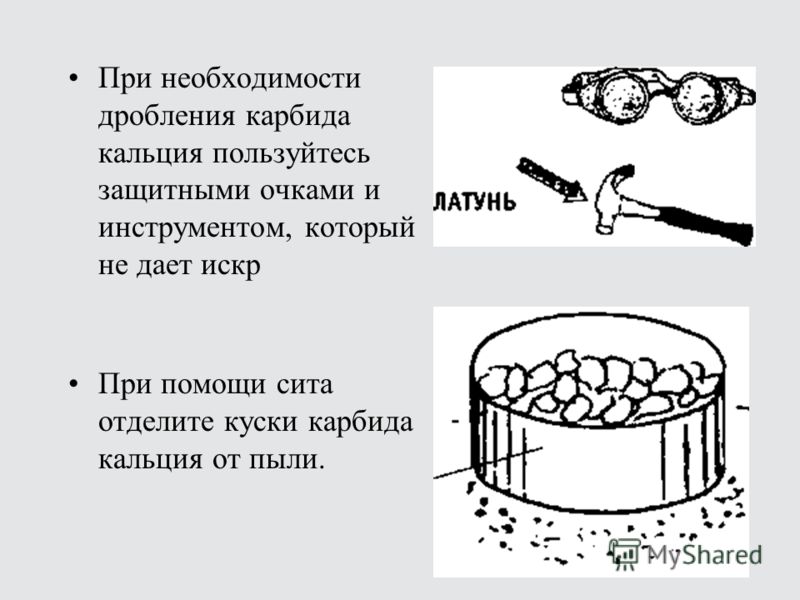
- Мы предлагаем 100% бесплатную настройку с нашей корпоративной лицензией!
- Получите бесплатную копию, если приобретенный вами отчет будет обновлен в течение 90 дней
- Независимо от того, где вы приобрели отчет, вы можете запросить у нас обновленную версию отчета.
Заполните форму ниже, и мы свяжемся с вами в ближайшее время.
Тенденции роста рынка карбида кальция, прогнозы на 2030 год
2021
Рынок карбида кальция
Pпо применению (ацетиленовый газ, цианамид кальция, восстановители и дегидратирующие агенты, деоксиданты и деоксиданты) промышленность (химическая, металлургическая, фармацевтическая, пищевая и др.): глобальный анализ возможностей и отраслевой прогноз, 2021–2030
COVID-19
Пандемия потрясла весь мир и затронула многие отрасли.
Получите подробный анализ воздействия COVID-19 на рынок карбида кальция
Запросите прямо сейчас!
Мировой рынок ненасыщенных полиэфирных смол на основе карбида кальция в 2020 г. оценивался в 11,3 млрд долл. США, а к 2030 г. ожидается, что он достигнет 18,2 млрд долл. США, увеличившись в среднем на 5,0% в период с 2021 по 2030 гг. привело к снижению спроса на карбид кальция со стороны химической, металлургической и пищевой промышленности на фоне введенных правительством мер по блокировке и нарушения цепочки поставок.
Карбид кальция представляет собой комочки серовато-черного цвета или кристаллический (пескообразный) порошок с чесночным запахом. Другое название карбида кальция – ацетилид кальция. Кроме того, его химическая формула CaC 2 . Это соединение, используемое в промышленности для производства. Он используется для производства газообразного ацетилена, в качестве восстановителя, а также в производстве стали и резке металлов. Это вредно для потребления человеком.
Это вредно для потребления человеком.
Карбид кальция производится в промышленных масштабах с использованием оксида кальция и кокса. Он используется в химической промышленности для различных применений, включая производство газообразного ацетилена и для производства ацетилена в карбидных лампах; производство химикатов для удобрений; а также в сталелитейном производстве. Сталь используется в строительной отрасли из-за ее исключительных качеств, таких как пластичность и долговечность. Это помогает в строительстве сейсмостойких конструкций. Более широкое использование высокоскоростных поездов в таких странах, как Китай, Япония и Индия, привело к разработке специальных рельсов, которые увеличили использование углеродистой стали. В результате прогнозируется, что спрос на сырую сталь увеличится в 9 раз.0107 рынок карбида кальция рост в течение прогнозируемого периода.
Размер рынка карбида кальция сегментируется в зависимости от области применения, отрасли конечного использования и региона. В зависимости от применения рынок карбида кальция делится на ацетиленовый газ, цианамид кальция, восстановитель и осушитель, десульфурирующий и раскисляющий агент и другие. По отраслям конечного использования рынок подразделяется на химическую, металлургическую, фармацевтическую, пищевую и другие. В зависимости от региона рынок карбида кальция изучается в Северной Америке, Европе, Азиатско-Тихоокеанском регионе и LAMEA. В настоящее время наибольшая доля рынка карбида кальция приходится на Азиатско-Тихоокеанский регион, за которым следуют LAMEA и Европа.
В зависимости от применения рынок карбида кальция делится на ацетиленовый газ, цианамид кальция, восстановитель и осушитель, десульфурирующий и раскисляющий агент и другие. По отраслям конечного использования рынок подразделяется на химическую, металлургическую, фармацевтическую, пищевую и другие. В зависимости от региона рынок карбида кальция изучается в Северной Америке, Европе, Азиатско-Тихоокеанском регионе и LAMEA. В настоящее время наибольшая доля рынка карбида кальция приходится на Азиатско-Тихоокеанский регион, за которым следуют LAMEA и Европа.
Основные игроки, работающие в мировой отрасли производства карбида кальция, включают Denka Company Limited, AlzChem, American Elements, Thermo Fisher Scientific, Carbide Industries LLC, KC Group, Merck KGaA, MCB Industries Sdn. Bhd., Mil-Spec Industries Corporation и Santa Cruz Biotechnology, Inc.
Рынок карбида кальция, по заявке На сегмент газообразного ацетилена приходится наибольшая доля рынка карбида кальция в 2020 году, а на сегмент десульфурирующих и раскисляющих агентов прогнозируется, что он будет расти с максимальным среднегодовым темпом роста в 7,5%. Ацетилен производится на заводах по производству ацетилена для различных промышленных и коммерческих целей.
Ацетилен производится на заводах по производству ацетилена для различных промышленных и коммерческих целей.
Рынок карбида кальция
По типу
Ацетилен Газ прогнозируется как наиболее прибыльный сегмент.
Получите дополнительную информацию об этом отчете: Страницы с образцами запросов
Рынок карбида кальция по отраслям конечного использованияНа химический сегмент приходится наибольшая доля рынка карбида кальция в 2020 году, в то время как на металлургический сегмент, по прогнозам, будет расти при самом высоком CAGR 5,7%. Прогнозируется, что сегмент биополировки будет занимать доминирующую долю на мировом рынке карбида кальция в течение прогнозируемого периода из-за увеличения спроса на газообразный ацетилен, поскольку ацетилен также может использоваться в качестве сырья для производства ацетальдегида, уксусного ангидрита и уксусная кислота.
Рынок карбида кальция
По отраслям конечного использования
Химическая промышленность считается наиболее прибыльным сегментом.

Получите дополнительную информацию об этом отчете: Запросить образцы страниц
Рынок карбида кальция по регионамНа Азиатско-Тихоокеанский регион приходится наибольшая доля рынка карбида кальция в 2020 году. Китай является ведущим производителем и потребителем в мире. из карбида кальция.
Рынок карбида кальция
По регионам
2030
Азиатско-Тихоокеанский регион
Северная Америка
Европа
Lamea
Азиатско-Тихоокеанский регион считается наиболее прибыльным рынком.
Получите дополнительную информацию об этом отчете: Запросите образцы страниц
Ключевые преимущества для заинтересованных сторон
- Анализ мирового рынка карбида кальция содержит подробную информацию об основных участниках отрасли.
- Анализ пяти сил Портера помогает проанализировать потенциал покупателей и поставщиков и конкурентный сценарий отрасли для построения стратегии.

- Основные страны нанесены на карту в соответствии с их индивидуальным вкладом в доход на региональном рынке.
- В отчете представлен углубленный анализ прогноза мирового рынка карбида кальция на период 2021–2030 гг.
- В отчете описываются текущие тенденции мирового рынка карбида кальция и будущий сценарий мирового рынка карбида кальция с 2020 по 2030 год, чтобы понять преобладающие возможности и потенциальные инвестиционные карманы.
- Основные движущие силы, ограничения и возможности, а также подробный анализ их воздействия объясняются в исследовании мирового рынка карбида кальция.
Влияние Covid-19 на мировой рынок карбида кальция
- COVID-19 распространился почти на 213 стран мира, и 11 марта 2020 года Всемирная организация здравоохранения объявила его чрезвычайной ситуацией в области общественного здравоохранения.
- Некоторые из крупнейших экономик, пострадавших от кризиса COVID-19, включают Германию, Францию, Италию, Испанию, Великобританию и Норвегию.

- Карбид кальция в основном используется в химической, промышленной и пищевой промышленности. Ожидается, что к 2021 году онлайн-продажи бакалейных товаров составят 12,4% всех продаж электронной коммерции в США9.0042
- Карбид кальция в основном используется в производстве ацетилена и других химических соединений в промышленности. Карбид кальция в основном используется в химической и металлургической промышленности. Вспышка COVID-19 затронула многие отрасли обрабатывающей промышленности и общую экономическую деятельность.
- На химическую промышленность повлияло введение ограничений во многих странах и нехватка поставок. В то же время спад экономической активности препятствует развитию инфраструктуры, внедрению новых производств и расширению, что негативно сказывается на спросе на металлопродукцию, влияя на металлургическую промышленность.
- Во многих странах экономика упала из-за остановки нескольких отраслей, особенно транспорта и цепочки поставок. Спрос на продукт был затруднен из-за отсутствия развития из-за блокировки.

- Эпидемия COVID-19 негативно повлияла на обрабатывающую и промышленную отрасли из-за нехватки ресурсов в различных частях мира. Ведущие игроки отрасли обеспокоены перспективами рынка и переосмысливают свои стратегии, чтобы справиться с этой задачей.
Calcium Carbide Market Report Highlights
| Aspects | Details |
|---|---|
| BY APPLICATION |
|
| ПО ОТРАСЛЯМ КОНЕЧНОГО ПРИМЕНЕНИЯ |
|
| BY REGION |
|
| Ключевые участники рынка | ALZCHEM, AMERICAN ELEMENTS, KC GROUP, MCB INDUSTRIES SDN. BHD., MIL-SPEC INDUSTRIES CORPORATION, DENKA COMPANY LIMITED, CARBIDE INDUSTRIES, Praxair S.T. Technology, Inc., Merck KGaA, Thermo Fisher Scientific, Santa Cruz Biotechnology, Inc. BHD., MIL-SPEC INDUSTRIES CORPORATION, DENKA COMPANY LIMITED, CARBIDE INDUSTRIES, Praxair S.T. Technology, Inc., Merck KGaA, Thermo Fisher Scientific, Santa Cruz Biotechnology, Inc. |
Загрузка оглавления…
По мнению аналитика, рынок карбида кальция определяется увеличение использования расшлихтовки и биополировки тканей в связи с изменением образа жизни. Кроме того, рынок карбида кальция может выиграть от роста мирового текстильного производства. Значительный потенциал сектора джинсовой одежды, а также инновации в текстильном производстве открывают новые перспективы роста для участников рынка карбидов кальция. Однако из-за правил производства ферментов рынок карбида кальция может затормозиться.
В отчете объясняются факторы роста, ограничения и возможности, чтобы лучше понять динамику рынка. В этом отчете дополнительно освещаются ключевые области инвестиций. Кроме того, он включает анализ пяти сил Портера, чтобы понять сценарий конкуренции в отрасли и роль каждой заинтересованной стороны. В отчете представлены стратегии, принятые ключевыми игроками рынка для сохранения своих позиций на рынке. Кроме того, он подчеркивает конкурентную среду ключевых игроков, чтобы увеличить их долю на рынке и поддерживать острую конкуренцию в отрасли.
В отчете представлены стратегии, принятые ключевыми игроками рынка для сохранения своих позиций на рынке. Кроме того, он подчеркивает конкурентную среду ключевых игроков, чтобы увеличить их долю на рынке и поддерживать острую конкуренцию в отрасли.
Карбид кальция | 75-20-7
Описание
Карбид кальция (молекулярная формула: CaC2) представляет собой важное химическое сырье, получаемое в результате химической обработки известняка. В 1892 г. Х. Майсан (Франция) и Х. Уилсон (США) одновременно разработали подход к производству карбида кальция, основанный на печном восстановлении. Соединенные Штаты успешно достигли промышленного производства в 1895 году. Свойство карбида кальция связано с его чистотой. Его промышленный продукт в основном представляет собой смесь карбида кальция и оксида кальция, а также содержит следовые количества серы, фосфора, азота и других примесей. С увеличением содержания примесей цвет становится серым, коричневым до черного. Температура плавления и электропроводность снижаются с уменьшением чистоты. Чистота его промышленного продукта обычно составляет 80% с т.пл. 1800~2000 °С. При комнатной температуре он не реагирует с воздухом, но может вступать в реакцию окисления при температуре выше 350 ℃ и реагировать с азотом при 600–700 ℃ с образованием цианамида кальция. Карбид кальция при контакте с водой или паром образует ацетилен и выделяет большое количество тепла. CaC2 + 2h3O─ → C2h3 + Ca(OH) 2 + 125185,32 Дж, из 1 кг чистого карбида кальция можно получить 366 л ацетилена 366л (15 ℃, 0,1 МПа). Таким образом, для его хранения: карбид кальция следует хранить вдали от воды. Обычно его упаковывают в герметичный железный контейнер, а иногда хранят в сухом складе, при необходимости заполняя азотом.
Температура плавления и электропроводность снижаются с уменьшением чистоты. Чистота его промышленного продукта обычно составляет 80% с т.пл. 1800~2000 °С. При комнатной температуре он не реагирует с воздухом, но может вступать в реакцию окисления при температуре выше 350 ℃ и реагировать с азотом при 600–700 ℃ с образованием цианамида кальция. Карбид кальция при контакте с водой или паром образует ацетилен и выделяет большое количество тепла. CaC2 + 2h3O─ → C2h3 + Ca(OH) 2 + 125185,32 Дж, из 1 кг чистого карбида кальция можно получить 366 л ацетилена 366л (15 ℃, 0,1 МПа). Таким образом, для его хранения: карбид кальция следует хранить вдали от воды. Обычно его упаковывают в герметичный железный контейнер, а иногда хранят в сухом складе, при необходимости заполняя азотом.
Использование
Промышленность
Применение
Преимущества
Химическое производство
Производство ацетиленового газа
Сырье, CAC 2 + 2 H 4148. Ca(OH) 2
Ca(OH) 2
Производство цианамида кальция
Сырье, CaC 2 + N 2 → CACN 2 + C
Производство различных производных ацетилена
Источник ацетиленового газа
Гидроксида кальция
Сырье, CAC 2 + 2 H 2 , CAC 2 + 2 H 2 . 2 + Ca(OH) 2
Производство стали
Десульфурация чугуна (чугун, чугун и сталь)
Десульфуризатор
В качестве топлива в сталеплавильном производстве
Увеличение коэффициента брака для жидкого чугуна
Очистка ковша
Мощный дексидизатор
Mining, автомобили и уличное освещение
карбид -лампы
реагируют с водой для создания ацетиленового газа, который может сжигать, чтобы светиться
Fruit
Artificifial Fruit Fruit
Fruit Fruit
888888 гг. газ
Сигнальные ракеты
Плавающие самовозгорающиеся морские сигнальные ракеты
Используются вместе с фосфидом кальция
Баллонный газ
Производство металлов и строительство
Источник газообразного ацетилена
Обучающий эксперимент
Реагент для обучения
Реактив для эксперимента
Реакция с водой
Карбид кальция немедленно вступает в реакцию при контакте с водой с образованием ацетилена и гидроксида кальция, что является подходом к промышленному получению ацетилена (метод карбида), уравнение реакции:
CaC2 + 2h3O = C2h3 + Ca(OH) 2
Из-за примеси карбида кальция образующийся газообразный ацетилен обычно смешивается с небольшим количеством сероводорода, газообразного фосфина и других загрязняющих веществ, поэтому возникает неприятный запах. Карбид кальция получают из извести и кокса в электропечи при высокой температуре 3000 ℃:
Карбид кальция получают из извести и кокса в электропечи при высокой температуре 3000 ℃:
3C + CaO = CaC2 + CO. , мы можем применить насыщенный рассол для замены воды, чтобы можно было получить чистый и равномерный воздушный поток ацетилена. Карбид кальция не вступает в реакцию с хлоридом натрия.
Метод производства
Метод восстановления в электропечи является единственным методом промышленного производства карбида кальция в настоящее время. Помещаем оксид кальция и кокс на реакцию восстановления при 2000~2200 ℃: CaO + 3C─ → CaC2 + CO-480644.64J, полученный расплав карбида кальция поступает в приемную емкость со дна реактора, а конечный продукт получаем после охлаждение. Производство карбида кальция относится к высокотемпературным операциям с образованием относительно большого количества пыли и потреблением большого количества электроэнергии. В 1980-х годов производство тонны карбида кальция потребляет промышленную мощность около 10 ~ 11 ГДж. Чтобы снизить энергопотребление, люди в основном применяют крупномасштабные и закрытые печи из карбида кальция, чтобы уменьшить потери тепла, а также улучшить рециркуляцию окиси углерода.
Чтобы снизить энергопотребление, люди в основном применяют крупномасштабные и закрытые печи из карбида кальция, чтобы уменьшить потери тепла, а также улучшить рециркуляцию окиси углерода.
Описание
Карбид кальция представляет собой бинарную соль. Это серовато-черное твердое вещество, которое реагирует с водой с образованием газообразного ацетилена, твердого коррозионного вещества, представляющего собой гидроксид кальция, и выделяет тепло. Газообразный ацетилен получают путем взаимодействия карбида кальция с водой. Поскольку ацетилен очень нестабилен, его не отгружают в больших количествах.
Карбид кальция отгружается на ацетиленовые установки, где вступает в реакцию с водой в контролируемой реакции. После процесса реакции газообразный ацетилен помещается в специально разработанные контейнеры с сотовой сеткой внутри для транспортировки и использования. Для стабильности растворяют в ацетоне. Карбид кальция имеет удельный вес 2,22, что тяжелее воды. Четырехзначный идентификационный номер ООН для карбида кальция – 1402. Обозначение NFPA 704 – здоровье 3, воспламеняемость 3 и реакционная способность 2. Белая часть в нижней части ромба содержит букву W с косой чертой, что указывает на реакционную способность воды. Его отгружают в металлических канистрах, бочках и специально сконструированных крытых контейнерах на железнодорожных и грузовых автомобилях. При транспортировке и хранении его следует хранить в прохладном, сухом месте. Основное использование – производство газообразного ацетилена для сварки, мономера винилацетата и в качестве восстановителя.
Четырехзначный идентификационный номер ООН для карбида кальция – 1402. Обозначение NFPA 704 – здоровье 3, воспламеняемость 3 и реакционная способность 2. Белая часть в нижней части ромба содержит букву W с косой чертой, что указывает на реакционную способность воды. Его отгружают в металлических канистрах, бочках и специально сконструированных крытых контейнерах на железнодорожных и грузовых автомобилях. При транспортировке и хранении его следует хранить в прохладном, сухом месте. Основное использование – производство газообразного ацетилена для сварки, мономера винилацетата и в качестве восстановителя.
Химические свойства
твердое вещество серого или черного цвета с чесночным запахом
Физические свойства
Серовато-черный орторомбический кристалл; плотность 2,22 г/см 3 ; плавится при 2200°С; реагирует с водой.
Использование
Карбид кальция используется как десульфуризатор, осушитель стали, топливо в сталеплавильном производстве, мощный раскислитель и как источник газообразного ацетилена. Он используется в качестве исходного материала для получения цианамида кальция, этилена, хлоропренового каучука, уксусной кислоты, дициандиамида и ацетата цианида. Он используется в карбидных лампах, игрушечных пушках, таких как пушка большого взрыва и бамбуковая пушка. Он связан с фосфидом кальция и используется в плавучих самовоспламеняющихся морских сигнальных ракетах. Кроме того, он участвует в восстановлении сульфида меди до металлической меди.
Он используется в качестве исходного материала для получения цианамида кальция, этилена, хлоропренового каучука, уксусной кислоты, дициандиамида и ацетата цианида. Он используется в карбидных лампах, игрушечных пушках, таких как пушка большого взрыва и бамбуковая пушка. Он связан с фосфидом кальция и используется в плавучих самовоспламеняющихся морских сигнальных ракетах. Кроме того, он участвует в восстановлении сульфида меди до металлической меди.
Использование
Карбид кальция (CaC2) имеет чесночный запах и реагирует с водой с образованием газообразного ацетилена. плюс гидроксид кальция и тепло. В прошлом он использовался в шахтерских лампах для непрерывного производят небольшое ацетиленовое пламя, чтобы обеспечить некоторое освещение в угольных шахтах.
Использование
Карбид кальция является наиболее подходящим карбидом в промышленности из-за его важной роли в качестве основы ацетиленовой промышленности. В местах с нехваткой нефти карбид кальция используется в качестве исходного материала для производства ацетилена (из 1 кг карбида получается ~300 литров ацетилена), который, в свою очередь, может использоваться в качестве строительного блока для ряда органические химикаты (например, винилацетат, ацетальдегид и уксусная кислота). В некоторых местах ацетилен также используется для производства винилхлорида, сырья для производства ПВХ.
В местах с нехваткой нефти карбид кальция используется в качестве исходного материала для производства ацетилена (из 1 кг карбида получается ~300 литров ацетилена), который, в свою очередь, может использоваться в качестве строительного блока для ряда органические химикаты (например, винилацетат, ацетальдегид и уксусная кислота). В некоторых местах ацетилен также используется для производства винилхлорида, сырья для производства ПВХ.
Менее важное применение карбида кальция связано с производством удобрений. Он реагирует с азотом с образованием цианамида кальция, который является исходным материалом для производства цианамида (Ch3N2). Цианамид — распространенный сельскохозяйственный продукт, используемый для стимуляции раннего листообразования.
Карбид кальция также можно использовать в качестве десульфурирующего агента для производства углеродистой стали с низким содержанием серы. Кроме того, он используется в качестве восстановителя для получения металлов из их солей, например, для прямого восстановления сульфида меди до металлической меди.
Подготовка
Карбид кальция (CaC2) получают путем нагревания смеси извести и углерода до 2000–2100°C (3632–3812°F) в электродуговой печи. При этих температурах известь восстанавливается углеродом до карбида кальция и монооксида углерода (CO) в соответствии со следующей реакцией: CaO + 3C → CaC2 + CO
Известь для реакции обычно производится путем прокаливания известняка в печи на заводе. Источниками углерода для реакции являются нефтяной кокс, металлургический кокс и антрацитовый уголь. Поскольку примеси в шихте остаются в продукте из карбида кальция, известь должна содержать не более 0,5% оксида магния, оксида алюминия и оксида железа и 0,004% фосфора. Кроме того, коксовая шихта должна быть с низким содержанием золы и серы. Анализы показывают, что для нефтяного кокса типичны от 0,2 до 1,0 процента золы и от 5 до 6 процентов серы. Около 9Для производства 1 мегаграмма (Мг) ) из карбида кальция.
Реакции
Карбид кальция представляет собой серовато-черное твердое вещество, реагирует с водой с образованием газообразного ацетилена и гидроксида кальция, образующегося при температуре электропечи из оксида кальция и углерода.
Общее описание
Серовато-черный твердый комок неправильной формы. Используется для производства ацетилена и в производстве стали.
Реакции воздуха и воды
Быстро реагирует с водой с образованием легковоспламеняющегося газа ацетилена и основного гидроксида кальция. Может выделяться достаточно тепла для воспламенения газа [Jones, G.W. БМ Отчет Инвест. 3755 1944].
Профиль реактивности
Карбид кальция является восстановителем. Может бурно реагировать с окислителями. Порошкообразная смесь ацетилида и оксида железа и хлорида железа сильно горит при воспламенении, образуя расплавленное железо. Карбид кальция накаливается с хлором, бромом или йодом при 245, 350 или 305°С соответственно [Mellor, 1946, Vol. 5, 862]. Карбид горит добела при смешивании и нагревании с дифторидом свинца, магнием, хлористым водородом и хлоридом олова (II) [Mellor, 19]. 46, 1940, 1946 и 1941] соответственно. Взаимодействие карбида кальция с метанолом с образованием метоксида кальция протекает энергично, но с индукционным периодом различной продолжительности. Как только начинается реакция, выделение газообразного ацетилена происходит очень быстро, неопубликованные наблюдения [Bretherick 1995]. При смешивании карбида кальция с растворами нитрата серебра образуется ацетилид серебра, высокочувствительное взрывчатое вещество. Аналогично будут вести себя растворы солей меди [Photogr. науч. Eng., 1966, 10, 334]. Смесь карбида кальция и пероксида натрия взрывоопасна, как и карбид кальция и перхлорилфторид в виде газов при 100-300°С.
46, 1940, 1946 и 1941] соответственно. Взаимодействие карбида кальция с метанолом с образованием метоксида кальция протекает энергично, но с индукционным периодом различной продолжительности. Как только начинается реакция, выделение газообразного ацетилена происходит очень быстро, неопубликованные наблюдения [Bretherick 1995]. При смешивании карбида кальция с растворами нитрата серебра образуется ацетилид серебра, высокочувствительное взрывчатое вещество. Аналогично будут вести себя растворы солей меди [Photogr. науч. Eng., 1966, 10, 334]. Смесь карбида кальция и пероксида натрия взрывоопасна, как и карбид кальция и перхлорилфторид в виде газов при 100-300°С.
Опасность
Образует легковоспламеняющийся и взрывоопасный газ и коррозионное твердое вещество с влагой.
Опасность для здоровья
Это едкое твердое вещество. Поскольку он сильно реагирует с водой, контакт с кожей может вызвать ожог.
Опасность пожара
Поведение в огне: При намокании водой образуется легковоспламеняющийся газ ацетилен.
Профиль безопасности
Реакция на контакт с влагой образует взрывоопасный газ ацетилен. Воспламеняется при контакте с влагой, кислотой или кислотные пары; выделяет тепло или воспламеняется пары. Умеренная взрывоопасность. Реакция накаливания с Cl2 (245℃), Brz (350 ℃), IS (305 ℃), газ HCl + тепло, PbF2, Мг + тепло. Несовместим с Se, (KOH + гл), AgNO3, Na2O2, SnCl2, S, вода. Смеси с хлоридом железа(IⅡ), железом(IⅡ) оксид, хлорид олова (Ⅱ) легко воспламеняются и яростно гореть. Бурная реакция с метанол после индукционного периода. Добавление к растворам нитрата серебра осаждает опасно взрывоопасное серебро ацетилид. Растворы солей меди ведут себя по аналогии. См. также КАЛЬЦИЙ ГИДРОКСИД и АЦЕТИЛЕН.
Анализ рынка карбида кальция (2022–27)
Анализ рынка карбида кальция (2022–27) | Доля отраслиОбзор рынка
| Период обучения: | 2017-2027 гг. |
| Базисный год: | 2021 |
| Самый быстрорастущий рынок: | Азиатско-Тихоокеанский регион |
| Самый большой рынок: | Азиатско-Тихоокеанский регион |
| CAGR: | >4,5 % |
Нужен отчет, отражающий влияние COVID-19 на этот рынок и его рост?
Обзор рынка
Рынок карбида кальция в 2021 году составил более 27 миллионов тонн, и прогнозируется, что в течение прогнозируемого периода (2022-2027 годы) среднегодовой темп роста составит более 4,5%.
Карбид кальция в основном используется в промышленности и для производства ацетилена и других химических продуктов. Химическая и металлургическая промышленность преобладают в потреблении карбида кальция. COVID-19вспышка затронула многие отрасли обрабатывающей промышленности и общую экономическую деятельность. Введение карантина в разных странах и перебои с поставками также повлияли на химическую промышленность. В то же время спад экономической активности сказался на развитии инфраструктуры, создании новых производств и расширении, что серьезно повлияло на спрос на металлопродукцию и металлургическую промышленность.
В то же время спад экономической активности сказался на развитии инфраструктуры, создании новых производств и расширении, что серьезно повлияло на спрос на металлопродукцию и металлургическую промышленность.
- В краткосрочной перспективе растущий спрос со стороны химической промышленности, вероятно, будет стимулировать рыночный спрос. Химическая промышленность составляет наибольшую долю, занимая более 70% от общего объема рынка карбида кальция.
- Однако вредное воздействие карбида кальция на здоровье может препятствовать росту рынка.
- Азиатско-Тихоокеанский регион доминировал на рынке, при этом Китай был крупнейшим производителем и потребителем карбида кальция в мире. В росте рынка преобладают хорошо зарекомендовавшие себя химическая и металлургическая отрасли в Азиатско-Тихоокеанском регионе.
Объем отчета
Карбид кальция производится в промышленных масштабах с использованием оксида кальция и кокса. Он используется для различных применений в химической промышленности. Рынок карбида кальция сегментирован по применению, отрасли конечного пользователя и географии. По применению рынок подразделяется на газообразный ацетилен, цианамид кальция, восстановитель и дегидратирующий агент, десульфурирующий и раскисляющий агент и другие области применения. По отраслям конечных пользователей рынок делится на химическую, металлургическую, пищевую и другие отрасли конечных пользователей. Отчет также охватывает размер рынка и прогнозы в 15 странах по основным регионам. Для каждого сегмента размер рынка и прогноз были сделаны на основе объема (килотонны).
Рынок карбида кальция сегментирован по применению, отрасли конечного пользователя и географии. По применению рынок подразделяется на газообразный ацетилен, цианамид кальция, восстановитель и дегидратирующий агент, десульфурирующий и раскисляющий агент и другие области применения. По отраслям конечных пользователей рынок делится на химическую, металлургическую, пищевую и другие отрасли конечных пользователей. Отчет также охватывает размер рынка и прогнозы в 15 странах по основным регионам. Для каждого сегмента размер рынка и прогноз были сделаны на основе объема (килотонны).
| Application | |
| Acetylene Gas | |
| Calcium Cyanamide | |
| Reducing and Dehydrating Agent | |
| Desulfurizing and Deoxidizing Agent | |
| Other Applications (Modulizing Agent and Finishing Шлак) |
| Конечный потребитель Промышленность | |
| Химическая | |
| Metallurgy | |
| Food | |
Other End-user Industries (Pyrotechnics, Carbide Lamps, Etc. ) ) |
| Geography | |||||||
| |||||||
| |||||||
| |||||||
| |||||||
|
Объем отчета может быть
настроены в соответствии с вашими требованиями. Кликните сюда.
Кликните сюда.
Ключевые тенденции рынка
Применение ацетилена для доминирования на рынке
- Газообразный ацетилен производится путем взаимодействия карбида кальция с водой. Это горючий газ с характерным запахом. Газ становится взрывоопасным при сжижении, сжатии, нагревании или смешивании с воздухом. По этой причине при обращении с газом принимаются особые меры предосторожности.
- Одним из наиболее распространенных применений газообразного ацетилена является его использование для получения различных органических химикатов. Одним из таких химических веществ является 1,4-бутандиол, который широко используется для синтеза полиуретановых и полиэфирных пластиков.
- Нерасфасованный ацетилен также может использоваться в качестве сырья для производства ацетальдегида, уксусного ангидрита и уксусной кислоты.
- Ацетилен также используется для кислородно-ацетиленовой резки, сварки и термообработки. Пламя ацетиленового газа имеет самую высокую температуру пламени среди многих обычных углеводородов из-за структуры тройной связи.
 При горении кислородом температура пламени достигает 3090°C с выделением 54,8 кДж/литр (1470 БТЕ/фут3) энергии. Газообразный ацетилен
При горении кислородом температура пламени достигает 3090°C с выделением 54,8 кДж/литр (1470 БТЕ/фут3) энергии. Газообразный ацетилен - также используется для огневой очистки поверхностей листового металла. Этот процесс удаляет ржавчину, прокатную окалину и другие отложения путем недорогой очистки пламенем, что повышает коррозионную стойкость поверхностей. Таким образом, очищенные пламенем поверхности обеспечивают отличную адгезию красок и покрытий.
- В связи с увеличением спроса на газообразный ацетилен прогнозируется увеличение потребления карбида кальция в течение прогнозируемого периода.
Чтобы понять основные тенденции, загрузите образец Отчет
Китай будет доминировать на рынке в Азиатско-Тихоокеанском регионе и во всем мире
- Китай является крупнейшим в мире производителем и потребителем карбида кальция. Страна является самым доминирующим игроком на рынке с долей более 85%.

- В стране насчитывается более 120 производителей карбида кальция с годовой производственной мощностью около 40 миллионов тонн в 2020 году. Согласно торговой карте ITC, страна является крупнейшим экспортером карбида кальция с объемом экспорта 122 тысячи тонн в 2020 году.
- Из-за больших запасов и растущего спроса на VCM (мономер винилхлорида), VAM (мономер винилацетата) и BDO (бутандиол) из ацетилена потребление карбида кальция увеличивается в среднем более чем на 8% в год.
- В последнее время в стране используется карбид кальция для преобразования угля в ацетилен, что привело к увеличению производства акрилонитрила (ACN), мономера винилхлорида (VCM), 1,4-бутандиола (BDO) и акриловой кислоты (АК).
- Преобразование CaC2 в поливинилхлорид (ПВХ) составляет более 80% от общего объема производства ПВХ в Китае. Таким образом, ожидается, что использование карбида кальция будет играть важную роль в производстве химических веществ на основе ацетилена в течение прогнозируемого периода.

- Китай является одним из крупнейших производителей стали в мире. В 2021 году годовой объем производства сырой стали в стране составлял 1032,8 метрических тонны, что составляет более 50% мирового производства. Растущее производство стали в стране косвенно стимулирует рынок карбида кальция.
- Экономический рост в стране, вероятно, будет умеренным, а спрос на карбид кальция, по оценкам, будет расти здоровыми темпами в течение прогнозируемого периода.
Чтобы понять тенденции географии, загрузите образец Отчет
Конкурентная среда
Рынок карбида кальция фрагментирован, и между ведущими игроками ведется острая конкуренция за увеличение своей доли рынка. На семь ведущих игроков приходится около 25% доли мирового рынка. На Китай приходится более 85% всего производства и потребления на рынке. Основными игроками на рынке (не в каком-либо определенном порядке) являются Xinjiang Zhongtai Chemical Co. Ltd, Xinjiang Tianye (Group) Co. Ltd, Ningxia Jinhaoyuan Chemical Group Co. Ltd, Внутренняя Монголия Baiyanhu Chemical Limited Liability Company и Denka Company Limited. .
Ltd, Xinjiang Tianye (Group) Co. Ltd, Ningxia Jinhaoyuan Chemical Group Co. Ltd, Внутренняя Монголия Baiyanhu Chemical Limited Liability Company и Denka Company Limited. .
Основные игроки
- Синьцзян Zhongtai Chemical Co. Ltd
- Синьцзян Тянье (Группа) Ко. Лтд
- Нинся Цзиньхаоюань Химическая Группа Лтд
- Внутренняя Монголия Baiyanhu Chemical Co. Ltd
- Компания Денка с ограниченной ответственностью
СОДЕРЖАНИЕ
1. ВВЕДЕНИЕ
1.1. Допущения исследования
1,2 Области исследования
2. Методология исследования
3. Резюме
4. Рыночная динамика
4.1 Драйверы
4.1.1. из химической промышленности
4.2 Ограничения
4.2.1 Вредное влияние карбида кальция на здоровье
4.2.2 Другие ограничения
2
4.
 3 Анализ цепочки создания стоимости в отрасли
3 Анализ цепочки создания стоимости в отрасли4.4 Анализ Портера
4.4.1 Торговая мощность поставщиков
4.4.2. Новые участники
4.4.4 Угроза замены продуктов и услуг
4.4.5 Степень конкуренции
4.5 Торговый анализ
5. Сегментация рынка
5,1 Применение
5,1,1 Ацетилен -газ
5.1.2 Calcium Cyanamide
5.1.2 Calcium Cyanamide
5.1.2. 4 Десульфурирующий и раскисляющий агент
5.1.5 Прочие области применения (модулирующий агент и чистовой шлак)
5.2 Конечный потребитель Промышленность
5.2.1 Chemical
5.2.2 Металлургия
5.2.3 Food
5.2.4 Другие отрасли конечных пользователей (пиротехника, карбид-лампы и т. Д.).
5.
 3.1 Asia-Pacific
3.1 Asia-Pacific5.3.1.1 China
5.3.1.2 India
5.3.1.3 Japan
5.3.1.4 South Korea
5.3.1.5 Остальная часть Азиатско-Тихоокеанского региона
5.3.2 North America
5.3.2.1 United States
5.3.2.2 Canada
5.3.2.3 Mexico
5.3.3 Europe
5.3.3.1 Германия
5.3.3.2 Соединенное Королевство
5.3.3.3 Италия
5.3.3.4 Франция
5.3.3.5 Остальное Европу
5.3.3.5.0247
5.3.4 South America
5.3.4.1 Brazil
5.3.4.2 Argentina
5.3.4.3 Rest of South America
5.3.5 Middle-East and Africa
5.3.5.11 Саудовская Аравия
5.
 3.5.20003
3.5.200036.1 слияния и приобретения, совместные предприятия, совместные работы и соглашения
6.2 Анализ доли рынка **
6.3 Стратегии, принятые ведущими игроками
6.3. AlzChem Group AG
6.4.2 American Elements
6.4.3 Carbide Industries LLC
6.4.4 DCM Shriram
8 6.4.5 Denka Company Limited
6.4.6 Inner Mongolia Baiyanhu Chemical Co. Ltd
6.4.7 Iran Carbide
6.4.8 MCB Industrials SDN BHD 9003
9797
6.4.8 MCB Industries SDN BHD 9003
97
7
7- 47
6.4.8 MCB.
6.4.10 MIL-SPEC CORPORATION
6.4.11 NGO Chemical Group Ltd
6.4.12 Ningxia Jinhaoyuan Chemic Group Co. Ltd
988898988.148 8.148.148.148.148.148.148.148.148.148.
6.4.14. . Ltd
*List Not Exhaustive
7. MARKET OPPORTUNITIES AND FUTURE TRENDS
MARKET OPPORTUNITIES AND FUTURE TRENDS
7.1 Growing Downstream Application of Acetylene
**При наличии
Вы также можете приобрести части этого отчета. Вы хотите проверить раздел мудро прайс-лист?
Часто задаваемые вопросы
Каков период изучения этого рынка?
Рынок карбида кальция изучается с 2017 по 2027 год.
Каковы темпы роста рынка Карбид кальция?
Рынок карбида кальция будет расти со среднегодовым темпом роста более 4,5% в течение следующих 5 лет.
Какой регион имеет самые высокие темпы роста на рынке Карбид кальция?
Азиатско-Тихоокеанский регион демонстрирует самый высокий среднегодовой темп роста в 2021–2026 годах.
Какой регион имеет наибольшую долю рынка Карбид кальция?
Азиатско-Тихоокеанский регион будет иметь наибольшую долю в 2021 году.
Кто является ключевыми игроками на рынке Карбид кальция?
Xinjiang Zhongtai Chemical Co.

