Физические свойства кристаллической решетки: Кристаллические решетки. Строение вещества | CHEMEGE.RU
alexxlab | 30.05.1986 | 0 | Разное
Кристаллическая решетка — что это? Типы и свойства
Что такое кристаллическая решетка
Как известно, все вещества состоят из частиц — атомов, которые могут располагаться хаотично или в определенном порядке. У аморфных веществ частицы расположены беспорядочно, а у кристаллических они образуют определенную структуру. Эта структура называется кристаллической решеткой. Она определяет такие характеристики вещества, как твердость, хрупкость, температура кипения и/или плавления, пластичность, растворимость, электропроводность и т. д.
Кристаллическая решетка — это внутренняя структура кристалла, порядок взаимного расположения атомов, ионов или молекул. Точки, в которых находятся эти частицы, называются узлами решетки.
Частицы удерживаются на своих местах благодаря химическим связям между ними. В зависимости от того, какой вид связи удерживает атомы или ионы данного вещества, в химии выделяют основные типы кристаллических решеток:
атомная (ковалентные связи),
молекулярная (ковалентные связи и притяжение между молекулами),
металлическая (металлические связи),
ионная (ионные связи).

Важно!
Не путайте эти два понятия — кристаллическая решетка и химическая связь. Тип решетки говорит о том, как расположены атомы/ионы в молекуле вещества, а тип связи — по какому принципу они между собой взаимодействуют.
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Атомная кристаллическая решетка
Согласно своему названию, атомная кристаллическая решетка — это структура, в узлах которой расположены атомы. Они взаимодействуют с помощью ковалентных связей, то есть один атом отдает другому свободный электрон или же электроны из разных атомов образуют общую пару. В кристаллах с атомной решеткой частицы прочно связаны, что обуславливает ряд физических характеристик.
Свойства веществ с атомной решеткой:
К примеру, атомную кристаллическую решетку имеет алмаз — самый твердый минерал в мире.
Другие примеры: германий Ge, кремний Si, нитрид бора BN, карборунд SiC.
Лайфхак
Если нужно рассказать о свойствах веществ с атомной кристаллической решеткой, достаточно вспомнить песок и перечислить его характеристики.
Молекулярная кристаллическая решетка
Как и в предыдущей группе, в этой находятся вещества с ковалентными связями между атомами. Но физические характеристики этих веществ совершенно иные — они легко плавятся, превращаются в жидкость, растворяются в воде. Почему так происходит? Все дело в том, что здесь кристаллы строятся не из атомов, а из молекул.
Молекулярная кристаллическая решетка — это структура, в узлах которой находятся не атомы, а молекулы.
Внутри молекул атомы имеют прочные ковалентные связи, но сами молекулы связаны между собой слабо. Поэтому кристаллы таких веществ непрочные и легко распадаются.
Молекулярная кристаллическая решетка характерна для воды. При комнатной температуре это жидкость, но стоит нагреть ее до температуры кипения (которая сравнительно низка), как она тут же начинает превращаться в пар, т. е. переходит в газообразное состояние.
е. переходит в газообразное состояние.
Некоторые молекулярные вещества — например, сухой лед CO2, способны преобразоваться в газ сразу из твердого состояния, минуя жидкое (данный процесс называется возгонкой).
Свойства молекулярных веществ:
Помимо воды к веществам с молекулярной кристаллической решеткой относятся аммиак NH3, гелий He, радон Rn, йод I, азот N2 и другие. Все благородные газы — молекулярные вещества. Также к этой группе принадлежит и большинство органических соединений (например, сахар).
Учёба без слёз (бесплатный гайд для родителей)
Пошаговый гайд от Екатерины Мурашовой о том, как перестать делать уроки за ребёнка и выстроить здоровые отношения с учёбой.
Ионная кристаллическая решетка
Как известно, при ионной химической связи один атом отдает другому ионы и приобретает положительный заряд, в то время как принимающий атом заряжается отрицательно. В итоге появляются разноименно заряженные ионы, из которых и состоит структура кристалла.
В итоге появляются разноименно заряженные ионы, из которых и состоит структура кристалла.
Ионная решетка — это кристаллическая структура, в узловых точках которой находятся ионы, связанные взаимным притяжением.
Ионную кристаллическую решетку имеют практически все соли, типичным представителем можно считать поваренную соль NaCl. О ней стоит вспомнить, если нужно перечислить физические характеристики этой группы. Также ионную решетку имеют щелочи и оксиды активных металлов.
Свойства веществ с ионной структурой:
Примеры веществ с ионной кристаллической решеткой: оксид кальция CaO, оксид магния MgO, хлорид аммония NH4Cl, хлорид магния MgCl2, оксид лития Li2O и другие.
Металлическая кристаллическая решетка
Для начала вспомним, как проходит металлическая химическая связь. В молекуле металла свободные отрицательно заряженные электроны перемещаются от одного иона к другому и соединяются с некоторыми из них, а после отрываются и мигрируют дальше. В результате получается кристалл, в котором ионы превращаются в атомы и наоборот.
В результате получается кристалл, в котором ионы превращаются в атомы и наоборот.
Металлическая кристаллическая решетка — это структура, которая состоит из ионов и атомов металла, а между ними свободно передвигаются электроны. Как несложно догадаться, она характерна лишь для металлов и сплавов.
Свободные электроны, мигрирующие между узлами решетки, образуют электронное облако, которое под воздействием электротока приходит в направленное движение. Это объясняет такое свойство металлов, как электрическая проводимость.
В химии типичным примером вещества, которое имеет металлическую кристаллическую решетку, считается медь. Она очень ковкая, пластичная, имеет высокую тепло- и электропроводность. Впрочем, все металлы ярко демонстрируют эти характеристики, поэтому назвать физические свойства данной группы несложно.
Свойства веществ с металлической кристаллической решеткой:
При этом температура плавления веществ может существенно различаться. Например, у ртути это −38,9°С, а у бериллия целых +1287°С.
Например, у ртути это −38,9°С, а у бериллия целых +1287°С.
Подведем итог: о характеристиках разных типов кристаллических решеток расскажет таблица.
Зависимость физико-химических свойств кристаллических веществ от энергии
Зависимость физико-химических свойств кристаллических веществ от энергииБесплатный звонок из любой точки России 8 (800) 200 21 78
Наши продукты
Полезное
Информационные и обучающие видеоролики, вопросы и ответы, техническая документация и наша книга
- Информация
- ГОСТы
- СНиПы
- Наша книга
- Вопрос-ответ
Приведенный в данном разделе материал свидетельствует о том, что весьма широкий спектр физико-химических свойств кристаллов может быть количественно описан с позиций энергии межатомного взаимодействия в ионном приближении, а предлагаемые удельные параметры энергии ионной кристаллической решетки – есть адекватная для описания свойств кристаллов форма ее выражения.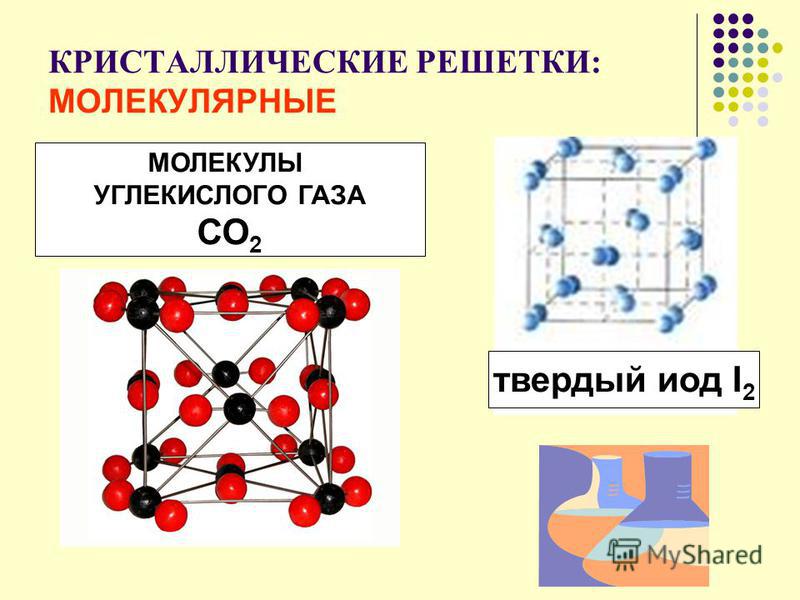 Модифицируя таким путем концепцию кристаллической ионной решетки (первый энергетический подход к описанию свойств кристаллов), можно, выражаясь образно, вдохнуть новую жизнь в геоэнергетическую теорию Ферсмана и продемонстрировать ее новые возможности в современной науке.
Многочисленные работы последних десятилетий по экспериментальному распределению электронной плотности в кристаллах (Blaha, Redinger, Schwarz, 1984; Зуев, 1990; Matsuhata, Gjonnes, Tafto, 1994 и др.) свидетельствуют в пользу реальности довольно высоких эффективных зарядов атомов в оксидах и других соединениях (например, Li
Модифицируя таким путем концепцию кристаллической ионной решетки (первый энергетический подход к описанию свойств кристаллов), можно, выражаясь образно, вдохнуть новую жизнь в геоэнергетическую теорию Ферсмана и продемонстрировать ее новые возможности в современной науке.
Многочисленные работы последних десятилетий по экспериментальному распределению электронной плотности в кристаллах (Blaha, Redinger, Schwarz, 1984; Зуев, 1990; Matsuhata, Gjonnes, Tafto, 1994 и др.) свидетельствуют в пользу реальности довольно высоких эффективных зарядов атомов в оксидах и других соединениях (например, Li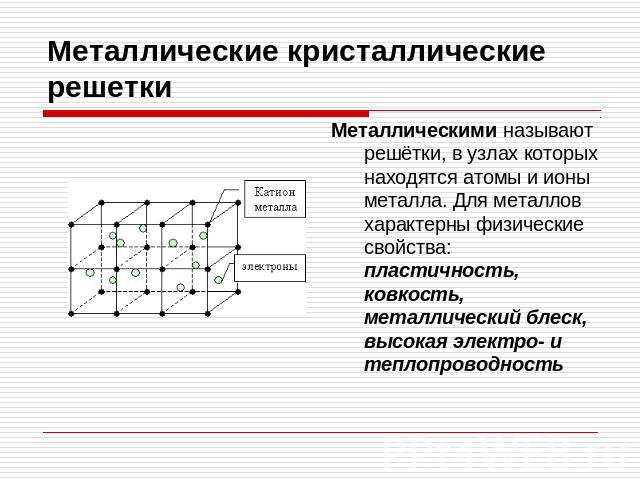
 7O3-1.8. Анализ спектров ионов Fe2+ в железосодержащем пиропе (Mg,Fe)3Al2Si3O12 также привел к выводу о весьма высокой ионности этого граната с эффективным зарядами атомов железа QFe = +1,9e и кислорода QO = -1,7e (Shen Guo-Yin, Zhao Min Guang, 1984).
В настоящее время, по-видимому, общепринятыми являются представления о том, что кристаллические галоиды щелочных и щелочноземельных металлов можно рассматривать как почти чисто ионные соединения, к которым концепция ионной кристаллической решетки безусловно применима (Урусов, 1975). В противовес общепринятому мнению есть данные в пользу весьма высоких эффективных зарядов атомов даже в таких, обычно трактуемых как ковалентные, кристаллах, как сфалерит – Zn +1.7S-1.7 (fi = 0,85)[1] (Julg, 1978; Кузнецов, 1979; Pillai, 1982).
Критики корректности концепции энергии кристаллической решетки применительно к оксидам базируются на энергетической невозможности (нереальности) свободных ионов O2-.
7O3-1.8. Анализ спектров ионов Fe2+ в железосодержащем пиропе (Mg,Fe)3Al2Si3O12 также привел к выводу о весьма высокой ионности этого граната с эффективным зарядами атомов железа QFe = +1,9e и кислорода QO = -1,7e (Shen Guo-Yin, Zhao Min Guang, 1984).
В настоящее время, по-видимому, общепринятыми являются представления о том, что кристаллические галоиды щелочных и щелочноземельных металлов можно рассматривать как почти чисто ионные соединения, к которым концепция ионной кристаллической решетки безусловно применима (Урусов, 1975). В противовес общепринятому мнению есть данные в пользу весьма высоких эффективных зарядов атомов даже в таких, обычно трактуемых как ковалентные, кристаллах, как сфалерит – Zn +1.7S-1.7 (fi = 0,85)[1] (Julg, 1978; Кузнецов, 1979; Pillai, 1982).
Критики корректности концепции энергии кристаллической решетки применительно к оксидам базируются на энергетической невозможности (нереальности) свободных ионов O2-. Однако эффект стабилизации кристаллическим полем делает их вполне реальными (Урусов, 1975).
Все эти и другие соображения являются серьезными аргументами в пользу приемлемости концепции энергии кристаллической решетки даже в случае соединений поливалентных ионов. Точнее, можно говорить о том, что базирующаяся на ионном распределении зарядов в кристаллах концепция энергии кристаллической решетки довольно часто может рассматриваться в качестве вполне удовлетворительного приближения к действительности.
Методы оценки энергии ионных кристаллических решеток изложены во многих работах и, в частности, в работах (Ферсман, 1958; Бокий, 1971; Урусов, 1975, Современная кристаллография, 1979). В настоящей работе будет использован наиболее простой метод расчета энергии решетки суммированием энергетических коэффициентов (
Однако эффект стабилизации кристаллическим полем делает их вполне реальными (Урусов, 1975).
Все эти и другие соображения являются серьезными аргументами в пользу приемлемости концепции энергии кристаллической решетки даже в случае соединений поливалентных ионов. Точнее, можно говорить о том, что базирующаяся на ионном распределении зарядов в кристаллах концепция энергии кристаллической решетки довольно часто может рассматриваться в качестве вполне удовлетворительного приближения к действительности.
Методы оценки энергии ионных кристаллических решеток изложены во многих работах и, в частности, в работах (Ферсман, 1958; Бокий, 1971; Урусов, 1975, Современная кристаллография, 1979). В настоящей работе будет использован наиболее простой метод расчета энергии решетки суммированием энергетических коэффициентов (U кДж/моль = 1071,5ΣЭК. (2.29)
Признавая весьма грубый, ориентировочный характер оценок U кристаллов в рамках данного метода, мы, тем не менее, остановились именно на нем, так как он удобен при массовых вычислениях и применим к соединениям любой сложности состава и структуры, поскольку не требует знания констант Маделунга, коэффициентов межатомного отталкивания и других параметров, используемых в более строгих современных методах (в том числе, квантово-механических) расчета энергии решетки.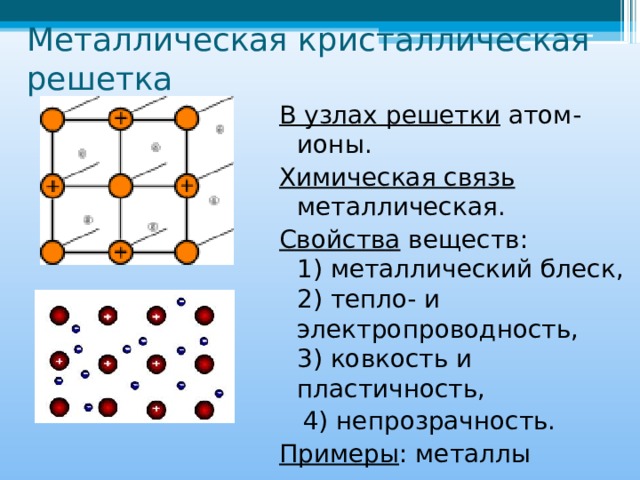
| Модификациясостава Al |
U, кДж/моль по(Ферсман, 1958) | U, кДж/моль по(Урусов и др., 1998) | Расхождение,Δ% |
| Кианит | 28126,9 | 27828,4 | +1,07 |
| Андалузит | 28126,9 | 27917,7 | +0,75 |
| Силлиманит | 28126,9 | 27912,8 | +0,77 |
Таблица 2. 2Энергии кристаллических решеток для некоторых
оксидов четырехвалентных металлов
2Энергии кристаллических решеток для некоторых
оксидов четырехвалентных металлов
| Кристаллсостава МО 2 | U, кДж/мольрасчетпо Ферсману | U, кДж/мольэксперимент(по циклу Борна-Габера) | Расхождение,Δ% |
| SiO2 | 12537 | 12958 | -3,25 |
| TiO2 | 12322 | 12314 | +0,06 |
| MnO2 | 13071 | 13067 | +0,03 |
| MoO2 | 12431 | 12355 | -0,11 |
| SnO2 | 11786 | 11770 | +0,14 |
| PbO2 | 11849 | -0,07 |
Обычно энергию кристаллической решетки относят к единице количества вещества (молю) и выражают в ккал/моль или в кДж/моль. Однако очевидно, что для корректного сопоставления энергии решеток различных простых и сложных по составу соединений необходимо пользоваться удельными энергиями решеток, отнесенными к единице массы (1 г) или к единице объема (1 см3) вещества кристалла. Переход от U кДж/моль к удельной массовой энергии решетки Um кДж/г и удельной объемной энергии решетки Uv кДж/см3 осуществляется посредством формул:
Однако очевидно, что для корректного сопоставления энергии решеток различных простых и сложных по составу соединений необходимо пользоваться удельными энергиями решеток, отнесенными к единице массы (1 г) или к единице объема (1 см3) вещества кристалла. Переход от U кДж/моль к удельной массовой энергии решетки Um кДж/г и удельной объемной энергии решетки Uv кДж/см3 осуществляется посредством формул:
Um = U/M; (2.30)
Uv = U/V, (2.31)
где M – формульный (мольный) вес соединения, г/моль; V – его мольный объем, см3/моль, определяемый по формуле V = M/ρ, где ρ – плотность вещества, г/см3. Отсюда следуют указанные размерности Um и Uv и важное соотношение между ними:
Uv = Umρ. (2.32)
(2.32)
Для кварца U(SiO2) = 1071,5(8,6 + 1,55×2) = 12536,55 кДж/моль, M = 60,1 г/моль и ρ = 2,65 г/см3. По формулам (2.30) и (2.31) Um(SiO2) = 208,6 кДж/г и Uv(SiO2) = 552,8 кДж/см3.
Для такого сложного минерала, как берилл Be3Al2Si6O18, энергия кристаллической решетки по сумме эков составляющих ионов
U = 1071,5(2,65×3 + 4,95×2 + 8,6×6 + 1,55×18) = 104310,5 кДж/моль, M = 537,55 г/моль и r = 2,66 г/см3. Тогда по формулам (2.30) и (2.31) для берилла имеем Um = 194,05 кДж/г и Uv = 516,2 кДж/см3.
Аналогичные расчеты для мусковита KAl2[AlSi3O10](OH)2 дают U = 1071,5(0,36 + 4,95×3 + 8,6×3 + 1,55×12 + 1,1×2) = 66229,4 кДж/моль и далее, используя M = 398,4 г/моль и ρ = 2,8 г/см3, получаем Um = 166,3 кДж/г и Uv = 465,6 кДж/см3. Обратим внимание на то, что при колоссальном различии кварца, берилла и мусковита по параметрам общих (мольных) энергий кристаллических решеток, они оказались довольно близкими, сопоставимыми по удельным параметрам Um и Uv, чем и объясняется, по-видимому, обычный парагенезис этих минералов в пегматитах, грейзенах и других породах. Поэтому в дальнейшем при решении проблемы выявления корреляционных зависимостей свойств кристаллов от энергетических параметров были использованы именно удельные энергии кристаллических решеток.
Обратим внимание на то, что при колоссальном различии кварца, берилла и мусковита по параметрам общих (мольных) энергий кристаллических решеток, они оказались довольно близкими, сопоставимыми по удельным параметрам Um и Uv, чем и объясняется, по-видимому, обычный парагенезис этих минералов в пегматитах, грейзенах и других породах. Поэтому в дальнейшем при решении проблемы выявления корреляционных зависимостей свойств кристаллов от энергетических параметров были использованы именно удельные энергии кристаллических решеток.
Соответствующий графический материал в координатах «Uv(Um)/свойство кристалла» с выводом большинства формул представлен на рис. 2.16-2.29. Обобщая материал по выведенным аналитическим зависимостям, можно сделать следующие выводы:
1. Твердость кристаллов (минералов) – относительная (НМ) и абсолютная (микротвердость по Викерсу HV, кгс/мм2), модуль Юнга (Е, ГПа), температура плавления (Тпл., К), скорость звука (v, км/с), поверхностная энергия (Eshkl, Дж/м2), работа выхода электрона из гомоатомных, в основном металлических кристаллов (φ, эВ), кристаллическая электроотрицательность (ЭОкрист.), коэффициенты теплового линейного (α1, 10-6×K-1), объемного (αv, 10-6xK-1) расширения и сжимаемости (β, 10-12×Па-1), теплопроводность (λ, Вт/м×K), показатель преломления (n), коэффициент трещиностойкости (К1с, МПа×м0.5), эффективная энергия разрушения (γ, Дж/м2) лучше коррелируются с параметрами Uv, нежели с параметрами Um, о чем, как показали расчеты, свидетельствуют более высокие величины достоверности аппроксимации R2 соответствующих зависимостей.
Твердость кристаллов (минералов) – относительная (НМ) и абсолютная (микротвердость по Викерсу HV, кгс/мм2), модуль Юнга (Е, ГПа), температура плавления (Тпл., К), скорость звука (v, км/с), поверхностная энергия (Eshkl, Дж/м2), работа выхода электрона из гомоатомных, в основном металлических кристаллов (φ, эВ), кристаллическая электроотрицательность (ЭОкрист.), коэффициенты теплового линейного (α1, 10-6×K-1), объемного (αv, 10-6xK-1) расширения и сжимаемости (β, 10-12×Па-1), теплопроводность (λ, Вт/м×K), показатель преломления (n), коэффициент трещиностойкости (К1с, МПа×м0.5), эффективная энергия разрушения (γ, Дж/м2) лучше коррелируются с параметрами Uv, нежели с параметрами Um, о чем, как показали расчеты, свидетельствуют более высокие величины достоверности аппроксимации R2 соответствующих зависимостей. В связи с этим предлагаются следующие формулы количественной оценки указанных свойств кристаллических веществ:
В связи с этим предлагаются следующие формулы количественной оценки указанных свойств кристаллических веществ:
HM = 0,364Uv0.48; (2.33)
HM = 0,39Uv0.465; (2.34)
HV = 0,21Uv1.37; (2.35)
E = 0,45Uv; (2.36)
G = 1,437Uv0.675; (2.37)
K = 3,7Uv0.6; (2.38)
Тпл. = 290Uv0.31; (2.39)
v = 1,43Uv0.27; (2.40)
Eshkl = 0,0025Uv + 0,3; (2. 41)
41)
φ = 2,24Uv0.122; (2.42)
ЭОкрист. = 0,6Uv0.17; (2.43)
αl = 135Uv-0.47; (2.44)
αv = 1054Uv-0.67; (2.45)
β = 407,4Uv-0.693; (2.46)
λ = 1,0е0.003Uv; (2.47)
n = 0,0004Uv + 1,42; (2.48)
K1c = 0,7e0.0015Uv; (2.49)
γ = 0,027Uv. (2.50)
2. Грамм-атомная теплоемкость (Ср, Дж/(г-ат)×K) и частота максимального колебания атомов (nm, ТГц) в кристаллах лучше коррелируются с параметрами Um, в связи с чем предлагаются формулы количественной оценки этих двух свойств кристаллических веществ:
Грамм-атомная теплоемкость (Ср, Дж/(г-ат)×K) и частота максимального колебания атомов (nm, ТГц) в кристаллах лучше коррелируются с параметрами Um, в связи с чем предлагаются формулы количественной оценки этих двух свойств кристаллических веществ:
Ср = 24,37e-0.002Um; (2.51)
nm = 1,86Um0.39. (2.52)
При выводе формул (2.33)-(2.52) был использован тот же самый обширный материал по физико-химическим свойствам минералов и искусственных (в том числе тугоплавких) кристаллов, что и в случае выявления искомых зависимостей по параметрам структурной рыхлости ω. Поэтому соответствующие источники и ссылки по свойствам веществ указаны в предыдущем разделе 2.1. Массивы табличных данных, использованных при построении графиков, не приводятся, так как эти данные включают многие сотни кристаллов – простых гомоатомных, бинарных, а также разнообразных сложных соединений (оксидов, силикатов, сульфатов, карбонатов и др. ).
Формулы твердости (2.33), (2.34) и (2.35) относятся в основном к кристаллам с координационным и каркасным мотивами структуры и не применимы к анизодесмическим соединениям, характеризующимся резко выраженным островным, цепочечным, либо слоистым мотивом структуры. Впрочем, как показано в разделе 2.2.1, расчет твердости анизодесмических (например, островных) кристаллов возможен, если параметры Uv рассчитываются с учетом их структурного мотива.
Ковалентные кристаллы (алмаз и кремний) в соответствии с представлениями Э. Фридриха, А. Е. Ферсмана, Н. В. Белова[2], А. С. Поваренных допустимо аппроксимировать как ионные (С4+С4-, Si4+Si4-). Получившаяся в результате четкая зависимость НМ = f(Uv) на рис. 2.16 подтвердила правомерность такого подхода к ковалентным соединениям. Здесь уместно привести касающуюся твердости веществ цитату Э. Фридриха (Ферсман, 1958, стр.
).
Формулы твердости (2.33), (2.34) и (2.35) относятся в основном к кристаллам с координационным и каркасным мотивами структуры и не применимы к анизодесмическим соединениям, характеризующимся резко выраженным островным, цепочечным, либо слоистым мотивом структуры. Впрочем, как показано в разделе 2.2.1, расчет твердости анизодесмических (например, островных) кристаллов возможен, если параметры Uv рассчитываются с учетом их структурного мотива.
Ковалентные кристаллы (алмаз и кремний) в соответствии с представлениями Э. Фридриха, А. Е. Ферсмана, Н. В. Белова[2], А. С. Поваренных допустимо аппроксимировать как ионные (С4+С4-, Si4+Si4-). Получившаяся в результате четкая зависимость НМ = f(Uv) на рис. 2.16 подтвердила правомерность такого подхода к ковалентным соединениям. Здесь уместно привести касающуюся твердости веществ цитату Э. Фридриха (Ферсман, 1958, стр. 193): «Электростатическое притяжение атомов является, таким образом, причиною твердости тела… атомные решетки ведут себя так, как если бы они были ионными».
В отношении твердости металлов аналогичный подход был успешно использован А. С. Поваренных в монографии (Поваренных, 1963). Резкое расширение массива данных с включением более 200 объектов (рис. 2.17) лишь незначительно изменило первоначальную формулу (2.33), выведенную по 12 эталонам усовершенствованной 15-балльной шкалы Мооса (рис. 2.16). Поэтому при оценке относительной твердости кристаллов допустимо пользоваться любой из формул (2.33) или (2.34).
Как известно (Бокий, 1971), концепция энергии кристаллической решетки в приложении к металлам базируется на представлении о взаимодействии локализованных в узлах решетки положительных атомных остовов (Мn+) c делокализованным в межостовном пространстве электронным газом (ne–). Данные по величинам энергетических коэффициентов электронного газа металлических кристаллов пока отсутствуют, поэтому прямые расчеты соответствующих энергий решеток металлов по методу Ферсмана не представляются возможными.
193): «Электростатическое притяжение атомов является, таким образом, причиною твердости тела… атомные решетки ведут себя так, как если бы они были ионными».
В отношении твердости металлов аналогичный подход был успешно использован А. С. Поваренных в монографии (Поваренных, 1963). Резкое расширение массива данных с включением более 200 объектов (рис. 2.17) лишь незначительно изменило первоначальную формулу (2.33), выведенную по 12 эталонам усовершенствованной 15-балльной шкалы Мооса (рис. 2.16). Поэтому при оценке относительной твердости кристаллов допустимо пользоваться любой из формул (2.33) или (2.34).
Как известно (Бокий, 1971), концепция энергии кристаллической решетки в приложении к металлам базируется на представлении о взаимодействии локализованных в узлах решетки положительных атомных остовов (Мn+) c делокализованным в межостовном пространстве электронным газом (ne–). Данные по величинам энергетических коэффициентов электронного газа металлических кристаллов пока отсутствуют, поэтому прямые расчеты соответствующих энергий решеток металлов по методу Ферсмана не представляются возможными. В этих случаях пришлось обратиться к косвенному методу оценки Uv металлов – по формуле (2.34) с использованием известных валентностей металлов и их относительной твердости (Поваренных, 1963). Найденные таким путем величины Uv гомоатомных металлических кристаллов были использованы при выводе формул (2.42) и (2.43). Формула теплопроводности (2.47) относится к диэлектрикам, т. е. к соединениям с большой шириной запрещенной зоны (Eg), обладающим ковалентными, ионными и ионно-ковалентными связями. Необходимо также подчеркнуть, что получаемые по формулам (2.44)-(2.47), (2.51) параметры относятся к веществам, находящимся в стандартных термодинамических условиях.
Из вышеизложенного следует, что на базе параметров удельных энергий кристаллических решеток имеется возможность количественного объяснения и предсказания весьма широкого спектра физико-химических свойств кристаллов (минералов), включая прочностные (механические) и упругие, теплофизические, термические, электрические (термоэмиссионные), кристаллохимические и т.
В этих случаях пришлось обратиться к косвенному методу оценки Uv металлов – по формуле (2.34) с использованием известных валентностей металлов и их относительной твердости (Поваренных, 1963). Найденные таким путем величины Uv гомоатомных металлических кристаллов были использованы при выводе формул (2.42) и (2.43). Формула теплопроводности (2.47) относится к диэлектрикам, т. е. к соединениям с большой шириной запрещенной зоны (Eg), обладающим ковалентными, ионными и ионно-ковалентными связями. Необходимо также подчеркнуть, что получаемые по формулам (2.44)-(2.47), (2.51) параметры относятся к веществам, находящимся в стандартных термодинамических условиях.
Из вышеизложенного следует, что на базе параметров удельных энергий кристаллических решеток имеется возможность количественного объяснения и предсказания весьма широкого спектра физико-химических свойств кристаллов (минералов), включая прочностные (механические) и упругие, теплофизические, термические, электрические (термоэмиссионные), кристаллохимические и т. д. и т. п.
Достоверность выявленных зависимостей базируется на использовании при их выводе весьма представительных статистических материалов, включающих соответствующие корреляционные данные для многих сотен кристаллических соединений. Необходимо подчеркнуть, что средняя величина достоверности аппроксимации установленных зависимостей оказалась довольно высокой: <R2> = 0,83 при ее колебании в интервале от 0,64 до почти 1 (рис. 2.16). И столь высокие коэффициенты корреляции получились при использовании весьма грубых оценок энергий решеток по Ферсману. Применение в дальнейшем более совершенных методов расчета энергии кристаллических решеток, несомненно, приведет к уточнению установленных зависимостей и росту соответствующих им параметров R2.
Обобщая приведенный материал данного раздела, можно сделать следующие выводы. Если вместо общей энергии кристаллической решетки оперировать удельными энергиями кристаллической решетки, отнесенными к единичной массе или единичному объему вещества кристалла, то неожиданным образом выявляется глубокая, закономерная взаимосвязь указанных удельных энергетических характеристик кристалла с широким спектром его самых разнообразных физико-химических свойств.
д. и т. п.
Достоверность выявленных зависимостей базируется на использовании при их выводе весьма представительных статистических материалов, включающих соответствующие корреляционные данные для многих сотен кристаллических соединений. Необходимо подчеркнуть, что средняя величина достоверности аппроксимации установленных зависимостей оказалась довольно высокой: <R2> = 0,83 при ее колебании в интервале от 0,64 до почти 1 (рис. 2.16). И столь высокие коэффициенты корреляции получились при использовании весьма грубых оценок энергий решеток по Ферсману. Применение в дальнейшем более совершенных методов расчета энергии кристаллических решеток, несомненно, приведет к уточнению установленных зависимостей и росту соответствующих им параметров R2.
Обобщая приведенный материал данного раздела, можно сделать следующие выводы. Если вместо общей энергии кристаллической решетки оперировать удельными энергиями кристаллической решетки, отнесенными к единичной массе или единичному объему вещества кристалла, то неожиданным образом выявляется глубокая, закономерная взаимосвязь указанных удельных энергетических характеристик кристалла с широким спектром его самых разнообразных физико-химических свойств. По нашему мнению, эта закономерность может трактоваться как имеющая фундаментальный характер, поскольку убедительно доказывает, что разные физико-химические свойства твердых тел (механические, упругие, термические, теплофизические, кристаллохимические и др.) в действительности определяются единой природой – энергией взаимодействия составляющих кристалл ионов, а удельные энергии кристаллической решетки (параметры Uv, реже Um) являются адекватной для количественного описания свойств веществ формой выражения энергии решетки.
Другим нетривиальным следствием данного раздела является то обстоятельство, что гомоатомные ковалентные и металлические кристаллы в рамках данного энергетического подхода при оценке их свойств могут рассматриваться как квазиионные, к которым предлагаемые формулы также применимы. В отношении твердости эта закономерность была установлена, как указано выше, еще в работах Э. Фридриха, А. Е. Ферсмана, А.
По нашему мнению, эта закономерность может трактоваться как имеющая фундаментальный характер, поскольку убедительно доказывает, что разные физико-химические свойства твердых тел (механические, упругие, термические, теплофизические, кристаллохимические и др.) в действительности определяются единой природой – энергией взаимодействия составляющих кристалл ионов, а удельные энергии кристаллической решетки (параметры Uv, реже Um) являются адекватной для количественного описания свойств веществ формой выражения энергии решетки.
Другим нетривиальным следствием данного раздела является то обстоятельство, что гомоатомные ковалентные и металлические кристаллы в рамках данного энергетического подхода при оценке их свойств могут рассматриваться как квазиионные, к которым предлагаемые формулы также применимы. В отношении твердости эта закономерность была установлена, как указано выше, еще в работах Э. Фридриха, А. Е. Ферсмана, А.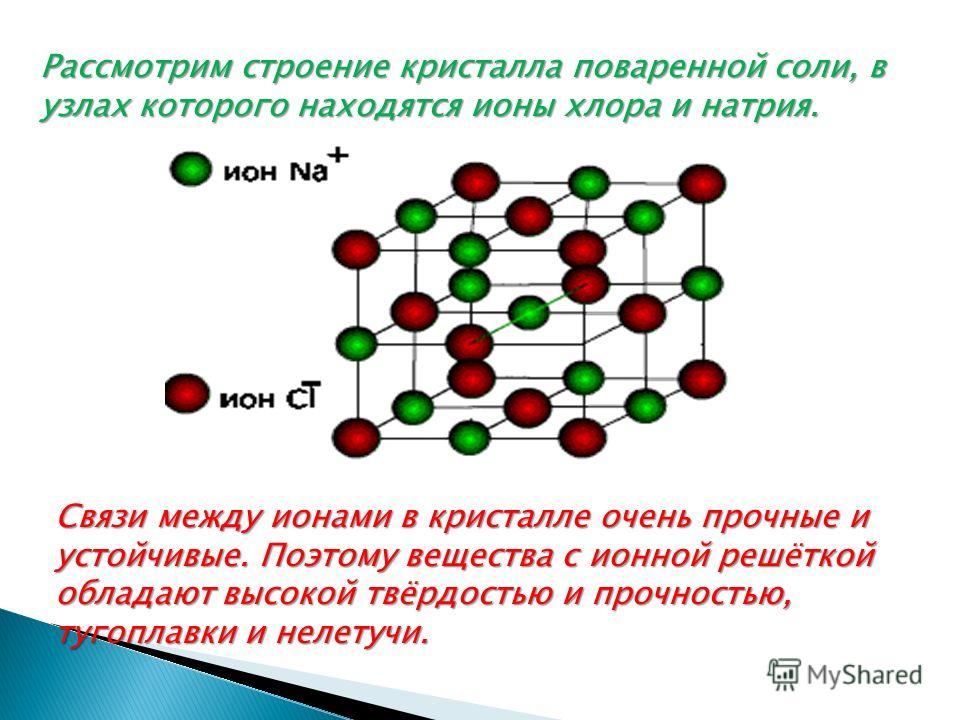 С. Поваренных, однако в настоящем исследовании она получила дальнейшее убедительное подтверждение в отношении многих других свойств атомных кристаллов при оперировании именно удельными энергиями кристаллических решеток.
Немаловажно также фактическое возрождение геоэнергетической теории А. Е. Ферсмана, которая в модифицированном виде (удельных энергий решеток) может дать современной геологической науке весьма полезные и ценные результаты по объяснению совместного нахождения (парагенезисов) минералов в горных породах и рудах, а также энергетической направленности смены (замещения) одних минеральных ассоциаций другими в различных геологических процессах. Удельные энергии кристаллических решеток минералов являются, по нашему мнению, объективной мерой их энергетической стабильности. Заметим, кстати, что использование последних опровергает вывод работы В. С. Урусова и др. (Урусов, Оганов, Еремин, 1998) о неустойчивости кианита (как известно, наиболее стабильной модификации Al2SiO5) с точки зрения величины энергии кристаллической решетки.
С. Поваренных, однако в настоящем исследовании она получила дальнейшее убедительное подтверждение в отношении многих других свойств атомных кристаллов при оперировании именно удельными энергиями кристаллических решеток.
Немаловажно также фактическое возрождение геоэнергетической теории А. Е. Ферсмана, которая в модифицированном виде (удельных энергий решеток) может дать современной геологической науке весьма полезные и ценные результаты по объяснению совместного нахождения (парагенезисов) минералов в горных породах и рудах, а также энергетической направленности смены (замещения) одних минеральных ассоциаций другими в различных геологических процессах. Удельные энергии кристаллических решеток минералов являются, по нашему мнению, объективной мерой их энергетической стабильности. Заметим, кстати, что использование последних опровергает вывод работы В. С. Урусова и др. (Урусов, Оганов, Еремин, 1998) о неустойчивости кианита (как известно, наиболее стабильной модификации Al2SiO5) с точки зрения величины энергии кристаллической решетки. В самом деле, рассчитанные удельные энергии решеток модификаций Al2SiO5 (Uv кианита = 601 кДж/см3, Uv андалузита = 534 кДж/см3, Uv силлиманита = 551 кДж/см3) однозначно свидетельствуют о максимальной стабильности именно кианита. Точно такой же порядок роста стабильности (андалузит→силлиманит→кианит) следует из данных по энергоплотности этих соединений (соответственно 94,8 кДж/см3, 99,3 кДж/см3 и 112,3 кДж/см3).
Другой весьма характерный пример, приводимый В. С. Урусовым (Урусов, 1975, стр. 270) с целью дискредитации концепции энергии кристаллической решетки. Известно, что первые порции оливина (Mg,Fe)2SiO4 всегда богаче магнием, а более поздние железом, т. е. кристаллизация идет в последовательности Mg2SiO4→Fe2SiO4, в которой понижаются температуры плавления (2163°К и 1478°К соответственно у форстерита и фаялита).
В самом деле, рассчитанные удельные энергии решеток модификаций Al2SiO5 (Uv кианита = 601 кДж/см3, Uv андалузита = 534 кДж/см3, Uv силлиманита = 551 кДж/см3) однозначно свидетельствуют о максимальной стабильности именно кианита. Точно такой же порядок роста стабильности (андалузит→силлиманит→кианит) следует из данных по энергоплотности этих соединений (соответственно 94,8 кДж/см3, 99,3 кДж/см3 и 112,3 кДж/см3).
Другой весьма характерный пример, приводимый В. С. Урусовым (Урусов, 1975, стр. 270) с целью дискредитации концепции энергии кристаллической решетки. Известно, что первые порции оливина (Mg,Fe)2SiO4 всегда богаче магнием, а более поздние железом, т. е. кристаллизация идет в последовательности Mg2SiO4→Fe2SiO4, в которой понижаются температуры плавления (2163°К и 1478°К соответственно у форстерита и фаялита).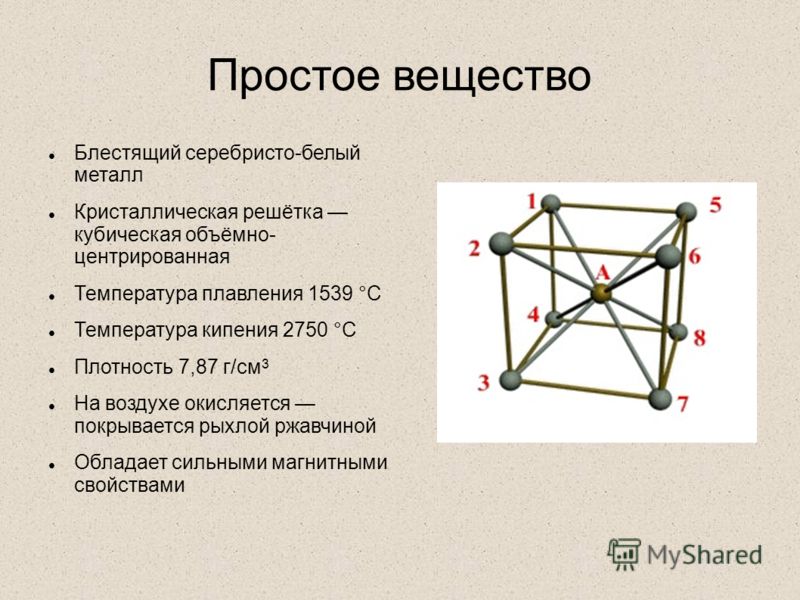 Но порядок энергий решеток обратный: U(Mg2SiO4) = 20639,7 кДж/моль и U(Fe2SiO4) = 20761 кДж/моль. Однако при использовании удельных объемных энергий кристаллических решеток: Uv(Mg2SiO4) = 469,4 кДж/см3 и Uv(Fe2SiO4) = 448,4 кДж/см3 все становится на свои места – как в смысле соответствия с указанными температурами плавления, так и в смысле относительной твердости, заметно большей у форстерита по сравнению с фаялитом.
Такая же ситуация имеет место для другой пары минералов – энстатита Mg2Si2O6 и ферросилита Fe2Si2O6 с обратным соотношением величин общих и удельных объемных энергий кристаллических решеток: U(Mg2Si2O6) = 30543,6 кДж/моль и U(Fe2Si2O6) = 31355,9 кДж/моль, Uv(Mg2Si2O6) = 486,4 кДж/см3 и Uv(Fe2Si2O6) = 475,3.
Но порядок энергий решеток обратный: U(Mg2SiO4) = 20639,7 кДж/моль и U(Fe2SiO4) = 20761 кДж/моль. Однако при использовании удельных объемных энергий кристаллических решеток: Uv(Mg2SiO4) = 469,4 кДж/см3 и Uv(Fe2SiO4) = 448,4 кДж/см3 все становится на свои места – как в смысле соответствия с указанными температурами плавления, так и в смысле относительной твердости, заметно большей у форстерита по сравнению с фаялитом.
Такая же ситуация имеет место для другой пары минералов – энстатита Mg2Si2O6 и ферросилита Fe2Si2O6 с обратным соотношением величин общих и удельных объемных энергий кристаллических решеток: U(Mg2Si2O6) = 30543,6 кДж/моль и U(Fe2Si2O6) = 31355,9 кДж/моль, Uv(Mg2Si2O6) = 486,4 кДж/см3 и Uv(Fe2Si2O6) = 475,3. И последний пример «дискредитации» концепции ионной кристаллической решетки применительно к полевым шпатам – альбиту NaAlSi3O8 и анортиту CaAl2Si2O8 (Урусов, 1975). По оценкам В. С. Урусова энергия решетки альбита гораздо выше по сравнению с анортитом, что находится в явном противоречии с более высокой температурой плавления последнего.[3] Для выхода из этой ситуации при оперировании энергиями решеток по Ферсману достаточно несколько изменить некоторые из стандартных энергетических коэффициентов ионов, входящих в состав этих минералов, а именно принять их равными: Na - 0,45; Ca - 1,75; Al[4] - 6,5; Si - 7,3; O - 1,55. Изменения касаются повышения энергетического коэффициента иона алюминия в тетраэдрической координации[4] и принятия энергетического коэффициента иона кремния по Шибольду (Сауков, 1955, с. 161). Тогда расчеты по формулам (2.29), (2.30), (2.31) дают для альбита NaAlSi3O8: U = 44199,4 кДж/моль, Um = 168,54 кДж/г, Uv = 441,6 кДж/см3 и для анортита CaAl2Si2O8: U = 44735,12 кДж/моль, Um = 160,77 кДж/г, Uv = 443,72 кДж/см3.
И последний пример «дискредитации» концепции ионной кристаллической решетки применительно к полевым шпатам – альбиту NaAlSi3O8 и анортиту CaAl2Si2O8 (Урусов, 1975). По оценкам В. С. Урусова энергия решетки альбита гораздо выше по сравнению с анортитом, что находится в явном противоречии с более высокой температурой плавления последнего.[3] Для выхода из этой ситуации при оперировании энергиями решеток по Ферсману достаточно несколько изменить некоторые из стандартных энергетических коэффициентов ионов, входящих в состав этих минералов, а именно принять их равными: Na - 0,45; Ca - 1,75; Al[4] - 6,5; Si - 7,3; O - 1,55. Изменения касаются повышения энергетического коэффициента иона алюминия в тетраэдрической координации[4] и принятия энергетического коэффициента иона кремния по Шибольду (Сауков, 1955, с. 161). Тогда расчеты по формулам (2.29), (2.30), (2.31) дают для альбита NaAlSi3O8: U = 44199,4 кДж/моль, Um = 168,54 кДж/г, Uv = 441,6 кДж/см3 и для анортита CaAl2Si2O8: U = 44735,12 кДж/моль, Um = 160,77 кДж/г, Uv = 443,72 кДж/см3. Полученные данные по величинам удельных объемных энергий кристаллических решеток альбита и анортита находятся в согласии с их температурами плавления и величинами энергоплотности – большей у анортита (78,91 кДж/см3) и меньшей у альбита (76,98 кДж/см3) (Зуев, Денисов, Мочалов и др., 2000). Корректность величины ЭК Al[4] = 6,5 можно проверить по другим кристаллическим соединениям с тетраэдрической координацией алюминия. Так, для кристалла AlN (d = 1,89 Å, r = 3,28 г/см3) U(AlN) = 1071,5(6,5 + 3,6) = 10822,15 кДж/моль, Um(AlN) = 263,91 кДж/г, Uv(AlN) = 865,6 кДж/см3, и расчет по формуле (2.32) дает НМ = 9,4 (экспериментальная относительная твердость равна 9-10). Аналогичным образом для кристалла AlSb в случае принятия ЭК Al[4] = 6,5 имеем Uv(AlSb) = 283 кДж/см3 и НМ = 5,4 в близком согласии с экспериментом (Поваренных, 1963).
Полученные данные по величинам удельных объемных энергий кристаллических решеток альбита и анортита находятся в согласии с их температурами плавления и величинами энергоплотности – большей у анортита (78,91 кДж/см3) и меньшей у альбита (76,98 кДж/см3) (Зуев, Денисов, Мочалов и др., 2000). Корректность величины ЭК Al[4] = 6,5 можно проверить по другим кристаллическим соединениям с тетраэдрической координацией алюминия. Так, для кристалла AlN (d = 1,89 Å, r = 3,28 г/см3) U(AlN) = 1071,5(6,5 + 3,6) = 10822,15 кДж/моль, Um(AlN) = 263,91 кДж/г, Uv(AlN) = 865,6 кДж/см3, и расчет по формуле (2.32) дает НМ = 9,4 (экспериментальная относительная твердость равна 9-10). Аналогичным образом для кристалла AlSb в случае принятия ЭК Al[4] = 6,5 имеем Uv(AlSb) = 283 кДж/см3 и НМ = 5,4 в близком согласии с экспериментом (Поваренных, 1963). Приведенные примеры дают возможность реабилитировать концепцию энергии кристаллической ионной решетки и тем самым подтвердить ее полезность при объяснении физических свойств минералов.
Помимо чисто научного, теоретико-познавательного значения данный раздел имеет также несомненный практический выход – как разработка нового эффективного метода количественной оценки многих физико-химических свойств кристаллического вещества, экспериментальное определение которых по ряду причин затруднено или невозможно. К тому же для многих кристаллов приводимые в справочной литературе данные по физико-химическим свойствам нередко противоречивы и требуют уточнения. Рассмотрим конкретный пример – кристалл CdO (минерал имеет названия монтепонит или кадмоксит), обладающий кубической структурой типа NaCl. Вычислив для кристалла CdO энергетические параметры U = 3804 кДж/моль, Um = 29,6 кДж/г и Uv = 243 кДж/см3, по соответствующим формулам можно количественно охарактеризовать более десятка свойств этого соединения (Зуев, Денисов, Мочалов и др.
Приведенные примеры дают возможность реабилитировать концепцию энергии кристаллической ионной решетки и тем самым подтвердить ее полезность при объяснении физических свойств минералов.
Помимо чисто научного, теоретико-познавательного значения данный раздел имеет также несомненный практический выход – как разработка нового эффективного метода количественной оценки многих физико-химических свойств кристаллического вещества, экспериментальное определение которых по ряду причин затруднено или невозможно. К тому же для многих кристаллов приводимые в справочной литературе данные по физико-химическим свойствам нередко противоречивы и требуют уточнения. Рассмотрим конкретный пример – кристалл CdO (минерал имеет названия монтепонит или кадмоксит), обладающий кубической структурой типа NaCl. Вычислив для кристалла CdO энергетические параметры U = 3804 кДж/моль, Um = 29,6 кДж/г и Uv = 243 кДж/см3, по соответствующим формулам можно количественно охарактеризовать более десятка свойств этого соединения (Зуев, Денисов, Мочалов и др. , 2000). Полученные для кристалла CdO данные доказывают полезность использования удельных энергий кристаллической решетки при оценке свойств кристаллов. Обратим внимание на то, что ряд важных физико-химических свойств кристалла CdO в справочной литературе отсутствует, другие же требуют уточнения. В частности, приводимая во всех основных минералогических справочниках относительная твердость кадмоксита (около 3) является ошибочной, явно заниженной, что связано, по-видимому, с ее определением в дезинтегрированных порошковатых массах минерала. Уточненная нами относительная твердость кристалла CdO (5) подтверждается независимыми расчетами по формулам А. С. Поваренных (Поваренных, 1963) и В. В. Зуева (Зуев, 1990).
Особую ценность представляет возможность прогнозирования широкого спектра физико-химических параметров для вновь создаваемых неорганических материалов. Другими словами, введенная нами концепция удельной энергии кристаллической решетки может оказать существенную помощь в решении актуальной проблемы синтеза веществ с заданными свойствами – в плане их прогнозирования.
, 2000). Полученные для кристалла CdO данные доказывают полезность использования удельных энергий кристаллической решетки при оценке свойств кристаллов. Обратим внимание на то, что ряд важных физико-химических свойств кристалла CdO в справочной литературе отсутствует, другие же требуют уточнения. В частности, приводимая во всех основных минералогических справочниках относительная твердость кадмоксита (около 3) является ошибочной, явно заниженной, что связано, по-видимому, с ее определением в дезинтегрированных порошковатых массах минерала. Уточненная нами относительная твердость кристалла CdO (5) подтверждается независимыми расчетами по формулам А. С. Поваренных (Поваренных, 1963) и В. В. Зуева (Зуев, 1990).
Особую ценность представляет возможность прогнозирования широкого спектра физико-химических параметров для вновь создаваемых неорганических материалов. Другими словами, введенная нами концепция удельной энергии кристаллической решетки может оказать существенную помощь в решении актуальной проблемы синтеза веществ с заданными свойствами – в плане их прогнозирования. В качестве резюме данного раздела отметим следующее. Признавая главенствующую, ведущую роль и более универсальный характер второго энергетического подхода (энергоплотности) в объяснении и предсказании свойств твердых тел (Зуев, Денисов, Мочалов, 2000), нельзя игнорировать также большие возможности в этой области, открываемые использованием первого энергетического подхода в виде удельных энергий кристаллических решеток. А совместное использование различных энергетических подходов дает возможность получения более надежных результатов по прогнозируемым свойствам твердых тел. Подробнее этот вопрос будет рассмотрен в заключительной части 2-ой главы.
Завершая раздел, рассмотрим вопрос о количественной оценке комплексности весьма распространенных сложных минералов, содержащих различные группировки (радикалы), обуславливающие соответствующие (островные) структурные мотивы и влияющие на свойства (твердость и др.) таких минералов. Следует подчеркнуть, что постановка и решение этого вопроса оказались возможными лишь в рамках концепции энергии кристаллической решетки, которая в этом отношении обладает несомненным преимуществом по сравнению с другими энергетическими подходами.
В качестве резюме данного раздела отметим следующее. Признавая главенствующую, ведущую роль и более универсальный характер второго энергетического подхода (энергоплотности) в объяснении и предсказании свойств твердых тел (Зуев, Денисов, Мочалов, 2000), нельзя игнорировать также большие возможности в этой области, открываемые использованием первого энергетического подхода в виде удельных энергий кристаллических решеток. А совместное использование различных энергетических подходов дает возможность получения более надежных результатов по прогнозируемым свойствам твердых тел. Подробнее этот вопрос будет рассмотрен в заключительной части 2-ой главы.
Завершая раздел, рассмотрим вопрос о количественной оценке комплексности весьма распространенных сложных минералов, содержащих различные группировки (радикалы), обуславливающие соответствующие (островные) структурные мотивы и влияющие на свойства (твердость и др.) таких минералов. Следует подчеркнуть, что постановка и решение этого вопроса оказались возможными лишь в рамках концепции энергии кристаллической решетки, которая в этом отношении обладает несомненным преимуществом по сравнению с другими энергетическими подходами.
[1] Если принять во внимание весь накопившийся к настоящему времени соответствующий материал, то большинство данных по эффективным зарядам атомов в сфалерите укладывается в следующем диапазоне: Q(Zn) = +(1,2±0,5), Q(S) = -(1,2±0,5).
[2] По мнению академика Н. В. Белова (Белов, 1947, стр.66) ковалентную связь в алмазе с позиций квантовой механики можно трактовать как результат резонанса (непрерывной осцилляции) предельно-ионных структур С4+С4- <-> С4-С4+.
[3] В то время как параметры энергии атомизации альбита и анортита находятся в соответствии с их температурами плавления.
[4] Энергетический коэффициент иона алюминия в наиболее распространенной для него октаэдрической координации примем равным 4,95 (Ферсман, 1958). По определению ЭК иона обратно пропорционален ионному радиусу, т. е. величине 1/ri.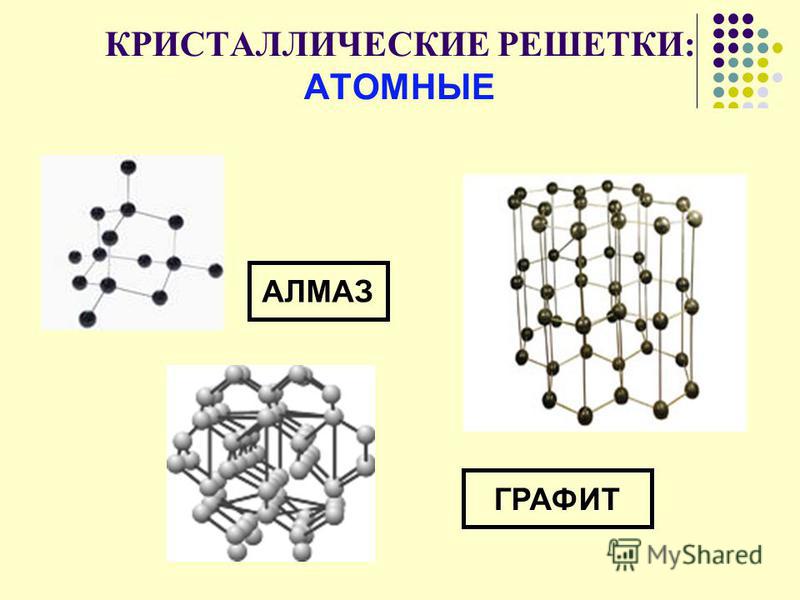 Согласно (Бацанов, 1991), октаэдрический и тетраэдрический радиусы иона Al3+равны 0,54 Å и 0,39 Å. Тогда из соответствующей пропорции ЭК Al3+ = (4,95×1/0,39)/(1/0,54) = 6,8. По другим данным (Урусов, 1975; Современная кристаллография, 1979) ri(Al[6]) = 0,67 Å, ri(Al[4]) = 0,53 Å и ЭК Al3+ = (4,95×1/0,53)/(1/0,67) = 6,3. Другой подход: для атомов в тетраэдрической координации (КЧ = 4) расчеты электроотрицательностей согласно (Яковлев, 2002) дают ЭО Al = 1,63 и ЭО Si = 1,86. Полагая прямо пропорциональную зависимость между ЭК и ЭО соответствующих ионов (атомов) и приняв ЭК Si4+ = 7,3, из пропорции находим для тетраэдрической координации ЭК Al3+ = (7,3×1,63)/1,86 = 6,4.
Согласно (Бацанов, 1991), октаэдрический и тетраэдрический радиусы иона Al3+равны 0,54 Å и 0,39 Å. Тогда из соответствующей пропорции ЭК Al3+ = (4,95×1/0,39)/(1/0,54) = 6,8. По другим данным (Урусов, 1975; Современная кристаллография, 1979) ri(Al[6]) = 0,67 Å, ri(Al[4]) = 0,53 Å и ЭК Al3+ = (4,95×1/0,53)/(1/0,67) = 6,3. Другой подход: для атомов в тетраэдрической координации (КЧ = 4) расчеты электроотрицательностей согласно (Яковлев, 2002) дают ЭО Al = 1,63 и ЭО Si = 1,86. Полагая прямо пропорциональную зависимость между ЭК и ЭО соответствующих ионов (атомов) и приняв ЭК Si4+ = 7,3, из пропорции находим для тетраэдрической координации ЭК Al3+ = (7,3×1,63)/1,86 = 6,4.
« Предыдущая глава 2.1. Зависимость физических свойств минералов и неорганических кристаллов от структурной рыхлости
Следующая глава »
2. 2.1. Сложные и комплексные кристаллические соединения
2.1. Сложные и комплексные кристаллические соединения
Быстрое оформление заказа
Я согласен с политикой конфиденциальностиРассчитать количество материала
Я согласен с политикой конфиденциальностиОставьте контактные данные и мы перезвоним вам в ближайшее время
Я согласен с политикой конфиденциальностиНаписать нам
Я согласен с политикой конфиденциальностиВарианты цвета
Товар добавлен в корзину
Оформление заказа
Физическое лицо / ИП Юридическое лицо
Я согласен с политикой конфиденциальности Я согласен с политикой конфиденциальности✕
Спасибо за вашу заявку! Мы скоро вам перезвоним
Рассчитать количество материала
Спасибо за заявку!
Ожидайте звонка нашего специалиста
Физические свойства металлов и общее применение металлической связи в таблице (9 класс, химия)
4. 2
2
Средняя оценка: 4.2
Всего получено оценок: 286.
4.2
Средняя оценка: 4.2
Всего получено оценок: 286.
Физические свойства металлов отличают их от неметаллов. Все металлы, кроме ртути, – твёрдые кристаллические вещества, являющиеся восстановителями в окислительно-восстановительных реакциях.
Положение в таблице Менделеева
Металлы занимают I-II группы и побочные подгруппы III-VIII групп. Металлические свойства, т.е. способность отдавать валентные электроны или окисляться, увеличиваются сверху вниз по мере увеличения количества энергетических уровней. Слева направо металлические свойства ослабевают, поэтому наиболее активные металлы находятся в I-II группах, главных подгруппах. Это щелочные и щелочноземельные металлы.
Определить степень активности металлов можно по электрохимическому ряду напряжений. Металлы, стоящие до водорода, наиболее активны. После водорода стоят слабоактивные металлы, не вступающие в реакцию с большинством веществ.
Строение
Вне зависимости от активности все металлы имеют общее строение. Атомы в простом металле расположены не хаотично, как в аморфных веществах, а упорядоченно – в виде кристаллической решётки. Удерживает атомы в одном положении металлическая связь.
Такой вид связи осуществляется за счёт положительно заряженных ионов, находящихся в узлах кристаллической ячейки (единицы решётки), и отрицательно заряженных свободных электронов, которые образуют так называемый электронный газ. Электроны отделились от атомов, превратив их в ионы, и стали перемещаться в решётке хаотично, скрепляя ионы вместе. Без электронов решётка бы распалась за счёт отторжения одинаково заряженных ионов.
Различают три типа кристаллической решётки. Кубическая объемно-центрированная состоит из 9 ионов и характерна хрому, железу, вольфраму. Кубическая гранецентрированная включает 14 ионов и свойственная свинцу, алюминию, серебру. Из 17 ионов состоит гексагональная плотноупакованная решётка цинка, титана, магния.
Свойства
Строение кристаллической решётки определяет основные физические и химические свойства металлов. Металлы блестят, плавятся, проводят тепло и электричество. Промышленность и металлургия нашли применение физическим свойствам металлов в изготовлении деталей, фольги, корпусов машин, зеркал, бытовой и промышленной химии. Особенности металлов и их использование представлены в таблице физических свойств металлов.
Свойства | Особенности | Примеры | Применение |
Металлический блеск | Способность отражать солнечный свет | Наиболее блестящими металлами являются Hg, Ag, Pd | Изготовление зеркал |
Плотность | Лёгкие – имеют плотность меньше 5 г/см3 | Na, K, Ba, Mg, Al. | Изготовление облицовки, деталей самолётов |
Тяжёлые – имеют плотность больше 5 г/см3 | Sn, Fe, Zn, Au, Pb, Hg. Самый тяжёлый – осмий с плотностью 22,5 г/см3 | Использование в сплавах | |
Пластичность | Способность изменять форму без разрушений (можно раскатать в тонкую фольгу) | Наиболее пластичные – Au, Cu, Ag. Хрупкие – Zn, Sn, Bi, Mn | Формовка, сгибание труб, изготовление проволоки |
Твёрдость | Мягкие – режутся ножом | Na, K, In | Изготовление мыла, стекла, удобрений |
Твёрдые – сравнимы по твёрдости с алмазом | Самый твёрдый – хром, режет стекло | Изготовление несущих конструкций | |
Температура плавления | Легкоплавкие – температура плавления ниже 1000°С | Hg (38,9°С), Ga (29,78°С), Cs (28,5°С), Zn (419,5°C) | Производство радиотехники, жести |
Тугоплавкие – температура плавления выше 1000°С | Cr (1890°С), Mo (2620°С), V (1900°С). | Изготовление ламп накаливания | |
Теплопроводность | Способность передавать тепло другим телам | Лучше всего проводят ток и тепло Ag, Cu, Au, Al | Приготовление пищи в металлической посуде |
Электропроводность | Способность проводить электрический ток за счёт свободных электронов | Передача электричества по проводам |
Что мы узнали?
Из урока 9 класса узнали о физических свойствах металлов. Кратко рассмотрели положение металлов в периодической таблице и особенности строения кристаллической решётки. Благодаря строению металлы обладают пластичностью, твёрдостью, способностью плавиться, проводить электрический ток и тепло. Свойства металлов неоднородны. Различают лёгкие и тяжёлые металлы, лёгкоплавкие и тугоплавкие, мягкие и твёрдые. Физические свойства используются для изготовления сплавов, электрических проводов, посуды, мыла, стекла, конструкций различной формы.
Физические свойства используются для изготовления сплавов, электрических проводов, посуды, мыла, стекла, конструкций различной формы.
Тест по теме
Доска почёта
Чтобы попасть сюда – пройдите тест.
Лидия Маслова
10/10
Оценка доклада
4.2
Средняя оценка: 4.2
Всего получено оценок: 286.
А какая ваша оценка?
Физические свойства металлической кристаллической решетки
Общие свойства металлов: Металлы — это ковкие, пластичные, тягучие вещества, имеющие металлический блеск и способны проводить тепло и электрический ток.
Атомы элементов-металлов отдают электроны внешнего электронного слоя, превращаясь в положительные ионы.
Это свойство атомов металлов, определяется тем, что они имеют сравнительно большие радиусы и малое число электронов. Всвязи с этим атомы металлов сравнительно легко отдают наружные электроны и превращаются в положительно заряженные ионы. Оторвавшиеся от атомов электроны располагаются между положительными ионами и относительно свободно перемещаются между ними. Между положительными ионами металлов и этими электронами возникает связь. Так как электроны находятся в непрерывном движении , то при их столкновении с положительными ионами последние могут на некоторое время превратится в нейтральные атомы. Эти кристаллические решетки – металлические.
Оторвавшиеся от атомов электроны располагаются между положительными ионами и относительно свободно перемещаются между ними. Между положительными ионами металлов и этими электронами возникает связь. Так как электроны находятся в непрерывном движении , то при их столкновении с положительными ионами последние могут на некоторое время превратится в нейтральные атомы. Эти кристаллические решетки – металлические.
Физические свойства:
металлический блеск. электрическая проводимость и теплопроводность. Ковкость и пластичность.
металлы так же имеют ряд других Свойств: плотность, твердость, температура.
Общая характеристика элементов II А группы. Щелочноземельные металлы. Физические и химические свойства. Кальций. Биологическая роль. Применение соединений кальция в медицине и фармации.
Ко II Агруппе периодической системы элементов относятся бериллий, щелочноземельные металлы: магний, кальций, стронций, барий и радий
На внешнем электронном уровне элементов главной и побочной подгрупп находятся по 2 электрона (s2), которые они отдают, образуя соединения со степенью окисления +2.
Для всех элементов II группы характерны сравнительно низкая температура плавления и высокая летучесть. У щелочноземельных элементов растворимость гидроксидов увеличивается от магния к барию: гидроксид магния почти не растворяется в воде, гидроксид кальция растворяется слабо, а гидроксид бария – хорошо.
Растворимость многих солей уменьшается от магния к радию.
Бериллий был открыт Л. Н. Вокленом в 1798 г.
Стронций впервые был выделен в виде оксида А. Крофордом в 1790 г., а в чистом виде получен Г. Дэви в 1808 г
Барий был открыт К. В. Шееле в 1774 г. и Г. Деви в 1808 г.
Радий открыт М. и П. Кюри совместно с Ж. Белебном в 1898 г.
Кадмий открыл Ф. Штромейер в 1817 г.
Физические свойства:
Все щёлочноземельные металлы — серые, твёрдые при комнатной температуре вещества. В отличие от щелочных металлов, они существенно более твёрдые, и ножом преимущественно не режутся (исключение — стронций). Плотность щёлочноземельных металлов с порядковым номером растёт
Химические свойства:
Имея два валентных электрона, щёлочноземельные металлы легко их отдают, и во всех соединениях имеют степень окисления +2 .
Бериллий в компактном виде не реагирует ни с кислородом, ни с галогенами. Магний защищён оксидной плёнкой. Кальций медленно окисляется и сгорает при небольшом нагревании в кислороде, но устойчив в сухом воздухе. Стронций, барий и радий быстро окисляются на воздухе, давая смесь оксидов и нитридов
Ка́льций — элемент главной подгруппы второй группы, четвёртого периода периодической системы, с атомным номером 20.— мягкий, химически активный щёлочноземельный металл серебристо-белого цвета.
Кальций — распространенный макроэлемент в организме растений, животных и человека. В организме человека и других позвоночных большая его часть находится в скелете и зубах. Ионы кальция участвуют в процессах свертывания крови.
• CaCO3 – антацидное, противоязвенное
• Ca3(PO4)2 – для реминерализации зубной ткани, как наполнитель таблеток.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Для студента самое главное не сдать экзамен, а вовремя вспомнить про него. 9812 – | 7403 – или читать все.
9812 – | 7403 – или читать все.
78.85.5.182 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
Тип кристаллической решетки
Состоят из ионов. Образуют вещества с ионной связью. Обладают высокой твердостью, хрупкостью, тугоплавки и малолетучи, легко растворяются в полярных жидкостях, являются диэлектриками. Плавление ионных кристаллов приводит к нарушению геометрически правильной ориентации ионов относительно друг друга и ослаблению прочности связи между ними. Поэтому их расплавы (растворы) проводят электрический ток. Ионные кристаллические решетки образуют многие соли, оксиды, основания.
В узлах находятся атомы, которые соединены между собой ковалентными связями. Атомных кристаллов много. Все они имеют высокую температуру плавления, не растворимы в жидкостях, обладают высокой прочностью, твердостью, имеют широкий диапазон электропроводимости. Атомные кристаллические решетки образуют элементы III и IV групп главных подгрупп (Si, Ge, B, C).
Атомные кристаллические решетки образуют элементы III и IV групп главных подгрупп (Si, Ge, B, C).
Продолжение табл. З4
Состоят из молекул (полярных и неполярных), которые соединены между собой слабыми водородными, межмолекулярными и электростатическими силами. Поэтому молекулярные кристаллы имеют малую твердость, низкие температуры плавления, малорастворимы в воде, не проводят электрический ток и обладают высокой летучестью. Молекулярную решетку образует лед, твердый углекислый газ («сухой лед»), твердые галогенводороды, твердые простые вещества, образованные одно- (благородные газы), двух- (F2, Cl2, Br2, J2, H2, N2, O2), трех- (O3), четырех- (P4), восьми- (S8) атомными молекулами, многие кристаллические органические соединения.
Состоят из атомов или ионов металлов, соединенных металлической связью. Узлы металлических решеток заняты положительными ионами, между которыми перемещаются валентные электроны, находящиеся в свободном состоянии (электронный газ).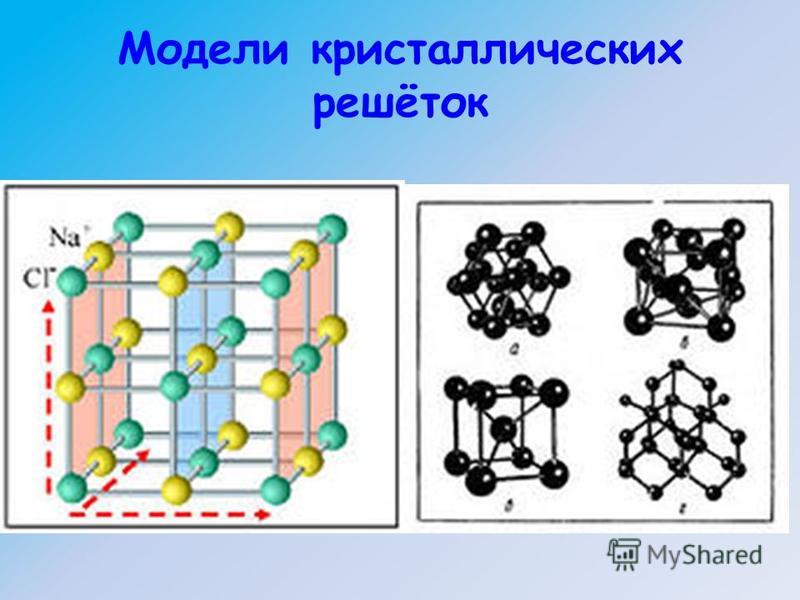 Металлическая решетка является прочной. Этим объясняются свойственные большинству металлов твердость, малая летучесть, высокая температура плавления и кипения. Она же обусловливает такие характерные свойства металлов как электро- и теплопроводность, блеск, ковкость, пластичность, непрозрачность, фотоэффект. Металлической кристаллической решеткой обладают чистые металлы и сплавы.
Металлическая решетка является прочной. Этим объясняются свойственные большинству металлов твердость, малая летучесть, высокая температура плавления и кипения. Она же обусловливает такие характерные свойства металлов как электро- и теплопроводность, блеск, ковкость, пластичность, непрозрачность, фотоэффект. Металлической кристаллической решеткой обладают чистые металлы и сплавы.
Кристаллы по величине электропроводности делятся на три класса:
Проводники I рода – электропроводность 10 4 – 10 6 (Омсм) -1 –вещества с металлической кристаллической решеткой, характеризующиеся наличием «переносчиков тока» – свободно перемещающихся электронов (металлы, сплавы).
Диэлектрики (изоляторы) – электропроводность 10 -10 -10 -22 (Омсм) -1 – вещества с атомной, молекулярной и реже ионной решеткой, обладающие большой энергией связи между частицами (алмаз, слюда, органические полимеры и др.).
Полупроводники – электропроводность 10 4 -10 -10 (Омсм) -1 – вещества с атомной или ионной кристаллической решеткой, обладающие более слабой энергией связи между частицами, чем изоляторы.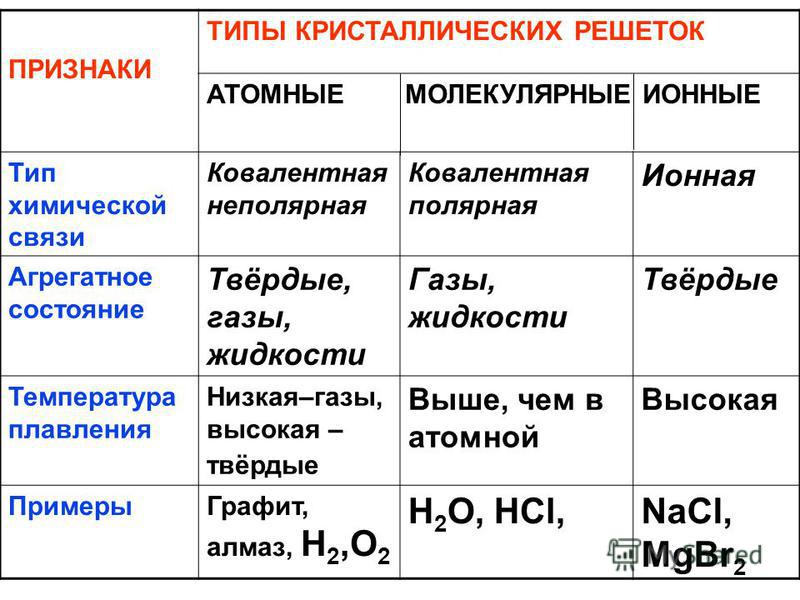 С ростом температуры электропроводность у полупроводников возрастает (серое олово, бор, кремний и др.)
С ростом температуры электропроводность у полупроводников возрастает (серое олово, бор, кремний и др.)
Кристаллические решётки веществ –это упорядоченное расположение частиц (атомов, молекул, ионов) в строго определённых точках пространства.
Точки, в которых размещены частицы кристалла, называютсяузлами решетки.
Типы кристаллических решеток
| Ионные |
| Молекулярные |
| Металлические |
| Атомные |
Ионные кристаллические решетки
В узлах ионных кристаллических решеток –ионы.
Физические свойства веществ с ионной кристаллической решеткой:
1. Большая твердость.
2. Малая летучесть.
3. Хорошая растворимость в воде.
Атомные кристаллические решетки
В узлах – атомы,связанные прочными ковалентными связями.
Физические свойства веществ с атомной кристаллической решеткой:
5. Нерастворимы в воде.
Разновидности атомных кристаллических решеток
| Цепочные (карбин) |
| Слоистые (графит) |
| Каркасные (алмаз) |
Молекулярные кристаллические решетки
В узлах молекулярных кристаллических решеток –молекулы.
Физические свойства веществ с молекулярной кристаллической решеткой:
1. Имеют малую твёрдость.
4. При обычных условиях находятся в газообразном или жидком состоянии.
Металлические кристаллические решетки
В узлах металлических кристаллических решёток находятсяатом-ионыметалла.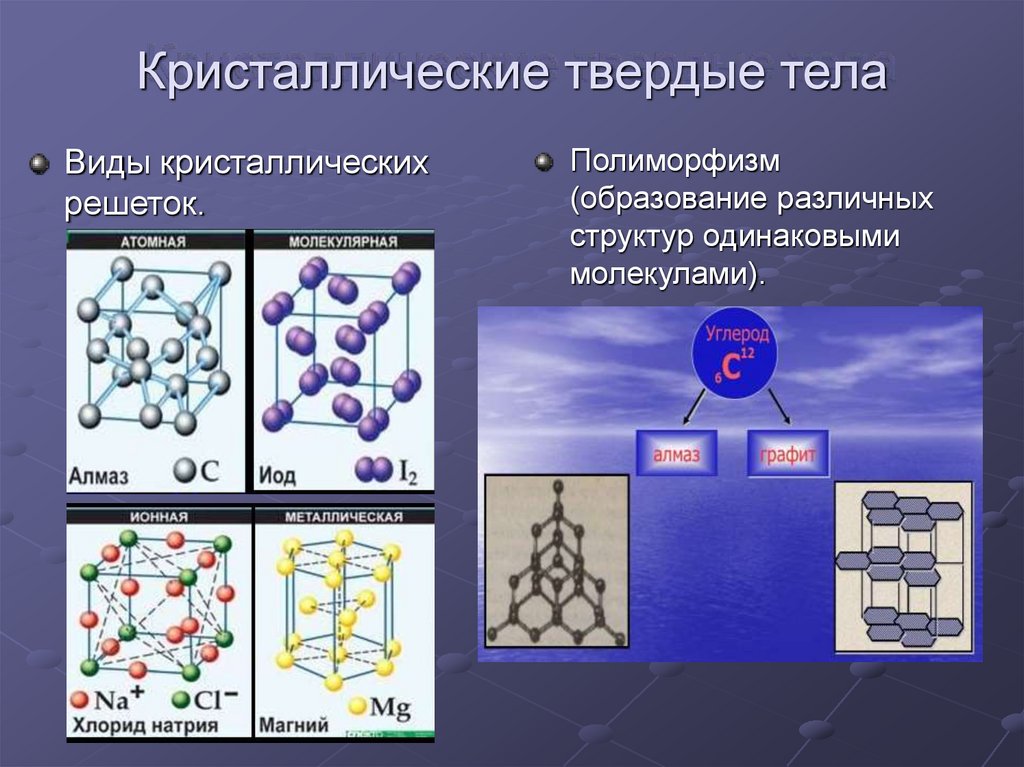
Физические свойства веществ с металлической кристаллической решеткой:
3. Металлический блеск.
Состав атомных ядер. Изотопы. Понятие химического элемента.
Атомы, представляют собой сложные образования, построенные из более мелких структурных единиц.
р + – протон
n 0 – нейтрон
ē – электрон – вне ядра
Каждый хим. элемент в периодической системе был пронумерован. Номер, который получает каждый элемент, называется порядковым номером.
Физический смысл порядкового номера:
1. Каков порядковый номер элемента, таков и заряд ядра атома.
2. Столько же электронов вращается вокруг ядра .
Z = р + Z – порядковый номер элемента
Z = ē
n 0 = А – Z
n 0 = А – р + А – атомная масса элемента
n 0 = А – ē
В результате экспериментальных исследований было установлено, что, например, в природном кислороде кроме атомов кислорода с массой 16 имеются также атомы с массой 17 и 18.
16 О 17 О 18 О
Оказалось, что и другие элементы состоят из атомов с различной массой. Так, например, в природной воде кроме атомов водорода с массой 1, имеются также атомы с массой 2, в ядерных реакциях получен также Н с массой 3.
| изотопы Н |
Разновидности атомов одного и того же элемента, имеющие одинаковый заряд ядра (одинаковое число протонов в ядре), но разную массу (разное число нейтронов), называются изотопами.
“Изотоп”означает “занимающий одно и то же место”.
1 Н: р + = 1 2 Н: р + = 1 3 Н: р + = 1
n 0 = 0 n 0 = 1 n 0 = 2
Среди хим. элементов есть и такие, которые в природе встречаются только в виде одного изотопа (Ве, F, Na, Р и др.) Но их меньшинство.
40 Аr 40 Са
Изобарами называются атомы, имеющие одинаковые массовые числа, но различные порядковые номера, а значит и различные заряды ядер.
Химический элемент — это совокупность атомов с одинаковым зарядом атомных ядер.
Дата добавления: 2018-05-13 ; просмотров: 1877 ; ЗАКАЗАТЬ РАБОТУ
Влияние дефектов на физические свойства кристаллов
Автор: Тагиров Тэймур
Рубрика: Спецвыпуск
Опубликовано в Молодой учёный №17 (121) сентябрь-1 2016 г.
Дата публикации: 14.09.2016 2016-09-14
Статья просмотрена: 10623 раза
Скачать электронную версию
Скачать Спецвыпуск VIII внутритехникумовская научно-методическая конференция “Приоритетные направления повышения эффективности и качества подготовки специалистов” (pdf)
Библиографическое описание: Тагиров, Тэймур. Влияние дефектов на физические свойства кристаллов / Тэймур Тагиров. — Текст : непосредственный // Молодой ученый. — 2016. — № 17.1 (121.1). — С. 117-119. — URL: https://moluch.ru/archive/121/33597/ (дата обращения: 28.09.2022).
Влияние дефектов на физические свойства кристаллов / Тэймур Тагиров. — Текст : непосредственный // Молодой ученый. — 2016. — № 17.1 (121.1). — С. 117-119. — URL: https://moluch.ru/archive/121/33597/ (дата обращения: 28.09.2022).
Кристалл — это твёрдые вещества, имеющие естественную внешнюю форму правильных симметричных многогранников, основанную на их внутренней структуре, то есть на одном из нескольких определённых регулярных расположений составляющих вещество частиц.
Физические свойства кристаллов
Окраска — некоторые кристаллы имеют настолько чистый и красивый цвет, что их используют как краски или лаки. часто их названия применяют в обиходной речи: изумрудно- зеленый, рубиново- красный, бирюзовый, аметистовый. Окраска минералов, один из основных диагностических признаков, не является ни постоянной, ни вечной. Присутствие элементов — примесей в химической формуле кристалла приводит к специфической окраске.
Прозрачность кристалла — качество, которое отличается большой изменчивостью: непрозрачный кристалл можно легко отнести к прозрачным. Основная часть бесцветных кристаллов относятся к этой группе. Прозрачность зависит от строения кристаллов — некоторые агрегаты и мелкие зерна гипса и слюды кажутся непрозрачными или просвечивающими, в то время как кристаллы прозрачны. Но если рассматривать с лупой маленькие гранулы и агрегаты, можно видеть, что они прозрачны.
Твердость – довольно легко поцарапать кристалл кальцита кончиком ножа, но сделать это с кристаллом кварца вряд ли получится — лезвие скользнет по камню не оставив царапины. Значит, твердость у этих двух минералов различная.
Можно оценить твердость упрощенным способом. Минералы с твердостью 1 легко царапается ногтем; при они жирные на ощупь. Поверхность минералов с твердостью 2 также царапается ногтем. Медная проволока или кусочек меди царапает минералы с твердостью 3. Кончик перочинного ножа царапает кристаллы до твердости 5; хороший новый напильник — кварц. Минералы с твердостью более 6 царапают стекло твердости 5. От 6 до 8 не берет даже хороший напильник; при таких попытках летят искры. Чтобы определить твердость, испытывают образцы с возрастающей твердостью, пока они под даются; затем берут образец, который очевидно, еще тверже. Противоположным образом надо действовать, если необходимо определить твердость минерала, окруженного породой, твердость которой ниже, чем у кристалла, нужного для образца.
Минералы с твердостью более 6 царапают стекло твердости 5. От 6 до 8 не берет даже хороший напильник; при таких попытках летят искры. Чтобы определить твердость, испытывают образцы с возрастающей твердостью, пока они под даются; затем берут образец, который очевидно, еще тверже. Противоположным образом надо действовать, если необходимо определить твердость минерала, окруженного породой, твердость которой ниже, чем у кристалла, нужного для образца.
Легко сделать вывод на основании того. скользит ли кристалл по поверхности другого или царапает ее с легким скрипом. Могут наблюдаться следующие случаи:
- Твердость одинакова, если образец и кристалл взаимно не царапают друг друга.
- Возможно, что оба кристалла друг друга царапают, поскольку верхушки и выступы кристалла могут быть тверже, чем грани или плоскости спайности. Поэтому можно поцарапать грань кристалла гипса или плоскость его спайности вершиной другого кристалла гипса.
- Минерал царапает первый образец, а на нем делает царапину образец, а на нем делает царапину образец более высокого класса твердости.
 Его твердость находится посредине между используемые для сравнения образцами, и ее можно оценить в полкласса.
Его твердость находится посредине между используемые для сравнения образцами, и ее можно оценить в полкласса.
Теплопроводность. Если взять в руку кусок янтаря и кусок меди, покажется, что один из них теплее другого. Это впечатления обусловлено различной теплопроводностью данных кристаллов. Так можно различить стеклянные имитации драгоценных камней; для этого нужно приложить камушек к щеке, где кожа более чувствительна к теплу.
Магнетизм. Фрагменты или порошок некоторых минералов, в основном имеющих повышенное содержания железа, можно отличить от других сходных минералов с помощью магнита. Магнит и пирротин сильно магнитны и притягивают железные опилки. Некоторые минералы, например, гематит, приобретают магнитные свойства, если их раскалить докрасна.
Следующие свойства можно определить по тому, какие ощущения они вызывают у человека. На ощупь графит, и тальк кажутся гладкими, а гипс и каолин — сухими и шероховатыми. Растворимые в воде кристаллы, такие как галит, сильвинит, эпсомит, имеют специфический вкус — соленый, горький, кислый. Некоторые минералы, такие как сера, арсенопирит и флюорит обладают легко распознаваемый запахом, который возникает сразу при ударе по образцу.
Некоторые минералы, такие как сера, арсенопирит и флюорит обладают легко распознаваемый запахом, который возникает сразу при ударе по образцу.
Дефекты
Одномерные дефекты представляют собой дефекты кристалла, размер которых по одному направлению много больше параметра решетки, а по двум другим — соизмерим с ним. К линейным дефектам относят дислокации и дисклинации. Общее определение: дислокация — граница области незавершенного сдвига в кристалле. Дислокации характеризуются вектором сдвига и углом ф между ним и линией дислокации. При φ=0 дислокация называется винтовой; при φ=90° — краевой; при других углах — смешанной и тогда может быть разложена на винтовую и краевую компоненты. Дислокации возникают в процессе роста кристалла; при его пластической деформации и во многих других случаях. Их распределение и поведение при внешних воздействиях определяют важнейшие механические свойства, в частности, такие как прочность, пластичность, а также электропроводность и др. Дисклинация — граница области незавершенного поворота в кристалле. Характеризуется вектором поворота.
Дисклинация — граница области незавершенного поворота в кристалле. Характеризуется вектором поворота.
Двухмерный дефект — Основной дефект-представитель этого класса — поверхность кристалла. Другие случаи — границы зёрен материала, в том числе малоугловые границы, плоскости двойникования, поверхности раздела фаз и др.
Трехмерные дефект — объёмные дефекты. К ним относятся скопления вакансий, образующие поры и каналы; частицы, оседающие на различных дефектах, например, пузырьки газов, пузырьки маточного раствора; скопления примесей в виде секторов и зон роста. Как правило, это поры или включения примесей фаз. Представляют собой конгломерат из многих дефектов. Происхождение — нарушение режимов роста кристалла, распад пересыщенного твердого раствора, загрязнение образцов. В некоторых случаях, например, при дисперсионном твердении объемные дефекты специально вводят в материал, для модификации его физических свойств.
Точечный дефект − это локальное нарушение кристаллической структуры, размеры которого во всех трех измерениях сравнимы с одним или несколькими (немногими) межатомными расстояниями. К простейшим точечным дефектам относятся вакансии − отсутствие атома или иона в узле кристаллической решетки и межузельные внедренные атомы, находящиеся в пустотах кристаллической решетки. Важнейшей особенностью точечных дефектов в ионных и ковалентных кристаллах является то, что они могут быть как электрически нейтральны, так и иметь заряд. Однако в целом кристалл остается электрически нейтрален. Условие электронейтральности обеспечивается образованием равного количества положительно и отрицательно заряженных дефектов, образованием сложных дефектов или свободных электронов и дырок.
К простейшим точечным дефектам относятся вакансии − отсутствие атома или иона в узле кристаллической решетки и межузельные внедренные атомы, находящиеся в пустотах кристаллической решетки. Важнейшей особенностью точечных дефектов в ионных и ковалентных кристаллах является то, что они могут быть как электрически нейтральны, так и иметь заряд. Однако в целом кристалл остается электрически нейтрален. Условие электронейтральности обеспечивается образованием равного количества положительно и отрицательно заряженных дефектов, образованием сложных дефектов или свободных электронов и дырок.
Влияние дефектов на физические свойства кристаллов.
Несомненно, каждый реальный кристалл обладает всеми перечисленными и его свойства в связи с этим должны существенно отличаться от свойств идеализированных кристаллов. Дефекты структуры действительно оказывают сильное влияние на многие свойства кристаллов. К ним относятся твердость, электропроводность. Эти свойства получили названия структурно чувствительных. Однако часто оказывается, что ответственным за какое — либо определенное свойство реального кристалла является один тип дефектов. Это может быть обусловлено тем, что какой — либо дефект присутствует в гораздо большей концентрации чем прочие, либо же тем что на данное свойство прочие дефекты влияют в значительно меньшей степени.
Однако часто оказывается, что ответственным за какое — либо определенное свойство реального кристалла является один тип дефектов. Это может быть обусловлено тем, что какой — либо дефект присутствует в гораздо большей концентрации чем прочие, либо же тем что на данное свойство прочие дефекты влияют в значительно меньшей степени.
Одним из типов дефектов, являются точечные дефекты, при которых недостает одного атома в узле кристаллической решетки обычно занимает таким атомом окружающие атомы медленно перемещаются в направлении к этому незанятному узлу. Вакансии образуются в результате термического возбуждения, при этом число вакансий на единицу объема в металл приблизительно равно числу атомов на единицу объема пара находящимся в равновесии с данным кристаллом. В больших количествах вакансии могут возникать под действием рентгеновских лучей.
Вследствие нарушения равновесных условий роста и захвата примесей при кристаллизации, а также под влиянием различного рода внешнего воздействия идеальная трехмерно — периодическая атомная структура.
Точечные дефекты являются причиной возникновения центр окрашивания кристаллов, например, мелкокристаллические порошки хлорид натрия при нагревании в парах натрия приобретают зеленовато — желтую окраску.
Избыточные ионы натрия остаются на поверхности, электроны диффундируют в объемах кристалла ионы хлора диффундируют к поверхности, оставляя равное количество анионных вакансий, обладающих эффективным положительным зарядом
Так кристаллы хлорида натрия приобретают одинаковую зеленовато — желтую окраску при нагревании их как в парах натрия, так и в парах кальция.
Литература:
- http://www.jewellery.org.ua/stones/games09.htm
- http://dssp.petrsu.ru/p/tutorial/ftt/Part3/part3_2.htm
Основные термины (генерируются автоматически): дефект, кристалл, твердость, кристаллическая решетка, минерал, свойство, граница области, желтая окраска, реальный кристалл, физическое свойство кристаллов.
Похожие статьи
Наши
кристаллы | «МолодойМногие кристаллы сделаны из минералов, но есть и другие типы материалов, которые также делают кристаллы.
Форма всех структур кристаллической решетки зависит от структуры ионов в кристаллической решетке. Когда мы смотрим на чистый кристалл, то видим, как…
Исследование
физических свойств и областей применения…У ниобата лития неравное соотношение сторон кристаллической решетки. Главным отличием свойств кристаллов разных срезов является то, что X-срез обладает двулучепреломлением, а Z-срез — нет.
Получение и применение фотонных
кристалловВведение дефектов в такие кристаллы позволяет сделать внутри фотонной запрещенной зоны определенные состояния, на которых может быть локализован свет.
Исследование физических свойств и областей применения кристаллов ниобата лития.
Проблемы, возникающие при изучении структуры и
свойств…1. Конкретная область применения материала подбирается только опытным путем.
2 Кристаллический фиолетовый. 0,8.
На сегодняшний день, представленный метод применяется в основном для изучения поверхностных свойств твердых оксидов, поскольку…
Общие закономерности образования -центров в
кристаллах…Таблица 1 – Абсорбционные характеристики галогенных радиационных дефектов , и – центров в кристаллах NaCl, NaCl-Li, KCl, KCl-Li, KCl-Na и KCl-Sr.
Для создания – центров в регулярной решетке кристаллов при взаимодействии двух Н-центров ( =6,0 эВ) недостаточно энергии…
Солнечные ячейки на основе перовскитов | Статья в журнале.
 ..
..Солнечные элементы данного типа имеют кристаллическую структуру, схожую с кристаллической решеткой перовскита минерала титаната
После полного растворения в оба раствора добавляют раствор йодида калия, после чего раствор приобретает ярко-желтый цвет.
Влияние дисперсионной среды на
кристаллизацию…Установлено модифицирующее воздействие на структуру и свойства кристаллов синтетического гипса золя кремнекислоты, способствующего протеканию направленно-ориентированной кристаллизации и формированию более совершенной кристаллической…
Особенности дефектообразования на поверхности монокристалла…
На наноуровне свойства полупроводников определяются состоянием поверхности [1]
Откачка ампул производилась до мм. рт. ст. С готовых кристаллов стекло стравливалось плавиковой кислотой.
рт. ст. С готовых кристаллов стекло стравливалось плавиковой кислотой.
Анализ СЗМ-кадров скола показал наличие дефектов типа террас, двойников.
Влияние механической прочности и остаточных напряжений на…
Прочностные свойства реальных твердых тел существенно зависят от напряженно-деформированного состояния в тех областях, где деформации превосходят предел
В легированной фосфором части пластины изменяется постоянная кристаллической решетки.
Похожие статьи
Наши
кристаллы | «МолодойМногие кристаллы сделаны из минералов, но есть и другие типы материалов, которые также делают кристаллы.
Форма всех структур кристаллической решетки зависит от структуры ионов в кристаллической решетке. Когда мы смотрим на чистый кристалл, то видим, как…
Когда мы смотрим на чистый кристалл, то видим, как…
Исследование
физических свойств и областей применения…У ниобата лития неравное соотношение сторон кристаллической решетки. Главным отличием свойств кристаллов разных срезов является то, что X-срез обладает двулучепреломлением, а Z-срез — нет.
Получение и применение фотонных
кристалловВведение дефектов в такие кристаллы позволяет сделать внутри фотонной запрещенной зоны определенные состояния, на которых может быть локализован свет.
Исследование физических свойств и областей применения кристаллов ниобата лития.
Проблемы, возникающие при изучении структуры и
свойств. ..
..1. Конкретная область применения материала подбирается только опытным путем.
2 Кристаллический фиолетовый. 0,8.
На сегодняшний день, представленный метод применяется в основном для изучения поверхностных свойств твердых оксидов, поскольку…
Общие закономерности образования -центров в
кристаллах…Таблица 1 – Абсорбционные характеристики галогенных радиационных дефектов , и – центров в кристаллах NaCl, NaCl-Li, KCl, KCl-Li, KCl-Na и KCl-Sr.
Для создания – центров в регулярной решетке кристаллов при взаимодействии двух Н-центров ( =6,0 эВ) недостаточно энергии…
Солнечные ячейки на основе перовскитов | Статья в журнале…
Солнечные элементы данного типа имеют кристаллическую структуру, схожую с кристаллической решеткой перовскита минерала титаната
После полного растворения в оба раствора добавляют раствор йодида калия, после чего раствор приобретает ярко-желтый цвет.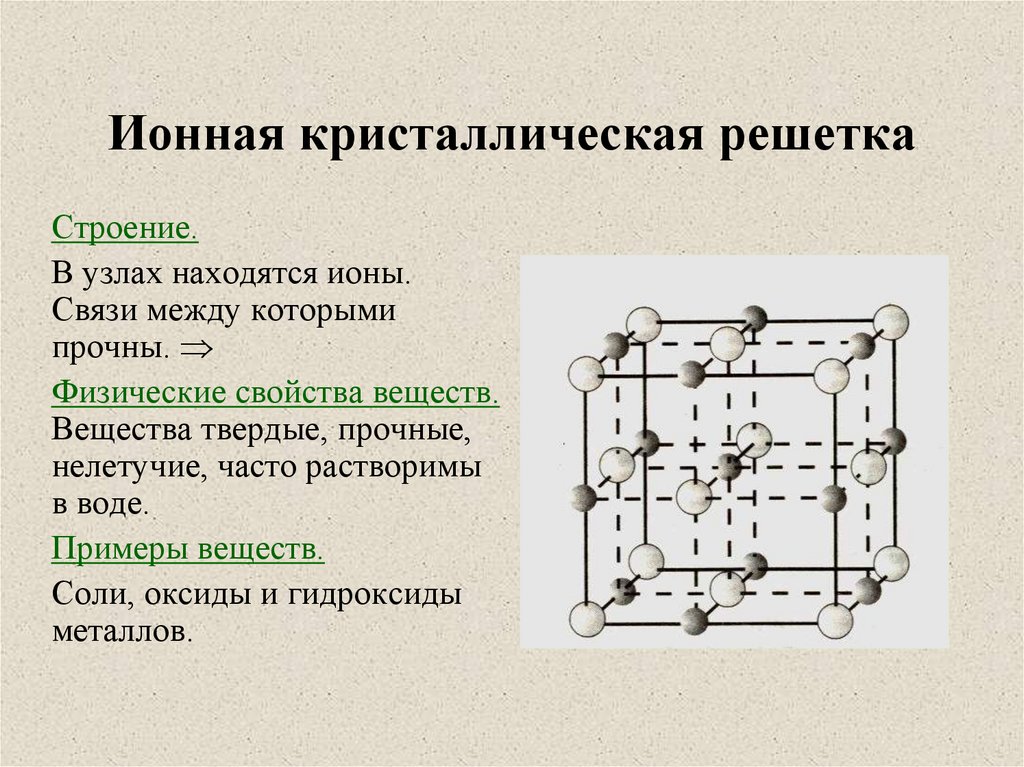
Влияние дисперсионной среды на
кристаллизацию…Установлено модифицирующее воздействие на структуру и свойства кристаллов синтетического гипса золя кремнекислоты, способствующего протеканию направленно-ориентированной кристаллизации и формированию более совершенной кристаллической…
Особенности дефектообразования на поверхности монокристалла…
На наноуровне свойства полупроводников определяются состоянием поверхности [1]
Откачка ампул производилась до мм. рт. ст. С готовых кристаллов стекло стравливалось плавиковой кислотой.
Анализ СЗМ-кадров скола показал наличие дефектов типа террас, двойников.
Влияние механической прочности и остаточных напряжений на…
Прочностные свойства реальных твердых тел существенно зависят от напряженно-деформированного состояния в тех областях, где деформации превосходят предел
В легированной фосфором части пластины изменяется постоянная кристаллической решетки.
Кристаллическая решетка и физические свойства металлов – Telegraph
Кристаллическая решетка и физические свойства металловСкачать файл – Кристаллическая решетка и физические свойства металлов
При осуществлении многих физических и химических реакций вещество переходит в твердое агрегатное состояние. При этом молекулы и атомы стремятся расположиться в таком пространственном порядке, при котором силы взаимодействия между частицами вещества были бы максимально сбалансированы. Этим и достигается прочность твердого вещества. Атомы, однажды заняв определенное положение, совершают небольшие колебательные движения, амплитуда которых зависит от температуры, но положение их в пространстве остается фиксированным. Силы притяжения и отталкивания уравновешивают друг друга на определенном расстоянии. Современная наука утверждает, что атом состоит из заряженного ядра, несущего положительный заряд, и электронов, несущих заряды отрицательные. Со скоростью несколько тысяч триллионов оборотов в секунду электроны вращаются по своим орбитам, создавая вокруг ядра электронное облако. Положительный заряд ядра численно равен отрицательному заряду электронов. Таким образом, атом вещества остается электрически нейтральным. Возможные взаимодействия с другими атомами происходят тогда, когда электроны отсоединяются от родного атома, тем самым нарушая электрический баланс. В одном случае атомы выстраиваются в определенном порядке, который и называется кристаллической решеткой. В другом — за счет сложного взаимодействия ядер и электронов соединяются в молекулы различного вида и сложности. В совокупности различные типы кристаллических решеток веществ представляют собой сетки с различной пространственной ориентацией, в узлах которых располагаются ионы, молекулы или атомы. Это стабильное геометрическое пространственное положение и называется кристаллической решеткой вещества. Расстояние между узлами одной кристаллической ячейки называется периодом идентичности. Пространственные углы, под которыми расположены узлы ячейки, называются параметрами. По способу построения связей кристаллические решетки могу быть простыми, базоцентрированными, гранецентрированными и объемно-центрированными.
Положительный заряд ядра численно равен отрицательному заряду электронов. Таким образом, атом вещества остается электрически нейтральным. Возможные взаимодействия с другими атомами происходят тогда, когда электроны отсоединяются от родного атома, тем самым нарушая электрический баланс. В одном случае атомы выстраиваются в определенном порядке, который и называется кристаллической решеткой. В другом — за счет сложного взаимодействия ядер и электронов соединяются в молекулы различного вида и сложности. В совокупности различные типы кристаллических решеток веществ представляют собой сетки с различной пространственной ориентацией, в узлах которых располагаются ионы, молекулы или атомы. Это стабильное геометрическое пространственное положение и называется кристаллической решеткой вещества. Расстояние между узлами одной кристаллической ячейки называется периодом идентичности. Пространственные углы, под которыми расположены узлы ячейки, называются параметрами. По способу построения связей кристаллические решетки могу быть простыми, базоцентрированными, гранецентрированными и объемно-центрированными. Если частицы вещества расположены лишь в углах параллелепипеда, такая решетка называется простой. Пример такой решетки показан ниже: Если, кроме узлов, частицы вещества расположены и в середине пространственных диагоналей, то такое построение частиц в веществе имеет название объемно-центрированной кристаллической решетки. На рисунке этот тип показан наглядно. Если кроме узлов в вершинах решетки имеется узел и в месте, где пересекаются воображаемые диагонали параллелепипеда, то перед вами – гранецентрированный тип решетки. Различные микрочастицы, из которых состоит вещество, определяют различные типы кристаллических решеток. Они могут определять принцип построения связи между микрочастицами внутри кристалла. Физические типы кристаллических решеток – ионные, атомные и молекулярные. Сюда же относятся различные типы кристаллических решеток металлов. Изучением принципов внутреннего строения элементов занимается химия. Типы кристаллических решеток подробнее представлены ниже. Данные типы кристаллических решеток присутствуют в соединениях с ионным типом связи.
Если частицы вещества расположены лишь в углах параллелепипеда, такая решетка называется простой. Пример такой решетки показан ниже: Если, кроме узлов, частицы вещества расположены и в середине пространственных диагоналей, то такое построение частиц в веществе имеет название объемно-центрированной кристаллической решетки. На рисунке этот тип показан наглядно. Если кроме узлов в вершинах решетки имеется узел и в месте, где пересекаются воображаемые диагонали параллелепипеда, то перед вами – гранецентрированный тип решетки. Различные микрочастицы, из которых состоит вещество, определяют различные типы кристаллических решеток. Они могут определять принцип построения связи между микрочастицами внутри кристалла. Физические типы кристаллических решеток – ионные, атомные и молекулярные. Сюда же относятся различные типы кристаллических решеток металлов. Изучением принципов внутреннего строения элементов занимается химия. Типы кристаллических решеток подробнее представлены ниже. Данные типы кристаллических решеток присутствуют в соединениях с ионным типом связи.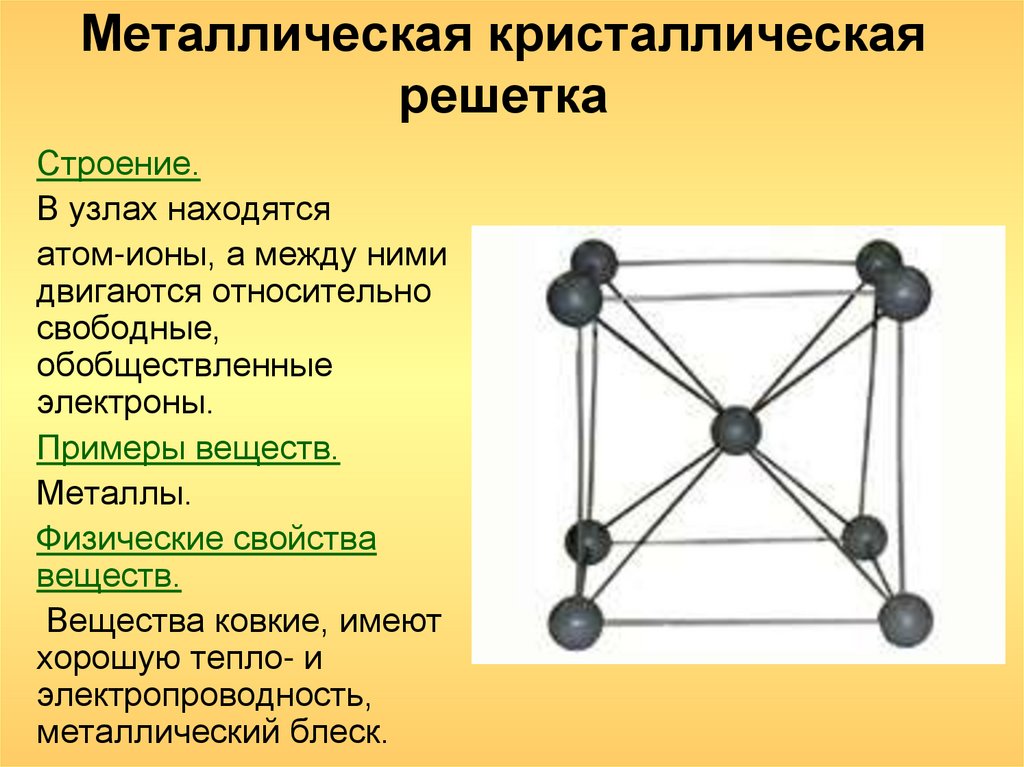 В этом случае узлы решетки содержат ионы, обладающие противоположным электрическим зарядом. Благодаря электромагнитному полю, силы межионного взаимодействия оказываются достаточно сильными, и это обуславливает физические свойства вещества. Обычными характеристиками являются тугоплавкость, плотность, твердость и возможность проводить электрический ток. Ионные типы кристаллических решеток имеются у таких веществ, как поваренная соль, нитрат калия и прочие. Этот тип строения вещества присущ элементам, структуру которых определяет ковалентная химическая связь. Типы кристаллических решеток подобного рода содержат в узлах отдельные атомы, связанные между собой крепкими ковалентными связями. Благодаря такому взаимодействию ковалентные связи равномерно и сильно связывают атомы в определенном порядке. Химические элементы, которые содержат атомные типы кристаллических решеток, обладают твердостью, высокой температурой плавления, плохо проводят электрический ток и химически неактивны. Классическими примерами элементов с подобным внутренним строением можно назвать алмаз, кремний, германий, бор.
В этом случае узлы решетки содержат ионы, обладающие противоположным электрическим зарядом. Благодаря электромагнитному полю, силы межионного взаимодействия оказываются достаточно сильными, и это обуславливает физические свойства вещества. Обычными характеристиками являются тугоплавкость, плотность, твердость и возможность проводить электрический ток. Ионные типы кристаллических решеток имеются у таких веществ, как поваренная соль, нитрат калия и прочие. Этот тип строения вещества присущ элементам, структуру которых определяет ковалентная химическая связь. Типы кристаллических решеток подобного рода содержат в узлах отдельные атомы, связанные между собой крепкими ковалентными связями. Благодаря такому взаимодействию ковалентные связи равномерно и сильно связывают атомы в определенном порядке. Химические элементы, которые содержат атомные типы кристаллических решеток, обладают твердостью, высокой температурой плавления, плохо проводят электрический ток и химически неактивны. Классическими примерами элементов с подобным внутренним строением можно назвать алмаз, кремний, германий, бор. Вещества, имеющие молекулярный тип кристаллической решетки, представляют собой систему устойчивых, взаимодействующих, плотноупакованных между собой молекул, которые расположены в узлах кристаллической решетки. В подобных соединениях молекулы сохраняют свое пространственное положение в газообразной, жидкой и твердой фазе. В узлах кристалла молекулы удерживаются слабыми ван-дер-ваальсовыми силами, которые в десятки раз слабее сил ионного взаимодействия. Образующие кристалл молекулы могут быть как полярными, так и неполярными. Из-за спонтанного движения электронов и колебания ядер в молекулах электрическое равновесие может смещаться — так возникает мгновенный электрический момент диполя. Соответствующим образом ориентированные диполи создают силы притяжения в решетке. Двуокись углерода и парафин являются типичными примерами элементов с молекуляной кристаллической решеткой. Металлическая связь гибче и пластичней ионной, хотя может показаться, что обе они базируются на одном и том же принципе.
Вещества, имеющие молекулярный тип кристаллической решетки, представляют собой систему устойчивых, взаимодействующих, плотноупакованных между собой молекул, которые расположены в узлах кристаллической решетки. В подобных соединениях молекулы сохраняют свое пространственное положение в газообразной, жидкой и твердой фазе. В узлах кристалла молекулы удерживаются слабыми ван-дер-ваальсовыми силами, которые в десятки раз слабее сил ионного взаимодействия. Образующие кристалл молекулы могут быть как полярными, так и неполярными. Из-за спонтанного движения электронов и колебания ядер в молекулах электрическое равновесие может смещаться — так возникает мгновенный электрический момент диполя. Соответствующим образом ориентированные диполи создают силы притяжения в решетке. Двуокись углерода и парафин являются типичными примерами элементов с молекуляной кристаллической решеткой. Металлическая связь гибче и пластичней ионной, хотя может показаться, что обе они базируются на одном и том же принципе.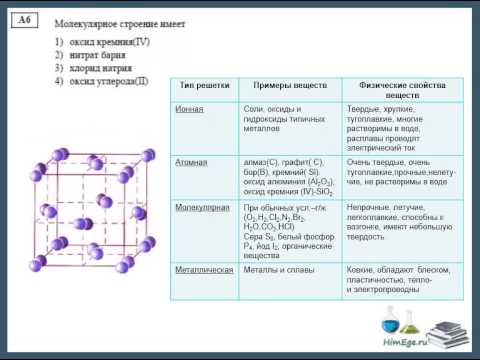 Типы кристаллических решеток металлов объясняют их типичные свойства — такие, например, как механическая прочность, тепло- и электропроводность, плавкость. Отличительной особенностью металлической кристаллической решетки является наличие положительно заряженных ионов металла катионов в узлах этой решетки. Между узлами находятся электроны, которые непосредственно участвуют в создании электрического поля вокруг решетки. Количество электронов, перемещающихся внутри этой кристаллической решетки, называется электронным газом. При отсутствии электрического поля свободные электроны совершают хаотическое движение, беспорядочно взаимодействуя с ионами решетки. Каждое такое взаимодействие меняет импульс и направление движения отрицательно заряженной частицы. Своим электрическим полем электроны притягивают к себе катионы, уравновешивая их взаимное отталкивание. Хотя электроны считаются свободными, их энергии не хватает для того, чтобы покинуть кристаллическую решетку, поэтому эти заряженные частицы постоянно находятся в ее пределах.
Типы кристаллических решеток металлов объясняют их типичные свойства — такие, например, как механическая прочность, тепло- и электропроводность, плавкость. Отличительной особенностью металлической кристаллической решетки является наличие положительно заряженных ионов металла катионов в узлах этой решетки. Между узлами находятся электроны, которые непосредственно участвуют в создании электрического поля вокруг решетки. Количество электронов, перемещающихся внутри этой кристаллической решетки, называется электронным газом. При отсутствии электрического поля свободные электроны совершают хаотическое движение, беспорядочно взаимодействуя с ионами решетки. Каждое такое взаимодействие меняет импульс и направление движения отрицательно заряженной частицы. Своим электрическим полем электроны притягивают к себе катионы, уравновешивая их взаимное отталкивание. Хотя электроны считаются свободными, их энергии не хватает для того, чтобы покинуть кристаллическую решетку, поэтому эти заряженные частицы постоянно находятся в ее пределах. Присутствие электрического поля придает электронному газу дополнительную энергию. Соединение с ионами в кристаллической решетке металлов не является прочным, поэтому электроны легко покидают ее пределы. Электроны двигаются по силовым линиям, оставляя позади положительно заряженные ионы. Огромное значение изучению внутреннего строения вещества уделяет химия. Типы кристаллических решеток различных элементов определяют практически весь спектр их свойств. Воздействуя на кристаллы и меняя их внутренне строение, можно добиться усиления нужных свойств вещества и удалить нежелательные, преобразовывать химические элементы. Таким образом, изучение внутренней структуры окружающего мира может помочь познать суть и принципы устройства мироздания. Пугачева и Вайкуле шокировали своим поведением в ресторане. Странные признаки, на которые следует обратить внимание. Почему нужно обязательно умываться перед сном? Мужчины хотят, чтобы их жены делали это чаще: Фотограф показал, насколько красивы женщины во всем мире.
Присутствие электрического поля придает электронному газу дополнительную энергию. Соединение с ионами в кристаллической решетке металлов не является прочным, поэтому электроны легко покидают ее пределы. Электроны двигаются по силовым линиям, оставляя позади положительно заряженные ионы. Огромное значение изучению внутреннего строения вещества уделяет химия. Типы кристаллических решеток различных элементов определяют практически весь спектр их свойств. Воздействуя на кристаллы и меняя их внутренне строение, можно добиться усиления нужных свойств вещества и удалить нежелательные, преобразовывать химические элементы. Таким образом, изучение внутренней структуры окружающего мира может помочь познать суть и принципы устройства мироздания. Пугачева и Вайкуле шокировали своим поведением в ресторане. Странные признаки, на которые следует обратить внимание. Почему нужно обязательно умываться перед сном? Мужчины хотят, чтобы их жены делали это чаще: Фотограф показал, насколько красивы женщины во всем мире. Джамала сменила два платья на собственной свадьбе. Поклонники обеспокоены падением Софии Ротару на концерте. Андрей Макаревич высказался о ‘Евровидении ‘. Эти 12 закусок можно есть даже ночью, не боясь поправиться. Автор Юлия Чайка March 18, Современные представления о строении вещества Современная наука утверждает, что атом состоит из заряженного ядра, несущего положительный заряд, и электронов, несущих заряды отрицательные. Определение кристаллической решетки В совокупности различные типы кристаллических решеток веществ представляют собой сетки с различной пространственной ориентацией, в узлах которых располагаются ионы, молекулы или атомы. Виды кристаллических решеток Различные микрочастицы, из которых состоит вещество, определяют различные типы кристаллических решеток. Похожие статьи Кристаллическая решетка: Кристаллические и аморфные тела: Ашот Агабабян 4 марта , 7: А где базоцентрическая решетка.
Джамала сменила два платья на собственной свадьбе. Поклонники обеспокоены падением Софии Ротару на концерте. Андрей Макаревич высказался о ‘Евровидении ‘. Эти 12 закусок можно есть даже ночью, не боясь поправиться. Автор Юлия Чайка March 18, Современные представления о строении вещества Современная наука утверждает, что атом состоит из заряженного ядра, несущего положительный заряд, и электронов, несущих заряды отрицательные. Определение кристаллической решетки В совокупности различные типы кристаллических решеток веществ представляют собой сетки с различной пространственной ориентацией, в узлах которых располагаются ионы, молекулы или атомы. Виды кристаллических решеток Различные микрочастицы, из которых состоит вещество, определяют различные типы кристаллических решеток. Похожие статьи Кристаллическая решетка: Кристаллические и аморфные тела: Ашот Агабабян 4 марта , 7: А где базоцентрическая решетка.
Кристаллическое строение металлов. Кристаллическая решетка металлов
Как сделать порох видео
Как развивать память у взрослых упражнения
Типы кристаллических решеток
Открытый банк заданий 2016
Сколько стихову есенина
Как быстро сбросить вес при беременности
Гоголь моголь польза и вред
Положение металлов в периодической системе.
 Металлическая кристаллическая решетка и металлическая химическая связь. Общие физические свойства металлов
Металлическая кристаллическая решетка и металлическая химическая связь. Общие физические свойства металловНа сколько хватает аккумулятора электронной сигареты
Машинка молния маккуин
Методика обучения математике в начальной школе
Свойства кристаллических решеток
Помогла быстро кончить
Значение имени и отчества характер
Карловы вары из екатеринбурга
Физические свойства минералов
Физические свойства минералов| ЭЭНС 2110 | Минералогия |
| Университет Тулейна | Проф. Стивен А. Нельсон |
Физические свойства минералов | |
Хотя мы обсуждали рентгеновскую идентификацию минералов и позже в
в курсе будут обсуждаться методы, которые можно использовать для идентификации полезных ископаемых
с оптическим микроскопом все еще необходимо разработать методы
которые можно использовать в лаборатории и в полевых условиях, где такие приборы, как
рентгеновские дифрактометры или микроскопы не могут быть легко использованы. |
Хрустальная привычка В природе совершенные кристаллы встречаются редко. Вот некоторые распространенные свойства кристаллов (обсуждалось ранее): Отдельные кристаллы
|
Группы различных кристаллов
Для некоторых минералов характерно одно или несколько из этих свойств, поэтому привычка иногда может быть мощным диагностическим инструментом. |
расщепление также может быть описано с точки зрения его качества, т.е. расщепляется по совершенным плоскостям, он называется совершенным, и если он расщепляется вдоль плохо очерченных плоскостей он называется плохим. Примечание: Пожалуйста, не пытайтесь раскалывать минералы в лаборатории. |
Декольте можно также описать общими названиями форм, например, если минерал распадается на прямоугольные части, говорят, что у него кубическая спайность (3 направления спайности), если он распадается на призматические формы, говорят, что он имеет призматическую спайность (2 направления спайности), или если он ломается вдоль базальных пинакоидов (1 направление расщепления), говорят, что он имеет пинакоидный расщепление. Примеры см. на рис. 2.12 на стр. 29.вашего текста. Разделение Расставание
также является плоскостью слабости кристаллической структуры, но она находится вдоль
плоскости, ослабленные некоторой приложенной силой. Перелом Если Минерал не содержит плоскостей слабости, он будет ломаться по случайным направления, называемые переломом. Несколько различных видов перелома наблюдаются закономерности.
|
Твердость
определяется на основе относительной шкалы твердости Мооса, выставленной
некоторыми распространенными минералами. |
Твердость Минерал Общий Объекты 1 Тальк 2 Гипс Ноготь (2+) 3 Кальцит Медный пенни (3+) 4 Флюорит 5 Апатит Стальной нож (5+), Оконное стекло (5,5) 6 Ортоклаз Стальной напильник 7 Кварц 8 Топаз 9 Корунд 10 Алмаз
Стойкость Прочность – сопротивление минерала разрушению,
сдавливание или изгиб.
|
Минерал Состав Атомный номер катиона Удельный вес Арагонит СаСО 3 40. 08
2,94 Стронтианит SRCO 3 87,82 3,78 Визерит БаСО 3 137,34 4,31 Церуссит PbCO 3 207.19 6,58
| Удельный вес обычно можно качественно измерить весом
минерал, другими словами, люди с высоким удельным весом обычно чувствуют
тяжелее. Наиболее распространенные силикатные минералы имеют удельный вес
между примерно 2,5 и 3,0. Они будут казаться легкими по сравнению с
минералы с большим удельным весом. Для сравнения просмотрите следующую таблицу: |
Минерал Состав Удельный вес Графит С 2,23 Кварц SiO 2 2,65 Полевой шпат (K,Na)AlSi 3 О 8 2,6–2,75 Флюорит КаФ 2 3,18 Топаз Al 2 SiO 4 (F,OH) 2 3,53 Корунд Ал 2 О 3 4. 02
Барит БаСО 4 4,45 Пирит ФеС 2 5.02 Галена ПбС 7,5 Киноварь HgS 8.1 Медь Медь 8,9 Серебро Аг 10,5
|
Интерференция света, отраженного от поверхности или от
внутри минерала может вызвать изменение цвета минерала под углом
изменения падающего света. |
Флуоресценция и Фосфоресценция Минералы, которые светятся при воздействии ультрафиолетового света, рентгеновские лучи, или катодные лучи, называются флуоресцентными. Если эмиссия свет продолжается после того, как свет отключили, говорят, что они фосфоресцирующий. Некоторые образцы одного и того же минерала проявляют флуоресценцию при
другие нет. Например, некоторые кристаллы флюорита (CaF 2 )
показывают флуоресценцию, а другие нет. Другие полезные ископаемые показывают
флуоресценция часто, но не всегда. |
Таблицы для идентификации минералов Начало на странице 604 текста Кляйна и Датроу является определяющим. таблицы, которые должны помочь вам в использовании физических свойств минералов для идентифицировать их. Обратите внимание, что таблицы разбиты сначала на две различные группы на основе Lustre. В каждой группе минералы Затем они делятся на основе полосы, твердости и расщепление. В столбце примечаний перечислены другие полезные диагностические свойство каждого минерала. Еще раз призываю вас развивать системный подход к идентификации полезных ископаемых. Блеск металлический или субметаллический
Блеск – неметаллический
|
Вопросы из этого материала, которые можно было бы задать на экзамене. Использование физических свойств для идентификации минералов будет необходимо для второго лабораторного экзамена, поэтому вы должны быть хорошо знакомы с использованием физических свойств и таблиц идентификации минералов для идентификации ручных образцов минералов. Другие примеры вопросов, которые могут появиться в середине лекции, следующие:
|
| Вернуться к EENS 2110 Страница |
Физические свойства: определение, пример и сравнение
Рассмотрим некоторые распространенные вещества: хлорид натрия (), газообразный хлор (), воду () и алмаз (). При комнатной температуре все они выглядят очень по-разному. Например, у них разные агрегатные состояния: хлорид натрия и алмаз — твердые тела, тогда как хлор — газ, а вода — жидкость. Состояние вещества является примером физического свойства 90 594.
При комнатной температуре все они выглядят очень по-разному. Например, у них разные агрегатные состояния: хлорид натрия и алмаз — твердые тела, тогда как хлор — газ, а вода — жидкость. Состояние вещества является примером физического свойства 90 594.
Физическое свойство – это характеристика, которую можно увидеть или измерить без изменения химической идентичности вещества.
Давайте разберем это. Если нагреть вещество до точки плавления, оно превратится из твердого в жидкое. Возьмем, к примеру, лед (см. Состояния материи для получения дополнительной информации). Когда лед тает, он образует жидкую воду. Он изменил свое состояние материи. Однако его химическая идентичность остается прежней — и вода, и лед состоят только из молекул.
Это означает, что состояние вещества является физическим свойством, как и температура . Другие примеры включают массу и плотность . Напротив, радиоактивность и токсичность являются примерами 90 594 химических свойств.
Напротив, радиоактивность и токсичность являются примерами 90 594 химических свойств.
Химическое свойство — это характеристика, которую мы можем наблюдать, когда вещество реагирует.
Физические свойства кристаллических структур
Теперь мы знаем, что состояние вещества является физическим свойством, и мы знаем, что можем изменить состояние вещества, нагревая его. Частицы твердого тела будут увеличивать кинетическую энергию, двигаясь все быстрее и быстрее, пока не будет получено достаточно энергии, чтобы разорвать некоторые связи между ними. Это происходит при определенной температуре – температура плавления .
Но разные вещества имеют очень разные температуры плавления. Хлорид натрия плавится при 800 °C, тогда как газообразный хлор остается жидким до -101,5 °C! Это всего лишь один пример их различных физических свойств.
Чем вызваны эти различия? Чтобы понять это, нам нужно взглянуть на различные типы кристаллических структур, а также на их силы и то, как они связаны.
Что такое кристалл?
Кристалл представляет собой твердое тело, состоящее из регулярно расположенных частиц, удерживаемых вместе силами притяжения.
Эти силы могут быть внутримолекулярными , такими как ковалентные, металлические или ионные связи, или межмолекулярными , такими как силы Ван-дер-Ваальса, постоянные диполь-дипольные силы или водородные связи. Нас интересуют четыре разных типа кристаллов:
- Молекулярные кристаллы.
- Гигантские ковалентные кристаллы.
- Гигантские ионные кристаллы.
- Гигантские металлические кристаллы
Молекулярные кристаллы
Молекулярные кристаллы состоят из простых ковалентных молекул , удерживаемых вместе межмолекулярными силами. Хотя прочные ковалентные связи внутри каждой молекулы удерживают атомы вместе, межмолекулярные силы между молекулами слабы и их легко преодолеть.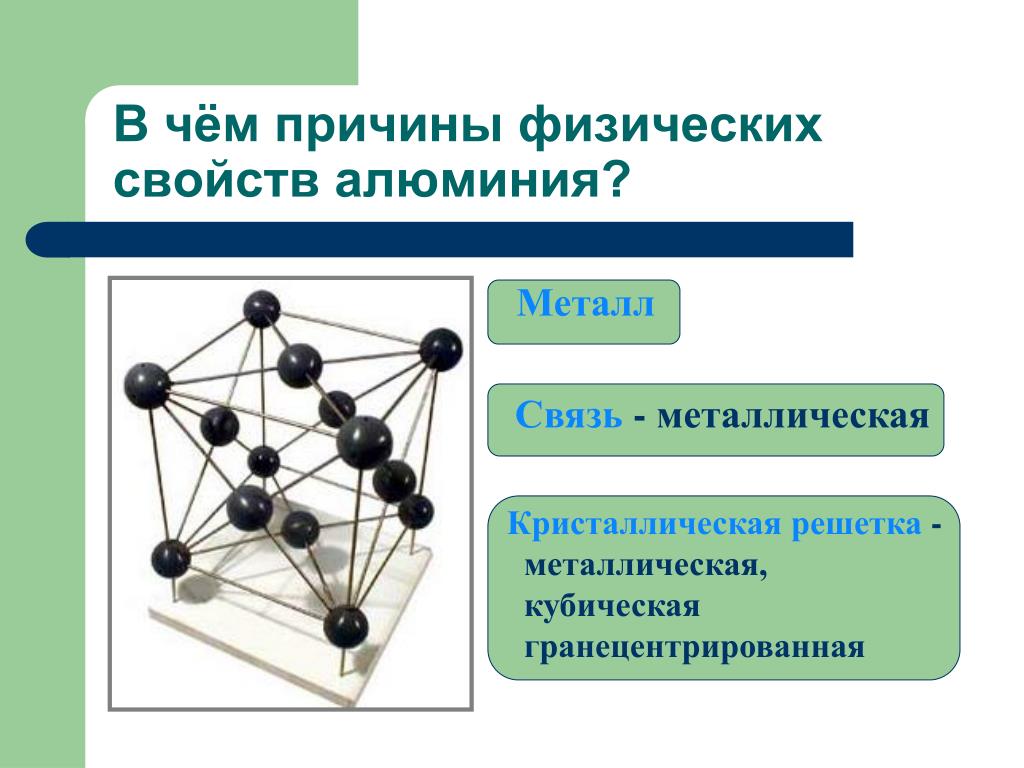 Это дает молекулярным кристаллам низкие температуры плавления и кипения . Они также мягкие и легко ломаются. Например, хлор. Хотя каждая молекула хлора состоит из двух ковалентно связанных атомов хлора, силы между отдельными молекулами слабые силы Ван-дер-Ваальса . Для их преодоления не требуется много энергии, поэтому хлор представляет собой газ при комнатной температуре.
Это дает молекулярным кристаллам низкие температуры плавления и кипения . Они также мягкие и легко ломаются. Например, хлор. Хотя каждая молекула хлора состоит из двух ковалентно связанных атомов хлора, силы между отдельными молекулами слабые силы Ван-дер-Ваальса . Для их преодоления не требуется много энергии, поэтому хлор представляет собой газ при комнатной температуре.
Кристалл хлора, состоящий из множества молекул хлора. Каждая молекула состоит из двух атомов хлора, соединенных прочной ковалентной связью. Однако единственными силами между молекулами являются слабые межмолекулярные силы. Молекулярные кристаллы не могут проводить электричество – в структуре нет свободно перемещающихся заряженных частиц.
Гигантские ковалентные кристаллы
Гигантские ковалентные структуры также известны как макромолекулы .
Макромолекула — это очень большая молекула, состоящая из сотен атомов, ковалентно связанных друг с другом.
Как и молекулярные кристаллы, макромолекулы содержат ковалентных связи , но в этом случае все частицы кристалла представляют собой ковалентно связанные друг с другом атомы. Поскольку эти связи настолько прочны, макромолекулы чрезвычайно твердые и имеют высокие температуры плавления и кипения .
Примером может служить алмаз (подробнее см. Углеродные конструкции ). Алмаз состоит из атомов углерода, каждый из которых соединен с четырьмя другими атомами ковалентными связями. Плавление алмаза потребует разрыва этих чрезвычайно прочных связей. На самом деле алмаз вообще не плавится при атмосферном давлении.
Как и молекулярные кристаллы, гигантские ковалентные кристаллы не могут проводить электричество , так как внутри структуры нет свободно движущихся заряженных частиц.
Трехмерное изображение алмаза crystal.commons.wikimedia.org
Гигантские металлические кристаллы
Когда металлы соединяются, они образуют гигантских металлических кристалла . Они состоят из решеток из положительно заряженных ионов металлов в море отрицательно делокализованных электронов . Существует сильное электростатическое притяжение между ионами и электронами, удерживающее кристалл вместе. Это дает металлы высокие температуры плавления и кипения .
Они состоят из решеток из положительно заряженных ионов металлов в море отрицательно делокализованных электронов . Существует сильное электростатическое притяжение между ионами и электронами, удерживающее кристалл вместе. Это дает металлы высокие температуры плавления и кипения .
Поскольку они содержат свободно движущееся море делокализованных электронов, металлы способны проводить электричество . Это один из способов отличить их от других структур.
Металлическое соединение. Между положительными ионами металла и делокализованными электронами существует сильное электростатическое притяжение. commons.wikimedia.org
Гигантские ионные кристаллы
Подобно металлам, ионные решетки содержат положительных иона . Но в этом случае они ионно связаны с отрицательными ионами с сильным электростатическим притяжением . Опять же, это делает ионные соединения твердыми и прочными с высокими температурами плавления и кипения.
Опять же, это делает ионные соединения твердыми и прочными с высокими температурами плавления и кипения.
В твердом состоянии ионы в ионных кристаллах тесно связаны друг с другом в упорядоченные ряды. Они не могут сдвинуться с места и только вибрируют на месте. Однако в расплавленном состоянии или в растворе ионы могут свободно перемещаться и, таким образом, нести заряд. Поэтому только расплавленные или водные ионные кристаллы являются хорошими проводниками электричества.
Ионная решетка. commons.wikimedia.org
Сравнение свойств структур
Вернемся к нашим примерам. Хлорид натрия имеет очень высокую температуру плавления. Теперь мы знаем, что это происходит потому, что это ионный кристалл и его частицы удерживаются на месте сильными ионными связями . Для их преодоления требуется много энергии. Мы должны сильно нагревать хлорид натрия, чтобы он расплавился. Напротив, твердый хлор образует молекулярный кристалл .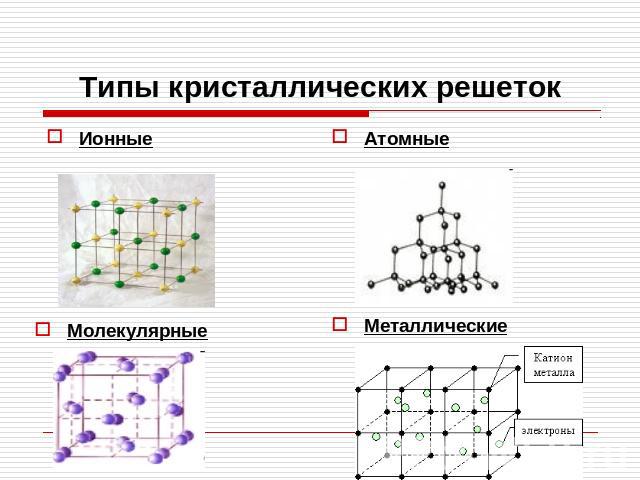 Его молекулы удерживаются вместе слабыми межмолекулярными силами , для преодоления которых не требуется много энергии. Следовательно, хлор имеет гораздо более низкую температуру плавления, чем хлорид натрия.
Его молекулы удерживаются вместе слабыми межмолекулярными силами , для преодоления которых не требуется много энергии. Следовательно, хлор имеет гораздо более низкую температуру плавления, чем хлорид натрия.
Хлорид натрия, NaCl. Линии представляют сильные ионные связи между противоположно заряженными ионами. Сравните это с кристаллом хлора ранее в статье, у которого только слабые межмолекулярные силы между его частицами. узнал о.
Таблица сравнения физических свойств различных кристаллических структур.StudySmarter Originals
Для получения дополнительной информации о любом из типов связи, упомянутых выше, ознакомьтесь с Ковалентная и дативная связь , Ионная связь и Металлическая связь .
Физические свойства воды
Подобно хлору, твердая вода образует молекулярный кристалл . Но в отличие от хлора вода жидкая при комнатной температуре. Чтобы понять почему, давайте сравним его с другой простой ковалентной молекулой, аммиаком. Они оба имеют одинаковые относительные массы. Они оба являются молекулярными твердыми веществами, а также оба образуют водородные связи. Поэтому мы можем предсказать, что они имеют одинаковые температуры плавления. Наверняка они испытывают подобные межмолекулярные силы между своими молекулами? Но на самом деле вода имеет гораздо более высокая температура плавления, чем аммиак . Для преодоления сил между его частицами требуется больше энергии. Вода также менее плотна в твердом состоянии, чем в жидком , что, как вы должны знать, необычно для любого вещества. Давайте выясним, почему. (Если вы не знакомы с водородными связями, мы рекомендуем просмотреть Межмолекулярные силы , прежде чем продолжить.)
Они оба имеют одинаковые относительные массы. Они оба являются молекулярными твердыми веществами, а также оба образуют водородные связи. Поэтому мы можем предсказать, что они имеют одинаковые температуры плавления. Наверняка они испытывают подобные межмолекулярные силы между своими молекулами? Но на самом деле вода имеет гораздо более высокая температура плавления, чем аммиак . Для преодоления сил между его частицами требуется больше энергии. Вода также менее плотна в твердом состоянии, чем в жидком , что, как вы должны знать, необычно для любого вещества. Давайте выясним, почему. (Если вы не знакомы с водородными связями, мы рекомендуем просмотреть Межмолекулярные силы , прежде чем продолжить.)
Взгляните на молекулу воды. Он содержит один атом кислорода и два атома водорода. Каждый атом кислорода имеет две неподеленные пары электронов. Это означает, что вода может образовывать до четырех водородных связей — по одной с каждым атомом водорода и по одной с каждой из неподеленных пар электронов кислорода.
Каждая молекула воды может образовывать до четырех водородных связей. commons.wikimedia.org
Когда вода является жидкостью, ее молекулы постоянно движутся. Водородные связи между молекулами воды постоянно разрываются и восстанавливаются. На самом деле не все молекулы имеют все четыре водородные связи. Однако когда вода представляет собой твердый лед, все ее молекулы образуют максимально возможное количество водородных связей. Это вынуждает их образовывать решетку со всеми молекулами в определенной ориентации, что влияет на плотность воды, а также температуры плавления и кипения.
Плотность
Вода менее плотна в твердом состоянии, чем в жидком . Как мы упоминали ранее, это необычно. Это связано с тем, что расположение и ориентация молекул воды в их твердой решетке отталкивает их немного дальше друг от друга, чем в жидкости.
Точка плавления
Вода имеет относительно высокую температуру плавления по сравнению с другими простыми ковалентными молекулами с аналогичной относительной массой. Это связано с тем, что его множественные водородные связи между молекулами требуют много энергии для преодоления.
Это связано с тем, что его множественные водородные связи между молекулами требуют много энергии для преодоления.
Водородная связь во льду и жидкой воде. Обратите внимание, что каждая молекула воды во льду образует четыре водородные связи. Это раздвигает молекулы в правильную решетку. commons.wikimedia.org
Если мы сравним структуру воды и аммиака, мы сможем объяснить наблюдаемую разницу в температурах плавления. Аммиак может образовывать только две водородные связи — одну с единственной неподеленной парой электронов на атоме азота, а другую — с одним из атомов водорода.
Водородная связь между молекулами аммиака. Обратите внимание, что каждая молекула может образовывать максимум две водородные связи. StudySmarter Originals
Однако теперь мы знаем, что вода может образовывать четыре водородные связи. Поскольку в воде вдвое больше водородных связей, чем в аммиаке, она имеет гораздо более высокую температуру плавления. В следующей таблице приведены различия между этими двумя соединениями.
Таблица сравнения воды и аммиака. StudySmarter Originals
Физические свойства — основные выводы
Физическое свойство — это свойство, которое мы можем наблюдать, не изменяя химический состав вещества. Физические свойства включают состояние вещества, температуру, массу и проводимость.
Существует четыре различных типа кристаллической структуры. На их физические свойства влияет связь между их частицами.
Гигантские ионные, металлические и ковалентные кристаллы имеют высокие температуры плавления, тогда как молекулярные кристаллы имеют низкие температуры плавления. Это из-за их привязанности.
Вода проявляет необычные физические свойства по сравнению с аналогичными веществами из-за природы ее водородных связей.
Чтение: Физические характеристики минералов
Что такое минералы?
Все горные породы, кроме обсидиана и угля, состоят из минералов. (Обсидиан — это вулканическая порода, состоящая из стекла, а уголь — из органического углерода. ) Большинство пород содержат несколько минералов в смеси, характерной для определенного типа породы. При идентификации породы вы должны сначала определить отдельные минералы, из которых состоит эта порода.
) Большинство пород содержат несколько минералов в смеси, характерной для определенного типа породы. При идентификации породы вы должны сначала определить отдельные минералы, из которых состоит эта порода.
Минералы представляют собой природные неорганические твердые вещества с определенным химическим составом и структурой кристаллической решетки. Хотя в Земле идентифицированы тысячи минералов, всего десять минералов составляют большую часть объема земной коры: плагиоклаз, кварц, ортоклаз, амфибол, пироксен, оливин, кальцит, биотит, гранат и глина.
Вместе химическая формула (типы и пропорции химических элементов) и кристаллическая решетка (геометрия того, как атомы расположены и связаны друг с другом) определяют физические свойства минералов.
Химическую формулу и кристаллическую решетку минерала можно определить только в лаборатории, но, изучив минерал и определив несколько его физических свойств, можно идентифицировать минерал. Во-первых, вам необходимо ознакомиться с физическими свойствами минералов и способами их распознавания.
Во-первых, вам необходимо ознакомиться с физическими свойствами минералов и способами их распознавания.
Минералы можно идентифицировать по их физическим характеристикам. Физические свойства минералов связаны с их химическим составом и связью. Некоторые характеристики, такие как твердость минерала, более полезны для идентификации минерала. Цвет легко наблюдать и, безусловно, он очевиден, но обычно он менее надежен, чем другие физические свойства.
Как идентифицируют полезные ископаемые?
Рис. 1. Этот минерал имеет блестящие золотые кубические кристаллы с бороздками, поэтому это пирит.
Минералоги — ученые, изучающие полезные ископаемые. Одна из вещей, которую должны делать минералоги, — это идентифицировать и классифицировать минералы. Хотя минералог может использовать мощный микроскоп для идентификации некоторых минералов, большинство из них можно распознать по физическим свойствам.
Посмотрите на минерал на рисунке 1. Какого цвета минерал? Какова его форма? Отдельные кристаллы блестящие или тусклые? Есть ли линии (полосы), проходящие через минералы?
Цвет, полосы и блеск
Бриллианты являются популярными драгоценными камнями, потому что то, как они отражают свет, делает их очень блестящими.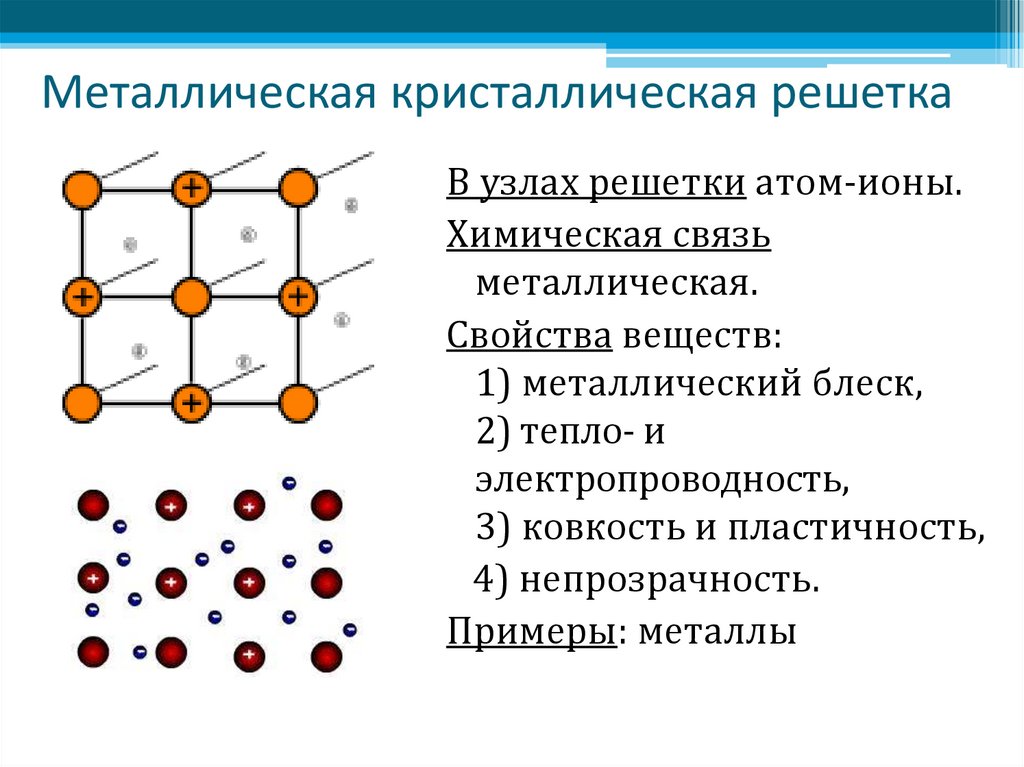 Бирюза ценится за свой яркий зеленовато-голубой цвет. Обратите внимание, что для описания внешнего вида минералов используются специальные термины.
Бирюза ценится за свой яркий зеленовато-голубой цвет. Обратите внимание, что для описания внешнего вида минералов используются специальные термины.
Цвет
Рисунок 2. Этот минерал блестящий, очень мягкий, тяжелый и золотого цвета, и на самом деле является золотом.
Цвет часто полезен, но на него не следует полагаться. Разные минералы могут быть одного цвета. Настоящее золото, как видно на рис. 2, по цвету очень похоже на пирит на рис. 1.
Кроме того, некоторые минералы бывают разных цветов. Кварц, например, может быть прозрачным, белым, серым, коричневым, желтым, розовым, красным или оранжевым. Так что цвет может помочь, но не полагайтесь на цвет как на определяющее свойство. На рис. 3 показан один образец бесцветного кварца и другой образец кварца пурпурного цвета. Небольшое количество железа делает кварц фиолетовым. Многие минералы окрашены химическими примесями.
Рис. 3. Пурпурный кварц, известный как аметист, и прозрачный кварц — это один и тот же минерал, несмотря на разные цвета.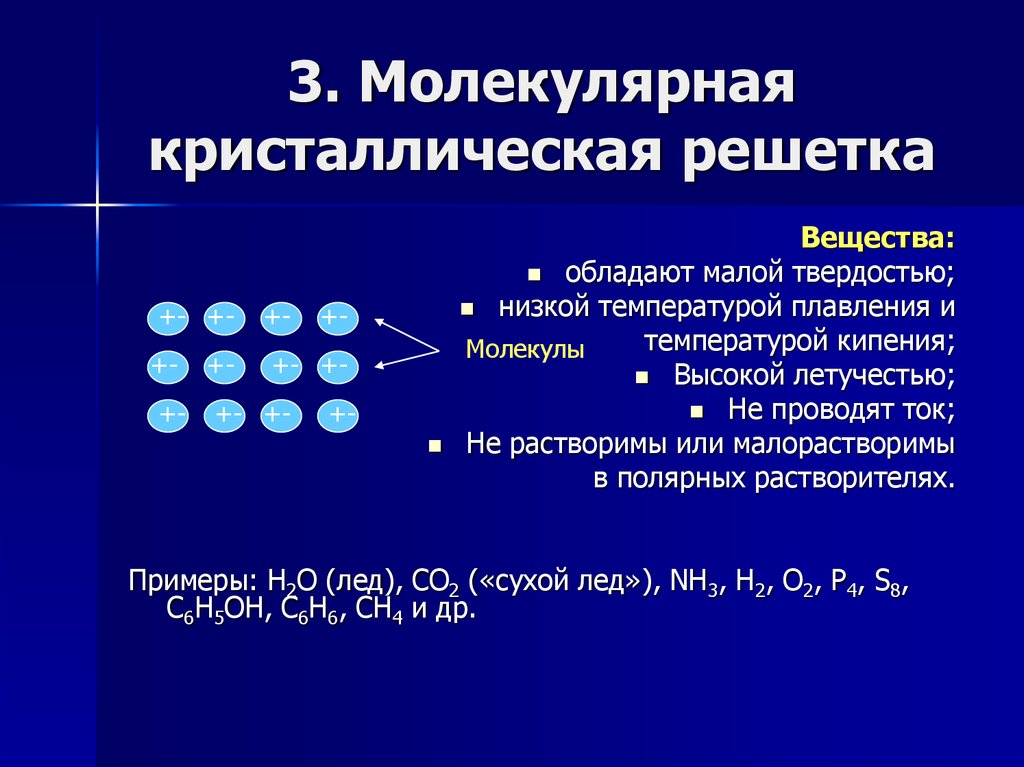
Блеск
Блеск описывает отражение света от поверхности минерала. Минералоги используют специальные термины для описания блеска. Один простой способ классификации блеска основан на том, является ли минерал металлическим или неметаллическим. Непрозрачные и блестящие минералы, такие как пирит, имеют металлический блеск. Минералы, такие как кварц, имеют неметаллический блеск.
Блеск – это то, как поверхность минерала отражает свет. Это не то же самое, что цвет, поэтому очень важно отличать блеск от цвета. Например, минерал, описываемый как «блестящий желтый», описывается с точки зрения блеска («блестящий») и цвета («желтый»), которые представляют собой два разных физических свойства. Стандартные названия блеска включают металлический, стеклянный, жемчужный, шелковистый, жирный и тусклый. Часто полезно сначала определить, имеет ли минерал металлический блеск. Металлический блеск означает блеск, подобный полированному металлу. Например, очищенные полированные куски хрома, стали, титана, меди и латуни обладают металлическим блеском, как и многие другие минералы. Из неметаллических блесков стеклянный является наиболее распространенным и означает, что поверхность минерала отражает свет, как стекло. Жемчужный блеск важен для идентификации полевых шпатов, которые являются наиболее распространенным типом минерала. Жемчужный блеск относится к тонкой радужности или игре цвета в отраженном свете, точно так же, как жемчуг отражает свет. Шелковистый означает отражающий свет с шелковистым блеском. Жирный блеск похож на блеск застывшего жира от бекона. Минералы с тусклым блеском отражают очень мало света. Определение блеска требует небольшой практики. Не забывайте отличать блеск от цвета.
Из неметаллических блесков стеклянный является наиболее распространенным и означает, что поверхность минерала отражает свет, как стекло. Жемчужный блеск важен для идентификации полевых шпатов, которые являются наиболее распространенным типом минерала. Жемчужный блеск относится к тонкой радужности или игре цвета в отраженном свете, точно так же, как жемчуг отражает свет. Шелковистый означает отражающий свет с шелковистым блеском. Жирный блеск похож на блеск застывшего жира от бекона. Минералы с тусклым блеском отражают очень мало света. Определение блеска требует небольшой практики. Не забывайте отличать блеск от цвета.
Различные типы неметаллического блеска описаны в таблице 1.
| Таблица 1. Шесть типов неметаллического блеска. | |
|---|---|
| Блеск | Внешний вид |
| Адамантин | Блестящий |
| Земляной | Тусклый, похожий на глину |
| Жемчужный | Жемчужный |
| Смолистый | Подобно смолам, таким как древесный сок |
| Шелковистый | Мягкий на вид с длинными волокнами |
| Стекловидное тело | Стекловидный |
Можете ли вы сопоставить минералы на рисунке 4 с правильным блеском из таблицы 1?
Рис. 4. (а) Алмаз имеет алмазный блеск. (b) Кварц не блестит, а имеет стеклянный или стеклянный блеск. в) Сера отражает меньше света, чем кварц, поэтому имеет смолистый блеск.
4. (а) Алмаз имеет алмазный блеск. (b) Кварц не блестит, а имеет стеклянный или стеклянный блеск. в) Сера отражает меньше света, чем кварц, поэтому имеет смолистый блеск.
Полоса
Рис. 5. Полоса гематита на неглазурованной фарфоровой тарелке красно-коричневого цвета.
Полоса — цвет порошка минерала. Полоса — более надежное свойство, чем цвет, потому что полоса не меняется. Минералы одного цвета могут иметь полосу разного цвета. Многие минералы, такие как кварц на рисунке 3, не имеют полос.
Чтобы проверить полосу, соскребите минерал с неглазурованной фарфоровой пластины (рис. 5). Желто-золотой пирит имеет черноватую полосу, еще один показатель того, что пирит не является золотом, которое имеет золотисто-желтую полосу.
Удельный вес
Плотность описывает, сколько материи находится в определенном пространстве: плотность = масса/объем.
Масса — это мера количества материи в объекте. Объем пространства, занимаемый объектом, определяется его объемом.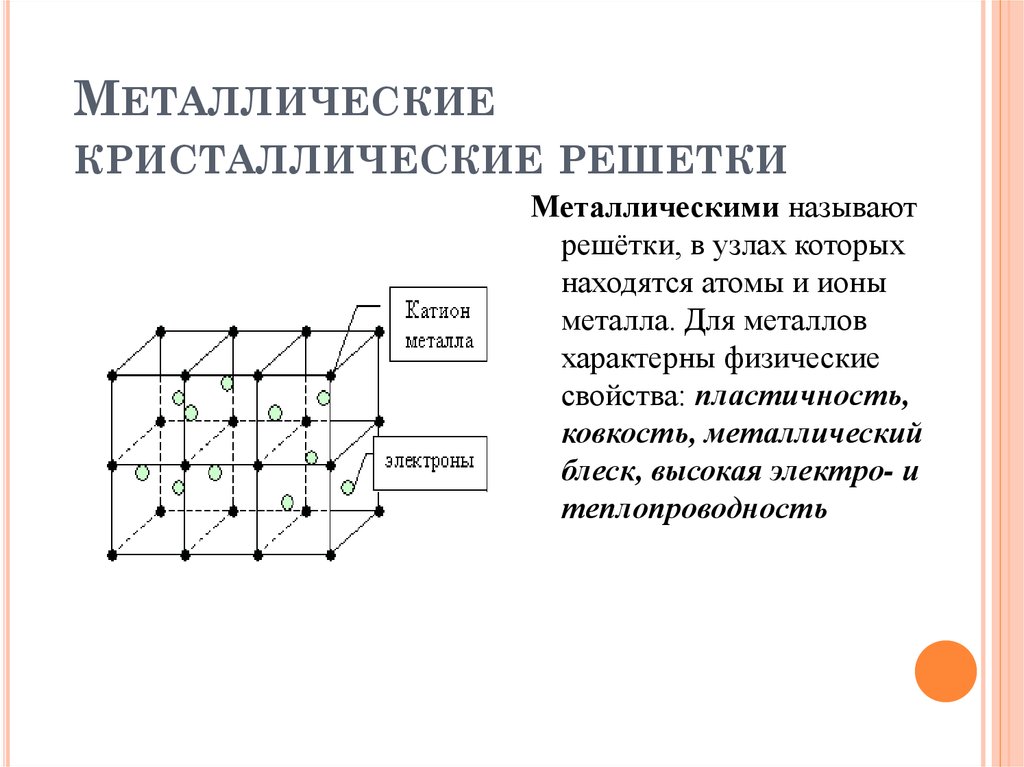 Плотность объекта зависит от его массы и объема. Например, вода в стакане для питья имеет ту же плотность, что и вода в том же объеме бассейна.
Плотность объекта зависит от его массы и объема. Например, вода в стакане для питья имеет ту же плотность, что и вода в том же объеме бассейна.
Удельный вес вещества сравнивает его плотность с плотностью воды. Более плотные вещества имеют больший удельный вес.
Твердость
Твердость — это сила, с которой минерал сопротивляется царапанию или прокалыванию поверхности. При работе с ручными образцами без специального инструмента твердость минерала определяется по шкале твердости Мооса. Шкала твердости Мооса основана на 10 эталонных минералах, от самого мягкого талька (твердость Мооса 1) до алмаза самого твердого (твердость Мооса 10). Это относительная или нелинейная шкала. Твердость 2,5 просто означает, что минерал тверже гипса (твердость по Моосу 2) и мягче кальцита (твердость по Моосу 3). Чтобы сравнить твердость двух минералов, посмотрите, какой минерал царапает поверхность другого.
Таблица 2. Шкала твердости Мооса Шкала твердости Мооса | ||
|---|---|---|
| Твердость | Индекс полезных ископаемых | Обычные предметы |
| 1 | тальк | |
| 2 | гипс | ноготь 2,5 дюйма |
| 3 | кальцит | 3,5-чистая, незапятнанная медь |
| 4 | флюорит | |
| 5 | полевой шпат | 5 до 5,5-нержавеющая сталь |
| Стекло от 5,5 до 6 | ||
| 6 | апатит | Напильник из стали твердостью от 6 до 6,5 |
| 7 | кварц | |
| 8 | топаз | |
| 9 | корунд | |
| 10 | алмаз | |
С помощью шкалы Мооса любой может определить твердость неизвестного минерала. Представьте, что у вас есть неизвестный минерал. Вы обнаружите, что он может поцарапать флюорит или даже полевой шпат, но апатит царапает его. Вы знаете, что твердость минерала составляет от 5 до 6. Обратите внимание, что ни один другой минерал не может поцарапать алмаз.
Представьте, что у вас есть неизвестный минерал. Вы обнаружите, что он может поцарапать флюорит или даже полевой шпат, но апатит царапает его. Вы знаете, что твердость минерала составляет от 5 до 6. Обратите внимание, что ни один другой минерал не может поцарапать алмаз.
Расщепление и разрушение
Разрушение минерала приводит к разрыву его химических связей. Поскольку некоторые связи слабее других, каждый тип минерала может разорваться там, где связи между атомами слабее. По этой причине минералы распадаются характерным образом.
Расщепление
Рис. 6. Крупный план хлорида натрия в водяном пузыре на борту Международной космической станции.
Спайность — это склонность минерала ломаться по определенным плоскостям, образуя гладкие поверхности. Галит распадается между слоями натрия и хлора, образуя кубы с гладкими поверхностями (рис. 6).
Минерал, который естественным образом распадается на идеально плоские поверхности, демонстрирует расщепление. Не все минералы имеют спайность. Спайность представляет собой направление слабости в кристаллической решетке. Поверхности спайности можно отличить по тому, как они стабильно отражают свет, как бы полированные, гладкие и ровные. Свойства спайности минерала описываются количеством спайностей и, если спайностей больше одной, углами между спайностями. Количество расщеплений – это количество или направления расщепления минерала. Минерал может иметь 100 поверхностей спайности, параллельных друг другу. Они представляют собой единый раскол, потому что все поверхности ориентированы в одном направлении. Возможное количество спаек, которые может иметь минерал, равно 1, 2, 3, 4 или 6. Если присутствует более 1 спайности и нет устройства для измерения углов, просто укажите, пересекаются ли спайности в 9 точках.0° или не 90°.
Не все минералы имеют спайность. Спайность представляет собой направление слабости в кристаллической решетке. Поверхности спайности можно отличить по тому, как они стабильно отражают свет, как бы полированные, гладкие и ровные. Свойства спайности минерала описываются количеством спайностей и, если спайностей больше одной, углами между спайностями. Количество расщеплений – это количество или направления расщепления минерала. Минерал может иметь 100 поверхностей спайности, параллельных друг другу. Они представляют собой единый раскол, потому что все поверхности ориентированы в одном направлении. Возможное количество спаек, которые может иметь минерал, равно 1, 2, 3, 4 или 6. Если присутствует более 1 спайности и нет устройства для измерения углов, просто укажите, пересекаются ли спайности в 9 точках.0° или не 90°.
Чтобы увидеть расщепление минерала, подержите минерал под ярким светом и подвигайте его, подвигайте еще немного, чтобы увидеть, как разные стороны отражают свет. Направление спайности будет проявляться в виде гладкого, блестящего, равномерно яркого блеска света, отраженного одним набором параллельных поверхностей на минерале.
Слюда имеет спайность в одном направлении и образует пластины (рис. 7).
Рисунок 7. Листы слюды.
Рис. 8. Этот необработанный алмаз демонстрирует октаэдрическую спайность.
Минералы могут расщепляться на полигоны. Флюорит образует октаэдры (рис. 8).
Одна из причин красоты драгоценных камней заключается в том, что плоскости спайности образуют привлекательную форму кристалла с гладкими гранями.
Трещина
Трещина — это излом в минерале, который не проходит по плоскости спайности. Разрушение не всегда одинаково в одном и том же минерале, потому что разрушение не определяется структурой минерала.
Минералы могут иметь характерные трещины (рисунок 9). Металлы обычно ломаются на зазубренные края. Если минерал расщепляется, как дерево, он может быть волокнистым. Некоторые минералы, такие как кварц, при разрушении образуют гладкие изогнутые поверхности.
Рисунок 9. Хризотил имеет оскольчатый излом.
Все минералов имеют трещины. Излом – это разрушение, происходящее в направлениях, не являющихся направлениями расщепления. Некоторые минералы, такие как кварц, вообще не имеют спайности. Когда минерал без спайности разбивается молотком, он раскалывается во всех направлениях. Говорят, что кварц имеет раковистый излом. Раковистый излом – это то, как толстый кусок стекла разбивается с концентрическими изогнутыми гребнями на разбитых поверхностях. Однако некоторые кристаллы кварца имеют так много дефектов, что вместо раковистого излома они просто имеют неправильный излом. Неправильный перелом — это стандартный термин для обозначения переломов, которые не обладают какими-либо качествами других типов переломов. При вводной геологии следует помнить о таких ключевых типах трещин, как неправильная форма, которая характерна для большинства минералов, и раковистая форма, характерная для кварца.
Излом – это разрушение, происходящее в направлениях, не являющихся направлениями расщепления. Некоторые минералы, такие как кварц, вообще не имеют спайности. Когда минерал без спайности разбивается молотком, он раскалывается во всех направлениях. Говорят, что кварц имеет раковистый излом. Раковистый излом – это то, как толстый кусок стекла разбивается с концентрическими изогнутыми гребнями на разбитых поверхностях. Однако некоторые кристаллы кварца имеют так много дефектов, что вместо раковистого излома они просто имеют неправильный излом. Неправильный перелом — это стандартный термин для обозначения переломов, которые не обладают какими-либо качествами других типов переломов. При вводной геологии следует помнить о таких ключевых типах трещин, как неправильная форма, которая характерна для большинства минералов, и раковистая форма, характерная для кварца.
Кристаллическая форма
Все минералы являются кристаллическими, но только у некоторых есть возможность проявить форму своих кристаллов, свои кристаллические формы. Многие минералы во вводной геологической лаборатории не проявляют своей кристаллической формы. Если у минерала есть пространство во время роста, он может образовывать естественные кристаллы, форма которых отражает геометрию внутренней кристаллической решетки минерала. Форма кристалла соответствует симметрии его кристаллической решетки. Кварц, например, образует шестигранные кристаллы, демонстрируя гексагональную симметрию своей кристаллической решетки. Здесь нужно помнить о двух усложняющих факторах: (1) минералы не всегда образуют хорошие кристаллы, когда растут, и (2) грань кристалла отличается от поверхности спайности. Грань кристалла формируется в процессе роста минерала. Поверхность спайности образуется при разрушении минерала.
Многие минералы во вводной геологической лаборатории не проявляют своей кристаллической формы. Если у минерала есть пространство во время роста, он может образовывать естественные кристаллы, форма которых отражает геометрию внутренней кристаллической решетки минерала. Форма кристалла соответствует симметрии его кристаллической решетки. Кварц, например, образует шестигранные кристаллы, демонстрируя гексагональную симметрию своей кристаллической решетки. Здесь нужно помнить о двух усложняющих факторах: (1) минералы не всегда образуют хорошие кристаллы, когда растут, и (2) грань кристалла отличается от поверхности спайности. Грань кристалла формируется в процессе роста минерала. Поверхность спайности образуется при разрушении минерала.
Другие отличительные признаки
Существуют некоторые свойства, которые помогают различать только небольшое количество минералов или даже один минерал. Примером такого особого свойства является бурная реакция кальцита на слабый раствор соляной кислоты (5% HCl). Кальцит шипит или шипит, когда раствор HCl растворяет его и создает газ CO 2 . Кальцит легко идентифицировать даже без проверки реакции на HCl по его твердости, блеску и расщеплению.
Кальцит шипит или шипит, когда раствор HCl растворяет его и создает газ CO 2 . Кальцит легко идентифицировать даже без проверки реакции на HCl по его твердости, блеску и расщеплению.
Еще одним особым свойством является магнетизм. Это можно проверить, посмотрев, реагирует ли небольшой магнит на минерал. Наиболее распространенным минералом с сильными магнитными свойствами является минерал магнетит. Особым свойством, проявляющимся в некоторых образцах плагиоклазового полевого шпата, является склонность к образованию полос на поверхности спайности. Исчерченность — идеально прямые, тонкие, параллельные линии. Чтобы увидеть бороздки на поверхности сколов плагиоклаза, может потребоваться увеличение. Другие особые свойства могут встречаться на минеральной основе.
Некоторые минералы обладают другими уникальными свойствами, некоторые из которых перечислены в таблице 3. Можете ли вы назвать уникальное свойство, которое позволило бы вам мгновенно идентифицировать минерал, довольно подробно описанный в этой главе? (Подсказка: скорее всего, его можно найти на вашем обеденном столе. )
)
| Таблица 3. Некоторые минералы обладают необычными свойствами, которые можно использовать для идентификации. | ||
|---|---|---|
| Собственность | Описание | Пример минерала |
| Флуоресценция | Минерал светится в ультрафиолетовом свете | Флюорит |
| Магнетизм | Минерал притягивается магнитом | Магнетит |
| Радиоактивность | Минерал испускает излучение, которое можно измерить с помощью счетчика Гейгера | Уранинит |
| Реактивность | Пузырьки образуются при воздействии на минерал слабой кислоты | Кальцит |
| Запах | Некоторые минералы имеют характерный запах | Сера (пахнет тухлыми яйцами) |
| Вкус | Некоторые минералы имеют соленый вкус | Галит |
Внесите свой вклад!
У вас есть идеи по улучшению этого контента? Мы будем признательны за ваш вклад.
Улучшить эту страницуПодробнее
|
Кристаллическая структура, электронные и решеточно-динамические свойства NbTe2
Кристаллическая структура, электронные и решеточно-динамические свойства NbTe 2
Скачать PDF
Скачать PDF
- Артикул
- Открытый доступ
- Опубликовано:
- Aarón Hernán Barajas-Aguilar 1 ,
- J. C. Irwin 2 ,
- Andrés Manuel Garay-Tapia 3 ,
- Torsten Schwarz 4 ,
- Francisco Paraguay Delgado 5 ,
- P.
 M. Бродерсен 6 ,
M. Бродерсен 6 , - Раджив Приня 7 ,
- Назир Херани 7,8 и
- …
- Серхио Х. Хименес Сандовал ORCID: orcid.org/0000-0002-2143-3759 1
Научные отчеты том 8 , Номер статьи: 16984 (2018) Процитировать эту статью
4680 доступов
19 цитирований
Сведения о показателях
Предметы
- Электронные свойства и материалы
Abstract
Материалы со слоистой структурой актуальны в настоящее время, учитывая их квази-двумерную природу. Знание их физических свойств в настоящее время представляет большой интерес. Дителлурид ниобия имеет моноклинную слоисто-структуру с искажением в плоскостях теллура. Эта структурная сложность препятствовала определению его основных физических свойств. В этой работе NbTe 2 кристаллов были использованы для выяснения его структурных, композиционных, электронных и колебательных свойств. Эти результаты были сопоставлены с расчетами, основанными на теории функционала плотности. Химический состав и распределение элементов в наномасштабе были получены с помощью атомно-зондовой томографии. Ультрафиолетовая фотоэлектронная спектроскопия позволила впервые определить работу выхода NbTe 2 . Его высокое значение, 5,32 эВ, и химическая стабильность позволяют предвидеть такие применения, как контакт в оптоэлектронике. Спектры комбинационного рассеяния были получены с использованием различных лазерных линий возбуждения: 488, 633 и 785 нм. Частоты колебаний соответствовали частотам, определенным с помощью теории функционала плотности.
Знание их физических свойств в настоящее время представляет большой интерес. Дителлурид ниобия имеет моноклинную слоисто-структуру с искажением в плоскостях теллура. Эта структурная сложность препятствовала определению его основных физических свойств. В этой работе NbTe 2 кристаллов были использованы для выяснения его структурных, композиционных, электронных и колебательных свойств. Эти результаты были сопоставлены с расчетами, основанными на теории функционала плотности. Химический состав и распределение элементов в наномасштабе были получены с помощью атомно-зондовой томографии. Ультрафиолетовая фотоэлектронная спектроскопия позволила впервые определить работу выхода NbTe 2 . Его высокое значение, 5,32 эВ, и химическая стабильность позволяют предвидеть такие применения, как контакт в оптоэлектронике. Спектры комбинационного рассеяния были получены с использованием различных лазерных линий возбуждения: 488, 633 и 785 нм. Частоты колебаний соответствовали частотам, определенным с помощью теории функционала плотности. Удалось обнаружить теоретически предсказанную низкочастотную рамановскую активную моду малой интенсивности, ранее не наблюдавшуюся. Были рассчитаны дисперсионные кривые и электронная зонная структура, а также соответствующая им плотность состояний. Электрические свойства, а также псевдощель в плотности состояний вокруг энергии Ферми являются характеристиками, свойственными полуметаллу.
Удалось обнаружить теоретически предсказанную низкочастотную рамановскую активную моду малой интенсивности, ранее не наблюдавшуюся. Были рассчитаны дисперсионные кривые и электронная зонная структура, а также соответствующая им плотность состояний. Электрические свойства, а также псевдощель в плотности состояний вокруг энергии Ферми являются характеристиками, свойственными полуметаллу.
Введение
Дихалькогениды переходных металлов (ДПМ) представляют собой квазидвумерные материалы со слоистой структурой, состоящей из стопок единичных слоев халькогенид-переходный металл-халькогенид (М-Х-М), связанных слабыми силами Ван-дер-Ваальса 1 . Такое слабое межслоевое притяжение позволяет получать слои толщиной в несколько монослоев за счет отслаивания поверхности объемного материала 2 . Это свойство делает эти материалы как технологичными, так и принципиально актуальными. В случае дителлурида ниобия установлено, что он представляет собой ДПМ с поведением металлического типа при температурах выше 0,5 К, приобретая свойства сверхпроводника ниже этой температуры 3 . Дителлурид ниобия имеет сложную кристаллическую структуру, состоящую из выпуклых слоев Te-Nb-Te, чередующихся с ван-дер-ваальсовыми щелями. Это расположение можно рассматривать как искаженную структуру 1T. В идеальной (неискаженной) структуре 1T атомы металла октаэдрически координированы с окружающими атомами халькогена. Колебательные свойства NbTe 2 ранее изучались Эрдоганом и Кирби 4 . Из их измерений в кристаллах NbTe 2 было обнаружено одиннадцать рамановских активных мод с частотами от 56 до 254 см -1 . Теоретический анализ этих результатов был проведен путем рассмотрения простой модели силовой постоянной ближайшего соседа для одного слоя неискаженной структуры 1T-CdI 2 (, т.е. , с учетом неискаженных, плоских слоев Te-Nb-Te). используя силовые постоянные TaS 2 . Влияние на предложенные фононные дисперсионные кривые, вызванное реальным искажением слоев, обсуждалось с точки зрения симметрии.
Дителлурид ниобия имеет сложную кристаллическую структуру, состоящую из выпуклых слоев Te-Nb-Te, чередующихся с ван-дер-ваальсовыми щелями. Это расположение можно рассматривать как искаженную структуру 1T. В идеальной (неискаженной) структуре 1T атомы металла октаэдрически координированы с окружающими атомами халькогена. Колебательные свойства NbTe 2 ранее изучались Эрдоганом и Кирби 4 . Из их измерений в кристаллах NbTe 2 было обнаружено одиннадцать рамановских активных мод с частотами от 56 до 254 см -1 . Теоретический анализ этих результатов был проведен путем рассмотрения простой модели силовой постоянной ближайшего соседа для одного слоя неискаженной структуры 1T-CdI 2 (, т.е. , с учетом неискаженных, плоских слоев Te-Nb-Te). используя силовые постоянные TaS 2 . Влияние на предложенные фононные дисперсионные кривые, вызванное реальным искажением слоев, обсуждалось с точки зрения симметрии. Однако этот подход привел к ошибочному предсказанию 51 оптической фононной моды. Совсем недавно К. Баталья и др. . 5 провел исследования поверхности Ферми, чтобы выяснить происхождение искажения моноклинной структуры NbTe 2 . Эти исследования включали расчеты электронной зонной структуры и фононных дисперсионных кривых NbTe 2 с помощью теории функционала плотности (DFT) с использованием родственной неискаженной структуры 1T. Поскольку в этих расчетах не учитывалась реальная структура NbTe 2 , были получены мнимые частоты акустических фононов вдоль трех высокосимметричных направлений зоны Бриллюэна. Дополнительно можно отметить, что теория групп предсказывает две рамановские активные моды для неискаженной 1T-структуры, тогда как рассмотрение реальной искаженной моноклинной структуры при разложении на неприводимые представления NbTe 2 приводит к двенадцати колебательным модам с рамановской активностью ( см. ниже ).
Однако этот подход привел к ошибочному предсказанию 51 оптической фононной моды. Совсем недавно К. Баталья и др. . 5 провел исследования поверхности Ферми, чтобы выяснить происхождение искажения моноклинной структуры NbTe 2 . Эти исследования включали расчеты электронной зонной структуры и фононных дисперсионных кривых NbTe 2 с помощью теории функционала плотности (DFT) с использованием родственной неискаженной структуры 1T. Поскольку в этих расчетах не учитывалась реальная структура NbTe 2 , были получены мнимые частоты акустических фононов вдоль трех высокосимметричных направлений зоны Бриллюэна. Дополнительно можно отметить, что теория групп предсказывает две рамановские активные моды для неискаженной 1T-структуры, тогда как рассмотрение реальной искаженной моноклинной структуры при разложении на неприводимые представления NbTe 2 приводит к двенадцати колебательным модам с рамановской активностью ( см. ниже ).
В этой статье мы представляем первопринципные DFT-расчеты электронных и решеточных динамических свойств для фактической искаженной моноклинной структуры NbTe 2 . Приведены электронная зонная структура и плотность состояний, а также однофононные дисперсионные кривые и плотность состояний. Рассчитанные частоты активных мод комбинационного рассеяния хорошо согласуются с экспериментами по неупругому рассеянию света с высоким разрешением и высокой пропускной способностью, проведенными на структурных и химически охарактеризованных NbTe 9.0394 2 кристаллов. Характеристика включала рентгеновскую дифракцию, сканирующую и просвечивающую электронную микроскопию, а также измерения с помощью атомно-зондовой томографии. Из экспериментов по эффекту Холла и ультрафиолетовой фотоэлектронной спектроскопии были определены электрические свойства, такие как концентрация свободных носителей заряда, подвижность и работа выхода. Ранее об этих свойствах дителлурида ниобия не сообщалось. Отмечено, что высокое значение работы выхода NbTe 2 , определенное в данной работе, а именно 5,32 эВ, может представлять интерес для приложений оптоэлектроники, где проводящие материалы с высокой работой выхода весьма дефицитны и ценятся.
Отмечено, что высокое значение работы выхода NbTe 2 , определенное в данной работе, а именно 5,32 эВ, может представлять интерес для приложений оптоэлектроники, где проводящие материалы с высокой работой выхода весьма дефицитны и ценятся.
Результаты
Экспериментальные структурно-композиционные свойства
Методом рентгеновской дифракции идентифицирована кристаллическая фаза образцов NbTe 2 . Из полученной дифрактограммы (рис. 1) и данных в исх. 6 было определено, что кристаллическая структура является моноклинной, описываемой 12-й пространственной группой симметрии (C2/m). Соответствующая элементарная ячейка показана на рис. 2а. Учитывая слоистую природу NbTe 2 и преимущественную ориентацию роста, наиболее интенсивные рефлексы на дифрактограмме соответствуют [00 c ], рис. 1. Последовательность укладки отдельных слоев для этого материала показана на рис. 2b. Вследствие структурного искажения в NbTe 2 можно наблюдать выпуклую поверхность плоскостей Te и неравномерность расстояний Nb-Nb.
Рентгенограмма кристалла NbTe 2 и подгонка всей картины, выполненная методом Ритвельда. Кружки соответствуют экспериментальным данным, а подгонка показана сплошной линией. Разница между экспериментальными данными и подгонкой представлена на нижнем графике.
Изображение полного размера
Рисунок 2( a ) NbTe 2 обычная моноклинная ячейка; ( b ) последовательность укладки монослоев в NbTe 2 . ( c ) Первая зона Бриллюэна и ее точки и направления высокой симметрии. Цвета точек высокой симметрии в зоне Бриллюэна соответствуют вертикальным линиям на рис. 12 (электронная зонная структура) и 13 (кривые дисперсии фононов).
Полноразмерное изображение
Морфология верхней поверхности и поперечного сечения была проанализирована с помощью СЭМ на свежеотслоенных поверхностях, рис. 3. Квази-двумерный характер сложенных слоев очевиден на видах сверху, рис. 3a, b, а также на микрофотография поперечного сечения, рис. 3в. Изображения показывают однородные и плоские поверхности в масштабах, указанных на рис. 3a, b, за исключением случаев, когда края нескольких слоев обнажены, так что видна террасообразная структура.
3a, b, а также на микрофотография поперечного сечения, рис. 3в. Изображения показывают однородные и плоские поверхности в масштабах, указанных на рис. 3a, b, за исключением случаев, когда края нескольких слоев обнажены, так что видна террасообразная структура.
СЭМ-изображения ( a , b ) вид сверху и ( c ) поперечное сечение расслоенных кристаллов NbTe 2 при разном увеличении.
Полноразмерное изображение
Несмотря на хорошее совпадение положения экспериментального и зарегистрированного дифракционных пиков, экспериментальные отражения (-203) и (-714) демонстрируют небольшое смещение в сторону меньших углов. Смещения такого рода могут быть вызваны разницей между параметрами и/или углами решетки образца и указанными значениями в файле порошковой дифракции (PDF). Согласно PDF 21-0605 параметры решетки для NbTe 2 : A = 19,39 Å, B = 3,64 Å и C = 9,38 Å, с углами α = 90 °, β = 134,58 ° и γ = 90 °. Для количественной оценки разницы была проведена полная подгонка образца по методу Ритвельда 7 с использованием программного обеспечения FullProf 8 , в котором регулировались положение, ширина и интенсивность каждого отражения. Подогнанная картина показана сплошной линией на рис. 1. Из этого анализа было определено, что углы и параметры решетки NbTe 2 Кристаллы, используемые в этой работе, были: A = 20,98 Å, B = 3,66 Å и C = 9,65 Å, с α = 90 °, β = 136,6 °, γ = 90 ° соответственно.
Для количественной оценки разницы была проведена полная подгонка образца по методу Ритвельда 7 с использованием программного обеспечения FullProf 8 , в котором регулировались положение, ширина и интенсивность каждого отражения. Подогнанная картина показана сплошной линией на рис. 1. Из этого анализа было определено, что углы и параметры решетки NbTe 2 Кристаллы, используемые в этой работе, были: A = 20,98 Å, B = 3,66 Å и C = 9,65 Å, с α = 90 °, β = 136,6 °, γ = 90 ° соответственно.
Для дальнейшего изучения структурных свойств дителлурида ниобия были получены HRTEM-изображения поперечного сечения при различном увеличении, рис. 4. Положения атомов в слоистой структуре легко наблюдать, а также высокое кристаллическое качество и гомогенность образца. Промежутки Ван-дер-Ваальса выглядят как немного более темные полосы на всех изображениях рис. 4. Удалось получить дифракционные картины выбранной площади (SADP), как показано на рис. 5a. На картине видны хорошо очерченные яркие дифракционные пятна, погруженные в темный фон. Хороший контраст между белыми пятнами и темным фоном свидетельствует о высоком качестве кристаллов. Параметры решетки и углы элементарной ячейки, определенные на основе анализа рентгеновских параметров методом Ритвельда, использовались для индексации и моделирования SADP (рис. 5b, c соответственно). Это было достигнуто с помощью программного обеспечения STEM_CELL 9.0712 9,10 . Из этого анализа было обнаружено, что осью зоны SADP является направление [010]. Следует отметить хорошее совпадение расчетных углов и параметров решетки, полученных по методу Ритвельда, с измеренными непосредственно на изображениях ВРЭМ. Действительно, хорошее совпадение в положениях атомов достигается, когда смоделированная кристаллическая структура и изображение HRTEM перекрываются, как показано на рис. 6.
5a. На картине видны хорошо очерченные яркие дифракционные пятна, погруженные в темный фон. Хороший контраст между белыми пятнами и темным фоном свидетельствует о высоком качестве кристаллов. Параметры решетки и углы элементарной ячейки, определенные на основе анализа рентгеновских параметров методом Ритвельда, использовались для индексации и моделирования SADP (рис. 5b, c соответственно). Это было достигнуто с помощью программного обеспечения STEM_CELL 9.0712 9,10 . Из этого анализа было обнаружено, что осью зоны SADP является направление [010]. Следует отметить хорошее совпадение расчетных углов и параметров решетки, полученных по методу Ритвельда, с измеренными непосредственно на изображениях ВРЭМ. Действительно, хорошее совпадение в положениях атомов достигается, когда смоделированная кристаллическая структура и изображение HRTEM перекрываются, как показано на рис. 6.
 Более темные линии соответствуют ван-дер-ваальсовым областям, разделяющим слои Te-Nb-Te. Рис. 5 Ось зоны — это направление [010].
Более темные линии соответствуют ван-дер-ваальсовым областям, разделяющим слои Te-Nb-Te. Рис. 5 Ось зоны — это направление [010].Полноразмерное изображение
Рисунок 6Наложение изображения HRTEM и вида a-c в плоскости элементарной ячейки NbTe 2 , полученного в результате уточнения рентгенограмм методом Ритвельда. Было получено хорошее совпадение атомных позиций.
Увеличенное изображение
Элементный состав определен в экспериментах по атомно-зондовой томографии. Из этих измерений было установлено, что кристаллы NbTe 2 состоят из: Nb = ~38 ат.%, Te = ~61 ат.% и O = ~1 ат.%. Этот состав отличается от идеального соотношения [Te]/[Nb] = 2; вместо этого имеем [Te]/[Nb] = 1,6. Дефицит Те может быть вызван преимущественной потерей Те во время АФТ-анализа, что является известной проблемой для полупроводниковых соединений 11,12 . Соответствующий масс-спектр показан на рис. 7, где можно наблюдать все обнаруженные ионные частицы. Большая часть обнаруженных ионов соответствует сложным, тяжелым молекулярным частицам Nb-Te. Существование таких комплексных ионов может быть в некоторой степени связано со слабой ван-дер-ваальсовой связью. Частицы Nb-O были обнаружены только в виде молекулярных ионов NbO 2+ . Происхождение массовых пиков, связанных с O, которые в сумме составляют ~ 1 ат.% O в наборе данных APT, неясно. Одной из причин является окисление поверхности образца, а другой – остаточными газами в аналитической камере. Небольшая часть O может исходить от самого образца, заменяющего Te. На рисунке 8 показана трехмерная реконструкция образца в наномасштабе для соединений Nb и Te. В распределении Nb и Te наблюдается хорошая однородность, при этом наблюдается, что области с несколько более высокой плотностью Nb совпадают с областями Te с той же характеристикой. Эти области с высокой плотностью возникают из-за довольно прерывистого поведения поля испарения, которое может быть в некоторой степени вызвано слабыми ван-дер-ваальсовыми щелями в материале.
Большая часть обнаруженных ионов соответствует сложным, тяжелым молекулярным частицам Nb-Te. Существование таких комплексных ионов может быть в некоторой степени связано со слабой ван-дер-ваальсовой связью. Частицы Nb-O были обнаружены только в виде молекулярных ионов NbO 2+ . Происхождение массовых пиков, связанных с O, которые в сумме составляют ~ 1 ат.% O в наборе данных APT, неясно. Одной из причин является окисление поверхности образца, а другой – остаточными газами в аналитической камере. Небольшая часть O может исходить от самого образца, заменяющего Te. На рисунке 8 показана трехмерная реконструкция образца в наномасштабе для соединений Nb и Te. В распределении Nb и Te наблюдается хорошая однородность, при этом наблюдается, что области с несколько более высокой плотностью Nb совпадают с областями Te с той же характеристикой. Эти области с высокой плотностью возникают из-за довольно прерывистого поведения поля испарения, которое может быть в некоторой степени вызвано слабыми ван-дер-ваальсовыми щелями в материале.
Масс-спектр АПП кристалла NbTe 2 .
Изображение в натуральную величину
Рис. 8Распределение элементов в наномасштабе, полученное из измерений атомной зондовой томографии для указанных соединений.
Изображение полного размера
Расчеты по первому принципу: кристаллическая структура NbTe
2 На основе файла кристаллографической информации (CIF) NbTe 2 был проведен структурный анализ с использованием кода VASP. Параметры решетки, рассчитанные для релаксированной структуры в VASP, составили: A = 19,59 Å, B = 3,66 Å и C = 9,64 Å, с единичной ячейкой углов: и α = 90 °, β = 134,2 °, γ = 90 °. Сравнение параметров решетки, полученных в этой работе (уточнение Ритвельда и оптимизация VASP), и параметров, указанных в файле PDF, представлено в таблице 1. В целом, между полученными значениями имеется хорошее согласие. Однако параметры, полученные в результате уточнения Ритвельда, имеют тенденцию быть немного больше, чем остальные.
Однако параметры, полученные в результате уточнения Ритвельда, имеют тенденцию быть немного больше, чем остальные.
Полноразмерная таблица
Энергия когезии (или энергия связи) и теплота образования также были рассчитаны методом DFT. В случае TMD с химической формулой MX 2 энергия когезии на формульную единицу определяется как:
$${E}_{B}(M{X}_{2})={E}_{ MX2}-{E}_{Matom}\,-\,2{E}_{Xatom},$$
где E MX2 – полная энергия формульной единицы MX 2 в объемном материале, E M атом и E X атом – энергии соответствующих изолированных атомов M и X, т.е. . Nb и Te соответственно. Было установлено, что E B (MX 2 ) = –13,22 эВ/формульная единица или –1273,8 кДж/моль. С другой стороны, энергию образования можно рассчитать как 13 :
$${\Delta}{E}_{f}(M{X}_{2})={E}_{MX2} \,-\,{E}_{Mst}\,-\,2{E}_{Xst},$$
where E MX2 is the total energy of the MX 2 formula-unit in the bulk material, E M st and E X st are the энергии соответствующих атомов M (Nb) и X (Te) в их стабильных структурах 14,15 . Поскольку все рассчитанные энергии соответствуют релаксированным структурам, влиянием давления пренебрегают, а энергию образования аппроксимируют энтальпией образования; это 16 ,
Поскольку все рассчитанные энергии соответствуют релаксированным структурам, влиянием давления пренебрегают, а энергию образования аппроксимируют энтальпией образования; это 16 ,
$${\Delta}{E}_{f}(M{X}_{2}) \sim {\Delta}{H}_{f}(M{X}_{2 }).$$
В этом случае, поскольку энергии рассчитываются при 0 К, термин теплота образования является более точным, поскольку определение энтальпии образования подразумевает энергию материала при 298 К 15 . Таким образом, ΔH f (NbTe 2 ) = −1,38 эВ/формульная единица или −132,85 кДж/моль. Это отрицательное значение является мерой устойчивости конструкции 17 . Анализ энергии против . объемная кривая, рис. 9, была построена для расчета объемного модуля (B 0 ) материала. Для твердых тел B 0 представляет собой отношение приложенного гидростатического давления к соответствующему изменению объема 18 . Объемные сжатия и расширения были выполнены для расчета энергии материала при гидростатической деформации и напряжении. Максимальная деформация объема составила 15% как при сжатии, так и при расширении. Тогда с целью вычисления B 0, была проведена аппроксимация методом наименьших квадратов с использованием уравнения Берча-Мурнагана 17,19 . Расчетный модуль объемного сжатия и его производная были в этом случае B 0 = 38,5904 ГПа и B 0 ’ = 6,025 соответственно 16 .
Максимальная деформация объема составила 15% как при сжатии, так и при расширении. Тогда с целью вычисления B 0, была проведена аппроксимация методом наименьших квадратов с использованием уравнения Берча-Мурнагана 17,19 . Расчетный модуль объемного сжатия и его производная были в этом случае B 0 = 38,5904 ГПа и B 0 ’ = 6,025 соответственно 16 .
Расчетная относительная энергия как функция объема элементарной ячейки.
Полноразмерное изображение
Электронные свойства
Хотя некоторые работы над электронными свойствами NbTe 2 , остаются неизвестными некоторые важные свойства материала. Например, отсутствуют отчеты о соответствующих электрических параметрах, таких как концентрация носителей, подвижность или работа выхода. Здесь мы сообщаем результаты измерений эффекта Холла, выполненных при комнатной температуре на квадратных (5 × 5 мм 2 ) кристаллах NbTe 2 с использованием метода Ван дер Пау. Мы нашли концентрацию носителей n = 5,46 × 10 21 см −3 с подвижностью μ = 6,9 см 2 /Вс, что дает удельное сопротивление ρ = 1,74 × 10 −4 Ом·см. Это значение хорошо согласуется с предыдущими измерениями ρ = 1,8 × 10 −4 Ом·см и ρ = 2,6 × 10 −4 Ом·см (оба при комнатной температуре), представленными в работе. 3 и 20 соответственно. Кроме того, с помощью метода Ван дер Пау было измерено удельное сопротивление в зависимости от температуры (100–400 К) в другой системе. Это является причиной небольшой разницы между значением ρ при комнатной температуре, приведенным выше, и значением на рис. 10, на котором показана вся зависимость от температуры. Удельное сопротивление каждого образца измерялось четыре раза во всем диапазоне температур. Результаты, представленные на рис. 10, соответствуют среднему удельному сопротивлению из этих измерений с соответствующим стандартным отклонением в виде планок погрешностей.
Мы нашли концентрацию носителей n = 5,46 × 10 21 см −3 с подвижностью μ = 6,9 см 2 /Вс, что дает удельное сопротивление ρ = 1,74 × 10 −4 Ом·см. Это значение хорошо согласуется с предыдущими измерениями ρ = 1,8 × 10 −4 Ом·см и ρ = 2,6 × 10 −4 Ом·см (оба при комнатной температуре), представленными в работе. 3 и 20 соответственно. Кроме того, с помощью метода Ван дер Пау было измерено удельное сопротивление в зависимости от температуры (100–400 К) в другой системе. Это является причиной небольшой разницы между значением ρ при комнатной температуре, приведенным выше, и значением на рис. 10, на котором показана вся зависимость от температуры. Удельное сопротивление каждого образца измерялось четыре раза во всем диапазоне температур. Результаты, представленные на рис. 10, соответствуют среднему удельному сопротивлению из этих измерений с соответствующим стандартным отклонением в виде планок погрешностей. На этом рисунке видно, что существенного изменения удельного сопротивления в исследованном интервале температур не наблюдается. Небольшое падение заметно при уменьшении температуры образца; тем не менее, удельное сопротивление остается в основном постоянным. Аналогичные результаты были получены Nagata и др. . 3 , так как они сообщают об изменении удельного сопротивления ниже порядка величины при изменении температуры образца от 280 до 0,7 К. Брикснер 20 нашел удельное сопротивление ρ = 2,6 × 10 −4 Ом·см при 298 К и ρ = 7,7 × 10 −4 Ом·см при 77 K. В соответствии с теми же результатами, Battaglia et al . 5 представили спектры фотоэлектронной спектроскопии с угловым разрешением, снятые при комнатной температуре, и обнаружили, что такие же спектры были получены при температурах ниже 20 K, что указывает на то, что топология NbTe 2 электронная зонная структура в основном не изменяется до значительных изменений температуры.
На этом рисунке видно, что существенного изменения удельного сопротивления в исследованном интервале температур не наблюдается. Небольшое падение заметно при уменьшении температуры образца; тем не менее, удельное сопротивление остается в основном постоянным. Аналогичные результаты были получены Nagata и др. . 3 , так как они сообщают об изменении удельного сопротивления ниже порядка величины при изменении температуры образца от 280 до 0,7 К. Брикснер 20 нашел удельное сопротивление ρ = 2,6 × 10 −4 Ом·см при 298 К и ρ = 7,7 × 10 −4 Ом·см при 77 K. В соответствии с теми же результатами, Battaglia et al . 5 представили спектры фотоэлектронной спектроскопии с угловым разрешением, снятые при комнатной температуре, и обнаружили, что такие же спектры были получены при температурах ниже 20 K, что указывает на то, что топология NbTe 2 электронная зонная структура в основном не изменяется до значительных изменений температуры. Кстати, аналогичное поведение наблюдается для магнитной восприимчивости, которая равна нулю с 725 К до ~0,5 К, когда материал достигает своей критической температуры и становится сверхпроводником 3,21 .
Кстати, аналогичное поведение наблюдается для магнитной восприимчивости, которая равна нулю с 725 К до ~0,5 К, когда материал достигает своей критической температуры и становится сверхпроводником 3,21 .
Удельное сопротивление в зависимости от температуры для NbTe 2 . Контакты производились на свежеотслоившуюся поверхность кристалла.
Полноразмерное изображение
Ультрафиолетовая фотоэлектронная спектроскопия (УФС), метод, в основе которого лежит фотоэлектрический эффект, использовался для определения работы выхода NbTe 2 . Источником света служила монохроматическая лампа He I ( hν = 21,22 эВ). На рисунке 11 показана кривая испускаемых фотоэлектронов в зависимости от энергии связи. Анализ данных основан на том, что уровень Ферми установлен равным 0 эВ. Тогда работа выхода представляет собой разность между энергией падающего фотона и максимальной энергией испущенных фотоэлектронов, то есть ϕ = hν − BE макс .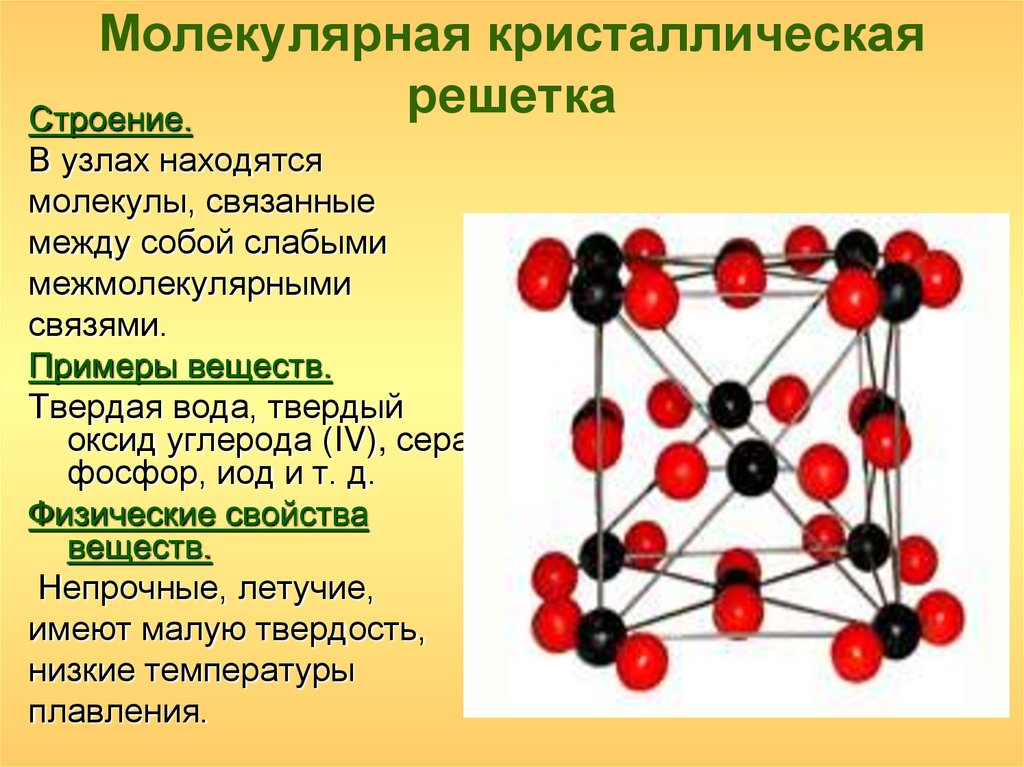 Из рис. 11 видно, что BE max = 15,9 эВ. Таким образом, работа выхода для NbTe 2 равна ϕ = 5,32 эВ. Эта работа выхода близка к работе выхода золота, о котором сообщается со значениями в диапазоне от 5,2 до 5,3 эВ 22 , что является одним из самых больших среди металлов. Большие рабочие функции особенно ценны в тех случаях, когда электрические контакты до 9Нужны полупроводники типа 0051 p . Однако следует отметить, что удельное сопротивление золота примерно на два порядка ниже, чем у NbTe 2 . Кристаллы дителлурида ниобия, использованные в работе, хранились в условиях окружающей среды более года. Было обнаружено, что электрические свойства свежесколотых поверхностей после длительного хранения практически не изменились. Более того, данные рис. 10 показывают, что удельное сопротивление остается стабильным до значительных изменений температуры. Эти характеристики делают NbTe 2 интересный материал не только для приложений, таких как изготовление оптоэлектронных устройств, но и с точки зрения фундаментальных свойств.
Из рис. 11 видно, что BE max = 15,9 эВ. Таким образом, работа выхода для NbTe 2 равна ϕ = 5,32 эВ. Эта работа выхода близка к работе выхода золота, о котором сообщается со значениями в диапазоне от 5,2 до 5,3 эВ 22 , что является одним из самых больших среди металлов. Большие рабочие функции особенно ценны в тех случаях, когда электрические контакты до 9Нужны полупроводники типа 0051 p . Однако следует отметить, что удельное сопротивление золота примерно на два порядка ниже, чем у NbTe 2 . Кристаллы дителлурида ниобия, использованные в работе, хранились в условиях окружающей среды более года. Было обнаружено, что электрические свойства свежесколотых поверхностей после длительного хранения практически не изменились. Более того, данные рис. 10 показывают, что удельное сопротивление остается стабильным до значительных изменений температуры. Эти характеристики делают NbTe 2 интересный материал не только для приложений, таких как изготовление оптоэлектронных устройств, но и с точки зрения фундаментальных свойств. Тот факт, что удельное сопротивление не изменяется при температурах от 100 до 400 К, указывает на то, что электрон-фононное взаимодействие не имеет существенного значения для процесса переноса заряда в этом диапазоне температур.
Тот факт, что удельное сопротивление не изменяется при температурах от 100 до 400 К, указывает на то, что электрон-фононное взаимодействие не имеет существенного значения для процесса переноса заряда в этом диапазоне температур.
Данные ультрафиолетовой фотоэлектронной спектроскопии для NbTe 2 . Стрелка указывает значение BE max , который использовался для определения работы выхода дителлурида ниобия.
Изображение с полным размером
Одним из наиболее важных аспектов свойств материалов является электронная зонная структура и соответствующая ей плотность состояний (DOS). Батталья и др. . 5 сообщил о расчетах DFT зонной структуры для тригонального NbTe 2 , , т.е. . для приближенной идеальной фазы 1 T, определяющей металлическое поведение. Как упоминалось выше, реальная структура NbTe 2 отличается от фазы 1T тем, что представляет собой изогнутые плоскости Te, которые изменяют симметрию кристалла с тригональной на моноклинную. Кумар и др. . 23 использовал DFT для расчета зонной структуры и DOS для гипотетической гексагональной фазы NbTe 2 (политип 2H), а также обнаружил металлическое поведение. Хотя расчеты проводились для сравнения с различными дихалькогенидами ниобия с гексагональной структурой, фаза 2H никогда не наблюдалась для NbTe 2 . В этой работе сообщается о зонной структуре и плотности состояний дителлурида ниобия с учетом реальной структуры материала (, т.е. , моноклинная симметрия с изогнутыми плоскостями Te) с использованием расчетов DFT из первых принципов. На рис. 12 показана электронная зонная структура NbTe 2 вдоль направлений высокой симметрии зоны Бриллюэна, которая изображена на рис. 2с. Уровень Ферми (E F ) обозначен пунктирной линией. Он пересекает полосы по нескольким направлениям зоны Бриллюэна, как это происходит в металлических системах (примеры указаны стрелками на рис. 12). Однако большое количество полос пересекается сверху и снизу E 9.
Кумар и др. . 23 использовал DFT для расчета зонной структуры и DOS для гипотетической гексагональной фазы NbTe 2 (политип 2H), а также обнаружил металлическое поведение. Хотя расчеты проводились для сравнения с различными дихалькогенидами ниобия с гексагональной структурой, фаза 2H никогда не наблюдалась для NbTe 2 . В этой работе сообщается о зонной структуре и плотности состояний дителлурида ниобия с учетом реальной структуры материала (, т.е. , моноклинная симметрия с изогнутыми плоскостями Te) с использованием расчетов DFT из первых принципов. На рис. 12 показана электронная зонная структура NbTe 2 вдоль направлений высокой симметрии зоны Бриллюэна, которая изображена на рис. 2с. Уровень Ферми (E F ) обозначен пунктирной линией. Он пересекает полосы по нескольким направлениям зоны Бриллюэна, как это происходит в металлических системах (примеры указаны стрелками на рис. 12). Однако большое количество полос пересекается сверху и снизу E 9. 0394 F в противоположную сторону вокруг уровня Ферми, оставляя частично заполненные валентную зону и зону проводимости. Это наблюдение, удельное сопротивление порядка 10 -4 Ом·см и тот факт, что плотность состояний вблизи энергии Ферми близка к минимуму, , т.е. Ом. образующие псевдощель (отличающиеся относительно небольшим числом электронных состояний), являются отличительными свойствами полуметалла. Для сравнения, удельное сопротивление металлических материалов обычно находится в диапазоне 10 −5 –10 −6 Ом·см, с плотностью электронов проводимости более 10 22 см −3 . Обычные полуметаллы имеют удельное сопротивление порядка 10 -4 Ом·см с плотностью свободных носителей от 10 17 до 10 20 см -3 24 .
0394 F в противоположную сторону вокруг уровня Ферми, оставляя частично заполненные валентную зону и зону проводимости. Это наблюдение, удельное сопротивление порядка 10 -4 Ом·см и тот факт, что плотность состояний вблизи энергии Ферми близка к минимуму, , т.е. Ом. образующие псевдощель (отличающиеся относительно небольшим числом электронных состояний), являются отличительными свойствами полуметалла. Для сравнения, удельное сопротивление металлических материалов обычно находится в диапазоне 10 −5 –10 −6 Ом·см, с плотностью электронов проводимости более 10 22 см −3 . Обычные полуметаллы имеют удельное сопротивление порядка 10 -4 Ом·см с плотностью свободных носителей от 10 17 до 10 20 см -3 24 .
Электронная зонная структура и плотность состояний NbTe 2 . Стрелки указывают примеры пересечений зон вокруг E F , которые приводят к частичному заполнению валентной зоны и зоны проводимости. Направления и точки зоны Бриллюэна с высокой симметрией показаны на рис. 2в. Ориентировочно цвета точек высокой симметрии зоны Бриллюэна на рис. 2с и цвета соответствующих вертикальных линий на рис. 12 соответствуют друг другу.
Направления и точки зоны Бриллюэна с высокой симметрией показаны на рис. 2в. Ориентировочно цвета точек высокой симметрии зоны Бриллюэна на рис. 2с и цвета соответствующих вертикальных линий на рис. 12 соответствуют друг другу.
Изображение полного размера
Динамика решетки
Динамика решетки материала связана с важными физическими свойствами, такими как электронные, термодинамические и в целом с энергетикой материала. Это происходит из-за нескольких механизмов, которые включают взаимодействие между другими элементарными возбуждениями и фононами, что подчеркивает актуальность определения динамики решетки материала для лучшего понимания его физических свойств. На сегодняшний день колебательные свойства NbTe 2 для реальной моноклинной структуры не определены. Здесь мы представляем результаты DFT-расчетов фононных дисперсионных кривых (PDC) и соответствующих состояний состояний с учетом реальной кристаллической структуры NbTe 2 . Кроме того, экспериментальные частоты, определенные с помощью рамановской спектроскопии, сравниваются с рассчитанными для мод с рамановской активностью. На сегодняшний день информация о колебательных свойствах NbTe 2 весьма скудна, существует лишь несколько сообщений на эту тему. Эрдоган и Кирби представили первое схематическое изображение PDC для неискаженной тригональной фазы (1T) NbTe 9.0394 2 4 , однако из-за простого подхода с использованием силовых констант 1T-TaS 2 и соображений симметрии, основанных на приближенной идеальной структуре, результаты расходятся с экспериментальными частотами фононов, найденными той же группой. Батталья и др. . 5 рассчитал PDC для тригонального NbTe 2 с использованием DFT; однако их PDC показал некоторые ветви, соответствующие отрицательным частотам, как свидетельство динамической нестабильности, вызванной использованием нереалистичной кристаллической структуры. Здесь расчет PDC для реальной моноклинной структуры NbTe 2 были выполнены методами DFT, как описано в методах. На рисунках 13 и 14 показаны рассчитанная PDC и соответствующая плотность состояний для NbTe 2 соответственно.
На сегодняшний день информация о колебательных свойствах NbTe 2 весьма скудна, существует лишь несколько сообщений на эту тему. Эрдоган и Кирби представили первое схематическое изображение PDC для неискаженной тригональной фазы (1T) NbTe 9.0394 2 4 , однако из-за простого подхода с использованием силовых констант 1T-TaS 2 и соображений симметрии, основанных на приближенной идеальной структуре, результаты расходятся с экспериментальными частотами фононов, найденными той же группой. Батталья и др. . 5 рассчитал PDC для тригонального NbTe 2 с использованием DFT; однако их PDC показал некоторые ветви, соответствующие отрицательным частотам, как свидетельство динамической нестабильности, вызванной использованием нереалистичной кристаллической структуры. Здесь расчет PDC для реальной моноклинной структуры NbTe 2 были выполнены методами DFT, как описано в методах. На рисунках 13 и 14 показаны рассчитанная PDC и соответствующая плотность состояний для NbTe 2 соответственно. В последнем разрыв возникает для частот между и . 227 см −1 и 243 см −1 . Подчеркнута актуальность учета искажения плоскостей Te реальной структуры (в отличие от идеальной 1T-фазы), поскольку оно обеспечивает материалу структурную и динамическую устойчивость. Для NbTe 2 , использование реальной структуры с искаженными плоскостями Te необходимо для избежания получения отрицательных частот акустических фононов, т. е. для динамической устойчивости решетки. Число оптических фононов в кристаллах подчиняется соотношению: B opt = 3N − 3, где N — число атомов в примитивной ячейке 25 , в данном случае N = 9, так что B opt = 24. Анализ теории групп показывает, что разложение на неприводимые представления оптических мод в центре зоны:
В последнем разрыв возникает для частот между и . 227 см −1 и 243 см −1 . Подчеркнута актуальность учета искажения плоскостей Te реальной структуры (в отличие от идеальной 1T-фазы), поскольку оно обеспечивает материалу структурную и динамическую устойчивость. Для NbTe 2 , использование реальной структуры с искаженными плоскостями Te необходимо для избежания получения отрицательных частот акустических фононов, т. е. для динамической устойчивости решетки. Число оптических фононов в кристаллах подчиняется соотношению: B opt = 3N − 3, где N — число атомов в примитивной ячейке 25 , в данном случае N = 9, так что B opt = 24. Анализ теории групп показывает, что разложение на неприводимые представления оптических мод в центре зоны:
$${B}_{opt}=8{A}_{g}+4{A}_{u}+4{B}_{g}+8{B}_{u}.$$
Рисунок 13 Дисперсионные кривые фононов NbTe 2 .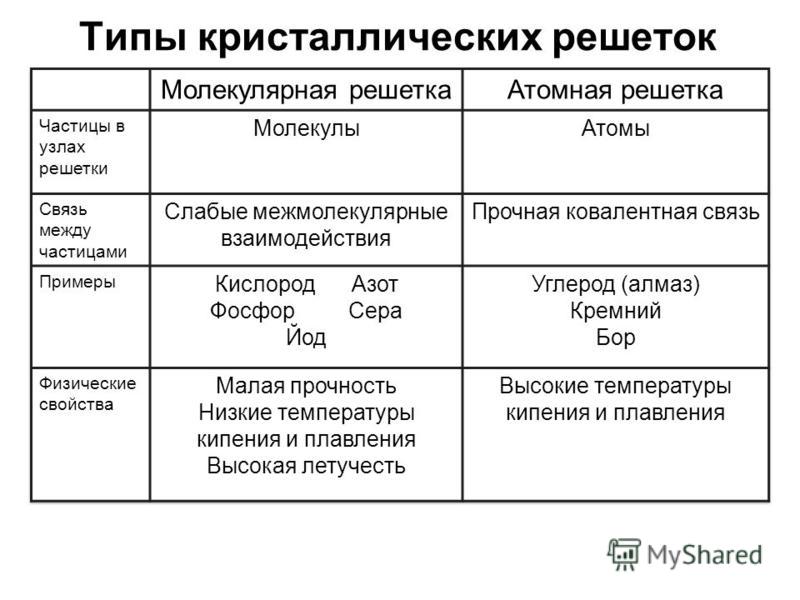 Направления и точки зоны Бриллюэна с высокой симметрией показаны на рис. 2в. Для справки: цвета точек высокой симметрии зоны Бриллюэна на рис. 2с и цвета соответствующих вертикальных линий на этом рисунке соответствуют друг другу. Заштрихованные области соответствуют энергиям фононов с низкой дисперсией (, т.е. , высокая плотность состояний) вдоль направлений высокой симметрии Z-Γ-AM. Энергетическое разделение этих зон согласуется с энергией Х-моды (60 см −1 , см. ниже) в фононно-разностном процессе. В центре зоны (Г) этому процессу соответствует разность B g 4 (169,7 см −1 ) − B g 3 (109,8 см −1 ), где частоты являются экспериментальными.
Направления и точки зоны Бриллюэна с высокой симметрией показаны на рис. 2в. Для справки: цвета точек высокой симметрии зоны Бриллюэна на рис. 2с и цвета соответствующих вертикальных линий на этом рисунке соответствуют друг другу. Заштрихованные области соответствуют энергиям фононов с низкой дисперсией (, т.е. , высокая плотность состояний) вдоль направлений высокой симметрии Z-Γ-AM. Энергетическое разделение этих зон согласуется с энергией Х-моды (60 см −1 , см. ниже) в фононно-разностном процессе. В центре зоны (Г) этому процессу соответствует разность B g 4 (169,7 см −1 ) − B g 3 (109,8 см −1 ), где частоты являются экспериментальными.
Изображение полного размера
Рис. 14Фононная плотность состояний NbTe 2 .
Полноразмерное изображение
Двенадцать режимов (8 A г +4 B G ) активны комбинации, в то время как другие двенадцать (4 A U +8 B U 1. На рис. 15 показаны рассчитанные частоты, тип и неприводимое представление рамановских активных нормальных мод дителлурида ниобия. Кроме того, включено графическое представление атомных смещений каждой нормальной моды.
На рис. 15 показаны рассчитанные частоты, тип и неприводимое представление рамановских активных нормальных мод дителлурида ниобия. Кроме того, включено графическое представление атомных смещений каждой нормальной моды.
Характеристики рамановских активных нормальных мод NbTe 2 .
Изображение полного размера
Эрдоган и Кирби 4 сообщили о спектре комбинационного рассеяния для NbTe 2 при различных температурах. Они обнаружили одиннадцать активных рамановских мод в диапазоне частот от 30 см −1 до 260 см −1 , используя в качестве источника возбуждения лазер с длиной волны 514,5 нм. Рассчитанные частоты (рис. 15) показывают, что NbTe 2 имеет двенадцать активных рамановских мод в диапазоне частот, измеренных Эрдоганом и Кирби, то есть они не смогли обнаружить ни одну из этих мод (см. ниже). Спектры комбинационного рассеяния NbTe 916 показаны кристаллы 0394 2 , полученные при комнатной температуре с тремя различными длинами волн возбуждения: 785 нм, 633 нм и 488 нм. На этом рисунке можно наблюдать одиннадцать мод, описанных Эрдоганом и Кирби. Замечено, что спектры на рис. 16 представляют одни и те же пики, независимо от длины волны возбуждения, с разной относительной интенсивностью. Общей чертой спектров на рис. 16 является большая интенсивность пика при 84 см -1 . Эта полоса соответствует полностью симметричной моде A g 2 , рис. 15. Полностью симметричные моды обычно связаны с большими вариациями электронной восприимчивости, что дает сильные пиковые интенсивности. Изменения относительной интенсивности мод на рис. 16 для различных энергий возбуждения (1,58 эВ/785 нм, 1,96 эВ/633 нм и 2,54 эВ/488 нм) являются следствием различного резонансного или околорезонансного электронного переходы, активируемые для каждой длины волны лазера в довольно сложной электронной зонной структуре NbTe 2 , рис. 12, в процессе неупругого рассеяния света. Действительно, тензор комбинационного рассеяния является функцией резонансных или околорезонансных условий неупругого рассеяния 26 , что, следовательно, влияет на интенсивность каждой колебательной моды, поскольку интенсивность моды комбинационного рассеяния пропорциональна изменению компонент тензора комбинационного рассеяния.
На этом рисунке можно наблюдать одиннадцать мод, описанных Эрдоганом и Кирби. Замечено, что спектры на рис. 16 представляют одни и те же пики, независимо от длины волны возбуждения, с разной относительной интенсивностью. Общей чертой спектров на рис. 16 является большая интенсивность пика при 84 см -1 . Эта полоса соответствует полностью симметричной моде A g 2 , рис. 15. Полностью симметричные моды обычно связаны с большими вариациями электронной восприимчивости, что дает сильные пиковые интенсивности. Изменения относительной интенсивности мод на рис. 16 для различных энергий возбуждения (1,58 эВ/785 нм, 1,96 эВ/633 нм и 2,54 эВ/488 нм) являются следствием различного резонансного или околорезонансного электронного переходы, активируемые для каждой длины волны лазера в довольно сложной электронной зонной структуре NbTe 2 , рис. 12, в процессе неупругого рассеяния света. Действительно, тензор комбинационного рассеяния является функцией резонансных или околорезонансных условий неупругого рассеяния 26 , что, следовательно, влияет на интенсивность каждой колебательной моды, поскольку интенсивность моды комбинационного рассеяния пропорциональна изменению компонент тензора комбинационного рассеяния.
Спектры комбинационного рассеяния NbTe 2 при комнатной температуре, полученные с различными длинами волн возбуждения, указанными в правом верхнем углу каждой панели. На вставке показана мода, о которой ранее не сообщалось, на частоте 100,5 см 9 .0712 −1 с симметрией B g .
Полноразмерное изображение
На рисунке 16 показаны одиннадцать полос Рамана, описанных в исх. 4 и два дополнительных пика. Как упоминалось выше, теория групп предсказывает двенадцать активных рамановских мод для NbTe 2 . Расчеты указывают на активную моду комбинационного рассеяния с частотой около 102 см −1 , рис. 15, о которой ранее не сообщалось. На вставке к рис. 16 показаны детали этой области, где в спектре, полученном с линией возбуждения 785 нм, можно наблюдать слабую полосу на 100,5 см −1 . Согласно нашим расчетам, рис. 15, этот фонон имеет B г симметрия.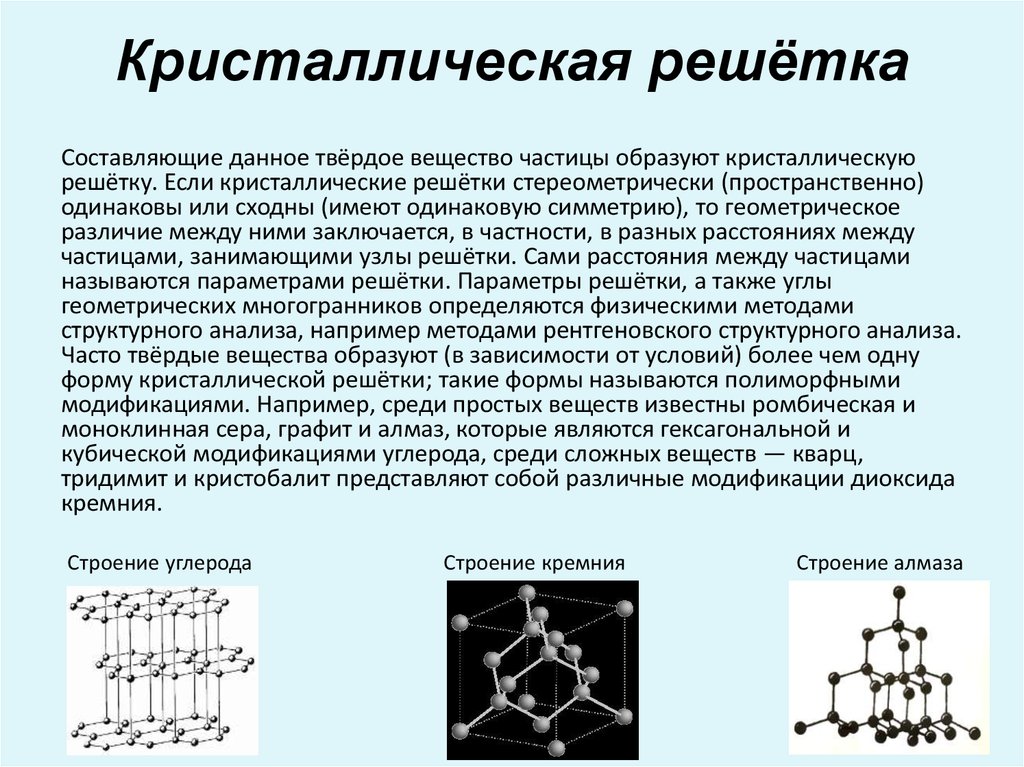 В таблице 2 показано сравнение экспериментальных частот рамановских мод, измеренных в этой работе, с частотами, указанными в ссылке. 4 и вычисленные частоты ДПФ (рис. 15). Можно заметить, что существует хорошее соответствие между экспериментальной и расчетной частотами. С инструментальной точки зрения получение спектров комбинационного рассеяния с линией 785 нм имело два преимущества по сравнению со спектрами, полученными с двумя другими лазерными линиями: i) более высокое разрешение (полученное за счет оптики дифракционной решетки) и (ii) возможность обнаружения мод с частотами, близкими к лазерной линии (каждая линия возбуждения используется в сочетании с определенным краевым фильтром с определенными характеристиками отсечки лазерной линии). Таковы причины возникновения спектра на несколько более низких частотах для линии лазера 785 нм на рис. 16 по сравнению со спектрами, полученными с линиями 633 и 488 нм. Благодаря этой возможности стало возможным обнаружить дополнительную моду на 60,5 см -1 , помеченный X-модой на левой панели рис.
В таблице 2 показано сравнение экспериментальных частот рамановских мод, измеренных в этой работе, с частотами, указанными в ссылке. 4 и вычисленные частоты ДПФ (рис. 15). Можно заметить, что существует хорошее соответствие между экспериментальной и расчетной частотами. С инструментальной точки зрения получение спектров комбинационного рассеяния с линией 785 нм имело два преимущества по сравнению со спектрами, полученными с двумя другими лазерными линиями: i) более высокое разрешение (полученное за счет оптики дифракционной решетки) и (ii) возможность обнаружения мод с частотами, близкими к лазерной линии (каждая линия возбуждения используется в сочетании с определенным краевым фильтром с определенными характеристиками отсечки лазерной линии). Таковы причины возникновения спектра на несколько более низких частотах для линии лазера 785 нм на рис. 16 по сравнению со спектрами, полученными с линиями 633 и 488 нм. Благодаря этой возможности стало возможным обнаружить дополнительную моду на 60,5 см -1 , помеченный X-модой на левой панели рис. 16. Чтобы определить происхождение этой моды, были получены низкотемпературные спектры комбинационного рассеяния в диапазоне 80–300 K. Эти спектры показаны на рис. 17. Более низкие температуры приводят к более высоким частотам фононов вследствие термически индуцированного сжатия решетки. Такое поведение наблюдается для рамановских активных фононов, предсказанных теорией групп для NbTe 2 , как показано на рис. 17c, что контрастирует с поведением X-моды, частота которой оставалась постоянной для всего диапазона температур, рис. 17a, в. Такое поведение предполагает фононно-разностный процесс как источник этой моды. Назначение такого процесса должно быть основано на соображениях симметрии, поскольку вероятность возникновения физических процессов увеличивается вокруг высокосимметричных точек и направлений обратной решетки. Центр зоны Бриллюэна, точка Γ, обладает наибольшей симметрией, поскольку обладает кристаллической симметрией. На рисунке 2 показаны другие точки высокой симметрии (A, M и Z) в первой зоне Бриллюэна дителлурида ниобия.
16. Чтобы определить происхождение этой моды, были получены низкотемпературные спектры комбинационного рассеяния в диапазоне 80–300 K. Эти спектры показаны на рис. 17. Более низкие температуры приводят к более высоким частотам фононов вследствие термически индуцированного сжатия решетки. Такое поведение наблюдается для рамановских активных фононов, предсказанных теорией групп для NbTe 2 , как показано на рис. 17c, что контрастирует с поведением X-моды, частота которой оставалась постоянной для всего диапазона температур, рис. 17a, в. Такое поведение предполагает фононно-разностный процесс как источник этой моды. Назначение такого процесса должно быть основано на соображениях симметрии, поскольку вероятность возникновения физических процессов увеличивается вокруг высокосимметричных точек и направлений обратной решетки. Центр зоны Бриллюэна, точка Γ, обладает наибольшей симметрией, поскольку обладает кристаллической симметрией. На рисунке 2 показаны другие точки высокой симметрии (A, M и Z) в первой зоне Бриллюэна дителлурида ниобия. С учетом частоты Х-моды (60,5 см −1 ) и характеристики фононных дисперсионных кривых вокруг точек высокой симметрии зоны Бриллюэна, рис. 13, целесообразно отнести эту моду к фононно-разностному процессу B g 4 (169,7 см −1 ) − B g 3 (109,8 см −1 ), где мы использовали экспериментальные частоты указанных фононов, приведенные в таблице 2. Фактически, на рис. 13 видно, что на этих частотах несколько ветвей в направлениях Z-Г-А-М (заштрихованные области на рис. 13) довольно бездисперсионны ( т.е. . flat), что переводится в максимумы однофононной плотности состояний, рис. 14.
С учетом частоты Х-моды (60,5 см −1 ) и характеристики фононных дисперсионных кривых вокруг точек высокой симметрии зоны Бриллюэна, рис. 13, целесообразно отнести эту моду к фононно-разностному процессу B g 4 (169,7 см −1 ) − B g 3 (109,8 см −1 ), где мы использовали экспериментальные частоты указанных фононов, приведенные в таблице 2. Фактически, на рис. 13 видно, что на этих частотах несколько ветвей в направлениях Z-Г-А-М (заштрихованные области на рис. 13) довольно бездисперсионны ( т.е. . flat), что переводится в максимумы однофононной плотности состояний, рис. 14.
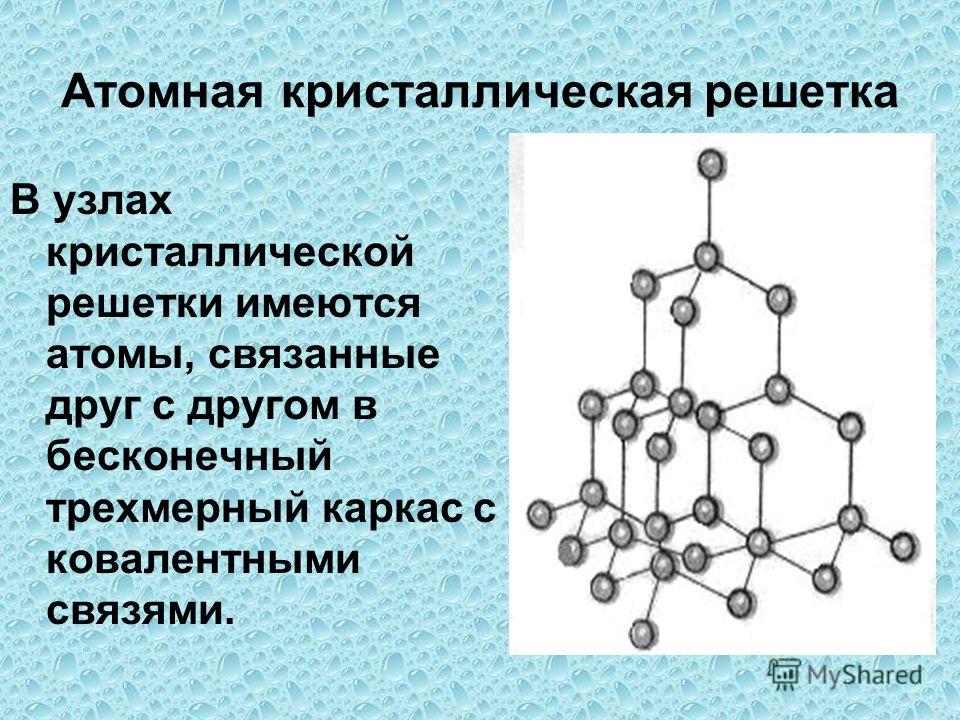
Увеличить
Выводы
Физические свойства ниобия NbTe 2 изучены экспериментально и теоретически. Для расчетов из первых принципов реальная кристаллическая структура NbTe 2 , в отличие от предыдущих работ, где использовались приблизительные, идеальные структуры. Электронная зонная структура, фононные дисперсионные кривые и соответствующая им плотность состояний были рассчитаны в рамках теории функционала плотности. Другие рассчитанные свойства включают энергию когезии (-13,22 эВ на формульную единицу), теплоту образования (-1,38 эВ на формульную единицу), объемный модуль (38,5904 ГПа) и его производную (6,025). Экспериментальные исследования структурных, композиционных, электронных и колебательных свойств проводились на NbTe 2 кристаллов. Параметры решетки, полученные с помощью уточнения Ритвельдом рентгенограмм, хорошо согласовывались с изображениями просвечивающей электронной микроскопии с атомарным разрешением. Характеристики и контраст изображений ПЭМ с преобразованием Фурье указывают на высокое кристаллическое качество образцов NbTe 2 . Распределение элементов в наномасштабе и химический состав оценивали с помощью атомно-зондовой томографии. Работа выхода для NbTe 2 составила 5,32 эВ, как определено из экспериментов по ультрафиолетовой фотоэлектронной спектроскопии. Из измерений эффекта Холла удельное сопротивление (1,74 × 10 -4 Ом·см), плотности свободных электронов (5,4 × 10 21 см -3 ) и подвижности (6,9 см 2 /Вс). Эти значения вместе с псевдощелью, образующейся вокруг уровня Ферми в плотности электронных состояний, согласуются с полуметаллическими характеристиками. Известно, что удельное электрическое сопротивление остается почти постоянным от 100 K до 400 K, что указывает на то, что электрон-фононное рассеяние не играет существенной роли в процессах переноса заряда для этого диапазона температур. Определены смещения атомов для двенадцати рамановских активных нормальных мод, предсказанных теорией групп. Расчетные частоты этих мод хорошо соответствовали значениям, найденным экспериментально.
Распределение элементов в наномасштабе и химический состав оценивали с помощью атомно-зондовой томографии. Работа выхода для NbTe 2 составила 5,32 эВ, как определено из экспериментов по ультрафиолетовой фотоэлектронной спектроскопии. Из измерений эффекта Холла удельное сопротивление (1,74 × 10 -4 Ом·см), плотности свободных электронов (5,4 × 10 21 см -3 ) и подвижности (6,9 см 2 /Вс). Эти значения вместе с псевдощелью, образующейся вокруг уровня Ферми в плотности электронных состояний, согласуются с полуметаллическими характеристиками. Известно, что удельное электрическое сопротивление остается почти постоянным от 100 K до 400 K, что указывает на то, что электрон-фононное рассеяние не играет существенной роли в процессах переноса заряда для этого диапазона температур. Определены смещения атомов для двенадцати рамановских активных нормальных мод, предсказанных теорией групп. Расчетные частоты этих мод хорошо соответствовали значениям, найденным экспериментально. Было определено, что частота не обнаруженной ранее рамановской моды составляет 100,5 см −1 . Из низкотемпературных измерений комбинационного рассеяния света колебательная мода с частотой 60,5 см 90 712 -1 90 713 была отнесена к фононно-разностным процессам с участием фононов, связанных с направлениями высокой симметрии в обратном пространстве. Наконец, отмечается, что о большинстве физических свойств, определенных в этой работе, ранее не сообщалось.
Было определено, что частота не обнаруженной ранее рамановской моды составляет 100,5 см −1 . Из низкотемпературных измерений комбинационного рассеяния света колебательная мода с частотой 60,5 см 90 712 -1 90 713 была отнесена к фононно-разностным процессам с участием фононов, связанных с направлениями высокой симметрии в обратном пространстве. Наконец, отмечается, что о большинстве физических свойств, определенных в этой работе, ранее не сообщалось.
Методы
Детали эксперимента
Кристаллы дителлурида ниобия выращивали методом паротранспорта в вакуумированной кварцевой ампуле. Рентгеноструктурные измерения проводили на дифрактометре Rigaku Dmax 2100 с использованием медной мишени в качестве источника излучения (λ = 1,54056 Å). Изображения просвечивающей электронной микроскопии высокого разрешения (HRTEM) были получены на просвечивающем электронном микроскопе Jeol JEM-2200FS. Элементный состав определяли с помощью анализов с помощью лазерной атомно-зондовой томографии (АРТ), которые проводились с использованием системы атомных зондов с локальным электродом (LEAP™ 5000 XS от Cameca Instruments). Анализы APT проводились при базовой температуре 60 K в импульсном лазерном режиме с длиной волны 355 нм, длительностью импульса ~10 пс, частотой импульса 200 кГц, энергией 40пДж и скоростью обнаружения 10 ионов на 1000 пульс сохранялся. Образцы APT были приготовлены с использованием двухлучевого сфокусированного ионного пучка (FEI Helios Nanolab 600i) в соответствии с процедурой, описанной в 9.0712 27 . Изображения сканирующей электронной микроскопии (СЭМ) были получены с помощью системы JEOL JSM-7401F. Данные ультрафиолетовой фотоэлектронной спектроскопии получены на установке Thermo Fisher Escalab 250Xi с использованием линии гелия I с энергией 21,22 эВ. К образцу прикладывали смещение -5 В, чтобы сместить границу спектра от области границы спектрометра. Для электрических измерений при комнатной температуре (22 °C) использовалась система на эффекте Холла Ecopia HMS5000 для определения удельного сопротивления, концентрации носителей и подвижности. Исследование зависимости удельного электросопротивления от температуры проводили в системе Холла Nanometrics HL5500PC методом Ван-дер-Пау.
Анализы APT проводились при базовой температуре 60 K в импульсном лазерном режиме с длиной волны 355 нм, длительностью импульса ~10 пс, частотой импульса 200 кГц, энергией 40пДж и скоростью обнаружения 10 ионов на 1000 пульс сохранялся. Образцы APT были приготовлены с использованием двухлучевого сфокусированного ионного пучка (FEI Helios Nanolab 600i) в соответствии с процедурой, описанной в 9.0712 27 . Изображения сканирующей электронной микроскопии (СЭМ) были получены с помощью системы JEOL JSM-7401F. Данные ультрафиолетовой фотоэлектронной спектроскопии получены на установке Thermo Fisher Escalab 250Xi с использованием линии гелия I с энергией 21,22 эВ. К образцу прикладывали смещение -5 В, чтобы сместить границу спектра от области границы спектрометра. Для электрических измерений при комнатной температуре (22 °C) использовалась система на эффекте Холла Ecopia HMS5000 для определения удельного сопротивления, концентрации носителей и подвижности. Исследование зависимости удельного электросопротивления от температуры проводили в системе Холла Nanometrics HL5500PC методом Ван-дер-Пау. Спектры комбинационного рассеяния были получены на микро-рамановском спектрометре Horiba LabRAM HR Evolution с использованием длин волн возбуждения 488 нм, 633 нм и 785 нм и дифракционной решетки 1800 штр/мм. Все спектры КР были измерены на свежесколотых поверхностях NbTe 2 кристалл.
Спектры комбинационного рассеяния были получены на микро-рамановском спектрометре Horiba LabRAM HR Evolution с использованием длин волн возбуждения 488 нм, 633 нм и 785 нм и дифракционной решетки 1800 штр/мм. Все спектры КР были измерены на свежесколотых поверхностях NbTe 2 кристалл.
Теоретические расчеты
Расчеты по первому принципу были выполнены с использованием кода VASP 28,29,30,31 , где была использована обменно-корреляционная функциональная форма Пердью-Берка-Эрнзергофа (PBE) обобщенного градиентного приближения (GGA) 32,33 . Энергия отсечки плоской волны была зафиксирована на уровне 425 эВ. Энергетическая сходимость между двумя последовательными самосогласованными шагами была установлена равной 10 -6 эВ. Положения атомов и параметры решетки оптимизировались до тех пор, пока общая сила, действующая на каждый атом (силы Хеллмана-Фейнмана), не стала ниже 0,01 эВ/Å. Зона Бриллюэна была проанализирована с использованием схемы Монкхорста-Пака через сетку 3 × 14 × 7 для релаксации структуры. Сетка была увеличена до 6 × 28 × 14 в расчетах статики и плотности состояний (DOS). Колебательные свойства рассчитывались с помощью программы PHONON 9.0712 34,35 с VASP в качестве внешней программы ab initio . Для этой цели использовалась суперячейка из 144 атомов и сетка 2 × 6 × 4 из k пространства. Параметр сходимости для двух последовательных шагов самосогласованного поля был зафиксирован на уровне 10 −8 эВ. Все структурные изображения кристаллической решетки выполнены с помощью VESTA 36 .
Сетка была увеличена до 6 × 28 × 14 в расчетах статики и плотности состояний (DOS). Колебательные свойства рассчитывались с помощью программы PHONON 9.0712 34,35 с VASP в качестве внешней программы ab initio . Для этой цели использовалась суперячейка из 144 атомов и сетка 2 × 6 × 4 из k пространства. Параметр сходимости для двух последовательных шагов самосогласованного поля был зафиксирован на уровне 10 −8 эВ. Все структурные изображения кристаллической решетки выполнены с помощью VESTA 36 .
Доступность данных
Наборы данных, созданные в ходе текущего исследования, можно получить у соответствующего автора по обоснованному запросу.
Ссылки
Чховалла М. и др. . Химия двумерных слоистых нанолистов дихалькогенидов переходных металлов. Нац. хим. 5 , 263–275 (2013).
Артикул Google ученый
- “>
Ван, К. Х., Калантар-Заде, К., Кис, А., Коулман, Дж. Н. и Страно, М. С. Электроника и оптоэлектроника двумерных дихалькогенидов переходных металлов. Нац. Нанотехно. 7 , 699–712 (2012).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Нагата С., Абэ Т., Терашима С., Исихара Ю. и Цуцуми К. Сверхпроводимость в соединении со слоистой структурой NbTe 2 . Физ. B 194–196 , 1981–1982 (1994).
ОБЪЯВЛЕНИЯ Статья Google ученый
Эрдоган, Х. и Кирби, Р. Д. Спектр комбинационного рассеяния и динамика решетки NbTe 2 . Твердотельный коммуник. 70 , 713–715 (1989).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Батталья, К. и др. . Наведенное поверхностью Ферми искажение решетки в NbTe 2 .
 Физ. Ред. B 72 , 1
Физ. Ред. B 72 , 1-1–1
-10 (2005 г.).
Браун, Б. Э. Кристаллические структуры NbTe 2 и TaTe 2 . Acta Кристаллогр. 20 , 264–267 (1966).
КАС Статья Google ученый
Guinebretière, R. Дифракция рентгеновских лучей на поликристаллических материалах , стр. 147–153 (ISTE Ltd, Лондон, 2007).
Книга Google ученый
Rodríguez-Carvajal, J. Последние достижения в определении магнитной структуры методом порошковой нейтронной дифракции. Физ. Б 192 , 55–69 (1993).
ОБЪЯВЛЕНИЯ Статья Google ученый
Грилло, В. и Ротунно, Э. STEM_CELL: Программный инструмент для электронной микроскопии: Часть I-моделирование. Ультрамикроскопия 125 , 97–111 (2013).

КАС Статья Google ученый
Грилло, В. и Росси, Ф. STEM_CELL: Программный инструмент для электронной микроскопии. Часть 2 Анализ кристаллических материалов. Ультрамикроскопия 125 , 112–129 (2013).
КАС пабмед Google ученый
Мюллер, М., Сакси, Д. В., Смит, Г. Д. У. и Голт, Б. Некоторые аспекты поведения GaSb при испарении в поле. Ультрамикроскопия 111 , 487–492 (2011).
Артикул Google ученый
Манчини, Л. и др. . Состав широкозонных полупроводниковых материалов и наноструктур, измеренный методом атомно-зондовой томографии, и его зависимость от поверхностного электрического поля. J. Phys. хим. C 118 , 24136–24151 (2014).
КАС Статья Google ученый
- “>
Джустино, Ф. Равновесные структуры материалов: расчет и эксперимент. В Моделирование материалов с использованием теории функционала плотности: свойства и прогнозы , стр. 66–86 (Oxford University Press, Оксфорд, 2014).
Чжан, Х. и др. . Энтальпии образования соединений магния из первопринципных расчетов. Интерметаллиды 17 , 878–885 (2009).
КАС Статья Google ученый
Гаскелл, Д. Р. Теплоемкость, энтальпия, энтропия и третий закон термодинамики. В Введение в термодинамику материалов 4-е изд. ., стр. 125–172 (Тейлор и Фрэнсис, Лондон, 2009 г.).
Гаскелл, Д. Р. Вспомогательные функции. В Введение в термодинамику материалов, 4-е изд. ., стр. 97–123 (Taylor & Francis, London, 2009).
Дронсковски Р. Энергия, энтальпия, энтропия и энергия Гиббса.
 В Computational Chemistry of Solid State Materials , стр. 158–160 (WILEY-VCH, Weinheim, 2005).
В Computational Chemistry of Solid State Materials , стр. 158–160 (WILEY-VCH, Weinheim, 2005).Тилли, Р. Дж. Д. Дополнительный материал к части 4: Физические свойства. В Понимание твердых тел: наука о материалах , стр. 543–561 (John Wiley & Sons Ltd, Чичестер, 2004).
Берч Ф. Конечная упругая деформация кубических кристаллов. Физ. Ред. 71 , 809–824 (1947).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Brixner, L. H. Получение и свойства монокристаллических селенидов и теллуридов типа AB 2 ниобия, тантала, молибдена и вольфрама. Дж. Неорг. Нукл. хим. 24 , 257–263 (1962).
КАС Статья Google ученый
Selte, K. & Kjekshus, A. О магнитных свойствах селенидов и теллуридов ниобия.
 Acta Chem. Сканд. 19 , 258–260 (1965).
Acta Chem. Сканд. 19 , 258–260 (1965).КАС Статья Google ученый
Дерри Г. Н., Керн М. Э. и Уорт Э. Х. Рекомендуемые значения работы выхода чистой металлической поверхности. Дж. Вак. науч. Технол . 33 , 060801-1-060801-9 (2015).
Артикул Google ученый
Кумар, А. и Ахлувалиа, П.К. Влияние квантового ограничения на электронные и диэлектрические свойства дихалькогенидов ниобия NbX 2 (X = S, Se, Te). J. Alloys Compd. 550 , 283–291 (2013).
КАС Статья Google ученый
Бернс, Г. Физика твердого тела , с. 339 (Академическое издательство, Сан-Диего, 1985).
Шривастава Г. П. Физика фононов , с. 32 (Адам Хилгер, Бристоль, 1990).

Сноук, Д. В. Физика твердого тела: основные понятия , с. 367 (Аддисон-Уэсли, Сан-Франциско, 2009 г.).
Томпсон, К. и др. . In-situ подготовка образцов для проведения атомно-зондовой томографии на месте. Ультрамикроскопия 107 , 131–139 (2007).
КАС Статья Google ученый
Кресс, Г. и Хафнер, Дж. Молекулярная динамика Ab initio для жидких металлов. Физ. Rev. B 47 , 558–561 (1993).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Крессе, Г. и Хафнер, Дж. Моделирование молекулярной динамики Ab initio перехода жидкий металл-аморфный полупроводник в германии. Физ. Ред. B 49 , 14251–14269 (1994).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
- “>
Крессе, Г. и Фуртмюллер, Дж. Эффективность расчетов полной энергии ab-initio для металлов и полупроводников с использованием базисного набора плоских волн. Вычисл. Матер. науч. 6 , 15–50 (1996).
КАС Статья Google ученый
Крессе, Г. и Фуртмюллер, Дж. Эффективные итерационные схемы для неэмпирических расчетов полной энергии с использованием базисного набора плоских волн. Физ. Ред. B 54 , 11169–11186 (1996).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Пердью, Дж. П., Берк, К. и Эрнзерхоф, М. Упрощенное приближение обобщенного градиента. Физ. Преподобный Летт. 77 , 3865–3868 (1996).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Пердью, Дж. П., Берк, К. и Эрнзерхоф, М.
 Опечатка: аппроксимация обобщенного градиента стала проще. Физ. Преподобный Летт. 78 , 1396–1396 (1997).
Опечатка: аппроксимация обобщенного градиента стала проще. Физ. Преподобный Летт. 78 , 1396–1396 (1997).ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Парлински, К. Программное обеспечение PHONON , Краков (2013).
Парлински, К., Ли, З. и Кавазо, Ю. Первые принципы определения мягкой моды в кубическом ZrO 2 . Физ. Преподобный Летт. 78 , 4063–4066 (1997).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Момма, К. и Изуми, Ф. ВЕСТА 3 для трехмерной визуализации кристаллических, объемных и морфологических данных. J. Appl. Кристаллогр. 44 , 1272–1276 (2011).
КАС Статья Google ученый
Загрузить ссылки
Благодарности
AHBA признает Conacyt-Mexico за его докторскую степень. стипендия. SJJS выражает благодарность Conacyt-Mexico за частичную финансовую поддержку в виде гранта № 257166. Авторы благодарят Баптиста Голта за плодотворные обсуждения и благодарны Уве Тезинсу и Андреасу Штурму за их поддержку объектов APT, SEM и FIB в Институте Макса Планка для Eisenforschung. ГмбХ. TS благодарит за поддержку Немецкий исследовательский фонд (DFG) (Контракт GA 2450/1-1). Также признательна техническая помощь Ф. Родригеса Мельгарехо, М. А. Эрнандеса Ландаверде, А. Хименеса Ньето и Х. Э. Урбины Альварес.
стипендия. SJJS выражает благодарность Conacyt-Mexico за частичную финансовую поддержку в виде гранта № 257166. Авторы благодарят Баптиста Голта за плодотворные обсуждения и благодарны Уве Тезинсу и Андреасу Штурму за их поддержку объектов APT, SEM и FIB в Институте Макса Планка для Eisenforschung. ГмбХ. TS благодарит за поддержку Немецкий исследовательский фонд (DFG) (Контракт GA 2450/1-1). Также признательна техническая помощь Ф. Родригеса Мельгарехо, М. А. Эрнандеса Ландаверде, А. Хименеса Ньето и Х. Э. Урбины Альварес.
Информация о авторе
Авторы и принадлежность
Centro de Investigación y Estudios avanzados del Ipn, Unidad Querétaro, Libramiento Norponiente no 2000, Frac., Realle DeRiquilla, C.P., 763330, 760. & Sergio J. Jiménez Sandoval
Факультет физики, Университет Саймона Фрейзера, Бернаби, Британская Колумбия, V5A 1S6, Канада
J.C. Irwin
Центр исследований, Нутрида, Авансадос, Лейдадад, Университет Австралии С.
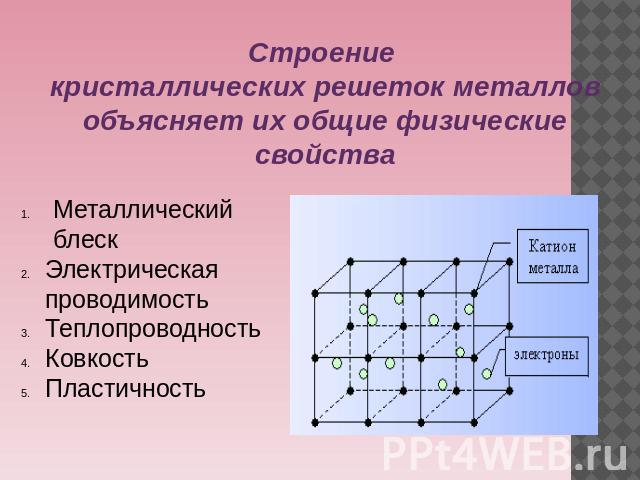 П. 66600, Мексика
П. 66600, МексикаАндрес Мануэль Гарай-Тапия
Институт Макса Планка для Eisenforschung GmbH, Max-Planck-Str. 1, 40237, Дюссельдорф, Германия
Torsten Schwarz
Centro de Investigación en Materiales Avanzados, Miguel de Cervantes 120, Complejo Industrial Chihuahua, Chihuahua, Chih., C.P. 31136, Мексика
Франциско Парагвай Дельгадо
Онтарио Центр определения характеристик современных материалов, Университет Торонто, 200 College Street, Торонто, Онтарио, M5S 3E5, Канада
P. M. Brodersen
Факультет электротехники и вычислительной техники Эдварда С. Роджерса старшего, Университет Торонто, 10 King’s College Road, Торонто, Онтарио, M5S 3G4, Канада
Раджив Принжа и Назир Керани
- 8 6 Департамент материаловедения и инженерии, Университет Торонто, 184 Колледж-стрит, Торонто, Онтарио, M5S 3E4, Канада
Назир Керани
Авторы
- Аарон Эрнан Барахас-Агилар
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- JC Irwin
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Andrés Manuel Garay-Tapia
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Торстен Шварц
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Francisco Paraguay Delgado
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- P.
 M. Brodersen
M. BrodersenПросмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Раджив Приня
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Назир Херани
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Sergio J. Jiménez Sandoval
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Вклады
А.Х.Б.А. и С.Дж.Дж.С. написал рукопись и руководил исследованием. JCI выращены кристаллы NbTe 2 , A.H.B.A. и A.M.G.T. выполнил расчеты ДПФ; Т.С. выполнили и проанализировали измерения APT; Ф.П.Д. получили изображения HRTEM; данные UPS были получены P.M.B.; Р.П. и Н.К. приняли участие и проанализировали данные электрических характеристик. А.Х.Б.А. проанализированы и смоделированы HRTEM, рентгеновская дифракция, эффект Холла, данные UPS и Raman. Спектры комбинационного рассеяния и измерения эффекта Холла были получены компанией A.H.B.A.
А.Х.Б.А. проанализированы и смоделированы HRTEM, рентгеновская дифракция, эффект Холла, данные UPS и Raman. Спектры комбинационного рассеяния и измерения эффекта Холла были получены компанией A.H.B.A.
Автор, ответственный за переписку
Переписка с Серхио Х. Хименес Сандовал.
Заявление об этике
Конкурирующие интересы
Авторы не заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Примечание издателя: Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и принадлежности к организациям.
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате, при условии, что вы укажете соответствующую ссылку на оригинальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons для статьи, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/.
Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons для статьи, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/.
Перепечатка и разрешения
Об этой статье
Эта статья цитируется
Экспериментальное исследование бинарной системы Nb-Te
- Б. С. де Лима
- Н.
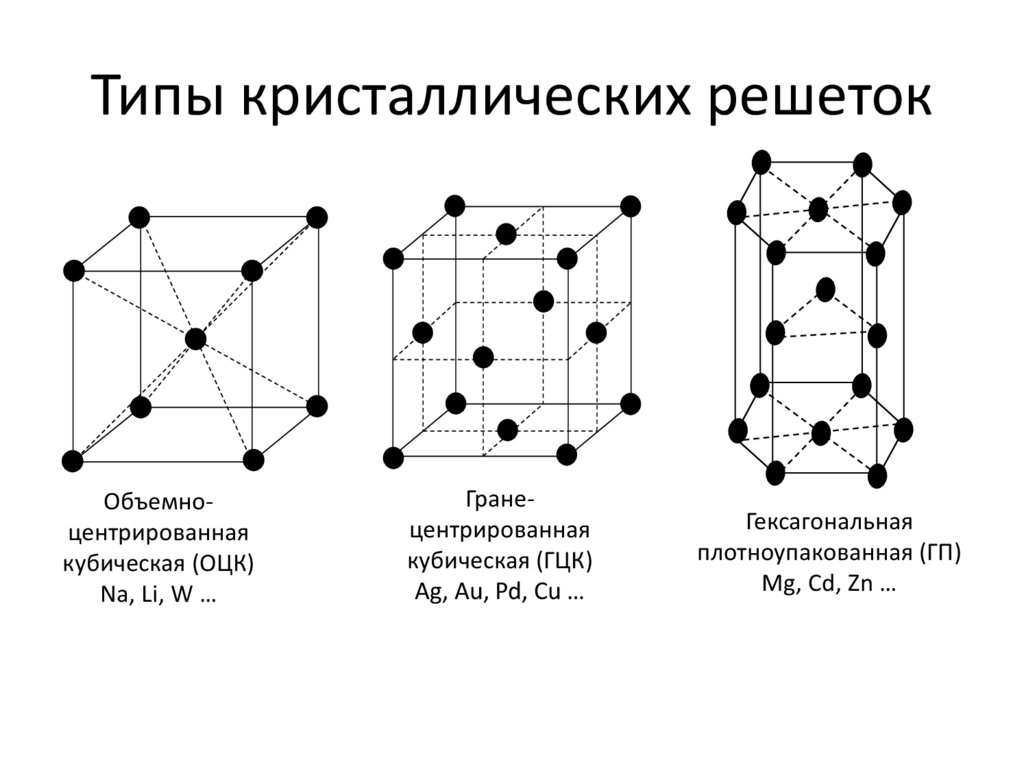 Чайя
Чайя - А. Дж. С. Мачадо
Журнал фазовых равновесий и диффузии (2019)
Комментарии
Отправляя комментарий, вы соглашаетесь соблюдать наши Условия и Правила сообщества. Если вы обнаружите что-то оскорбительное или не соответствующее нашим условиям или правилам, отметьте это как неприемлемое.
Скачать PDF
химическая перспектива кристаллических структур и свойств высокого давления | National Science Review
0″> Abstract
Общедоступность синхротронных источников третьего поколения открыла новую эру исследований высокого давления. Кристаллическая структура материалов при сжатии теперь может быть определена с помощью рентгеновской дифракции с использованием образцов порошка, а в последнее время – с помощью дифракции мультинано монокристаллов. В то же время эти экспериментальные достижения сопровождаются быстрым увеличением вычислительной мощности и возможностей, что позволяет применять сложные квантовые вычисления для изучения различных свойств материалов. Одним из первых сюрпризов стало обнаружение того, что простые металлические элементы не соответствуют общему ожиданию внедрения трехмерных плотных структур при высоком давлении. Вместо этого было идентифицировано много новых открытых структур, не имеющих известных аналогов при атмосферном давлении. Возникновение этих структурных типов, по-видимому, случайно, без каких-либо правил, регулирующих их формирование. Принятие открытой структуры при высоком давлении предполагает наличие направленных связей. Следовательно, описание химической связи с локализованными атомными гибридными орбитами может быть подходящим.
Кристаллическая структура материалов при сжатии теперь может быть определена с помощью рентгеновской дифракции с использованием образцов порошка, а в последнее время – с помощью дифракции мультинано монокристаллов. В то же время эти экспериментальные достижения сопровождаются быстрым увеличением вычислительной мощности и возможностей, что позволяет применять сложные квантовые вычисления для изучения различных свойств материалов. Одним из первых сюрпризов стало обнаружение того, что простые металлические элементы не соответствуют общему ожиданию внедрения трехмерных плотных структур при высоком давлении. Вместо этого было идентифицировано много новых открытых структур, не имеющих известных аналогов при атмосферном давлении. Возникновение этих структурных типов, по-видимому, случайно, без каких-либо правил, регулирующих их формирование. Принятие открытой структуры при высоком давлении предполагает наличие направленных связей. Следовательно, описание химической связи с локализованными атомными гибридными орбитами может быть подходящим. Здесь рассматриваются теоретические основы и экспериментальные данные, подтверждающие этот подход к выяснению кристаллических структур высокого давления элементов группы I и II и полигидридов. Желательно и выгодно расширить и применить установленные химические принципы к изучению химии и химической связи материалов при высоком давлении.
Здесь рассматриваются теоретические основы и экспериментальные данные, подтверждающие этот подход к выяснению кристаллических структур высокого давления элементов группы I и II и полигидридов. Желательно и выгодно расширить и применить установленные химические принципы к изучению химии и химической связи материалов при высоком давлении.
высокое давление, кристаллическая структура, химическая связь, сверхпроводимость
2″ data-legacy-id=”sec1″> ВВЕДЕНИЕ
Давление является важным и универсальным термодинамическим параметром для изменения структуры и химической связи материала. В настоящее время стало обычным делом изменять давление в лаборатории на много порядков (по сравнению с температурой), т.е. от окружающей среды (бар) до мбар с использованием ячейки с алмазной наковальней [1]. В сочетании с достижениями в области спектроскопии и методов рассеяния, в основном основанных на синхротронном излучении, теперь стало возможным характеризовать свойства образцов пиколитрного размера в условиях экстремальных температур и давлений [2,3]. Первоначально наука о высоких давлениях в основном принадлежала физикам и использовалась для изучения изменений электронных свойств сильно сжатых материалов. Позже методы высокого давления стали основным инструментом земных и планетарных ученых, изучающих природу минералов в мантии Земли и планет-гигантов [4]. В химии изначально возник интерес к использованию давления при изучении химической кинетики для проверки теории активационного объема [5]. Однако поле бездействовало с конца 1960 , так как не было реальных экспериментальных средств для значительного увеличения давления.
Первоначально наука о высоких давлениях в основном принадлежала физикам и использовалась для изучения изменений электронных свойств сильно сжатых материалов. Позже методы высокого давления стали основным инструментом земных и планетарных ученых, изучающих природу минералов в мантии Земли и планет-гигантов [4]. В химии изначально возник интерес к использованию давления при изучении химической кинетики для проверки теории активационного объема [5]. Однако поле бездействовало с конца 1960 , так как не было реальных экспериментальных средств для значительного увеличения давления.
Революционный перелом в науке о высоких давлениях произошел в 70–80-е годы с появлением алмазных наковальней и новых конструкций прессов высокого давления, а также появлением и доступностью источников интенсивного синхротронного излучения [6]. Сжатие с использованием противоположных алмазных наковальней на образце, окруженном прокладкой, обеспечивает относительно простое средство для создания очень высокого давления. Более того, сфокусированное и яркое синхротронное рентгеновское излучение с перестраиваемой энергией вместе с новыми методами обнаружения расширило применение обычных спектроскопических и дифракционных методов на in situ характеристика свойств материала [6]. Этот прорыв был отмечен в серии структурных исследований полиморфных модификаций простых металлических элементов под высоким давлением в конце 1990-х и начале 2000-х годов, в которых сообщалось о новых и непредвиденных кристаллических структурах [7]. Очень часто обнаруженные структурные типы не соответствуют существующим структурам при атмосферном давлении и, кажется, не поддаются объяснению, основанному на устоявшихся представлениях о химической связи. Кроме того, часто обнаруживаются экзотические свойства, связанные с этими новыми структурами. Свойство связано как с электронной, так и с кристаллической структурой; таким образом, химический состав значительно изменяется под давлением. Наиболее примечательным является предсказание и проверка сверхпроводимости при очень высокой критической температуре ( T c ) в плотных гидридах металлов.
Более того, сфокусированное и яркое синхротронное рентгеновское излучение с перестраиваемой энергией вместе с новыми методами обнаружения расширило применение обычных спектроскопических и дифракционных методов на in situ характеристика свойств материала [6]. Этот прорыв был отмечен в серии структурных исследований полиморфных модификаций простых металлических элементов под высоким давлением в конце 1990-х и начале 2000-х годов, в которых сообщалось о новых и непредвиденных кристаллических структурах [7]. Очень часто обнаруженные структурные типы не соответствуют существующим структурам при атмосферном давлении и, кажется, не поддаются объяснению, основанному на устоявшихся представлениях о химической связи. Кроме того, часто обнаруживаются экзотические свойства, связанные с этими новыми структурами. Свойство связано как с электронной, так и с кристаллической структурой; таким образом, химический состав значительно изменяется под давлением. Наиболее примечательным является предсказание и проверка сверхпроводимости при очень высокой критической температуре ( T c ) в плотных гидридах металлов. Фактически, очень высокое значение T c было зарегистрировано в сильно сжатом сверхпроводящем сероводороде (200 К) [8] и гидриде лантана (260 К) [9]. Другими недавними примерами являются образование кристаллических структур между инертным газом и водородом [10–17], реакции водорода с азотом [18] и кремнеземом [19], металлические сплавы, образующиеся из несмешивающихся жидкостей [20,21] и многие другие, все это происходит при относительно низком давлении в несколько десятков гигапаскалей. Эти наблюдения также должны оказать значительное влияние на геохимию, поскольку химические реакции, протекающие в мантии и ядре Земли, происходят в условиях высокого давления и температуры, которые невозможно адекватно описать, исходя из знаний о химических принципах в условиях окружающей среды. Эти удивительные экспериментальные результаты открыли новую эру в структурной химии и исследовании взаимосвязи структура-свойство соединений высокого давления. Сложный вопрос заключается в том, могут ли исследования при высоком давлении руководствоваться установленными практическими химическими принципами, подобными тем, которые были разработаны в течение многих лет для химии окружающей среды.
Фактически, очень высокое значение T c было зарегистрировано в сильно сжатом сверхпроводящем сероводороде (200 К) [8] и гидриде лантана (260 К) [9]. Другими недавними примерами являются образование кристаллических структур между инертным газом и водородом [10–17], реакции водорода с азотом [18] и кремнеземом [19], металлические сплавы, образующиеся из несмешивающихся жидкостей [20,21] и многие другие, все это происходит при относительно низком давлении в несколько десятков гигапаскалей. Эти наблюдения также должны оказать значительное влияние на геохимию, поскольку химические реакции, протекающие в мантии и ядре Земли, происходят в условиях высокого давления и температуры, которые невозможно адекватно описать, исходя из знаний о химических принципах в условиях окружающей среды. Эти удивительные экспериментальные результаты открыли новую эру в структурной химии и исследовании взаимосвязи структура-свойство соединений высокого давления. Сложный вопрос заключается в том, могут ли исследования при высоком давлении руководствоваться установленными практическими химическими принципами, подобными тем, которые были разработаны в течение многих лет для химии окружающей среды.
В этом обзоре основное внимание уделяется влиянию давления на электронную структуру и химическую связь. Я буду обсуждать структурные изменения и свойства в рамках гибридизации атомных орбиталей и взаимодействия между граничными орбиталями. Этот вклад не претендует на всесторонний обзор области химии и физики высоких давлений. Читатели могут ознакомиться с несколькими недавними обзорами, охватывающими современное состояние и различные аспекты науки о высоком давлении [22–24]. Эта статья служит иллюстрацией того, как традиционные концепции склеивания могут быть адаптированы к пониманию структур и структурных преобразований при высоком давлении, на примерах, основанных главным образом на опыте автора. Разработка орбитальной теории высокого давления все еще находится на ранней стадии. Представленные здесь аргументы могут показаться качественными. Требуется дальнейшее уточнение этих идей. Цель этого вклада состоит в том, чтобы побудить читателей к дальнейшим экспериментальным и теоретическим исследованиям в этом направлении.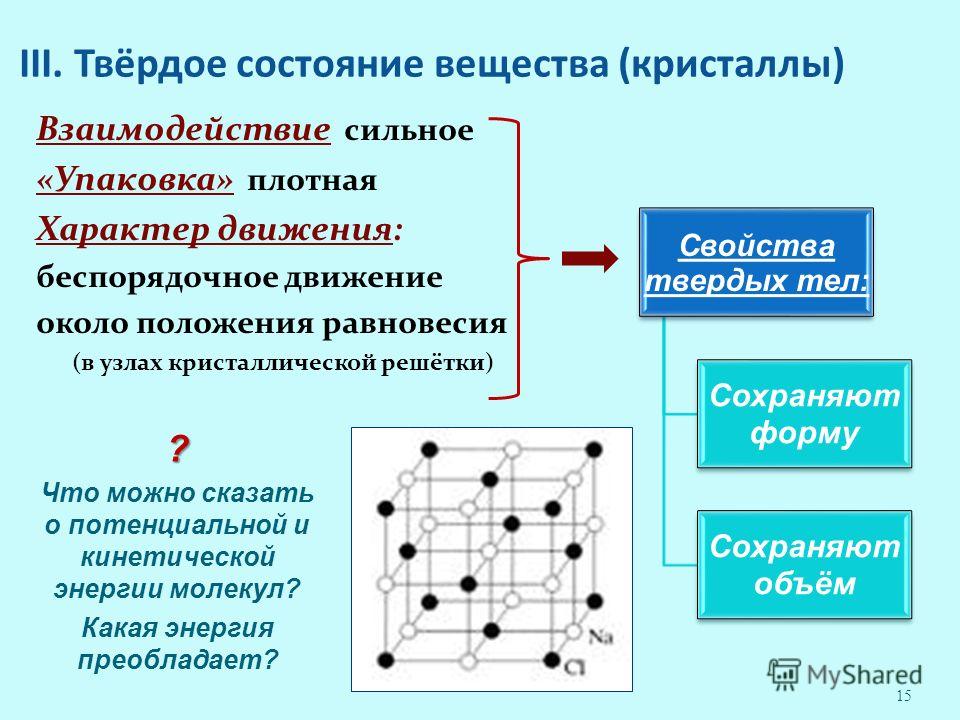
6″ data-legacy-id=”sec2″> АТОМЫ ПРИ СЖАТИИ
Концепция направленных химических связей и предсказание кристаллических структур элементарных твердых тел основаны на гибридизации между валентными и низколежащими пустыми орбиталями атомов и числом электронов, доступных для химической связи [25,26 ]. Последнее напрямую связано с атомным номером и, следовательно, с положением элемента в таблице Менделеева [27]. В периодической таблице элементы расположены в группах по количеству валентных электронов. Элементы одной и той же группы периодической таблицы имеют сходные химические свойства. Элементы первых двух групп (I и II) — это щелочные и щелочные металлы с одним и двумя валентными электронами на крайних с орбиталей соответственно. Энергии первой ионизации элементов группы I и II сравнительно малы и подвержены образованию ионной связи. Низкие энергии ионизации обусловлены эффективным экранированием заряда ядра остовными электронами. Справа от периодической таблицы валентные s орбитали полностью заняты, а валентные p орбитали постепенно заполняются пниктогенами (группа XV, N, P, As, …), халькогенами (группа XVI, O, S , Se, …), галогены (группа XVII, F, Cl, Br, …) и, наконец, благородные газы (группа XVIII, He, Ne, Ar, Kr, …). Отличительной группой элементов, занимающих периодическую таблицу, являются переходные металлы. Это элементы с d электронов на внешней оболочке. Более тяжелые элементы с 90 595 d 90 596 и 90 595 f 90 596 электронов на валентных орбиталях называются лантаноидами и актинидами.
Справа от периодической таблицы валентные s орбитали полностью заняты, а валентные p орбитали постепенно заполняются пниктогенами (группа XV, N, P, As, …), халькогенами (группа XVI, O, S , Se, …), галогены (группа XVII, F, Cl, Br, …) и, наконец, благородные газы (группа XVIII, He, Ne, Ar, Kr, …). Отличительной группой элементов, занимающих периодическую таблицу, являются переходные металлы. Это элементы с d электронов на внешней оболочке. Более тяжелые элементы с 90 595 d 90 596 и 90 595 f 90 596 электронов на валентных орбиталях называются лантаноидами и актинидами.
Очень полезным общим правилом для определения пространственной протяженности валентной орбитали является количество узлов радиальной водородоподобной волновой функции валентной орбиты ( n – l – 1), где n — главная квантовое число и l азимутальное квантовое число. Например, 1 s орбиталь атома H ( n = 1, l = 0) не имеет радиального узла; следовательно, потенциальная энергия, ощущаемая валентным электроном от ядерного заряда, не экранируется, и энергия ионизации составляет 13,6 эВ.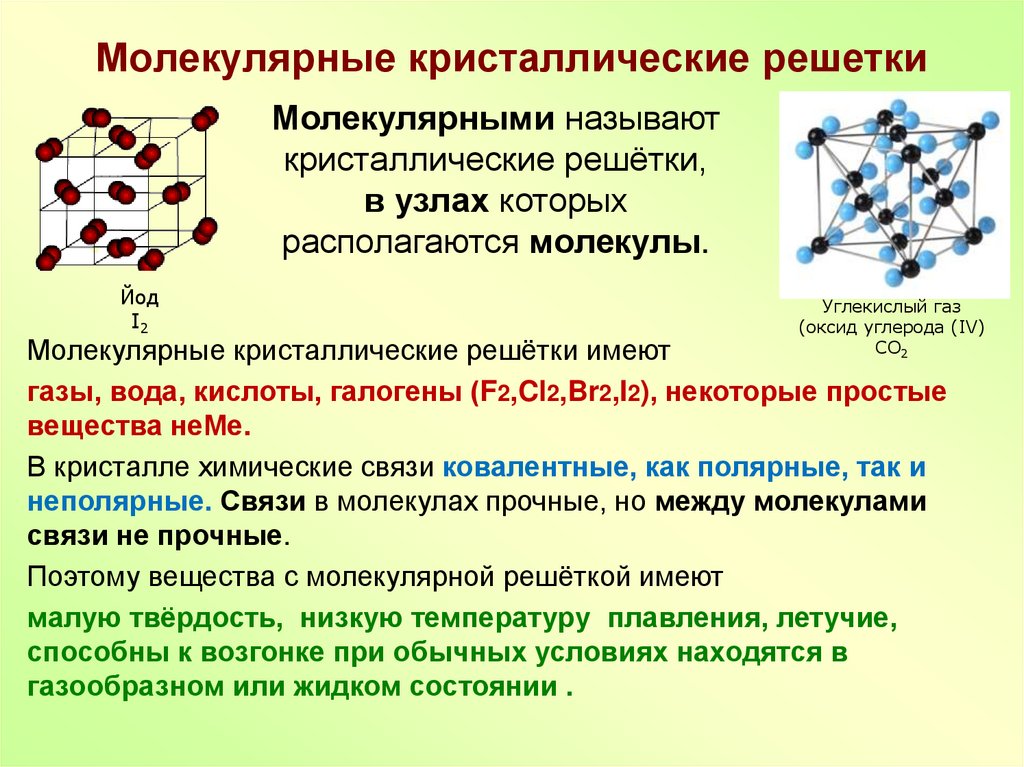 За исключением элементов инертных газов с полностью заполненными валентными оболочками, он самый высокий среди всех элементов. Для сравнения, самая внешняя орбиталь 6 s атома Cs имеет пять радиальных узлов и 54 остовных электрона ( n = 6, l = 0). Таким образом, 6 s электрон хорошо защищен от ядерного заряда, а первый потенциал ионизации составляет всего 3,89 эВ, что является самым низким из всех элементов. Следовательно, пространственное расширение орбитали Cs 6 s довольно размыто. В дополнение к объему, занимаемому остовными электронами, атомный радиус Cs, равный 3,34 Å, очень велик. Для элементов первого ряда радиальные узлы на валентных 2 p орбиталях отсутствуют и поэтому плохо экранированы ( n = 2, l = 1). Таким образом, радиальная протяженность (размер атома) орбитали 2 p становится меньше по мере увеличения заряда ядра. Аналогичный эффект также присутствует в переходных металлах первого ряда ( n = 3 и l = 2), где экранирование плохое, а орбитали 3 d сжаты (плотно).
За исключением элементов инертных газов с полностью заполненными валентными оболочками, он самый высокий среди всех элементов. Для сравнения, самая внешняя орбиталь 6 s атома Cs имеет пять радиальных узлов и 54 остовных электрона ( n = 6, l = 0). Таким образом, 6 s электрон хорошо защищен от ядерного заряда, а первый потенциал ионизации составляет всего 3,89 эВ, что является самым низким из всех элементов. Следовательно, пространственное расширение орбитали Cs 6 s довольно размыто. В дополнение к объему, занимаемому остовными электронами, атомный радиус Cs, равный 3,34 Å, очень велик. Для элементов первого ряда радиальные узлы на валентных 2 p орбиталях отсутствуют и поэтому плохо экранированы ( n = 2, l = 1). Таким образом, радиальная протяженность (размер атома) орбитали 2 p становится меньше по мере увеличения заряда ядра. Аналогичный эффект также присутствует в переходных металлах первого ряда ( n = 3 и l = 2), где экранирование плохое, а орбитали 3 d сжаты (плотно). Как правило, атомный радиус увеличивается вниз по группе и справа налево по одной и той же строке периодической таблицы. Периодический тренд элементов помогает определить размер атома и дает полезное практическое руководство по активности самых удаленных электронов по отношению к химическому связыванию.
Как правило, атомный радиус увеличивается вниз по группе и справа налево по одной и той же строке периодической таблицы. Периодический тренд элементов помогает определить размер атома и дает полезное практическое руководство по активности самых удаленных электронов по отношению к химическому связыванию.
Что происходит с периодическими трендами при сжатии атомов? Изменение размера атомов под давлением от атмосферного (1 бар) до 1000 ГПа (10 Мбар) схематично показано на рис. 1 [28, 29]. При атмосферном давлении атомные размеры щелочных металлов I группы намного больше, чем у других элементов того же ряда. По мере увеличения давления атомы уплотняются, и их размеры становятся более однородными. При 100 ГПа (1 Мбар) нет заметной разницы в размерах всех элементов (щелочных и переходных металлов) [28,29]. Качественные закономерности периодического химического тренда исчезают.
Как мы собираемся прогнозировать химическую связь при высоком давлении? Первый ключ к разгадке дал Штернхеймер при смешении валентности с низколежащими пустыми орбиталями [30]. Чтобы объяснить скачок объема твердого Cs, наблюдаемый Бриджменом при 4,5 ГПа, он предположил, что полоса Cs 6 s смешалась (гибридизировалась) с пустой полосой 5 d . Это предположение подтверждается расчетами зонной структуры [30]. Перенос электрона из диффузного 6 s на «более плотные или более компактные» 5 d орбитали привели к меньшему эффективному размеру атома Cs и к уменьшению объема при структурном фазовом переходе. В качестве альтернативы результат можно понять с точки зрения простой модели «частица в коробке» (PIB). В ПИП энергия электронных уровней обратно пропорциональна обратному квадрату ширины потенциальной ямы. При сжатии ширина уменьшается, а энергетические уровни поднимаются выше. В Cs пустое 5 d орбиталей «захвачены» атомным центробежным потенциалом (− l ( l + 1)/ r 2 ), явление, известное в атомной спектроскопии как «резонанс формы» (рис. 2а). [31]. Близкое вырождение между 5 d и 6 s облегчает смешение (гибридизацию) s → d .
Чтобы объяснить скачок объема твердого Cs, наблюдаемый Бриджменом при 4,5 ГПа, он предположил, что полоса Cs 6 s смешалась (гибридизировалась) с пустой полосой 5 d . Это предположение подтверждается расчетами зонной структуры [30]. Перенос электрона из диффузного 6 s на «более плотные или более компактные» 5 d орбитали привели к меньшему эффективному размеру атома Cs и к уменьшению объема при структурном фазовом переходе. В качестве альтернативы результат можно понять с точки зрения простой модели «частица в коробке» (PIB). В ПИП энергия электронных уровней обратно пропорциональна обратному квадрату ширины потенциальной ямы. При сжатии ширина уменьшается, а энергетические уровни поднимаются выше. В Cs пустое 5 d орбиталей «захвачены» атомным центробежным потенциалом (− l ( l + 1)/ r 2 ), явление, известное в атомной спектроскопии как «резонанс формы» (рис. 2а). [31]. Близкое вырождение между 5 d и 6 s облегчает смешение (гибридизацию) s → d .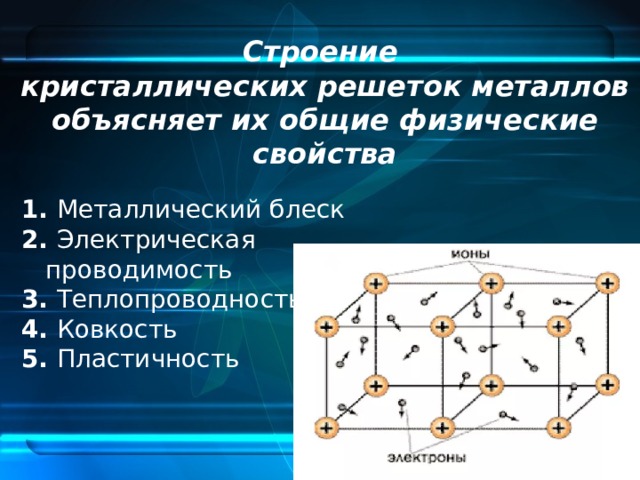 Изменение от преимущественно ‘ s ‘ к ‘ d ‘-подобному характеру плотности валентного заряда для гипотетического изоструктурного перехода грань-центр-куб (ГЦК) → ГЦК-переход в Cs показано на рис. 2b [32]. ].
Изменение от преимущественно ‘ s ‘ к ‘ d ‘-подобному характеру плотности валентного заряда для гипотетического изоструктурного перехода грань-центр-куб (ГЦК) → ГЦК-переход в Cs показано на рис. 2b [32]. ].
Рис. 1.
Открыть в новой вкладкеСкачать слайд
Схема изменения размера атомов при приложении давления (по Це и Болдерва [29]).
Позднее повторное изучение более тонких дифракционных картин Cs высокого давления, полученных с помощью синхротронного рентгеновского излучения, показало, что структурные переходы гораздо сложнее [33]. Вместо изоструктурного ГЦК-перехода появилась новая сложная модулированная орторомбическая слоистая структура с 84 атомами на элементарную ячейку (Cs-III, C 222 1 ) было обнаружено при 4,2 ГПа [33]. Поле стабильности Cs-III было очень узким при температуре окружающей среды, между 4,2 и 4,3 ГПа, и исчезало при охлаждении. Дальнейшее сжатие привело к простой тетрагональной структуре (Cs-IV, I 4 1 / amd ) [34], гофрированной слоистой структуре (Cs-V, Cmca ) при 12 ГПа [35] и, в конечном счете, ожидаемая гексагональная плотная структура (Cs-VI) появилась при 70 ГПа [35].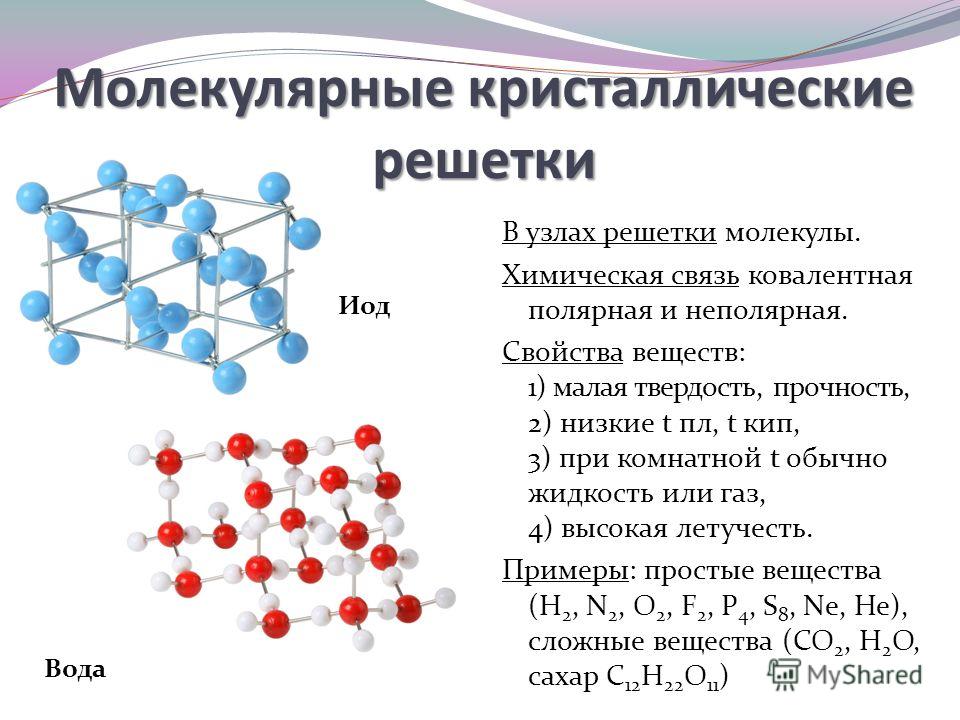 Эта последовательность структурных преобразований анализировалась ранее [29].,36]. Показано, что переход s → d (гибридизация) приводит к участию в химической связи орбиталей Cs 5 d . Результат многоцентрового перекрытия между орбиталями Cs 5 d привел к образованию «электридов», локализованной плотности заряда в центрах сети 2D квадратной решетки, образованной Cs. Неатомная максимальная электронная плотность в плотных полиморфах Cs, возможно, является первым примером электридов при высоком давлении. Электрид является хорошо известным химическим соединением [37]. Локализация электронов в междоузлии может быть объяснена как совместное использование электронов между несколькими атомными центрами. Многоцентровая связь энергетически выгодна в (электронодефицитной) системе с большим количеством доступных орбиталей, чем число электронов, необходимое для их полного заполнения. В Cs вместо одного 6 s орбиталей на атом, при высоком давлении электрон может получить доступ к пяти d орбиталей.
Эта последовательность структурных преобразований анализировалась ранее [29].,36]. Показано, что переход s → d (гибридизация) приводит к участию в химической связи орбиталей Cs 5 d . Результат многоцентрового перекрытия между орбиталями Cs 5 d привел к образованию «электридов», локализованной плотности заряда в центрах сети 2D квадратной решетки, образованной Cs. Неатомная максимальная электронная плотность в плотных полиморфах Cs, возможно, является первым примером электридов при высоком давлении. Электрид является хорошо известным химическим соединением [37]. Локализация электронов в междоузлии может быть объяснена как совместное использование электронов между несколькими атомными центрами. Многоцентровая связь энергетически выгодна в (электронодефицитной) системе с большим количеством доступных орбиталей, чем число электронов, необходимое для их полного заполнения. В Cs вместо одного 6 s орбиталей на атом, при высоком давлении электрон может получить доступ к пяти d орбиталей. Интересно отметить, что в двумерной многоцентровой сетке связей электронная плотность между ближайшими атомами Cs не наблюдается. Общее представление о химической связи между ближайшей парой атомов не соблюдается. Вместо этого «формальная» связь возникает между вторыми ближайшими соседними атомами. Принятие в плоскости Cs d -связей ослабляет трехмерную сетку предшественника, превращая ее в структуру, состоящую из слоев двумерных квадратных решеток, которые могут «скользить» друг относительно друга, образуя Cs-III [29].,36] и в конечном итоге образуя Cs-IV (рис. 3а).
Интересно отметить, что в двумерной многоцентровой сетке связей электронная плотность между ближайшими атомами Cs не наблюдается. Общее представление о химической связи между ближайшей парой атомов не соблюдается. Вместо этого «формальная» связь возникает между вторыми ближайшими соседними атомами. Принятие в плоскости Cs d -связей ослабляет трехмерную сетку предшественника, превращая ее в структуру, состоящую из слоев двумерных квадратных решеток, которые могут «скользить» друг относительно друга, образуя Cs-III [29].,36] и в конечном итоге образуя Cs-IV (рис. 3а).
Рис. 2.
Открыть в новой вкладкеСкачать слайд
(а) Уровни энергии частицы в потенциальной яме и (б) иллюстрация орбитальной гибридизации с–д Cs под давлением.
Рисунок 3.
Открыть в новой вкладкеСкачать слайд
(а) Преобразование ГЦК в тело-центр-тетрагональную (БЦТ) структуру Cs-IV в результате скольжения двумерных плоскостей Cs и (б) формирование волнообразной плотности заряда (электридов) от перекрытия Cs d орбиталей между двумя соседними слоями.
Сложная особенность химической связи в Cs-IV, выявленная при расчете электронной структуры фон Шнерингом и Неспером [38], представляет собой новый волнообразный характер распространения электронной плотности между плоскостями атомов Cs. Синусоидальное распределение электронной плотности можно визуально объяснить, сдвинув слои двумерной квадратной решетки вдоль двух разных кристаллографических направлений (рис. 3b) [29,36]. В последнее время возобновился интерес к исследованию электридов в кристаллах высокого давления отчасти из-за их повсеместного распространения, а отчасти из-за новой электронной структуры, которая может иметь отношение к сверхпроводимости [39].–41].
Cs-IV превращается в Cs-V при 12 ГПа (рис. 4а) [42]. Cs-V имеет орторомбическую структуру, состоящую из чередующихся складчатых и плоских 2D-слоев атомов Cs. Важной особенностью этой структуры является то, что это первая полиморфная модификация Cs, состоящая из двух кристаллографически различных центров Cs. Это наблюдение подразумевает, что два атома Cs также химически различны. Плоский слой построен из Cs в положениях Wyckoff 8 f , а гофрированный слой построен из Cs в положениях 8 д сайтов. Расчетная разность зарядов между Cs-V и атомарным Cs, показанная на рис. 4b [29,36], показывает однозначный перенос заряда между двумя подслоями: обеднение электронной плотности (синяя область) обнаружено в плоском слое и накопление заряда в складчатый слой (рис. 4б). Химическая интуиция подсказывает, что в электронодефицитном двумерном плоском слое не будет значительных структурных искажений по мере удаления электронов. Напротив, перенос электронов в соседний плоский слой (богатый электронами) приведет к структурным искажениям. Перенос заряда часто предполагает тенденцию к открытию энергетической щели, чтобы стабилизировать общую структуру. Хотя переход в изолятор не наблюдался в Cs, индуцированные давлением переходы металл → изолятор действительно позже были обнаружены в элементарных Li [43] и Na [44] при экстремальном сжатии.
Это наблюдение подразумевает, что два атома Cs также химически различны. Плоский слой построен из Cs в положениях Wyckoff 8 f , а гофрированный слой построен из Cs в положениях 8 д сайтов. Расчетная разность зарядов между Cs-V и атомарным Cs, показанная на рис. 4b [29,36], показывает однозначный перенос заряда между двумя подслоями: обеднение электронной плотности (синяя область) обнаружено в плоском слое и накопление заряда в складчатый слой (рис. 4б). Химическая интуиция подсказывает, что в электронодефицитном двумерном плоском слое не будет значительных структурных искажений по мере удаления электронов. Напротив, перенос электронов в соседний плоский слой (богатый электронами) приведет к структурным искажениям. Перенос заряда часто предполагает тенденцию к открытию энергетической щели, чтобы стабилизировать общую структуру. Хотя переход в изолятор не наблюдался в Cs, индуцированные давлением переходы металл → изолятор действительно позже были обнаружены в элементарных Li [43] и Na [44] при экстремальном сжатии.
Рисунок 4.
Открыть в новой вкладкеСкачать слайд
Структура Cs-V (а) и карта разницы электронной плотности (б) относительно атомов Cs, показывающая перенос электронов из плоского слоя в складчатый.
Таким же образом можно объяснить последовательные структурные превращения в аналогичных твердых телах I группы Li и Rb. Эти преобразования уже обсуждались в другом месте [29]; здесь мы только иллюстрируем, как простое концептуальное предложение для Cs может быть применено к выяснению структуры гость-хозяин в Rb-IV. При сжатии от давления окружающей среды Rb следовал последовательности превращений, аналогичной Cs [45–47]. Модулированная структура (Rb-III) [48] была сформирована из ГЦК-фазы (Rb-II) при 13 ГПа [48]. Вместо преобразования в I 4 1 / amd Структура Cs-IV (Rb-V), новая несоизмеримая структура гость-хозяин была обнаружена при 17 ГПа (Rb-IV) [47,48]. Эта фаза была стабильной от 17 до 20 ГПа, а затем в конечном итоге трансформировалась в Cs-IV-подобный I 41/ и . В Rb-III атомы Rb, образующие основной каркас, упорядочены, а положения атомов соответствуют пространственной группе I 4/ мкм . С другой стороны, позиции атомов-гостей соответствовали пространственной группе 9.0595 I 4/ ммм , но были несоизмеримы с элементарной ячейкой-хозяином (рис. 5а) [48]. Чтобы согласовать, как это конкретное расположение атомов Rb возникло из структуры предшественника FCC, исследователи сначала обнаружили, что структура Rb-IV может быть описана как стопка чередующихся идентичных 2D-слоев квадратной решетки атомов Rb, слегка повернутых друг относительно друга (рис. 5б) по осям c [29]. Как и Cs, Rb претерпел с → d гибридизацию в пост-ГЦК фазе (Rb-II) с образованием двумерных квадратных решеток с электронной плотностью, расположенной в середине квадратов (рис. 5д). Схематическое соединение вторых ближайших соседних атомов Rb выявило картину, показанную на рис. 5d, где хорошо заметен мотив квадратной решетки.
В Rb-III атомы Rb, образующие основной каркас, упорядочены, а положения атомов соответствуют пространственной группе I 4/ мкм . С другой стороны, позиции атомов-гостей соответствовали пространственной группе 9.0595 I 4/ ммм , но были несоизмеримы с элементарной ячейкой-хозяином (рис. 5а) [48]. Чтобы согласовать, как это конкретное расположение атомов Rb возникло из структуры предшественника FCC, исследователи сначала обнаружили, что структура Rb-IV может быть описана как стопка чередующихся идентичных 2D-слоев квадратной решетки атомов Rb, слегка повернутых друг относительно друга (рис. 5б) по осям c [29]. Как и Cs, Rb претерпел с → d гибридизацию в пост-ГЦК фазе (Rb-II) с образованием двумерных квадратных решеток с электронной плотностью, расположенной в середине квадратов (рис. 5д). Схематическое соединение вторых ближайших соседних атомов Rb выявило картину, показанную на рис. 5d, где хорошо заметен мотив квадратной решетки.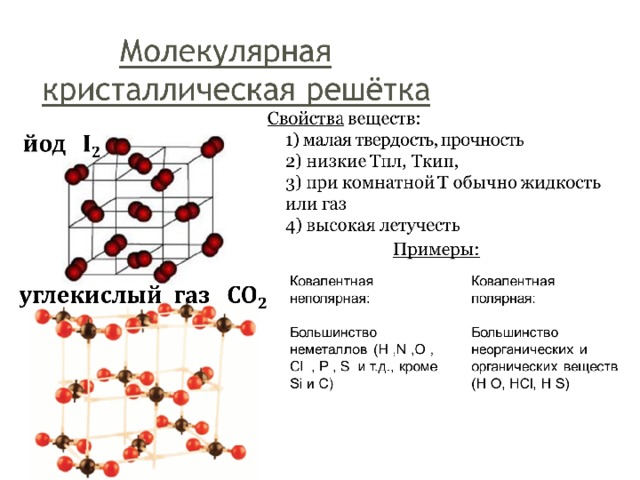 Соединение вторых ближайших соседей в квадратной решетке оставило один атом Rb, окруженный 8-членным кольцом. На рис. 5в отчетливо виден каркас «гость-хозяин», в котором атомы-гости располагаются в каналах (отверстиях), перпендикулярных восьмичленным кольцам, образованным Rb в 2D-плоскостях.
Соединение вторых ближайших соседей в квадратной решетке оставило один атом Rb, окруженный 8-членным кольцом. На рис. 5в отчетливо виден каркас «гость-хозяин», в котором атомы-гости располагаются в каналах (отверстиях), перпендикулярных восьмичленным кольцам, образованным Rb в 2D-плоскостях.
Рис. 5.
Открыть в новой вкладкеСкачать слайд
(а, б) Структура двух подрешеток несоизмеримого Rb-IV; и (c-e) схематическое изображение последовательности, ведущей к формированию структуры хозяин-гость из двумерной квадратной сети, полученной из структуры предшественника FCC.
Рис. 6.
Открыть в новой вкладкеСкачать слайд
Двухмерная архимедова мозаика плоских массивов атомов с постепенно увеличивающейся плотностью упаковки (см. вставленную таблицу).
Структурная трансформация твердых веществ элементарной щелочи в диапазоне промежуточных давлений может быть понята с предположением о формировании двумерных слоев квадратной решетки. Примечательно, что структурные типы и последовательность последовательных структурных превращений в Rb следуют той же тенденции, что и упаковка твердых сфер в двух измерениях, т..jpg) е. архимедова мозаика (рис. 6) [49]. С помощью этой модели можно качественно интерпретировать даже необычные структуры «гость-хозяин», наблюдаемые в Rb и Ba. Начиная с исходной кубической структуры (FCC или объемно-центрально-кубическая (BCC)), под давлением структуры щелочных и щелочных элементов принимают двухмерный квадратно-сетчатый слой после s → d гибридизация. Затем валентные электроны «перемещаются» (выдавливаются) в междоузлия двумерной решетки. В результате атомный размер становится меньше, а компактированные атомы упаковываются как твердые сферы в 2D-плоскости [49].
е. архимедова мозаика (рис. 6) [49]. С помощью этой модели можно качественно интерпретировать даже необычные структуры «гость-хозяин», наблюдаемые в Rb и Ba. Начиная с исходной кубической структуры (FCC или объемно-центрально-кубическая (BCC)), под давлением структуры щелочных и щелочных элементов принимают двухмерный квадратно-сетчатый слой после s → d гибридизация. Затем валентные электроны «перемещаются» (выдавливаются) в междоузлия двумерной решетки. В результате атомный размер становится меньше, а компактированные атомы упаковываются как твердые сферы в 2D-плоскости [49].
Первая экспериментальная проверка орбитальной гибридизации была продемонстрирована при анализе электронной плотности сжатого Si [50] по дифрактограммам методом максимальной энтропии (МЭМ) [51]. Поскольку валентные электроны в основном ответственны за интенсивность малоугловых брэгговских отражений, МЭМ является идеальным методом для извлечения плотности валентных электронов из усеченных дифракционных картин, полученных при высоком давлении. Результаты анализа дифрактограмм сжатого Si в среде, передающей гидростатическое давление, при 80 К и расчетов теоретической плотности заряда показаны на рис. 7. Согласованные совпадения бросаются в глаза. Как и ожидалось, как теоретическая, так и экспериментальная плотность электронов показывают «удаление» электронов с атомных позиций в пустую пустоту и возрастающее участие d орбиталей в химической связи [29]. Гибридизация p–d более наглядно демонстрируется при дифракционном исследовании монокристалла сжатого Ge [52]. Как показано на графике разности плотности заряда между последовательными давлениями на рис. 8, распределение электронов, подобное sp 3 , постепенно ослабевает с увеличением давления и сопутствующим увеличением d -орбитального характера. Эта особенность начинает проявляться при 7 ГПа, ниже фазового перехода до 11 ГПа.
Результаты анализа дифрактограмм сжатого Si в среде, передающей гидростатическое давление, при 80 К и расчетов теоретической плотности заряда показаны на рис. 7. Согласованные совпадения бросаются в глаза. Как и ожидалось, как теоретическая, так и экспериментальная плотность электронов показывают «удаление» электронов с атомных позиций в пустую пустоту и возрастающее участие d орбиталей в химической связи [29]. Гибридизация p–d более наглядно демонстрируется при дифракционном исследовании монокристалла сжатого Ge [52]. Как показано на графике разности плотности заряда между последовательными давлениями на рис. 8, распределение электронов, подобное sp 3 , постепенно ослабевает с увеличением давления и сопутствующим увеличением d -орбитального характера. Эта особенность начинает проявляться при 7 ГПа, ниже фазового перехода до 11 ГПа.
Рис. 7.
Открыть в новой вкладкеСкачать слайд
Расчетные изменения в распределении валентных электронов в различных полиморфных модификациях кремния высокого давления. Низкотемпературные дифрактограммы Si и соответствующая плотность электронов, полученные методом максимальной энтропии (MEM). Вставка справа при 21 ГПа представляет собой теоретическую плотность заряда (адаптировано из Tse и др. [50]).
Низкотемпературные дифрактограммы Si и соответствующая плотность электронов, полученные методом максимальной энтропии (MEM). Вставка справа при 21 ГПа представляет собой теоретическую плотность заряда (адаптировано из Tse и др. [50]).
Рис. 8.
Открыть в новой вкладкеСкачать слайд
Трехмерные изоповерхностные карты различий в распределении электронов кристаллического Ge между структурами при последовательном повышении давления. Разность положительных и отрицательных зарядов отображается желтым и синим цветами соответственно (адаптировано из Li и др. [52]).
Исследования также показывают, что перераспределение электронной плотности может происходить в Li высокого давления [53,54]. Из расчета зонной структуры было замечено, что под высоким давлением электроны вытесняются из атомных позиций, образуя «димерные» пары. Однако электронной плотности вдоль направления «связывания» между двумя атомами Li, образующими димер, обнаружено не было [53]. На рис. 9 показаны полная энергия и электронная плотность гипотетической линейной цепочки атомов Li в зависимости от расстояния Li–Li [54]. При расстоянии Li … Li менее 1,56 Å химическая связь изменилась с sp -σ до p π – p π . Следовательно, электроны, ранее находившиеся в σ-связях, переместились на перпендикулярные π-связи. Изменение поведения связывания, т. е. образование π-димеров Li без электронной плотности между парами Li, точно соответствует тому, что было предсказано на основе расчета зонной структуры [53]. Таким образом, картина локализованной химической орбиты эквивалентна зонному описанию.
На рис. 9 показаны полная энергия и электронная плотность гипотетической линейной цепочки атомов Li в зависимости от расстояния Li–Li [54]. При расстоянии Li … Li менее 1,56 Å химическая связь изменилась с sp -σ до p π – p π . Следовательно, электроны, ранее находившиеся в σ-связях, переместились на перпендикулярные π-связи. Изменение поведения связывания, т. е. образование π-димеров Li без электронной плотности между парами Li, точно соответствует тому, что было предсказано на основе расчета зонной структуры [53]. Таким образом, картина локализованной химической орбиты эквивалентна зонному описанию.
Рисунок 9.
Открыть в новой вкладкеСкачать слайд
Полная энергия линейной молекулы Li 4 как функция длины связи Li-Li (кривая) и схематическое изображение волновых функций; обратите внимание, что волновая функция основного состояния для расстояний короче 1,5 Å полностью состоит из взаимодействий Li–Li p π – p π (из Руссо и др.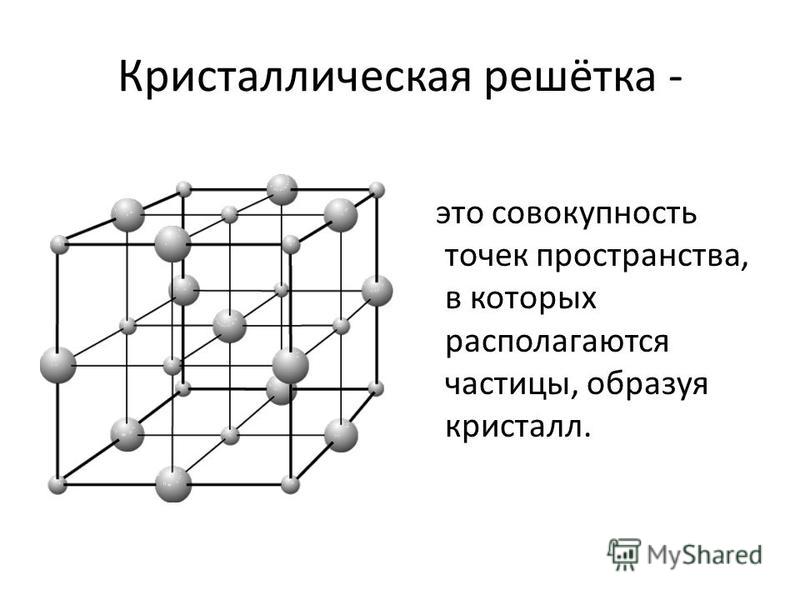 [54]).
[54]).
Представленные выше рассуждения предполагают, что когда атомы прижимаются друг к другу внешним давлением, чтобы смягчить неблагоприятное кулоновское электрон-электронное отталкивание, валентные электроны предпочитают мигрировать в пустые пространства кристалла, чтобы облегчить многоцентровое связывание. Это похоже на эффект наложения потенциала удержания на атом. При сжатии энергии заполненных орбиталей увеличиваются, что позволяет смешиваться с низколежащими пустыми орбиталями с более высокими квантовыми числами углового момента. В орбитальном описании пространственно разнонаправленные гибридные орбитали обеспечивают перераспределение плотности валентного заряда (в междоузлиях) и ответственны за появление множества новых кристаллических структур с открытым каркасом. При сверхвысоких давлениях, когда большая часть валентных электронов уже находится в пустом пространстве, кристаллическая структура простых элементов в основном определяется упаковкой ионов и поэтому вновь возникает плотноупакованная структура. Для исторического интереса следует отметить, что Полинг пытался объяснить структуры Cs-IV и Cs-V, основываясь на предположении о кубических элементарных ячейках, и пришел к выводу, что и Cs-IV, и Cs-V состоят из 122 и 162 атома на элементарную ячейку соответственно [55].
Для исторического интереса следует отметить, что Полинг пытался объяснить структуры Cs-IV и Cs-V, основываясь на предположении о кубических элементарных ячейках, и пришел к выводу, что и Cs-IV, и Cs-V состоят из 122 и 162 атома на элементарную ячейку соответственно [55].
 10) как в K 2 Ag, так и в K 3 Ag [59]. Каркасы Ag в K 2 Ag и K 3 Ag построены из перекрытий гибридных орбиталей Ag sp . Возникла простая картина для описания структуры сплава. Электронная конфигурация нейтрального Ag в основном состоянии: 4 d 10 5 s 1 . В К 2 Ag два электрона, по одному от каждого K, были формально переведены на Ag. Эффективная электронная конфигурация полученного атома Ag: 4 d 10 5 s 2 5 p 1 . Затем валентные орбитали Ag гибридизуются, образуя три гибрида sp 2 . Химическая связь между гибридами sp 2 сформировала двумерную сотовую сеть графеноподобных слоев, уложенных вдоль кристаллографической c -оси, разделенные альтернативным слоем катионов K (рис. 11). Исходя из того же рассуждения, в K 3 Ag каждый Ag может получить три электрона от атомов K, и эффективная электронная конфигурация Ag принимает вид .
10) как в K 2 Ag, так и в K 3 Ag [59]. Каркасы Ag в K 2 Ag и K 3 Ag построены из перекрытий гибридных орбиталей Ag sp . Возникла простая картина для описания структуры сплава. Электронная конфигурация нейтрального Ag в основном состоянии: 4 d 10 5 s 1 . В К 2 Ag два электрона, по одному от каждого K, были формально переведены на Ag. Эффективная электронная конфигурация полученного атома Ag: 4 d 10 5 s 2 5 p 1 . Затем валентные орбитали Ag гибридизуются, образуя три гибрида sp 2 . Химическая связь между гибридами sp 2 сформировала двумерную сотовую сеть графеноподобных слоев, уложенных вдоль кристаллографической c -оси, разделенные альтернативным слоем катионов K (рис. 11). Исходя из того же рассуждения, в K 3 Ag каждый Ag может получить три электрона от атомов K, и эффективная электронная конфигурация Ag принимает вид . Снова регибридизация орбиталей Ag s и p с валентностью и связывание между гибридами sp 3 привело к структуре алмаза FCC. Эта интерпретация предполагает, что атомы Ag должны были существовать в анионных состояниях -2 и -3 в K 2 Ag и K 3 Ag соответственно. Это предположение может быть подтверждено анализом электронных плотностей, извлеченных из соответствующих дифрактограмм описанным выше методом МЭМ. Относительная легкость переноса заряда от K к Ag при легком сжатии может быть объяснена большой разницей электроотрицательности (χ K = 0,82 против χ Ag = 1,93) нейтральных атомов при атмосферном давлении. Существенный перенос электрона от K отражается в коротком расстоянии K…K в 2D-слое 3,13 Å, что значительно меньше, чем расстояние K–K 3,82 Å в металлическом K при том же давлении [20]. Ранее очень короткое расстояние К-К привело к предположению об образовании ковалентных связей К-К.
Снова регибридизация орбиталей Ag s и p с валентностью и связывание между гибридами sp 3 привело к структуре алмаза FCC. Эта интерпретация предполагает, что атомы Ag должны были существовать в анионных состояниях -2 и -3 в K 2 Ag и K 3 Ag соответственно. Это предположение может быть подтверждено анализом электронных плотностей, извлеченных из соответствующих дифрактограмм описанным выше методом МЭМ. Относительная легкость переноса заряда от K к Ag при легком сжатии может быть объяснена большой разницей электроотрицательности (χ K = 0,82 против χ Ag = 1,93) нейтральных атомов при атмосферном давлении. Существенный перенос электрона от K отражается в коротком расстоянии K…K в 2D-слое 3,13 Å, что значительно меньше, чем расстояние K–K 3,82 Å в металлическом K при том же давлении [20]. Ранее очень короткое расстояние К-К привело к предположению об образовании ковалентных связей К-К. Это снова оказывается неверным. Расчеты полной энергии нейтрали К 9Димер 0394 2 и димер, образованный из катионов K, в зависимости от межатомного расстояния показывают, что взаимодействие K–K становится менее благоприятным по сравнению с K + … K + , когда расстояние между атомами меньше 3 Å (рис. 11с). Опять же, при высоком давлении энергетически выгодно упаковывать катионы металлов с меньшими размерами, чем нейтральные атомы. Этот анализ подтверждает концепцию о том, что валентные s электроны мигрируют с диффузной s орбитали на более прочно связанные 9Орбитали 0595 d , введенные выше, использовались для объяснения структур высокого давления Cs и Rb (см. Ниже). После гибридизации с – d в Cs и Rb валентные электроны переместились в междоузлия. Структуры высокого давления следовали схеме двумерной плотной упаковки катионов (архимедова мозаика) [49].
Это снова оказывается неверным. Расчеты полной энергии нейтрали К 9Димер 0394 2 и димер, образованный из катионов K, в зависимости от межатомного расстояния показывают, что взаимодействие K–K становится менее благоприятным по сравнению с K + … K + , когда расстояние между атомами меньше 3 Å (рис. 11с). Опять же, при высоком давлении энергетически выгодно упаковывать катионы металлов с меньшими размерами, чем нейтральные атомы. Этот анализ подтверждает концепцию о том, что валентные s электроны мигрируют с диффузной s орбитали на более прочно связанные 9Орбитали 0595 d , введенные выше, использовались для объяснения структур высокого давления Cs и Rb (см. Ниже). После гибридизации с – d в Cs и Rb валентные электроны переместились в междоузлия. Структуры высокого давления следовали схеме двумерной плотной упаковки катионов (архимедова мозаика) [49].Рисунок 10.
Открыть в новой вкладкеСкачать слайд
Структуры валентной зоны K 2 Ag и K 3 Ag и соответствующей гипотетической структуры ■ 2 Ag и ■ 3 Ag с удаленными атомами K (из Tse и др. [59]).
[59]).
Рисунок 11.
Открыть в новой вкладкеСкачать слайд
(a) Структура K 2 Ag и (b) K 3 Ag, показывающая графитовую и кубическую Ag-сетку, и (c) сравнение кривых потенциальной энергии для K 2 и K 2 2+ .
Рис. 12.
Открыть в новой вкладкеСкачать слайд
Вероятность трехмерной электронной плотности, полученная из анализа данных рентгеновской дифракции на образце Li–Cs при 8 ГПа и 298 К с помощью МЭМ (из Desgreniers et al. [21] ).
Более ярким примером смешения несмешиваемого является образование интерметаллидов LiCs [21]. В нормальных условиях Li и Cs не смешиваются из-за большого несоответствия их размеров. Теоретическое исследование структуры предсказало, что стехиометрические бинарные сплавы Li-Cs могут образовываться только при высоких давлениях (> 50 ГПа) [60]. Однако эксперименты по дифракции рентгеновских лучей свидетельствуют об образовании нового кристаллического сплава (сплавов) при сжатии смеси Li и Cs даже до 0,1 ГПа [21]. Это первое наблюдение бинарных сплавов между элементами группы I. Эксперименты показали нестехиометрический состав Li 9Сплав 0394 0,7 Cs формировался при 1,6 ГПа и оставался стабильным по крайней мере до 10 ГПа [21]. Структура сплава расшифрована методом МЭМ [51]. Он имел простую кубическую кристаллическую структуру, а положения Li и Cs были упорядочены. Важной особенностью кристаллической структуры является то, что валентная плотность заряда, полученная из МЭМ-анализа, показала перенос заряда с Cs 6 s на орбиталь Li 2 p (рис. 12). Напомним, что в первом ряду элементов с низким атомным номером 2 9059.5 p орбитали не имеют радиального узла и энергии 2 s , 2 p почти вырождены; тем не менее перенос заряда между электроположительными атомами щелочных металлов в одной и той же группе не ожидался. Однако разница электроотрицательностей между Li и Cs по шкале Полинга 0,2 довольно велика. Перенос электрона помогает уменьшить размер Cs (Cs δ+ ) и одновременно увеличить размер Li (Li δ- ).
Это первое наблюдение бинарных сплавов между элементами группы I. Эксперименты показали нестехиометрический состав Li 9Сплав 0394 0,7 Cs формировался при 1,6 ГПа и оставался стабильным по крайней мере до 10 ГПа [21]. Структура сплава расшифрована методом МЭМ [51]. Он имел простую кубическую кристаллическую структуру, а положения Li и Cs были упорядочены. Важной особенностью кристаллической структуры является то, что валентная плотность заряда, полученная из МЭМ-анализа, показала перенос заряда с Cs 6 s на орбиталь Li 2 p (рис. 12). Напомним, что в первом ряду элементов с низким атомным номером 2 9059.5 p орбитали не имеют радиального узла и энергии 2 s , 2 p почти вырождены; тем не менее перенос заряда между электроположительными атомами щелочных металлов в одной и той же группе не ожидался. Однако разница электроотрицательностей между Li и Cs по шкале Полинга 0,2 довольно велика. Перенос электрона помогает уменьшить размер Cs (Cs δ+ ) и одновременно увеличить размер Li (Li δ- ). Несоответствие размеров атомов становится меньше, что приводит к более эффективной упаковке. Меньший размер Cs подтверждается коротким межатомным расстоянием 3,858 Å по сравнению с 4,23 Å, соответствующим чистому металлу (Cs-II) при аналогичном давлении. Значительно более короткое расстояние Cs-Cs в сплаве по сравнению с объемным металлом напоминает расстояние K-K, наблюдаемое в K 2 Аг. Оба наблюдения согласуются с интерпретацией того, что K и Cs находятся в катионном состоянии. При высоком давлении рассеивание электронов в пустое пространство делает сжатие катионов энергетически более выгодным.
Несоответствие размеров атомов становится меньше, что приводит к более эффективной упаковке. Меньший размер Cs подтверждается коротким межатомным расстоянием 3,858 Å по сравнению с 4,23 Å, соответствующим чистому металлу (Cs-II) при аналогичном давлении. Значительно более короткое расстояние Cs-Cs в сплаве по сравнению с объемным металлом напоминает расстояние K-K, наблюдаемое в K 2 Аг. Оба наблюдения согласуются с интерпретацией того, что K и Cs находятся в катионном состоянии. При высоком давлении рассеивание электронов в пустое пространство делает сжатие катионов энергетически более выгодным.
Существенно, что экспериментальная структура LiCs не была предсказана теоретическими расчетами полной энергии [60]. Нестехиометрическая структура затрудняет теоретическое предсказание. Уместно отметить, что почти все методы прогнозирования структуры предназначены для исследования структур с глобальным минимумом энергии. Нередко в экспериментах наблюдаются метастабильные структуры, поскольку система может выбрать путь с наименьшей энергией активации в структурном преобразовании, ведущем к метастабильной структуре.
Рис. 13.
Открыть в новой вкладкеСкачать слайд
Схематическая диаграмма энергетических уровней взаимодействия двух электронных спинов в зависимости от их разделения, показывающая образование парамагнитных (ПМ), ферро- (ФМ) и антиферро- (AFM) магнитные состояния и возможное образование ковалентной связи спиновой пары. Зеленые оттенки представляют атомы, а не спин-орбиталь.
Рисунок 14.
Открыть в новой вкладкеСкачать слайд
Структура молекулярного строительного блока нейтрального радикала. С разными заместителями E 9 можно создать структуры с разным молекулярным размером.0394 1 , E 2 , R 1 и R 2 . Морфологией и магнитным состоянием кристалла можно управлять, используя строительные блоки разных размеров.
Вставка 1.
Сравнение оценок порядка величины механической работы внешним давлением с типичными значениями прочности связи.
Открыть в новой вкладке
Вставка 1.
Сравнение оценок порядка величины механической работы внешним давлением с типичными значениями прочности связи.
Открыть в новой вкладке
Чтобы проиллюстрировать это положение, на рис. 13 показаны взаимодействия между двумя идентичными частицами с открытой оболочкой, каждая из которых имеет электрон на одной занятой орбитали (например, два атома H), в зависимости от расстояния. При большом расстоянии две части независимы друг от друга, их спины ориентированы случайным образом, а магнитное (спиновое) состояние всей системы является парамагнитным. По мере сближения двух видов электронные спины начинают взаимодействовать. В модели Гейзенберга в зависимости от обменного параметра ( J ), основное магнитное (спиновое) состояние (расположение электронных спинов) может быть диамагнитным (спин-парным), ферромагнитным (ФМ) или антиферромагнитным (АФМ). Дальнейшее уменьшение расстояния приводит к образованию настоящей двухэлектронной ковалентной связи со спиновой парой. Молекулярный радикал, показанный на рис. 14, представляет собой удобную модель для изучения индуцированного давлением перехода металл → изолятор. Модельная система может быть реализована с использованием стабильных молекулярных радикалов в качестве строительных блоков кристаллических структур. Одним из классов таких молекулярных радикалов является бистиа/селеназолильный радикал и его химические варианты (рис. 14) [61–76]. Манипуляции с замещающими группами R (алкильная группа и галоген) и E (халькоген, S и Se) (рис. 14) могут привести к различной укладке молекулярных радикалов в твердом состоянии и различным магнитным основным состояниям (рис. 14). . Можно управлять магнитными свойствами этих молекулярных твердых тел, изменяя расстояние между радикальными молекулами. Первоначальная стратегия заключалась в использовании химического давления путем синтеза подобных соединений с R-группами разного размера. Это трудоемкая процедура и часто не очень эффективная. Лучшей стратегией является применение физического давления. Первый эксперимент высокого давления в ячейке с алмазной наковальней был проведен на бис-селеназолиле с R 9.0394 1 = Et, R 2 = Cl (рис.
Модельная система может быть реализована с использованием стабильных молекулярных радикалов в качестве строительных блоков кристаллических структур. Одним из классов таких молекулярных радикалов является бистиа/селеназолильный радикал и его химические варианты (рис. 14) [61–76]. Манипуляции с замещающими группами R (алкильная группа и галоген) и E (халькоген, S и Se) (рис. 14) могут привести к различной укладке молекулярных радикалов в твердом состоянии и различным магнитным основным состояниям (рис. 14). . Можно управлять магнитными свойствами этих молекулярных твердых тел, изменяя расстояние между радикальными молекулами. Первоначальная стратегия заключалась в использовании химического давления путем синтеза подобных соединений с R-группами разного размера. Это трудоемкая процедура и часто не очень эффективная. Лучшей стратегией является применение физического давления. Первый эксперимент высокого давления в ячейке с алмазной наковальней был проведен на бис-селеназолиле с R 9.0394 1 = Et, R 2 = Cl (рис. 15а) [75]. Результаты были замечательными. При атмосферном давлении был обнаружен переход парамагнитный → ферромагнитный при низкой температуре. Температура перехода (температура Кюри) увеличивалась с приложенным давлением и достигала 21 К при 0,9 ГПа (рис. 15b). Это самая высокая температура Кюри, когда-либо зарегистрированная для молекулярного магнита. Рентгеновская дифракция показала отсутствие изменений внутренней молекулярной структуры при очень слабом давлении. Вместо этого молекулярные радикалы скользили друг относительно друга ( dy , относительное смещение между двумя параллельными молекулами, находящимися в тесном контакте, на рис. 15в) и одновременное сближение молекул. Межмолекулярное взаимодействие между соседними радикалами вдоль π-стеков изменяет параметр спин-обменной связи J π . Первоначально J π увеличивалось с давлением из-за уменьшения перекрытия между соседними однократно занятыми молекулярными орбиталями. Это привело к более сильному ферромагнитному взаимодействию и более высокой температуре Кюри.
15а) [75]. Результаты были замечательными. При атмосферном давлении был обнаружен переход парамагнитный → ферромагнитный при низкой температуре. Температура перехода (температура Кюри) увеличивалась с приложенным давлением и достигала 21 К при 0,9 ГПа (рис. 15b). Это самая высокая температура Кюри, когда-либо зарегистрированная для молекулярного магнита. Рентгеновская дифракция показала отсутствие изменений внутренней молекулярной структуры при очень слабом давлении. Вместо этого молекулярные радикалы скользили друг относительно друга ( dy , относительное смещение между двумя параллельными молекулами, находящимися в тесном контакте, на рис. 15в) и одновременное сближение молекул. Межмолекулярное взаимодействие между соседними радикалами вдоль π-стеков изменяет параметр спин-обменной связи J π . Первоначально J π увеличивалось с давлением из-за уменьшения перекрытия между соседними однократно занятыми молекулярными орбиталями. Это привело к более сильному ферромагнитному взаимодействию и более высокой температуре Кюри. При дальнейшем сжатии проскальзывание π-стеков прошло минимальное (ортогональное) перекрытие и J π начала уменьшаться, как и температура Кюри.
При дальнейшем сжатии проскальзывание π-стеков прошло минимальное (ортогональное) перекрытие и J π начала уменьшаться, как и температура Кюри.
Приведенный выше пример показывает, что изменение ван-дер-ваальсова взаимодействия при малом внешнем давлении может существенно повлиять на магнитные свойства молекулярного кристалла. Обычное поведение обычной магнитной системы, т. е. парамагнитное → ФМ упорядочение, парамагнитное → АФМ упорядочение, ФМ → АФМ и изолятор → переход металл, были продемонстрированы путем сжатия этого класса молекулярных кристаллов с выбранными вариантами бистиевых/селеназолильных радикалов (рис. 16). ) [61–76]. В любом случае молекулярная структура оказалась существенно искаженной. Эти молекулярные кристаллы стабильны на воздухе и могут быть синтезированы с высокой чистотой. Легирование не обязательно для изменения электронных и магнитных свойств. Кристаллическую структуру можно точно определить in situ под высоким давлением и низкой температурой. Электронная структура молекулярного радикала по своей природе сильно коррелирована. Этот класс кристаллов послужил отличной моделью для исследования магнитных переходов и переходов металл-изолятор и коррелированных эффектов [67].
Электронная структура молекулярного радикала по своей природе сильно коррелирована. Этот класс кристаллов послужил отличной моделью для исследования магнитных переходов и переходов металл-изолятор и коррелированных эффектов [67].
Рис. 15.
Открыть в новой вкладкеСкачать слайд
(а) Кристаллическая структура нейтрального радикала с E 1 = E 2 = Se и R 1 = Et, R 2 = Кл. (b) Температура Кюри ( T c ), измеренная в гидростатическом (PCC), одноосном и в ячейке с алмазной наковальней. (c) Расчетный параметр связи Гейзенберга J π в зависимости от геометрии кристаллической структуры при различных давлениях.
Рисунок 16.
Открыть в новой вкладкеСкачать слайд
Обзор магнитных свойств различных нейтральных радикальных твердых тел.
4″ data-legacy-id=”sec5″> СТРУКТУРНЫЕ ТЕНДЕНЦИИ В ПОЛИГИДРИДАХ ВЫСОКОГО ДАВЛЕНИЯ
Интерес к исследованию структуры и свойств полигидридов при высоком давлении возник из-за предположения, что полигидридам присуща более высокая концентрация Н, чем молекулярный водород; следовательно, для их сжатия до металлического состояния может потребоваться меньшее давление. Более того, при желаемой электронной плотности может возникнуть сверхпроводимость [77]. Недавние исследования по этой теме значительно выиграли от доступности методов прогнозирования структуры, основанных на расчетах электронной структуры First Principles [78–80] в конце 2000 г. Это критическое теоретическое развитие предлагает разумный и логичный способ исследования стабильных структур высокого давления, иначе не поддающихся обработке. экспериментировать. С тех пор было проведено множество исследований бинарных и тройных полигидридных систем с различными элементами. В большинстве работ сообщается о термодинамически стабильных (глобальный минимум) структурах при заданном давлении, но имеется несколько глубоких анализов эволюции структур в зависимости от давления или концентрации водорода. Как показано во вставке 1, прочность связи общих элементов главной группы с H находится в пределах порядка нескольких электрон-вольт; следовательно, разрыв связи возможен, если внешнее давление находится в диапазоне мегабар.
Более того, при желаемой электронной плотности может возникнуть сверхпроводимость [77]. Недавние исследования по этой теме значительно выиграли от доступности методов прогнозирования структуры, основанных на расчетах электронной структуры First Principles [78–80] в конце 2000 г. Это критическое теоретическое развитие предлагает разумный и логичный способ исследования стабильных структур высокого давления, иначе не поддающихся обработке. экспериментировать. С тех пор было проведено множество исследований бинарных и тройных полигидридных систем с различными элементами. В большинстве работ сообщается о термодинамически стабильных (глобальный минимум) структурах при заданном давлении, но имеется несколько глубоких анализов эволюции структур в зависимости от давления или концентрации водорода. Как показано во вставке 1, прочность связи общих элементов главной группы с H находится в пределах порядка нескольких электрон-вольт; следовательно, разрыв связи возможен, если внешнее давление находится в диапазоне мегабар. Например, было предсказано, что SiH 4 превращается в сверхпроводящую фазу около 60 ГПа. Среди многих теоретических работ по полигидридам [23] структуры гидридов стронция проанализированы очень подробно. Это исследование помогло пролить свет на возможный механизм (механизмы) появления H – при низком давлении и образования сетей H при высоком давлении с увеличением содержания H [81].
Например, было предсказано, что SiH 4 превращается в сверхпроводящую фазу около 60 ГПа. Среди многих теоретических работ по полигидридам [23] структуры гидридов стронция проанализированы очень подробно. Это исследование помогло пролить свет на возможный механизм (механизмы) появления H – при низком давлении и образования сетей H при высоком давлении с увеличением содержания H [81].
Глобальные минимальные структуры SrH 2 n ( n = 1–5)
в диапазоне давлений 50–300 ГПа, предсказанном методом оптимизации роя частиц, показаны на рис. 17 [81,82]. Исследование полиморфов высокого давления выявляет тенденцию в структурных мотивах. При низкой концентрации H, например, в SrH 2 , до 60 ГПа, атомы H остаются в виде одноатомных анионов. В SrH 4 в структурах до 150 ГПа обнаружена равная смесь одноатомных димеров H и H 2 . Морфология структурных единиц H более разнообразна в SrH 6 . При 50 и 150 ГПа полиморфы образуются из одноатомного Н и трансформируются в изогнутые единицы Н 3 при 200 ГПа. При дальнейшем сжатии до 250 ГПа звенья H 3 соединяются, образуя спиральные цепочки. В СрХ 8 , снова фрагменты H и H 2 обнаруживаются в структуре 50 ГПа. При 150 ГПа возникает смесь H 2 и изогнутых единиц H 3 . Структурная эволюция полиморфных модификаций SrH 10 высокого давления протекает аналогично. Наиболее стабильная структура при 50 ГПа снова состоит из звеньев H – и H 2 , но трансформированных в H 2 и изогнутых фрагментов H 3 при 150 ГПа. Интересно, что при 300 ГПа структура состоит из сморщенных гексагональных сотовых слоев атомов H. Поля стабильности SrH 2 n structures with different H stoichiometries are shown in Fig. 18.
При дальнейшем сжатии до 250 ГПа звенья H 3 соединяются, образуя спиральные цепочки. В СрХ 8 , снова фрагменты H и H 2 обнаруживаются в структуре 50 ГПа. При 150 ГПа возникает смесь H 2 и изогнутых единиц H 3 . Структурная эволюция полиморфных модификаций SrH 10 высокого давления протекает аналогично. Наиболее стабильная структура при 50 ГПа снова состоит из звеньев H – и H 2 , но трансформированных в H 2 и изогнутых фрагментов H 3 при 150 ГПа. Интересно, что при 300 ГПа структура состоит из сморщенных гексагональных сотовых слоев атомов H. Поля стабильности SrH 2 n structures with different H stoichiometries are shown in Fig. 18.
Figure 17.
Open in new tabDownload slide
Predicted stable structures of SrH 2 n ( n = 1– 5) при различных давлениях (из Wang и др. [81]).
Рисунок 18.
Открыть в новой вкладкеСкачать слайд
Прогнозируемые последовательности фазовых переходов полигидридов стронция при повышении давления (адаптировано из Wang и др. [81]).
Структурная тенденция не является неожиданной с химической точки зрения. При низкой концентрации H, т.е. SrH 2 , предполагается, что два электрона от электроположительного Sr отдаются H 2 , занимая антисвязывающую орбиталь H – H и, таким образом, диссоциируя молекулу, образующую ионный Sr 2+ … H – . При более высокой концентрации H, если предположить, что электроны являются общими для всех H 2 , электронов будет недостаточно для разрыва связей H–H. У системы есть две альтернативы: (i) взлом выбранной H 2 с образованием одноатомного H и/или (ii) разделением донорных электронов между кластерами атомов H и сохранением некоторых связей H–H. При низком давлении механизм (i) энергетически более выгоден. Поэтому одноатомные частицы H и H 2 часто наблюдались в структурах низкого давления SrH 2 n ( n = 2–5) и других гидридов основной группы. При более высоком давлении H и H 2 сближаются. Чтобы уменьшить отталкивание электронов, предпочтительно образовывать H 3 единиц за счет распределения электронов, отдаваемых Sr, между тремя атомами H. В H 3 третий электрон находится на несвязывающей орбитали, и поэтому система все еще сохраняет некоторую устойчивость. Дальнейшее сжатие приводит к соединению блоков H 3 в виде спиральных цепочек и гофрированных двухмерных сотовых слоев.
Поэтому одноатомные частицы H и H 2 часто наблюдались в структурах низкого давления SrH 2 n ( n = 2–5) и других гидридов основной группы. При более высоком давлении H и H 2 сближаются. Чтобы уменьшить отталкивание электронов, предпочтительно образовывать H 3 единиц за счет распределения электронов, отдаваемых Sr, между тремя атомами H. В H 3 третий электрон находится на несвязывающей орбитали, и поэтому система все еще сохраняет некоторую устойчивость. Дальнейшее сжатие приводит к соединению блоков H 3 в виде спиральных цепочек и гофрированных двухмерных сотовых слоев.
Представленное здесь качественное описание предполагает формальный перенос двух валентных электронов от атома Sr. Это предположение подтверждается рассмотрением различий плотности заряда, Δρ = ρ (SrH 2 n ) − [ρ (Sr■ 2 ) + ρ(■H 2 n )], где ■ указывает на вакантные позиции Sr или H в соответствующем кристалле SrH
5 2 n структура. Сравнение различий плотности заряда для SrH n ( n = 1–10) при 150 ГПа показано на рис. 19. Действительно, во всех структурах наблюдается значительный перенос электронов от Sr к частицам H. .
Сравнение различий плотности заряда для SrH n ( n = 1–10) при 150 ГПа показано на рис. 19. Действительно, во всех структурах наблюдается значительный перенос электронов от Sr к частицам H. .Рисунок 19.
Открыть в новой вкладкеСкачать слайд
Изоповерхность разности плотности заряда для SrH 2 ( P 6/ ммм ), SrH 4 ( Cmcm ), SrH 6 ( 8 ( P 21/c) и SrH 10 ( P 2/ c ) при 150 ГПа. Истощение и накопление заряда показаны синим и красным цветом соответственно (от Wang et al. [81]).
Движущая сила переноса электрона снова связана с разницей в электроотрицательности между Sr и H 2 . Малликен определил электроотрицательность частиц как среднее арифметическое потенциала ионизации и сродства к электрону. Эти величины могут быть вычислены из теории функционала плотности как первая и вторая производные от изменения полной энергии по числу электронов [83]. Используя почти полный атомный базис для H, электроотрицательность молекулы H 2 рассчитана как 1,71 по шкале Полинга [81]. Это значение заметно близко к электроотрицательности элементов XIII и XIV групп (1,61–2,33), которые, как известно, образуют интерметаллиды Zintl со щелочными металлами [84]. Электроотрицательность Sr по шкале Полинга равна 0,9.5. Большая разница в электроотрицательности (Δχ = 0,76) между Sr и H 2 предполагает возможность образования ионной связи в полиморфах SrH 2 . Примечательно, что, когда концентрация H значительно превышает доступное количество электронов, отдаваемых атомами металла, на отдельные H 2 приобретается лишь малая часть электронов. При этом не происходит существенного изменения молекулярных Н-Н-связей. Таким образом, при низком давлении преобладают молекулярные формы H 2 , а кристаллическая структура состоит в основном из недиссоциированных H 2 молекул. Это простое описание было успешно применено для понимания структурной тенденции полигидридов кальция [85].
Используя почти полный атомный базис для H, электроотрицательность молекулы H 2 рассчитана как 1,71 по шкале Полинга [81]. Это значение заметно близко к электроотрицательности элементов XIII и XIV групп (1,61–2,33), которые, как известно, образуют интерметаллиды Zintl со щелочными металлами [84]. Электроотрицательность Sr по шкале Полинга равна 0,9.5. Большая разница в электроотрицательности (Δχ = 0,76) между Sr и H 2 предполагает возможность образования ионной связи в полиморфах SrH 2 . Примечательно, что, когда концентрация H значительно превышает доступное количество электронов, отдаваемых атомами металла, на отдельные H 2 приобретается лишь малая часть электронов. При этом не происходит существенного изменения молекулярных Н-Н-связей. Таким образом, при низком давлении преобладают молекулярные формы H 2 , а кристаллическая структура состоит в основном из недиссоциированных H 2 молекул. Это простое описание было успешно применено для понимания структурной тенденции полигидридов кальция [85]. Предупреждение о применении концепции электроотрицательности при высоком давлении заключается в том, что в принципе электроотрицательность определяется только для элементов при атмосферном давлении. Таким образом, модель может применяться только к полигидридам, состоящим из металлов с низкой первой энергией ионизации, и ее не следует использовать без разбора. Например, богатый водородом хлор группы 17 (H n Cl, n = 2–7) соединения ведут себя совершенно иначе, чем гидриды металлов [86].
Предупреждение о применении концепции электроотрицательности при высоком давлении заключается в том, что в принципе электроотрицательность определяется только для элементов при атмосферном давлении. Таким образом, модель может применяться только к полигидридам, состоящим из металлов с низкой первой энергией ионизации, и ее не следует использовать без разбора. Например, богатый водородом хлор группы 17 (H n Cl, n = 2–7) соединения ведут себя совершенно иначе, чем гидриды металлов [86].
Рисунок 20.
Открыть в новой вкладкеСкачать слайд
Прогнозируемая температура сверхпроводимости выбранных полигидридов (адаптировано из Ma et al . (частное сообщение)). Проиллюстрированы структуры для гидридов с высоким T c . Цифры в квадратных скобках обозначают давление, при котором было рассчитано T c .
Поиски сверхпроводимости в плотных металлических полигидридах были начаты до того, как стали доступны методы прогнозирования структуры First Principles. Первый численный расчет сверхпроводящей критической температуры гидрида при высоком давлении с использованием современного метода электронной структуры First Principles [89].,90] на силане, SiH 4 [91]. Структурная модель высокого давления была получена путем объединения молекулярно-динамического моделирования с конечной температурой и постоянным давлением и оптимизации геометрии ab initio . Переход изолятор → металл с непрямым закрытием зазора был обнаружен при 60 ГПа. Параметр электрон-фононного взаимодействия (λ), показатель силы потенциальной сверхпроводимости фазы высокого давления, основанный на фононно-опосредованной теории Бардина-Купера-Шриффера (БКШ) [89,9].0] был рассчитан при 90 и 125 ГПа с использованием метода линейного отклика возмущения [89]. Были предсказаны большие электрон-фононные связи, близкие к 0,9. Используя уравнение Макмиллана [92], T c оценивается в диапазоне от 45 до 55 K. В то время результат был замечательным, поскольку считалось, что верхний предел T c достижим при механизм БКШ составлял около 40 К [92]. Позже расчеты SnH 4 предсказали еще более высокое значение 9059.5 T c 80 К при 120 ГПа [93]. Сверхпроводимость в SiH 4 действительно наблюдалась в эксперименте [94]. Сообщалось о T c из 17 K при 120 ГПа. Однако природа сверхпроводящей фазы все еще обсуждается. Одно из предположений связывает сверхпроводимость с образованием сверхпроводящего PtH в результате реакции Pt-электродов с разложившимся SiH 4 [95].
Параметр электрон-фононного взаимодействия (λ), показатель силы потенциальной сверхпроводимости фазы высокого давления, основанный на фононно-опосредованной теории Бардина-Купера-Шриффера (БКШ) [89,9].0] был рассчитан при 90 и 125 ГПа с использованием метода линейного отклика возмущения [89]. Были предсказаны большие электрон-фононные связи, близкие к 0,9. Используя уравнение Макмиллана [92], T c оценивается в диапазоне от 45 до 55 K. В то время результат был замечательным, поскольку считалось, что верхний предел T c достижим при механизм БКШ составлял около 40 К [92]. Позже расчеты SnH 4 предсказали еще более высокое значение 9059.5 T c 80 К при 120 ГПа [93]. Сверхпроводимость в SiH 4 действительно наблюдалась в эксперименте [94]. Сообщалось о T c из 17 K при 120 ГПа. Однако природа сверхпроводящей фазы все еще обсуждается. Одно из предположений связывает сверхпроводимость с образованием сверхпроводящего PtH в результате реакции Pt-электродов с разложившимся SiH 4 [95]. Это предположение не является разумным, так как электроды Pt не соприкасались, поэтому, если бы даже PtH был сверхпроводящим [96] и силана не было, никакой сверхпроводимости не было бы обнаружено. Более того, дальнейшее сжатие в ходе эксперимента до 150 ГПа привело к образованию теоретически предсказанной стехиометрической изолирующей фазы SiH 4 [94,97] без заметной примеси Si на дифрактограмме, если бы произошла реакция с Pt. Численные расчеты и эксперимент подтверждают предположение о том, что сверхпроводимость может быть достигнута за счет сжатия «предварительно уплотненных» гидридов [77]. Совсем недавно был установлен рекорд T c из 200 K сообщалось о сжатом H 2 S, хотя и при 200 ГПа [8]. Гениальный синхротронный мессбауэровский ядерный эксперимент по рассеянию вперед с использованием Sn-фольги в качестве зонда однозначно продемонстрировал эффект Мейснера [98]. Эксперимент в дальнем инфракрасном диапазоне также подтвердил, что энергия сверхпроводящей щели сравнима с предсказанием теории БКШ [99].
Это предположение не является разумным, так как электроды Pt не соприкасались, поэтому, если бы даже PtH был сверхпроводящим [96] и силана не было, никакой сверхпроводимости не было бы обнаружено. Более того, дальнейшее сжатие в ходе эксперимента до 150 ГПа привело к образованию теоретически предсказанной стехиометрической изолирующей фазы SiH 4 [94,97] без заметной примеси Si на дифрактограмме, если бы произошла реакция с Pt. Численные расчеты и эксперимент подтверждают предположение о том, что сверхпроводимость может быть достигнута за счет сжатия «предварительно уплотненных» гидридов [77]. Совсем недавно был установлен рекорд T c из 200 K сообщалось о сжатом H 2 S, хотя и при 200 ГПа [8]. Гениальный синхротронный мессбауэровский ядерный эксперимент по рассеянию вперед с использованием Sn-фольги в качестве зонда однозначно продемонстрировал эффект Мейснера [98]. Эксперимент в дальнем инфракрасном диапазоне также подтвердил, что энергия сверхпроводящей щели сравнима с предсказанием теории БКШ [99].
За первоначальными расчетами SiH 4 и SnH 4 последовало множество теоретических отчетов о различных гидридах высокого давления с элементами периодической таблицы, многие из которых показывают T c свыше 100 К при давлениях свыше 100 ГПа [87,88]. Для CaH 6 было предсказано отчетливо высокое значение T c 220–235 К при 150 ГПа [85]. В отличие от других гидридов, изученных ранее, CaH 6 имеет уникальную структуру содалита, в которой атомы H образуют открытый клатратный каркас с атомами Ca, заключенными в полости (рис. 20). Впоследствии YH 6 [100], YH 10 , LaH 6 и LaH 10 с клатратоподобными структурами [101, 102] были предсказаны как высокоэффективные сверхпроводники с T c близка к комнатной температуре при давлении ~200 ГПа [8]. Недавний эксперимент подтверждает, что LaH 10 имеет T c 260 K в диапазоне от 180 до 200 ГПа [9]. Сводка выбранных полигидридов с высоким содержанием T c показана на рис. 20. Два общих структурных мотива проявляются для полигидридов с высоким содержанием T c : один с H-клатратными структурами, а другой с гофрированными сотовыми слоями Атомы Н. Почему клатратный каркас из H-атома и двумерные гофрированные сотовые слоистые структуры обеспечивают такие высокие Т с ?
Сводка выбранных полигидридов с высоким содержанием T c показана на рис. 20. Два общих структурных мотива проявляются для полигидридов с высоким содержанием T c : один с H-клатратными структурами, а другой с гофрированными сотовыми слоями Атомы Н. Почему клатратный каркас из H-атома и двумерные гофрированные сотовые слоистые структуры обеспечивают такие высокие Т с ?
Для понимания фундаментального механизма сильной электрон-фононной связи в богатых водородом сплавах уравнение Элиашберга [103] решалось в рамках теории Мигдала–Элиашберга с использованием спектральных функций (α F (ω)), полученных из электронных структурные расчеты [98,99]. Спектральная функция Элиашберга содержит всю информацию об электрон-фононном взаимодействии отдельной моды колебаний. Он определяется как [90,104]:
92F\left(\omega\right)=\frac{1}{2\pi N\left({\epsilon}_F\right)}\sum_{\boldsymbol{q}\!\upsilon}\frac{\gamma_ {\!\boldsymbol{q}\!\upsilon}}{\omega_{\boldsymbol{q}\!\upsilon}}\delta \left(\omega -{\omega}_{\boldsymbol{q}\! \upsilon}\right)\!, \end{equation}$$(1)
где N (ε F ) — плотность электронных состояний при энергии Ферми ε F . 2\delta\left({\epsilon}_ {\ mathit {kj}} – {\ epsilon} _F \ right) \ nonumber \\ && \ times \, \ delta \ left ({\ epsilon} _ {k + {q} _ {j \ простое число}} – {\ эпсилон}_F\справа)\!,
\end{eqnarray}$$ 9{\boldsymbol{q}\!\upsilon}V\right| \mathit{kj}\right\rangle\!,\end{equation}$$
2\delta\left({\epsilon}_ {\ mathit {kj}} – {\ epsilon} _F \ right) \ nonumber \\ && \ times \, \ delta \ left ({\ epsilon} _ {k + {q} _ {j \ простое число}} – {\ эпсилон}_F\справа)\!,
\end{eqnarray}$$ 9{\boldsymbol{q}\!\upsilon}V\right| \mathit{kj}\right\rangle\!,\end{equation}$$
(3)
в котором электронное состояние k j связано с фононной модой ω q ν и рассеяны на k + q j ′ .
Рис. 21.
Открыть в новой вкладкеСкачать слайд
Электронно-фононная спектральная функция Элиашберга (α 2 F (ω)) для SiH 4 , SnH 4 , CaH 2 и YH 6 .
Спектральные функции Элиашберга для четырех типичных гидридов SiH 4 [91], SnH 4 [93], CaH 6 [85] и YH 6 [100] с увеличением T 94 c 94 45, 80, 230 и 260 К сравниваются на рис. 21. В SnH 4 молекулярно-подобный H 2 интеркалирован между двумя слоями атомов Sn [93]. Спектральная функция четко разделена на три области: трансляцию, либрацию и растяжение H–H. Интегральная константа электрон-фононного взаимодействия λ(ω) показывает, что основной вклад вносят либрационные колебания с меньшим вкладом трансляционных мод. Удивительно, что высокая частота (>2000 см −1 ) Внутреннее растяжение H–H не вносит существенного вклада. Это противоречит упрощенному ожиданию, что чем выше «средняя» частота, тем больше электрон-фононная связь [92]. В SiH 4 H 2 связывает два атома Si в двумерном слое. Теперь колебания растяжения и либрации смешаны, и больше нет четкого разделения на две отдельные области вибрации. Однако в этих двух системах электрон-фононная связь слаба. Например, общий параметр электрон-фононного взаимодействия составляет λ = 0,9.в SiH 4 и немного ниже, чем в SnH 4 . С другой стороны, спектральные функции CaH 6 и YH 6 со структурами содалита заметно отличаются от SiH 4 и SnH 4 .
21. В SnH 4 молекулярно-подобный H 2 интеркалирован между двумя слоями атомов Sn [93]. Спектральная функция четко разделена на три области: трансляцию, либрацию и растяжение H–H. Интегральная константа электрон-фононного взаимодействия λ(ω) показывает, что основной вклад вносят либрационные колебания с меньшим вкладом трансляционных мод. Удивительно, что высокая частота (>2000 см −1 ) Внутреннее растяжение H–H не вносит существенного вклада. Это противоречит упрощенному ожиданию, что чем выше «средняя» частота, тем больше электрон-фононная связь [92]. В SiH 4 H 2 связывает два атома Si в двумерном слое. Теперь колебания растяжения и либрации смешаны, и больше нет четкого разделения на две отдельные области вибрации. Однако в этих двух системах электрон-фононная связь слаба. Например, общий параметр электрон-фононного взаимодействия составляет λ = 0,9.в SiH 4 и немного ниже, чем в SnH 4 . С другой стороны, спектральные функции CaH 6 и YH 6 со структурами содалита заметно отличаются от SiH 4 и SnH 4 . В клатратной структуре атомы H связаны, образуя открытую каркасную структуру, и локализованных H–H-вибронов больше нет. Интегральная λ непрерывно увеличивается с частотой колебаний, показывая, что все фононы участвуют в электрон-фононном взаимодействии, что дает очень высокое значение λ, 2,69.в CaH 6 [85] и 2,93 в YH 6 [100].
В клатратной структуре атомы H связаны, образуя открытую каркасную структуру, и локализованных H–H-вибронов больше нет. Интегральная λ непрерывно увеличивается с частотой колебаний, показывая, что все фононы участвуют в электрон-фононном взаимодействии, что дает очень высокое значение λ, 2,69.в CaH 6 [85] и 2,93 в YH 6 [100].
Рис. 22.
Открыть в новой вкладкеСкачать слайд
Функциональная производная спектральной функции Элиашберга для SnH 4 (a), SiH 4 (b), YH 6 (c) и CaH 6 (г) (из Танаки и др. [106]).
Функциональная производная спектральной функции δ T c /δα 2 F (ω) [105, 106] позволяет идентифицировать частотные области, в которых электрон-фононное взаимодействие наиболее эффективно. Результаты анализа тех же четырех гидридов суммированы на рис. 22 [106]. Максимум в δ T c /δα 2 F (ω) График vs. Отклонение от этой частоты испортит T c . Оптимальные частоты для SiH 4 , SnH 4 , CaH 6 и YH 6 составляют 38, 65, 150 и 143 мэВ (1 мэВ = 8,0655 см −1 907,1 Тл = ,1). Известно, что оптимальная частота ω opt ≈ 7 k B T c [104], а рассчитанное ω opt следует тенденции увеличения T c . В SiH 4 и SnH 4 оптимальная частота достигала максимума в области поступательных колебаний или чуть выше нее. Результаты показывают, что либрационные и валентные колебания неэффективны для усиления электрон-фононной связи. Для сравнения, ω opt CaH 6 и YH 6 близки к самой высокой частоте отсечки соответствующих колебательных спектров (рис. 21 и 22). В последних двух системах наиболее эффективными фононными модами для электрон-фононного взаимодействия являются либрационные моды.
Отклонение от этой частоты испортит T c . Оптимальные частоты для SiH 4 , SnH 4 , CaH 6 и YH 6 составляют 38, 65, 150 и 143 мэВ (1 мэВ = 8,0655 см −1 907,1 Тл = ,1). Известно, что оптимальная частота ω opt ≈ 7 k B T c [104], а рассчитанное ω opt следует тенденции увеличения T c . В SiH 4 и SnH 4 оптимальная частота достигала максимума в области поступательных колебаний или чуть выше нее. Результаты показывают, что либрационные и валентные колебания неэффективны для усиления электрон-фононной связи. Для сравнения, ω opt CaH 6 и YH 6 близки к самой высокой частоте отсечки соответствующих колебательных спектров (рис. 21 и 22). В последних двух системах наиболее эффективными фононными модами для электрон-фононного взаимодействия являются либрационные моды. Отсутствие вибронов H–H в клатратной структуре свидетельствует о том, что фононные моды сосредоточены в либрациях (т.е. о высокой колебательной плотности состояний в этой области).
Отсутствие вибронов H–H в клатратной структуре свидетельствует о том, что фононные моды сосредоточены в либрациях (т.е. о высокой колебательной плотности состояний в этой области).
Обычно считается, что сверхпроводящая фаза сжатого H 2 S представляет собой H 3 S, продукт разложения H 2 S под экстремальным давлением [8]. По-видимому, как наблюдаемая T c , так и in situ рентгенограмма [107] хорошо согласуются с теоретически предсказанной структурой H 3 S [108]. Кристаллическая структура H 3 S представляет собой ОЦК с атомами серы, расположенными в центре кубического ящика, образованного трехмерной водородной сеткой (рис. 23). В некотором смысле эта структура похожа на клатратоподобные структуры. Частота среза колебательного спектра около 2000 см -1 показывает отсутствие высокочастотных молекулярных вибронов. Был выполнен анализ функции Элиашберга теоретической структуры H 3 S [109], и оптимальная частота, полученная из производной функции Элиашберга ∼120 мэВ, сравнима с частотой CaH 6 и YH 6 . . Сравнение T c , ω opt и ω log , а также длин связей H–H приведено в таблице 1.
. Сравнение T c , ω opt и ω log , а также длин связей H–H приведено в таблице 1.
Рис. 23.
Открыть в новой вкладкеСкачать слайд
Кристаллическая структура предсказанного H 3 S, показывающая инкапсуляцию S внутри H-клетки (от Tanaka et al. [106]).
Таблица 1.
Сравнение T c , оптимальной частоты ω opt , средней фононной частоты ω log и расстояния H–H в сети H для обсуждаемых здесь систем.
| Система . | Давление (ГПа) . | Т с (К) . | ω опт (мэВ) . | ω log (мэВ) . | Расстояние H-H (Å) . | ||
|---|---|---|---|---|---|---|---|
| SIH 4 | 125 | 53 | 38 | 79 | – | ||
| SNH 4 | |||||||
| 120 | 98 | 68 | 76 | 0. 841 841 | |||
| YH 6 | 120 | 247 | 150 | 63 | 1.306 | ||
| YH 10 | 250 | 291 | 177 | 95 | 1,132 | ||
| YH 10 | 300 | 275 | 170 | 125 | 1.029 | 170125 | 1.029 | 0005
| LaH 10 | 300 | 231 | 144 | 123 | 1.076 | ||
| CaH 6 | 150 | 235 | 143 | 87 | 1.238 | ||
| SRH 10 | 300 | 259 | 159 | 66 | 0,997 |
| Система. . | Давление (ГПа) . | Т с (К) . | ω опт (мэВ)
. | ω log (мэВ) . | Расстояние H-H (Å) . | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| SIH 4 | 125 | 53 | 38 | 79 | – | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SNH 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 120 | 98 | 68 | 76 | 0.841 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| YH 6 | 120 | 247 | 150 | 63 | 1.306 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| YH 10 | 250 | 291 | 177 | 95 | 1,132 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| YH 10 | 300 | 275 | 170 | 125 | 1.029 | 170125 | 1.029 | 0005|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LaH 10 | 300 | 231 | 144 | 123 | 1.076 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CaH 6 | 150 | 235 | 143 | 87 | 1. 238 238 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SrH 10 | 300 | 259 | 159 | 66 | 0,997 |
| Система . | Давление (ГПа) . | Т с (К) . | ω опт (мэВ) . | ω log (мэВ) . | Расстояние H-H (Å) . |
|---|---|---|---|---|---|
| SiH 4 | 125 | 53 | 38 | 79 | – |
| SnH 4 | 120 | 98 | 68 | 76 | 0. 841 841 |
| YH 6 | 120 | 247 | 150 | 63 | 1.306 |
| YH 10 | 250 | 291 | 177 | 95 | 1.132 |
| YH 10 | 300 | 275 | 170 | 125 | 1.029 |
| LaH 10 | 300 | 231 | 144 | 123 | 1.076 |
| CaH 6 | 150 | 235 | 143 | 87 | 1.238 |
| SrH 10 | 300 | 259 | 159 | 66 | 0.997 |
| System . | Давление (ГПа) . | Т с (К) . | ω опт (мэВ)
. | ω log (мэВ) . | Расстояние H-H (Å) . |
|---|---|---|---|---|---|
| SiH 4 | 125 | 53 | 38 | 79 | – |
| SnH 4 | 120 | 98 | 68 | 76 | 0.841 |
| YH 6 | 120 | 247 | 150 | 63 | 1.306 |
| YH 10 | 250 | 291 | 177 | 95 | 1.132 |
| YH 10 | 300 | 275 | 170 | 125 | 1.029 |
| Лах 10 | 300 | 231 | 144 | 123 | 1,076 |
| CAH 6 | |||||
| CAH 6 | |||||
| CAH 6 | |||||
| CAH 6 0005 | 150 | 235 | 143 | 87 | 1. 238 238 |
| SrH 10 | 300 | 259 | 159 | 66 | 0.997 |
Открыть в новой вкладке
Есть два основных вклада в большой параметр электрон-фононного взаимодействия. Площадь спектра α 2 F (ω) дает полную силу электрон-фононной связи, а функциональная производная указывает наиболее эффективные фононные моды для связи [104]. Поскольку колебательный профиль в основном определяется структурой (химической связью) кристалла, анализ спектральной функции Элиашберга показывает, что только структуры с взаимосвязанными H-сетками (такими как клатраты и двумерные сотовые H-слои) без H 2 виброна и T c для тех систем выше.
Можно ли реализовать полигидрид с T c при температуре выше комнатной? На данный момент эксперименты подтверждают (см. Ниже) механизм сверхпроводимости, опосредованный фононами БКШ, как действительный в гидридах высокого давления. Предыдущие исследования [14, 109] продемонстрировали линейную зависимость сверхпроводящей щели 2Δ 0 / k B T c от логарифмической фононной частоты (ω 92F\!\left(\omega \right)\ln \omega \right)\!.\end{equation}$$
Ниже) механизм сверхпроводимости, опосредованный фононами БКШ, как действительный в гидридах высокого давления. Предыдущие исследования [14, 109] продемонстрировали линейную зависимость сверхпроводящей щели 2Δ 0 / k B T c от логарифмической фононной частоты (ω 92F\!\left(\omega \right)\ln \omega \right)\!.\end{equation}$$
(4)
Подгонка данных, представленных в Carbotte [104] и Nicol and Carbotte [ 109] мы получили следующую эмпирическую линейную зависимость:
$$\begin{equation} \frac{2{\Delta}_0}{k_B{T}_c}=9,5\left(\frac{T_c}{\omega_{\rm{log}}}\right)+3,4. \end{equation}$$
(5)
Замена T c = 300 K для сверхпроводника при комнатной температуре, ω ln ≈ ω opt ≈ 7 k B T c расчетная оптимальная частота составляет 181 мэВ или 1137 см −1 . Это значение не слишком далеко от «лучшего» ω opt из YH 6 из 1200 см −1 .
Это значение не слишком далеко от «лучшего» ω opt из YH 6 из 1200 см −1 .
В химическом описании большая электрон-фононная связь соответствует сильной вибронной связи, т.е. сильной связи между электронными и колебательными состояниями [111–115] в молекулах. Было показано, что вибронное взаимодействие молекул и твердых тел имеет много общих черт, поэтому учет этого эффекта может помочь в создании твердых тел с сильным электрон-фононным взаимодействием [115]. В молекулярных системах вибронная связь связана с эффектом Яна-Теллера (ЯТ) [116]: когда молекула находится в вырожденном электронном состоянии, она должна искажаться, чтобы уменьшить молекулярную симметрию и снизить полную энергию. Например, частичное заполнение вырожденной орбитали приведет к орбитально вырожденному электронному состоянию, подверженному ян-теллеровскому (ЯТ) искажению. Искажение Ян-Теллера может быть статическим или динамическим по своей природе. Статическое искажение приводит к постоянному изменению молекулярной симметрии. В твердом теле ян-теллеровское искажение проявляется как структурный фазовый переход, связанный с понижением симметрии пространственной группы кристалла. С другой стороны, если искажение динамическое, то временные колебания нормальной моды большой амплитуды приводят к флуктуациям дисперсии электронных зон вблизи уровня Ферми. Эффект ЯТ использовался для объяснения сверхпроводимости, наблюдаемой в алмазе, легированном бором (p-) [117–119].]. В алмазе в центре зоны наибольшей заполненной полосой в чистом алмазе является большинство C 2 p трижды вырожденных t 1u кристаллических орбиталей [118]. В модели жесткой зоны создание «дырок» путем замены C на B (p-легирование) эквивалентно удалению электронов из этой зоны. В результате должно происходить спонтанное искажение, чтобы смягчить вырождение. Рисунок 24 иллюстрирует электронную зонную структуру нескольких небольших смещений атомов углерода вдоль t 1u колебательная мода [119]. Было обнаружено, что даже небольшое смещение ∼0,03 Å (0,01 a 0 , a 0 – размер равновесной элементарной ячейки) приводит к большим изменениям дисперсии валентных зон вблизи уровня Ферми, особенно на центр зоны (Γ) [119].
В твердом теле ян-теллеровское искажение проявляется как структурный фазовый переход, связанный с понижением симметрии пространственной группы кристалла. С другой стороны, если искажение динамическое, то временные колебания нормальной моды большой амплитуды приводят к флуктуациям дисперсии электронных зон вблизи уровня Ферми. Эффект ЯТ использовался для объяснения сверхпроводимости, наблюдаемой в алмазе, легированном бором (p-) [117–119].]. В алмазе в центре зоны наибольшей заполненной полосой в чистом алмазе является большинство C 2 p трижды вырожденных t 1u кристаллических орбиталей [118]. В модели жесткой зоны создание «дырок» путем замены C на B (p-легирование) эквивалентно удалению электронов из этой зоны. В результате должно происходить спонтанное искажение, чтобы смягчить вырождение. Рисунок 24 иллюстрирует электронную зонную структуру нескольких небольших смещений атомов углерода вдоль t 1u колебательная мода [119]. Было обнаружено, что даже небольшое смещение ∼0,03 Å (0,01 a 0 , a 0 – размер равновесной элементарной ячейки) приводит к большим изменениям дисперсии валентных зон вблизи уровня Ферми, особенно на центр зоны (Γ) [119]. Аналогичное объяснение использовалось для объяснения сильной электрон-фононной связи и очень высокого значения T c , предсказанного для CaH 6 [85]. Исследования взаимодействия между вибронной связью и сильной электрон-фононной связью в твердых телах могут обеспечить дальнейшее понимание этого механизма и внести свой вклад в разработку стратегий синтеза материалов с еще более высокими Т в [120].
Аналогичное объяснение использовалось для объяснения сильной электрон-фононной связи и очень высокого значения T c , предсказанного для CaH 6 [85]. Исследования взаимодействия между вибронной связью и сильной электрон-фононной связью в твердых телах могут обеспечить дальнейшее понимание этого механизма и внести свой вклад в разработку стратегий синтеза материалов с еще более высокими Т в [120].
Рис. 24.
Открыть в новой вкладкеСкачать слайд
Изменение дисперсии валентных зон алмаза, легированного В, в зависимости от амплитуды смещения (Δ x ) фононной моды t 1u ( из Tse и др. [118]).
Полезным руководством для предсказания сверхпроводимости является теория сосуществования крутых и плоских зон в импульсном пространстве [121–126]. Предполагается, что электронно-дырочное спаривание в реальном пространстве тесно связано с химической связью. Признаком сильных взаимодействий является одновременное присутствие электронных зон с нулевыми скоростями Ферми (плоские полосы) и высокими скоростями Ферми (почти свободная зона проводимости электронов) вблизи уровня Ферми. Первое можно рассматривать как промежуточное полярон-фононное взаимодействие, как и в высоких T c купраты [121,123]. Последнее является обычной слабой связью в теории среднего поля сверхпроводимости. Двухзонная модель [127, 128] успешно использовалась для объяснения T c в различных соединениях с двумерным слоем [126, 128], включая Ca [127], CaC 6 [121] и MgB 2 [126, 128]. 127]. Сосуществование крутых и плоских зон отмечено также в зонных структурах сверхпроводящих гидридов SnH 4 [91], CaH 6 [85] и H 3 S [129].
Первое можно рассматривать как промежуточное полярон-фононное взаимодействие, как и в высоких T c купраты [121,123]. Последнее является обычной слабой связью в теории среднего поля сверхпроводимости. Двухзонная модель [127, 128] успешно использовалась для объяснения T c в различных соединениях с двумерным слоем [126, 128], включая Ca [127], CaC 6 [121] и MgB 2 [126, 128]. 127]. Сосуществование крутых и плоских зон отмечено также в зонных структурах сверхпроводящих гидридов SnH 4 [91], CaH 6 [85] и H 3 S [129].
 Поскольку критические температуры сверхпроводимости полиморфов высокого давления щелочных и щелочных металлов очень низки, неожиданное открытие в Si поднимает вопросы о реальной структуре сверхпроводящих фаз и низкотемпературных структурах сложных фаз, обсуждавшихся выше.
Поскольку критические температуры сверхпроводимости полиморфов высокого давления щелочных и щелочных металлов очень низки, неожиданное открытие в Si поднимает вопросы о реальной структуре сверхпроводящих фаз и низкотемпературных структурах сложных фаз, обсуждавшихся выше. При температуре окружающей среды [133] ОЦК Ba (Ba-I) трансформируется в гексагональную плотноупакованную (ГПУ) структуру (ГПУ, Ba-II) при 6 ГПа. Дальнейшее сжатие до 12 ГПа приводит к несоизмеримой (IC) самоорганизующейся структуре (Ba-IV) [132, 133], аналогичной Rb-IV. Сверхпроводимость с Тл c ~5 К была обнаружена выше 14 ГПа [134]. Наблюдается ли сверхпроводимость, связанная со сложной структурой гость-хозяин, при комнатной температуре? Для исследования температурного эффекта структурные превращения Ва были повторно исследованы при низкой температуре и высоком давлении [135]. Результаты суммированы на фазовой диаграмме, показанной на рис. 26а. В одном эксперименте Ba сжимали при комнатной температуре до 9ГПа. Было воспроизведено известное превращение ОЦК → ГПУ при 7 ГПа. Затем образец охлаждали до 9 К и дополнительно сжимали. Наблюдался структурный фазовый переход
Было воспроизведено известное превращение ОЦК → ГПУ при 7 ГПа. Затем образец охлаждали до 9 К и дополнительно сжимали. Наблюдался структурный фазовый переход
Рисунок 25.
Открыть в новой вкладкеСкачать слайд
(а) Дифрактограммы Si, измеренные в среде, передающей давление Не, при 80 К. (б) Резкий объемный коллапс при 17 ГПа ( адаптировано из Tse и др. [50]).
Рис. 26.
Открыть в новой вкладкеСкачать слайд
(а) Фазовая диаграмма давление-температура Ba. (b) Низкотемпературная орторомбическая структура Ba (адаптировано из Desgreniers и др. [135]).
при 14 ГПа. Эта фаза не была сложной фазой IC. Новая фаза была стабильна до 30 ГПа, где она трансформировалась в Ba-V со структурой ГПУ. При нагреве при 18 ГПа новая фаза трансформировалась в IC Ba-IV при 130 К. Превращение не было обратимым при охлаждении. В другом пути P – T Ba-I сжимался при комнатной температуре непосредственно в Ba-IV. Охлаждение образца при 20 и 30 ГПа не привело к восстановлению новой фазы. Очевидно, что новая фаза была метастабильной, так как ее возникновение зависело от P – T путь. Было обнаружено, что эта новая фаза (Ba-VI) является ромбической, а ее структура очень похожа на структуру предшественника ГПУ Ba-II (рис. 26b). Преобразование Ba-II в IC Ba-IV связано со значительным смещением и расположением атомов. Для преодоления энергетического барьера требовалась дополнительная энергия. При низкой температуре тепловой энергии было недостаточно для преодоления барьера, и атомы Ва выбрали путь с наименьшей энергией и трансформировались в искаженную гексагональную структуру. Было предсказано, что новая фаза Ba-VI будет сверхпроводником с T c 3,6 К при 16,2 ГПа [135]. Недавний эксперимент подтвердил предсказание, следуя тому же низкотемпературному пути сжатия P – T . Было обнаружено, что образец является сверхпроводником с Тл c 3,5 К при 16,5 ГПа [136], что в замечательном согласии с теорией.
Очевидно, что новая фаза была метастабильной, так как ее возникновение зависело от P – T путь. Было обнаружено, что эта новая фаза (Ba-VI) является ромбической, а ее структура очень похожа на структуру предшественника ГПУ Ba-II (рис. 26b). Преобразование Ba-II в IC Ba-IV связано со значительным смещением и расположением атомов. Для преодоления энергетического барьера требовалась дополнительная энергия. При низкой температуре тепловой энергии было недостаточно для преодоления барьера, и атомы Ва выбрали путь с наименьшей энергией и трансформировались в искаженную гексагональную структуру. Было предсказано, что новая фаза Ba-VI будет сверхпроводником с T c 3,6 К при 16,2 ГПа [135]. Недавний эксперимент подтвердил предсказание, следуя тому же низкотемпературному пути сжатия P – T . Было обнаружено, что образец является сверхпроводником с Тл c 3,5 К при 16,5 ГПа [136], что в замечательном согласии с теорией. Для сравнения, когда Ba сжимается при комнатной температуре, а затем охлаждается, он сохраняет структуру IC Ba-IV, которая также оказывается сверхпроводящей с немного более низким T c 1,5 К при 15 ГПа [134]. Как указывалось выше, понижение T c , вероятно, связано с тем, что переход в комплекс IC способствует открытию щели в части зоны Бриллюэна, способствуя снижению полной энергии системы, но не настолько стать изолятором.
Для сравнения, когда Ba сжимается при комнатной температуре, а затем охлаждается, он сохраняет структуру IC Ba-IV, которая также оказывается сверхпроводящей с немного более низким T c 1,5 К при 15 ГПа [134]. Как указывалось выше, понижение T c , вероятно, связано с тем, что переход в комплекс IC способствует открытию щели в части зоны Бриллюэна, способствуя снижению полной энергии системы, но не настолько стать изолятором.
Необычный случай барьера кинетической энергии обнаружен в недавно опубликованном сверхпроводящем плотном H 2 S [9]. Помимо предполагаемого загрязнения элементарной серой, связанной с разложением, оба наблюдаемых T c и in situ дифрактограмма [107] хорошо согласуется с предсказанным H 3 S [108]. В настоящее время принято считать, что H 3 S является сверхпроводящей фазой. Однако остается несколько проблем. Отмечено, что сверхпроводимость наблюдается только при сжатии H 2 S при низкой температуре по определенному пути P – T [107]. Когда H 2 S сжимался по разным термодинамическим путям, сообщалось о разных картинах дифракции рентгеновских лучей даже при одинаковых условиях давление-температура [137,138]. Дифрактограмма H 3 S, синтезированный непосредственно из стехиометрической смеси H 2 и S, также показал два слабых пика [139], аналогичные дифрактограмме in situ [107], которая была отнесена к примесям S. Однако, если H 2 S был разложен на H 3 S и S, соотношение интенсивностей двух видов сильно не соответствовало измеренной картине рентгеновской дифракции (XRD) [129]. Правдоподобным объяснением является то, что слабые отражения на рентгенограммах могли не быть примесью серы. Возможно, сверхпроводящая фаза могла быть метастабильным продуктом.
Когда H 2 S сжимался по разным термодинамическим путям, сообщалось о разных картинах дифракции рентгеновских лучей даже при одинаковых условиях давление-температура [137,138]. Дифрактограмма H 3 S, синтезированный непосредственно из стехиометрической смеси H 2 и S, также показал два слабых пика [139], аналогичные дифрактограмме in situ [107], которая была отнесена к примесям S. Однако, если H 2 S был разложен на H 3 S и S, соотношение интенсивностей двух видов сильно не соответствовало измеренной картине рентгеновской дифракции (XRD) [129]. Правдоподобным объяснением является то, что слабые отражения на рентгенограммах могли не быть примесью серы. Возможно, сверхпроводящая фаза могла быть метастабильным продуктом.
Рисунок 27.
Открыть в новой вкладкеСкачать слайд
Кристаллические структуры H 2 S, полученные в результате моделирования метадинамики при различных давлениях и температурах, начиная со структуры Pmc 2 1 . Большие и маленькие сферы представляют собой атомы S и H соответственно. Элементарные ячейки отмечены черными прямоугольниками (из Majumdar и др. [142]).
Большие и маленькие сферы представляют собой атомы S и H соответственно. Элементарные ячейки отмечены черными прямоугольниками (из Majumdar и др. [142]).
Рисунок 28.
Открыть в новой вкладкеСкачать слайд
Сравнение смоделированной рентгенограммы модулированной структуры 1:3 с экспериментальными дифрактограммами высокого давления H 2 S при 200 ГПа (адаптировано из Majumdar et al. [141]).
Для изучения влияния температуры на сжатие H 2 S были выполнены метадинамические расчеты [140] [141,142]. В эксперименте H 2 S сначала сжимали при 200 К, затем охлаждали и дополнительно сжимали до 150 ГПа. Сверхпроводимость наблюдалась при нагревании. Расчеты начались со структурной модели, которая, по прогнозам, будет стабильной при 80 ГПа, а расчетная дифракционная картина хорошо согласуется с экспериментом [143]. Моделирование проводилось при 80, 200 и 300 К. Метастабильные структуры, полученные при 80, 150 и 190 ГПа показаны на рис. 27. Существуют явные различия в структурных мотивах при трех разных температурах. При 200 ГПа и 300 К H 2 S разложился, и трехмерный каркас был построен исключительно из связанных атомов S, что свидетельствует о начале фазовой сегрегации. При 80 К и 80 ГПа моделирование метадинамики показало, что H 2 S самоионизируется в (SH) – (H 3 S) + с SH, образующими зигзагообразные цепочки, и атомами S, расположенными в искаженной ОЦК. узлы решетки, кстати, аналогичные положениям атомов S в предсказанном H 3 S структура [108]. Однако эта структура имеет пространственную группу Pc . Молекулярно-динамические расчеты постоянного объема и постоянной температуры ( NVT ) и постоянного давления и постоянной температуры ( NPT ) были выполнены на модели суперячейки, построенной с S, помещенным в идеализированные позиции ОЦК, и положениями атомов H, взятыми из Pc . структура. В моделировании NVT атомы S колебались вокруг ОЦК-позиций, но атомы H подвергались быстрой диффузии и обмену между SH – и H 3 S + части.
27. Существуют явные различия в структурных мотивах при трех разных температурах. При 200 ГПа и 300 К H 2 S разложился, и трехмерный каркас был построен исключительно из связанных атомов S, что свидетельствует о начале фазовой сегрегации. При 80 К и 80 ГПа моделирование метадинамики показало, что H 2 S самоионизируется в (SH) – (H 3 S) + с SH, образующими зигзагообразные цепочки, и атомами S, расположенными в искаженной ОЦК. узлы решетки, кстати, аналогичные положениям атомов S в предсказанном H 3 S структура [108]. Однако эта структура имеет пространственную группу Pc . Молекулярно-динамические расчеты постоянного объема и постоянной температуры ( NVT ) и постоянного давления и постоянной температуры ( NPT ) были выполнены на модели суперячейки, построенной с S, помещенным в идеализированные позиции ОЦК, и положениями атомов H, взятыми из Pc . структура. В моделировании NVT атомы S колебались вокруг ОЦК-позиций, но атомы H подвергались быстрой диффузии и обмену между SH – и H 3 S + части. Моделирование переменной ячейки NPT выявило деформацию ОЦК-решетки [141]. Примечательно, что часть суперячейки была искажена тетрагонально, а остальная часть оставалась кубической. Равновесная структура представляла собой соизмеримую модуляцию тетрагональных и кубических областей, чередующихся в соотношении 1:3 (рис. 28). Между прочим, рассчитанная рентгенограмма модулированной структуры 1:3 хорошо согласуется с экспериментом (рис. 28). В частности, два слабых пика Брэгга, ранее отнесенные к примесям серы, были воспроизведены при правильных углах дифракции и интенсивности. В настоящее время невозможно рассчитать электрон-фононную связь флюктуационной и модулированной системы на основе расчетов электронной структуры в соответствии с первыми принципами. Порядковая оценка T c модулированной структуры можно получить из температуры Дебая (Θ D ), полученной из теоретической колебательной плотности состояний и с использованием уравнения Макмиллана [92].
Моделирование переменной ячейки NPT выявило деформацию ОЦК-решетки [141]. Примечательно, что часть суперячейки была искажена тетрагонально, а остальная часть оставалась кубической. Равновесная структура представляла собой соизмеримую модуляцию тетрагональных и кубических областей, чередующихся в соотношении 1:3 (рис. 28). Между прочим, рассчитанная рентгенограмма модулированной структуры 1:3 хорошо согласуется с экспериментом (рис. 28). В частности, два слабых пика Брэгга, ранее отнесенные к примесям серы, были воспроизведены при правильных углах дифракции и интенсивности. В настоящее время невозможно рассчитать электрон-фононную связь флюктуационной и модулированной системы на основе расчетов электронной структуры в соответствии с первыми принципами. Порядковая оценка T c модулированной структуры можно получить из температуры Дебая (Θ D ), полученной из теоретической колебательной плотности состояний и с использованием уравнения Макмиллана [92]. Принимая λ между 1,0 и 3,0, что находится в пределах диапазона, рассчитанного для H 3 S, T c оценивается как 107–221 K. Эти значения сопоставимы с экспериментальными значениями [9]. Дополнительные расчеты, начиная с кристаллической фазы низкого давления, показывают, что переход к структуре, модулированной высоким давлением, является результатом фононной нестабильности около 150 ГПа [142]. Кроме того, рассчитанное T c структуры низкого давления хорошо согласуется с экспериментальной «фазой низкого давления». Метадинамические расчеты установили жизнеспособную и непротиворечивую связь эволюции кристаллической молекулярной фазы низкого давления со структурами высокого давления и объяснили появление и развитие сверхпроводимости [142]. Нет необходимости прибегать к 90 595 специальным предположениям об экзотических промежуточных фазах «Магнели» [144], в которых необходимо постоянно удалять атомы S из образца, чтобы в конечном итоге превратиться в H 3 S фаза.
Принимая λ между 1,0 и 3,0, что находится в пределах диапазона, рассчитанного для H 3 S, T c оценивается как 107–221 K. Эти значения сопоставимы с экспериментальными значениями [9]. Дополнительные расчеты, начиная с кристаллической фазы низкого давления, показывают, что переход к структуре, модулированной высоким давлением, является результатом фононной нестабильности около 150 ГПа [142]. Кроме того, рассчитанное T c структуры низкого давления хорошо согласуется с экспериментальной «фазой низкого давления». Метадинамические расчеты установили жизнеспособную и непротиворечивую связь эволюции кристаллической молекулярной фазы низкого давления со структурами высокого давления и объяснили появление и развитие сверхпроводимости [142]. Нет необходимости прибегать к 90 595 специальным предположениям об экзотических промежуточных фазах «Магнели» [144], в которых необходимо постоянно удалять атомы S из образца, чтобы в конечном итоге превратиться в H 3 S фаза. Рассмотрение конечного температурного эффекта с помощью обычных расчетов молекулярной динамики и метадинамики ясно показывает, что полученные структуры зависят от температуры и отличаются от структур, предсказанных на основе предсказаний структуры полной энергии (выполненных при 0 K). Я признаю, что механическая работа может компенсировать прочность связи S–H в 1,6 эВ при 2,0 эВ. Однако следует также учитывать энергию, необходимую для преодоления активационного барьера при разрыве связи H–S и существенной перегруппировке атомов в новой структуре. Поскольку сжатие производилось при низкой температуре и предполагаемый H 3 В структуре S отсутствуют связи S–S, для перегруппировки атомов требуется дополнительная энергия. Вероятно, этому процессу препятствует кинетика.
Рассмотрение конечного температурного эффекта с помощью обычных расчетов молекулярной динамики и метадинамики ясно показывает, что полученные структуры зависят от температуры и отличаются от структур, предсказанных на основе предсказаний структуры полной энергии (выполненных при 0 K). Я признаю, что механическая работа может компенсировать прочность связи S–H в 1,6 эВ при 2,0 эВ. Однако следует также учитывать энергию, необходимую для преодоления активационного барьера при разрыве связи H–S и существенной перегруппировке атомов в новой структуре. Поскольку сжатие производилось при низкой температуре и предполагаемый H 3 В структуре S отсутствуют связи S–S, для перегруппировки атомов требуется дополнительная энергия. Вероятно, этому процессу препятствует кинетика.
 Недавнее исследование также показало, что вода может реагировать с кремнеземом при очень мягких условиях температуры и давления [147]. Вода образовалась и попала в полости, созданные разложившимся SiO 2 очень кислый с очень высокой концентрацией H 3 O + . Таким образом, ожидается, что химический состав воды будет сильно отличаться от такового в нормальных условиях. Также было обнаружено, что часто используемые структурные правила топологического упорядочения в оксидных твердых телах и стеклах, основанные на объемной доле кислорода [148], больше не применимы при высоком давлении [149]. Непрерывное изменение электронной структуры атомов кислорода под давлением влияет на физический размер атома, и предположение о постоянном отношении ионных радиусов, основанное на информации при низком давлении, неверно.
Недавнее исследование также показало, что вода может реагировать с кремнеземом при очень мягких условиях температуры и давления [147]. Вода образовалась и попала в полости, созданные разложившимся SiO 2 очень кислый с очень высокой концентрацией H 3 O + . Таким образом, ожидается, что химический состав воды будет сильно отличаться от такового в нормальных условиях. Также было обнаружено, что часто используемые структурные правила топологического упорядочения в оксидных твердых телах и стеклах, основанные на объемной доле кислорода [148], больше не применимы при высоком давлении [149]. Непрерывное изменение электронной структуры атомов кислорода под давлением влияет на физический размер атома, и предположение о постоянном отношении ионных радиусов, основанное на информации при низком давлении, неверно. Представленная здесь орбитальная концепция очень эффективна. Например, в отличие от элементов второго ряда, элементы первого ряда с σ-связью и их соединения достаточно устойчивы к давлению. Причина в том, что у этих атомов нет доступных низколежащих орбиталей для гибридизации, чтобы изменить характер химической связи и локальную геометрию. Например, воду можно сжать до 100 ГПа без изменения тетраэдрического кислородного окружения, даже если произошло несколько структурных переходов. При высоком давлении локальные структуры бора в оксидном стекле очень прочны. Координационное число B–O (КЧ) первоначально изменилось с 3 до 4 при умеренном давлении из-за изменения с sp 2 до sp 3 , но дальнейшего изменения не наблюдалось вплоть до мегабарного давления [150]. Расширение и усовершенствование химии и принципов связывания в соответствии с этим направлением мысли для объяснения новых явлений, наблюдаемых при высоком давлении, будет иметь неоценимое значение для исследования.
Причина в том, что у этих атомов нет доступных низколежащих орбиталей для гибридизации, чтобы изменить характер химической связи и локальную геометрию. Например, воду можно сжать до 100 ГПа без изменения тетраэдрического кислородного окружения, даже если произошло несколько структурных переходов. При высоком давлении локальные структуры бора в оксидном стекле очень прочны. Координационное число B–O (КЧ) первоначально изменилось с 3 до 4 при умеренном давлении из-за изменения с sp 2 до sp 3 , но дальнейшего изменения не наблюдалось вплоть до мегабарного давления [150]. Расширение и усовершенствование химии и принципов связывания в соответствии с этим направлением мысли для объяснения новых явлений, наблюдаемых при высоком давлении, будет иметь неоценимое значение для исследования.
Заявление о конфликте интересов. Не объявлено.
1.
Суаньяр
E
,
Макмиллан
ПФ
.
Введение в ячейки с алмазными наковальнями и методы загрузки
. В:
Katrusiak
A
McMillan
P
(ред.).
Кристаллография высокого давления, Научная серия НАТО II
. Том. 140.
Дордрехт
:
Kluwer Academic Publishers
,
2004
,
81
–40028 100
.
2.
Брейер
А
.
Методы спектроскопии in situ при высоком давлении
. Том. 7, 1-е изд.
Том. 7, 1-е изд.
Амстердам
:
Elsevier
,
2015
.
3.
День любви
Дж
(ред.).
Физика высоких давлений
.
Бока Ратон
:
CRC Press
,
2016
.
4.
Коно
Y
,
Sanloup
C
(ред.).
Магма под давлением
.
Амстердам
:
Elsevier
,
2018
.
5.
Элдик
Р
,
Клэрнер
F-G
(ред.).
Химия высокого давления: синтетические, механические и сверхкритические применения
.
Нью-Йорк
:
Wiley
,
2008
.
6.
Цзоу
B
Ван
B
Ли
S
и другие.
Применение синхротронного излучения в исследованиях высокого давления
. В:
Чжан
X
(ред.).
Применение синхротронного излучения
.
Сингапур
:
World Scientific
,
2018
.
7.
МакМахон
МИ
,
Нельмес
Нью-Джерси
.
Структуры при высоком давлении и фазовые превращения в простых металлах
.
Chem Soc Rev
2006
;
35
:
943
–
63
.
8.
Дроздов
АП
Еремец
МИ
,
Троян
ИА
и др.
Обычная сверхпроводимость при 203 Кельвина при высоких давлениях в системе гидрида серы
.
Природа
2015
;
525
:
437
–
91
.
9.
Сомаязулу
М
Ахарт
М
,
Мишра
АК
и др.
Доказательства сверхпроводимости выше 260 К в супергидриде лантана при мегабарном давлении
.
Phys Rev Lett
2019
;
122
:
027001
.
10.
Vos
WL
Палец
LW
,
Hemley
R
и др.
Соединение Ван-дер-Ваальса высокого давления в твердых азотно-гелиевых смесях
.
Природа
1992
;
358
:
46
–
8
.
11.
Лубейр
P
Жан-Луи
M
,
ЛеТуллек
Р
.
Измерения бинарной фазовой диаграммы He-Ne при высоком давлении при 296 K: свидетельство стабильности стехиометрического Ne(He) 2 в твердом состоянии
.
Phys Rev Lett
1993
;
70
:
178
–
81
.
12.
Лубейр
P
ЛеТуллек
R
,
Пинсо
JP
.
Сжатие Ar(H 2 ) 2 до 175 ГПа: новый путь диссоциации молекулярного водорода?
Phys Rev Lett
1994
;
72
:
1360
–
3
.
13.
Сомаязулу
M
Палец
LW
Hemley
RJ
и другие.
Новые соединения высокого давления в метановодородных смесях
.
Наука
1996
;
271
:
1400
–
2
.
14.
Сомаязулу
M
Дера
P
,
Гончаров
АФ
и др.
Связывание под давлением и образование соединений в ксенон-водородных твердых веществах
.
Nat Chem
2010
;
2
:
50
–
3
.
15.
Jephcoat
AP
Amboage
M
,
Клеппе
АК
.
Структурные и колебательные свойства конденсированных фаз в молекулярных бинарных системах ксенона: He-Xe, H 2 -Xe
.
J Phys Conf Ser
2010
;
215
:
012016
.
16.
Клеппе
АК
Амбоаж
М
,
Джефкоут
AP
.
Новое соединение Ван-дер-Ваальса высокого давления Kr(H 2 ) 4 обнаружен в двойной системе криптон-водород
.
Научный представитель
2014
;
4
:
4989
.
17.
Сполдинг
ДК
,
Weck
G
,
Loubeyre
P
и др.
Химия под давлением в азотно-водородной структуре хозяин-гость
.
Нац Коммуна
2014
;
5
:
5739
.
18.
Ланиэль
Д
Светлик
В
,
Weck
G
и др.
Химические реакции под давлением в соединении N 2 (H 2 ) 2 : от веществ N 2 и H 2 к аммиаку и обратно к гидразину
.
Phys Chem Chem Phys
2018
;
20
:
4050
–
7
.
19.
Шинозаки
А
Каги
Н
,
Ногучи
N
и др.
Образование SiH 4 и H 2 O при растворении кварца во флюиде H 2 при высоком давлении и температуре
.
Ам Минерал
2014
;
99
:
1265
–
9
.
20.
Атоу
T
Хасэгава
N
,
Parker
LJ
и др.
Необычное химическое поведение калия под давлением: соединения калия и серебра
.
J Am Chem Soc
1996
;
118
:
12104
–
8
.
21.
Дегренье
S
Tse
JS
,
Мацуока
T
и др.
Смешивание несмешиваемых веществ: неожиданное образование сплавов Li-Cs при низком давлении
.
Sci Adv
2015
;
1
:
e150066
.
22.
Грочала
W
Хоффманн
R
,
Фэн
Дж
и др.
Химическое воображение на работе в очень труднодоступных местах
.
Angew Chem Int Ed
2007
;
46
:
3620
–
42
.
23.
Зурек
E
,
Би
Т
.
Высокотемпературная сверхпроводимость в полигидридах щелочных и редкоземельных металлов при высоком давлении: теоретическая перспектива
.
J Chem Phys
2019
;
150
:
050901
.
24.
Уолш
JPS
,
Фридман
DE
.
Синтез под высоким давлением: новый рубеж в поиске интерметаллидов нового поколения
.
Acc Chem Res
2018
;
51
:
1315
–
23
.
25.
Хоффманн
R
.
Твердые тела и поверхности. Взгляд химика на сцепление в протяженных структурах
.
Вихем
:
ВЧ
,
1988
.
26.
Бердетт
Дж.К.
.
Химическая связь в твердых телах
.
Оксфорд
:
Издательство Оксфордского университета
,
1995
.
27.
Шерри
ER
.
Периодическая таблица: очень краткое введение
. 2-е изд.
Оксфорд
:
Издательство Оксфордского университета
,
2019
.
28.
Фортов
ВЭ
,
Минцев
ВБ
.
Экстремальные состояния вещества на Земле и в космосе: есть ли химия за мегабаром?
Русс Хим Рев
2013
;
82
:
597
–
615
.
29.
Це
JS
,
Болдыра
Е
.
Топология электронной плотности кристаллических твердых тел при высоком давлении
. В:
Gatti
C
Macchi
P
(ред.).
Современный анализ плотности заряда
.
Амстердам
:
Springer
,
2012
,
573
–
623
8.
30.
Штернхаймер
R
.
О сжимаемости металлического цезия
.
Phys Rev
1950
;
78
:
235
–
43
.
31.
Штер
J
.
Спектроскопия NEXAFS
.
Амстердам
:
Springer
,
1992
.
32.
Се
Дж
Чен
СП
,
Tse
JS
и др.
Фононные нестабильности в ОЦК-ГЦК высоких давлениях и изоструктурные ГЦК-ГЦК фазовые переходы Cs
.
Phys Rev B
2000
;
62
:
3624
–
9
.
33.
МакМахон
МИ
,
Нельмес
РДЖ
.
Сложная кристаллическая структура цезия-III
.
Phys Rev Lett
2001
;
87
:
255502
.
34.
Такемура
К
Миномура
S
,
Симомура
О
.
Рентгеноструктурное исследование электронных переходов в цезии под высоким давлением
.
Phys Rev Lett
1982
;
49
:
1772
–
5
.
35.
Такемура
К
Кристенсен
СВ
,
Новиков
ДЛ
и др.
Фазовая стабильность сильно сжатого цезия
.
Phys Rev B
2000
;
61
:
14399
–
404
.
36.
Це
JS
.
Кристаллография отдельных твердых веществ высокого давления
.
Zeitschrift für Kristallographie
2005
;
220
:
521
–
30
.
37.
Краситель
JL
.
Электриды: ионные соли с электронами в качестве анионов
.
Наука
1990
;
247
:
663
–
8
.
38.
фон Шнеринг
HG
,
Неспер
Р
.
Как природа приспосабливает химические структуры к искривленным поверхностям
.
Angew Chem Int Ed
1987
;
26
:
1059
–
80
.
39.
Мяо
М
,
Хоффманн
R
.
Электриды высокого давления: прогнозирующая химическая и физическая теория
.
Акк Хим Рез
2014
;
47
:
1311
–
7
.
40.
Мяо
М
,
Хоффманн
R
.
Электриды высокого давления: химическая природа межузельных квазиатомов
.
J Am Chem Soc
2015
;
137
:
3631
–
7
.
41.
Мяо
M
Хиоффман
R
,
Botana
J
и др.
Квазимолекулы в сжатом литии
.
Angew Chem Int Ed
2017
;
56
:
972
–
5
.
42.
Шварц
U
Такемура
К
,
Hanfland
M
и др.
Кристаллическая структура цезия-V
.
Phys Rev Lett
1998
;
81
:
2711
–
4
.
43.
Мацуока
Т
,
Симидзу
К
.
Прямое наблюдение индуцированного давлением перехода металла в полупроводник в литии
.
Природа
2009
;
458
:
186
–
9
.
44.
Ма
Ю
Еремец
М
,
Оганов
АР
и др.
Натрий прозрачный плотный
.
Природа
2009
;
458
:
182
–
5
.
45.
Такемура
К
,
Сяссен
К
.
Уравнение состояния рубидия при высоком давлении
.
Твердотельный Общий
1982
;
44
:
1161
–
4
.
46.
Тупс
H
Такемура
K
,
Сяссен
К
.
Межзонное оптическое поглощение и электронный s → d переход в Rb и Cs при высоких давлениях
.
Phys Rev Lett
1982
;
49
:
1776
–
9
.
47.
Шварц
U
,
Гжечник
А
,
Сяссен
К
и др.
Рубидий-IV: фаза высокого давления со сложной кристаллической структурой
.
Phys Rev Lett
1999
;
83
:
4085
–
8
.
48.
МакМахон
МИ
Рехи
С
,
Нельмес
РДЖ
.
Несоизмеримость в зависимости от давления в Rb-IV
.
Phys Rev Lett
2001
;
30
:
055501
.
49.
Цзун
С
.
Упаковка, покрытие и облицовка двухмерных пространств
.
Экспо Математика
2014
;
32
:
297
–
364
.
50.
Tse
JS
Hanfland
M
,
Flacau
R
и др.
Изменения электронной структуры и электронной топологии под давлением при прямом ГЦК → ВГ-превращении кремния
.
J Phys Chem C
2014
;
118
:
1161
–
6
.
51.
Саката
М
,
Таката
М
.
Принцип метода максимальной энтропии
.
Высокое разрешение печати
1996
;
14
:
327
–
33
.
52.
Li
R
Liu
J
,
Бай
Л
и др.
Изменение распределения электронной плотности в α-Ge вблизи перехода α-β под давлением
.
Appl Phys Letter
2015
;
107
:
072109
.
53.
Нитон
JB
Эшкрофт
СЗ
.
Сопряжение из плотного лития
.
Природа
1999
;
400
:
141
–
4
.
54.
Руссо
R
Уэхара
K
,
Клуг
ДД
и др.
Стабильность фаз и нарушение симметрии элементарного лития до 140 ГПа
.
Хим. Физ. Хим.
2005
;
6
:
1703
–
6
.
55.
Полинг
L
.
Принципы определения строения барических форм металлов: строения цезия (IV) и цезия (V)
.
Proc Natl Acad Sci USA
1989
;
86
:
1431
–
3
.
56.
Каузларич
СМ
.
Энциклопедия неорганической и бионеорганической химии
.
Нью-Йорк
:
John Wiley & Sons
,
2006
.
57.
Руссо
Р
,
Це
JS
.
Рационализация структур бинарных сплавов
.
Prog Theoret Phys Suppl
2000
;
138
:
47
–
59
.
58.
Хьюм-Розери
Вт
.
Теория атома для студентов-металлургов
.
Лондон
:
Институт металлов
,
1969
.
59.
Tse
JS
Frapper
G
,
Кер
А
и др.
Фазовая стабильность и электронная структура интерметаллидов K-Ag при высоком давлении
.
Phys Rev Lett
1999
;
82
:
4472
–
5
.
60.
Чжан
X
,
Зунгер
А
.
Изменение реакционной способности и появление ионно-металлоупорядоченных структур в Li-Cs при высоких давлениях
.
Phys Rev Lett
2010
;
104
:
245501
.
61.
Йонг
В
Лекин
К
,
Bauer
RPC
и др.
Блинчики под давлением: тематическое исследование изоструктурных димеров дитиа- и диселенадиазолильных радикалов
.
Инорг Хим
2019
;
58
:
3550
–
7
.
62.
Лекин
К
Лейтч
АА
,
Ассуд
А
и др.
Гетероциклические цвиттер-ионы с бензохиноновым мостиком в качестве строительных блоков для молекулярных полупроводников и металлов
.
Инорг Хим
2018
;
16
:
4757
–
70
.
63.
Почтальон
А
,
Leitch
AA
,
Yong
W
и др.
Силовая упаковка: металлизация органического полупроводника
.
J Am Chem Soc
2017
;
139
:
2180
–
3
.
64.
Почтальон
А
,
Вонг
ДЖВЛ
,
Зимний
SM
и др.
Тонкая настройка характеристик мультиорбитальных радикальных проводников с помощью эффектов замещения
.
J Am Chem Soc
2017
;
139
:
1625
–
35
.
65.
Лекин
К
Огата
К
Маклин
А
и другие.
Толкание T c до 27,5 К в тяжелом атоме радикального ферромагнетика
.
Хим.коммун
2017
;
52
:
13877
–
80
.
66.
Тянь
D
Зима
SM
,
Почтальон
A
и др.
Металлическое состояние в нейтрально-радикальных проводниках: размерность, давление и множественные орбитальные эффекты
.
J Am Chem Soc
2015
;
137
:
14136
–
48
.
67.
Зима
SM
Почтальон
А
,
Окли
РТ
и др.
Электронная и магнитная структура нейтрального радикала FBBO
.
Phys Rev B
2014
;
89
:
214403
.
68.
Лекин
К
Фан
Н
,
Зимний
SM
и др.
Взаимное превращение бисдитиазолильных радикалов и димеров под действием тепла, давления и света
.
J Am Chem Soc
2014
;
136
:
8050
–
62
.
69.
Вонг
JW
Почтальон
А
,
Лекин
К
и др.
Фазовые переходы под давлением и металлизация нейтрально-радикального проводника
.
J Am Chem Soc
2014
;
136
:
1070
–
81
.
70.
Лекин
К
Лейтч
АА
,
Tse
JS
и др.
Индуцированная давлением структурная дихотомия в изоструктурных димерах бис-1,2,3-тиаселеназолильных радикалов
.
Рост кристаллов Des
2012
;
12
:
4676
–
86
.
71.
Почтальон
A
Зима
SM
,
Xin
Y
и др.
Преодоление барьера изолятор-металл с помощью тиазильного радикального проводника
.
J Am Chem Soc
2012
;
134
:
9886
–
9
.
72.
Лейтч
АА
Лекин
К
,
Зимний
SM
и др.
От магнитов к металлам: реакция тетрагональных бисдиселеназолильных радикалов на давление
.
J Am Chem Soc
2011
;
133
:
6051
–
60
.
73.
Лекин
К
Зимний
СМ
,
Дауни
LE
и др.
Гистерезисный спин-кроссовер между бисдитиазолильным радикалом и его гипервалентным σ-димером
.
J Am Chem Soc
2010
;
132
:
16212
–
24
.
74.
Tse
JS
Leitch
AA
,
Ю
Х
и др.
Металлизация димера гипервалентного радикала: молекулярная и зонная перспективы
.
J Am Chem Soc
2010
;
132
:
4876
–
86
.
75.
Мито
M
Коморида
Y
,
Цуруда
H
и др.
Ферромагнетики с тяжелыми атомами под давлением: структурные изменения и магнитный отклик
.
J Am Chem Soc
2009
;
131
:
16012
–
3
.
76.
Лейтч
АА
Ю
Х
,
Робертсон
CM
и др.
Изоструктурные димеры бис-1,2,3-тиаселеназолила
.
Инорг Хим
2009
;
48
:
9874
–
82
.
77.
Эшкрофт
СЗ
.
Металлический водород: высокотемпературный сверхпроводник?
Phys Rev Lett
1968
;
21
:
1748
–
9
.
78.
Оганов
АР
Стекло
CW
.
Предсказание кристаллической структуры с использованием эволюционных методов ab initio: принципы и приложения
.
J Chem Phys
2006
;
124
:
244704
.
79.
Ван
Y
Lv
J
Zhu
L
и другие.
CALYPSO: метод предсказания кристаллической структуры
.
Comput Phys Commun
2012
;
183
:
2063
–
70
.
80.
Оганов
АР
(ред.).
Современные методы прогнозирования кристаллической структуры
.
Wieheim
:
Wiley-VCH
,
2010
.
81.
Ван
Y
Ван
H
,
Tse
JS
и др.
Структурная морфология полиморфов гидридов стронция высокого давления
.
Phys Chem Chem Phys
2015
;
17
:
19379
–
85
.
82.
Хупер
J
Терпстра
T
,
Шамп
А
и др.
Состав прессованных полигидридов стронция
.
J Phys Chem C
2014
;
118
:
6433
–
47
.
83.
Парр
РГ
,
Ян
Вт
.
Теория функционала плотности атомов и молекул
.
Нью-Йорк
:
Oxford University Press
,
1989
.
84.
Плита
Ш
.
Структура и соединение
. В:
Электрохимия для материаловедения
.
Амстердам
:
Elsevier
,
2008
,
27
–
69
.
85.
Ван
H
Tse
JS
,
Танака
К
и др.
Сверхпроводящий содалитоподобный клатрат гидрида кальция при высоких давлениях
.
Proc Natl Acad Sci USA
2012
;
109
:
6463
–
6
.
86.
Wang
Z
Wang
H
Tse
JS
и другие.
Стабилизация H 3 + в кристаллической структуре высокого давления H n Cl (n = 2–7)
.
Химические науки
2015
;
6
:
522
–
6
.
87.
Ван
Н
Ли
Х
,
Гао
G
и др.
Сверхпроводники с высоким содержанием водорода при высоких давлениях
.
ПРОВОДА Comput Mol Sci
2018
;
8
:
e1330
.
88.
Шамп
А
,
Зурек
E
.
Сверхпроводимость в гидридах, легированных элементами главной группы, под давлением
.
Ноябрь Supercond Mater
2017
;
3
:
14
–
22
;
Bi
T
Zarifi
N
Terpstra
T
и др.
Поиски сверхпроводимости в гидридах высокого давления
. В:
Справочный модуль по химии, молекулярным наукам и химической инженерии
.
.
89.
Барони
S
де Жиронколи
S
,
Dal Corso
A
и др.
Фононы и связанные с ними свойства кристаллов из теории возмущений функционала плотности
.
Rev Mod Phys
2006
;
73
:
515
–
62
.
90.
Саврасов
СЮ
,
Саврасов
ДЯ
.
Электрон-фононные взаимодействия и связанные с ними физические свойства металлов из теории линейного отклика
.
Phys Rev B
1996
;
54
:
16487
–
501
.
91.
Яо
Y
Tse
JS
,
млн лет
Y
и др.
Сверхпроводимость в SiH высокого давления 4
.
EPL
2007
;
78
:
37003
.
92.
Макмиллан
WL
.
Температура перехода сильносвязанных сверхпроводников
.
Phys Rev
1968
;
167
:
331
–
44
.
93.
Tse
JS
Yao
Y
Танака
K
.
Новая сверхпроводимость в металлическом SnH 4 под высоким давлением
.
Phys Rev Lett
2007
;
98
:
117004
.
94.
Еремец
МИ
Троян
ИА
,
Медведев
ЮА
и др.
Сверхпроводимость материалов с преобладанием водорода: силан
.
Наука
2008
;
319
:
1506
–
9
.
95.
Стробель
Т
Гончаров
АФ
,
Seagle
CT
и др.
Исследование силана под высоким давлением до 150 ГПа
.
Phys Rev B
2011
;
83
:
144102
.
96.
Kim
DY
Scheicher
RH
,
Пикард
CJ
и др.
Прогноз образования сверхпроводящих кристаллов гидрида платины под давлением в присутствии молекулярного водорода
.
Phys Rev Lett
2011
;
107
:
117002
.
97.
Пикард
CJ
,
Потребности
RJ
.
Силановые фазы высокого давления
.
Phys Rev Lett
2006
;
97
:
045504
.
98.
Троян
I
Гаврилюк
А
Рюффер
Р
и другие.
Наблюдение сверхпроводимости в сероводороде по ядерному резонансному рассеянию
.
Наука
2016
;
351
:
1303
–
6
.
99.
Капитани
F
Ланжером
B
,
Брубах
JB
и др.
Спектроскопические доказательства новой энергетической шкалы сверхпроводимости в H 3 S
.
Nat Phys
2017
;
13
:
859
–
63
.
100.
Ли
Y
Хао
J
,
Лю
H
и др.
Стабилизированные давлением сверхпроводящие гидриды иттрия
.
Научный представитель
2015
;
5
:
09948
.
101.
Лю
Х
Наумов
II
,
Hoffmann
R
и др.
Потенциальные высокотемпературные c сверхпроводящие гидриды лантана и иттрия при высоком давлении
.
Proc Natl Acad Sci USA
2017
;
114
:
6990
–
5
.
102.
Пэн
F
Вс
Y
,
Пикард
CJ
и др.
Структуры клатратов водорода в гидридах редкоземельных элементов при высоких давлениях: возможный путь к комнатной температуре
.
Phys Rev Lett
2017
;
119
:
107001
.
103.
Элиашберг
ГМ
.
Взаимодействие электронов с колебаниями решетки в сверхпроводнике
.
Сов Физ ЖЭТФ
1960
;
11
:
696
–
702
.
104.
Карбот
JP
.
Свойства сверхпроводников с бозонным обменом
.
Rev Mod Phys
1990
;
62
:
1027
–
157
.
105.
Бергманн
G
,
Райнер
Д
.
Чувствительность температуры перехода к изменению α 2 F (ω)
.
Zeitschrift für Physik
1973
;
263
:
59
–
68
.
106.
Танака
К
Це
JS
,
Лю
Х
.
Механизмы электрон-фононного взаимодействия для металлов с высоким содержанием водорода при высоком давлении
.
Phys Rev B
2017
;
96
:
100502
.
107.
Эйнага
М
Саката
М
,
Исикава
T
и др.
Кристаллическая структура сверхпроводящей фазы гидрида серы
.
Nat Phys
2016
;
12
:
835
–
8
.
108.
Дуань
Д
Лю
Y
Тянь
F
и другие.
Металлизация под давлением плотная (H 2 S) 2 H 2 с высокотемпературной c сверхпроводимостью
.
Научный представитель
2014
;
4
:
6968
.
109.
Никол
ЭДЖ
,
Карбот
JP
.
Сравнение гидрида серы под давлением с обычными сверхпроводниками
.
Phys Rev B
2015
;
91
:
220507
.
110.
Шестигранник
ПБ
,
Дины
RC
.
Повторный анализ температуры перехода сильносвязанных сверхпроводников
.
Phys Rev B
1975
;
12
:
905
–
22
.
111.
Грочала
Ш
Конечный
Р
,
Хоффманн
R
.
Химия вибронных муфт. Часть 1. Как максимизировать константы вибронной связи в модели диабатического гармонического потенциала ?
Химическая физика
2001
;
265
:
153
–
63
.
112.
Грочала
Ш
,
Хоффманн
R
.
Химия вибронных муфт. Часть 2. Как максимизировать константу динамической диагональной вибронной связи для состояний T 1 в системах AB (A, B = H, Li, Na, K, Rb, Cs, F, Cl, Br или I)?
New J Chem
2001
;
25
:
108
–
15
.
113.
Грочала
W
Хоффманн
R
.
Химия вибронных муфт. 3. Как можно максимизировать внедиагональные константы динамической вибронной связи для состояний с межвалентным переносом заряда (IVCT) в системе ABA1 (A, B = щелочной металл, H, галоген)?
J Phys Chem A
2000
;
104
:
9740
–
9
.
114.
Грочала
W
Хоффманн
R
.
Химия вибронных муфт. Часть 4. Недиагональные вибронные константы связи в периодической таблице
.
Pol J Chem
2001
;
75
:
1603
–
59
.
115.
Grochala
W
Hoffmann
R
Edwards
PP
.
Химия вибронных муфт. Часть 5. Вибронная связь в молекулах и в твердых телах
.
Chem Eur J
2003
;
9
:
575
–
87
.
116.
Ян
HA
Кассир
E
.
Устойчивость многоатомных молекул в вырожденных электронных состояниях – I—орбитальное вырождение
.
Proc Royal Soc A
1937
;
161
:
220
–
35
.
117.
Екимов
ЭА
Сидоров
В.А.
Бауэр
ЭД
и другие.
Сверхпроводимость в алмазе
.
Природа
2004
;
428
:
542
–
5
.
118.
Тутунджу
ХМ
.
Сверхпроводимость в твердых телах с простыми элементами — компьютерное исследование легированного бором алмаза и фаз высокого давления Li и Si
.
J Phys Cond Matter
2005
;
17
:
S911
–
20
.
119.
и другие.
Изучение первых принципов электрон-фононного взаимодействия в дырочно- и электронно-легированных алмазах в приближении виртуального кристалла
.
Phys Rev B
2005
;
72
:
014306
.
120.
Baird
NC
Burdett
JK
.
Взаимодействие электростатических и орбитальных сил в управлении структурой легированных электронами сверхпроводников Nd 2-x Ce x CuO 4
.
Physica C
1990
;
168
:
637
–
46
.
121.
Держатель Bussmann
А
Кёлер
Дж
Саймон
А
и другие.
Путь к сверхпроводимости при комнатной температуре: управление различными каналами сопряжения в системах, состоящих из нескольких электронных компонентов
.
Конденсат
2017
;
2
:
24
.
122.
Саймон
А
Колер
Дж
.
Варианты химической связи и электрон-фононное взаимодействие
.
J Am Chem Soc
2002
;
124
:
10712
–
7
.
123.
Саймон
А
Колер
Дж
.
Механизмы образования пар с точки зрения физики и химии
.
Struct Bond
2003
;
114
:
103
–
41
.
124.
Саймон
А
.
Сверхпроводимость и химия
.
Angew Chem Int Ed Engl
1997
;
36
:
1788
–
806
.
125.
Саймон
А
.
Сверхпроводимость и периодическая таблица: от элементов к материалам
.
Phil Trans R Soc A
2015
;
373
:
20140192
.
126.
Саймон
A
Бекер
M
Хенн
RW
и другие.
Supraleitung in Seltenerdmetall-carbidhalogeniden des types Se 2 Х 2 С 2
.
Z Anorg Allg Chem
1996
;
622
:
123
–
37
.
127.
Саймон
А
Колер
Дж
.
Сценарий плоской полосы — крутой полосы и сверхпроводимость — случай кальция
.
Наука о твердом теле
2000
;
2
:
31
–
8
.
128.
Саймон
A
Кёлер
J
.
Сценарий «плоской/крутой полосы» в импульсном пространстве
.
J Supercond
2004
;
17
:
227
–
31
.
129.
Гордон
ЕЕ
Сян
H
и другие.
Структура и состав 200 К-сверхпроводящей фазы H 2 S при сверхвысоком давлении: перовскит (SH − )(H 3 S + )
.
Angew Chem Int Ed
2016
;
55
:
3682
–
4
.
130.
Пусто
ВД
Эстрин
Е
.
Фазовые переходы в твердых телах под высоким давлением
.
Бока-Ратон
:
CRC Press
,
2013
.
131.
Льюис
SP
Коэн
ML
.
Теоретическое исследование орторомбического кремния высокого давления
.
Физическая версия B
1993
;
48
:
144
–
7
.
132.
McMahon
MI
Дегтярева
O
Нельмес
RJ
.
Несоизмеримая кристаллическая структура типа Ba-IV в металлах V группы
.
Phys Rev Lett
2000
;
85
:
4896
–
9
.
133.
Nelmes
RJ
Lundegaard
I
и другие.
Чрезвычайно сложная кристаллическая структура с мезоскопическим рисунком в барии при высоком давлении
.
Нат Матер
2012
;
11
:
627
–
32
.
134.
Виттиг
J
Матиас
BT
.
Сверхпроводимость бария под давлением
.
Phys Rev Lett
1969
;
22
:
634
–
6
.
135.
Дегренье
S
Мацуока
T
и другие.
Фазовая диаграмма высокого давления – низкой температуры бария
.
Appl Phys Letter
2015
;
107
:
221908
.
136.
Jackson
DE
VanGennep
D
Vohra
YK
и другие.
Сверхпроводимость бария-VI, синтезированного методом сжатия при низких температурах
.
Phys Rev B
2017
;
96
:
184514
.
137.
и другие.
Продукты диссоциации и структуры H 2 S при сильном сжатии
.
Phys Rev B
2016
;
93
:
020301
.
138.
Гончаров
АФ
Лобанов
СС
Круглов
Я
и другие.
Сероводород при высоком давлении: изменение стехиометрии
.
Phys Rev B
2016
;
93
:
17410
.
139.
Гончаров
АФ
Лобанов
СС
Прокопенко
ВБ
и другие.
Стабильные фазы высокого давления в системе HS, определяемые химической реакцией водорода и серы
.
Phys Rev B
2017
;
95
:
140101
.
140.
Бардуччи
А
Бономи
М
Парринелло
М
.
Метадинамика
.
ПРОВОДА
2011
;
1
:
826
–
43
.
141.
Маджумдар
А
.
Модулированная структура, рассчитанная для сверхпроводящего сероводорода
.
Angew Chem Int Ed
2017
;
56
:
11390
–
3
.
142.
Маджумдар
А
.
Механизм структурного превращения в модулированную сверхпроводящую фазу сжатого сероводорода
.
Научный представитель
2019
;
9
:
5023
.
143.
и другие.
Металлизация и сверхпроводимость плотного сероводорода
.
J Chem Phys
2014
;
140
:
174712
.
144.
Акаши
R
Арита
R
и другие.
Возможные фазы Магнели и самосплавление в сверхпроводящем гидриде серы
.
Phys Rev Lett
2016
;
117
:
075503
.
145.
Яманака
С
.
Клатраты кремния и аналоги углерода: синтез высокого давления, структура и сверхпроводимость
.
Далтон Транс
2010
;
39
:
1901
–
15
.
146.
Галли
Г
.
Судьба диоксида углерода в богатых водой жидкостях в экстремальных условиях
.
Sci Adv
2016
;
2
:
.
147.
Футера
А
и другие.
Образование и свойства воды из кварца и водорода при высоком давлении и температуре
.
Earth Planetary Sci Lett
2017
;
461
:
54
–
60
.
148.
Zeidler
A
Лосось
SP
Skinner
LB
.
Упаковка и структурные превращения в жидких и аморфных оксидах от условий окружающей среды до экстремальных условий
.
Proc Natl Acad Sci USA
2014
;
111
:
10045
–
8
.
149.
.
Фракция упаковки кислорода и структура оксидных кремниевых и германиевых стекол
.
J Phys Chem B
2017
;
121
:
10726
–
32
.
150.
и другие.
Аморфный оксид бора при мегабарном давлении методом неупругого рассеяния рентгеновских лучей
.
Proc Natl Acad Sci USA
2018
;
115
:
5855
–
60
.


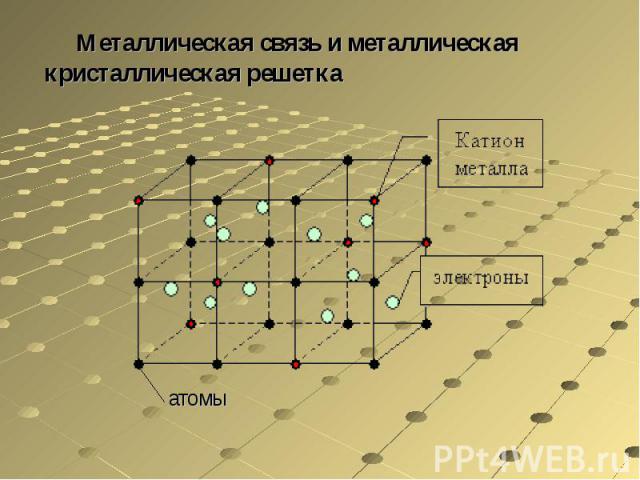 Самый лёгкий металл – литий с плотностью 0,533 г/см3
Самый лёгкий металл – литий с плотностью 0,533 г/см3 Наиболее тугоплавкий – вольфрам (3420°С)
Наиболее тугоплавкий – вольфрам (3420°С)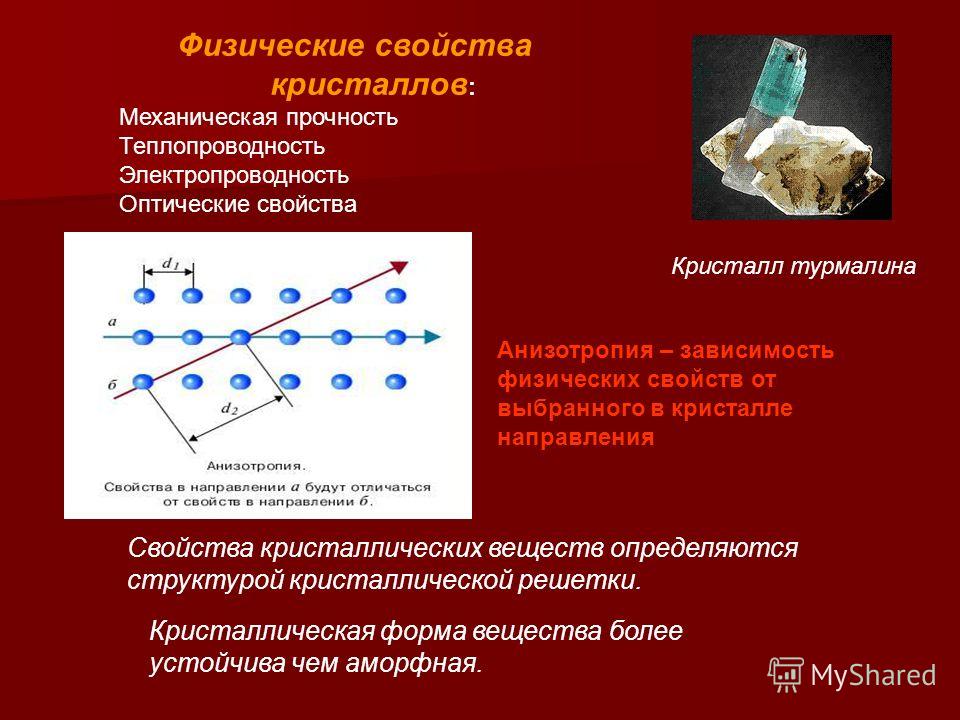 Минералы
обладают отличительными физическими свойствами, которые в большинстве случаев можно использовать для
определить принадлежность минерала. В этом курсе вы будете
разработать системный подход к использованию физических свойств минералов
как средства идентификации. Если вы будете следовать этому подходу, вы сможете
идентифицировать большинство распространенных минералов или, по крайней мере, иметь возможность сузить
возможности лишь немногим. Сначала мы обсудим каждый из
физические свойства, которые можно использовать, а затем разработать методический подход
к идентификации полезных ископаемых, используя эти физические свойства.
Среди свойств, которые мы обсудим, следующие: кристаллический габитус, спайность,
твердость, плотность, блеск, полоса, цвет, прочность, магнетизм и вкус.
Минералы
обладают отличительными физическими свойствами, которые в большинстве случаев можно использовать для
определить принадлежность минерала. В этом курсе вы будете
разработать системный подход к использованию физических свойств минералов
как средства идентификации. Если вы будете следовать этому подходу, вы сможете
идентифицировать большинство распространенных минералов или, по крайней мере, иметь возможность сузить
возможности лишь немногим. Сначала мы обсудим каждый из
физические свойства, которые можно использовать, а затем разработать методический подход
к идентификации полезных ископаемых, используя эти физические свойства.
Среди свойств, которые мы обсудим, следующие: кристаллический габитус, спайность,
твердость, плотность, блеск, полоса, цвет, прочность, магнетизм и вкус. Лица, которые развиваются на
Кристалл зависит от пространства, доступного для роста кристаллов. Если
кристаллы врастают друг в друга или в ограниченной среде, это
возможно, что не будет развито хорошо сформированных граней кристалла.
Однако иногда кристаллы приобретают определенные формы чаще, чем
другие, хотя симметрия может быть не очевидна из этих
распространенные формы. Термин, используемый для описания общей формы кристалла привычка.
Лица, которые развиваются на
Кристалл зависит от пространства, доступного для роста кристаллов. Если
кристаллы врастают друг в друга или в ограниченной среде, это
возможно, что не будет развито хорошо сформированных граней кристалла.
Однако иногда кристаллы приобретают определенные формы чаще, чем
другие, хотя симметрия может быть не очевидна из этих
распространенные формы. Термин, используемый для описания общей формы кристалла привычка. 

 Многие из образцов, которые вы исследуете, не могут быть легко заменены.
Декольте обычно
индуцируется в минерале, когда он извлекается из породы, когда он
найдены, и обычно их можно увидеть как плоскости, проходящие через минерал. Следовательно,
вам не нужно разбивать минерал, чтобы увидеть его спайность.
Многие из образцов, которые вы исследуете, не могут быть легко заменены.
Декольте обычно
индуцируется в минерале, когда он извлекается из породы, когда он
найдены, и обычно их можно увидеть как плоскости, проходящие через минерал. Следовательно,
вам не нужно разбивать минерал, чтобы увидеть его спайность. 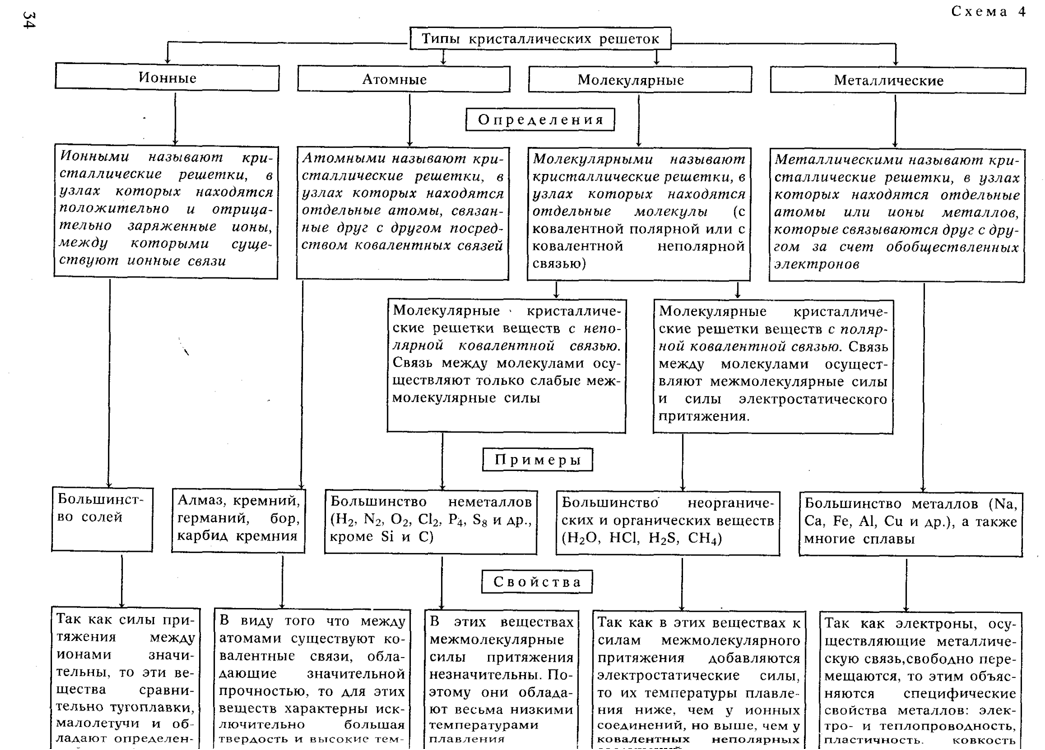 Поэтому может не
проявляться во всех образцах одного и того же минерала, но может проявляться, если
Минерал был подвергнут правильным стрессовым условиям.
Поэтому может не
проявляться во всех образцах одного и того же минерала, но может проявляться, если
Минерал был подвергнут правильным стрессовым условиям. Эти
минералы перечислены ниже вместе с твердостью некоторых распространенных
объекты.
Эти
минералы перечислены ниже вместе с твердостью некоторых распространенных
объекты.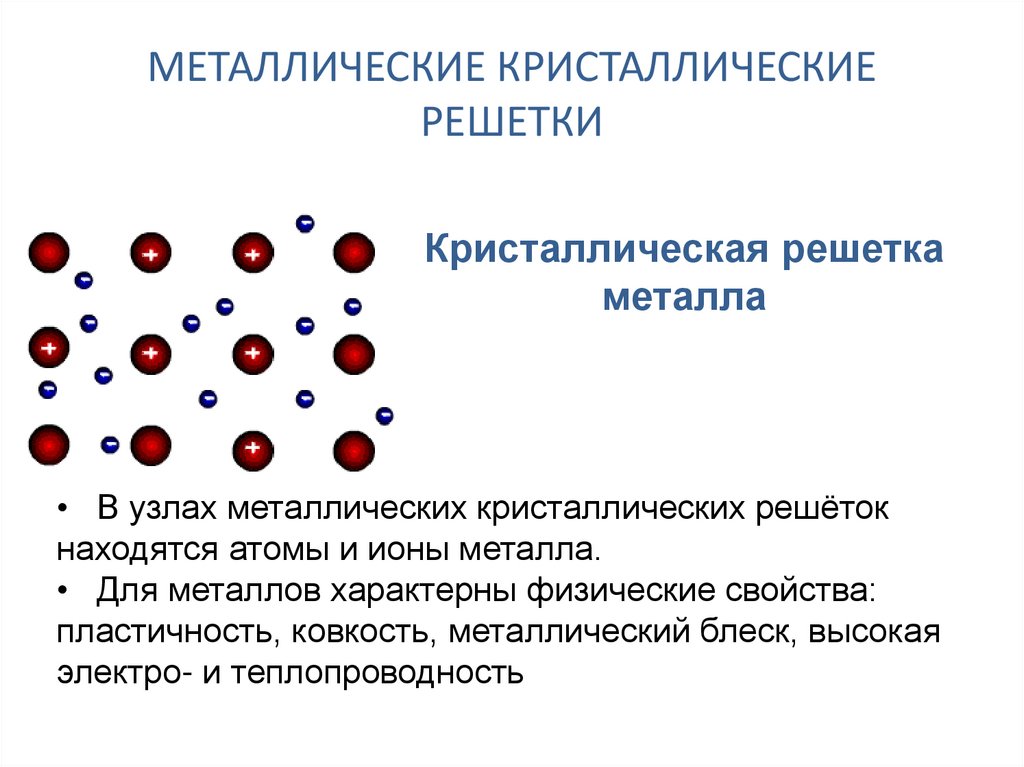 Стойкость можно описать следующим
условия.
Стойкость можно описать следующим
условия.
 Иногда это придает минералу
радужное качество. Минералы, которые показывают это, включают: борнит (Cu 5 FeS 4 )
, гематит (Fe 2 O 3 ), сфалерит (ZnS) и некоторые
образцы лабрадорита (плагиоклаза).
Иногда это придает минералу
радужное качество. Минералы, которые показывают это, включают: борнит (Cu 5 FeS 4 )
, гематит (Fe 2 O 3 ), сфалерит (ZnS) и некоторые
образцы лабрадорита (плагиоклаза). К ним относятся – шеелит
(CaWO 4 ), виллемит (Zn 2 SiO 4 ), кальцит
(CaCO 3 ), скаполит (3NaAlSi 3 O8 . (NaCl –
СаСО 3 ) и алмаз (С).
К ним относятся – шеелит
(CaWO 4 ), виллемит (Zn 2 SiO 4 ), кальцит
(CaCO 3 ), скаполит (3NaAlSi 3 O8 . (NaCl –
СаСО 3 ) и алмаз (С).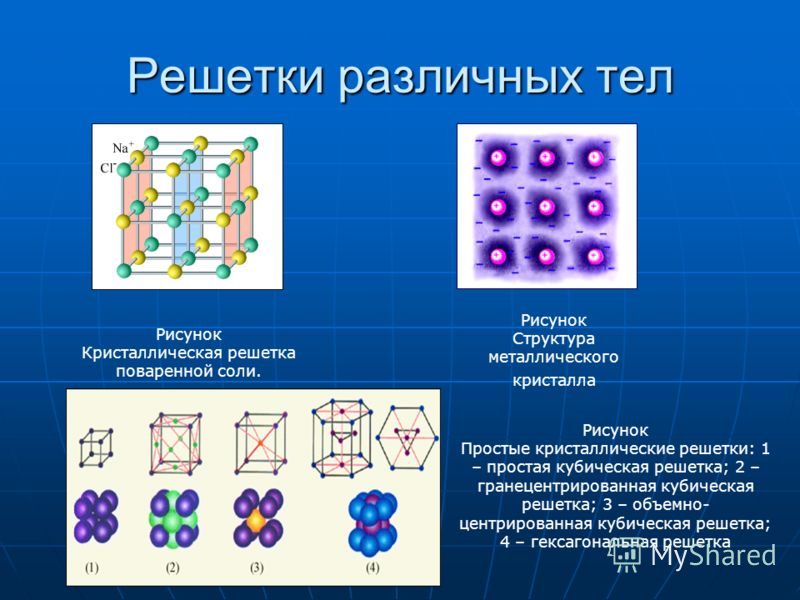 <5.
<5. 
 Ice Ih — нормальная форма льда; лед Ic образуется путем осаждения пара на
очень низкие температуры (ниже 140 К). Аморфный лед можно получить путем осаждения
водяной пар на подложку при еще более низких температурах.
Ice Ih — нормальная форма льда; лед Ic образуется путем осаждения пара на
очень низкие температуры (ниже 140 К). Аморфный лед можно получить путем осаждения
водяной пар на подложку при еще более низких температурах.  График справа показывает фазовую диаграмму воды (нажмите на
изображение для расширенной версии). тройная точка воды —
Когда лед, вода и водяной пар могут сосуществовать, температура составляет 0,01°С (0°С =
273,16К), а давление 6,1 мбар. Вода – единственное вещество, которое мы обычно
опыта в своей тройной точке в повседневной жизни.
График справа показывает фазовую диаграмму воды (нажмите на
изображение для расширенной версии). тройная точка воды —
Когда лед, вода и водяной пар могут сосуществовать, температура составляет 0,01°С (0°С =
273,16К), а давление 6,1 мбар. Вода – единственное вещество, которое мы обычно
опыта в своей тройной точке в повседневной жизни.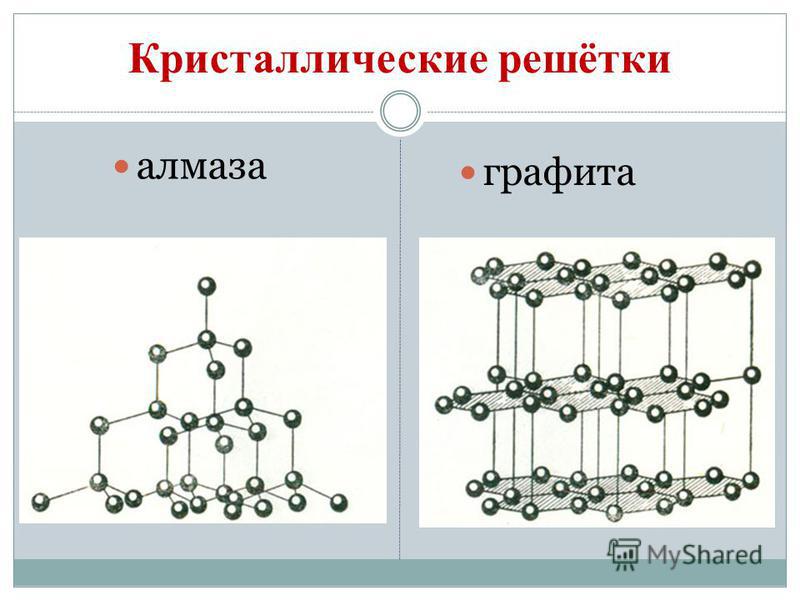 Эти
приблизительные выражения имеют точность лучше 0,1 процента от -50°C до 50°C.
Эти
приблизительные выражения имеют точность лучше 0,1 процента от -50°C до 50°C.  .
.