Физические свойства меди таблица 8 класс: Attention Required! | Cloudflare
alexxlab | 16.11.2020 | 0 | Разное
Характеристика меди – химические и физические свойства
Свойства меди, металла, который встречается и в виде довольно больших самородков, люди изучали еще в древности. Тогда из меди и его сплавов создавали предметы посуды, оружие, украшения, разные предметы бытового назначения. Столь высокая популярность этого металла на протяжении столетий была обусловлена не только его особыми качествами, но и легкостью обработки. Медь, присутствующую в руде в форме карбонатов и окислов, довольно легко восстановить, что и научились делать наши предки в древности. В этой статье поговорим о свойствах меди и методах ее определения.
Физические свойства меди
Чистая медь – это металл, цвет которого варьируется от розового до красного оттенка. Радиус положительно заряженных ионов меди, может принимать такие значения:
- при координационном показателе равном 6-ти — до 0,091 нм
- при координационном показателе равном 2 — до 0,06 нм.
Радиус атома меди равняется 0,128 нм. Величина сродства к электрону достигает 1,8 эВ. Процесс ионизации данного атома увеличивает сродство к электрону от 7,726 до 82,7 эВ.
Поскольку медь в потенциальном ряду расположена справа от водорода, то она не способна вытеснять этот элемент из воды и разного типа кислот. Медь имеет кристаллическую решетку кубического гранецентрированного типа, а ее величина достигает 0,36150 нм. Плавление меди начинается при температуре 1083 градусов, а закипает она при 26570 градусах. Плотность меди определяется ее физическими свойствами и составляет 8,92 г/см3.
Кроме вышеперечисленных, стоит выделить еще и такие физические и механические свойства меди:
- показатель термического линейного расширения составляет 0,00000017 единиц
- показатель предела прочности на растяжение достигает 22 кгс/мм2
- уровень твердости меди по шкале Бринелля равен 35 кгс/мм2
- удельная масса составляет 8,94 г/см3
- показатель упругости равен 132000 Мн/м2
- относительное удлинение равняется 60%.
Абсолютно неповторимыми можно назвать магнитные свойства этого металла, который является полностью диамагнитным. Именно благодаря этим показателям, вместе с физическими свойствами, к примеру, удельным весом и удельной проводимостью, можно объяснить такую широкую популярность этого металла в производстве изделий электротехнической отрасли. Несколько похожие свойства имеет алюминий, который тоже активно применяется в изготовлении различной электротехнической продукции, к примеру, проводов, кабелей и прочего.
Единственная характеристика меди, которую можно изменить – это предел прочности. Этот показатель может быть улучшен почти в два раза (до 420–450 МН/м2), путем специальной технологической операции, называемой наклеп.
Химические свойства меди
Химическая характеристика меди определяется ее расположением в периодической таблице элементов Менделеева, где ей присвоен порядковый номер 29. Находится она в четвертом периоде и в одной группе с благородными металлами. Таким образом, лишний раз подтверждается уникальность ее химических качеств, о которых дальше мы расскажем более детально.
Если уровень влажный не высокий, то медь почти не проявляет химической активности. Однако, все кардинально меняется, когда изделия помещают в условия высокой влажности и повышенного содержания углекислого газа. Именно такие условия являются идеальными для начала активного окисления меди. В процессе окисления на поверхности медного предмета создается зеленоватая пленка, которая состоит из CuCO3, Cu(OH)2, а также разных сернистых соединений. Эту пленку называют патиной и она очень важна, поскольку защищает металл от дальнейшего разрушения.
Медь довольно легко вступает в реакции с элементами, находящимися в группе галогенов. Под действием паров серы металл воспламеняется. Высокий уровень родства медь демонстрирует и к селену. Общие свойства меди не позволяют ей вступить в реакцию с азотом, углеродом и водородом даже при нагревании.
Взаимодействие с кислотами:
- результатом реакции с серной кислотой является сульфат и чистая медь
- с бромоводородной и иодоводородной кислотой соответственно образуются бромид и иодид меди.
А вот взаимодействие со щелочами позволяет получить купрат. Реакции получения меди, при которых происходит восстановление металла до свободного состояния, невозможны без присутствия оксида углерода, аммиака, метана и некоторых других веществ.
Свойства солей меди
Одно- и двухвалентная медь может формировать комплексные соединения, которые выделяются высоким уровнем устойчивости. К подобным соединениям можно отнести двойные соли меди и аммиачные смеси. Они активно используются в различных отраслях промышленности.
Сульфат меди (II) – CuSO4 в безводном состоянии является белым порошком. При добавлении воды он приобретает синюю окраску. Поэтому его используют для выявления остатков воды в органических жидкостях. Водный раствор сульфата меди отличается сине-голубым оттенком. За этот цвет отвечают гидратированные ионы [Cu(h3O)4]2+, следовательно, такого же цвета и все остальные разбавленные растворы солей меди (II). Исключением являются растворы с содержанием окрашенных анионов.
- в процессе электролитического нанесения меди на металлы
- для создания минеральных красок
- как исходный материал для получения прочих соединений меди.
В сельскохозяйственной отрасли разбавленный раствор медного купороса очень популярен для опрыскивания растений и замачивания семян перед посевом, потому что он уничтожает споры вредных грибов.
Хлорид меди (II) – CuCl2. 2h3O. Это легко растворимое в воде соединение темно-зеленого цвета. Высокая концентрация хлорида меди позволяет получить растворы зеленого цвета, а разбавление приводит к окраске в сине-голубой оттенок.
Нитрат меди (II) – Cu(NO3)2.3h3O. Его получают путем растворения меди в азотной кислоте. В процессе нагревания синие кристаллы нитрата меди сначала отдают воду, после чего с легкостью разлагаются, выделяя кислород и бурый диоксид азота, становясь оксидом меди (II).
2CuSO4 + 2Na2CO3 + h3O = (CuOH)2CO3↓ + 2Na2SO4 + CO2↑
Кроме этого, его используют, чтобы получить хлорид меди (II), а также приготовить синие и зеленые минеральные краски.
Ацетат меди (II) – Cu (Ch4COO)2.h3O. Это соединение можно получить, если провести обработку металлической меди или оксида меди (II) раствором уксусной кислоты. Чаще всего – это смесь основных солей разного состава и цвета (от зеленого до сине-зеленого).
Помните, что все без исключения соли меди являются ядовитыми. По этой причине, во избежание формирования медных солей, вся медная посуда должна быть изнутри покрыта слоем олова.
Методы определения меди
Определение меди может проводиться такими методами:
- химическими
- количественными
- фотометрическими.
Различные химические составы способны оказывать влияние на расщепление молекул и атомов вещества, следовательно, можно выделить его составные части. Химический метод определения количества заключается в электролитическом методе измерения медной части в сплавах других металлов. Его осуществляют при помощи таких элементов:
- ацетилен
- винная кислота
- водный аммиак
- азотнокислый аммоний
- динатриевая соль
- этиловый спирт
- купризон.
Прежде всего, происходит взвешивание медного состава (навески). После этого ее отправляют в подготовленный раствор реактивов. В этом растворе навеска должна полностью раствориться. Далее весь раствор нужно нагреть, так как в процессе нагревания удаляются окиси азота. Очищенный раствор необходимо разбавить водой и снова нагреть до 40 оС. Теперь массу можно подвергать процессу электролиза. Электроды, погружаемые в раствор создают из платины. Далее включается ток силой 2,2 В и в условиях постоянного помешивания происходит выделение меди.
Разработано большое количество видов химических растворов для очистки медных изделий.
Количественное определение массы меди в общем объеме металла целесообразно использовать для сплавов с никелем, бронзой или цинком. При воздействии на вещество происходит осаждение меди и в таком виде ее можно измерить. Осаждение может быть осуществлено неорганическими и органическими элементами. Из неорганических веществ можно выделить:
- тетрароданодиаминхромиат аммония, называемый солью Рейнеке
- тиокарбонат калия способен осадить медь при температуре выше 80 оС
- уксусной кислотой можно осадить медный оксалат.
Из органических веществ применяются:
- оксихинолин-8, который способен осадить медь в комплексе с аммиачным и щелочным раствором. Нагревание осадка приводит к образованию оксида меди
- α-бензоиноксим при участии спирта может осадить металл в форме хлопьев. Реакция невозможна, если в составе есть никель
- йодид калия применяют в нейтральной и кислой среде. Нет смысла использовать его, когда в сплаве имеется железо, сурьма и мышьяк.
Достоинства фотометрического метода заключаются в высоком показателе точности измерения количества меди, а также простота применения. Для реализации этого метода потребуются такие соединения:
- купризон
- диэтилдитиокарбамат свинца.
Смысл фотометрического метода определения меди состоит в фиксации интенсивности цвета материала, прошедшего через концентрированный раствор. Раствор состоит из:
- аммиака
- лимоннокислого раствора аммония
- диэтилдитиокарбамата свинца
- сернокислого натрия.
Вещество, в котором нужно выявить количество меди пропускают через указанные выше растворы. Отметим, что здесь важно соблюдать пропорции. Далее происходит процесс фотометрии.
Определение меди возможно также и в сточных, канализационных, речных, морских водах, и в составе почве. Существует три способа:
- атомноабсорбционный прямой
- атомноабсорбционный при участии хелатообразования
- атомноабсорбционный, подразумевающий использование графитовой печи.
Чтобы определить количество меди в почве самым надежным методом является метод с использованием графитной печи.
Для этого пробу почвы нужно поместить в графитовую трубу, обезводить при помощи сжигания и распылить. Процедура распыления сопряжена с разделением вещества на атомы, с последующей фильтрацией и выделением из них нужного металла. Чтобы оценить пробу грунта можно воспользоваться любым фотометрическим методом определения меди.
Характеристики основных физико-механических и физико-химических свойств, температуры литья и горячей обработки меди
Атомное строение меди
Медь в Периодической системе имееет атомный номер 29 является первым элементом 1B группы или первым элементом одиннадцатой группы. Электроннная конфигурация свободного атома в нормальном состоянии (OK) ls22s22p63s23p63d104s1.
Медь изоморфна и кристаллизуется с образованием гранецентрированной кубической решетки типа A1. Период решетки меди при 18°С равен 0,36074нм; с повышением температуры он возрастает.
Элементы, находящиеся в твердом растворе, изменяют период решетки меди. Чем больше разница в размерах атомов меди и растворенного элемента, тем больше эти изменения.
| T, °K | 0 | 291 | 573 | 773 | 944 | 1044 | 1144 |
| Период решетки, нм | 0,35957 | 0,36074 | 0,36260 | 0,36308 | 0,36526 | 0,36603 | 0,36683 |
Атомный радиус по Гольдшмидту для координационного числа 12 составляет 0,12773нм, межатомное расстояние 0,25546нм. Большинство физических свойств зависит от чистоты и состояния меди.
Атомный номер | 29 |
Относительная атомная масса | 63,54 |
Решетка | Кубическая гранецентрированная ( α = 3,6080 Å) |
Плотность г/см2 | 8,94 |
| Температура плавления, °С | 1083 |
Скрытая теплота плавления, кал/г | 50,6 |
Температура кипения, °С | 2595 |
Скрытая теплота испарения, кал/г | 1290 |
Теплопроводность, кал / (см·с·°С), при: | 0,941 |
100° С | 0,900 |
700°С | 0,840 |
Удельная теплоемкость, кал/(г·°С), при: | 0,092 |
600° С | 0,103 |
1000° С | 0,112 |
Коэффициент линейного расширения α · 10-6, 1/° С, при: | 16,7 |
25—300° С | 17,7 |
0 — 600° С | 18,6 |
0—900° С | 19,3 |
Отражательная способность, %, при λ= 5500 Å | 61 |
Излучательная способность, % (λ = 6650 Å), при: | 9,6 |
1080° С | 11,7 |
1100° С | 15,0 |
Удельное электросопротивление, Ом·мм2/м, при:
| 0,0178 |
500° С | 0,053 |
Электропроводность, м/(Om·мм2) при 20°С | 57 |
Температурный коэффициент электросопротивления,1/°С, при 20°С | 3,93·10-3 |
Мощность излучаемой энергии, Вт/см2, при: | 0,05 |
227°С | 0,11 |
1227°С | 4,26 |
Работа выхода, э·В | 4,46 |
Сжатие объема при затвердевании, % | 4,05-4,2 |
Вязкость при 1145° С, г/(см·с) | 0,0341 |
Поверхностное натяжение, дин/см | 1178 |
Нормальный потенциал по отношению к водородному электроду, В | +0,34 |
Предел прочности, кгс/мм2: | 20-25 |
твердой меди | 40-49 |
Относительное удлинение, %: | 60 |
твердой меди | 6 |
Твердость по Бринелю, кгс/мм2: | 45 |
твердой меди | 110 |
Предел текучести, кгс/мм2: | |
мягкой меди | 9-15 |
твердой меди | 30-45 |
Ударная вязкость, кгс·м/см2 | 10-18 |
Сопротивление сжатию, кгс/мм2 | 55-65 |
Предел прочности на срез, кгс/мм2: | 15 |
твердой меди | 21 |
Предел ползучести кгс/мм2, при: | 7 |
200° С | 5 |
400° С | 1,4 |
Модуль сдвига, кгс/мм2 | 4240 |
Модуль упругости, кгс/мм2: | 11700—12600 |
твердой меди | 12200—13500 |
Температура рекристаллизации,° С | 180-300 |
Температура горячей деформации ° С | 1050—750 |
Температура литья ° С | 1150 — 1250 |
Линейная усадка, % | 2,1 |
Травитель после отжига на воздухе | 10%-ная серная кислота |
Характеристики упругости
Упругие свойства меди характеризуется модулем нормальной упругости Е (модуль Юнга), сдвига G и объемного сжатия Есж, а также величиной отношения поперечной и продольной упругой деформации, т. е. коэффициентом Пуассона μ. Эти характеристики упругих свойств связаны между собой. Для большинства металлов абсолютное значение коэффициента Пуассона мало отличается от 1/3. Для меди оно составляет :
μ = 0,33 Есж = E G ≅ 3/8E
Статистически усредненные значения характеристик упругости меди при 20°С по данным многочисленных исследований представлены с указанием стандартных отклонений:
Е= 123,5 ± 0,7 ГПа
Есж = 140,2 ± 3,9 ГПа
G = 45,4 ± 1,2 ГПа;
μ = 0,33 ± 0,09
Константы упругости монокристаллов меди зависят от кристаллографических направлений. У поликристаллов квазиизотропной меди вследствие произвольной ориентации зерен эти константы усредняются.
| Состояние | Направление кристаллической решетки | Е, ГПа | G, ГПа | Есж, ГПа | м |
| <111> | 159 | 33,8 | – | – | |
| Монокристаллическое | <100> | 77,5 | 61,0 | – | – |
| <110> | 126 | 38,0 | – | – | |
| Поликристаллическое | — | 115—125 | 42—46 | 139 | 0,32—0,34 |
Значения модулей Е и G в интервале температур 300—1300°К уменьшаются по линейному закону. Лишь в области низких температур наблюдается отклонение от равномерного изменения модулей.
| Т. к | 4,2 | 100 | 200 | 300 | 500 | 700 | 900 | 1100 | 1300 |
| Е, ГПа | 141 | 139 | 134 | 128 | 115 | 103 | 89,7 | 76,8 | 63,7 |
| G, ГПа | 50 | 49,5 | 47,3 | 44,7 | 37,8 | 31,0 | 24,1 | 18,5 | 11,5 |
Плотность
В качестве международного стандарта (IACS) плотность меди равна 8890кг/м3, при температуре 20°С. Плотность меди различных марок при температуре 20°С имеет небольшие различия:
| Марка | Плотность, кг/м3 |
| Медь бескислородная М00б | 8963 ± 3 |
| Медь бескислородная М00б | 8950 |
| Медь, раскисленная фосфором М2р (0,04%Р) | 8930 |
Литая медь имеет плотность 8920кг/м3. Холодная деформация отожженной меди уменьшает ее плотность вследствие увеличения концентрации вакансий, дислоцированных атомов, дислокаций и других дефектов тонкой структуры. Возврат и рекристаллизация при нагреве наклепанного металла повышают плотность меди до исходного значения.
При нагреве плотность меди уменьшается вследствие расширения решетки, при плавлении она снижается на 5%.

| T, °C | 20 | 600 | 700 | 800 | 900 | 1000 | 1100 | 1200 | 1300 | 1400 |
| Плотность, кг/м3 | 8890 | 8680 | 8610 | 8550 | 8470 | 8400 | 7960 | 7860 | 7770 | 7700 |
СВОЙСТВА МЕДИ
МЕДЬ и МЕДНЫЙ ПРОКАТ
Марки и химический состав технической меди
Марки меди и их химический состав определен в ГОСТ 859-2001. Сокращенная информация о марках меди приведена ниже (указано минимальное содержание меди и предельное содержание только двух примесей – кислорода и фосфора):
| Марка | Медь | О2 | P | Способ получения, основные примеси |
| М00к | 99.98 | 0.01 | – | Медные катоды:продукт электролитического рафинирования, заключительная стадия переработки медной руды. |
| М0к | 99.97 | 0.015 | 0.001 | |
| М1к | 99.95 | 0.02 | 0.002 | |
| М2к | 99.93 | 0.03 | 0.002 | |
| М00 | 99.99 | 0.001 | 0.0003 | Переплавка катодов в вакууме, инертной или восстановительной атмосфере.Уменьшает содержание кислорода. |
| М0 | 99.97 | 0.001 | 0.002 | |
| М1 | 99.95 | 0.003 | 0.002 | |
| М00 | 99.96 | 0.03 | 0.0005 | Переплавка катодов в обычной атмосфере.Повышенное содержание кислорода. Отсутствие фосфора |
| М0 | 99.93 | 0.04 | – | |
| М1 | 99.9 | 0.05 | – | |
| М2 | 99.7 | 0.07 | – | Переплавка лома.Повышенное содержание кислорода, фосфора нет |
| М3 | 99.5 | 0.08 | – | |
| М1ф | 99.9 | – | 0.012 – 0.04 | Переплавка катодов и лома медис раскислением фосфором.Уменьшает содержание кислорода, но приводит к повышенному содержанию фосфора |
| М1р | 99.9 | 0.01 | 0.002 – 0.01 | |
| М2р | 99.7 | 0.01 | 0.005 – 0.06 | |
| М3р | 99.5 | 0.01 | 0.005 – 0.06 |
Первая группа марок относится к катодной меди, остальные – отражают химический состав различных медных полуфабрикатов (медные слитки, катанка и изделия из неё, прокат).
Специфические особенности меди, присущие разным маркам, определяются не содержанием меди (различия составляют не более 0.5%), а содержанием конкретных примесей (их количество может различаться в 10 – 50 раз). Часто используют классификацию марок меди по содержанию кислорода:
– бескислородная медь (М00 , М0 и М1 ) с содержанием кислорода до 0.001%.
– рафинированная медь (М1ф, М1р, М2р, М3р) с содержанием кислорода до 0.01%, но с
повышенным содержанием фосфора.
– медь высокой чистоты (М00, М0, М1) с содержанием кислорода 0.03-0.05%.
– медь общего назначения (М2, М3) с содержанием кислорода до 0.08%.
Примерное соответствие марок меди, выпускаемой по разным стандартам, приведено ниже:
ГОСТ | EN, DIN |
М00 | Cu-OFE |
| М0 | Cu-PHC, OF-Cu |
| М1 | Cu-OF, Cu-OF1 |
| М1 | Cu-ETP, Cu-ETP1,Cu-FRTP, Cu-FRHC, SE-Cu, E-Cu, E Cu57, E Cu58 |
| М1ф | Cu-DHP, SF-Cu |
| М1р | Cu-DLP, SW-Cu |
Разные марки меди имеют различное применение, а отличия в условиях их производства определяют существенные различия в цене.
Для производства кабельно-проводниковой продукции катоды переплавляют по технологии, которая исключает насыщение меди кислородом при изготовлении продукции. Поэтому медь в таких изделях соответствует маркам М00, М0 , М1 .
Требованиям большинства технических задач удовлетворяют относительно дешевые марки М2 и М3. Это определяет массовое производство основных видов медного проката из М2 и М3.
Прокат из марок М1, М1ф, М1р, М2р, М3р производится в основном для конкретных потребителей и стоит намного дороже.
Физические свойства меди
Главное свойство меди, которое определяет её преимущественное использование – очень высокая электропроводность (или низкое удельное электросопротивление). Такие примеси как фосфор, железо, мышьяк, сурьма, олово, существенно ухудшают её электропроводность. На величину электропроводности существенное влияние оказывает способ получения полуфабриката и его механическое состояние. Это иллюстрируется приведенной ниже таблицей:
Удельное электрическое сопротивление меди для различных полуфабрикатов разных марок (гарантированные значения) при 20оС.| мкОм*м | марка | Вид и состояние полуфабриката | ГОСТ, ТУ |
| 0.01707 | М00 | Слитки (непрерывное вертикальное литье) | 193-79 |
М00 | Катанка кл.А ( кислород: 0.02-0.035%) | ТУ 1844 01003292517 -2004 | |
0.01718 | М0 | Катанка кл.В (кислород: 0.045%) | |
| 0.01724 | М1 | Катанка кл.С (кислород: 0.05%) | |
М1 | Слитки (горизонтальное литье) | 193-79 | |
М1 | Слитки (горизонтальное литье) | ||
| 0.01748 | М1 | Ленты | 1173-2006 |
М1 | Прутки отожженные | 1535-2006 | |
0.01790 | М1 | Прутки полутвердые, твердые, прессованные |
Различия в сопротивлении катанки марок М00, М0 и М1, обусловлены разным количеством примесей и составляют около 1%. В то же время различия в сопротивлении, обусловленные разным механическим состоянием, достигают 2 – 3%. Удельное сопротивление изделий из меди маркиМ2 примерно 0.020 мкОм*м.
Второе важнейшее свойство меди – очень высокая теплопроводность.
Примеси и легирующие добавки уменьшают электро- и теплопроводность меди, поэтому сплавы на медной основе значительно уступают меди по этим показателям. Значения параметров основных физических свойств меди в сравнении с другими металлами приведены в таблице (данные приведены в двух разных системах единиц измерения):
Показатели при | Единица измерения | Медь | Алю- миний | Латунь Л63, ЛС | Бронза БрАЖ | Сталь 12Х18Н10 |
Удельное элетросопротивление, | мкОм*м | 0.0172 – 0.0179 | 0.027- 0.030 | 0.065 | 0.123 | 0.725 |
Теплопроводность, | кал/см*с*град | 0.93 | 0.52 | 0.25 | 0.14 | 0.035 |
Вт/м*град | 386 – 390 | 217 | 106 | 59 | 15 |
По электро- и теплопроводности медь незначительно уступает только серебру.
Влияние примесей и особенности свойств меди различных марок
Отличия в свойствах меди разных марок связаны с влиянием примесей на базовые свойства меди. О влиянии примесей на физические свойства (тепло- и электропроводность) говорилось выше. Рассмотрим их влияние на другие группы свойств.
Влияние на механические свойства.
Железо, кислород, висмут, свинец, сурьма ухудшают пластичность. Примеси, малорастворимые в меди (свинец, висмут, кислород, сера), приводят к хрупкости при высоких температурах.
Температура рекристаллизации меди для разных марок составляет 150-240оС. Чем больше примесей, тем выше эта температура. Существенное увеличение температуры рекристаллизации меди дает серебро, цирконий. Например введение 0.05% Ag увеличивает температуру рекристаллизации вдвое, что проявляется в увеличении температуры размягчения и уменьшении ползучести при высоких температурах, причем без потери тепло- и электропроводности.
Влияние на технологические свойства.
К технологическим свойствам относятся 1) способность к обработке давлением при низких и высоких температурах, 2) паяемость и свариваемость изделий.
Примеси, особенно легкоплавкие, формируют зоны хрупкости при высоких температурах, что затрудняет горячую обработку давлением. Однако уровень примесей в марках М1 и М2 обеспечивают необходимую технологическую пластичность.
При холодном деформировании влияние примесей заметно проявляется при производстве проволоки. При одинаковом пределе прочности на разрыв ( ?в =16 кгс/мм2 ) катанки из марок М00, М0 и М1 имеют разное относительное удлинение ? (38%, 35% и 30% соответственно). Поэтому катанка класса А (ей соответствует марка М00) более технологична при производстве проволоки, особенно малых диаметров. Использование бескислородной меди для производства проводников тока обусловлено не столько величиной электропроводности, сколько технологическим фактором.
Процессы сварки и пайки существенно затрудняются при увеличении содержания кислорода, а также свинца и висмута.
Влияние кислорода и водорода на эксплуатационные свойства.
При обычных условиях эксплуатационные свойства меди (прежде всего долговечность эксплуатации) практически одинаковы для разных марок. В то же время при высоких температурах может проявиться вредное влияние кислорода, содержащегося в меди. Эта возможность обычно реализуется при нагреве меди в среде, содержащей водород.
Кислород изначально содержится в меди марок М0, М1, М2, М3. Кроме этого, если бескислородную медь отжечь на воздухе при высоких температурах, то вследствие диффузии кислорода поверхностный слой изделия станет кислородсодержащим. Кислород в меди присутствует в виде закиси меди, которая локализуется по границам зерен.
Кроме кислорода в меди может присутствовать водород. Водород попадает в медь в процессе электролиза или при отжиге в атмосфере, содержащей водяной пар. Водяной пар всегда присутствует в воздухе. При высокой температуре он разлагается с образованием водорода, который легко диффундирует в медь.
В бескислородной меди атомы водорода располагаются в междоузлиях кристаллической решетки и особо не сказываются на свойствах металла.
В кислородсодержащей меди при высоких температурах водород взаимодействует с закисью меди. При этом в толще меди образуется водяной пар высокого давления, что приводит к вздутиям, разрывам и трещинам. Это явление известно как «водородная болезнь» или «водородное охрупчивание». Оно проявляется при эксплуатации медного изделия при температурах свыше 200оС в атмосфере, содержащей водород или водяной пар.
Степень охрупчивания тем сильнее, чем больше содержание кислорода в меди и выше температура эксплуатации. При 200оС срок службы составляет 1.5 года, при 400оС – 70 часов.
Особенно сильно оно проявляется в изделиях малой толщины (трубки, ленты).
При нагреве в вакууме изначально содержащийся в меди водород взаимодействует с закисью меди и также ведет к охрупчиванию изделия и ухудшению вакуума. Поэтому изделия, которые эксплуатируются при высокой температуре, производятся из бескислородных (рафинированных) марок меди М1р, М2р, М3р.
Механические свойства медного проката
Большая часть медного проката, поступающего в свободную продажу, производится из марки М2. Прокат из марки М1 производится в основном под заказ, кроме того он примерно на 20% дороже.
Холоднодеформированный прокат – это тянутые (прутки, проволока, трубы) и холоднокатаные (листы, лента, фольга) изделия. Он выпускается в твердом, полутвердом и мягком (отожженном) состояниях. Такой прокат маркируется буквой «Д», а состояния поставки буквами Т, П или М.
Горячедеформированный прокат – результат прессования (прутки, трубы) или горячей прокатки (листы, плиты) при температурах выше температуры рекристаллизации. Такой прокат маркируется буквой «Г». По механическим свойствам горячедеформированный прокат близок (но не идентичен) к холоднодеформированному прокату в мягком состоянии.
Параметры при комнатной темп. | М | Т |
Модуль упругости E, кгс/мм2 | 11000 | 13000 |
Модуль сдвига G, кгс/мм2 | 4000 | 4900 |
Предел текучести ?0.2 , кгс/мм2 | 5 – 10 | 25 – 34 |
Предел прочности ?в , кгс/мм2 | 19 – 27 | 31 – 42 |
Относ. удлинение ? | 40 – 52 | 2 – 11 |
Твердость НВ | 40 – 45 | 70 – 110 |
Сопротивление срезу, кгс/мм2 | 10 – 15 | 18 – 21 |
Ударная вязкость, | 16 – 18 | |
Обрабатываем. резанием, % к Л63-3 | 18 | |
| Предел усталости ?-1 при 100 млн циклов | 7 | 12 |
Высокий предел прочности на сжатие (55 – 65 кгс/мм2) в сочетании с высокой пластичностью определяет широкое использование меди в качестве прокладок в уплотнениях неподвижных соединений с температурой эксплуатации до 250оС (давление 35 Кгс\см2 для пара и 100 Кгс\см2 для воды).
Медь широко используется в технике низких температур, вплоть до гелиевых. При низких температурах она сохраняет показатели прочности, пластичности и вязкости, характерные для комнатной температуры. Наиболее часто используемое свойство меди в криогенной технике – её высокая теплопроводность. При криогенных температурах теплопроводность марок М1 и М2становится существенной, поэтому в криогенной технике применение марки М1 становится принципиальным.
Медные прутки выпускаются прессованными (20 – 180 мм) и холоднодеформированными, в твердом, полутвердом и мягком состояниях (диаметр 3 – 50 мм) по ГОСТ 1535-2006.
Плоский медный прокат общего назначения выпускается в виде фольги, ленты, листов и плит по ГОСТ 1173-2006:
Фольга медная – холоднокатаная: 0.05 – 0.1 мм (выпускается только в твердом состоянии)
Ленты медные – холоднокатаные: 0.1 – 6 мм.
Листы медные – холоднокатаные: 0.2 – 12 мм
– горячекатаные: 3 – 25 мм (механич. свойства регламентируются до 12 мм)
Плиты медные – горячекатаные: свыше 25 мм (механические свойства не регламентируются)
Горячекатаные и мягкие холоднокатаные медные листы и ленты выдерживают испытание на изгиб вокруг оправки диаметром равным толщине листа. При толщине до 5 мм они выдерживают изгиб до соприкосновения сторон, а при толщине 6 – 12 мм – до параллельности сторон. Холоднокатанные полутвердые листы и ленты выдерживают испытание на изгиб на 90 град.
Таким образом допустимый радиус изгиба медных листов и лент равен толщине листа (ленты).
Глубина выдавливания лент и листов пуансоном радиусом 10 мм составляет не менее 7 мм для листов толщиной 0.1-0.14 мм и не менее 10 мм для листов толщиной 1-1.5 мм. По этому показателю (выдавливаемость) медь уступает латуням Л63 и Л68.Медные трубы общего назначения изготавливаются холоднодеформированными (в мягком, полутвердом и твердом состояниях) и прессованными (больших сечений) по ГОСТ 617-2006.
Медные трубы используются не только для технологических жидкостей, но и для питьевой воды. Медь инертна по отношению к хлору и озону, которые используются для очистки воды, ингибирует рост бактерий, при замерзании воды медные трубы деформируются без разрыва. Медные трубы для воды производятся по ГОСТ Р 52318-2005, для них ограничено содержание органических веществ на внутренней поверхности. Минимальные радиусы изгиба и допустимые давления для мягких медных труб приведены ниже:
Размер трубы, мм | Допустимое давление, бар | Радиус изгиба, мм | Размер трубы | Допустимое давление, бар |
Дюймы (мм) | ||||
6*1 | 230 | 30 | 1/4” (6.35*0.8) | 220 |
8*1 | 163 | 35 | – | – |
10*1 | 130 | 40 | 3/8” (9.52*0.8) | 120 |
12*1 | 105 | 45 | 1/2” (12.7*0.8) | 100 |
14*1 | 90 | 52 | – | – |
16*1 | 80 | 60 | 5/8” (15, 87*1) | 80 |
18*1 | 67 | 70 | 3/4” (19,05*1) | 67 |
20*1 | 60 | 75 | – | – |
22*1 | 54 | 80 | 7/8” (22.22*1) | 54 |
Коррозионные свойства меди.
При нормальных температурах медь устойчива в следующих средах:
– сухой воздух
– пресная вода (аммиак, сероводород, хлориды, кислоты ускоряют коррозию)
– в морской воде при небольших скоростях движения воды
– в неокислительных кислотах и растворах солей (в отсутствии кислорода)
– щелочные растворы (кроме аммиака и солей аммония)
– сухие газы-галогены
– органические кислоты, спирты, фенольные смолы
Медь неустойчива в следующих средах:
– аммиак, хлористый аммоний
– окислительные минеральные кислоты и растворы кислых солей
Коррозионные свойства меди в некоторых средах заметно ухудшаются с увеличением количества примесей.
Контактная коррозия.
Допускается контакт меди с медными сплавами, свинцом, оловом во влажной атмосфере, пресной и морской воде. В то же время не допускается контакт с алюминием, цинком вследствие их быстрого разрушения.
Свариваемость медиВысокая тепло- и электропроводность меди затрудняют её электросварку (точечную и роликовую). Особенно это касается массивных изделий. Тонкие детали можно сварить вольфрамовыми электродами. Детали толщиной более 2-х мм можно сваривать нейтральным ацетилено-кислородным пламенем. Надежный способ соединения медных изделий – пайка мягкими и твердыми припоями. Подробно о сварке меди см www.weldingsite.com.ua
Медные сплавы
Техническая медь имеет низкую прочность и износоустойчивость, плохие литейные и антифрикционные свойства. Этих недостатков лишены сплавы на медной основе – латуни и бронзы. Правда эти улучшения достигаются за счет ухудшения тепло- и электропроводности.
Имеются особые случаи, когда нужно сохранить высокую электро- или теплопроводность меди, но придать ей жаропрочность или износоустойчивость.
При нагревании меди выше температуры рекристаллизации происходит резкое снижение предела текучести и твердости. Это затрудняет использование меди в электродах для контакной сварки. Поэтому, для этой цели используют специальные медные сплавы с хромом, цирконием, никелем, кадмием (БрХ, БрХЦр, БрКН, БрКд). Электродные сплавы сохраняют относительно высокую твердость и удовлетворительную электро- и теплопроводность при температурах сварочного процесса (порядка 600С ).
Жаропрочность достигается также легированием серебром. Такие сплавы (МС) имеют меньшую ползучесть при неизменной электро- и теплопроводности.
Для использования в подвижных контактах (коллекторные пластины, контактный провод) применяют медь с небольшим уровнем легирования магнием или кадмием БрКд, БрМг. Они имеют повышенную износоустойчивость при высокой электропроводности.
Для кристаллизаторов используют медь с добавками железа или олова. Такие сплавы имеют высокую теплопроводность при повышенной износоустойчивости.
Низколегированные марки меди по сути являются бронзами, но часто их относят к группе медного проката с соответствующей маркировкой (МС, МК, МЖ).
§3. Физические свойства меди.
Tплавления | Tкипения | Ρ | Rудельное |
1083 0C | 2877 0C | 8,96 г/cм3 | 1,63*10-8 ом*м |
а) Плотность и твердость.
Металлы подгруппы меди, как и щелочные металлы, имеют по одному свободному электрону на один ион-атом металла. Казалось бы, эти металлы не должны особенно сильно отличатся от щелочных. Но они, в отличие от щелочных металлов, обладают довольно высокими температурами плавления. Большое различие в температурах плавления между металлами этих подгрупп объясняется тем, что между ион-атомами металлов подгруппы меди почти нет свободного пространства, и они расположены более близко. Вследствие этого количество свободных электронов в единице объема, электронная плотность, у них больше. Следовательно, и прочность химической связи у них больше. Поэтому металлы подгруппы меди плавятся и кипят при более высоких температурах.
Металлы подгруппы меди обладают, по сравнению с щелочными металлами, обладают большей твердостью. Объясняется это увеличением электронной плотностью и более плотной компоновкой атомов в кристаллической решетке. Необходимо отметить, что твердость и прочность металлов зависят от правильности расположения ион-атомов в кристаллической решетке. В металлах, с которыми мы практически сталкиваемся, имеются различного рода нарушения правильного расположения ион-атомов, например, пустоты в узлах кристаллической решетки. К тому же металл состоит из мелких кристалликов (кристаллитов), между которыми связь ослаблена. В Академии Наук СССР была получена медь без нарушения в кристаллической решетке. Для этого очень чистую медь возгоняли при высокой температуре в глубоком вакууме на глубокую подложку. Медь получалась в виде небольших ниточек – “усов”. Как оказалось, такая медь в сто раз прочнее, чем обычная.
б) Цвет меди и её соединений.
Чистая медь обладает и другой интересной особенностью. Красный цвет обусловлен следами растворенного в ней кислорода. Оказалось, что медь, многократно возогнанная в вакууме (при отсутствии кислорода), имеет желтоватый цвет. Медь в полированном состоянии обладает сильным блеском.
При повышении валентности окраска меди и ее соединений темнеет, например, CuCl – белый, Cu2O – красный, CuCl + H2O – голубой, CuО – черный. Карбонаты характеризуются синим и зеленым цветом при условии содержания воды, чем обусловлен интересный практический признак для поисков.
в) Электропроводимость.
Медь обладает наибольшей (после серебра) электропроводимостью, чем и обусловлено её обширное применение в электронике.
г) Кристаллическая решетка.
Медь
кристаллизируется по типу централизованного
куба (рис 1).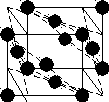
Рисунок 1. Кристаллическая решетка меди.
д) Изотопы.
Природная медь состоит из двух стабильных изотопов — 63Cu и 65Cu с распространённостью 69,1 и 30,9 атомных процентов соответственно. Известны более двух десятков нестабильных изотопов, самый долгоживущий из которых 67Cu с периодом полураспада 62 часа.
§4. Сплавы меди.
Медные сплавы — первые металлические сплавы, созданные человеком. Примерно до середины XXв. по мировому производству медные сплавы занимали 1-е место среди сплавов цветных металлов, уступив его затем алюминиевым сплавам. Со многими элементами медь образует широкие области твёрдых растворов замещения, в которых атомы добавки занимают места атомов меди в гранецентрированной кубической решётке. Медь в твёрдом состоянии растворяет до 39 % Zn, 15,8 % Sn, 9,4 % Al, a Ni — неограниченно. При образовании твёрдого раствора на основе меди растут её прочность и электросопротивление, снижается температурный коэффициент электросопротивления, может значительно повыситься коррозионная стойкость, а пластичность сохраняется на достаточно высоком уровне.
В настоящее время существуют бесчисленные сплавы на основе меди, здесь я приведу три самые основные и распространенные в технике и быту сплавы:
а) Латунь
Латунь – это медный сплав с добавлением цинка. Цинк, содержание которого в составе может доходить до 40%, повышает прочность и пластичность сплава. Наиболее пластична латунь, с долей цинка около 30%. Она применяется для производства проволоки и тонких листов. В состав также могут входить железо, олово, свинец, никель, марганец и другие компоненты. Они повышаю коррозийную устойчивость и механические свойства сплава. Латунь хорошо подвергается обработке: сварке и прокатке, отлично полируется. Широкий диапазон свойств, низкая себестоимость, легкость в обработке и красивый желтый цвет делают латунь наиболее распространенным медным сплавом с большой областью применения.
б) Бронза
Бро́нзы — сплав меди, обычно с оловом в качестве основного легирующего компонента, но к бронзам также относят медные сплавы с алюминием, кремнием, бериллием, свинцом и другими элементами, за исключением цинка (это латунь) и никеля. Как правило в любой бронзе в незначительных количествах присутствуют добавки: цинк, свинец, фосфор и др.
Традиционную оловянную бронзу человек научился выплавлять ещё в начале Бронзового века и очень длительное время она широко использовалась; даже с приходом века железа бронза не утрачивала своей важности (в частности вплоть до XIX века пушки изготавливались из пушечной бронзы)
Самые широко применимые бронзы это: кремниевые бронзы, бериллиевые бронзы, кремниевые бронзы, хромовые бронзы, но, безусловно, самой известной и наиболее применимой является оловянная бронза.
в) Медно-никелевые сплавы
Сплавы на основе меди, содержащие никель в качестве главного легирующего элемента – Мельхиор, Нейзильбер (сплав меди с 5—35% Ni и 13—45% Zn). Никель образует с медью непрерывный ряд твёрдых растворов. При добавлении никеля к меди возрастают её прочность и электросопротивление, снижается температурный коэффициент электросопротивления, сильно повышается стойкость против коррозии. Медно-никелевые сплавы хорошо обрабатываются давлением в горячем и холодном состоянии.
| Табл. 2. Значения температурного коэффициента линейного расширения меди при различных температурах | |||||
| t, К | α х 10 6 , К -1 | t, К | α х 10 6 , К -1 | t, К | α х 10 6 , К -1 |
| 200 | 15,2 | 450 | 17,6 | 900 | 20,9 |
| 220 | 15,6 | 500 | 17,9 | 950 | 21,4 |
| 240 | 15,9 | 550 | 18,3 | 1000 | 21,8 |
| 260 | 16,2 | 600 | 18,7 | 1050 | 22,3 |
| 280 | 16,5 | 700 | 19,4 | 1100 | 22,8 |
| 300 | 16,7 | 750 | 19,7 | 1150 | 23,3 |
| 350 | 17,0 | 800 | 20,1 | 1200 | 23,8 |
| 400 | 17,3 | 850 | 20,5 | 1250 | 24,4 |
Теплопроводность меди λ существенно снижают примеси и легирующие элементы (рис. 4).
Рис. 4. Влияние содержания элементов на теплопроводность меди
Теплопроводность меди разных марок при 20°С составляет:
Марка λ , Вт(м * К)
П овышение температуры меди приводит к уменьшению ее теплопроводности (табл. 3. ).
| Табл. 3. Значения теплопроводности λ меди при различных температурах | |||||||||
| t, К | λ, Вт/(м*К) | t, К | λ, Вт/(м*К) | t, К | λ, Вт/(м*К) | t, К | λ, Вт/(м*К) | t, К | λ, Вт/(м*К) |
| 100 | 500 | 350 | 393 | 600 | 382 | 850 | 376 | 1100 | 349 |
| 150 | 435 | 400 | 391 | 650 | 379 | 900 | 364 | 1150 | 345 |
| 200 | 414 | 450 | 383 | 700 | 376 | 950 | 360 | 1200 | 342 |
| 250 | 403 | 500 | 387 | 750 | 372 | 1000 | 356 | 1250 | 338 |
| 300 | 398 | 550 | 385 | 800 | 370 | 1050 | 353 | 1300 | 334 |
Влияние температу ры на физические свойства меди на примере М0 показано в табл. 4.
Главная страница » Медь: свойства характеристики применение металла

Медь (производная греческого слова «Κύπρος») — материал, с которым приходится сталкиваться повсеместно в обычной жизни, даже не замечая и не задумываясь о контакте. Каждый раз, применяя какое-то электрическое устройство, например, пылесос или стиральную машину, пользователь прямо или косвенно контактирует с медью. Универсальный металл – неотъемлемая часть высокотехнологичных гаджетов и машин — от электронных микроскопов и мобильных телефонов, до простых пищевых кастрюль. Примерно 10 000 лет насчитывает вся история существования меди с момента обнаружения этого металла на Кипре. Этого вполне достаточно, чтобы уделить внимание популярному металлу.
Что такое медь в общем смысле слова?
Медь физически выглядит мягким металлом, имеющим красновато-оранжевый окрас. Особенность металла хорошая электрическая проводимость и тепловой обмен. Среди распространённых химических элементов, присутствующих в земной коре, медь занимает 25 место своеобразного рейтинга.
 Медные прутки разного диаметра наглядно демонстрируют внешний вид материала и качество структуры в целом. Однако это наиболее простые изделия из всех возможных
Медные прутки разного диаметра наглядно демонстрируют внешний вид материала и качество структуры в целом. Однако это наиболее простые изделия из всех возможных
Ведущим поставщиком меди в мире является Чили (примерно треть мировой добычи). Также список достаточно мощных источников добычи дополняют:
- Польша
- Англия
- Канада
- Перу
- Соединенные Штаты
- Замбия
- Австралия
Если сравнивать с алюминием и титаном, медь при добыче нередко встречается в необработанном виде, смешанном в породах с другими металлами — золотом, серебром, свинцом.
Также встречаются медьсодержащие минералы — халькоцит, халькопирит, борнит. Несмотря на объёмную добычу меди из недр земли, достаточно большие объёмы производятся методом переработки материалов, к примеру, устаревшего электрооборудования.
Процесс производства химического элемента
Как правило, концентрация меди в руде отмечается на уровне не более 4%. Подавляющее большинство руды составляют отходы. Используются различные процессы для разделения меди и отходов.
Точный характер процесса переработки зависит от металлов и других примесей, смешанных с медью, а также от требований к чистоте конечного продукта. Процесс очистки обычно охватывает несколько этапов разной сложности. Каждая стадия удаления примесей даёт большую концентрацию и улучшение чистоты меди.
 Примерно таким выглядит природный медный минерал, встречающийся в процессе добычи популярного химического элемента. Подобные образования отличаются более высоким содержанием вещества
Примерно таким выглядит природный медный минерал, встречающийся в процессе добычи популярного химического элемента. Подобные образования отличаются более высоким содержанием вещества
Типичный процесс начинается с функции дробления руды с последующим приготовлением суспензии путём добавления воды. Суспензия загружается в резервуары, смешивается с воздухом и маслянистыми химикатами. Это примеси, помогающие отделить частицы «Cuprum» от других присутствующих минералов.
Затем оставшуюся руду нагревают в большой плавильной печи, где сжигаются оставшиеся примеси. После термообработки остаётся материал — медный штейн, по меньшей мере, содержащий 50% меди.
На следующем этапе проводится второй процесс нагревания медного штейна с кремнеземом и воздухом с целью ещё более «тонкого» удаления отходов. Остаётся переработанный материал — черновая медь, обладающий чистотой более 97%.
Максимально возможную чистоту меди получают электролизом, когда электрический ток пропускается через раствор, содержащий медь. Медь, полученная электролизом, характерна степенью чистоты на уровне 99,9% — идеальный материал для проводки электричества.
Физические свойства меди
Физически медь очень хорошо проводит тепло и электричество. Материал относительно мягкий и легкий. Металл не ржавеет, но подвержен эффекту окисления на открытом воздухе.
 Традиционное применение медных проводников в конструкции электрических двигателей. Вместе с тем существует огромный ассортимент медных проводов, в том числе изолированных, скрученных, многожильных, специальных и других
Традиционное применение медных проводников в конструкции электрических двигателей. Вместе с тем существует огромный ассортимент медных проводов, в том числе изолированных, скрученных, многожильных, специальных и других
Структура материала допускает значительное усложнение посредством образования более длинных кристаллов. Этим увеличивается общая структура с образованием нечто подобного «арматуре» железобетона.
Какие существуют соединения «Cuprum»?
Несмотря на слабую реакционную способность меди, этот металл допускает создание широкого спектра полезных соединений и сплавов. Когда атомы меди соединяется с атомами других металлов, химически отмечаются два совершенно разных поведения:
- Образуются соединения Cuprum I
- Образуются соединения Cuprum II
Двумя наиболее важными соединениями меди являются сульфат меди (II) ярко-синего цвета, используемый в сельском хозяйстве и в медицине, а также хлорид меди (II), применяемый в качестве антисептика древесины, а также в полиграфической и красильной индустрии.
Как получают медные сплавы?
Получение медных сплавов выполняется путём смешивания с одним или несколькими другими металлами. В результат получается новый материал, сочетающий лучшие свойства. Самые известные медные сплавы — бронза и латунь. Металл бронза — сплав, где основой структуры являются медь и олово. Иногда добавляется цинк или свинец.
 Продукт на основе никель-медного сплава характеризуется не только улучшенными механическими свойствами, но также демонстрирует улучшенный внешний вид
Продукт на основе никель-медного сплава характеризуется не только улучшенными механическими свойствами, но также демонстрирует улучшенный внешний вид
Бронза существенно твёрже, прочнее и устойчивее (с точки зрения коррозии) чистой меди. Разновидности бронзы отличаются разными пропорциями отмеченных ингредиентов в структуре. Например, твердая бронза для изготовления статуй обычно содержит:
Латунь также представляет сплав меди и обычно содержит 10-50% цинка, в зависимости от предназначения к использованию.
Для чего применим медный металл?
Конкретное применение материалов целиком и полностью зависит от физических и химических свойств, которыми эти материалы обладают. Собственно, в этом кроется суть науки, именуемой материаловедением. Что касается конкретно меди, мягкий, ковкий и пластичный материал проводит электричество и тепло, имеет приятный внешний вид.
Вот почему две основных сферы применения меди – это строительство зданий и производство электрического (электронного) оборудования. Крайне сложно найти электрический (электронный прибор), конструкция которого не содержит меди.
 Бытовые и хозяйственные аксессуары, предметы искусства и поделок достаточно часто выполняются на основе медного материала. Получаются очень интересные привлекательные изделия
Бытовые и хозяйственные аксессуары, предметы искусства и поделок достаточно часто выполняются на основе медного материала. Получаются очень интересные привлекательные изделия
Поскольку «Cuprum» хороший проводник тепла, этот материал также широко используется в производстве аксессуаров бытовой сферы. Классический пример — кастрюли с медным дном. Учитывая, что металл не ржавеет, актуальным видится применение в качестве покрытий (например, как в своё время для покрытия днищ кораблей). Наконец, производство денег никак не обходится без меди.
Особенности присущие популярному химическому элементу
Практически идеальным электрическим проводником считается именно медный материал. Лучшие свойства проводимости демонстрирует только серебро. Однако по сравнению с медью, проводник серебра – это достаточно дорогое удовольствие.
Поэтому серебряные электрические линии транспорта тока применяются очень ограниченно, в схемах устройств, предъявляющих особые требования к передаче электричества.
Многие живые организмы и природные растения нуждаются в некоторых количествах «Cuprum». Такая природная «добавка» помогает в прямом смысле выживать растениям и организмам.
Если среди живых организмов выделить именно человека, определённые количества меди, поступающей в организм, способствует образованию гемоглобина, ответственного за транспорт кислорода в крови.
Периодическая таблица в KnowledgeDoor
Ссылки (Щелкните рядом со значением выше, чтобы увидеть полную информацию о цитировании для этой записи)
Allred, A. L. «Значения электроотрицательности на основе термохимических данных». Журнал неорганической и ядерной химии, том 17, номер 3-4, 1961 г., стр. 215–221. DOI: 10.1016 /
Allred, A. L., and E. G. Rochow. «Шкала электроотрицательности, основанная на электростатической силе». Журнал неорганической и ядерной химии, том 5, номер 4, 1958 г., стр.264–268. DOI: 10.1016 /
Андерс, Эдвард и Николас Гревесс. «Изобилие элементов: метеоритное и солнечное». Geochimica et Cosmochimica Acta, том 53, номер 1, 1989 г., стр. 197–214. DOI: 10.1016 / -X
Андерсен, Т., Х. К. Хауген и Х. Хотоп. “Энергии связи в атомной Отрицательные ионы: III. “Journal of Physical and Chemical Reference Data, том 28, номер 6, 1999 г., стр. 1511–1533.
Assael, Marc J., Агни Э. Калива, Константинос Д. Антониадис, Р. Майкл Баниш, Иван Эгри, Цзянтао Ву, Эрхард Кашниц и Уильям А. Уэйкхэм. «Справочные данные по плотности и вязкости жидкой меди и жидкого олова». Справочный журнал физических и химических данных, том 39, номер 3, 2010 г., стр. 033105–1–033105–8. doi: 10.1063 /
Болл, Дэвид У. “Элементная этимология: что в имени?” Журнал химического образования, том 62, номер 9, 1985 г., стр. 787–788. DOI: 10.1021 /
Barron, T.Х. К. и Г. К. Уайт. Теплоемкость и тепловое расширение при низких температурах. Нью-Йорк: Kluwer Academic / Plenum Publishers, 1999.
Барсан, Майкл Э., редактор. Карманный справочник NIOSH по химической опасности. Цинциннати, Огайо: NIOSH Publications, 2007.
Batsanov, S. S. “Ван-дер-Ваальсовые радиусы элементов”. Неорганические материалы, том 37, номер 9, 2001 г., стр. 871–885. См. Реферат
Bearden, J. A., and A. F. Burr. «Переоценка рентгеновских уровней атомной энергии». Обзоры современной физики, том 39,
номер 1, 1967, с.125–142. DOI: 10.1103 /
Бонди, А. «Ван-дер-Ваальс объемы и радиусы». Журнал физической химии, том 68, номер 3, 1964 г., стр. 441–451. DOI: 10.1021 /
Боуэн, Х. Дж. М. Экологическая химия элементов. Лондон: Academic Press, Inc., 1979.
Bratsch, Steven G. “Пересмотренные значения электроотрицательности Малликена: I. Расчет
и преобразование в единицы Полинга “. Журнал химического образования, том 65, номер 1, 1988 г., стр.34–41. DOI: 10.1021 /
Cardarelli, François. Справочник по материалам: краткий Настольный справочник, 2-е издание. Лондон: Springer – Verlag, 2008.
Кардона, М. и Л. Лей, редакторы. Фотоэмиссия в твердых телах I: общие принципы. Берлин: Springer-Verlag, 1978.
Clementi, E., and D. L. Raimondi. «Константы атомарного экранирования из функций SCF». Журнал химической физики, том 38, номер 11, 1963 г., стр. 2686–2689. DOI: 10.1063 /
Коэн, Э.Ричард, Дэвид Р. Лид и Джордж Л. Тригг, редакторы. Настольный справочник по физике AlP, 3-е издание. Нью-Йорк: Springer-Verlag New York, Inc., 2003.
Коннелли, Нил Г., Туре Дамхус, Ричард М. Хартсхорн и Алан Т. Хаттон. Номенклатура неорганической химии: Рекомендации IUPAC 2005. Кембридж: RSC Publishing, 2005.
Кордеро, Беатрис, Вероника Гомес, Ана Э. Платеро-Пратс, Марк Ревес, Хорхе Эчеверрия, Эдуард Кремадес, Флавиа Барраган и Сантьяго. “Новый взгляд на ковалентные радиусы.”Dalton Transactions, номер 21, 2008 г., стр. 2832–2838. Doi: 10.1039 /
Cronan, DS” Базальные металлические отложения восточной части Тихого океана “. Бюллетень Геологического общества Америки, том 87, номер 6, 1976 г., pp. 928–934. doi: 10.1130 /
de Podesta, Michael. Understanding the Properties of Matter, 2nd edition. London: Taylor & Francis, 2002.
Dronskowski , Ричард. Вычислительная химия твердого тела. Государственные материалы.Вайнхайм, Германия: WILEY-VCH Verlag GmbH & Co. KGaA, 2005.
Эббинг, Даррелл Д. и Стивен Д. Гаммон. Общая химия, 8-е издание. Бостон, Массачусетс: Компания Houghton Mifflin, 2005.
Эмсли, Джон. Строительные блоки природы: руководство по элементам от А до Я. Оксфорд: издательство Оксфордского университета, 2003.
Эмсли, Джон. Элементы, 3-е издание. Оксфорд: Издательство Оксфордского университета, 1998.
Файерстоун, Ричард Б. Таблица изотопов, 8-е издание, том 2. Под редакцией Вирджинии С.Ширли с помощниками редактора Корал М. Бэглин, С. Ю. Фрэнк Чу и Джин Зипкин. Нью-Йорк: John Wiley & Sons, Inc., 1996.
Fuggle, John C., and Nils Mårtensson. «Энергии связи на уровне ядра в металлах». Журнал электронной спектроскопии и родственных явлений, том 21, номер 3, 1980 г., стр. 275–281. DOI: 10.1016 /
Галассо, Фрэнсис С. Структура и свойства неорганических твердых тел. Oxford: Pergamon Press, 1970.
Ghosh, Dulal C., и Картик Гупта. “Новая шкала электроотрицательности
54 элемента периодической таблицы на основе поляризуемости атомов ». Журнал теоретической и вычислительной химии, том 5, номер 4, 2006 г., стр. 895–911. Doi: 10.1142 /
Гринвуд, Н. Н. и А. Эрншоу. Химия элементов, 2-е издание. Оксфорд: Баттерворт-Хайнеманн, 1997.
Гвин Уильямс. Энергии связи электронов. http: //
Хо, К. Ю., Р. У. Пауэлл и П. Э. Лили. «Теплопроводность элементов: всесторонний обзор». Справочный журнал физических и химических данных, том 3, приложение 1, 1974 г., стр. С I – 1 по I – 796.
Хо, Джо, Кент М. Эрвин и У. К. Линебергер. «Фотоэлектронная спектроскопия кластерных анионов металлов: Cu-n, Ag-n и Au-n». Журнал химической физики, том 93, номер 10, 1990 г., стр. 6987–7002. DOI: 10.1063 /
Höhne, G.W.H., W.F. Hemminger и H.-J. Фламмерсхайм. Дифференциальная сканирующая калориметрия, 2-е издание. Берлин: Springer – Verlag, 2003.
Хорват, А. Л. «Критическая температура элементов и периодическая система». Журнал химического образования, том 50, номер 5,
1973, стр. 335–336. DOI: 10.1021 /
Хухи, Джеймс Э., Эллен А. Кейтер и Ричард Л. Кейтер. Неорганическая химия: основы структуры и реакционной способности, 4-е издание. Нью-Йорк: издатели колледжа Харпер Коллинз, 1993.
Международная организация труда (МОТ). Международная карта химической безопасности меди. http: // 0006
0006
0006 .htm
Дженсен, Дж. Э., Р. Б. Стюарт, У. А. Таттл, Х. Брехна и А. Г. Проделл, редакторы. Избранные криогенные данные Брукхейвенской национальной лаборатории Ноутбук.БНЛ 10200-Р, т. 1, Брукхейвенская национальная лаборатория, август 1980 г.
Каксирас, Эфтимиос. Атомная и электронная структура твердых тел. Кембридж: Издательство Кембриджского университета, 2003.
Киттель, Чарльз. Введение в физику твердого тела, 8-е издание. Хобокен, Нью-Джерси: John Wiley & Sons, Inc., 2005.
Краузе, М. О. «Атомные радиационные и безызлучательные выходы для K- и L-оболочек». Справочный журнал физических и химических данных, том 8, номер 2, 1979 г., стр. 307–327.
Ли, Ю.-H. И J. E. Schoonmaker. «Химический состав и минералогия морских отложений». С. 1–36 в Отложения, диагенез и осадочные породы. Отредактированный Фредом Т. Маккензи. Oxford: Elsevier Ltd., 2005.
Liboff, Ричард Л. Введение в квантовую механику, 3-е издание. Ридинг, Массачусетс: Addison Wesley Longman, Inc., 1998.
Лиде, Дэвид Р., редактор. CRC Справочник по химии и физике, 88-е издание. Бока-Ратон, Флорида: Taylor & Francis Group, 2008.
Манн, Джозеф Б., Терри Л. Мик, Юджин Т. Найт, Джозеф Ф. Капитани и
Лиланд С. Аллен. «Энергии конфигурации элементов d-блока». Журнал Американского химического общества, том 122, номер 21, 2000 г., стр. 5132–5137. DOI: 10.1021 /
Мануэль, О., редактор. Происхождение элементов в Солнце Система: последствия наблюдений после 1957 г. Нью-Йорк: Kluwer Academic Publishers, 2000.
Мартин, В. К. «Электронная структура элементов». Европейский физический журнал C – Частицы и поля, том 15, номер 1–4, 2000 г., стр.78–79. DOI: 10.1007 /
Матула Р. А. «Удельное электрическое сопротивление меди, золота, палладия и серебра». Журнал физических и химических справочных данных, том 8, № 4, 1979, с. 1147–1298.
Макдонаф, У. Ф. “Композиционная модель ядра Земли”. стр. 547–568 в The Mantle and Core. Под редакцией Ричарда В. Карлсона. Oxford: Elsevier Ltd., 2005.
Mechtly, Eugene A. «Свойства материалов». С. 4–1–4–33 в Справочных данных для инженеров: радио, электроника, компьютер и связь.Мак Э. Ван
Валкенбург, отредактированный Венди М. Миддлтон. Woburn, MA: Butterworth-Heinemann, 2002. doi: 10.1016 /
Miessler, Gary L., and Donald A. Tarr. Неорганическая химия, 3-е издание. Река Аппер Сэдл, Нью-Джерси: Пирсон Прентис Холл, 2004.
Нэгл, Джеффри К. “Атомная поляризуемость и электроотрицательность”. Журнал Американского химического общества, том 112, номер 12, 1990 г., стр. 4741–4747. DOI: 10.1021 /
Национальный институт охраны труда и здоровья (NIOSH).Международная карта химической безопасности меди. http: //
Национальный институт охраны труда и здоровья (NIOSH). Реестр токсического действия химических веществ на медь. http: //
Николас, Дж. В. и Д. Р. Уайт. «Температура». С. 8–41 в Измерение термодинамических свойств одиночных фаз.Под редакцией А. Р. Х. Гудвина, В. А. Уэйкхема и К. Н. Марша. Амстердам: Elsevier Science, 2003.
Нуммила, Кай К., Юха Т. Туориниеми, Реко Т. Вуоринен, Ким Лефманн, Альберт Мец и Финн Б. Расмуссен. “Нейтронографические исследования ядерного магнитного упорядочения
в серебре. “Journal of Low Temperature Physics, volume 112, number 1-2, 1998, pp. 73–116. doi: 10.1023 /
Oja, A. S., and H. E. Viertiö.” Antiferromagnets with Anisotropic
Спин-спиновые взаимодействия: устойчивость структуры нулевого поля во внешнем поле.”Physical Review B, том 47, номер 1, 1993 г., стр. 237–253. Doi: 10.1103 /
Орем, У. Х. и Р. Б. Финкельман.” Формирование угля и геохимия “. С. 191–222 в Отложениях, диагенезе и осадочных породах. Отредактированный Фредом Т. Маккензи. Oxford: Elsevier Ltd., 2005.
Oxtoby, Дэвид У., Х. П. Гиллис и Алан Кэмпион. Принципы современной химии, 6-е издание. Бельмонт, Калифорния: Томсон Брукс / Коул, 2008.
Пальм, Х. и Х. Бир. «Метеориты и состав солнечной фотосферы.”стр. 204–206 в журнале Landolt – Börnstein – Group VI: Astronomy and Astrophysics. Под редакцией
Х. Х. Фойгт. Нью-Йорк: Springer – Verlag, 1993. doi: 10.1007 /
Палм, Х. и Хью Сент-К. О’Нил. «Космохимические оценки состава мантии». стр. 1–38 в The Mantle and Core. Под редакцией Ричарда В. Карлсона. Оксфорд: Elsevier Ltd., 2005.
Полинг, Линус. Природа химической связи, 3-е издание. Итака, Нью-Йорк: Издательство Корнельского университета, 1960.
Пирсон, Ральф Г.«Абсолютная электроотрицательность и твердость: приложение к неорганической химии». Неорганическая химия, том 27, номер 4, 1988 г., стр. 734–740. DOI: 10.1021 /
Pekka Pyykkö. Самосогласованные, ковалентные радиусы 2009 г. http: //
Престон-Томас, Х. «Международная температурная шкала 1990 г. (ITS-90)». Метрология, том 27, номер 1, 1990 г., стр.3–10. DOI: 10.1088 /
Pyykkö, Pekka и Michiko Atsumi. «Ковалентные радиусы молекул с двойной связью для элементов Li-E112». Химия – Европейский журнал, том 15, номер 46, 2009 г., стр. 12770–12779. DOI: 10.1002 /
Pyykkö, Pekka и Michiko Atsumi. «Молекулярные ковалентные радиусы одинарной связи для элементов 1-118». Химия – Европейский журнал, том 15, номер 1, 2009 г., стр. 186–197.doi: 10.1002 /
Pyykkö, Pekka, Sebastian Riedel и Michael Patzschke. «Ковалентные радиусы с тройной связью». Химия – Европейский журнал, том 11, номер 12, 2005 г., стр. 3511–3520. DOI: 10.1002 /
Рорер, Грегори С. Структура и связь в кристаллических материалах. Кембридж: Cambridge University Press, 2001.
Самсонов Г.В., редактор. Справочник по физико-химическим свойствам элементов. Нью-Йорк: Plenum Publishing Corporation, 1968.
Сандерсон Р. Т. Простые неорганические вещества. Малабар, Флорида: Роберт Э. Кригер Publishing Co., Inc., 1989.
Сандерсон Р. Т. «Принципы электроотрицательности: Часть I. Общая природа». Журнал химического образования, том 65, номер 2, 1988 г., стр. 112–118. DOI: 10.1021 /
Sansonetti, J. E., and W. C. Martin. “Справочник основных данных атомной спектроскопии”. Справочный журнал физических и химических данных, том 34, номер 4, 2005 г., стр. 1559–2259.DOI: 10.1063 /
Шеннон Р. Д. «Пересмотренные эффективные ионные радиусы и систематические исследования межатомных расстояний в галогенидах и халькогенидах». Acta Crystallographica Раздел A, том 32, номер 5, 1976 г., стр. 751–767. DOI: 10.1107 /
Силби, Роберт Дж., Роберт А. Олберти и Мунги Г. Бавенди. Физическая химия, 4-е издание. Хобокен, Нью-Джерси: John Wiley & Sons, Inc., 2005.
Сингман, Чарльз Н. «Атомный объем и аллотропия элементов.”Журнал химического образования, том 61, номер 2, 1984 г., стр. 137–142. Doi: 10.1021 /
Слейтер, Дж. К.” Атомные радиусы в кристаллах. “Журнал
Химическая физика, том 41, номер 10, 1964, стр. 3199–3204. doi: 10.1063 /
Смит, Дерек В. «Электроотрицательность в двух измерениях: переоценка и разрешение парадокса Пирсона-Полинга». Журнал химической
Образование, том 67, номер 11, 1990 г., стр. 911–914. DOI: 10.1021 /
Смит, Дерек В.Неорганические вещества: прелюдия к изучению описательной неорганической химии. Кембридж: Кембриджский университет Press, 1990.
Суханов, Анна Х., редактор. Словарь английского языка американского наследия, 3-е издание. Бостон: Houghton Mifflin Company, 1992.
Стюарт, Г. Р. «Измерение низкотемпературной удельной теплоемкости». Review of Scientific Instruments, том 54, номер 1, 1983 г., стр. 1–11. DOI: 10.1063 /
Стюарт, Г. Р. “Измерение низкотемпературной удельной теплоемкости.”Review of Scientific Instruments, том 54, номер 1, 1983, стр. 1–11. Doi: 10.1063 /
Сахар, Джек и Арлин Масгроув.” Уровни энергии меди, от Cu I до Cu XXIX “. Справочник по физическим и химическим веществам Данные, том 19, номер 3, 1990 г., стр. 527–616.
Тари А. Удельная теплоемкость вещества при низких температурах. Лондон: Imperial College Press, 2003.
Вайнштейн, Борис К., Владимир М. Фридкин и Владимир Л. Инденбом. Структура кристаллов, 2-е издание.Современная кристаллография 2. Под ред. Б. К. Вайнштейна, А. А. Чернова, Л. А. Шувалова. Берлин: Springer-Verlag, 1995.
.Фойгт, Х. Х., редактор. Ландольт – Бернштейн — Астрономия и астрофизика VI группы. Берлин: Springer – Verlag, 1993.
Waber, J. T., and Don T. Cromer. «Радиусы орбит атомов и ионов». Журнал химической физики, том 42, номер 12, 1965, стр. 4116–4123. DOI: 10.1063 /
Уолдрон, Кимберли А., Эрин М. Ферингер, Эми Э. Стриб, Дженнифер Э.Троски и Джошуа Дж. Пирсон. «Проценты скрининга на основе эффективного ядерного заряда Слейтера как универсальный инструмент для обучения периодическим тенденциям». Журнал химического образования, том 78, номер 5, 2001 г., стр. 635–639. DOI: 10.1021 /
Уайт Г. К. и Дж. Г. Коллинз. «Термическое расширение меди, серебра и золота при низких температурах». Журнал физики низких температур, том 7, номер 1-2, 1972, стр. 43–75. DOI: 10.1007 /
Визер, Майкл Э., и Тайлер Б. Коплен. «Атомный вес элементов 2009 (Технический отчет ИЮПАК)». Чистая и прикладная химия, том 83, номер 2, 2011 г., стр. 359–396. DOI: 10.1351 /
Yaws, Carl L. Справочник физических свойств Yaws для углеводородов и химикатов. Хьюстон, Техас: издательство Gulf Publishing Company, 2005.
.| Атомный номер | 29 | |||
| Атомный вес | 63,54 | |||
| Структура решетки: гранецентрированная кубическая | ||||
| Плотность | ||||
| Стандартное значение IEC (1913) | 8,89 | г / см 3 | 0.321 | фунт / дюйм 3 |
| Типичное значение при 20 ° C | 8,92 | г / см 3 | 0,322 | фунт / дюйм 3 |
| при 1083 ° C (твердый) | 8,32 | г / см 3 | 0,300 | фунт / дюйм 3 |
| при 1083 (жидкость) | 7,99 | г / см 3 | 0,288 | фунт / дюйм 3 |
| Температура плавления | 1083 | ° С | 1981 | ° F |
| Температура кипения | 2595 | ° С | 4703 | ° F |
| Линейный коэффициент теплового расширения при: | ||||
|---|---|---|---|---|
| -253 ° C, -423 ° F | 0.3 х 10 -6 | ° С | 0,17 x 10 -6 | ° F |
| -183 ° C, -297 ° F | 9,5 x 10 -6 | ° С | 5,28 x 10 -6 | ° F |
| от -191 ° C до 16 ° C, -312-61 ° F | 14,1 х 10 -6 | ° С | 7,83 х 10 | ° F |
| от 25 ° C до 100 ° C, 77-212 ° F | 16,8 х 10 -6 | ° С | 9.33 х 10 -6 | ° F |
| от 20 ° C до 200 ° C, 68-392 ° F | 17,3 х 10-6 | ° С | 9,61 x 10 -6 | ° F |
| от 20 ° C до 300 ° C, 68-572 ° F | 17,7 x 10 -6 | ° С | 9,83 x 10 -6 | ° F |
| Удельная теплоемкость (теплоемкость) при: | ||||
| -253 ° С.-425 ° F ( | ° F)0,013 | Дж / г ° C | 0,0031 | БТЕ / фунт ° F |
| -150 ° C, -238 ° F | 0,282 | Дж / г ° C | 0,0674 | БТЕ / фунт ° F |
| -50 ° C, -58 ° F | 0,361 | Дж / г ° C | 0,0862 | БТЕ / фунт ° F |
| 20 ° C, 68 ° F | 0,386 | Дж / г ° C | 0,0921 | БТЕ / фунт ° F |
| 100 ° C, 212 ° F | 0.393 | Дж / г ° C | 0,0939 | БТЕ / фунт ° F |
| 200 ° C, 392 ° F | 0,403 | Дж / г ° C | 0,0963 | БТЕ / фунт ° F |
| Теплопроводность при: | ||||
| -253 ° C, -425 ° F | 12,98 | Вт-см / см 2 · ° C | 750 | БТЕ / фут / фут 2 ч ° F |
| -200 ° C, -328 ° F | 5.74 | Вт-см / см 2 · ° C | 330 | БТЕ / фут / фут 2 ч ° F |
| -183 ° C, -297 ° F | 4,73 | Вт-см / см 2 · ° C | 270 | БТЕ / фут / фут 2 ч ° F |
| -100 ° C, -148 ° F | 4,35 | Вт-см / см 2 · ° C | 252 | БТЕ / фут / фут 2 ч ° F |
| 20 ° C, 68 ° F | 3,94 | Вт-см / см 2 · ° C | 227 | БТЕ / фут / фут 2 ч ° F |
| 100 ° C, 212 ° F | 3.85 | Вт-см / см 2 · ° C | 223 | БТЕ / фут / фут 2 ч ° F |
| 200 ° C, 392 ° F | 3,81 | Вт-см / см 2 · ° C | 220 | БТЕ / фут / фут 2 ч ° F |
| 300 ° C, 572 ° F | 3,77 | Вт-см / см 2 · ° C | 217 | БТЕ / фут / фут 2 ч ° F |
| Электропроводность (объем) при: | ||||
| 20 ° C, 68 ° F (отожженный) | 58.0-58,9 | МС / м (мОм · мм 2 ) | 100,0-101,5 | % МАКО |
| 20 ° C, 68 ° F (полностью холодная обработка) | 56,3 | МС / м (мОм · мм 2 ) | 97,0 | % МАКО |
| Удельное электрическое сопротивление (объем) при: | ||||
| 20 ° C, 68 ° F (отожженный) | 0,017241-0,0170 | Ом · мм 2 / м | 10.371-10.2 | Ом (круговых мил / фут) |
| 20 ° C, 68 ° F (отожженный) | 1,7241–1,70 | мкОм · см | 0,6788-0,669 | мкОм-дюйм |
| 20 ° C, 68 ° F (полностью холодная обработка) | 0,0178 | Ом · мм 2 / м | 10,7 | Ом (круговых мил / фут) |
| 20 ° C, 68 ° F (полностью холодная обработка) | 1,78 | мкОм · см | 0,700 | мкОм-дюйм |
| Удельное электрическое сопротивление (масса) при 20 ° C, 68 ° F (отожженный) | ||||
| Обязательный максимум | 0.15328 | Ом · г / м 2 | 875,4 | Ом · фунт / милю 2 |
| Температурный коэффициент электрического сопротивления (a) при 20 ° C ° F: Отожженная медь , 100% IACS (применимо от от -100 ° C до 200 ° C, от 212 ° F до 392 ° F) | 0,00393 | ° С | 0,00218 | ° F |
| Полностью холодная деформация Медь 97% IACS (применимо от 0 ° C до 100 ° C, 68-212 ° F) | 0.00381 | ° С | 0,00238 | ° F |
| Модуль упругости (растяжения) при 20 ° C :, 68 ° F | ||||
| Отожженный | 118 000 | МПа | 17 х 103 | KSi |
| Холодная обработка | 118 000–132 000 | МПа | 17-19 х 10 3 | KSi |
| Модуль жесткости (кручение) при 20 ° C, 68 ° F | ||||
| Отожженный | 44 000 | МПа | 6.4 х 10 3 | KSi |
| Холодная обработка | 44 000–49 000 | МПа | 6,4-7 x 10 3 | KSi |
| Скрытая теплота плавления | 205 | Дж / г | ||
| Электрохимический эквивалент для: | ||||
| Cu ++ | 0,329 | мг / ц | ||
| Cu + | 0.659 | мг / ц | ||
| Нормальный потенциал электрода (водородный электрод) для: | ||||
| Cu ++ | -0,344 | В | ||
| Cu + | -0,470 | В |
Стандарты и свойства: Металлургия сплавов на медной основе
Уильям Д. Нильсен-младший
Western Reserve Manufacturing Co., Inc.
На основные свойства медных сплавов во многом влияют свойства самой меди. Известно, что медь обладает определенными уникальными качествами, которые делают ее лучшим инженерным материалом для подшипников. Это:
- Высокая теплопроводность
- Превосходная пластичность и вязкость в широком диапазоне температур
- Превосходная коррозионная стойкость в различных средах
Атомная структура меди
Все три перечисленных выше качества напрямую связаны со структурой и поведением структуры меди в атомном масштабе.
Рис. 1. Модель гранецентрированной кубической кристаллической структуры меди с одной элементарной ячейкой. Расстояние между центрами угловых атомов составляет 3,6 ангстрем (ссылка 1). Атом меди очень похож на атом золота или серебра, которые вместе с медью составляют группу в периодической таблице элементов. Всем известна прекрасная электропроводность меди, которая является следствием атомной структуры меди. Внутри решетки атомов меди облако свободных электронов является единственным доступным для передачи электрического тока.Это же облако электронов также увеличивает эффективную передачу тепловой энергии.Твердая медь может быть описана как расположение атомов меди в гранецентрированной кубической (ГЦК) конфигурации. Атом меди находится в каждом углу и в центре каждой грани куба, как показано на рис. 1 . Это элементарная ячейка, которая повторяется в трехмерном пространстве, составляя кристаллическую структуру металла.
Атомы удерживаются на месте в структуре за счет энергии атомного притяжения между ними.Именно это гранецентрированное кубическое расположение атомов придает меди ее высокую пластичность и прочность. Все металлы деформируются за счет механизма, называемого скольжением. Когда происходит скольжение, сила, действующая на металл, заставляет атомы скользить друг мимо друга группами. В медной ГЦК-структуре это движение происходит предпочтительно в любом или во всех трех направлениях вдоль определенной геометрической плоскости атомов в решетке, как показано на , рис. 2, .
Рис. 2. Единица ГЦК меди с удаленным угловым атомом, чтобы показать плоскость скольжения, на которой происходит преимущественная деформация.Это место воплощает самую плотную упаковку атомов, которая возможна геометрически (Ссылка 1). В медной ячейке таких плоскостей четыре. Если движение может происходить в трех направлениях на всех четырех плоскостях, существует двенадцать возможностей возникновения скольжения. Оказывается, это максимальное количество возможностей скольжения в любой металлической конструкции. Чем больше вероятность того, что металл может подвергнуться значительному скольжению, тем больше вероятность его деформации, а не разрушения и разрушения. Следовательно, медь обладает превосходной пластичностью и вязкостью, а также устойчива к усталости и ползучести.Дополнительным преимуществом является то, что медь, поскольку это гранецентрированная структура, не страдает охрупчиванием при низких (минусовых) температурах; явление, обычное для других кристаллических структур.Сочетание электронной и кристаллографической структур меди придает ей превосходную устойчивость к коррозии. Облако свободных электронов легко доступно для образования когерентных пленок на поверхности металла, которые защищают решетку от дальнейшей коррозии.
ГЦК-структура, образующая плоскости скольжения, придает этим самым плоскостям еще одну характеристику.Атомы на плоскостях скольжения упакованы настолько близко друг к другу, насколько это возможно в любой металлической системе (, рис. 2, ). Такое эффективное расположение атомов упаковывает большую часть материи в определенное пространство (что, кажется, знают пчелы, когда строят соты). Ионам водорода очень трудно найти свой путь через небольшие промежутки между атомами и вызвать коррозионное растрескивание под напряжением, за исключением наиболее агрессивных сред.
Мы видели, как медь, основной металл для литой бронзы, в атомном масштабе придает важные характеристики качественным материалам подшипников.Но подшипники изготавливаются не из чистой меди, а из широкого диапазона медных сплавов, которые сейчас доступны. Каждый из этих сплавов улучшает характеристики чистой меди и дополнительно адаптирует новый материал к конкретным условиям окружающей среды. Давайте рассмотрим некоторые из наиболее распространенных систем сплавов в отношении металлургии материала и его назначения в конструкции подшипников.
Сплавы из литой бронзы
Подшипниковые марки литой бронзы металлургически можно разделить на три категории:
- Однофазные твердые сплавы
- Сплавы полифазные
- Композиционные материалы
Чтобы понять характеристики различных сплавов, мы должны сначала понять, что происходит с основной структурой меди при добавлении небольших количеств легирующих металлов.Реакции происходят во время затвердевания и охлаждения сплавов из их расплавленного состояния.
Проще говоря, окончательное расположение легирующих металлов относительно нормальной ГЦК-решетки меди определяет свойства материала сплава.
Легирующие металлы находят свое место в решетке меди тремя основными способами:
- Замещают атомы меди в ГЦК решетке.
- Они соединяются с медью и образуют локализованные области (фазы), в которых кристаллическая структура имеет форму, отличную от кристалла меди с ГЦК-решеткой.
- Они отклоняются затвердевающей решеткой меди, но остаются в кристаллах сплава по мере их замораживания и роста.
В результате исследований было получено графическое изображение того, как реагируют простые бинарные системы сплавов. Такое представление называется фазовой диаграммой. Фазовые диаграммы некоторых бинарных систем, относящихся к бронзе, показывают поведение легирующих элементов, которое обычно приводит к одному из трех случаев, упомянутых ранее. На диаграмме равновесия медь-олово (, рис. 3, ) показаны случаи (1) и (2).
Рис. 3. Равновесная фазовая диаграмма медь-олово (Ссылка 2).Дело (1) – Замена
Рис. 4. Микроструктура однофазного (альфа) сплава медь-олово (88Cu-8Sn-4Zn). Структура показывает линии скольжения. Обратите внимание также на следы дельта-фазы (более темные острова) (ссылка 2). Ссылаясь на Фигуру 3, при содержании олова менее 11% (например, при 8% олова) видно, что сплав при охлаждении затвердевает в определенном диапазоне температур, становясь полностью твердым, когда температура опускается ниже примерно 850 ° C.В равновесных условиях медленного охлаждения образующаяся твердая фаза представляет собой гранецентрированный кубический кристалл (альфа-фаза). Атомы олова замещают непосредственно в решетке атомы меди. Атомы олова фактически усиливают чистую медь, потому что они деформируют решетку, то есть изменяют обычное расстояние между атомами меди. В промышленных условиях довольно медленного затвердевания почти весь металл затвердевает в виде альфа-фазы (, рис. 4, ).Это явление замещения приводит к однофазному твердому раствору олова в меди. Кристаллическая структура, хотя и прочнее чистой меди из-за деформации решетки, все же имеет ГЦК-структуру. Следовательно, характеристики скольжения остаются очень хорошими. Таким образом, однофазные твердые сплавы меди сохраняют высокую пластичность, несмотря на очень значительное увеличение прочности. Такие материалы находят широкое применение в условиях, когда материал может подвергаться значительному напряжению, но разрушение может быть катастрофическим (например, арматура в системах морской воды ядерных реакторов).Примером такого однофазного промышленного сплава является сплав C
| C | |||
|---|---|---|---|
| Cu | 99,9 | 88,0 | |
| Sn | – | 8,0 | |
| Zn | – | 4,0 | |
| Т.С., тыс. Кв. | 28 | 45 | |
| Ю.С., кси | 8 | 23 | |
| Удлинение,% в 2 дюйма | 45 | 25 | |
| Твердость, BHN | 40 | 77 | |
| (Значения даны для непрерывно литого материала диаметром менее 3 дюймов). | |||
Корпус (2) – Полифазный
Если содержание олова увеличивается до 11% или более, некоторая часть альфа-фазы преобразуется при охлаждении металла ниже 400 ° C.Появляется новая фаза, вкрапленная в нормальные альфа-кристаллы с ГЦК. Эта фаза, называемая дельта, может быть сохранена в материале при довольно быстром охлаждении ( Рисунок 5, ).
Рисунок 5 . Микроструктура непрерывнолитого сплава оловянной бронзы СДельта-фаза (хотя по-прежнему в основном ГЦК) содержит гораздо больше олова по сравнению с медью, чем в альфа-фазе, и она очень твердая и прочная, но не обладает большой пластичностью. В лучших условиях он выглядит как мелкодисперсные островки по всей микроструктуре материала.Влияние этой второй фазы на механизм скольжения является драматическим, так как происходит закрепление плоскостей скольжения после небольшого движения. Но дельта-фаза также значительно увеличивает износостойкость материала, о чем свидетельствует значительное увеличение твердости. Популярные алюминиевые бронзовые сплавы (C95400 и C95500) и марганцевые бронзы (C86300 и C86400) приобретают высокую прочность и твердость аналогичным образом, хотя акторы различны. Тем не менее, эти свойства являются результатом дисперсии другой фазы (или фаз) в основной ГЦК решетке, причем почти во всех случаях дисперсная фаза намного тверже и прочнее, чем основная часть материала окружающей матрицы.Эти «искусственные неоднородности» в материале служат для закрепления плоскостей скольжения и ограничения их движения.
Эти материалы известны как многофазные сплавы и характеризуются более высокой прочностью, твердостью и износостойкостью, чем альфа-сплавы; но они обладают гораздо меньшей пластичностью, как показано в таблице ниже. В результате они лучше всего подходят для деталей поверхности управления, где размерная целостность наиболее важна, и для тяжелых нагрузок и ударных нагрузок на малых скоростях, например, подшипников шасси самолетов.
Дополнительной характеристикой многофазных сплавов является то, что их свойства могут значительно изменяться в зависимости от температуры по сравнению с однофазными материалами. Такие сплавы часто подвергаются термической обработке. Путем изменения микроструктуры сплава, как показано на диаграмме состояния равновесия, путем «замыкания» равновесия можно получить определенные свойства, которые отсутствуют в состоянии литья.
| Однофазный | Полифазный | |||
|---|---|---|---|---|
| C | C | |||
| C92500 | C95400 | |||
| Cu | 88 | 89 | 87 | 85 |
| Sn | 8 | 11 | 11 | |
| Пб | 1 | |||
| Zn | 4 | |||
| Al | 11 | |||
| Ni | 1 | |||
| Fe | 4 | |||
| Т.С., кси | 49 | 52 | 50 | 85 |
| Ю.С., кси | 23 | 29 | 25 | 35 |
| Удлинение,% в 2 дюйма | 25 | 18 | 20 | 18 |
| Твердость, BHN | 77 | 95 | 83 | 170 |
| (Значения указаны для непрерывнолитого материала менее 3 дюймов.диаметром, за исключением C95400, которые являются литыми.) | ||||
В любом случае, многофазные материалы, не содержащие значительного количества свинца, следует использовать только в качестве подшипников против стальных сопрягаемых поверхностей, которые сами закалены термической обработкой. В случае применения алюминиевой бронзы или марганцевой бронзы часто рекомендуется, чтобы вал был хромированным или изготовлен из биметаллического материала, аналогичного тому, который используется для валков сталелитейных станов.
Ящик (3) – композитные смеси
Рисунок 6. Равновесная фазовая диаграмма медь-свинец (ссылка 2). Наиболее широко используемые материалы для подшипников – это действительно композиты. По сути, они могут иметь однофазные или многофазные структуры, служащие матрицей вокруг частиц или глобул свободного свинца. Взглянув на фазовую диаграмму равновесия медь-свинец (, рис. 6, ), можно увидеть, что свинец почти полностью отвергается решеткой меди при замерзании. Тем не менее инженеры-металлурги и литейщики в равной степени приложили большие усилия для улавливания свинца между кристаллами материала на основе меди, когда эти кристаллы замерзают и растут, потому что полученный сплав создает очень тонкие подшипники.Типичная микроструктура, показывающая диспергированный свинец, показана на , рис. 7, .Сегодня можно производить материал на основе меди с содержанием свинца более 30%, при этом частицы свинца имеют микроскопические размеры. С другой стороны, если применение подшипника указывает на то, что более желательны более крупные частицы свинца, можно также производить сплав в этой форме.
Рисунок 7. Микроструктура непрерывнолитого сплава свинцовой оловянной бронзы С94100 (20% Pb).Указаны частицы свинца (ссылка 3).Свинец выполняет три важные функции подшипника, все из которых служат для защиты вала и улучшения производительности оборудования. Первостепенное значение имеет способность частиц свинца уменьшать коэффициент трения между подшипником и валом. Механизм, с помощью которого это достигается, весьма интересен. Частицы свинца могут быть срезаны с поверхности подшипника за счет микроскопических шероховатостей на поверхности вала. Стальной вал покрывается свинцом, который постепенно перераспределяется, заполняя углубления на валу.Как только это будет выполнено, коэффициент трения снова повысится лишь незначительно, как показано в таблице ниже (ссылка 4). Это же явление имеет дополнительное преимущество в том, что температура, развиваемая в точках контакта между подшипником и сопряженной частью, ограничивается температурой плавления провода 327, ° C). Очевидно, что это свойство свинцовых сплавов очень ценно при отсутствии смазки (запланированной или случайной) или если рабочая среда машины сама подвержена значительным перепадам температур, например, на самолетах или оборудовании арктических нефтяных месторождений.
| Коэффициент трения (скольжения) | |
|---|---|
| Сталь на меди | 0,9 |
| Сталь на C94300 (23% Pb) | 0,18 |
| Сталь на C94300 после длительного использования | 0,30 |
| Сталь на стали | 1,00 |
Вторая важная функция свинца – поглощать грязь, которая попадает в поверхность раздела фаз, хотя этой проблемы можно избежать за счет конструкции должным образом герметичных подшипников, когда это возможно.
В-третьих, свинцовые сплавы, имеющие несколько меньшую прочность, чем сплавы медь-олово без свинца, и гораздо более низкую прочность, чем сплавы медь-алюминий или медь-цинк, демонстрируют высокую степень совместимости. То есть подшипник будет регулировать свою форму, чтобы допустить плохую центровку или вибрацию. Эта характеристика, в сочетании с характеристиками, описанными ранее, позволяет сказать, что свинцовые сплавы будут очень хорошо «изнашиваться», что особенно желательно для червячных передач, чтобы назвать один пример.Свинецсодержащие бронзы также легко обрабатываются.
Инженер должен напоминать себе, что эти сплавы не так прочны, как неэтилированные материалы, и при этом они не демонстрируют такого большого сопротивления ударам и последующей усталости, ведущей к разрушению. Однако одно утешительное соображение состоит в том, что полный отказ подшипника вряд ли приведет к разрушению вала или заклиниванию машины из-за «мягкости» этих сплавов.
Выбрав подходящую матрицу, в которую будут отливаться частицы свинца, инженер может выбрать из довольно широкого диапазона прочности материала, совместимого с умеренными и легкими нагрузками и высокими скоростями, как показано в таблице ниже.Значения указаны для непрерывного литья диаметром менее 3 дюймов.
| C83600 | C93200 | C93700 | C93800 | C94300 | |
|---|---|---|---|---|---|
| Cu | 85 | 83 | 80 | 78 | 70 |
| Sn | 5 | 7 | 10 | 7 | 5 |
| Пб | 5 | 7 | 10 | 15 | 25 |
| Zn | 5 | 3 | |||
| Т.С., кси | 45 | 45 | 41 | 34 | 27 |
| Ю.С., кси | 21 | 24 | 24 | 23 | 13 |
| Удлинение,% в 2 дюйма | 28 | 16 | 10 | 12 | 15 |
| Твердость, BHN | 72 | 72 | 80 | 62 | 48 |
Свойства литой бронзы
Давайте теперь рассмотрим семейства подшипниковых бронзовых сплавов с помощью двух таблиц, в которых сравниваются некоторые из их наиболее важных инженерных свойств. Таблица 1 обобщает химический состав и свойства применения. Таблица 2 показывает наиболее распространенные применения этих материалов и их рабочие характеристики в тех областях применения, в которых они находят наибольшее применение.
| Состав% | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Семейство сплавов | Cu | Sn | Пб | Zn | Ni | Fe | млн | Al | |
| Красная латунь | |||||||||
| C84400 | 81 | 3 | 7 | 9 | |||||
| C83600 | 85 | 5 | 5 | 5 | |||||
| Олово-свинцовая бронза | |||||||||
| C93200 | 83 | 7 | 7 | 3 | |||||
| C93700 | 80 | 10 | 10 | ||||||
| Олово бронза с высоким содержанием свинца | |||||||||
| C93800 | 78 | 7 | 15 | ||||||
| C94300 | 70 | 5 | 25 | ||||||
| Олово бронза | |||||||||
| C | 88 | 8 | 4 | ||||||
| C | 88 | 10 | 2 | ||||||
| C | |||||||||
| 89 | 11 | ||||||||
| C92500 | 87 | 11 | 1 | 1 | |||||
| C92700 | 88 | 10 | 2 | ||||||
| C92900 | 84 | 10 | 2.5 | 3,5 | |||||
| C94700-HT ** | 88 | 5 | 2 | 5 | |||||
| Алюминиевая бронза | |||||||||
| C95400 | 85 | 4 | 11 | ||||||
| C95400-HT | 85 | 4 | 11 | ||||||
| C95500 | 81 | 4 | 4 | 11 | |||||
| C95500-HT | 81 | 4 | 4 | 11 | |||||
| Марганцевая бронза | |||||||||
| C86300 | 63 | 25 | 3 | 3 | 6 | ||||
| C86400 | 59 | 1 | 40 | ||||||
| * БТЕ / фут2 / фут / час / фут ** HT – термообработанный | |||||||||
| Свойства непрерывного литья (типовые) | ||||||||
|---|---|---|---|---|---|---|---|---|
| Семейство сплавов | Т.С., тыс. Фунтов | Ю.С., тыс. Фунтов стерлингов | удлинн., % | BHN | Обрабатываемость Индекс | Компрессионный Y.S., тыс. Фунтов на квадратный дюйм | Thermal Проводимость * | |
| Красная латунь | ||||||||
| C84400 | 37 | 16 | 23 | 55 | 90 | 28 | 41 | |
| C83600 | 45 | 21 | 18 | 72 | 100 | 34 | 41 | |
| Олово-свинцовая бронза | ||||||||
| C93200 | 45 | 24 | 16 | 72 | 100 | 30 | 33 | |
| C93700 | 41 | 24 | 10 | 80 | 100 | 25 | 27 | |
| Олово бронза с высоким содержанием свинца | ||||||||
| C93800 | 34 | 23 | 12 | 62 | 100 | 23 | 30 | |
| C94300 | 27 | 13 | 15 | 48 | 100 | 20 | 36 | |
| Олово бронза | ||||||||
| C | 49 | 23 | 25 | 77 | 25 | 36 | 43 | |
| C | 51 | 29 | 18 | 92 | 25 | 29 | 43 | |
| C | ||||||||
| 51 | 29 | 18 | 95 | 20 | 38 | 41 | ||
| C92500 | 49 | 26 | 17 | 80 | 30 | 32 | 42 | |
| C92700 | 48 | 20 | 18 | 80 | 80 | 28 | 40 | |
| C92900 | 53 | 31 | 15 | 100 | 85 | 38 | 34 | |
| C94700-HT ** | 90 | 66 | 9 | 180 | 20 | 71 | 31 | |
| Свойства после литья | ||||||||
| Алюминиевая бронза | ||||||||
| C95400 | 85 | 35 | 18 | 170 | 60 | 50 | 34 | |
| C95400-HT | 105 | 54 | 8 | 195 | 20 | 75 | 34 | |
| C95500 | 100 | 44 | 12 | 195 | 50 | 60 | 24 | |
| C95500-HT | 120 | 68 | 10 | 230 | 15 | 80 | 24 | |
| Марганцевая бронза | ||||||||
| C86300 | 115 | 70 | 15 | 225 | 8 | 80 | 20 | |
| C86400 | 65 | 25 | 20 | 90 | 65 | 40 | 51 | |
| * БТЕ / фут2 / фут / час / фут ** HT – термообработка | ||||||||
| Качественная рабочая среда подшипников | |||||
|---|---|---|---|---|---|
| Сплав № | Скорость | нагрузка | Окружающая среда | Твердость вала | Типичные области применения |
| C94300 | (низкий) (высокий) | (нижний) | (более абразивный) (менее абразивный) | (низкий) | Топливные насосы для самолетов |
| C93800 | Шахтный водяной насос, изнашиваемые пластины | ||||
| C93700 | Высоконагруженные высокоскоростные подшипники | ||||
| C93200 | Подшипники общего назначения | ||||
| C83600 | Подшипники вала линейного насоса для глубоких скважин, легкие шестерни | ||||
| C92700 | Кольца поршневые | ||||
| C | Шестерни, направляющие клапана, рабочие колеса насоса | ||||
| C92900 | Шестерни, направляющие клапана, заменитель стальной задней стенки | ||||
| C | Компоненты клапана, паровая арматура | ||||
| C | |||||
| Шестерни | |||||
| C95400 | Панели управления | ||||
| C95500 | Панели управления | ||||
| C86300 | Винтовые гайки для прокатных станов | ||||
Все сплавы, показанные в таблицах, по существу являются вариациями обсуждаемых основных материалов.В некоторых случаях свинец мог быть добавлен для улучшения обрабатываемости (C92500 против C
Экономика
Важно несколько слов об относительной экономике материалов сплава. Все компоненты сплава подвержены влиянию мировых рынков, где их уровень цен определяется предложением, спросом, государственным контролем и спекулятивным интересом. Колебания на мировом рынке этих компонентов в конечном итоге сказываются на стоимости композитного металла для сплавов, и это также влияет на стоимость металлолома, когда он выводится из эксплуатации. Таблица 3 показывает приблизительные общие относительные значения меди и основных легирующих материалов на момент написания.
| Приблизительная Относительная стоимость | Приблизительная Относительная стоимость | ||
|---|---|---|---|
| Первичные металлы | Вторичный лом | ||
| Медь | 1.0 | Олово бронза с свинцом | 0,9 |
| Олово | 7,8 | Олово бронза | 1,0 |
| Свинец | 0,2 | Алюминиевая бронза | 0,3 |
| Цинк | 0,5 | Марганцевая бронза | 0,3 |
| Никель | 4,0 | ||
| Алюминий | 0,9 | Предварительно легированный слиток | |
| C93200 | 1.2 | ||
| C | |||
| 2,0 | |||
| C98400 | 1,2 |
Методы производства
Сплавы меди для подшипников доступны во многих формах, производимых различными методами производства. Методы производства литья кратко изложены в Таблица 4 .
Продукты для песка и охлаждения
| Метод производства | |||||
|---|---|---|---|---|---|
| Семейство сплавов | Песок | Охладитель Форма | Центробежный | непрерывный | Кованые |
| Красная латунь | Х | Х | Х | Х | НЕТ |
| Олово-свинцовая бронза | Х | Х | Х | Х | Х * |
| Олово-бронза с высоким содержанием свинца S = сегрегация свинца может быть проблемой | S | S | S | Х | НЕТ |
| Оловянная бронза | Х | Х | Х | Х | Х ** |
| Алюминиевая бронза | Х | Х | Х | Х | Х |
| Марганцевая бронза | Х | Х | Х | Х | Х |
| * Ограничено примерно 4% Pb ** Деформируемые сплавы C51000, C52100, C52400. | |||||
Литье в песчаные формы или кокильные формы – идеальные методы производства, идеально подходящие для очень небольших партий или очень мелких деталей, а иногда и обязательные для очень больших деталей, таких как гребные винты судов.
Все обсуждаемые сплавы доступны в этих формах, хотя могут возникнуть проблемы с серьезной сегрегацией свинца, когда содержание свинца приближается к 16%. Можно отливать широкий диапазон размеров и сложных форм. Красные латуни, которые очень популярны в качестве материалов для сантехнического оборудования, производятся этими методами, в основном в виде корпусов клапанов и фитингов.
Продукты центробежного литья
Опять же, все рассматриваемые сплавы легко производятся методом центробежного литья, за исключением оловянных бронз с высоким содержанием свинца, в которых содержание свинца приближается к 20%. Проблемы сегрегации свинца зависят от размера отливки. Этим методом изготавливаются втулки очень большого размера. Вероятно, что большинство вводов с наружным диаметром более 14 дюймов и примерно до 100 дюймов. центробежные отливки. Такие отливки могут быть длиной более 100 дюймов.Тем не менее, небольшие центробежные отливки также являются предметами больших объемов. Многие из более крупных фланцевых подшипников или зубчатых колес изготавливаются этим методом. Хотя они чувствительны к количеству продукции, небольшие тиражи могут быть очень экономичными. Дистрибьюторы складских запасов поддерживают запасы полуфабрикатов центробежного литья, в основном стандартных размеров и особенно из сплавов C95400 и C93200.
Продукция непрерывного литья
Все сплавы доступны в виде непрерывнолитых прутков; сегрегация свинца обычно не является проблемой.Может потребоваться снятие напряжений с некоторых отливок с очень тонкими стенками, особенно если используется сплав C95400, C95500 или C86300, чтобы предотвратить потерю зазора или допусков при изготовлении и использовании. Доступен широкий диапазон размеров цельных, трубчатых и изготавливаемых на заказ стержней поперечного сечения. Диаметр варьируется от менее 0,500 дюйма до примерно 14 дюймов по внешнему диаметру, длина – примерно до 13 футов. Возможно изготовление стержней с очень тонкими стенками, иногда менее 1/4 дюйма, в зависимости от внешнего диаметра. Эти изделия идеально подходят для дальнейшего изготовления на автоматических станках.
Большие партии изделий непрерывного литья значительно более экономичны, но, опять же, дистрибьюторы складских запасов берут на себя большую часть этой нагрузки, особенно в том, что касается сплавов C95400, C93200 и C
Кованые изделия
Деформируемые сплавы фосфористой бронзы (C51000, C52100, C52400, C54400) иногда используются в подшипниках. Эти сплавы также доступны в виде непрерывных отливок в отожженном состоянии. Кованая фосфористая бронза обычно ограничивается размером около 3 дюймов.О. и под. C54400 имеет самое высокое доступное содержание свинца, около 4%. Сплавы с более высоким содержанием свинца экструдируются или прокатываются.
Сплавы из алюминия и марганцевой бронзы также имеют кованые аналоги. Деформируемые сплавы обладают очень хорошими механическими свойствами, подвергались тяжелой обработке посредством экструзии, волочения, прокатки или ковки и широко используются в аэрокосмической промышленности. Некоторые из этих сплавов используются в качестве сварочных материалов. Эти сплавы также доступны в различных экструдированных формах, хотя их разнообразие зависит от количества.Термическая обработка литых сплавов дает механические свойства, аналогичные деформируемым материалам, как и при непрерывной разливке алюминиевых бронз. Вообще говоря, для того, чтобы изделия были экономичными, требуются большие объемы производства, хотя дистрибьюторы, занимающиеся складскими запасами, взяли на себя эту нагрузку для конечного пользователя меньших объемов.
Готовые подшипники
Некоторые производители, а также многие дистрибьюторы на складе и подшипниковые центры имеют запасы стандартных готовых втулок, особенно из сплава C93200.Эти детали выпускаются серийно и легко доступны.
Специальные подшипники
Ряд механических цехов специализируется на производстве подшипников, в частности подшипников нестандартных конструкций и критических сплавов на заказ. В этих цехах работают сложные обрабатывающие центры. Используя лучшее доступное оборудование, они обеспечивают высочайшую степень точности при производстве деталей и поддерживают высокие стандарты контроля качества материалов. Такие предприятия обслуживают те OEM-предприятия и отделы технического обслуживания крупных корпораций, которые предпочитают не производить свои собственные подшипники.Они обеспечивают экономичное обслуживание и хорошо осведомлены о технологии и источниках сплавов для подшипников, которые лучше всего подходят для производства данного подшипника.
Сводка
Металлургическое машиностроение – это в большей степени наука, но и искусство. Исследования, обширный опыт и глубокое понимание свойств, которые легирующие элементы могут придавать основному металлу меди, необходимы для хорошего дизайна материала. Не менее важно понимание экономики, связанной с материалами, производством деталей и эксплуатацией конечного оборудования.Замечательные свойства меди, латуни и бронзы принесли пользу отраслям во всем мире благодаря их надежной работе, общедоступности и экономическому качеству.
Список литературы
- Р.А. Флинн , Отливки из меди, латуни и бронзы, Общество учредителей цветных металлов, Кливленд (1961).
- R. Hultgren и P.D. Desai , Отдельные термодинамические значения и фазовые диаграммы для меди и некоторых из ее бинарных сплавов, Монография Инкры I, Международная ассоциация исследований меди, Inc., Нью-Йорк (1971).
- W.A. Glaeser и K.F. Дюфран , Конструкция подшипников из литой бронзы с граничной смазкой, Институт подшипников из литой бронзы, Inc. (1978).
- F. Bowden и D. Tabor , Трение и смазка твердых тел, Clarendon Press, Oxford (1950).

| 
| ||

| 
| ||

| 
| ||
 | 
|

