Гальваника серебрение – Механизм гальванического серебрения. Теория и технология
alexxlab | 29.07.2019 | 0 | Разное
Гальваника или чистое серебро: что лучше?

Серебро, наравне с золотом, является одним из наиболее известных и популярных драгоценных металлов. Сочетая благородный внешний вид, хорошую ковкость и пластичность, а также бактерицидные свойства, этот металл широко применялся для изготовления украшений, посуды и декоративных изделий начиная с незапамятных времен. Но в наши дни применяется метод, позволяющий снизить стоимость изделия в разы – гальваника.
Особенности гальваники при покрытии изделий серебром
Чаще всего гальваника применяется там, где речь идет о крупных массивных изделиях, которые получились бы слишком дорогостоящими, если бы их изготавливали из серебра. По ссылке можно посмотреть примеры серебрения, а также сделать заказ на изготовление по индивидуальному образцу.

Среди наиболее распространенных вариантов применения гальванического серебрения можно выделить:
- Статуэтки. Ограничение габаритов составляет 20х38х30 см, что позволяет обрабатывать довольно-таки крупные изделия. В результате заменив дорогостоящее серебро дешевой латунью, можно снизить себестоимость изделия в разы. А по виду, эстетике, массе и тактильным ощущениям продукт практически не будет отличаться от серебряного.

- Столовые приборы. Существует достаточно узкий сегмент столовых приборов из чистого металла, однако такие наборы могут стоить тысячи долларов. Чтобы удешевить данную продукцию, не потеряв в качестве, применяют гальванику. В частности, популярный еще с советских времён вариант – сплав нейзильбер или мельхиор с покрытием серебром. В результате обеспечиваются и преимущества серебряной поверхности (эстетика, бактерицидные свойства), и доступная цена.


- Наградные значки, медали. Серебряные медали за второе место – одна из востребованных разновидностей изделий с серебряной поверхностью, и гальваника позволяет максимально удешевить подобные изделия.

- Прочие сувенирные изделия, статуэтки, декоративные элементы. Можно найти множество применений такой продукции: от украшения интерьера до награждения лауреатов некой премии. В любом случае гальваника позволит добиться эффектного и выразительного внешнего вида. Подробнее – смотрите здесь.

Стоит ли переплачивать за серебро?
В завершение отметим, что с механической точки зрения серебро – не самый надежный и долговечный металл. Он легко подвержен деформациям, быстро теряет исходную геометрию, у него легко стирается рельеф. Поэтому можно переплатить немалые деньги за продукцию из серебра «в массе», при этом получив недолговечный продукт. С помощью гальваники можно добиться сочетания эстетики серебра и прочности стали, что обеспечивает дополнительные преимущества.
Friend me:
гальваниказолочениелатунированиеникелированиесеребрениеvdohnovenie2.ru
Серебрение
Серебряные покрытия занимают первое место по популярности среди всех покрытий из драгоценных металлов. В ювелирной промышленности, являющейся одним из главных потребителей серебра, одной из основных характеристик является декоративный вид серебряных покрытий, поэтому самый большой интерес представляют электролиты блестящего серебрения. Для гальванического серебрения и нанесенных блестящих серебреных покрытий используются различные электролиты серебрения, наилучшими по качеству из которых, признаны электролиты на основе цианистых комплексов. Данные электролиты имеют высокую рассеивающую способность и состоят из цианистого комплекса серебра, цианида щелочного металла и карбоната этого щелочного металла, который, растворяясь в электролите, повышает его проводимость и способствует образованию более качественных мелко кристаллических осадков. В процессе работы таких электролитов и осаждения серебра, содержание карбонатов в них постепенно повышается, в результате чего, понижается предельная плотность тока, ухудшается общее качество покрытия, серебро становится мягким и т.д. Поэтому, при избытке карбонатов, их необходимо удалять из раствора электролита. В электролитах, приготовленных на основе натриевых солей, работающих при более низких плотностях тока и имеющих более низкий показатель предельного содержания карбонатов, чем в калиевых электролитах, карбонаты можно удалять путем простого охлаждения раствора электролита до температуры 3-5 оС, в результате чего, накопившийся там карбонат натрия (Na2CO3), обладающий меньшей растворимостью, чем цианид, выпадает осадок. Для удаления карбонатов из электролитов, приготовленных на основе солей калия, в раствор электролита добавляют суспензию, состоящую из 45% цианида кальция (Ca(СN)
Для гальванического серебрения и нанесенных блестящих серебреных покрытий используются различные электролиты серебрения, наилучшими по качеству из которых, признаны электролиты на основе цианистых комплексов. Данные электролиты имеют высокую рассеивающую способность и состоят из цианистого комплекса серебра, цианида щелочного металла и карбоната этого щелочного металла, который, растворяясь в электролите, повышает его проводимость и способствует образованию более качественных мелко кристаллических осадков. В процессе работы таких электролитов и осаждения серебра, содержание карбонатов в них постепенно повышается, в результате чего, понижается предельная плотность тока, ухудшается общее качество покрытия, серебро становится мягким и т.д. Поэтому, при избытке карбонатов, их необходимо удалять из раствора электролита. В электролитах, приготовленных на основе натриевых солей, работающих при более низких плотностях тока и имеющих более низкий показатель предельного содержания карбонатов, чем в калиевых электролитах, карбонаты можно удалять путем простого охлаждения раствора электролита до температуры 3-5 оС, в результате чего, накопившийся там карбонат натрия (Na2CO3), обладающий меньшей растворимостью, чем цианид, выпадает осадок. Для удаления карбонатов из электролитов, приготовленных на основе солей калия, в раствор электролита добавляют суспензию, состоящую из 45% цианида кальция (Ca(СN)
В последние несколько лет разработан целый ряд электролитов, не содержащих свободных цианидов, которые способны заменить цианистые электролиты серебрения. Среди не цианистых электролитов блестящего серебрения можно выделить децианаргентатнороданистый, синеродистороданистый и йодистый электролиты.
Децианаргентатнороданистые и синеродистороданистые электролиты серебрения устойчивы в работе, позволяют получать мелкокристаллические износостойкие серебреные покрытия, ничем не отличающиеся от покрытий, полученных из цианистых электролитов, наличие в составе свободного роданида вместо цианида, позволяет снизить их вредность, а в случае использования децианаргентатнороданистого электролита, значительно повысить рабочую плотность тока (с перемешиванием электролита до 2 А/дм 2).
Состав дицианаргентатнородаснитого электролита:
Серебро (в виде KAg(CN)2) – 23-27 г/л
Роданистый калий (KCNS) – 250-270 г/л
Сегнетова соль (NaKC4H4O6) 70-80 г/л
Ализариновое масло (C14H8O4) – 40-45 г/л
Тетрагидрофурфуриловый спирт (C5H10O2) – 70-75 г/л
Сурьма (в виде сурьмяновинокислого калия SbOKC4H4O6) – 11-13 г/л
Катодная плотность тока 0,2-0,4 А/дм2
Йодистые электролиты серебрения просты в приготовлении, стабильны и безвредны в работе, не требуют фильтрации, частой корректировки, не имеют потерь серебра и дают возможность получать качественные серебреные покрытия с высокой степенью блеска. Недостатком данных электролитов серебрение является небольшой желтоватый оттенок на получаемом серебреном покрытии, а также получение хрупких и шероховатых покрытий при длительной эксплуатации электролита.
Состав йодистого электролита:
Йодистое серебро (AgI) – 50-60 г/л
Йодистый натрий (NaI) – 500-550 г/л
Тиосульфат натрия (Na2S2O3) – 4,0-6,0 г/л
Поливиниловый спирт CH2CH(OH) – 1,0-1,5 г/л
Борная (H3BO3) (или лимонная C6H8O7) кислота – 4,5-6,5 г/л
Катодная плотность тока 0,5-1,5 А/дм2. Температура электролита 18-25*С.

Серебро (Ag в пересчете на металл) 1-2г/л
Железосинеродистый калий (K3[Fe(CN)6]) – 45-60 г/л
Роданистый калий (KCNS) – 85-95 г/л
Температура электролита 18-20оС. Плотность тока 0,1-0,2 А/дм2. Время выдержки 3-4 минуты. Для процесса используют нерастворимые аноды из никеля или стали. Детали опускают в электролит под током. После промывки проводят основное серебрение.
Оборудование для серебрения использующееся для электролитического осаждения серебра, представляет собой источник постоянного или импульсного тока малой мощности, с возможностью регулировки очень малым “шагом” до 0.01 А. В качестве анодов для основного серебрения применяют аноды из чистого серебра. Для предотвращения загрязнения электролита шламом, аноды помещают в чехлы из полипропиленовой ткани. При длительных перерывах в работе аноды вытаскивают из ванны, очищают от шлама и хранят в сухом состоянии.
При серебрении “сложных” сплавов, например алюминия, сначала проводят цинкатную обработку алюминиевой поверхности, затем производят серебрение в три стадии в трех электролитах в каждом из которых содержится более высокая концентрация серебра, чем в предыдущем. Для серебрения алюминия и сплавов на его основе можно использовать процесс химического никелирования. Для этого, алюминиевая деталь или изделие предварительно обрабатывается в электролите следующего состава:
Хлорид никеля (NiCl2) – 30-35 г/л
Ацетат натрия (CH 3COONa) – 30-40 г/л
Гипофосфит натрия (Na(PH2O2) – 25-30 г/л
Температура электролита 85-90оС; показатель рН 4-5; выдержка 15-20 минут.
Полученное затем серебреное покрытие, нанесенное по слою химического никеля, обладает даже более высокими физико-химическими свойствами, чем серебреное покрытие, нанесенное по слою меди. Единственным недостатком данного метода, является низкая рассеивающая способность электролита химического никелирования, вследствие этого, сложность или невозможность осаждения никеля в углубленных местах, глубоких полостях, на деталях имеющих сложный профиль поверхности и т.д.
Из-за наличия в воздухе паров серы и ее соединений, на серебреном покрытии со временем образуется сульфид серебра, что приводит к появлению на поверхности серебреного изделия радужных разводов, пятен, которые затем приобретают коричневый оттенок и затем черный цвет. Для очистки серебреного покрытия, изделие, вместе с кусочками алюминия, опускают в 10% раствор соды, в результате чего, выделяющийся водород восстанавливает сульфид серебра до чистого серебра.
Для предохранения покрытия серебра от окисления и образования на нем сернистых пленок, а также для декоративной отделки серебреного покрытия, наиболее простым и эффективным способом является химическое пассивирование в растворе бихроматов. Для этого, серебреную деталь или изделие сначала активируют в растворе кислоты или в щелочи, затем опускают на 20-25 минут в 1% раствор хромпика (K2Сr2O7). Процесс хроматирования ведут при температуре 18-2оС при постоянном перемешивании, рН раствора поддерживают в пределах 3,0 – 4,5 (корректировку рН проводят хромовым ангидридом).
Если внешний вид не играет роли, можно окрасить серебреное покрытие в черный цвет в растворе следующего состава:
Тиосульфат натрия (Na2S2O3) – 18-20 г/л
Натрий сернистый (Na2S) – 40-50 г/л
Серная кислота (H2SO4) – 4-5 г/л
Ацетон (С2Н6О) – 4-5 г/л
Плотность тока 0,05- 0,2 А/дм2, продолжительность обработки 3-5 минут. Полученное серебреное покрытие черного цвета имеет прочное сцепление с основой и обладает высокой износостойкостью.
Для обезвреживания и утилизации отработанного цианистого электролита, его сначала прорабатывают до полного выделения серебра, затем окисляют электролит, вводя в него 0,5 г/л обычной поваренной соли (NaCl), после чего, прорабатывают раствор при плотности тока 1 А/дм2 с нерастворимыми анодами (Внимание! Процесс следует проводить при хорошей вытяжной вентиляции). Через 30 минут в электролит снова добавляют 0,5 г/л соли и снова прорабатывают в течении 30 минут при плотности тока уже 3 А/дм2. Еще через 30 минут снова добавляют такое же количество соли и снова прорабатывают отработанный раствор электролита при плотности тока 6 А/дм2.Дефекты при серебрении из цианистых электролитов и способы их устранения
| Дефект покрытия | Причина возникновения | Способ устранения |
|---|---|---|
| Отслаивание покрытия (или шелушения), в особенности при последующей полировке | Плохая подготовка поверхности перед покрытием или малая концентрация серебра в электролите | Улучшить подготовку изделия перед покрытием. Повысить концентрацию серебра до рабочего значения |
| Отслаивание – хрупкое покрытие | Пассивация серебряных анодов, аноды светлые, на катоде выделяется водород | Увеличить количество анодов, откорректировать электролит |
| Пятна или потемнение покрытия и потемнение анодов | Недостаток свободного цианистого калия в электролите | Откорректировать электролит по содержанию свободного цианистого калия |
| Шероховатость покрытия, темные пятна на покрытии при светлых анодах | Повышенная анодная плотность тока – усиленное растворение анодов, накопление анодного шлама | Отрегулировать анодную плотность тока, отфильтровать электролит, ввести необходимое количество аммиака |
| Грубое крупнокристаллическое покрытие, рыхлое, с потемнением | Повышенная катодная плотность тока, близкая к предельной, особенно в момент завешивания | Отрегулировать катодную плотность тока |
| Макро пористость покрытия, питтинг в форме блестящих точек или вертикальных полос | Выделение водорода – повышенная плотность тока, задержка пузырьков водорода на поверхности | Отрегулировать плотность тока, ввести перемешивание электролита, покачивание катодных штанг |
impgold.ru
Гальваническое серебрение | ЭлХимМет
Декоративное покрытие серебром находит применение, как в ювелирном так и в сувенирном производствах. Однако и техническое применение серебряных покрытий встречается тоже довольно часто.
В нашем распоряжении имеются несколько разных электролитов серебрения, с помощью которых мы можем решать практически все, связанные с серебрением, задачи. В процессе нанесения серебра на различные металлы одним из самых важных является вопрос подготовки поверхности изделий перед серебрением. Малейшая ошибка приводит к недостаточному «прилипанию» слоя серебра на изделия, а иногда и вовсе к отслоению только что нанесённого покрытия. Наиболее эффективно эта проблема решается при помощи электролитов предварительного серебрения. Серебро является мягким металлом и легко подвергается истиранию. Для снижения износостойкости серебра применяются электролиты позволяющие осаждать различные сплавы, например с сурьмой или палладием, повышающие стойкость серебряного покрытия к истиранию.
Пористость покрытий серебром аналогична пористости золотых покрытий и методы борьбы с этим нежелательным эффектом аналогичны тем, которые применяются при золочении. Серебро значительно дешевле золота и поэтому с целью недопущения протирания покрытия при носке можно наносить сравнительно более толстые покрытия. Возможно введение в состав серебра легирующих добавок, например сурьмы, с целью увеличения твёрдости и износостойкости.
Известна способность серебра к потемнению под воздействием следов сероводорода с образованием на поверхности тёмных слоев. Для борьбы с этим явлением применяется палладирование и родирование. Но это изменяет внешний вид изделия, так как эти металлы имеют иной, отличный от серебра цвет. Есть ещё возможность произвести хроматирование и нанести хроматный слой, но он имеет малую механическую устойчивость и может быть полезен только пока изделие не контактирует с руками или лежит на прилавке и ждет покупки, а при начале эксплуатации защитный слой за месяц стирается.
Для различных технических применений мы можем предложить также как покрытия чистым серебром, так и его сплавами с различными металлами, такими как сурьма, палладий, никель, медь, золото и др. В нашем распоряжении имеется колокольная ванна, в которой мы можем наносить покрытия на мелкие детали. На более крупные изделия покрытие любой толщины, мы наносим в обычных ваннах. Возможно нанесение серебряных покрытий также и на легкие металлы и сплавы.
exm.su
СЕРЕБРЕНИЕ. Гальваническое покрытие серебром
Заниматься гальваникой, как и любым другим делом, можно где угодно. Но желательно все же слегка оборудовать свое рабочее место. Прежде всего, необходимо учесть две вещи. В процессе работы, вы будете иметь дело с концентрированными кислотами и прочими едкими веществами. И второй момент – на различных этапах гальваники будут выделяться всякие ядовитые газы, едкие пары и прочие испарения. Поэтому желательно обустроить место там, где сложно что-нибудь прожечь и там должна быть вентиляция.
Первая мысль – это кухня. Сразу практический совет. Если на кухне есть вытяжка очень хорошо, только на вытяжке не должны стоять фильтры!
Первый эксперимент автора по получению концентрированной серной кислоты, закончился тем, что из вытяжки начала сыпаться всякая труха и мусор, типа сеточек и волокон. Это от паров серной кислоты разрушился фильтр и, следовательно, пришлось покупать вытяжку. Так что повторюсь, хорошая вентиляция, залог успеха всего процесса гальваники.
1. Респиратор.
Очень нужная вещь. Как мы уже упоминали, во время гальванизации выделяется много всякой газообразной гадости, которая здоровью никак не полезна. Добавим сюда же резиновые перчатки. Лучше найти прозекторские. Они достаточно прочные и в тоже время не грубые. Работать без перчаток – получить химические ожоги и другие проблемы для кожи рук. Очень рекомендую фартук из плотной клеенки. Обязательно на ноги какие-нибудь тапки.
2. Гальваническая станция.
Необходим блок питания на ток 30-50А, с амперметром, плавной регулировкой и желательно стабилизацией силы тока. Напряжение достаточно иметь в интервале 12-24В. Схему нетрудно найти в Интернете. Нужны 2 куска кабеля, площадью побольше, для соединения анода и детали с блоком питания. Если взять кабель с меньшей площадью, то он будет сильно греться, так как ток большой. Нужна неметаллическая емкость, такого объема, что бы туда помещалась твоя деталь целиком, плюс анод с такой же площадью. В качестве емкости можно использовать пластиковый тазик. Если электролит в тазике не хранить, то он прослужит долго, проверено.
3. Нагревательные приборы.
Использовать открытый огонь для нагрева – не советую. Не потому, что мы делаем что-то взрывчатое, нет. Просто с открытым огнем тяжело контролировать температурный режим, можно, невзначай, накипятить раствор, который кипятить совсем не надо и т.п. К тому же, есть риск испортить дорогую газовую плиту каким-нибудь раствором. Поэтому будем использовать электроплитку. Еще понадобится утюг с рабочим терморегулятором, чтобы можно было установить температуру подошвы от 80 градусов. Понадобится песчаная баня.
4. Посуда.
Лучше, конечно, найти где-нибудь набор химической посуды (колбы, чашки, кипелки). Но если нет, можно пользоваться любой бытовой стеклянной. Еще понадобится фарфоровая чашка для выпаривания, желательно со сферическим дном. Желательно найти стеклянные бутылки с притертой крышкой, для хранения реактивов и электролитов.
5. Измерительное оборудование.
Прежде всего, нужны весы, так как отмерять реактивы придется с точностью до грамма. Если есть возможность, используй заводские, если нет – можно изготовить самому. Берете стальной стержень d=10 мм, 1=200 мм. Точно находите середину, сверлите отверстие для подвеса. На оба конца стержня нарезаете резьбу миллиметров по 15, накручиваете гайки. Сразу за резьбой сверлите отверстия для подвеса чашек. Под подвес весов, крепите спицу под углом 90 градусов (нужно точно замерить угол). Спица это указатель шкалы. Подвешиваете чашки. Далее подвешиваете весы. Гайками юстируете положение, важно, чтобы спица была направленная вертикально вниз (можно проверить отвесом). Все весы готовы. Осталось найти гирьки и можно «отвешивать». В качестве гирек можно использовать старые советские монеты. Их номинал довольно точно соответствует весу (1 коп. – 1 г, 2 коп. – 2 г, 3 коп. – 3 г, 5 коп. – 5 г).
И, наконец, нужен термометр. Диапазон шкалы 10-130 градусов.
ГАЛЬВАНИКА – расходные материалы
В принципе, все необходимое можно купить в конторах торгующими химическими реактивами. Но по России этот процесс, в последнее время, стал очень тяжелым занятием. Покупателю реактивов требуется представить доверенность, какую-то выписку из разрешительного документа, что мол данное юридическое лицо может заниматься какой-то там деятельностью, оплата обычно безналичная и прочие сложности. Для решения этой задачи можно пойти более простым путем – хозмагазины, рынки, СТО, товарищи.
Здесь будем рассматривать только СЕРЕБРЕНИЕ поверхностей. Соответствующим будет и набор реактивов. Для меднения или никелирования химреактивы нужны другие (см. ниже).
Для СЕРЕБРЕНИЯ потребуется:
- Серная кислота (H2SO4) – СТО и автомагазины продают кислоту для заправки аккумуляторов, довольно хорошего качества. Те присадки и примеси что там есть, нашему занятию совершенно не мешают. Если брать кислоту на рынке – есть вероятность нарваться на плохую и в дальнейшем это отразится на качестве покрытия. Так что осторожнее. Обычно, она продается в пластиковых канистрах на 3 л, концентрация – 36%. На наши цели шесть литров – достаточно.
- Хлорид натрия (NaCl) – он же, пищевая соль. Покупаем в продмаге, 2 пачки (2 кг).
- Гидрокарбонат натрия (NaHCO3) – он же, пищевая сода. Опять идем в продмаг. Нужна одна пачка (100 г).
- Нитрат натрия (NaNO3) – известен под именем «натриевая селитра». Продается в магазинах, торгующими удобрениями. Берете пакет на 5 кг или немного меньше. Важное замечание, продавцы удобрениями могут посоветовать купить смесь из натриевой и аммиачной селитры (типа лучше) – не брать! Нужен, только, NaNO3, желательно без примесей и добавок.
- Силикат натрия (Na2SiO3) – или «Жидкое стекло» (он же силикатный конторский клей – можно купить в магазине канцелярских принадлежностей). В магазин стройматериалов или на рынок – 1 кг достаточно.
- Карбонат натрия (Na2CO3) – он же кальцинированная сода, он же стиральная сода. Вперед на рынок стройматериалов или магазины, торгующие моющими средствами. У кого-то из них эта сода обязательно будет. Пару килограмм достаточно.
- Железистосинеродистый калий (K4[Fe(CN)6]), он ещё известен под названием «жёлтая кровяная соль». Наиболее доступное место, где он может быть, школьная или институтская химическая лаборатория. Необходимо 200 г.
- Серебряный лом (Ag) – тут подойдут и любые серебросодержащие сплавы (серебряная ложка, сережки, контакты и т.п.). Количество – где-то на 15-20 грамм чистого металла.
- Любое моющее средство – 1 бутылка.
СЕРЕБРЕНИЕ – процесс
Прежде всего, изготовим концентрированную серную кислоту. Делаем емкость из пивной 0,5 л бутылки, желательно прозрачного стекла (легче контролировать процесс). Для этого отрезаем горлышко где-то на уровне верхней трети. Острые края бутылки желательно обработать напильником. Готовим песчаную баню – старая железная кастрюлька или большая кружка, заполненная песком слоем 10 см.
Заливаем аккумуляторную серную кислоту где-то на одну треть. Помещаем ее в песчаную баню. Включаем нагрев.
При нагревании серная кислота теряет влагу и ее концентрация растет. Дожидаемся, пока не появится легкий дымок. Это пошла окись серы. Не перегрейте смесь – окись серы моментом вытягивает влагу из воздуха и превращается в серную кислоту в виде взвеси – вдыхать ее не полезно. Быстренько снимаем баню с плитки и накрываем бутылку стеклом.
Выдерживаем в бане минут 15-20. Горячая серная кислота весьма опасна. В случае разлива обильно засыпаем это место пищевой содой, если попадет на кожу – проест быстрее, чем почувствуешь боль. Так что респиратор и перчатки должны быть в использовании. Подобным образом, повторяя, отгоняем где-то 300-400 мл концентрата. Храним в стеклянной посуде, лучше с притертой крышкой.
 Далее понадобится азотная кислота – делаем сами! Берем 2 бутылки, желательно «попузатее». В одну бутылку кладем 165 грамм натриевой селитры и заливаем туда же 100 мл концентрированной серной кислоты. Быстренько соединяем горлышками с пустой бутылкой и заматываем это место скотчем, чтобы внутрь не попадал воздух. Наклоняем получившуюся конструкцию так, что бы пустая бутылка была чуть выше. Начинаем нагревать бутылку со смесью, пустая заполняется красно-бурым газом – окисью азота, а селитра потихоньку растворяется в кислоте. Не перегревай! Сильный нагрев увеличивает газообразование, и окись азота стравится через соединение. После полного растворения, прекращаем нагрев.
Далее понадобится азотная кислота – делаем сами! Берем 2 бутылки, желательно «попузатее». В одну бутылку кладем 165 грамм натриевой селитры и заливаем туда же 100 мл концентрированной серной кислоты. Быстренько соединяем горлышками с пустой бутылкой и заматываем это место скотчем, чтобы внутрь не попадал воздух. Наклоняем получившуюся конструкцию так, что бы пустая бутылка была чуть выше. Начинаем нагревать бутылку со смесью, пустая заполняется красно-бурым газом – окисью азота, а селитра потихоньку растворяется в кислоте. Не перегревай! Сильный нагрев увеличивает газообразование, и окись азота стравится через соединение. После полного растворения, прекращаем нагрев.
Бутылки ставим в холодное место, часа на 3. Получаем в бутылке жидкость с осадком. Осадок, глауберова соль, нам не нужна, а жидкость – концентрированная азотная кислота, на воздухе она «дымит». Повторяя процесс, получаем 150-200 мл. Для временного хранения подойдет пластиковая бутылка, но для длительного нужно все-таки стекло.
Разбавляем азотную кислоту водой 1:1. То есть из 150 мл концентрата получаем 300 мл рабочего раствора. Начинаем растворять серебро или его сплавы. Чем мельче будут кусочки, тем быстрее пойдет процесс. При растворении выделяется красно-бурый газ (окись азота), весьма ядовит, так что нужна вентиляция! Пока растворяется серебро, готовим перенасыщенный раствор поваренной соли. В 300 мл воды, при 80°С добавляем соль до тех пор, пока она не перестанет растворяться. Фильтруем. Охлаждаем. Выпадает осадок (соль), снова фильтруем.
После растворения металла, начинаем приливать мелкими порциями раствор соли. Начинает интенсивно выпадать осадок. Подождем, пока осядет, приливаем еще чуть-чуть. Повторяем до тех пор, пока не прекратится выпадение осадка.
Не бойтесь переборщить с солью, лишнее останется в растворе. Далее рабочий раствор с осадком нагреваем до 90°С. и выдерживаем при такой температуре 10 минут.
Тонкий осадок при этом укрупнится. Далее аккуратно сливаем раствор с осадка, приливаем воду, взбалтываем, отстаиваем, опять сливаем раствор. Этот процесс называется декантация. Таким образом, хорошо промываем осадок. Жидкость с осадком фильтруем через промокашку. Полученный фильтрат и есть хлорид серебра (AgCl), который используется в большинстве рецептов для СЕРЕБРЕНИЯ. Но хранить его долго не получится. Это соединение весьма неустойчиво и довольно быстро разлагается до металлического серебра, особенно под действием света.
Отсыпаем хлорид серебра в количестве необходимом для СЕРЕБРЕНИЯ (об этом ниже), а остаток ведь не выбрасывать же! Поэтому оставшийся реактив заливаем водой. Бросаем туда мелкие, но такие, чтобы можно было, потом заметить кусочки оцинкованной проволоки, по весу в 2 раза больше чем хлорида серебра. Туда же приливаем грамм 50 раствора поваренной соли. Нагреваем эту смесь до 80-90°С и поддерживаем эту температуру. Весьма быстро хлорид серебра восстанавливается до металла. Греем и помешиваем до тех пор, пока весь осадок не станет серого цвета. Удаляем кусочки проволоки. Далее опять декантируем раствор. Последние порции промывки желательно делать дистиллятом. Полученный осадок фильтруем на промокашку. Фильтрат – чистое серебро.
В отдельной посуде, опять разводим концентрированную азотную кислоту с водой (желательно дистиллятом) в отношении 1:1. В посудину, где находится порошок серебра, мелкими дозами аккуратно приливаем раствор азотной кислоты до тех пор, пока не растворится весь металл (газы – вентиляция). Полученный раствор выпариваем до сухого остатка. Это азотнокислое серебро (AgNO3). Храним его в темном месте в стеклянной посуде с притертой крышкой. Реактив весьма едкий и может оставить язвы на руках, обращаться осторожно! В случае необходимости получить хлорид серебра – растворяем в воде, приливаем раствор соли и фильтруем (см. выше).
Теперь необходимо подготовить поверхность детали для СЕРЕБРЕНИЯ. Сначала обезжириваем. Готовим раствор:
- Вода – 1 л
- Жидкое стекло – 50 г
- Кальцинированная сода – 25 г
- Средство для мытья посуды – 25 г.
Нагреваем раствор до 70°С и опускаем туда деталь. Время обработки – 20 мин. Руками не трогать! Там где схватишься, серебро слезет. Непосредственно перед серебрением – декапируем поверхность (удаляем оксидную плёнку) – помещаем деталь в раствор азотной кислоты (1:1 – 15-20%) на 40-60 секунд и сразу в раствор для серебрения.
Итак, начнем серебрить …
Рекомендуется делать СЕРЕБРЕНИЕ электрохимическим способом. Гораздо более стойкое и качественное покрытие.
Для сравнения приведем краткое описание альтернативы, если кто-то хочет попробовать другой метод СЕРЕБРЕНИЯ.
СЕРЕБРЕНИЕ химическим способом
- 20 г хлористого серебра
- 120 г поваренной соли
- 150 г лимонной кислоты
- вода – 1л
Кипятим раствор 15 мин. Затем помещаем деталь на подвесах в ёмкость и кипятим. Постепенно она покрывается слоем серебра.
Недостаток данного способа серебрения – невозможно проконтролировать толщину покрытия серебром и низкая механическая стойкость. Подобным способом можно пользоваться только для декоративных целей.
СЕРЕБРЕНИЕ электрохимическим способом
Раствор:
- хлористое серебро – 20 г
- желтая кровяная соль – 50 г
- кальцинированная сода – 60 г
- вода – 1 л
Анод – графит, катод – деталь. Плотность тока – 0,1 А/кв. дм. Температура раствора – 20°С. Время гальванизации подбирается индивидуально, постоянно контролируя процесс. Очень важно чтобы источник питания был стабилизированный и давал чистый постоянный ток. На выходные цепи желательно повесить большую емкость 60000-100000 мкФ. Пульсирующий ток испортит поверхность.
После СЕРЕБРЕНИЯ есть рекомендации пассивировать поверхность в 1% растворе хромпика с выдержкой 20 мин. Пассивация – это нанесение оксидной пленки, предотвращающее дальнейшее окисление. Во многих случаях она не требуется.
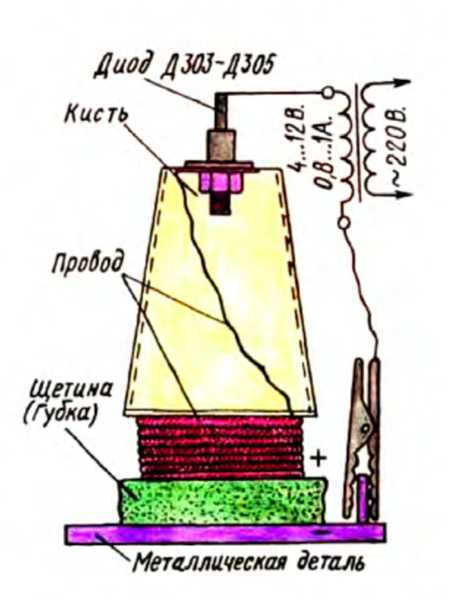 Покрытие металлов никелем, цинком, хромом, серебром и даже золотом можно делать без гальванической ванны с помощью несложного приспособления – миниатюрной гальванической установки. Она состоит из специальной кисти, внутрь которой может заливаться электролит, понижающего трансформатора с напряжением 4-12 В и током 0,8-1,0 А и соединительного шнура.
Покрытие металлов никелем, цинком, хромом, серебром и даже золотом можно делать без гальванической ванны с помощью несложного приспособления – миниатюрной гальванической установки. Она состоит из специальной кисти, внутрь которой может заливаться электролит, понижающего трансформатора с напряжением 4-12 В и током 0,8-1,0 А и соединительного шнура.
Щетина кисти обматывается медным проводом. Диод (с током более 2 А) устанавливается внутри кисти или снаружи. Диаметр кисти 20-25 мм. «Минус» источника напряжения соединяется при помощи зажима «крокодил» с обрабатываемым куском металла, а «плюс» – с намотанной на щетину проволокой. Вместо щетины можно применить пористую губку. Покрываемые металлические предметы должны быть тщательно очищены от грязи, жира, ржавчины и т. п. Ржавчину удаляют травлением в кислоте, а остатки краски – шлифовкой наждачной шкуркой. После этого поверхность протирается чистым куском материи и обезжиривается специальным раствором. Чем ровней и чище будет поверхность, тем прочнее будет гальваническое покрытие. После очистки покрываемых металлических предметов делают все указанные выше соединения, включают трансформатор в сеть, заливают электролит в кисть и равномерными движениями проводят кистью по поверхности металла, не отрывая кисть от поверхности. Тотчас же будет замечаться тонкий металлический осадок, который постепенно наращивается. Как правило, для прочного покрытия требуется до 20-25 раз пройти кистью по одному и тому же месту поверхности.
Электролит доливают в кисть по мере надобности.
После окончания гальванического покрытия деталь споласкивают водой и полируют смоченной в воде тряпкой, а затем промывают еще раз и сушат. Для каждого вида гальванического покрытия берется строго определенный электролит, который составляется по приведенным ниже рецептам (в граммах на 1 л раствора).
Электролит для меднения:
1. Медный купорос (сернокислая медь) – 200
2. Серная кислота чистая – 50
3. Этиловый спирт или фенол – 1-2
Электролит для никелирования:
1. Сернокислый никель – 70
2. Сернокислый натрий – 40
3. Борная кислота – 20
4 . Хлористый натрий – 5
Электролит для хромирования:
1. Хромовый ангидрид – 250
2. Серная кислота (уд. вес 1,84) – 2,5
Электролит для цинкования:
1. Сернокислый цинк – 300
2. Сернокислый натрий – 70
3. Алюминиевые квасцы – 30
4 . Борная кислота – 20
Электролит для серебрения:
1. Хлористое серебро свежеосажденное – 3-15
2. Железисто-синеродистый калий – 6-30
3. Сода кальцинированная – 6-30
Электролит для золочения:
1. Хлорное Золото – 2,65
2. Железисто-синеродистый калий – 15-50
3. Сода безводная – 20-25
Состав для обезжиривания:
1. Едкий натрий – 100-150
2. Сода кальцинированная – 40-50
3. Растворимое стекло – 3-5
В зависимости от степени загрязнения покрываемые предметы выдерживаются в обезжиривающем составе от 15 минут до одного часа при температуре состава 80-100°С. Номера 1, 2, 3, 4 в рецептах указывают на порядок приготовления растворов. Сначала берут 200-300 мл воды, в которой растворяют первый компонент, потом второй, третий и так далее, а затем доливают воду до 1 литра раствора.
Если необходимо приготовить меньшее количество раствора, то вес всех компонентов нужно уменьшить пропорционально новому объему раствора (например, на 0,5 л раствора соответственно в 2 раза, на 0,25 л – в 4 раза). Воду необходимо применять дистиллированную (в крайнем случае, кипяченую) при температуре, 15-40°С. Следует иметь в виду, что хотя вышеупомянутые растворы не содержат сильно ядовитых веществ, обращаться с ними во избежание ожогов и отравлений нужно с большой осторожностью. Растворы лучше хранить в темной стеклянной посуде с плотно закрывающимися крышками.
Похожие статьи:
Прошлые статьи:
hammering.su
Покрытие металлических изделий серебром – Ювелирные техники, отделка ювелирных украшений | Jevel.ru
Благодаря открытию батарей, как источников электрического тока, самым первым покрытием в гальванике стало именно нанесение тончайшего слоя серебра.
Для растворов, используемых для серебрения, применяются растворимые цианиды серебра, к которым для большей эффективности процесса добавляют небольшое количество цианистого натрия или цианистого калия. Избыток цианистых соединений часто называют « свободными» цианидами, потому что ионы серебра не связаны с этими соединениями.
 С помощью лабораторных анализов определяют наличие « свободных» цианистых соединений в растворе.
С помощью лабораторных анализов определяют наличие « свободных» цианистых соединений в растворе.
Роль « свободных» цианидов двояка: они не только улучшают внешний вид покрытия серебром, но и способствуют лучшему переходу в раствор серебряного покрытия анода. Такое растворенное серебро может составлять 60%, если в качестве « свободного» цианида используют цианистый калий и 46%, если в растворе присутствует цианистый натрий. Обогащенные серебром растворы делают процесс серебрения очень эффективным.
В процессе приготовления растворов для покрытия металлов серебром используются: цианистое серебро, цианистый калий и калийные соли углекислоты.
Применяемые растворы содержат серебро в количестве от нескольких граммов и до 90 граммов серебра на литр раствора. С увеличением концентрации возрастает и скорость реакции. Подобные высококонцентрированные растворы носят название «скоростных».
Для увеличения скорости реакции растворы нужно постоянно подогревать и перемешивать, а также проводить их фильтрование.
В некоторых случаях может проводиться покрытие серебром и без перемешивания раствора, и без нагревания, а также при небольшом значении тока. Но такой процесс требует гораздо большего количества времени и обычно на практике используется достаточно редко. Во всех случаях растворы, применяемые для серебрения, имеют высокую электропроводность.
Толщина серебряного покрытия и время, требуемое для серебрения
Можно заранее спланировать и определить то количество серебра, которое нужно нанести на изделие. Иногда точное значение толщины покрытия не очень важно, особенно тогда, когда оно наносится на серебряную поверхность, например, 800 пробы, так как изделие можно продать, измерив вес.
 Если же серебром покрывают более дешевые металлы, то необходимо учитывать и толщину, и вес серебряного покрытия, так как это определяет качество покрытия и его стоимость.
Если же серебром покрывают более дешевые металлы, то необходимо учитывать и толщину, и вес серебряного покрытия, так как это определяет качество покрытия и его стоимость.
Просматривая рецепты приготовления растворов, можно заметить, что там всегда указана плотность тока. Путем несложных арифметических действий, а именно умножением плотности тока на коэффициент 0,066, мы можем рассчитать вес серебра, которое будет откладываться на изделии за одну минуту. Умножением плотности тока на 4 получим вес серебряного покрытия, отложенного за один час.
Для того чтобы определить толщину слоя серебра, которое откладывается за минуту, в микронах на площади изделия, равной одному квадратному дециметру, нужно плотность тока умножить на коэффициент 9, 634. Если нужно узнать толщину такого слоя, отложенного за один час, то плотность тока умножают на коэффициент 38.
Некоторые рецепты растворов, применяемых для покрытия сплавов серебра
Если покрытие серебром проводится очень часто или даже ежедневно, то необходимо использовать растворы, которые обеспечивают качественное покрытие и немалую скорость течения этого процесса.
Часто, чтобы уменьшить производственные расходы и избежать процесса восстановления поверхности, пользуются специальными добавками, придающими блеск изделию, то есть его серебряному покрытию. Иногда применяют некоторые добавки, изменяющие твердость покрытия.
 В одном литре раствора, применяемого для нанесения серебряного покрытия, содержится 28, 7 граммов металлического серебра и 41 грамм на литр свободного цианистого калия.
В одном литре раствора, применяемого для нанесения серебряного покрытия, содержится 28, 7 граммов металлического серебра и 41 грамм на литр свободного цианистого калия.
Гальванический процесс покрытия серебром обычно проводят при температуре 21-26 градусов и силе тока 0,5-1,5 ампер на квадратный дециметр. В течение одного часа может отложиться от 19 и до 57 микрон серебра при весе 2-6 граммов на поверхности, равной одному квадратному дециметру.
Для того чтобы поверхность имела привлекательный блеск, часто используют соединения серы и углерода. Такие вещества делают покрытие намного прочнее. Излишки этих соединений могут быть вредными, поэтому процесс проводят следующим образом.
В пластиковую емкость, желательно темного цвета, наливается несколько литров раствора и затем добавляется одна ложка сероуглерода. Смесь нужно тщательно перемешать и оставить на одну ночь до полного растворения компонентов. Перед началом процесса серебрения в гальванический раствор добавляют небольшое количество раствора для образования блеска, причем раствор добавляют до получения блестящего покрытия.
Для образования блеска можно использовать тиосульфат аммония или тиосульфат калия, которые растворяют, пока концентрация в растворе не достигнет 60%. Первый раз добавляют 4 грамма на сто литров гальванического раствора, а в процессе работы периодически добавляют небольшие количества.
Вещество, применяемое для придания блеска, постепенно слабеет в растворе, поэтому, когда он перестает действовать, то добавляют новый, то есть свежий. Специализированные фирмы занимаются выпуском более совершенных и стабильных веществ для придания блеска серебряному покрытию. Купить их сегодня не представляет сложности.
Чтобы улучшить качество раствора, он может перемешиваться при помощи катода или насоса, снабженного фильтром. Это дает возможность поддерживать необходимую прозрачность рабочей жидкости.
Для нормального течения процесса нужно поддерживать pH в пределах 12, при необходимости, то есть при уменьшении pH, добавляя растворенную в воде гидроокись калия 10% крепости.
Электрод, сделанный из серебра, должен иметь поверхность, не меньше поверхности обрабатываемых изделий, умноженную на два.
Гальваническая пластика для утолщенных изделий
Если покрытия имеют большую толщину, то рациональнее использовать другой раствор. Такой раствор можно использовать для нанесения серебра на фарфор или стекло после его окраски металлизированной краской и последующей обработки его в электрической печи. Эти растворы применяются в гальванопластике для нанесения серебра на толстые покрытия. Процесс нанесения серебра проводится при комнатной температуре, поэтому можно применять и пластиковые материалы, которые не выдерживают нагревания. Желательно перемешивать раствор и постоянно фильтровать его.
Дефекты при нанесении серебряного покрытия
Если в растворе недостает свободных цианидов, то это может привести к появлению одного или нескольких дефектов. Это могут быть: неоднородность и шероховатость поверхности покрытия, изменение окраски поверхности от желтого цвета и до черного, образование пятен при касании пальцами, зернистость поверхности. Стрелка вольтметра при этом может опускаться, а стрелка амперметра может подниматься, когда изделие находится в растворе, грязный анод или анод черного цвета, который не белеет после отключения тока.
Слишком большая величина тока может вызвать недостаточное прилегание покрытия к изделию, либо образование поверхности покрытия, напоминающего порошок.
Покрытие может отслаиваться, если поверхность перед процессом была недостаточно обезжирена, ток завышен, а поверхность, на которую наносится покрытие, покрыта окислами. Недостаток толщины покрытия может быть вызван слишком малым током, недостатком времени для процесса или плохими электрическими контактами.
Если на блестящем покрытии появляется « апельсиновая корка», то такой дефект – следствие недостаточной механической подготовки.
Нанесение серебряного покрытия без применения цианидов
Высокая токсичность цианистых соединений и необходимость последующей очистки сточных вод, навела на мысль об открытии новых растворов для гальваники, не содержащих этих соединений.
Используются растворы, в которых вместо цианистых калия и натрия, пользуются хлористым серебром или его сульфатом, растворенным вместе с тиосульфатом натрия. Можно использовать и йодистое серебро, точнее его раствор в концентрированном растворе йодистого натрия.
Используя такие растворы, можно получать серебрение отличного качества.
Чтобы предотвратить потемнение серебряного покрытия, используют фиксацию. Она проводится в гальванической ванне с плотностью тока, при которой на поверхности изделия появляются пузырьки воздуха. Необходимое условие – предварительное обезжиривание материала.
www.jevel.ru
Мастерская гальваники в СПб – гальваника: золочение, серебрение
Что такое гальваника
Гальваника – это нанесение покрытия способом электролитического осаждения стойкого металла на поверхность менее стойких металлов. Гальванические покрытия в ювелирной практике используются в двух целях – как декоративная и как защитная.
На нашем предприятии возможно выполнить такие виды гальванического покрытия, как родирование, палладирование, золочение и серебрение чистотой.
Покрытие можно нанести на изделие впервые или восстановить утраченное (из-за пайки, полировки, ушедшее со временем при носке изделия).
Золочение (позолота) – нанесение на изделие тонкого слоя золота от десятых долей мкм до 2-3 мкм (1мкм=0,001мм) и до 20-25 мкм, не только на изделия из недрагоценных металлов, но и украшения из серебра и золота ( выделение декоративных элементов, изменение цвета изделия).
Слой золочения в 2 мкм обеспечивает ровное, плотное, беспористое, износостойкое покрытие. Твердость покрытия превышает твердость любого литого золота более чем в два раза
Золочение всегда являлось наиболее распространенным способом отделки, потому что золото — один из первых металлов, ставших известными человеку. Кроме того, золото по интенсивности цвета, мягкости блеска, глубине тона и устойчивости декоративных качеств превосходит все другие металлы.
Золочением осуществляют и реставрацию золотых украшений и придают более эффектный внешний вид новым украшениям, так называемая «подсветка» изделия.
Примечательно: В Древнем Египте применяли т. н. листовой метод золочения — на подготовленную поверхность изделий наклеивали 1-3 слоя тончайших лепестков золота. Этот способ широко применялся в Киевской Руси с 10-11 вв. н. э. Уже в 19 в. в России этим способом золотили железные или медные главы церквей, крыши, шпили дворцов. Срок службы листовых золотых покрытий достигал примерно 50 лет. Позднее стали применять огневой метод золочения — на поверхность наносили тестообразную пасту из амальгамы золота (соединение золота с ртутью). При нагреве изделия (из фарфора или металла) ртуть испарялась, а плотное золотое покрытие оставалось. Срок службы таких покрытий 100-150 лет. Начиная с середины 19 в. пользуются гальваническим методом золочения. Гальванический метод используют не только для Золочения, но и для покрытий из соединений золота с серебром, сурьмой, никелем, кобальтом, медью и др. Такие покрытия примерно вдвое повышают твёрдость поверхности и являются хорошим средством защиты её от коррозии.
Серебрение — гальваническое покрытие металлов слоем серебра толщиной от долей мкм (1мкм=0,001мм) до десятков микрон. Слоем серебра обычно покрываются изделия из недрагоценных металлов в декоративных целях, чтобы придать им более изысканный вид. В периодической системе элементов Менделеева серебро входит в группу благородных металлов, названых так из-за их неподверженности коррозии и окислению, т.е. химической стойкости.
Примечательно: Чистое серебро — тяжёлый (легче свинца, но тяжелее меди — плотность — 10,5 г/см), очень пластичный металл серебристо-белого цвета. Коэффициент отражения серебра близок к 100 %.
Родирование – нанесение на ювелирное украшение тонкого слоя родия, самого яркого и блестящего металла платиновой группы, толщиной 0,1—25 мкм на поверхность ювелирных изделий для повышения их отражательной способности и придания особой твердости и износостойкости, придает металлу интенсивный блеск, многократно увеличивая коэффициент отражения света от поверхности, благодаря чему ювелирное изделие, покрытое родием, сверкает и переливается.
Примечательно: Родий – драгоценный, редкий благородный металл платиновой группы, превосходящий золото, серебро и платину по химической стойкости Химически стойкий, гипоаллергенный. Твердость в 2,5 раза выше, чем у золота и серебра.
Покрытие родием придает повышенную прочность изделию, защиту от атмосферного воздействия (потемнение серебряных изделий). Декоративные свойства – выделение элементов «под белое золото», а также усиление яркости цвета белого золота (т.к. сам сплав белого золота имеет слегка желтоватый оттенок).
Оборудование и материалы:
Нанесение гальванических покрытий на различные металлы требует использования соответствующего оборудования и расходных материалов. Для серебрения, золочения а также для покрытия обрабатываемых деталей другими металлами используется однотипное гальваническое оборудование. Различия при выполнении таких процессов будут заключаться только в составе используемого электролита, его температуре и других режимах выполнения обработки.
Посеребрить, позолотить или родировать кольцо, серьги, сувениры, бижутерию и другие украшения — это к нам! Наша студия располагает всем необходимым оборудованием, чтобы помочь Вам воплотить в жизнь все идеи и проекты.
galvanikaspb.ru
технологический процесс и необходимое оборудование :: BusinessMan.ru
Гальваника – это раздел науки под названием «Электрохимия», в котором изучается осаждение электролитов на поверхности металлов. Так же называется и собственно процесс нанесения металлического покрытия на любое изделие. Для защиты от коррозии, например, используется цинкование или хромирование.
Несмотря на то что процесс нанесения электролитов достаточно сложный и небезопасный, сегодня становится популярной декоративная, то есть предназначенная для украшения и защиты гальваника в домашних условиях.
Есть и другое толкование этого термина, но об этом позднее.
Общее представление о гальванике
Гальваническое покрытие может быть как технологическим, так и декоративно-защитным. Оно представляет собой тонкий поверхностный слой металла, обладающего хорошим эстетичным видом (золото, серебро) или антикоррозионными свойствами (цинк, медь) на металлических или пластмассовых изделиях.
В общих чертах гальваника металла в домашних условиях выглядит несложно.  В ванночку с электролитом опускаются аноды, которые подключаются к «плюсу», а между ними – в качестве катода – обрабатываемая деталь, подключенная к «минусу». Когда электрическая цепь замыкается, металл, который содержится в электролите, осаждается на катод, то есть изделие.
В ванночку с электролитом опускаются аноды, которые подключаются к «плюсу», а между ними – в качестве катода – обрабатываемая деталь, подключенная к «минусу». Когда электрическая цепь замыкается, металл, который содержится в электролите, осаждается на катод, то есть изделие.
Оборудование для гальваники
В домашних условиях и оборудование можно сделать своими руками. В первую очередь нужен источник питания, так как процесс протекает под действием электрического тока. В показателях силы тока домашние мастера расходятся, называя их в очень большом диапазоне. Но обязательным условием является наличие регулятора напряжения для плавного изменения выходной мощности. Ток должен быть постоянным, поэтому в качестве источника называют выпрямитель собственного или заводского изготовления.
Умельцы приспосабливают сварочный аппарат для гальваники в домашних условиях.
Для электролита нужна емкость (ванночка) из химически нейтрального материала. Это может быть стеклянная или пластиковая посудина достаточных размеров, чтобы в нее помещалась для обработки деталь и необходимое количество электролита. Она должна выдерживать высокую, до 80 °С, температуру и быть достаточно прочной.
Еще нужны аноды, площадь которых должна быть больше площади детали. Они служат для подвода электрического тока в электролит и его равномерного распределения по детали. Кроме того, они должны в электролите возмещать убыль металла, который выделяется при покрытии изделий, и выполнять некоторые окислительные процессы.
Нагревательные приборы для доведения электролита до нужной температуры лучше использовать с возможностью регулирования тепловых режимов. Например, бытовая газовая плита для этой цели не подходит. Обычно используют маленькую электроплитку и утюг, в котором можно установить необходимую температуру подошвы.
Оборудование для приготовления электролита
Для хранения химических реактивов и электролитов нужна стеклянная посуда с притертыми крышками.
Для приготовления электролитов необходимые вещества нужно отмерять с точностью до одного грамма. Для этого нужны соответствующие весы. Их можно приобрести или изготовить самостоятельно, используя в качестве гирек советские монетки, номинал которых точно соответствует массе.
Гальваника в домашних условиях – это и приготовление электролита из добытых непростым путем химических реактивов. Специализированные фирмы, торгующие такими высококачественными веществами, не редкость, но их деятельность подконтрольна, и работа с ними требует наличия специальных разрешительных документов даже для юридических лиц. Частным лицам опасные химические вещества не продают.
Подготовка изделия к гальванике
Собрав все необходимое (найдя в гараже, закупив и смонтировав своими руками), можно приступать к подготовке детали. Этот этап работ очень ответственный. Успешная гальваника в домашних условиях требует тщательной очистки детали. От подготовки поверхности зависит и качество гальванического покрытия. Поэтому, в зависимости от желаемого результата, деталь не только обезжиривают. Во многих случаях требуется пескоструйная обработка, затем шлифовка с помощью наждачной бумаги и шлифовочных паст.

Для обезжиривания детали промывают либо в чистых органических растворителях, ацетоне, спирте или бензине, либо в подготовленных растворах. Например, для обезжиривания стальных или чугунных деталей используются горячие, до 90 °С, растворы с едким натром, кальцинированной содой, жидким стеклом, фосфорнокислым натрием.
А изделия из цветных металлов обрабатываются в растворах с хозяйственным мылом и тем же фосфорнокислым натрием.
Окисную пленку снимают в специальных декапирующих растворах с соляной или серной кислотой.
Техника безопасности при работах
Гальваника в домашних условиях (хромирование, меднение, никелирование) – процесс опасный. Во-первых, из-за токсичности используемых веществ. Во-вторых, из-за необходимости нагрева растворов до высоких температур. А в-третьих, из-за риска, с которым связаны любые электрохимические процессы.
Не стоит воспринимать термин «в домашних условиях» буквально. Лучше заниматься гальваникой в гараже или другом нежилом помещении с хорошей вентиляцией. Используемое электрическое оборудование нужно обязательно заземлять.
И очень важно позаботиться о личной безопасности. Ни в коем случае нельзя что-либо пить или есть во время процесса, чтобы не наглотаться заодно и вредных испарений.
Работать нужно в респираторе, резиновых, прочных и мягких перчатках, плотном клеенчатом фартуке и обуви, защищающей кожу ног. Нужно беречь глаза, чтобы в них не попали мелкие брызги реактивов. Не будет лишним и перечитать специальную литературу по этой теме, чтобы подготовиться к возможным неожиданностям.
Никелирование металлических изделий
Никелирование может быть финишным или промежуточным (перед хромированием) покрытием. Этот процесс не вызывает особых сложностей, поверхности имеют красивый внешний вид, стойки к атмосферным воздействиям.
Температура электролита не выше 25 °С при плотности тока до 1,2 А/кв. дм.
В электролит входят водные растворы сернокислого никеля, натрия и магния, чистая поваренная соль (хлористый натрий) и борная кислота.
Необходимую кислотность электролита – 4-5 рН – проверяют лакмусовой бумагой. Она должна окраситься в красный цвет. Процесс занимает около получаса в зависимости от плотности тока и толщины наносимого покрытия.
После окончания процесса изделие нужно промыть в воде, высушить и отполировать на войлочном круге с полирующей пастой.
Хромирование изделий из металла
Хромируют металлические детали для повышения их твердости и стойкости к коррозии, для получения декоративного эффекта. Из-за пористости хромового покрытия перед его нанесением сначала выполняется гальваника медью в домашних условиях или никелирование, а то и поочередное нанесение этих покрытий.
Стабильный процесс хромирования обеспечивают аноды, изготовленные из сплава свинца с оловом и сурьмой в пропорциях 85%:11%:4% соответственно.
Как гальваника в домашних условиях, хромирование сложней и многообразней никелирования. Во-первых, от температуры электролита зависит оттенок покрытия. При температурах в диапазоне от 35 до 55 °С оно блестящее, выше 55 °С – молочное, ниже 35 °С – матовое.
Во-вторых, от состава электролита зависит цвет и физические параметры хромового покрытия. Оно может быть обычным защитным, темно-голубым, агатовым, синим или даже черным декоративно-защитным. Износостойкое защитное покрытие в домашних условиях выполнить сложно, так как нужны токи высокой плотности – до 100 А/кв. дм.
Износостойкое защитное покрытие в домашних условиях выполнить сложно, так как нужны токи высокой плотности – до 100 А/кв. дм.
При комнатной температуре и плотности тока до 5 А/кв. дм получается декоративное мягкое покрытие.
После завершения гальванического процесса хромирования деталь промывают в воде, затем нейтрализуют в легком растворе обычной пищевой соды, опять тщательно промывают, сушат и полируют со специальными пастами.
Меднение металлических изделий
Для чего еще может понадобиться гальваника в домашних условиях? Меднение производят для нанесения на поверхность тонкого токопроводящего слоя с малым сопротивлением или для защиты основного металла детали.
Наносить медь на черные металлы в домашних условиях, так как в этом процессе используются цианистые электролиты, смертельно опасно. Поэтому стальные или чугунные детали сначала никелируют, а только потом покрывают медью в электролитах из раствора медного купороса и концентрированной серной кислоты в воде комнатной температуры. Плотность тока при этом невысокая – до 2 А/кв. дм.
Алюминиевые детали тоже требуют предварительной подготовки. Их сначала декапируют (очищают от окисной пленки), затем оксидируют в электролите из водного раствора серной кислоты, затем тщательно промывают. Только потом выполняется гальваника в домашних условиях – меднение в электролите из медного купороса и водного раствора серной кислоты при достаточно низких температурах, до 20 °С, и низкой плотности тока. В качестве анода используется обычная медная пластина подходящей площади.
Серебрение и золочение изделий
Гальваническое серебрение – это не только декоративное, но и защитное, и электропроводящее покрытие с хорошей отражающей способностью. Изделия из черных металлов предварительно покрываются никелем, на который уже осаждается серебро.
Электролит для серебрения состоит из хлористого серебра, железноцианистого калия, кальцинированной соды и дистиллированной воды. Рабочая температура электролита не выше 20 °С, не требуется и высокая мощность тока – она не больше 0,1 А/кв. дм. В качестве анода используются графические пластины.
Наиболее декоративная и потому соблазнительная гальваника в домашних условиях – золочение. Процесс производят в горячих растворах золота (до 5 г на литр воды) с синеродистым калием. В холодных растворах количество металла нужно увеличивать втрое. Пары синеродистой кислоты очень ядовиты, поэтому процесс золочения в горячем растворе необходимо производить только в помещениях с мощной принудительной вытяжкой.
При работе с холодным раствором с синеродистой кислотой тоже нужно соблюдать предельную осторожность: не склоняться над ванной, не совать в нее руки, особенно со свежими ссадинами или царапинами.
Еще лучше ядовитую кислоту заменить желтой кровавой солью, то есть железистосинеродистым калием. Перед приготовлением электролита обычное золото превращают в хлорное при помощи царской водки, если, конечно, нет возможности приобрести готовое.
Как сделать гальванику в домашних условиях? Нужно тщательно очистить изделие. Затем, если оно выполнено из свинца, олова, железа, цинка или стали, его нужно предварительно покрыть медью. Затем для того, чтобы облегчить приставание золота, предмет нужно окунуть в раствор азотнокислой ртути.
Плотность тока должна быть не выше 1 А/кв. дм, так как при более сильных токах золото из электролита оседает на дно ванны в виде черного порошка, а позолота на изделии становится буроватого цвета.
Для того чтобы была красивой позолота, нужно у анода подвесить достаточно большой листик золота. После завершения гальванического процесса позолоченное изделие нужно просушить в опилках и отполировать.
Гальваника в домашних условиях
Подводя итоги о возможности нанесения гальванического покрытия в домашних условиях, можно сказать, что человеку, не разбирающемуся в электрохимии хотя бы на начальном уровне, организовывать процесс не стоит – слишком опасно. Кроме информации на различных сайтах и форумах, нужно обязательно читать специальную литературу. К тому же частное лицо не имеет доступа к реактивам. Поэтому, если нужно восстановить хромирование на одной детали, значительно дешевле обратиться к специалистам.
Ну а если уж очень хочется освоить новое производство самостоятельно, то тоже нужно попросить о помощи профессионалов, которые подберут необходимое безопасное оборудование (ведь производство не должно быть совсем уж кустарным), блоки питания, электролиты, не содержащие токсичных веществ, рассчитают параметры ванн и анодов. А также обучат процессам нанесения металлического покрытия, всем тем процедурам (их ведь не так много), которые приводят к желаемому результату.
Гальваника для лица в домашних условиях
После всего описанного выше такое название звучит несколько угрожающе. На самом же деле это всего лишь глубокое очищение кожи с помощью гальванических токов малой мощности. Под воздействием этих токов кожные жиры растворяются и выходят на поверхность лица, покрытого специальным составом, взаимодействуя с которым, превращаются в мыло.
Гальванические токи в медицине используются для усиления работы ионов. Это активно заряженные частицы, отвечающие за многие рабочие процессы в клетках. Под воздействием постоянного тока ионы перемещаются, улучшается проницаемость клеточных мембран, запускается выработка волокон коллагена и эластина, увеличивая прочность, упругость и эластичность кожи.
Гальванические токи проводят в глубокие слои дермы косметические средства с собственным электрическим зарядом. То есть процесс оздоровления кожи проходит изнутри, исчезают глубокие морщины, сужаются расширенные поры, кожа усиленно насыщается кислородом.
Аппарат «Гальваника + микротоки» в домашних условиях M365 Gezatone на сегодня наиболее доступная модель косметологического прибора нового поколения. Он помогает избавиться от угрей, разгладить морщины на увядающей коже, снизить проявления сосудистой сеточки, укрепить сосуды, улучшить контуры лица, убрать второй подбородок.
Процедура гальванической чистки лица
До начала процедуры кожу очищают обычными средствами: молочком или гелем. Затем наносят щелочной состав. Затем начинается непосредственно гальваника в домашних условиях. Gezatone Beauty Lifting – специальный аппарат для процедуры не только гальванической чистки, но и для введения в кожу питательных веществ под действием тех же токов. Процедура длится около пятнадцати минут – только круговые движения наконечником вдоль массажных линий лица, и ничего более – затем образовавшееся при реакции жиров со щелочью мыло смывается теплой водой.
Но токи есть токи, даже с приставкой «микро». Запрещено проходить процедуру гальванической чистки людям с вживленным кардиостимулятором, онкологическими заболеваниями, невротическими состояниями, болезнями кожи.
Настолько ли эффективна, как утверждают производители, гальваника для лица в домашних условиях, отзывы женщин, пользующихся приборами, с уверенностью утверждать не могут. Как правило, дамы спешат поделиться впечатлениями в первые месяцы после покупки, когда еще не так ощущаются последствия. Но все равно отзывы оптимистические.
В заключение можно сказать, что гальваника в домашних условиях – это не только опасный для здоровья процесс нанесения металлического покрытия на изделия, который в собственно жилом помещении осуществлять не стоит, но и современная безболезненная, безопасная и достаточно эффективная процедура омоложения кожи лица, шеи и зоны декольте.
businessman.ru

