Газ co2: Углекислый газ CO2
alexxlab | 06.10.2019 | 0 | Разное
Углекислый газ CO2
Углекислый газ «един» на Земле во множестве разных «обличий»: не боясь ошибиться, его можно именовать «диоксид углерода», «двуокись углерода», «оксид углерода», «угольный ангидрид» или даже «углекислота». При обычных условиях данный газ обладает плотностью, большей, нежели плотность воздуха, практически не обладает запахом (что касается больших концентраций, он демонстрирует слабый кисловатый аромат «соды») и способен перевоплощаться из твёрдого вещества в газ, а при условии повышенного давления превращается в жидкость. Данный газ является растворимым в водной среде, он негорюч, однако в нём может осуществляться горение активных металлов – таких как, например, магний или барий. Химической формулой углекислоты является СО2.
Распространение углекислоты в природе и в человеческом организме
Ещё задолго до возникновения жизни на Земле углекислота была основой атмосферы. В настоящее время её нахождение в воздухе определяется средними отметками 0.04 %. Накопление СО2 в атмосфере приводит к образованию углекислотных облаков, что провоцирует похолодание.
Выделением углекислого газа сопровождаются гниение, а также горение органических веществ. Также он, как известно, производится при дыхании растительных культур и живых организмов: за сутки среднестатистический человек производит таким образом примерно один килограмм углекислого газа. Он транспортируется от тканей, в которых образуется как один из завершающих продуктов метаболизма, проходит по венам, а затем выдыхается через лёгкие. Следовательно, эпицентром скопления углекислого газа в организме является венозная система, чуть меньше его находится в лёгких и совсем в незначительных количествах он присутствует в артериальной крови.
В организме человека СО2 играет большую роль в ауторегуляции кровотока и регуляции рН крови. Кроме того, в определённых соотношениях он положительно влияет на миокард.
Распространённые сферы применения углекислого газа
Угольный ангидрид широко применяется в пищевом производстве – например, в качестве разрыхлителя и консервирующего вещества, что обозначается на упаковке продукта специальным кодом Е290. Кроме этого, углекислота получила распространение как средство для газирования лимонада, энергетиков и других популярных газированных напитков.
В медицине одной из важнейших сфер использования двуокиси углерода является криохирургия: здесь данный газ выступает в качестве главного инструмента криоабляции новообразований в человеческом организме.
Жидкий СО2 активно используется в системах пожаротушения. Углекислый газ формирует защитную среду в процессе сварки проволокой. Помещённая в баллоны, углекислота может служить источником питания двигателей в авиамоделировании. Твёрдый угольный ангидрид или так называемый «сухой лёд» находит применение в роли хладагента в лабораторной практике, а также в процессе ремонта оборудования.
Токсическое влияние СО2 на живые организмы
Увеличенное содержание углекислого газа в воздушной среде приводит к токсическому влиянию на живые организмы, так, что безобидная углекислота превращается в удушающий газ IV класса опасности. При слабом превышении СО2 (до 0.2-0.4 % или 2000−4000 ppm) у человека может отмечаться слабость, сонливость, снижение концентрации внимания. Содержание 7-10 % порождает головную боль, проблемы со слухом, провоцирует потерю сознания.
Для закрытых помещений уровень CO2 в норме должен составлять приблизительно 600 ppm, однако в учебных аудиториях, как правило, концентрация углекислоты находится на отметках 2000-2500 ppm, что значительно ухудшает результаты учебной деятельности и вызывает серьёзную обеспокоенность у исследователей.
Необходимость и основные методы регистрации углекислоты
Различные варианты исследований углекислого газа востребованы во многих отраслях деятельности человека. К примеру, в медицине и различных технологических процессах существует необходимость определения его парциального давления – для исследования дыхательных смесей, предназначенных для искусственной вентиляции лёгких, мониторинга концентрации газа в замкнутых пространствах для профилактики болезней и патологических состояний живых организмов и растений и т. д. Концентрация СО2 также является важным предметом исследования экологов – например, в ходе изучения парникового эффекта.
Регистрация углекислоты осуществляется посредством использования специализированных газоизмерительных систем – например, анализаторов газа, функционирующих по принципу инфракрасной спектроскопии. Медицинский газоанализатор качества СО2, регистрирующий содержание диоксида углерода в воздухе, выдыхаемом человеком, носит название капнограф.
Углекислый газ — Циклопедия
| Углекислый газ | |
| Общие | |
|---|---|
| Систематическое наименование | Диоксид углерода |
| Традиционные названия | углекислый газ, двуокись углерода, сухой лёд (в твёрдом состоянии) |
| Химическая формула | CO2 |
| Физические свойства | |
| Состояние | бесцветный газ |
| Молярная масса | 44,01 г/моль |
| Плотность | газ 1,97680 кг/м³ ж. 9250°С, 35,5 ат кг/м³ тв. 1560-78,5 кг/м³ |
| Динамическая вязкость | 8,5·10-5 Па·с (10°C; 5,7 МПа) |
| Термические свойства | |
| Т. субл. | -78,5 °C |
| Тройная точка | -56,6°C; 0,52 МПа |
| Кр. точка | 31,1 °C; 7,38 МПа |
| Уд. теплоёмк. | 846 Дж/(кг·К) |
| Удельная теплота плавления | 25,13 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 1,45 кг/м³ |
| Классификация | |
| Рег. номер CAS | 124-38-9 |
| RTECS | FF6400000 |
| Безопасность | |
| S-фразы | S9, S23, S36 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Диоксид углерода (оксид углерода (IV), углекислый газ, CO2) — прочное химическое соединение, распространено в природных газах, содержащих его в количестве от нескольких процентов до практически чистого углекислого газа. Конечный продукт окисления углерода, не горит, не поддерживает горения и дыхания. Токсическое действие углекислого газа оказывается при его содержании в воздухе 3-4 % и заключается в раздражении дыхательных путей, головокружении, головной боли, шуме в ушах, психическом возбуждении, бессознательном состоянии.
Удушающий газ, без цвета и запаха, является естественной составляющей атмосферы Земли. Углекислый газ является продуктом сжигания ископаемого топлива. Он способствует удержанию тепла на поверхности Земли и вносит основной вклад в глобальное потепление.
При температуре 20 °C в 1 объеме воды растворяется 0,88 объемов CO2. Водный раствор его имеет кисловатый вкус. В отличие от монооксида, диоксид углерода является солеобразующим оксидом — ангидридом угольной кислоты H2CO3.
Под давлением около 60 атм диоксид углерода при обычной температуре превращается в жидкость. В сжиженном состоянии в стальных баллонах его можно хранить и транспортировать. При сильном охлаждении он превращается в снегообразную массу (сухой лед), которая сублимирует (испаряется, не плавясь) при −78,5 °С.
Диоксид углерода не поддерживает дыхание и горение обычных видов топлива. Но некоторые активные металлы могут отнимать у него кислород. Так, например, зажженная свеча гаснет в атмосфере CO2, а зажженная магниевая лента продолжает гореть:
Незначительные количества CO2 безвредны для человека и животных, но при концентрации его в воздухе более 3 % по объему он становится вредным, а при 10 % и более — смертельным.
В народном хозяйстве диоксид углерода широко применяется в химической промышленности при производстве соды, мочевины и т. п., а также в производстве сахара, вина, пива, для изготовления газированной воды и т. д. Широко известны природные источники диоксида углерода в виде минеральных вод «Нарзан», «Боржоми» и другие. Спрессованный твердый CO2 под названием «сухой лед» применяют для охлаждения мяса, рыбы и других пищевых продуктов, которые быстро портятся. Сухой лед гораздо больше, чем обычный, снижает температуру и при испарении не оставляет никакой жидкости. В промышленности диоксид углерода получают разложением карбоната кальция:
В лабораторных условиях его обычно получают при действии соляной кислоты на мрамор:
- CaCO3 + 2HCl = CaCl2 + CO 2↑ + H2O
В природе диоксид углерода постоянно образуется при самых процессах: горении угля и других видов топлива, дыхании, брожении, гниении и т. п.
При выделении углекислого газа из почвы выработки и отсутствии активной струи воздуха в нижней её части могут образовываться застойные зоны с высокой концентрацией. В рудничной атмосфере углекислый газ присутствует всегда, потому что он образуется в большом количестве за счет биохимических и химических реакций окисления, протекающих в горных выработках. Конечно, выделения природного углекислого газа в горные выработки незначительны, исключением является выделение углекислого газа магматического происхождения в некоторых угольных и калийных месторождениях. Предельно допустимое содержание углекислого газа в шахтном воздухе 0,5-1 % (по объему). При 10 % наступает обморок, при 20-25 % — смертельное отравление. Первая помощь при отравлении заключается в вынесении пострадавшего на свежий воздух, проведении искусственного дыхания.
[править] Углекислый газ в атмосфере земли
По экспертной оценке ООН за 2016 год, содержание углекислоты в атмосфере выросло более чем на 45% по сравнению с доиндустриальным периодом[1].
По состоянию на 2018 год наибольшими источниками выбросов углекислого газа в атмосферу являются производственные предприятия, затем следует туристическая отрасль – выхлопы самолётов (до 10%), а так же предприятия общепита, рестораны и кафе[2].
[править] Концентрация углекислого газа в атмосфере Земли
Уровень углекислого газа в атмосфере[2]:
- XVIII—XIX век – не более 300 ppm (мл. на кубометр воздуха)
- 1958 год – 315 ppm
- 2018 год – 410 ppm
- Деркач Ф. А. Химия. — Львов: Львовский университет, 1968. — 312 с.
- Малая горная энциклопедия: в 3 т. / под ред. В. С. Белецкого. — Донецк: Донбасс, 2004.
Оксид углерода(IV) – это… Что такое Оксид углерода(IV)?
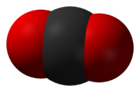
| Оксид углерода (IV) | |
|---|---|
_   | |
| Другие названия | углекислый газ, двуокись углерода, сухой лёд(твердый) |
| Формула | CO2 |
| Молярная масса | 44,0095(14) г/моль |
| В твердом виде | сухой лёд |
| Вид | бесцветный газ |
| Номер CAS | [124-38-9] |
| Свойства | |
| Плотность и фазовое состояние | 1,9769 кг/м³, при н.у.; 771 кг/м³, жидкий; 1512 кг/м³, твёрдый |
| Растворимость в воде | 1,45 кг/м³ |
| Удельная теплоемкость | 0,846 кДж/(кг*С) при 27 °C |
| Удельная теплота плавления | 25,13 кДж/моль |
| Точка плавления | −57 °C (216 K), под давлением |
| Точка кипения | −78 °C (195 K), возгоняется |
| Константа диссоциации кислоты (pKa) | 6,35 и 10,33 |
| Вязкость | 0,07 пз при −78 °C |
| Строение | |
| Форма молекулы | линейная |
| Кристаллическая решётка | молекулярная |
| Дипольный момент | ноль |
| Техника безопасности | |
| MSDS | External MSDS |
| Главные опасности | удушающее, раздражающее |
| NFPA 704 | |
| R-phrases | R: As, Fb [источник не указан 1315 дней] |
| S-phrases | S9, S23, S36 (ж) [источник не указан 1315 дней] |
| RTECS number | FF6400000 |
| Страница дополнительных сведений | |
| Структура и свойства | n, εr, и т. д. |
| Спектр | УФ, ИК, ЯМР, Масс-спектроскопия |
| Родственные соединения | |
| Оксиды | CO C стандартных условиях (25 °C, 100 кПа) Infobox disclaimer and references |
Оксид углерода(IV) (углекислый газ, диоксид углерода, двуокись углерода, угольный ангидрид) — CO2, бесцветный газ (в нормальных условиях), без запаха, со слегка кисловатым вкусом.
Концентрация углекислого газа в атмосфере Земли составляет в среднем 0,0395 %.[1]
Не следует путать с Диоксином.
Плотность при нормальных условиях 1,97 кг/м³. При атмосферном давлении диоксид углерода не существует в жидком состоянии, переходя непосредственно из твёрдого состояния в газообразное. Твёрдый диоксид углерода называют сухим льдом. При повышенном давлении и обычных температурах углекислый газ переходит в жидкость, что используется для его хранения.
Углекислый газ легко пропускает ультрафиолетовые лучи и лучи видимой части спектра, которые поступают на Землю от Солнца и обогревают её. В то же время он поглощает испускаемые Землёй инфракрасные лучи и является одним из парниковых газов, вследствие чего принимает участие в процессе глобального потепления. Постоянный рост уровня содержания этого газа в атмосфере наблюдается с начала индустриальной эпохи.
Свойства
Физические
Оксид углерода (IV) – углекислый газ, газ без цвета и запаха, тяжелее воздуха, растворим в воде, при сильном охлаждении кристаллизуется в виде белой снегообразной массы – «сухого льда». При атмосферном давлении он не плавится, а испаряется, температура сублимации -78 °С. Углекислый газ образуется при гниении и горении органических веществ. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Мало растворим в воде (1 объем углекислого газа в одном объеме воды при 15 °С).
Химические
По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует угольную кислоту. Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов. Вступает в реакции электрофильного замещения (например, с фенолом ) и нуклеофильного присоединения (например, с магнийорганическими соединениями).
Биологические
Диоксид углерода играет одну из главных ролей в живой природе, участвуя во многих процессах метаболизма живой клетки. Диоксид углерода получается в результате множества окислительных реакций у животных, и выделяется в атмосферу с дыханием. Углекислый газ атмосферы — основной источник углерода для растений. Однако, ошибкой будет утверждение, что животные только выделяют углекислый газ, а растения — только поглощают его. Растения поглощают углекислый газ в процессе фотосинтеза, а без освещения они тоже его выделяют.
Диоксид углерода не токсичен[источник не указан 60 дней], но не поддерживает дыхание. Большая концентрация в воздухе вызывает удушье (см. Гиперкапния). Однако недостаток углекислого газа тоже опасен (см. Гипокапния)[источник не указан 60 дней].
Углекислый газ в организмах животных имеет и физиологическое значение, например, участвует в регуляции сосудистого тонуса (см. Артериолы).
Получение
В промышленных количествах углекислота выделяется из дымовых газов, или как побочный продукт химических процессов, например, при разложении природных карбонатов (известняк, доломит) или при производстве алкоголя. Смесь полученных газов, промывают раствором карбоната калия, которые поглощают углекислый газ, переходя в гидрокарбонат. Раствор гидрокарбоната при нагревании или при пониженном давлении разлагается, высвобождая углекислоту. В современных установках получения углекислого газа вместо гидрокарбоната, чаще применяется водный раствор моноэтаноламина, который при определённых условиях способен абсорбировать СО₂, содержащийся в дымовом газе, а при нагреве отдавать его, таким образом, отделяется готовый продукт от других веществ.
Также углекислый газ получают на установках разделения воздуха, как побочный продукт получения чистого кислорода, азота и аргона.
В лабораторных условиях небольшие количества получают взаимодействием карбонатов и гидрокарбонатов с кислотами, например мрамора, мела или соды с соляной кислотой. Использование реакции серной кислоты с мелом или мрамором приводит к образованию малорастворимого сульфата кальция, который мешает реакции, и который удаляется значительным избытком кислоты.
Для приготовления напитков может быть использована реакция пищевой соды с лимонной кислотой или с кислым лимонным соком. Именно в таком виде появились первые газированные напитки. Их изготовлением и продажей занимались аптекари.
Применение
В пищевой промышленности углекислота используется как консервант и разрыхлитель, обозначается на упаковке кодом Е290.
Жидкая углекислота широко применяется в системах пожаротушения, в огнетушителях и для производства газированной воды и лимонада.
Углекислый газ используется в качестве защитной среды при сварке проволокой, но при высоких температурах происходит его диссоциация с выделением кислорода. Выделяющийся кислород окисляет металл. В связи с этим приходится в сварочную проволоку вводить раскислители, такие как марганец и кремний. Другим следствием влияния кислорода, также связанного с окислением, является резкое снижение поверхностного натяжения, что приводит, среди прочего, к более интенсивному разбрызгиванию металла, чем при сварке в аргоне или гелии.
Углекислота в баллончиках применяется в пневматическом оружии (в газобаллонной пневматике) и в качестве источника энергии для двигателей в авиамоделировании, а также для накачивания шин/камер велосипедных колес.[источник не указан 85 дней].
Когда углекислота применяется в газовой фазе, то для хранения она используется под давлением, как сжиженный газ, в виде жидкой фазы. Хранение углекислоты в баллоне в сжиженном состоянии намного выгоднее, чем в виде газа. Углекислота имеет сравнительно низкую критическую температуру 31°С. Когда в 40-литровый баллон с нормальным давлением 100 кгс/сm² залито 30 кг сжиженного углекислого газа, то при температуре 31°С в баллоне будет только жидкая фаза с давлением 100 кгс/сm². Если температура будет выше, то следует уменьшить заполнение баллона или использовать баллоны с более высоким рабочим давлением. Если углекислота будет охлаждаться, то при температуре 21°С при нормальном заполнении в баллоне появиться газовая фаза.
Твёрдая углекислота — «сухой лёд» — используется в качестве хладагента в лабораторных исследованиях, в розничной торговле и т.д.
Методы регистрации
Измерение парциального давления углекислого газа требуется в технологических процессах, в медицинских применениях — анализ дыхательных смесей при искусственной вентиляции лёгких и в замкнутых системах жизнеобеспечения. Анализ концентрации CO2 в атмосфере используется для экологических и научных исследований, для изучения парникового эффекта. Углекислый газ регистрируют с помощью газоанализаторов основанных на принципе инфракрасной спектроскопии и других газоизмерительных систем. Медицинский газоанализатор для регистрации содержания углекислоты в выдыхаемом воздухе называется капнограф.
Углекислый газ в природе
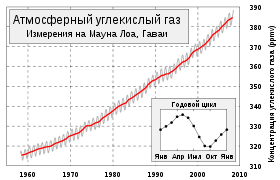 Изменения концентрации атмосферного углекислого газа (кривая Килинга). Измерения в обсерватории на горе Мауна-Лоа, Гавайи.
Изменения концентрации атмосферного углекислого газа (кривая Килинга). Измерения в обсерватории на горе Мауна-Лоа, Гавайи.Ежегодные колебания концентрации атмосферной углекислоты на планете определяются, главным образом, растительностью средних (40—70°) широт Северного полушария.
Вегетация в тропиках практически не зависит от сезона, сухой пояс пустынь 20—30° (обоих полушарий) дает малый вклад в круговорот углекислоты, а полосы суши, наиболее покрытые растительностью, расположены на Земле асимметрично (в Южном полушарии в средних широтах находится океан).
Поэтому с марта по сентябрь вследствие фотосинтеза содержание СО2 в атмосфере падает, а с октября по февраль — повышается. Вклад в зимний прирост дают как окисление древесины (гетеротрофное дыхание растений, гниение, разложение гумуса, лесные пожары), так и сжигание ископаемых топлив (угля, нефти, газа), заметно увеличивающееся в зимний сезон[2].
Большое количество углекислоты растворено в океане.
Углекислый газ составляет значительную часть атмосфер некоторых планет Солнечной системы: Венеры, Марса.
Токсичность
Углекислый газ является тяжелым, по сравнению с воздухом, газом без цвета и запаха. Воздействие его повышенных концентраций на живые организмы относит его к удушающим газам (англ.)русск.. Незначительные повышения концентрации до 2-4% в непроветриваемых помещениях приводят к развитию сонливости и слабости. Опасными концентрациями считаются уровни 7-10%, при которых развивается удушье, проявляющее себя в головной боли, головокружении, расстройстве слуха и в потери сознания в течение периода времени от нескольких минут до одного часа.[3] Отравление этим газом не приводит к долговременным последствиям и после его завершения происходит полное восстановление организма.[4]
Интересные факты
- Подземное животное голый землекоп отличается терпимостью к большим (смертельным для других животных) концентрациям углекислого газа.[5]
- Бо́льшая, по сравнению с человеком, чувствительность других животных к изменениям концентрации этого газа использовалась в качестве естественного детектора опасных концентраций этого газа. Повышенная чувствительность к углекислоте канареек использовалась шахтерами для определения начала скопления этого газа под землей.
- В результате обычного функционирования организма каждого человека в среднем в течение одного дня образуется 1 кг углекислого газа (300 гр углерода).[6]
См. также
Примечания
- ↑ Trends in Carbon Dioxide
- ↑ А. В. Бялко. Растения убыстряют рост. «Природа». No 10, 1996. (по Keeling C.D., Whorf Т.P., Wahlen M., van der Plicht J. // Nature. 1995. V. 375, № 6533. P.666-670)
- ↑ (англ.) Carbon Dioxide as a Fire Suppressant: Examining the Risks, U.S. Environmental Protection Agency:.
- ↑ (англ.) Glatte Jr H. A., Motsay G. J., Welch B. E. (1967). «Carbon Dioxide Tolerance Studies». Brooks AFB, TX School of Aerospace Medicine Technical Report SAM-TR-67-77. Проверено 2008-05-02.
- ↑ А. Шиндер. Животное, не чувствующее боли. 2000-Аспекты-Проблемы № 26(420), 27 июня-3 июля 2008
- ↑ (англ.) How much carbon dioxide do humans contribute through breathing?.(недоступная ссылка — история) Проверено 30 апреля 2009.
Литература
- Вукалович М.П., Алтунин В.В., Теплофизические свойства двуокиси углерода, Атомиздат, Москва, 1965. 456 с.
- Тезиков А.Д., Производство и применение сухого льда, Госторгиздат, Москва, 1960. 86 с.
- Гродник М.Г., Величанский А.Я., Проектирование и эксплуатация углеслотных установок, ″Пищевая промышленность″, Москва, 1966. 275 с.
- Талянкер Ю.Е., Особенности хранения баллонов со сжиженным газом, Журнал “Сварочное производство”, №11, 1972, Москва.
Ссылки
Химические свойства углекислого газа, реакции с другими веществами
Общие химические свойства углекислого газа: CO2 инертен, то есть химически не активен; при попадании в водный раствор легко вступает в реакции.
Большинство кислотных оксидов устойчивы к высоким температурам, но углекислота при их воздействии восстанавливается.
Взаимодействие с другими веществами:
1) Углекислота относится к кислотным оксидам, то есть в сочетании с водой образуется кислота. Однако угольная кислота неустойчива и распадается сразу. Эта реакция имеет обратимый характер:
СО2 + H2O ↔ CO2 × H2O (растворение) ↔ Н2СО3
Диоксид углерода + вода ↔ угольная кислота
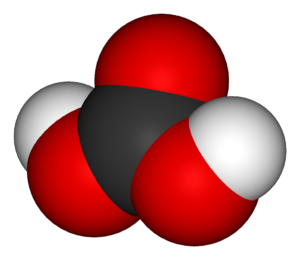
Молекула угольной кислоты
2) При взаимодействии углекислого газа и соединений азота с водородом (аммиаком) в водном растворе происходит разложение до углеаммонийной соли.
2NH3 + CO2 + H2O = NH4HCO3
Аммиак + углекислота = гидрокарбонат аммония

Углеаммонийная соль
Полученное вещество часто используется в приготовлении хлеба и различных кондитерских изделий.
3) Ход некоторых реакций должен поддерживаться высокими температурами. Примером является производство мочевины при 130 °C и давлении 200 атм., схематически изображаемое так:
2NH3 + СО2 → (NH2)2СО + H2O
Аммиак + диоксид углерода → карбамид + вода
Также под воздействием температуры около 800 градусов протекает реакция образования оксида цинка:
Zn + CO2 → ZnO + CO

Оксид цинка
Цинк + двуокись углерода → оксид цинка + оксид углерода
4) Возможно уравнение с гидроксидом бария, при котором выделяется средняя соль.
Ba(OH)2+CO2 = BaCO3 + H2O
Гидроксид бария + углекислота = карбонат бария + оксид водорода.
Применяется для регулировки калориметров по теплоемкости. Также вещество используют в промышленности для производства красных кирпичей, синтетических тканей, фейерверков, гончарных изделий, плитки для ванн и туалетов.
5) Углекислый газ выделяется при реакциях горения.
Горение метана.
CH4 + 2O2 → CO2 + 2H2O + 891кДж

Горение газа на плите
Метан + кислород = углекислота + вода (в газообразном состоянии) + энергия
Горение этилена
C2H4 + 3O2 → 2CO2 + 2H2O + Q
Этилен + кислород = диоксид углерода + оксид водорода + энергия
Горение этана
2С2Н6 + 7О2 → 4CO2 + 6H2O + Q
Этан + кислород = двуокись углерода + вода + энергия
Горение этанола
C2H5OH + 3O2 = 3H2O + 2CO2 + Q
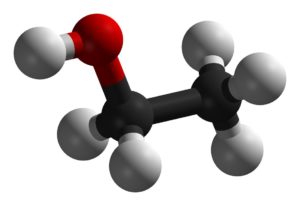
Молекула этанола
Этанол + кислород = вода + углекислота + энергия
6) Газ не поддерживает горения, этот процесс возможен только с некоторыми активными металлами, например, магнием.
2Mg + CO2 = C + 2MgO
Магний + углекислота = углерод + оксид магния.
MgO активно применяется при производстве косметических средств. Вещество используют в пищевой промышленности как пищевую добавку.
7) Двуокись углерода реагирует с гидроксидами с получением солей, которые существуют в двух формах, как карбонаты и бикарбонаты. Например, углекислый газ и гидроксид натрия, согласно формуле, образуют гидрокарбонат Na:
CO2 + NaOH → NaHCO3
диоксид углерода + гидроксид натрия → гидрокарбонат натрия.
Или же при большем количестве NaOH образуется карбонат Na с образованием воды:
CO2 + 2 NaOH → Na2CO3 + H2O
Диоксид углерода + гидроксид натрия → карбонат натрия + вода
Кислотно-щелочные реакции углекислоты используются на протяжении веков для затвердевания известкового раствора, что может быть выражено простым уравнением:
Ca(OH)2 + CO2 → CaCO3 + H2O
Гидроксид кальция + двуокись углерода → карбонат кальция + оксид водорода
8) В зелёных растениях играет важную роль в процессе фотосинтеза:
6CO2 + 6H2O → C6H12O6 + 6O2
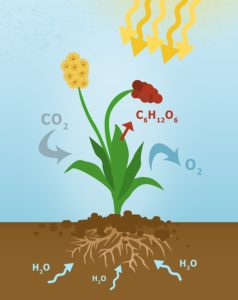
Образование глюкозы
Диоксид углерода + вода → глюкоза + кислород.
9) Химические свойства углекислоты используются в промышленности при производстве соды, суть этого процесса можно выразить суммарным уравнением:
NaCl + CO2 + NH3 + H2O → NaHCO3 + NH4Cl
Хлорид натрия + Диоксид углерода + аммиак + вода → гидрокарбонат натрия + хлорид аммония
10) Фенолят Na разлагается при взаимодействии с углекислым газом, при этом малорастворимый фенол выпадает в осадок:
C6H5ONa + CO2 + H2O = C6H5OH + NaHCO3
Фенолят натрия + двуокись углерода + оксид водорода = фенол + гидрокарбонат натрия
11) Пероксид натрия и углекислый газ, взаимодействуя, образуют среднюю соль карбоната Na с выделением кислорода.
2Na2O2 + 2CO2 → 2N2CO3 + O2
Пероксид натрия + углекислота → карбонат натрия + кислород

Колба с пероксидом натрия
Образование углекислоты происходит при растворении в воде кальцинированной соды (стиральной соды).
NaHCO3 + H2O → CO2 + H2O + NaOH
Гидрокарбонат натрия + вода → углекислота + вода + гидроксид натрия
При этой реакции (гидролиз по катиону) образуется сильнощелочная среда.
12) CO2 вступает в реакцию с гидроксидом калия, последний образуется путем электролиза хлористого калия.
2KOH + CO2 → K2CO3 + H2O
Гидроксид калия + углекислота → карбонат калия + вода
13) Газ в силу своего строения не реагирует с благородными газами, то есть гелием, неоном, аргоном, криптоном, ксеноном, радоном, оганесоном.
Заключение
Мы привели большую часть химических реакций, в которых участвует CO2. Ученые всего мира пытаются решить проблему увеличения концентрации углекислоты в воздухе, не без помощи реакций с другими веществами, которые известны химикам. А какие химические формулы взаимодействия углекислого газа знаете вы?
Разница между Диоксидом углерода (CO2) и Монооксидом углерода (CO)
Хотя обе молекулы содержат углерод и кислород, ключевое различие между Диоксидом углерода и Монооксидом углерода заключается в количестве у них атомов кислорода. Так Диоксид углерода или углекислый газ (CO2) имеет один атом углерода и два атома кислорода, а Монооксид углерода или угарный газ (СО) имеет один атом углерода и один атом кислорода.
Углекислый газ естественным образом присутствует в нашей атмосфере, поскольку он выделяется во время дыхания животных и людей. С другой стороны, угарный газ является токсичным и вызывает удушье, если он образуется при неполном сгорании угля или другого ископаемого топлива.
Содержание
- Обзор и основные отличия
- Что такое Диоксид углерода
- Что такое Монооксид углерода
- Сходство между Диоксидом углерода и Монооксидом углерода
- В чем разница между Диоксидом углерода и Монооксидом углерода
- Заключение
Что такое Диоксид углерода?
Диоксид углерода или углекислый газ — это химическое соединение состоящее из одного атома углерода и двух атомов кислорода. Он представлен молекулярной формулой как CO2. В твердом состоянии он известен как «сухой лед». Углекислый газ действует как парниковый газ и является одним из важнейших компонентов углеродного цикла.
 Диоксид углерода — углекислый газ
Диоксид углерода — углекислый газСуществует много источников CO2, которые включают природные источники, такие как сжигание органических веществ, вулканическая деятельность и процессы дыхания, выполняемые животными и людьми (где они вдыхают воздух насыщенный O2 и выдыхают воздух насыщенный CO2), а также процессы клеточного дыхания, выполняемый аэробными организмами. Другие источники CO2 включают сжигание древесины и ископаемого топлива, процесс ферментации, осуществляемый во многих отраслях промышленности.
Растения обеспечивают кислородом атмосферу и используют углекислый газ для осуществления процесса фотосинтеза, для выработки энергии. CO2 также является парниковым газом, который защищает атмосферу Земли от некоторых вредных излучений, отражая их обратно в космос.
CO2 имеет молекулярную массу 44 г/моль. Он имеет один атом углерода, присоединенный к двум атомам кислорода с обеих сторон и, таким образом, имеет линейную молекулярную форму. CO2 имеет ковалентные связи между атомами. Углекислый газ является негорючим газом. Отравление им встречается редко, но легкое отравление может наблюдаться, когда его концентрация становятся 3% от объёма воздуха, текущий уровень CO2 на планете составляет 0,0004% от объёма воздуха. Уровень CO2 8% от объёма воздуха считается опасным для жизни.
Что такое Монооксид углерода?
Монооксид углерода или окись углерода или угарный газ (CO) — это химическое соединение, имеющее молекулярную формулу СО и молекулярную массу 28,01 г/моль. Он имеет один атом углерода и один атом кислорода и имеет линейную структуру, в которой имеется тройная ковалентная связь между атомами. Среди этих связей одна связь является координатной ковалентной связью (один атом жертвует оба электрона в общей паре).
 Монооксид углерода — угарный газ
Монооксид углерода — угарный газCO — это газ без вкуса и запаха, но это ядовитый газ, и его вдыхание могут быть опасными для жизни. Как только окись углерода вдыхается, она попадает в кровоток и образует с гемоглобином — карбоксигемоглобин. В результате кровь не может снабжать кислородом клетки и ткани, что приводит к смерти человека. При слабом воздействии CO может вызвать головокружение, головную боль, боль в животе, замешательство и усталость.
Окись углерода образуется из-за неполного сгорания ископаемого топлива, газа, масел и древесины. Дым от сигарет и горящего угля также выделяет этот вредный газ. Бытовые приборы, такие как водонагреватели, плиты, газовые колонки, котлы, также являются источниками угарного газа.
Для контроля за уровнем CO в домах используются детекторы угарного газа, а также проводится профилактика систем вентиляции. Уровень угарного газа в 0.0001% от объёма воздуха является причиной головокружения и головной боли, тогда как 0.0000001% от объёма воздуха — это средний уровень СО на Земле. Концентрация около 0.0007% от объёма воздуха опасна для здоровья.
Сходство между Диоксидом углерода и Монооксидом углерода
- Оба газа безвкусны, бесцветны и не имеют запаха.
- Повышенные уровни CO2 и CO могут быть опасны для здоровья и иногда приводят к смерти.
- Углерод и кислород являются комбинациями образования для обоих газов.
- Они высвобождаются при сгорании.
Разница между Диоксидом углерода и Монооксидом углерода
- Углекислый газ — это это химическое соединение состоящее из углерода и кислорода. Его получают путем полного сжигания ископаемого топлива и углей. При комнатной температуре и нормальном давлении он находится в газообразном виде. Угарный газ также является химическим соединением углерода и кислорода и образуется при неполном сгорании угля, ископаемого топлива, древесины, а также при извержении вулканов.
- Молекулярная формула диоксида углерода — CO2, молярная масса 44 г/моль, тогда как молекулярная формула монооксида углерода — СО, а молярная масса 28 г/моль.
- Углерод и кислород имеют ковалентную связь в CO2, тогда как в СО углерод и кислород имеют тройную ковалентную связь.
- CO2 встречается в природе в атмосфере. Эти газы естественным образом образуются при дыхании животных и людей, при химических реакциях, ферментации и сжигании ископаемого топлива. Газ СО образуются при неполном сгорании ископаемого топлива, нефти, угля и природного газа.
- Углекислый газ является негорючим, безвкусным, без запаха и сравнительно безопасным газом, тогда как угарный газ — это горючий, ядовитый, бесцветный, безвкусный, а также без запаха.
Заключение — Диоксид углерода против Монооксида углерода
Разница между Диоксидом углерода и Монооксидом углерода заключается в атоме кислорода в этих молекулах. Диоксид углерода или углекислый газ имеет в молекуле два атома кислорода, а Монооксид углерода имеет один атом кислорода. Кроме того в больших концентрациях Диоксид углерода (углекислый газ) является токсичным газом, а Монооксид углерода (угарный газ) является чрезвычайно токсичным газом.
образование, транспорт кровью, влияние на здоровье
Содержание страницы
Вступление
Из курса биологии (анатомии) школьной программы известно, что наш организм дышит кислородом (O2). Однако на уроках не рассматривается вопрос о том, какое значение имеет углекислый газ в крови для нашего здоровья? Многие не знают, что CO2 влияет на здоровье всех органов человека и регулирует биохимические процессы, протекающие в организме.
Дыхание
При изучении дыхания и образования диоксида углерода в теле человека иногда путают углекислый и угарный газы между собой. Угарный газ имеет химическую формулу CO и совершенно другие свойства.
Оксид углерода (CO), это ядовитое вещество, которое при попадании через легкие в кровь даже в минимальном количестве опасно для жизни и здоровья.
Дыхание происходит следующим образом — человек сначала выдыхает углекислоту, а потом вдыхает кислород:
- В результате биохимических процессов при расщеплении жиров и белков в клетках происходит процесс образования углекислого газа в организме человека. Этот газ выделяется из клеток в капилляры, а затем поступает в кровь. При накоплении крови газом нервная система подает сигнал в мозг о выделении излишков двуокиси углерода за пределы нашего тела. Красные кровяные тельца (эритроциты) транспортируют молекулы углекислоты в виде химических соединений бикарбонатов и связанных с гемоглобином к альвеолам легких.
- В альвеолах происходит обмен молекул углекислого газа на молекулы O2, которые распространяются по всему организму. Эритроциты переносят молекулы кислорода к органам и тканям, связывая его с гемоглобином, а взамен опять забирают продукт жизнедеятельности этих клеток – CO2.
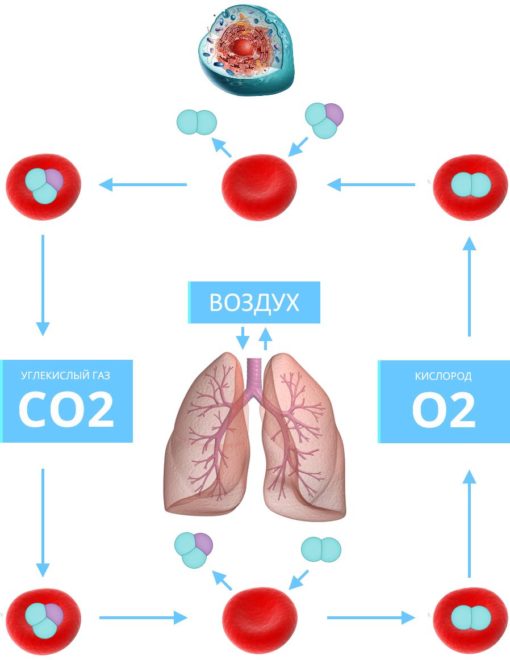
Процесс газообмена.
Доказанным фактом считается то, что углекислота, это основатель дыхательных процессов, а не кислород, как считалось ранее. Двуокись углерода является необходимым газом для дыхания человека наравне с O2.
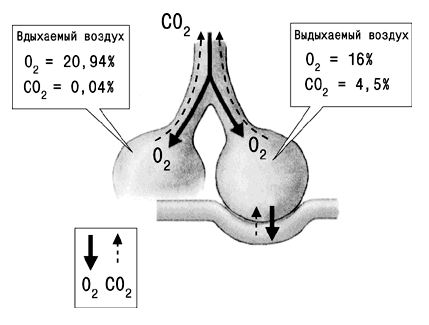
Газообмен в альвеолах
При выдохе человек выдыхает не только CO2, из легких уходит также избыточный O2. Рефлекс дыхания разделяется в 2 этапа:
- При выдыхании происходит снижение давления в легких, купол диафрагмы поднимается, легкие сжимаются, концентрация CO2 в крови повышается. Кровь движется по венам и окрашивается темный, почти черный цвет.
- За выдохом идет вдох. При вдохе грудная клетка расширяется, диафрагма опускается. Осуществляется отдача от гемоглобина через альвеолы в легкие и выброс в атмосферу диоксида углерода. Там же в альвеолах происходит прием гемоглобином молекулы O2. Кровь переходит на следующий круг и движется по артериям. Она окрашивается в ярко-розовый цвет.
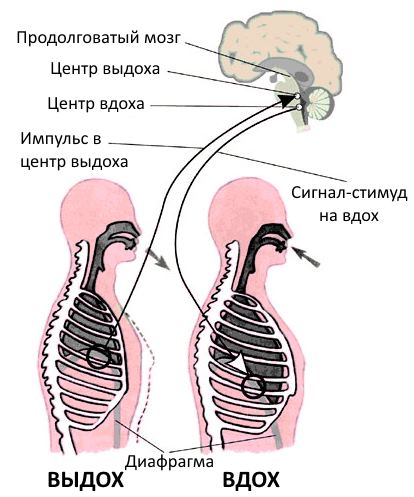
Нормальный здоровый человек дышит ровно и регулярно. Учащенное дыхание или с задержкой, если это не вызвано большими физическими или психологическими нагрузками, считается сигналом о серьезных заболеваниях организма.
Транспорт кровью и связь с кислородом.
Существует два круга кровообращения в организме: большой артериальный и малый венозный. По большому кругу транспортируется артериальная кровь, насыщенная кислородом. По малому кругу движется венозная кровь, насыщенная CO2.
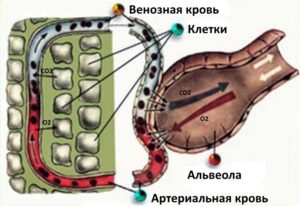
Транспорт газов кровью
Раньше существовало мнение, что с выдохом углекислый газ в организме человека не остается. Однако как показывают исследования, в артериальной крови всегда присутствует определенное количество углекислоты. Концентрация ее небольшая, в пределах 6,0-7,0%, но если она превышает или наоборот, меньше этого количества, то для организма это плохо. Появляется либо переизбыток O2 в крови (Гипероксия), либо его недостаток (Гипоксемия). Это происходит потому, что обмен этими газами взаимосвязан. Чтобы эритроцит мог поглотить молекулу кислорода и связать ее с гемоглобином, он должен удалить в атмосферу молекулу диоксида углерода.
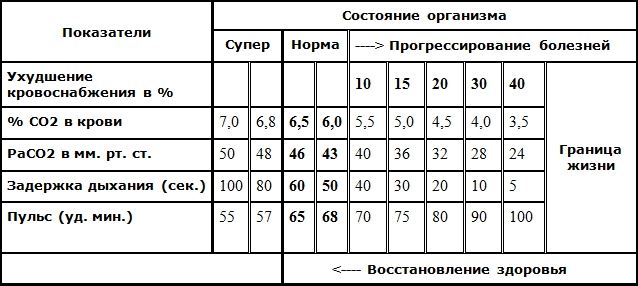
Зависимость здоровья от содержания углекислоты
При физических нагрузках обменные процессы в клетках ускоряются, чтобы вывести большее количество углекислоты, человеку необходимо чаще и глубже дышать. Процесс происходит рефлекторно. В таких случаях опасно находится в помещении с высокой концентрацией CO2, так как вместе с O2 человек вдыхает двуокись углерода. Это приводит к повышению ее концентрации в крови, а дальше к приступам удушья. Появляются головокружение, тошнота, вялость, учащается сердцебиение и дыхание (Гиперкапния).
Изучая процессы дыхания и газообмена в организме человека, ученые пришли к выводу, что опасен для здоровья не столько недостаток кислорода, сколько избыток диоксида углерода в воздухе.
Газ CO2 не является сильнодействующим отравляющим веществом, но так как гемоглобин занятый углекислым газом не принимает кислород, то происходит эффект удушения, вплоть до летального исхода.
Высокая концентрация этого вещества в крови приводит к гибели эритроцитов и воспалению стенок кровеносных сосудов. Так происходит если наличие углекислого газа в воздухе более 3 %. При таком уровне человек чувствует себя слабым, его тянет на сон. При концентрации 5% проявляется удушающий эффект, головные боли, головокружение.
Желудочно-кишечный тракт
Углекислый газ в организм попадает не только при дыхании, но и вместе с пищей. Углерод содержится практически во всех органических веществах, наибольшая концентрация содержится в продуктах растительного происхождения. Больше всего его образуется при расщеплении легкоусвояемых углеводов.

Углекислота влияет на химический состав жидкости в теле человека, хотя и не так значительно, но при сильном понижении или превышении может оказывать губительное воздействие. В организме почти все процессы жизнедеятельности клеток происходят при определенном уровне кислотно-щелочного баланса, который скорее близок к нейтральной воде, чем к кислоте. Наличие повышенной концентрации CO2 в употребляемых продуктах сильно меняет состав жидкости в теле человека. Это также влияет на протекание биохимических процессов. Происходит нарушение обмена веществ, гибель клеток или неправильный процесс их деления, что очень опасно.

Продукты и их кислотно-щелочной баланс
Поэтому продукты, содержащие CO2 в свободном состоянии (газировка) во многих странах запрещены к продаже.
Наибольший вред они наносят организму:
- При любых заболеваниях желудочно-кишечного тракта, в том числе хронических. Так как при приеме в пищу таких продуктов, происходит раздражение слизистой желудка. Они стимулируют выработку ферментов и повышают кислотность желудочного сока, что приводит к обострению имеющихся воспалительных процессов, образованию или углублению язвочек.
- Детям, до трех лет не стоит давать такие продукты, потому что их организм еще не совсем сформировался. Поэтому углекислота может привести к нарушению обмена веществ в организме и в будущем стать причиной высокой хрупкости костей.
- Диоксид углерода может вызвать аллергическую реакцию у человека.
- При наличии лишнего веса нельзя употреблять такие продукты, так как полнота, это следствие нарушения обмена веществ. А употребление продуктов с высоким содержанием CO2 приведет только к усугублению ситуации.
Во многих западных странах принят закон, в соответствии с которым наличие углекислого газа в продуктах не должно превышать 0,4%. Исключение дается только простой минеральной воде с газом, но только в том случае, если она содержит незначительное количество диоксида углерода. Но и это допустимо только по разрешению или рекомендации врача, особенно при болезнях желудка.
Красота и здоровье
Однако CO2 имеет и положительно действие на организм человека. Так диоксид углерода является очень мощным обеззараживающим средством. Его используют в медицине и косметологии. Применяют углекислый газ совместно с другими компонентами, наружно, а также производят инъекции (Карбокси-терапия). Крем или гель, содержащий углекислоту, хорошо обеззараживает и очищает кожу, а непосредственное введение его во внутренние ткани тела помогает бороться с целлюлитом.
Читайте также: Применение углекислого газа.
Вдыхание воздуха с высоким содержанием углекислоты в определенных пределах или задержка дыхания также приводят к омоложению и задержке процесса старения на клеточном уровне. Увеличенное содержание CO2 в артериальной крови способствует расширению сосудов и как следствие наилучшему и полному снабжению клеток организма кислородом.
Заключение
Очень жаль, что система образования в наших странах не уделяет столь важного внимания для пересмотра учебников в школах и институтах. Полученные знания об углекислоте необходимо доводить со школьной скамьи до учащихся образовательных учреждений. Знания многих процессов, протекающих в организме с участием диоксида углерода, могли бы научить нас правильному питанию и ведению здорового образа жизни. Продление жизни нашего организма тесно связано с наличием углекислого газа в нем, поэтому применяя на практике полученные знания, мы бы могли обеспечить себе здоровую и долгую жизнь.
Оксид углерода (II) | CHEMEGE.RU
Оксид углерода (II)
1. Строение молекулы и физические свойства
2. Способы получения
3. Химические свойства
3.1. Взаимодействие с кислородом
3.2. Взаимодействие с хлором
3.3. Взаимодействие с водородом
3.4. Взаимодействие с щелочами
3.5. Взаимодействие с оксидами металлов
3.6. Взаимодействие с прочими окислителями
Оксид углерода (II)
Строение молекулы и физические свойства
Оксид углерода (II) («угарный газ») – это газ без цвета и запаха. Сильный яд. Небольшая концентрация угарного газа в воздухе может вызвать сонливость и головокружение. Большие концентрации угарного газа вызывают удушье.
Строение молекулы оксида углерода (II) – линейное. Между атомами углерода и кислорода образуется тройная связь, за счет дополнительной донорно-акцепторной связи:

Способы получения
В лаборатории угарный газ можно получить действием концентрированной серной кислоты на муравьиную или щавелевую кислоты:
НСООН → CO + H2O
H2C2O4 → CO + CO2 + H2O
В промышленности угарный газ получают в газогенераторах при пропускании воздуха через раскаленный уголь:
C + O2 → CO2
CO2 + C → 2CO
Еще один важный промышленный способ получения угарного газа — паровая конверсия метана. При взаимодействии перегретого водяного пара с метаном образуется угарный газ и водород:
СН4 + Н2O → СО + 3Н2
Также возможна паровая конверсия угля:
C0 + H2+O → C+2O + H20
Угарный газ в промышленности также можно получать неполным окислением метана:
2СН4+О2 → 2СО + 4Н2
Химические свойства
Оксид углерода (II) – несолеобразующий оксид. За счет углерода со степенью окисления +2 проявляет восстановительные свойства.
1. Угарный газ горит в атмосфере кислорода. Пламя окрашено в синий цвет:
2СO + O2 → 2CO2
2. Оксид углерода (II) окисляется хлором в присутствии катализатора или под действием света с образованием фосгена. Фосген – ядовитый газ.
CO + Cl2 → COCl2
3. Угарный газ взаимодействует с водородом при повышенном давлении. Смесь угарного газа и водорода называется синтез-газ. В зависимости от условий из синтез-газа можно получить метанол, метан, или другие углеводороды.
Например, под давлением больше 20 атмосфер, при температуре 350°C и под действием катализатора угарный газ реагирует с водородом с образованием метанола:
СО + 2Н2 → СН3ОН
4. Под давлением оксид углерода (II) реагирует с щелочами. При этом образуется формиат – соль муравьиной кислоты.
Например, угарный газ реагирует с гидроксидом натрия с образованием формиата натрия:
CO + NaOH → HCOONa
5. Оксид углерода (II) восстанавливает металлы из оксидов.
Например, оксид углерода (II) реагирует с оксидом железа (III) с образованием железа и углекислого газа:
3CO + Fe2O3 → 2Fe + 3CO2
Оксиды меди (II) и никеля (II) также восстанавливаются угарным газом:
СО + CuO → Cu + CO2
СО + NiO → Ni + CO2
6. Угарный газ окисляется и другими сильными окислителями до углекислого газа или карбонатов.
Например, пероксидом натрия:
CO + Na2O2 → Na2CO3
Airgas
Что такое диоксид углерода?
Двуокись углерода (CO 2 ) – негорючий газ без цвета и запаха. Углекислый газ, содержащийся в воздухе в концентрации около 0,03%, может существовать одновременно в твердом, жидком и газообразном состоянии.
Покупка высококачественного газообразного диоксида углерода или жидкого диоксида углерода Мы предлагаем сжатый и жидкий CO 2 различных марок для различных областей применения, таких как:
CO 2 закачка для добычи нефти
• Сухой лед (твердый CO 2 гранул) для очистки и струйной обработки
• Оглушающий газ для животноводства
• Защитный газ для сварки
Промышленное применение
Напитки
Наша марка для напитков CO 2 и надежная цепочка поставок помогают клиентам поддерживать максимальную свежесть своих продуктов, избегая при этом загрязнения.Мы знаем, что чистота имеет значение при окончательной отделке напитков в бутылках, укупорке пивоварения или производства вина.
Пищевая промышленность
Воздушный газ жидкий CO 2 используется в наших системах охлаждения и замораживания для поддержания качества продукции за счет предотвращения порчи или старения на пути к вашим клиентам. Мы также предлагаем быстрый и простой способ очистить оборудование, ничего не оставляя. (См. Раздел «Струйная обработка сухим льдом ColdJet®»).
Контроль pH технологической воды
Более чистая, более безопасная альтернатива серной кислоте, CO 2 обычно используется в бетонной и целлюлозно-бумажной промышленности для эффективной очистки технологической воды.Он экономичен, экологически безопасен и помогает воде соответствовать ограничениям EPA по pH и общему содержанию взвешенных веществ (TSS).
Производство и изготовление металлов
CO 2 , смешанный с аргоном, используется в качестве защитного газа для предотвращения загрязнения расплавленного металла шва.
Науки о жизни
В лабораторных условиях CO 2 обычно используется для эвтаназии подопытных животных.
Upstream
Жизненно важный для увеличения нефтеотдачи, CO 2 растворяется в масле, снижая ее вязкость и улучшая скорость потока.
Режимы питания
Цилиндры высокого давления и жидкости
У нас 10 миллионов баллонов и около 300 установок для наполнения баллонов высокого давления. Воздушный газ постоянно обеспечивает потребности в сварочном, защитном и режущем газе с помощью сжатого газа CO 2 и CO 2 в баллонах с жидкостью.
MicroBulk
Когда у клиентов больше нет баллонов, Airgas MicroBulk Services предлагает решения для подачи газа, которые экономят время и место для хранения.Услуги Airgas MicroBulk могут помочь клиентам сэкономить деньги за счет снижения потребления газа и газовых отходов.
Массовые поставки
Мы поддерживаем наших клиентов в постоянном снабжении с помощью распределительной инфраструктуры, которая включает 16 воздухоразделительных установок, более 60 специалистов по газу и более 14 500 резервуаров.
Домашняя страница CO2 на Земле
Изменение глобальной температуры в марте *
Рейтинг за март: 1880-2020 Рекорд температуры
Сравнения со средней глобальной температурой поверхности 20-го века
(Температура здесь не сравнивается с доиндустриальным исходным уровнем)
Рейтинг | Год | Изменение |
Самый теплый март | 2016 | +0.92 ° C + 1,66 ° F |
3-е самое теплое марта | 2020 | + 0,80 ° C + 1,44 ° F |
Самый холодный март | 1911 | -0,56 ° C -1,01 ° F |
| Получено данных: 6 мая 2020 г. |
* Изменения температуры поверхности относительно среднего глобального значения за XX век (1901–2000)
Исходные данные NOAA-NCEI Состояние климата: глобальный анализ [Интернет + загрузка данных]
“В целом, глобальная температура поверхности суши и океана на март 2020 года составила 1.На 16 ° C (2,09 ° F) выше среднего показателя 20-го века, составлявшего 12,7 ° C (54,9 ° F), и является вторым по величине за 141-летний рекорд. Только март 2016 года был теплее – 1,31 ° C (2,36 ° F). Все 10 самых теплых маршей произошли с 1990 года, причем в маршах 2016, 2017, 2019 и 2020 годов глобальная температура поверхности суши и океана отклоняется от среднего значения выше 1,0 ° C (1,8 ° F). Глобальное отклонение температуры поверхности суши и океана в марте 2020 года, связанное с февралем 2020 года и декабрем 2015 года, является третьим по величине отклонением температуры за месяц от среднего за 1683-месячный рекорд.Только в феврале и марте 2016 года, когда в тропической части Тихого океана наблюдалось сильное Эль-Ниньо, отклонения температуры были более высокими.
«Март 2020 года ознаменовался 44-м март подряд и 423-м месяцем подряд с температурами, по крайней мере номинально, выше среднего значения для 20-го века. По данным Центра прогнозирования климата NOAA, в течение марта 2020 года в тропической части Тихого океана наблюдались нейтральные по отношению к ENSO условия. Март 2020 года отклонение глобальной температуры поверхности суши и океана от среднего значения связано с февралем 2020 года как наивысшим отклонением температуры за месяц без Эль-Ниньо в тропической зоне Тихого океана.Три самых высоких отклонения нейтральной температуры ЭНСО от средней произошли в 2020 году. CPC заявляет, что нейтральная температура ЭНСО предпочтительна весной в северном полушарии (осень в южном полушарии). Этот прогноз ориентирован на температуру поверхности океана между 5 ° северной широты и 5 ° южной широты и 170 ° западной долготы до 120 ° западной долготы, называемой регионом Ниньо 3.4.
«Отклонения глобальной температуры только на суше и только в океане от среднего значения за март 2020 года также были почти рекордно высокими по сравнению с рекордом, установленным в марте 2016 года.Глобальное отклонение температуры только на суше в марте 2020 года на + 2,05 ° C (+ 3,69 ° F) также стало пятым по величине за любой месяц для поверхности суши за 1683-месячный рекорд. С декабря 2015 года произошло 10 самых высоких месячных отклонений температуры только на суше. Между тем, отклонение глобальной температуры океана только в марте 2020 года на + 0,83 ° C (+ 1,49 ° F), связанное с февралем 2016 года и июлем 2019 года, является седьмым по величине для любого месяц для поверхности океана зарегистрировано.
“В регионе Южная Америка и Мексиканский залив показали самый теплый март за всю историю наблюдений, превзойдя предыдущие рекорды, установленные в 2010 и 1945 годах соответственно.Это также пятое по величине отклонение температуры в Южной Америке и четвертое по величине в Мексиканском заливе за любой месяц из 1323-месячного регионального рекорда. В Карибском бассейне был второй самый высокий показатель в марте за всю историю наблюдений – 0,90 ° C (1,62 ° F) выше среднего. Только март 2016 года был теплее. Между тем, в Европе, Африке и Азии в марте температура была одной из девяти самых высоких за всю историю наблюдений ».
[Глобальный анализ NOAA / NCEI, доступ к 6 мая 2020 г.]
«Наука отрезвляет – глобальная температура в 2012 году была одной из самых высоких с момента установления рекордов в 1880 году.Не заблуждайтесь: без согласованных действий само будущее нашей планеты окажется в опасности ».
~ Кристин Лагард, в 2012 г.
Управляющий директор, Международный валютный фонд
[видео] [текст]
Годовой глобальный анализ NOAA / NCEI за 2018 г .:
Средняя глобальная температура в 2017 году на суше и на поверхности океана была на 0,84 ° C (1,51 ° F) выше среднего значения за 20 век, составлявшего 13,9 ° C (57,0 ° F), по сравнению с рекордным 2016 годом (+ 0,94 ° C / +1.69 ° F) и 2015 (+ 0,90 ° C / + 1,62 ° F; второй самый теплый год за всю историю наблюдений) оба испытали влияние сильного эпизода Эль-Ниньо. 2017 год также является самым теплым годом, когда в тропической части Тихого океана не было Эль-Ниньо.
2017 также знаменует собой 41-й год подряд (с 1977 г.), когда глобальные температуры суши и океана, по крайней мере, номинально превышают средний показатель за 20 век, причем с 2010 года наблюдаются шесть самых теплых лет за всю историю наблюдений. С начала 21 века глобальная температура изменилась. было сломано пять раз, три из них были поставлены спиной друг к другу (2014–2016 годы).Ежегодная глобальная температура суши и океана с 1880 года повышалась в среднем на 0,07 ° C (0,13 ° F) за десятилетие; тем не менее, с 1980 года средняя скорость повышения температуры в два раза выше. С 1900 по 1980 год новый температурный рекорд устанавливался в среднем каждые 13,5 лет; однако с 1981 года он увеличивается до трех лет.
В целом, глобальная годовая температура повышалась в среднем на 0,07 ° C (0,13 ° F) за десятилетие с 1880 года и со средней скоростью на 0,17 ° C (0,31 ° F) за десятилетие с 1970 года.«
[Глобальный анализ NOAA / NCEI за 2018 г., по состоянию на 18 февраля 2019 г.].
«Глобальные усредненные температуры в 2015 году побили предыдущую отметку, установленную в 2014 году, на 0,23 градуса по Фаренгейту (0,13 по Цельсию). Только однажды, в 1998 году, новый рекорд был намного выше старого».
~ Институт космических исследований имени Годдарда НАСА [сообщение НАСА от 20 января 2016 г.]
До конца 2015 года ученые прогнозировали, что среднее повышение глобальной температуры в 2015 году превысит доиндустриальный уровень на 1 ° C.1850-1900 годы используются в качестве доиндустриального базового уровня Управлением МЕТ и Отделом исследований климата Университета Восточной Англии в Великобритании. В ноябре 2015 года МЕТА выпустило это заявление:
«Этот год знаменует собой первое важное событие, но это не обязательно означает, что каждый год с этого момента будет на градус или более выше доиндустриального уровня, поскольку естественная изменчивость по-прежнему будет играть роль в определении температуры в каждом конкретном году. Поскольку в ближайшие десятилетия в мире будет продолжаться потепление, однако мы увидим, что все больше и больше лет будет проходить отметку в 1 градус – со временем это станет нормой.«
~ Питер Стотт
Руководитель отдела климатического мониторинга и атрибуции (МЕТ-офис)
>> Подробнее
,
