Характеристика элемента 35: дайте полную характеристику химического элемента Br
alexxlab | 18.03.2023 | 0 | Разное
Бром и его характеристики
Онлайн калькуляторы
На нашем сайте собрано более 100 бесплатных онлайн калькуляторов по математике, геометрии и физике.
Справочник
Основные формулы, таблицы и теоремы для учащихся. Все что нужно, чтобы сделать домашнее задание!
Заказать решение
Не можете решить контрольную?!
Мы поможем! Более 20 000 авторов выполнят вашу работу от 100 руб!
Общая характеристика брома
Подобно хлору бром находится в природе преимущественно в виде солей калия, натрия и магния. Бромиды металлов содержатся в морской воде, в некоторых озерах и подземных рассолах.
В обычных условиях бром – красно-коричневая жидкость (рис. 1), малорастворимая в воде. При охлаждении водного раствора брома выделяются кристаллогидраты кларатного типа Br2×8H2O. Хорошо растворим в органических растворителях (спирт, бензол, эфир, сероуглерод и т. д.).
д.).
Рис. 1. Бром. Внешний вид.
Атомная и молекулярная масса брома
Относительная атомная масса безразмерна и обозначается Ar (индекс «r» — начальная буква английского слова relative, что в переводе означает «относительный»). Относительная атомная масса атомарного брома равна 79,901 а.е.м.
Массы молекул, также как массы атомов выражаются в атомных единицах массы.
Молекулярной массой вещества называется масса молекулы, выраженная в атомных единицах массы. Известно, что молекула брома двухатомна – Br2. Относительная молекулярная масса молекулы водорода будет равна:
Mr(Br2) = 79,901 × 2 ≈160.
Изотопы брома
Известно, что в природе бром может находиться в виде двух стабильных изотопов 79Br (50,56%) и 81Br (49,44%). Их массовые числа равны 79 и 81 соответственно. Ядро атома изотопа брома 79Br содержит тридцать пять протонов и сорок четыре нейтрона, а изотопа 81Br – столько же протонов и сорок шесть нейтронов.
Существуют искусственные нестабильные изотопы брома с массовыми числами от 67-ми до 97-ми, а также четырнадцать изомерных состояния ядер, среди которых наиболее долгоживущим является изотоп 82Br с периодом полураспада равным 35,282 часов.
Ионы брома
На внешнем энергетическом уровне атома брома имеется восемь электронов, которые являются валентными:
1s22s22p63s23p63d104s24p5.
В результате химического взаимодействия бром либо отдает свои валентные электроны, т.е. является их донором, и превращается в положительно заряженный ион, либо принимает электроны от другого атома, т.е. является их акцептором и превращается в отрицательно заряженный ион:
Br0 +1e → Br1-;
Br0 -1e → Br1+;
Br0 -3e → Br3+;
Br0 -5e → Br5+;
Br0 -7e → Br7+.
Молекула и атом брома
Молекула брома состоит из двух атомов – Br2. Приведем некоторые свойства, характеризующие атом и молекулу брома:
|
Энергия ионизации атома, эВ |
11,84 |
|
Относительная электроотрицательность |
2,96 |
|
Радиус атома, нм |
0,114 |
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
Бром
| Бром | |
|---|---|
| Атомный номер | 35 |
| Внешний вид простого вещества | красно-бурая жидкость с сильным неприятным запахом |
| Свойства атома | |
|
Атомная масса (молярная масса) |
79,904 а. е. м. (г/моль) е. м. (г/моль) |
| Радиус атома | n/a пм |
|
Энергия ионизации (первый электрон) |
1142,0 (11,84) кДж/моль (эВ) |
| Электронная конфигурация | [Ar] 3d10 4s2 4p5 |
| Химические свойства | |
| Ковалентный радиус | 114 пм |
| Радиус иона | (+5e)47 (-1e)196 пм |
|
Электроотрицательность (по Полингу) |
2,96 |
| Электродный потенциал | 0 |
| Степени окисления | 7, 5, 3, 1, -1 |
| Плотность | 3,12 г/см³ |
| Молярная теплоёмкость | 75,69 Дж/(K·моль) |
| Теплопроводность | 0,005 Вт/(м·K) |
| Температура плавления | 265,9 K |
| Теплота плавления | (Br—Br) 10,57 кДж/моль |
| Температура кипения | 331,9 K |
| Теплота испарения | (Br—Br) 29,56 кДж/моль |
| Молярный объём | 23,5 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | орторомбическая |
| Параметры решётки | a=6,67 b=4,48 c=8,72 Å |
| Отношение c/a | — |
| Температура Дебая | n/a K |
| Br | 35 |
| 79,904 | |
| [Ar]3d104s24p5 | |
| Бром | |
Бром — элемент главной подгруппы седьмой группы четвёртого периода периодической системы химических элементов Д.
История
Схема атома брома
Бром был открыт в 1826 году молодым преподавателем колледжа города Монпелье А. Ж. Баларом. Открытие Балара сделало его имя известным всему миру. Из одной популярной книги в другую кочует утверждение, что огорченный тем, что в открытии брома никому неизвестный Антуан Балар опередил самого Юстуса Либиха, Либих воскликнул, что, дескать, не Балар открыл бром, а бром открыл Балара. Однако это неправда, или, точнее, не совсем правда. Фраза-то была, но принадлежала она не Ю. Либиху, а Шарлю Жерару, который очень хотел, чтобы кафедру химии в Сорбонне занял Огюст Лоран, а не избранный на должность профессора А.
Происхождение названия
Название элемента происходит βρῶμος — зловоние.
Получение
Бром получают химическим путём из рассола Br–:
Физические свойства
При обычных условиях бром — красно-бурая жидкость с резким неприятным запахом, ядовит, при соприкосновении с кожей образуются ожоги. Плотность при 0 °C — 3, 19 г./см³. Температура плавления (затвердевания) брома −7,2 °C, кипения 58,8 °C, при кипении бром превращается из жидкости в буро-коричневые пары, при вдыхании раздражающие дыхательные пути. Стандартный электродный потенциал Br²/Вr– в водном растворе равен +1,065 В.
Обычный бром состоит из изотопов 79Br (50,56 %) и 81Br (49,44 %). Искусственно получены радиоактивные изотопы.
Химические свойства
В свободном виде существует в виде двухатомных молекул Br2. Заметная диссоциация молекул на атомы наблюдается при температуре 800 °C и быстро возрастает при дальнейшем росте температуры. Диаметр молекулы Br2 равен 0,323 нм, межъядерное расстояние в этой молекуле — 0,228 нм.
Диаметр молекулы Br2 равен 0,323 нм, межъядерное расстояние в этой молекуле — 0,228 нм.
Бром немного, но лучше других галогенов растворим в воде (3,58 г в 100 г воды при 20 °C), раствор называют бромной водой. В бромной воде протекает реакция с образованием бромоводородной и неустойчивой бромноватистой кислот:
Br2 + H2O → HBr + HBrO.
С большинством органических растворителей бром смешивается во всех отношениях, при этом часто происходит бромирование молекул органических растворителей.
По химической активности бром занимает промежуточное положение между хлором и иодом. При реакции брома с растворами иодидов выделяется свободный иод:
Br2 + 2KI → I2↓ + 2KBr.
Напротив, при действии хлора на бромиды, находящиеся в водных растворах, выделяется свободный бром:
Cl2 + 2NaBr → Br2 + 2NaCl.
При реакции брома с серой образуется S2Br2, при реакции брома с фосфором — PBr3 и PBr5. Бром реагирует также с неметаллами селеном и теллуром.
Бром реагирует также с неметаллами селеном и теллуром.
Реакция брома с водородом протекает при нагревании и приводит к образованию бромоводорода HBr. Раствор HBr в воде — это бромоводородная кислота, по силе близкая к соляной кислоте HCl. Соли бромоводородной кислоты — бромиды (NaBr, MgBr2, AlBr3 и др.). Качественная реакция на присутствие бромид-ионов в растворе — образование с ионами Ag
С кислородом и азотом бром непосредственно не реагирует. Бром образует большое число различных соединений с остальными галогенами. Например, со фтором бром образует неустойчивые BrF3 и BrF5, с иодом — IBr. При взаимодействии со многими металлами бром образует бромиды, например, AlBr3, CuBr2, MgBr2 и др. Устойчивы к действию брома тантал и платина, в меньшей степени — серебро, титан и свинец.
Бром — сильный окислитель, он окисляет сульфит-ион до сульфата, нитрит-ион — до нитрата и т. д.
д.
При взаимодействии с органическими соединениями, содержащими двойную связь, бром присоединяется, давая соответствующие дибромпроизводные:
C2H4 + Br2 → C2
H4Br2.Присоединяется бром и к органическим молекулам, в составе которых есть тройная связь. Обесцвечивание бромной воды при пропускании через нее газа или добавлении к ней жидкости свидетельствует о том, что в газе или в жидкости присутствует непредельное соединение.
При нагревании в присутствии катализатора бром реагирует с бензолом с образованием бромбензола C6H5Br (реакция замещения).
При взаимодействии брома с растворами щелочей и с растворами карбонатов натрия или калия образуются соответствующие бромиды и броматы, например:
3Br2 + 3Na2CO3 → 5NaBr + NaBrO3+ 3CO2↑.
Бромсодержащие кислоты
Помимо бескислородной бромоводородной кислоты HBr, бром образует ряд кислородных кислот: бромную HBrO4, бромноватую HBrO3, бромистую HBrO2, бромноватистую HBrO.
Применение
В химии
Вещества на основе брома широко применяются в основном органическом синтезе.
В технике
— Бромид серебра AgBr применяется в фотографии как светочувствительное вещество.
— Используется для создания антипиренов — добавок, придающих пожароустойчивость пластикам, древесине, текстильным материалам.
— Пентафторид брома иногда используется как очень мощный окислитель ракетного топлива.
— 1,2-дибромэтан в настоящее время применяют как антидетонирующую добавку в моторном топливе, взамен тетраэтилсвинца.
— Растворы бромидов используются в нефтедобыче.
В медицине
В медицине бромид натрия и бромид калия применяют как успокаивающие средства.
В производстве оружия
Со времен Первой Мировой войны бром используется для производства боевых отравляющих веществ.
Физиологическое действие
Уже при содержании брома в воздухе в концентрации около 0,001 % (по объёму) наблюдается раздражение слизистых оболочек, головокружение, а при более высоких концентрациях — спазмы дыхательных путей, удушье. ПДК паров брома 0,5 мг/м³. При попадании в организм токсическая доза составляет 3 г, летальная — от 35 г. При отравлении парами брома пострадавшего нужно немедленно вывести на свежий воздух; для восстановления дыхания можно на небольшое время пользоваться тампоном, смоченным нашатырным спиртом, на короткое время периодически поднося его к носу пострадавшего. Дальнейшее лечение должно проводиться под наблюдением врача. Жидкий бром при попадании на кожу вызывает болезненные ожоги.
ПДК паров брома 0,5 мг/м³. При попадании в организм токсическая доза составляет 3 г, летальная — от 35 г. При отравлении парами брома пострадавшего нужно немедленно вывести на свежий воздух; для восстановления дыхания можно на небольшое время пользоваться тампоном, смоченным нашатырным спиртом, на короткое время периодически поднося его к носу пострадавшего. Дальнейшее лечение должно проводиться под наблюдением врача. Жидкий бром при попадании на кожу вызывает болезненные ожоги.
Особенности работы
При работе с бромом следует пользоваться защитной спецодеждой, противогазом, специальными перчатками. Из-за высокой химической активности и токсичности, как паров брома, так и жидкого брома его следует хранить в стеклянной, плотно укупоренной толстостенной посуде. Склянки с бромом располагают в ёмкостях с песком, который предохраняет склянки от разрушения при встряхивании. Из-за высокой плотности брома склянки с ним ни в коем случае нельзя брать только за горло (горло может оторваться, и тогда бром окажется на полу).
Для нейтрализации пролитого брома поверхность с ним надо залить раствором сульфита натрия Na2SO3
Мифы и легенды
Существует широко распространенная легенда о том, что в армии будто бы добавляют бром в еду для снижения полового влечения. Этот миф не имеет под собой никаких оснований — влечение успешно снижают физические нагрузки, а действительно добавляемые в еду добавки чаще всего оказываются аскорбиновой кислотой для предотвращения авитаминоза. К тому же, препараты брома соленые на вкус и не влияют ни на влечение, ни на потенцию. Они обладают снотворным и успокаивающим эффектом.
Br Информация об элементе брома: факты, свойства, тенденции, использование и сравнение – Периодическая таблица элементов
Кристаллическая структура брома
Твердотельная структура брома Орторомбическая с центром в основании .
Кристаллическая структура может быть описана с точки зрения ее элементарной ячейки. Единичные Клетки повторяются в трехмерном пространстве, образуя структуру.
Единичные Клетки повторяются в трехмерном пространстве, образуя структуру.
Параметры элементарной ячейки
Элементарная ячейка представлена в терминах ее параметров решетки, которые являются длинами ребер ячейки Константы решетки (a, b и c)
| a | b | c |
|---|---|---|
| 672.65 pm | 464.51 pm | 870.23 pm |
and the angles between them Lattice Angles (alpha, beta and gamma).
| alpha | beta | gamma |
|---|---|---|
| π/2 | π/2 | π/2 |
The positions of the atoms inside the unit cell are described by the set атомных позиций ( x i , y i , z i ), измеренные от опорной точки решетки.
Свойства симметрии кристалла описываются концепцией пространственных групп. Все возможные симметричные расположения частиц в трехмерном пространстве описываются 230 пространственными группами (219 различных типов или 230, если считать киральными копиями различными). Штаты
Штаты
Атомно -атомно -атомный и орбитальный. ] с символом атомного термина (квантовые числа)
2 P 3/2 .| Атомный номер | 35 |
| Число электронов (бесплатно) | 35 |
| Number of Protons | 35 |
| Mass Number | 80 |
| Number of Neutrons | 45 |
| Shell structure (Electrons per energy level) | 2, 8, 18, 7 |
| Электронная конфигурация | [AR] 3D10 4S2 4P5 |
| Валентные электроны | 4S2 4P5 |
| Валентность (Валентность) | 5 |
| Валентность (Валентность) | 5 |
| (Валентность) | 5 |
| (Валентность) | 5 |
| (Валентность) | 777 5 |
| (Валентность) | 77 5 |
| (Валентность)0028 | |
| Main Oxidation States | -1, 1, 3, 5 |
| Oxidation States | -1, 1, 3, 4, 5, 7 |
| Atomic Term Symbol (Quantum Numbers) | 2 P 3/2 |
Атомная модель брома по Бору – количество электронов на энергетический уровень0011
Сокращенная электронная конфигурация основного состояния нейтрального атома брома: [Ar] 3d10 4s2 4p5. Часть конфигурации брома, эквивалентная благородному газу предыдущего периода, обозначается аббревиатурой [Ar]. Для атомов с большим количеством электронов это обозначение может стать длинным, поэтому используется сокращенное обозначение. Это важно, поскольку именно валентные электроны 4s2 4p5, электроны в самой внешней оболочке, определяют химические свойства элемента.
Часть конфигурации брома, эквивалентная благородному газу предыдущего периода, обозначается аббревиатурой [Ar]. Для атомов с большим количеством электронов это обозначение может стать длинным, поэтому используется сокращенное обозначение. Это важно, поскольку именно валентные электроны 4s2 4p5, электроны в самой внешней оболочке, определяют химические свойства элемента.
Полная электронная конфигурация нейтрального брома
Полная электронная конфигурация атома брома в основном состоянии. Полная электронная конфигурация
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5
Электроны заполняются атомными орбиталями в порядке, определяемом принципом Ауфбау, принципом запрета Паули и правилом Хунда.
 …
…Атомная структура брома
Атомный радиус брома составляет 94 пм, а его ковалентный радиус равен 114 пм.
| Расчетный атомный радиус | 94 пм (0,94 Å) |
| Atomic Radius Empirical | 115 pm (1.15 Å) |
| Atomic Volume | 19.78 cm3/mol |
| Covalent Radius | 114 pm (1.14 Å) |
| Van der Waals Radius | 185 PM |
| Нейтронный сечение | 6,8 |
| Абсорбция нейтронной массы | 0,002 |
Ат.0011
Химические свойства брома: Энергия ионизации брома и сродство к электрону
Сродство к электрону брома составляет 324,6 кДж/моль.
| Valence | 5 |
| Electronegativity | 2.96 |
| ElectronAffinity | 324.6 kJ/mol |
Ionization Energy of Bromine
Refer to table below for Ionization energies of Bromine
| Ionization energy number | Enthalpy – kJ/mol |
|---|---|
| 1st | 1139.9 |
| 2nd | 2103 |
| 3rd | 3470 |
| 4th | 4560 |
| 5th | 5760 |
| 6th | 8550 |
| 7th | 9940 |
| 8th | 18600 |
Физические свойства брома
См. Ниже таблицы для физических свойств брома
| Плотность | 3,12 г/см3 (когда плотность M.P составляет $ 3,12 г/см3) | м. П. mol П. mol |
Elastic Properties
| Young Modulus | – |
| Shear Modulus | – |
| Bulk Modulus | 1.9 GPa |
| Poisson Ratio | – |
Hardness of Bromine – Tests to Measure of Hardness of Element
| Mohs Hardness | – |
| Vickers Hardness | – |
| Твердость по Бринеллю | – |
Электрические свойства брома
Бром является проводником электричества. Обратитесь к таблице ниже для получения информации об электрических свойствах брома 9.0007
| Electrical Conductivity | 1e-10 S/m |
| Resistivity | 10000000000 m Ω |
| Superconducting Point | – |
Bromine Heat and Conduction Properties
| Thermal Проводимость | 0,12 Вт/(м·К) |
| Тепловое расширение | – |
Магнитные свойства брома
| Magnetic Type | Diamagnetic |
| Curie Point | – |
| Mass Magnetic Susceptibility | -4.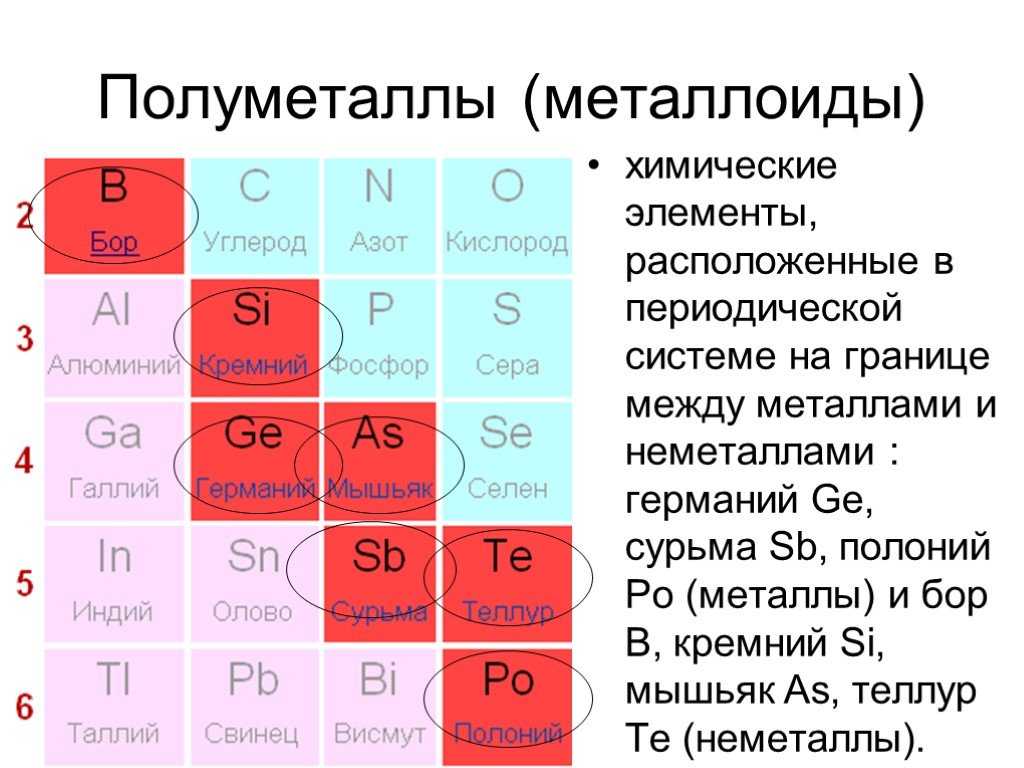 9e-9 m3/kg 9e-9 m3/kg |
| Molar Magnetic Susceptibility | -7.83e-10 m3/ моль |
| Объемная магнитная восприимчивость | -0,0000153 |
Оптические свойства брома
| 0028 |
Акустические свойства Bromine
| Скорость звука | – |
Термические.
Enthalpies of Bromine
| Heat of Fusion | 5.8 kJ/mol |
| Heat of Vaporization | 14.8 kJ/ моль |
| Теплота сгорания | – |
Изотопы брома.
 Ядерные свойства брома
Ядерные свойства бромаБром имеет 31 изотоп, от 67 до 97 нуклонов. Бром имеет 2 стабильных природных изотопа.
Изотопы брома – Встречающиеся в природе стабильные изотопы: 79Br, 81Br.
| Isotope | Z | N | Isotope Mass | % Abundance | T half | Decay Mode | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 67Br | 35 | 32 | 67 | Synthetic | |||||||||||
| 68Br | 35 | 33 | 68 | Synthetic | |||||||||||
| 69Br | 35 | 34 | 69 | Synthetic | |||||||||||
| 70Br | 35 | 35 | 70 | Synthetic | |||||||||||
| 71Br | 35 | 36 | 71 | Synthetic | |||||||||||
| 72Br | 35 | 37 | 72 | Synthetic | |||||||||||
| 73Br | 35 | 38 | 73 | Synthetic | |||||||||||
| 74Br | 35 | 39 | 74 | Synthetic | |||||||||||
| 75Br | 35 | 40 | 75 | Синтетический | |||||||||||
| 76BR | 35 | 41 | 76 | 76 | 76 | 76 | 76 | 76 | 76 | 76 | 0632|||||
| 77Br | 35 | 42 | 77 | Synthetic | |||||||||||
| 78Br | 35 | 43 | 78 | Synthetic | |||||||||||
| 79Br | 35 | 44 | 79 | 50,69% | Стабильная | N/A | |||||||||
| 80BR | 35 | 45 | 80 | Синтетичный | 78 | 80287 | 78 | 70028 | 70028 | 0632 | |||||
| 81Br | 35 | 46 | 81 | 49.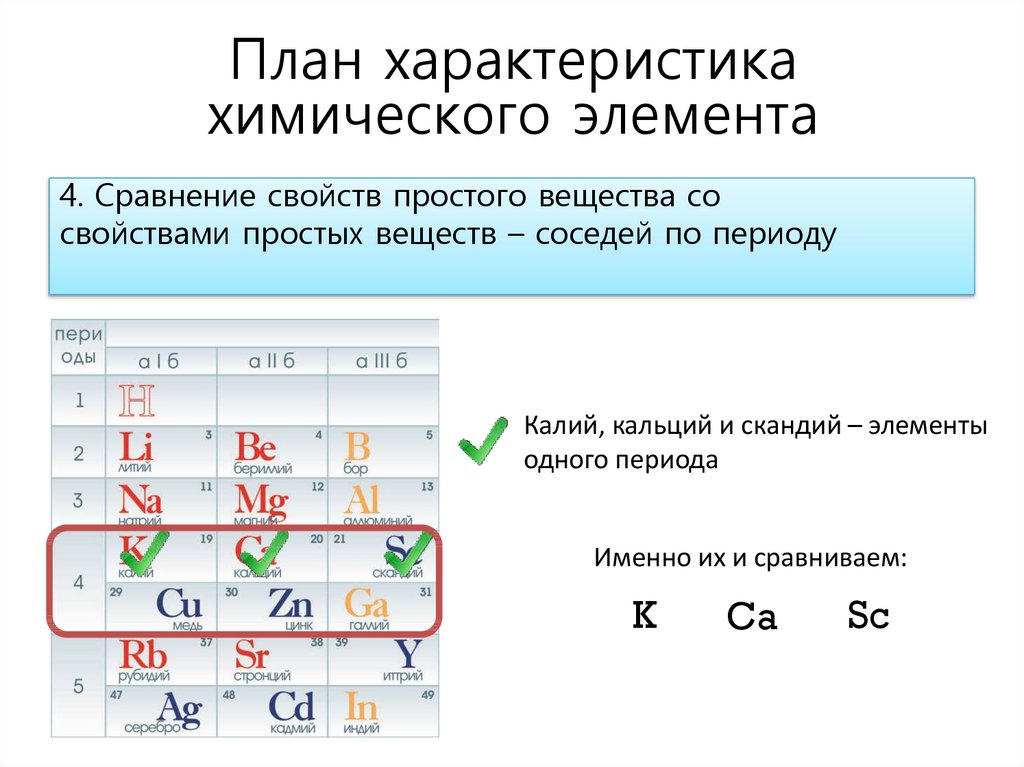 31% 31% | Stable | N/A | |||||||||
| 82Br | 35 | 47 | 82 | Synthetic | |||||||||||
| 83Br | 35 | 48 | 83 | Synthetic | |||||||||||
| 84Br | 35 | 49 | 84 | Synthetic | |||||||||||
| 85Br | 35 | 50 | 85 | Synthetic | |||||||||||
| 86Br | 35 | 51 | 86 | Synthetic | |||||||||||
| 87Br | 35 | 52 | 87 | Synthetic | |||||||||||
| 88Br | 35 | 53 | 88 | Synthetic | |||||||||||
| 89Br | 35 | 54 | 89 | Synthetic | |||||||||||
| 90Br | 35 | 55 | 90 | Synthetic | |||||||||||
| 91Br | 35 | 56 | 91 | Synthetic | |||||||||||
| 92Br | 35 | 57 | 92 | Synthetic | |||||||||||
| 93Br | 35 | 58 | 93 | Synthetic | |||||||||||
| 94Br | 35 | 59 | 94 | Synthetic | |||||||||||
| 95Br | 35 | 60 | 95 | Synthetic | |||||||||||
| 96Br | 35 | 61 | 96 | Synthetic | |||||||||||
| 97Br | 35 | 62 | 97 | Synthetic |
Chem4Kids.
 com: Элементы и периодическая таблица
com: Элементы и периодическая таблица Теперь мы подходим к сердцу и душе того, как работает Вселенная. Вы знаете, что в обычном атоме есть несколько протонов и нейтронов в ядре и несколько электронов, бегающих по орбитам. Когда эти части начинают объединяться в определенные количества, вы можете создавать атомы с узнаваемыми чертами. Если у вас есть восемь протонов, нейтронов и электронов, у вас будет атом кислорода (O). Если у вас есть семь протонов, нейтронов и электронов, у вас будет атом азота (N). Атомы каждого элемента уникальны, хотя все они состоят из одинаковых субатомных частей.
Помните, что “атом” – это общий термин. Все состоит из атомов. Термин «элемент» используется для описания атомов с определенными характеристиками. Известно почти 120 элементов. Например, вы состоите из миллиардов миллиардов атомов, но вы, вероятно, не найдете более 40 элементов (типов атомов) в своем теле. Химики выяснили, что более 95% вашего тела состоит из водорода (H), углерода (C), азота, кислорода, фосфора (P) и кальция (Ca).
Насколько нам известно, существует ограниченное количество базовых элементов. На данный момент мы открыли или создали около 120. Ученые только что подтвердили создание 117-го элемента в 2014 году. Хотя есть еще элементы, которые нужно открыть, основные элементы остаются прежними. Атомы железа (Fe), обнаруженные на Земле, идентичны атомам железа, обнаруженным на метеоритах. Атомы железа в красной почве Марса тоже такие же.
С помощью инструментов, которые вы здесь изучите, вы сможете исследовать и понимать Вселенную. Вы никогда не перестанете открывать новые реакции и соединения, но элементы останутся прежними.
С момента запуска сайта нас спрашивали: «Почему мы начинаем с 18?» Правила для первых восемнадцати элементов очень просты:
(1) Электроны прекрасно вписываются в три орбитали. Помните, что орбитали — это места, где обычно находятся электроны, вращающиеся вокруг ядра.
(2) Эти восемнадцать элементов составляют большую часть материи во Вселенной.
(3) Намного легче запомнить факты о 18 элементах, чем о более чем 100 элементах.
| Элемент 1: Водород Элемент 2: Гелий Элемент 3: Литий Элемент 4: Бериллий Элемент 5: Бор Элемент 6: Углерод Элемент 7: Азот Элемент 8: Кислород Элемент 9: Фтор | Элемент 10: Неон Элемент 11: Натрий Элемент 12: Магний Элемент 13: Алюминий Элемент 14: Кремний Элемент 15: Фосфор Элемент 16: Сера Элемент 17: Хлор Элемент 18: Аргон |
Когда мы пройдем первые восемнадцать элементов, вы сможете начать узнавать о переходных элементах в четвертом периоде (строке) периодической таблицы. Электронные конфигурации переходных металлов немного отличаются от первых восемнадцати. Прежде чем перейти к этой строке, убедитесь, что вы понимаете основы электронных орбиталей.

