Химия 8 класс характерные свойства меди и серы: Сравните физические свойства меди и серы
alexxlab | 07.02.2023 | 0 | Разное
Сера
Электронное строение атома.
Сера относится к элементу, находящемуся в VI-й группе главной подгруппы периодической системы Д.И.Менделеева. Его электронная конфигурация атома 1s22s22p63s23p4.
Нахождение в природе.
В обычных условиях сера представляет собой лёгкие, жёлтые кристаллы, нерастворимые в воде, но хорошо растворимые в сероуглероде. Кристаллическая решётка серы – молекулярная, в узлах которой находится циклическая молекула S8. Сера имеет ряд аллотропных модификаций.
Вышеуказанная форма серы называется моноклинной серой, при охлаждении которой переходит в устойчивые кристаллы ромбической серы.
Если расплавленную серу влить в холодную воду, то образуется ещё одна аллотропная модификация – пластическая сера. Температура кипения серы +445оС. В парах расплавленной серы содержатся молекулы S
В природе сера встречается в трёх формах:
1) Самородная сера
2) Сульфидная сера:
FeS2 – серный или железный колчедан, пирит.
CuS – медный блеск.
CuFeS2 – халькопирит или медный колчедан.
PbS – свинцовый блеск.
ZnS – цинковая обманка.
HgS – киноварь.
3) Сульфатная сера:
CaSO4x2h3O – гипс.
CaSO4xh3O – алебастр.
Na2SO4x10h3O – глауберова соль.
MgSO4x 7h3O – горькая соль.
Химические свойства.
1. Свойства простого вещества.
Сера может проявлять как окислительные, так и восстановительные свойства. Окислителем сера является в первую очередь по отношению к металлам:
S + 2Na = Na2S
S + Ca = CaS
3S +2Al = Al2S3
В качестве окислителя сера проявляет свои свойства и при взаимодействии с неметаллами:
S + h3 = h3S
2S + C = CS2
Однако с неметаллами, имеющими электроотрицательность бóльшую, чем у серы, она реагирует в качестве восстановителя:
S +3F2 = SF6
S + Cl2 = SCl2
Сера реагирует со сложными веществами, как правило, окислителями. Причём азотная кислота окисляет её до серной кислоты:
Причём азотная кислота окисляет её до серной кислоты:
S + 6HNO3 = h3SO4 + 6NO2 + 2h3O
Другие окислители окисляют серу до степени окисления (+4):
S + 2h3SO4 = 3SO2 + 2h3O
3S + 2KClO3 = 3SO2 + 2KCl
По механизму реакции ДИСПРОПОРЦИОНИРОВАНИЯ сера реагирует с щелочами. В процессе этой реакции образуются соединения серы (-2) и (+4):
3S + 6KOH = K2SO3 + 2K2S + 3h3O
Непосредственно с водой сера не реагирует, однако при нагревании подвергается дисмутации в атмосфере водяного пара.
Сера может быть получена в процессе реакций:
SO2 + 2CO = S + 2CO2
Na2S2O3 + 2HCl = S + SO2 + 2NaCl + h3O
2. Соединения серы (-2).
У серы в степени окисления (-2) соединения называются сульфидами. Это бинарные соединения, в которых одним из элементов является металл: Na2S, ZnS, Al2S3, PbS2 и др.
Соединение серы (-2) с водородом называется сероводород – h3S. Сероводород – газ без цвета, неприятного запаха, тяжелее воздуха, очень ядовит, мало растворим в воде. Сероводород можно получить различными способами. Oбычно, в лаборатории, сероводород получают, действуя на сульфиды сильными кислотами:
Сероводород – газ без цвета, неприятного запаха, тяжелее воздуха, очень ядовит, мало растворим в воде. Сероводород можно получить различными способами. Oбычно, в лаборатории, сероводород получают, действуя на сульфиды сильными кислотами:
FeS + 2HCl = FeCl2 + h3S
Для сероводорода и его солей характерны восстановительные свойства:
h3S + SO2 = 3S + 2h3O
В указанной реакции сера образуется по механизму конпропорционирования ( из двух атомов серы, имеющих различные степени окисления (-2) и (+4) образуется соединение серы со степенью окисления (0).
SO2 + 2CO = S + 2CO2
Na2S2O3 + 2HCl = S + SO2 + 2NaCl + h3O
В лаборатории сероводород получают:
FeS + 2HCl = FeCl2 + h3S
При сгорании в кислороде он образует различные продукты:
2h3S + O2 = 2h3O + 2S (недостаток кислорода)
2h3S + 3O2 = 2h3O + 2SO2 (избыток кислорода)
Cероводород легко окисляется галогенами, оксидом серы, хлоридом железа (III):
h3S + Cl2 = 2HCl + S
2h3S + SO2 = 2h3O + 3S
h3S + 2FeCl3 = 2FeCl2 + S + 2HCl
На воздухе сероводород окисляет серебро, чем и объясняется почернение серебряных изделий со временем:
2h3S + 4Ag + O2 = 2Ag2S + 2h3O
Водные растворы сероводорода являются слабой кислотой.
h3S ↔ HS-1 + H+
HS-1 ↔ H+ + S-2
Сульфиды большинства металлов нерастворимы и имеют различную окраску. Это является фактором, благодаря которому можно распознавать те или иные катионы в растворах:
Чёрные – HgS, Ag2S, PbS, CuS, FeS, NiS;
Коричневые – SnS, Bi2S3;
Оранжевые – Sb2S3, Sb2S5;
Жёлтые – As2S3, As2S5, SnS2, CdS;
Розовые – MnS
Белые – ZnS, Al2S3, BaS, CaS;
Cульфиды в водной среде проявляют восстановительные свойства, обычно окисляясь до серы:
3h3S + 2KMnO4 = 3S + 2MnO2 + 2KOH + 2h3O
h3S + 2HNO3 = S + 2NO2 + 2h3O
3h3S + 2FeCl3 = S + FeS + 6HCl
h3S + J2 = S + 2HJ
При взаимодействии с более сильными окислителями сульфиды окисляются до соединений со степенью окисления (+6):
h3S + 4h3O + Cl2 = h3SO4 + 8HCl
MnS + 3HNO3 = MnSO4 + 8NO2 + 4h3O
PbS + 4h3O2 = PbSO4 + 4h3O
3. Соединение серы (+4).
Соединение серы (+4).
Из соединений серы со степенью окисления (+4) наиболее характерны оксид серы (SO2) или сернистый газ и сернистая кислота (h3SO3) и её соли. Оксид серы представляет собой газ с резким запахом, бесцветный, тяжелее воздуха, хорошо растворяется в воде. Получают при неполном горении сероводорода или при окислении сульфидов. В лаборатории его получают при взаимодействии меди с концентрированной серной кислотой:
Cu + h3SO4 = CuSO4 + SO2 + h3O
Na2SO3 + 2HCl = 2NaCl + SO2 + h3O
Для оксида серы (+4) характерны как окислительные:
SO2 + h3S = 3S + 2h3O
так и восстановительные свойства:
2SO2 + O2 = 2SO3
2SO2 + 2h3O + Br2 = h3SO4 + 2HBr
SO2 + Cl2 = SO2Cl2
SO2 + 2HNO3 = h3SO4 + 2NO2
Оксид серы (+4) – типичный кислотный оксид, он реагирует с основания-ми с образованием солей, с водой образует сернистую кислоту:
SO2 + 2NaOH = Na2SO4 + h3O
SO2 + h3O = h3SO3
Сернистая кислота – слабая кислота, диссоциирует в две стадии, образует два типа солей: кислые – гидросульфитыи средние –сульфиты :
h3SO3 ↔ HSO3– + H+
HSO3–↔ SO32- + H+
Соли сернистой кислоты неустойчивы, разлагаются при действии более сильных кислот и при нагревании:
Na2SO3 + HNO3 = 2NaNO3 + SO2 + h3O
K2SO3 = K2O + SO2
В растворах сульфит-ионы проявляют чаще всего восстановительные свойства:
Na2SO3 + 2KOH + KMnO4 = Na2SO4 + 2K2MnO4 + h3O
4. Соединения серы (+6)
Соединения серы (+6)
Из соединений серы в степени окисления (+6) наиболее характерны оксид серы – SO3 или серный ангидрид и h3SO4 – cерная кислота. SO3 – бесцветный газ с характерным резким запахом, тяжелее воздуха, хорошо растворим в воде.
Оксид серы (+6) получают окислением оксида серы (+4) в присутствии катализатора и высоком давлении:
2SO2 + O2 = 2SO3
SO3 + h3O = h3SO4
Оксид серы (+6) является сильным окислителем:
SO3 + 2KJ = J2 + K2SO3
SO3 + h3S = 4SO2 + h3O2
5SO3 + 2P = P2O5 + 5SO2
Кроме того, он проявляет кислотные свойства, так как является кислотным оксидом:
SO3 + ZnO = ZnSO4
SO3 + KOH = KHSO4
SO3 + 2KOH = K2SO4 + h3O
Серная кислота, её соли.
Серная кислота представляет собой бесцветную маслообразную жидкость, максимальная плотность которой 1,84 г/мл. Исходным сырьём для получения серной кислоты является серный колчедан или пирит:
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
Далее, под воздействием катализатора – V2O5 происходит окисление оксида серы (+4) до оксида серы (+6):
2SO2 + O2 = 2SO3
Полученная безводная серная кислота называется олеум, т.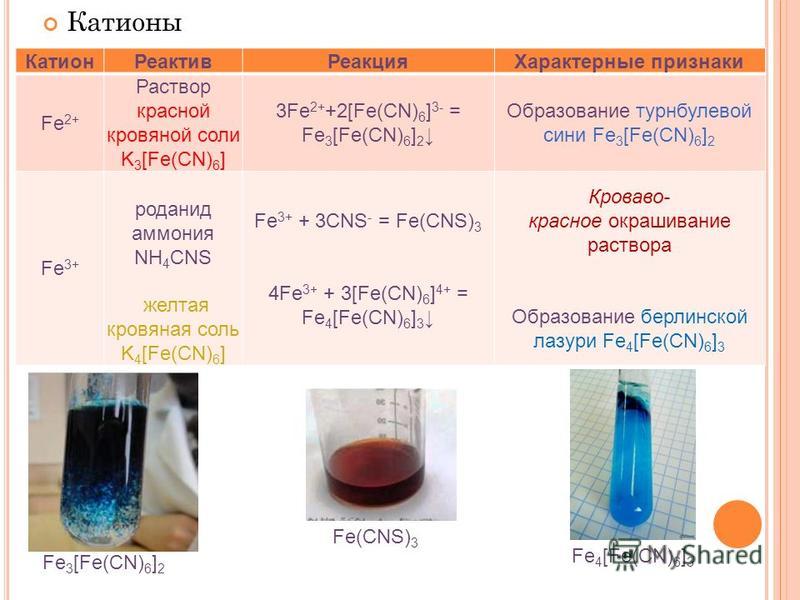 к. в действительности, оксид серы (+4) растворяют в 98%-ной серной кислоте.
к. в действительности, оксид серы (+4) растворяют в 98%-ной серной кислоте.
SO3 + h3O = h3SO4
Концентрированная серная кислота проявляет сильное водоотнимающее действие. Это свойство положено в основу многочисленных химических процессов, особенно в органической химии (получение спиртов, простых и сложных эфиров, альдегидов и т.д.). Концентрированная серная кислота является сильным окислителем. Например, при взаимодействии с просты-ми веществами, она окисляет их до кислот или оксидов:
2P + 5h3SO4 = 2h4PO4 + 5SO2 + 2h3O
C + h3SO4 = 2SO2 + CO2 + 2h3O
При обычной температуре она окисляет галогенводороды и сероводород:
h3SO4 + 8HJ = 4J2 + h3S + 4h3O
h3SO4 + 2HBr = Br2 + SO2 + 2h3O
Серная кислота термически устойчива и не летуча, поэтому способна вытеснять другие кислоты из их солей:
h3SO4 + KClO3 = KHSO4 + HClO4
Cерная кислота диссоциирует в две стадии, образует два типа солей:
кислые – гидросульфатыи средние – сульфаты:
h3SO4 ↔ HSO4– + H+
HSO4– ↔ SO42– + H+
Серная кислота проявляет свойства, характерные для остальных кислот: она реагирует с металлами, оксидами металлов, гидроксидами, солями слабых кислот. Качественной реакцией на сульфат-ионы в растворах является взаимодействие её с ионами бария Ва2+, в результате чего выпадает белый осадок:
Качественной реакцией на сульфат-ионы в растворах является взаимодействие её с ионами бария Ва2+, в результате чего выпадает белый осадок:
Ba2+ + SO42- = BaSO4
При прокаливании сульфаты разлагаются на различные классы соединений в зависимости от металла, входящего в состав соли. Сульфаты щелочных металлов плавятся без разложения. Сульфаты металлов средней активности разлагаются на соответствующие оксиды:
ZnSO4 = ZnO + SO3
Сульфат железа (II) разлагается по механизму внутримолекулярной ОВР:
4FeSO4 = 2Fe2O3 + 4SO2 + O2
Сульфаты наиболее тяжёлых или малоактивных металлов разлагаются с образованием простых веществ – металла и кислорода:
HgSO4 = Hg + SO2 + O2
Некоторые сульфаты, являясь окислителями, реагируют с простыми веществами:
CaSO4 + C = CaO + SO2 + CO
BaSO4 + 4C = BaS + 4CO
Большое значение в промышленности, лабораторных исследованиях имеет взаимодействие серной кислоты с металлами. Эта тема заслуживает особого внимания, т.к. образуются различные продукты реакции в зависимости от положения реагируемого металла в ряду напряжений, степени разбавленности кислоты, температуры, катализаторов.
Эта тема заслуживает особого внимания, т.к. образуются различные продукты реакции в зависимости от положения реагируемого металла в ряду напряжений, степени разбавленности кислоты, температуры, катализаторов.
Разбавленная серная кислота с металлами, стоящими в ряду активности до водорода, при обычной температуре образует соль и водород:
h3SO4 + Zn = ZnSO4 + h3
Разбавленная кислота не реагирует с металлами, стоящими в ряду активности после водорода (медь, серебро, ртуть), но концентрированная кислота образует с ними соль, оксид серы (+4) и воду:
h3SO4 + Cu = CuSO4 + SO2 + h3O
Такие же продукты реакции концентрированная серная кислота образует при взаимодействии с металлами, стоящими в ряду активности до водорода:
2h3SO4 + Zn = ZnSO4 + SO2 + 2h3O
Однако, концентрированная серная кислота реагирует не со всеми металлами. Алюминий, железо, свинец и олово она пассивирует с образованием на их поверхности тонких оксидных плёнок, предотвращающих дальнейшее растворение металла:
h3SO4 + Al = Al2O3 + SO2 + h3O
Активные щелочные и щелочноземельные металлы могут образовывать с разбавленной кислотой не только водород.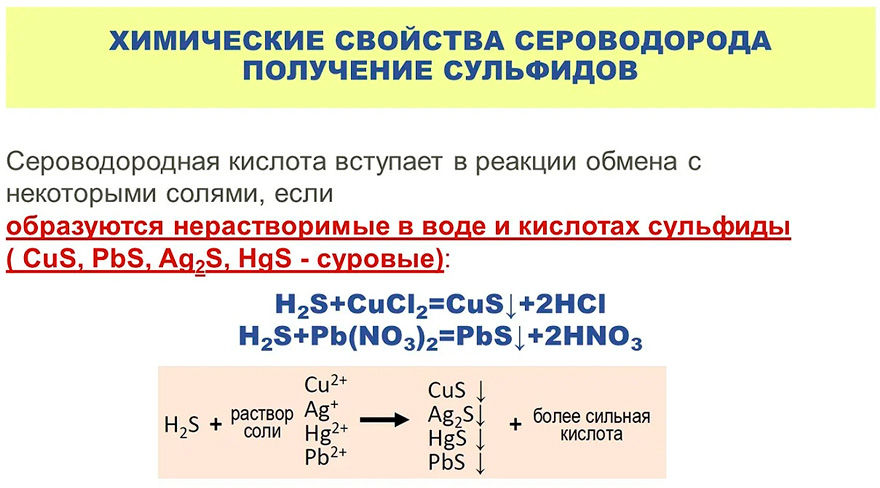 Например, магний с очень разбавленной серной кислотой на холоду образует соль, серу и воду:
Например, магний с очень разбавленной серной кислотой на холоду образует соль, серу и воду:
h3SO4 + Mg = MgSO4 + S + h3O
Натрий при обычной температуре с очень разбавленной серной кислотой образует соль, серу и воду:
h3SO4 + Na = Na2SO4 + S + h3O,
а при охлаждении образует сероводород:
h3SO4 + Na = Na2SO4 + Н2S + h3O
Соли серной кислоты находят большое применение в промышленности, сельском хозяйстве, в быту.
Na2SO4x 10h3O – глауберова соль, применяется в медицине в качестве слабительного,
(Nh5)2SO4 – азотное удобрение для сельского хозяйства,
CaSO4 – безводный гипс, применяется в строительстве.
CaSO4x 2h3O – водный гипс,
2CaSO4 xh3O – алебастр, продукт получения гипса,
MgSO4 – горькая соль, применяется в медицине как слабительное и гипотензивное средство,
BaSO4 – баритова каша, средство, применяемое как рентгеноконтрастное средство.
CuSO4 x 5h3O – медный купорос, применяется в строительстве,
FeSO4x 7h3O – железный купорос,
ZnSO4 x 7h3O – цинковый купорос,
KАl(SO4)2 x 12h3O – алюмокалиевые квасцы.
© blog.tutoronline.ru, при полном или частичном копировании материала ссылка на первоисточник обязательна.
Химические свойства кислот, химия 8 класс
Общие свойства кислот. Классификация
Кислоты — класс сложных химических веществ, состоящих из атомов водорода и кислотных остатков.
В первую очередь кислоты делятся на:
- органические или карбоновые и
- неорганические или минеральные.
Свойства карбоновых кислот подробно разбираются в статье Карбоновые кислоты (ссылка на статью)
В зависимости от количества атомов водорода, которые могут замещаться в химических реакциях различают:
- одноосновные кислоты
- двухосновные кислоты
- трехосновные кислоты.
Не смотря на то, что в уксусной кислоте четыре атома водорода, три из них принадлежат кислотному остатку и в реакциях замещения не участвуют.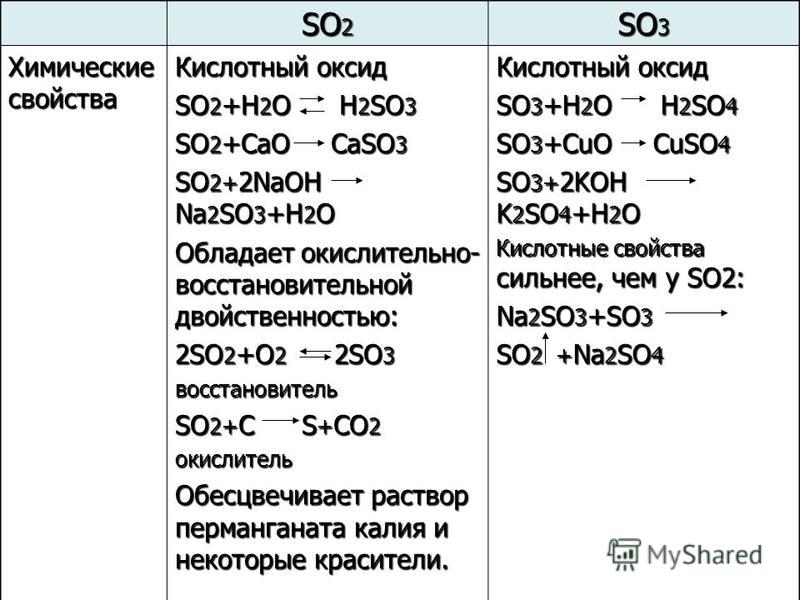 Соответственно, уксусная кислота — одновалентная.
Соответственно, уксусная кислота — одновалентная.
Свойства неорганических кислот также зависят от наличия в их составе кислорода и делятся на
- бескислородные
- кислородсодержащие.
Растворы кислот способны диссоциировать и проводить электрический ток т.е. являются электролитами. В зависимости от степени диссоциации делятся на:
- сильные
- слабые электролиты.
Химические свойства кислот
1. Диссоциация
При диссоциации кислот образуются катионы водорода и анионы кислотного остатка.
HNO3 → H+ + NO–3
HCl → H+ + Cl–
Многоосновные кислоты диссоциируют ступенчато.
Н3РО4 ↔ Н+ + Н2РО–4 (первая ступень)
Н2РО–4 ↔ Н+ + НРO2-4 (вторая ступень)
НРО2-4 ↔ Н+ + PОЗ-4 (третья ступень)
2.
 Разложение
РазложениеКислородсодержащие кислоты разлагаются на оксиды и воду.
H2CO3 → H2O + CO2↑
Бескислородные на простые вещества
| t | ||
| 2HCl | → | Cl2 + H2. |
3. Реакция с металлами
Кислоты реагируют лишь с теми металлами, что стоят в ряду активности до кислорода. В результате взаимодействия образуется соль и выделяется водород.
Mg + 2HCl → MgCl2 + H2↑
Найти ряд активности можно на последней странице электронного учебника «Химия 9 класс» под редакцией В. В. Еремина.
Бдительные ученики могут сказать: «Золото стоит в ряду активности металлов после водорода, а с „царской водкой“ реагирует. Как же так?»
Как же так?»
Из всех правил есть исключения.
Поскольку в состав азотной кислоты входит азот со степенью окисления +5, а в состав серной — сера со степенью окисления +6, то с металлами реагируют не ионы водорода, а более сильные окислители. Образуется соль, но не происходит выделения водорода.
Au + HNO3 + 4HCl → HAuCl4 + NO + 2H2O.
4. Реакции с основаниями
В результате образуются соль и вода, происходит выделение тепла.
Na2CO3 + 2CH3 — COOH → 2CH3 — COONa + H2O + CO2↑.
Реакции такого типа называются реакциями нейтрализации. Простейшая реакция, которую можно провести на собственной кухне — гашение соды столовым уксусом или 9%раствором уксусной кислоты.
5. Реакции кислот с солями
Вспомним, когда мы разбирали ионные уравнения ( ссылка на статью), одним из условий протекания реакций было образование в ходе взаимодействия нерастворимой соли, выделение летучего газа или слабо диссоциирующего вещества — например, воды. Те же условия сохраняются и для реакций кислот с солями.
Те же условия сохраняются и для реакций кислот с солями.
BaCl2 + H2SO4 → BaSO4↓ + 2HCl↑
6. Реакция кислот с основными и амфотерными оксидами
В ходе реакции образуется соль и происходит выделение воды.
K2O + 2HNO3 → 2KNO3 + H2O
7. Восстановительные свойства бескислородных кислот
Если в окислительных реакциях первую скрипку играет водород, то в восстановительных реакциях основная роль принадлежит анионному остатку. В результате реакций образуются свободные галогены.
4HCl + MnO2 → MnCl2 + Cl2↑ + 2H2O
Физические свойства кислот
При нормальных условиях (Атмосферное давление = 760 мм рт. ст. Температура воздуха 273,15 K = 0°C) кислоты чаще жидкости, хотя встречаются и твердые вещества: например ортофосфорная H3PO4 или кремниевая H2SiO3.
Некоторые кислоты представляют собой растворы газов в воде: фтороводородная-HF, соляная-HCl, бромоводородная-HBr.
Кислотные свойства кислот в ряду HF → HCl → HBr → HI усиливаются.
Для некоторых кислот (соляная, серная, уксусная) характерен специфический запах.
Благодаря наличию ионов водорода в составе, кислоты обладают характерным кислым вкусом.
Химическая лаборатория не ресторан, и в целях безопасности существует жесткий запрет на опробование на вкус химических веществ.
Как же можно определить кислота в пробирке или нет?
В 1300 году был открыт лакмус, и с тех пор алхимикам и химикам не пришлось рисковать своим здоровьем, пробуя на вкус содержимое пробирок. Запомните, что лакмус в кислой среде краснеет.
Вторым широко используемым индикатором является фенолфталеин.
Простой мнемонический стишок поможет запомнить, как ведут себя индикаторы в разных средах.
Индикатор лакмус — красный
Кислоту укажет ясно.
Индикатор лакмус — синий,
Щёлочь здесь — не будь разиней,
Когда ж нейтральная среда,
Он фиолетовый всегда.
Фенолфталеиновый — в щелочах малиновый
Но несмотря на это в кислотах он без цвета.
Что ещё почитать?
Неметаллы
Биография Д.И. Менделеева. Интересные факты из жизни великого химика
Карбоновые кислоты
Массовая доля вещества
18HBr + 2KMnO4 →2KBr + 2MnBr2 + 8H2O + 5Br2
14НI + K2Cr2O7 →3I2↓ + 2Crl3 + 2KI + 7H2O
#ADVERTISING_INSERT#
3.5: Различия в физических и химических свойствах вещества
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 47458
Цели обучения
Отделить физические свойства от химических.
Все вещества обладают физическими и химическими свойствами. Физические свойства — это характеристики, которые ученые могут измерить без изменения состава исследуемого образца, такие как масса, цвет и объем (объем пространства, занимаемый образцом). Химические свойства описывают характерную способность вещества реагировать с образованием новых веществ; они включают его воспламеняемость и подверженность коррозии. Все образцы чистого вещества обладают одинаковыми химическими и физическими свойствами. Например, чистая медь всегда представляет собой красновато-коричневое твердое вещество (физическое свойство) и всегда растворяется в разбавленной азотной кислоте с образованием синего раствора и коричневого газа (химическое свойство).
Физическое свойство
Физическое свойство — это характеристика вещества, которую можно наблюдать или измерять без изменения идентичности вещества. Серебро — это блестящий металл, который очень хорошо проводит электричество. Из него можно формовать тонкие листы, это свойство называется пластичностью. Соль тусклая и ломкая и проводит электричество, когда она растворена в воде, что она делает довольно легко. К физическим свойствам вещества относятся цвет, твердость, ковкость, растворимость, электропроводность, плотность, температура плавления и температура кипения.
Из него можно формовать тонкие листы, это свойство называется пластичностью. Соль тусклая и ломкая и проводит электричество, когда она растворена в воде, что она делает довольно легко. К физическим свойствам вещества относятся цвет, твердость, ковкость, растворимость, электропроводность, плотность, температура плавления и температура кипения.
Для элементов цвет не сильно отличается от одного элемента к другому. Подавляющее большинство элементов бесцветные, серебристые или серые. Некоторые элементы имеют отличительные цвета: сера и хлор — желтые, медь (разумеется) медного цвета, а элементарный бром — красный. Однако плотность может быть очень полезным параметром для идентификации элемента. Из материалов, существующих в твердом состоянии при комнатной температуре, йод имеет очень низкую плотность по сравнению с цинком, хромом и оловом. Золото имеет очень высокую плотность, как и платина. Чистая вода, например, имеет плотность 0,998 г/см 3 при 25°C. Средние плотности некоторых распространенных веществ приведены в таблице \(\PageIndex{1}\). Обратите внимание, что кукурузное масло имеет более низкое отношение массы к объему, чем вода. Это означает, что при добавлении в воду кукурузное масло будет «плавать».
Обратите внимание, что кукурузное масло имеет более низкое отношение массы к объему, чем вода. Это означает, что при добавлении в воду кукурузное масло будет «плавать».
| Вещество | Плотность при 25°C (г/см3) |
|---|---|
| кровь | 1,035 |
| жировые отложения | 0,918 |
| цельное молоко | 1,030 |
| масло кукурузное | 0,922 |
| майонез | 0,910 |
| мед | 1,420 |
Твердость помогает определить, как можно использовать элемент (особенно металл). Многие элементы довольно мягкие (например, серебро и золото), в то время как другие (например, титан, вольфрам и хром) намного тверже. Углерод — интересный пример твердости. В графите («грифеле» карандашей) углерод очень мягкий, в то время как углерод в алмазе примерно в семь раз твёрже.
Многие элементы довольно мягкие (например, серебро и золото), в то время как другие (например, титан, вольфрам и хром) намного тверже. Углерод — интересный пример твердости. В графите («грифеле» карандашей) углерод очень мягкий, в то время как углерод в алмазе примерно в семь раз твёрже.
Точки плавления и кипения являются уникальными идентификаторами, особенно для соединений. Помимо получения некоторого представления об идентичности соединения, можно получить важную информацию о чистоте материала.
Химические свойства
Химические свойства вещества описывают его способность подвергаться некоторым химическим изменениям или реакциям в силу своего состава. Присутствующие элементы, электроны и связи придают материи потенциал для химических изменений. Довольно сложно определить химическое свойство, не используя слово «изменение». В конце концов, после изучения химии в течение некоторого времени, вы сможете взглянуть на формулу соединения и указать некоторые химические свойства. Например, водород может воспламениться и взорваться при определенных условиях — это химическое свойство. Металлы вообще имеют химическое свойство реагировать с кислотой. Цинк реагирует с соляной кислотой с образованием газообразного водорода — это химическое свойство.
В конце концов, после изучения химии в течение некоторого времени, вы сможете взглянуть на формулу соединения и указать некоторые химические свойства. Например, водород может воспламениться и взорваться при определенных условиях — это химическое свойство. Металлы вообще имеют химическое свойство реагировать с кислотой. Цинк реагирует с соляной кислотой с образованием газообразного водорода — это химическое свойство.
Химическим свойством железа является его способность соединяться с кислородом с образованием оксида железа, химическое название ржавчины (Рисунок \(\PageIndex{2}\)). Более общим термином для ржавчины и других подобных процессов является коррозия. Другими терминами, которые обычно используются при описании химических изменений, являются горение, гниение, взрыв, разложение и брожение. Химические свойства очень полезны при идентификации веществ. Однако, в отличие от физических свойств, химические свойства можно наблюдать только тогда, когда вещество находится в процессе превращения в другое вещество.
Химические свойства очень полезны при идентификации веществ. Однако, в отличие от физических свойств, химические свойства можно наблюдать только тогда, когда вещество находится в процессе превращения в другое вещество.
| Физические свойства | Химические свойства |
|---|---|
| Металлический галлий плавится при 30 o C. | Железный металл ржавеет. |
| Ртуть — очень плотная жидкость. | Зеленый банан при созревании становится желтым. |
| Золото блестит. | Горит сухой лист бумаги. |
Пример \(\PageIndex{1}\)
Какое из следующих химических свойств железа?
- Железо разъедает во влажном воздухе.
- Плотность = 7,874 г/см 3
- Железо в чистом виде мягкое.
- Железо плавится при 1808 К.
Раствор
«Железо разъедает во влажном воздухе» — единственное химическое свойство железа из списка.
Упражнение \(\PageIndex{1A}\)
Какое из перечисленных ниже физических свойств материи?
- коррозионная активность
- рН (кислотность)
- плотность
- воспламеняемость
- Ответить
- с
Упражнение \(\PageIndex{1B}\)
Какое из следующих свойств является химическим?
- воспламеняемость
- температура плавления
- точка кипения
- плотность
- Ответить
- и
Резюме
Физическое свойство – это характеристика вещества, которую можно наблюдать или измерять без изменения свойств вещества. Физические свойства включают цвет, плотность, твердость, температуры плавления и кипения. Химическое свойство описывает способность вещества подвергаться определенному химическому изменению. Чтобы идентифицировать химическое свойство, мы ищем химическое изменение. Химическое изменение всегда производит один или несколько типов материи, которые отличаются от материи, существовавшей до изменения. Образование ржавчины — это химическое изменение, потому что ржавчина — это вещество, отличное от железа, кислорода и воды, существовавших до образования ржавчины.
Физические свойства включают цвет, плотность, твердость, температуры плавления и кипения. Химическое свойство описывает способность вещества подвергаться определенному химическому изменению. Чтобы идентифицировать химическое свойство, мы ищем химическое изменение. Химическое изменение всегда производит один или несколько типов материи, которые отличаются от материи, существовавшей до изменения. Образование ржавчины — это химическое изменение, потому что ржавчина — это вещество, отличное от железа, кислорода и воды, существовавших до образования ржавчины.
ПОД ЛИЦЕНЗИЕЙ
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- СК-12
- Показать страницу TOC
- № на стр.

- Теги
- автор@Генри Эгнью
- автор@Мариса Альвиар-Агнью
- химическое свойство
- физическое имущество
- источник@https://www.ck12.org/c/chemistry/
Q10 Сравните свойства сульфида железа II со смесью железа с серой, учитывая сульфид железа II…
Перейти к
- Упражнение
- Вопросы объективного типа
- Иметь значение
- Физические и химические изменения
- Элементы, соединения и смеси
- Атомная структура
- Язык химии
- Химические реакции
- Водород
- Вода
- Углерод и его соединения
Главная >
Союзные решения
Класс 8
Химия
>
Глава 3. Элементы, соединения и смеси
>
Упражнение
>
Вопрос 10
Элементы, соединения и смеси
>
Упражнение
>
Вопрос 10
Вопрос 10 Упражнение
В10) Сравните свойства сульфида железа (II) со смесью железа и серы, рассматривая сульфид железа (II) как соединение и частицы железа и серы, смешанные вместе, в качестве примера смеси.
Ответ:
Решение:
| Сульфид железа [II] | Железо – Сера |
|---|---|
| Это твердое вещество черного цвета. | Железо и сера можно увидеть отдельно. |
| Их нельзя разделить с помощью магнита. | Когда магнит приближается к смеси, железо притягивается к магниту. |
| При добавлении разбавленной HCl выделяется газообразный водород. | При добавлении разбавленной HCl выделяется [[> widget <]]. |
Стенограмма видео
“Всем привет, так что
Все у вас хорошо. Таким образом, сегодняшний вопрос состоит в том, чтобы сравнить свойства двухкомпонентного файла серы со смесью железа и серы. Итак, учитывая тот факт, что я сделал с сульфидом, это соединение, в то время как частицы железа и серы были смешаны вместе, и это пример смеси. Итак, мы должны сравнить железо с сульфидом со смесью железа и серы. И так это
Соединение найти имею ввиду. Это миссия. Хорошо. Таким образом, в основном первым моментом, который отличает соединение сульфата железа II от смеси железа и серы, является тот факт, что добавление к сере и сульфиду представляет собой твердое вещество черного цвета. Хорошо. Это сплошной черный цвет, а когда мы говорим о железе и сере так хорошо, убедитесь, что их можно увидеть отдельно. Итак, это как первый пункт переходит ко второму. Итак, во втором мы можем видеть здесь, во втором. Их можно разделить по связи с химическим процессом любого соединения. Они требуют химического процесса, который не может быть разделен в отличие от физических процессов. Поэтому, конечно, для добавления к сульфиду, который является соединением, мы можем разделить элементы с помощью электрического электрохимического процесса. Хорошо,
Это идентифицировано сейчас, приближаясь к железной сере, убедитесь, что ее можно легко отделить с помощью магнита, когда вы поднесете магнит близко к смеси. Железо отделится от смеси, которая сейчас идет. К Пойнту здесь. Хорошо железо до сульфида имеет однородный композиционный состав. Хорошо, а между тем смесь железа и серы имеет неоднородный состав. Итак, это кубок по очкам, но есть еще один момент. Итак, если мы хотим добавить разбавленную HCL, давайте посмотрим, что произойдет с соединением железа с сульфидом. И когда мы добавим I в качестве STL к смеси железа с серой, реакция будет другой. Так что в основном эти
Вместе разные соединения, поскольку они имеют разный набор свойств, а не разные соединения.
Итак, во втором мы можем видеть здесь, во втором. Их можно разделить по связи с химическим процессом любого соединения. Они требуют химического процесса, который не может быть разделен в отличие от физических процессов. Поэтому, конечно, для добавления к сульфиду, который является соединением, мы можем разделить элементы с помощью электрического электрохимического процесса. Хорошо,
Это идентифицировано сейчас, приближаясь к железной сере, убедитесь, что ее можно легко отделить с помощью магнита, когда вы поднесете магнит близко к смеси. Железо отделится от смеси, которая сейчас идет. К Пойнту здесь. Хорошо железо до сульфида имеет однородный композиционный состав. Хорошо, а между тем смесь железа и серы имеет неоднородный состав. Итак, это кубок по очкам, но есть еще один момент. Итак, если мы хотим добавить разбавленную HCL, давайте посмотрим, что произойдет с соединением железа с сульфидом. И когда мы добавим I в качестве STL к смеси железа с серой, реакция будет другой. Так что в основном эти
Вместе разные соединения, поскольку они имеют разный набор свойств, а не разные соединения. Это соединение. Это смесь. Ладно, так давайте так, ладно. Я напишу этот момент, когда добавлю cael. Добавление разбавленной HCL.
Водород
Газы
Информация на циферблате при добавлении одной секунды. Так да.
А я думаю разбавить HCL.
Задыхается нормально, выделяется сероводородный газ. Итак, как я уже сказал, у них совершенно разные наборы свойств. Итак, да, это различия между железом и сульфидом и миссией железа и серы. Надеюсь, это помогло вам. Спасибо.
Это соединение. Это смесь. Ладно, так давайте так, ладно. Я напишу этот момент, когда добавлю cael. Добавление разбавленной HCL.
Водород
Газы
Информация на циферблате при добавлении одной секунды. Так да.
А я думаю разбавить HCL.
Задыхается нормально, выделяется сероводородный газ. Итак, как я уже сказал, у них совершенно разные наборы свойств. Итак, да, это различия между железом и сульфидом и миссией железа и серы. Надеюсь, это помогло вам. Спасибо.
Связанные вопросы
Q1) Изобразите с помощью простой схемы, как материя классифицируется на чистую или нечистую субстанцию…
Q2) Дайте определение терминам элементы, соединения и смеси, чтобы показать их основное различие.
Q3) «Атом — это основная единица элемента». Нарисуйте схему атома — делимого, как это видно сегодня.
Q4) «Современная периодическая таблица состоит из элементов, расположенных в порядке возрастания их атомного числа.