Химия электропроводность меди: Электротехническая медь, основные характеристики
alexxlab | 14.12.1991 | 0 | Разное
Электропроводность металлов | PHYWE
Nach oben
Информация
- Контактное лицо
- Условия сотрудничества
- Декларация о конфиденциальности
- Вводные данные
Обслуживание
- Краткий обзор услуг
- Скачать
- Каталоги
- Вебинары и Видео
- Связаться со службой поддержки клиентов
Компания
- О нас
- Качественная политика
- Безопасность в классе
Please note
* Prices subject to VAT.
We only supply companies, institutions and educational facilities. No sales to private individuals.
Please note: To comply with EU regulation 1272/2008 CLP, PHYWE does not sell any chemicals to the general public. We only accept orders from resellers, professional users and research, study and educational institutions.
Пожалуйста, введите имя, под которым должна быть сохранена Ваша корзина.
Сохраненные корзины вы можете найти в разделе My Account.
Название корзины
С этим файлом связано 2 файл(ов). Среди них: Все части курсача-Лист 1.pdf, Расчёт кран башенный задачка кр 1.docx. Показать все связанные файлы Подборка по базе: Лев Яшин реферат.docx, Наследственность и изменчивость – свойства организмов.  11класс.do, Сестринский уход. Реферат. Уход за хирургическим больным.docx, Новообразование Уматов Реферат (1).docx, Порядок оказания медицинской помощи по профилю акушерство и гине, требования к реферату.docx, Психология реферат.docx, Темы рефератов по дисциплине Философия.pdf, Формирование информационной культуры и медиакомпетентностей всех, Основы ГМУ реферат.docx 11класс.do, Сестринский уход. Реферат. Уход за хирургическим больным.docx, Новообразование Уматов Реферат (1).docx, Порядок оказания медицинской помощи по профилю акушерство и гине, требования к реферату.docx, Психология реферат.docx, Темы рефератов по дисциплине Философия.pdf, Формирование информационной культуры и медиакомпетентностей всех, Основы ГМУ реферат.docx1 2 3 МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ «МОСКОВСКИЙ АВИАЦИОННЫЙ ИНСТИТУТ (национальный исследовательский университет)» (МАИ) Кафедра «Технология испытаний и эксплуатации» Реферат «Свойства меди и его соединений » по дисциплине «Общая химия» (1 семестр) Студент Лахонина А.В Группа Т12О-109Б-19 Дата сдачи Подпись Проверила Максина Т.Я. Дата Подпись МОСКВА 2019 МОСКВА 2019 Содержание История открытия………………………………………………3 Нахождение в природе…………………………………………4 Получение……………………………………………………….4 Физические свойства……………………………………………7 Элекронное строение атома……………………………………8 Химические свойства…………………………………………..8 Оксиды и гидроксиды меди …………………………………9 Отношение меди к различным агрессивным средам………10 Применение меди и его соединений……………………………12 Список источников………………………………………………13 История открытия Медь повсюду. Оглянитесь вокруг. Она в стенах вашего дома, в электрических и телефонных проводах, в компьютерах, холодильниках, микроволновых печах и автомобилях. Медь наиболее универсальный и прочный из всех металлов, за что получила название «вечный материал».  Без меди никогда не было бы электрического света и космического полета. Это чудесный металл и ее сплавы используются во всех технологиях от телекоммуникаций до транспорта. Что мы можем узнать из истории открытия меди? Без меди никогда не было бы электрического света и космического полета. Это чудесный металл и ее сплавы используются во всех технологиях от телекоммуникаций до транспорта. Что мы можем узнать из истории открытия меди?Считается, что латинское название меди Cuprum (Cu) произошло от названия острова Кипр, где римляне добывали медь из богатых медью рудников. Никто не знает точно, где имеет свое начало история открытия меди. Археологические данные свидетельствуют, что медь была в употреблении еще 10.000 лет назад в Западной Азии. В доисторический период энеолита, медь использовали для производства украшений и орудий. Уже с 3-4-го тысячелетия до н.э., медь активно извлекают из рудников в районе города Уэльвы в Испании. Около 2500 г. До н.э., открытие полезных свойств медно-оловянных сплавов привело к бронзовому веку. Археологи восстановили часть водной системы водопровода пирамиды Хеопса в Египте. Медные трубы, использованные в ней, были в исправном состояниине смотря на то что им более чем 5000 лет. Было документально подтверждено, что в израильской долине Тимна добывали медь для фараонов. Запись на папирусе из Древнего Египта показывает, что медь была использована для лечения инфекций и стерилизации воды. Остров Кипр, как известно, поставлял много меди, необходимой для Финикии, Греции и Рима. Хотя греки в эпоху Аристотеля были знакомы с латунью, однако до Римской империи Августа, медь не была активно использованной. В Южной Америке племена майя, ацтеков, инков и прочих древних цивилизаций использовали медь, а также золото и серебро. В средние века, использование меди и бронзы процветает в Китае, Индии и Японии. Бронзовый век назван в честь бронзы, сплава меди и олова. История открытия меди считается историей развития человечества. Медь и ее сплавы являются одной из основных групп коммерческих металлов. Они широко используются из-за их отличных электрической и тепловой проводимости, высокой стойкости к коррозии, и простоты изготовления, а также хорошей прочность и сопротивлению усталости. Они, как правило, немагнитные. Медь легко спаивается, поэтому она используется для производства котлов. Медь и ее сплавы используется для декоративных деталей, т.к. легко полируется почти до любой желаемой текстуры и блеска. Нахождение в природе В земной коре содержание меди составляет около 5·10–3% по массе. Очень редко медь встречается в самородном виде (самый крупный самородок в 420 тонн найден в Северной Америке). Из руд наиболее широко распространены сульфидные руды: халькопирит, или медный колчедан, CuFeS2 (30% меди), ковеллин CuS (64,4% меди), халькозин, или медный блеск, Cu2S (79,8% меди), борнит Cu5FeS4 (52-65% меди). Существует также много и оксидных руд меди, например: куприт Cu2O, (81,8% меди), малахит CuCO3·Cu(OH)2 (57,4% меди) и другие.  Различных руд меди много, а вот богатых месторождений на земном шаре мало, к тому же медные руды добывают уже многие сотни лет, так что некоторые месторождения полностью исчерпаны. Часто источником меди служат полиметаллические руды, в которых, кроме меди, присутствуют железо (Fe), цинк (Zn), свинец (Pb), и другие металлы. Как примеси медные руды обычно содержат рассеянные элементы (кадмий, селен, теллур, галий, германий и другие), а также серебро, а иногда и золото. Для промышленных разработок используют руды, в которых содержание меди составляет немногим более 1 % по массе, а то и менее. В морской воде содержится примерно 1·10–8 % меди. Получение · Получение меди методом электролиза. Электролиз широко применяют для очистки (рафинирования) меди. Для очистки меди из черновой меди отливают аноды – толстые пластины. Их подвешивают в ванну, содержащую раствор медного купороса. Примеси, входящие в состав черновой меди ведут себя по-разному. Более электроотрицательные элементы – цинк, железо, кадмий и другие растворяются на аноде. Но на катоде эти металлы не выделяются, так как электрохимическом ряду напряжений они находятся левее меди и имеют более отрицательные потенциалы. · Металлотермический метод получения. 3CuO+2Al=>Al2O3+3Cu 3Cu+2Fe=>Fe2O3+3Cu+Q · Пирометаллургический способ получения меди. Поскольку содержание меди не превышает 1. Сульфидную руду сначала обжигают при свободном токе воздуха для удаления части серы: 2CuS+3O2. Этот обжиг проводят в механических печах, похожих на устройства для обжига серного колчедана. 3Cu’>2CuO+4CuS=>3Cu2S+SO2. Пустая порода, часть сульфидов и окислов железа переходит в шлак, а на дне печи скапливается штейн – расплав сульфида меди Cu2S и сульфида железа FeS. Штейн сливают из печи и перерабатывают в конвекторе, который по устройству похож на конвектор для переработки стали. Частичное удаление серы происходит за счет продувки воздуха через расплавленный штейн: 2Cu2S+3O2 =>2Cu2O+2SO2. Сульфид меди и закись меди дают металлическую черновую медь: Cu 2S+2Cu2O=>SO2+6Cu Она содержит около 95-98% меди. Более просто перерабатывают окисные руды меди, состоящие из закиси меди, окиси меди и карбонатов меди (Cu2O, CuO, CuCO3•Cu(OH)2). Эти руды обогащения прокаливают с коксом при высокой температуре: 2CuO+C=>CO2+2Cu. Добыча и получение солей меди из природных месторождений. Около 15% всех руд меди перерабатывается гидрометаллургическим методом – на измельченную руду действуют растворителем, который переводит медь в раствор. На руды, содержащие оксид меди, действуют разбавленной серной кислотой: CuO+H2SO4 =>CuSO4+H2O По сравнению со многими другими оксидами, встречающимися в руде, оксид меди растворяется сравнительно хорошо. Если медь находится в руде в виде сульфида, то ее в раствор можно перевести, обрабатывая ее руду раствором сульфата железа: CuSO4+2Fe2SO4 =>4FeSO4+2CuSO+S · Гидрометаллургическом способе получения Этот способ используют бедные медные руды, которые подвергают выщелачиванию. Для выщелачивания руду желательно мелко раздробить. Процесс ведется в кучах, а также в деревянных и бетонных чанах. Выщелачивания ведется при помощи растворителей H2S04, Fe (SO4)3, Nh5OH и др. Легче всего растворяются окисленные медные руды: CuO + H2SO4 =>CuSO4 + H2O СuСО3 * Сu(ОН)2 + 2 Н2SO4 =>2СuSO4 + 3 Н2О +СO2. Сернистые соединения меди выщелачиваются сернокислым железом: Cu2S + 2 Fe2 (SО4)3 =>2 СuSO4 + 4 FeSO4 + S. При выщелачивании медных руд достигается почти полное извлечение меди, что дает возможность перерабатывать даже к бедные окисленные руды. Полученные растворы солей меди при выщелачивании подвергают дальнейшей обработке с целью извлечения меди. Из бедных цттиоров медь добывают методом цементации. В раствор опускают обрезки железа (листы, проволоку). Железо замещает медь в сернокислых солях и медь выделяется в виде металлического мелкого порошка: CuSО4 + Fe =>FeSО4 + Cu. Цементационная медь содержит до 70% Сu. Растворы, содержащие большое количество сернокислых солей меди, подвергают электролизу с нерастворимыми постоянными анодами. Физические свойства Плотность. По международному стандарту по отожженной меди (International Annealed Copper Standard – IACS) плотность меди принята равной 8890 кг/м3 при температуре 20°С. Однако в зависимости от вида обработки и химического состава плотность меди может иметь небольшие отличия. Например, литая медь имеет плотность 8920 кг/м3. При холодной деформации отожженной меди уменьшается ее плотность. При нагреве плотность меди заметно уменьшается, что видно на примере марки M1:
t,°С 20 600 700 800 900 1000 γ, кг/м3 8890 8680 8610 8550 8470 8400 Электрические свойства. Высокая электропроводность меди является основным свойством, обусловливающим ее широкое применение. Тепловые свойства. Удельная теплоемкость с меди заметно увеличивается с повышением температуры. В жидком состоянии в интервале температур перегрева при литье слитков удельная теплоемкость меди практически не зависит от температуры и может быть принята равной 545 Дж/(кгК). Краткие характеристики: в чистом виде плотность металла составляет 8.93 г/см3; хорошая электропроводность с показателем 55,5S, при температуре около 20⁰; теплопередача 390 Дж/кг; кипение происходит на отметке 2600°, после чего начинает выделение углерода; удельное электрическое сопротивление в среднем температурном диапазоне – 1.78×10 Ом/м. Элекронное строение атома Степень окисления меди в соединениях Медь может существовать в виде простого вещества – металла, а степень окисления металлов в элементарном состоянии равна нулю, так как распределение электронной плотности в них равномерно. В своих соединениях медь может проявлять степени окисления: (+1) (Cu+12O, Cu+1OH, K[Cu+1(CN)2] Cu+1Cl и т.д.) (+2) (Cu+2O, Cu+2Cl2, Cu+2(OH)2) (+3) (Kcu+3O2) Химические свойства 6.1 Соединения металла с неметалла а) с серой 1 2 3 |
Трудности меднения в производстве печатных плат
Фазлутдинов К.К.
12.12.2018 (обновленно 17.05.2021)
2327 просмотров
В настоящее время одной из важнейших проблем в технологии изготовления печатных плат является получение равномерных по толщине покрытий на поверхности и в отверстиях. При металлизации отверстий применяют электролиты меднения. Но равномерное покрытие медью требуется не только в отверстиях, но и по всей заготовке платы, т.к. от этого будет зависеть равномерность травления проводящего рисунка и, отчасти, величина бокового подтрава под фоторезистом.
При металлизации отверстий применяют электролиты меднения. Но равномерное покрытие медью требуется не только в отверстиях, но и по всей заготовке платы, т.к. от этого будет зависеть равномерность травления проводящего рисунка и, отчасти, величина бокового подтрава под фоторезистом.
Медь — пластичный и легко полирующийся металл с удельным весом 8,9 кг/м3 и температурой плавления 1084°С. Теплопроводность меди 330 ккал/м·час·°С, а удельное электрическое сопротивление 0,0175 Ом·мм2/м.
Гальваническое осаждение меди было открыто в 1838 г. русским академиком Б.С. Якоби. С этого времени меднение широко применяется во многих отраслях промышленности.
Нормальный потенциал меди +0,34 В. Гальванически осажденная медь имеет красивый розовый цвет, но в атмосферных условиях легко реагирует с влагой, углекислотой воздуха, с сернистыми газами – покрывается окислами, гидроксидами, карбонатами, сульфидами и в результате темнеет. При этом ее переходное электрическое сопротивление резко возрастает. Медь интенсивно растворяется в азотной кислоте, медленнее – в хромовой, значительно слабее – в серной, и почти не реагирует с соляной кислотой. введение окислителей резко увеличивает скорость этих реакций. Органические кислоты и аммиак легко взаимодействуют с медью.
Медь интенсивно растворяется в азотной кислоте, медленнее – в хромовой, значительно слабее – в серной, и почти не реагирует с соляной кислотой. введение окислителей резко увеличивает скорость этих реакций. Органические кислоты и аммиак легко взаимодействуют с медью.
Часто применяется меднение посредством химического восстановления меди из ее растворов, особенно при покрытии диэлектриков. Толщина получающегося при этом слоя меди весьма мала, измеряется долями микрона и образовавшийся слой, вернее налет, металлической меди служит основой для последующего гальванического наращивания меди из кислых электролитов.
1. Этапы изготовления ПП
Процесс производства печатных плат прошло долгий путь от приклеивания медной фольги к диэлектрику и ручного лужения, до сложных автоматизированных химических и электрохимических процессов. Качество, ремонтопригодность, а также габаритные размеры готовой продукции во многом зависят от качества изготовления печатных плат.
Перечень технологических операций входящих в процесс производства печатных плат:
1) нарезка заготовок и образование базовых отверстий – в производстве нарезку материала выполняют методом штамповки с одновременной пробивкой базовых отверстий на технологическом поле;
2) химическая металлизация печатных плат заключается в последовательности химических реакций осаждения меди, используемой в качестве слоя, или подслоя при нанесении основного слоя токопроводящего рисунка гальваническим способом;
3) гальваническая металлизация применяются для увеличения тонкого слоя химической меди с целью последующего нанесения на поверхность проводящего слоя;
4) нанесение рисунка схемы на печатные платы или их слои необходимо для получения защитной маски требуемой конфигурации при осуществлении процессов и травления проводящего слоя;
5) травление меди с пробельных мест – формирование проводящего рисунка схемы;
6) удаление защитной маски после операций травлений;
7) оплавление металлорезиста – гальванически нанесенный металлорезист олово-свинец;
8) нанесение защитного покрытия на плату наносится в специальной распылительной камеры, в качестве защитного материала может использоваться лак, флюсы ацитоноканифольные или спиртоканифольные.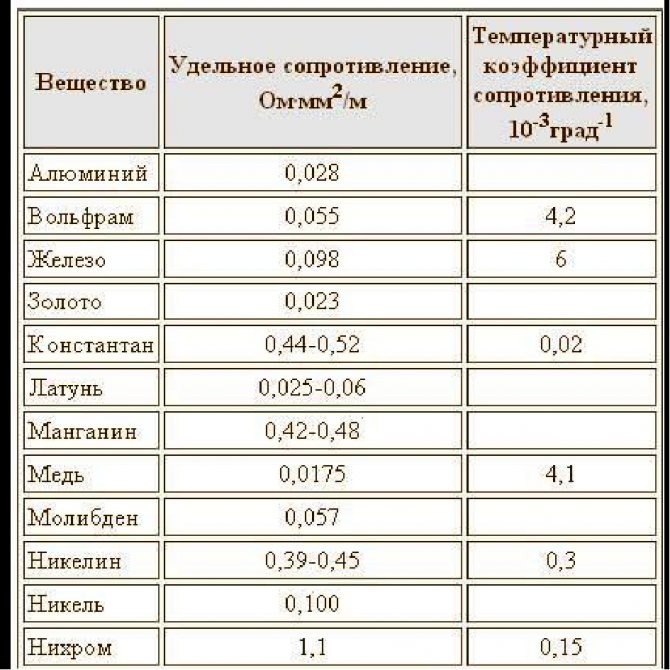
Одной из основных стадий процесса производства ПП является создание проводников электрического тока на поверхности диэлектрического материала путем нанесения гальванического покрытия – меди.
Гальваническую металлизацию в производстве ПП применяют:
- для образования проводящего рисунка схемы с толщиной меди в отверстиях не менее 25 мкм;
- для предварительного увеличения тонкого слоя химической меди до толщины 5‒8 мкм с целью последующего формирования рисунка схемы; для нанесения металлического резиста, например олово-свинец, толщиной 10‒20 мкм либо специальных покрытий золотом, серебром толщиной 2‒5 мкм.
2. Гальваническое осаждение меди
Для гальванического осаждения меди разработано большое количество электролитов, которые, обычно, разделяют на две группы: кислые и щелочные.
2.1. Кислые электролиты
К кислым электролитам относятся сульфатные и фторборатные электролиты. Их основные достоинства – простота состава и устойчивость в эксплуатации, но они обладают низкой рассеивающей способностью. Также из них невозможно непосредственно меднить сталь из-за выпадения контактной меди, а, следовательно, плохое сцепление со сталью слоя меди. Вследствие этого меднение осуществляется после предварительного осаждения медного слоя (3-4 мкм) из щелочных электролитов или после осаждения никелевого слоя (3-5 мкм).
Также из них невозможно непосредственно меднить сталь из-за выпадения контактной меди, а, следовательно, плохое сцепление со сталью слоя меди. Вследствие этого меднение осуществляется после предварительного осаждения медного слоя (3-4 мкм) из щелочных электролитов или после осаждения никелевого слоя (3-5 мкм).
Из кислых электролитов наиболее распространен сульфатный электролит. Основными компонентами сульфатных электролитов являются сульфат меди и серная кислота.
Предполагается, что на катоде разряд двухвалентных ионов меди протекает в две стадии:
Cu2+ → Cu+ → Cu0.
Причем, замедленной стадией является:
Cu2+ + e- → Cu+.
Доля каждой стадии зависит от состава электролита и режима электролиза: плотности тока, температуры перемешивания. Электропроводность нейтральных растворов сульфата меди невелика, поэтому в них добавляют серную кислоту, которая значительно повышает электропроводность растворов температуры перемешивания.
Выход меди по току составляет практически 100 %, так как выделение водорода на катоде не происходит, поскольку потенциалы выделения меди имеют более положительные значения, чем потенциалы выделения водорода.
Повышение кислотности электролита способствует уменьшению растворимости сульфата меди, что приводит к снижению верхнего предела допустимой плотности тока. Для увеличения концентрации ионов меди в прикатодном слое применяют перемешивание. В этом случае кислотность электролитов можно увеличивать. Чем интенсивнее перемешивание, тем выше может быть содержание серной кислоты. Повышение температуры способствует увеличению растворимости сульфата меди: при 25 °С- 23,05 г CuSO4 на 100 г воды; при 100 °С – 73,6 г. Повышенная кислотность способствует получению более мелкокристаллических осадков.
Вблизи анодов наряду с ионами Cu2+ в растворе могут находиться в незначительном количестве ионы одновалентной меди, образующиеся в результате протекания реакции:
Cu + Cu2+ → 2Cu+.
При накоплении в растворе ионов Cu+ равновесие будет сдвигаться влево, и металлическая медь будет выпадать в виде осадка.
При недостаточной кислотности раствора сульфат одновалентной меди будет гидролизоваться с образованием Сu(ОН)2 или Сu2О
Cu2SO4 + H2O ↔ Cu2O + H2SO4.
В результате в электролите будут взвешенные частицы металлической меди и оксида меди, которые, включаясь в катодный осадок, делают его темным, шероховатым, а иногда – рыхлым.
Присутствие серной кислоты способствует протеканию реакций окисления одновалентной меди:
Cu2SO4 + H2SO4 + 1/2О2 → 2CuSO4 + Н2О;
Cu2O + 2H2SO4 + 1/2O2 → 2CuSO4 + 2H2O.
Таким образом, серная кислота прежде всего нужна для предупреждения накопления ионов Cu+ и гидролиза ее солей.
В сульфатные электролиты иногда вводят поверхностно-активные вещества. Эти вещества вводят для повышения катодной поляризации, что способствует получению более мелкозернистых плотных, иногда блестящих, осадков. Благоприятное действие этих добавок сказывается в том, что они предупреждают образование наростов на краях и выступающих частях деталей. Наилучшими добавками являются декстрин (не более 1 г/л).
Для получения блестящих медных покрытий предложено большое количество блескообразующих добавок, обеспечивающих зеркальный блеск покрытий, придающих им пластичность и снижающих внутренние напряжения.
При работе с электролитами для получения блестящих покрытий особое внимание следует уделять анодам. Используют аноды марки АМФ, не дающие шлама и содержащие 0,03‒0,06 % фосфора. В остальных случаях применяют аноды из чистой рафинированной меди (99,9 %), содержащей не более 0,1 % примесей.
Взвешенные частицы шлама обычно являются причиной грубого шероховатого осадка. Для предотвращения попадания шлама в электролит рекомендуется аноды помещать в чехлы из кислотостойкого материала и вести непрерывную фильтрацию электролита.
На качество получаемых блестящих покрытий большое влияние оказывает концентрация ионов Сl–.При пониженной концентрации снижается блеск покрытий и образуются прижоги на острых кромках деталей, при повышенном содержании образуются полосы на покрытиях.
Вредными примесями в медных сульфатных электролитах являются мышьяк, сурьма, некоторые органические вещества, образующие коллоидные растворы, анодный шлам.
Кроме сульфатных, используют фторборатные электролиты. Эти электролиты обладают высокой устойчивостью; получающиеся покрытия плотные и мелкокристаллические, рассеивающая способность электролитов примерно такая же, как у сульфатных. Большая растворимость фторбората меди позволяет применять повышенные плотности тока. Из этих электролитов осаждать медь непосредственно на стальные детали нельзя; необходим подслой никеля или меди из цианидных электролитов.
2.2. Щелочные электролиты
К щелочным электролитам относятся цианидные, пирофосфатные и этилендиаминовые электролиты. Основные достоинства: высокая рассеивающая способность, получение мелкокристаллических осадков, возможность непосредственно меднить стальные детали.
Основные достоинства: высокая рассеивающая способность, получение мелкокристаллических осадков, возможность непосредственно меднить стальные детали.
Довольно распространены цианидные электролиты. Условия осаждения меди из цианидных электролитов существенно отличаются от условий осаждения в кислых электролитах.
В цианидных электролитах медь находится в составе комплексных ионов. Степень диссоциации, а, следовательно, и активность ионов меди очень мала. Поэтому потенциал выделения меди в них примерно на 0,9‒1,2 В отрицательнее, чем в сульфатных растворах.
При малом количестве цианида аноды пассивируются. При недостаточном количестве свободного цианида, когда происходит пассивация анодов и на них разряжаются ионы ОН‒ с выделением кислорода, то не весь образующийся кислород выделяется в виде газа, а часть его расходуется на окисление цианида в цианит. Уменьшение содержания цианидов происходит также из-за взаимодействия их с углекислотой воздуха и образования карбонатов (NаCN→ Nа2CO3 ).
Содержание свободного цианида оказывает на катодный и анодный процессы противоположное влияние: для катодного процесса требуется минимальное содержание цианидов, для анодного – максимальное. При недостатке свободного KCN на анодах образуется зеленоватая пленка CuCN из-за того, что ионы меди не в состоянии перейти в комплексное соединение. Свободная поверхность анода уменьшается, плотность тока растет, и анодное растворение происходит с образованием ионов двухвалентной меди, которые в виде нерастворимого гидрата осаждаются на аноде. При этом аноды пассивируются и наблюдается интенсивное выделение кислорода.
Основными компонентами медных цианидных электролитов являются комплексный цианид меди и свободный цианид натрия. Степень диссоциации комплексных ионов очень мала и уменьшается с увеличением содержания CN‒ в комплексе. Этим, по-видимому, объясняется повышение катодной поляризации при увеличении содержания свободного цианида в электролите.
Содержание меди в электролите во время работы обычно уменьшается вследствие недостаточной растворимости анодов. Снижение концентрации ионов меди в электролитах приводит к образованию пористых осадков. Работая с малоконцентрированными медными электролитами, можно применять только пониженные плотности тока.
Снижение концентрации ионов меди в электролитах приводит к образованию пористых осадков. Работая с малоконцентрированными медными электролитами, можно применять только пониженные плотности тока.
Постоянным компонентом цианидных электролитов является карбонат. Он накапливается в результате окисления цианида кислородом воздуха, особенно при нагревании:
2NаCN + 2Н2О + 2NаOH + О2 = 2Nа2CO3 + 2NH3.
Присутствие карбонатов в небольших количествах полезно, поскольку при этом повышается электропроводность электролитов. Однако при их накоплении свыше 70 г/л, а в концентрированных – до 140 г/л аноды проявляют склонность к пассивированию, а покрытия получаются пористыми. Карбонаты можно удалять при помощи хлорида бария и вымораживанием, охлаждая электролит до ‒ 5 °С. Карбонаты натрия легче выпадают в осадок, чем калиевые. Сульфаты существенного влияния на процесс электролиза не оказывают.
Введение в электролит депассиваторов, в качестве которых применяют сегнетову соль KNаC4H4O6·4H2O и роданид калия KCNS, позволяет повысить рабочую плотность тока и устранить пассивацию анодов, но при этом следует одновременно повышать температуру электролита.
Высококонцентрированные по меди электролиты, содержащие депассиваторы, позволяют применять высокие плотности тока (до 10 А/дм2) при повышенной температуре и перемешивании. При этом возможно получить выход по току, близкий к 100 %.
Сульфиды, вводимые в электролит, играют роль восстановителя, предупреждая накопление в ванне ионов меди Cu2+[5, 6].
Для замены ядовитых цианидных электролитов применяют пирофосфатные и этилендиаминовые электролиты.
Из пирофосфатных электролитов получают медные осадки с мелкозернистой структурой. При нанесении тонких слоев осадки получаются гладкими, блестящими или полублестящими. Преимущества пирофосфатных электролитов перед кислыми заключаются в высокой рассеивающей способности и возможности непосредственно проводить меднение стальных деталей в разбавленном пирофосфатном электролите.
Основные компоненты пирофосфатных электролитов: CuSO4 или Сu2Р2О7 и К4Р2О7 или Nа4P2O7. В растворах в присутствии Nа4P2O7 образуется комплексная соль Nа6[Cu(P2O7)2]. При избытке свободного пирофосфата может образовываться Nа2[Cu(P2O7)2]. Константы нестойкости комплексов [Сu(Р2О7)2]6‒ и [Сu(Р2О7)2]2‒ соответственно равны 3·10‒3 и 2·10‒9.
В растворах в присутствии Nа4P2O7 образуется комплексная соль Nа6[Cu(P2O7)2]. При избытке свободного пирофосфата может образовываться Nа2[Cu(P2O7)2]. Константы нестойкости комплексов [Сu(Р2О7)2]6‒ и [Сu(Р2О7)2]2‒ соответственно равны 3·10‒3 и 2·10‒9.
В щелочных растворах при рН = 8 и достаточном избытке свободных ионов Р2О74‒ медь находится преимущественно в виде шестизарядных комплексных ионов [Сu(Р2О7)2]6‒.
В пирофосфатные электролиты вводят азотнокислый аммоний NH4NO3, который способствует повышению допустимой катодной и анодной плотностей тока и улучшает качество осадков. Из пирофосфатных электролитов можно получать блестящие осадки. В качестве блескообразующих добавок вводят Nа2SeO3 совместно с лимонной или триоксиглутаровой кислотой, 2-меркаптотиазол и другие вещества.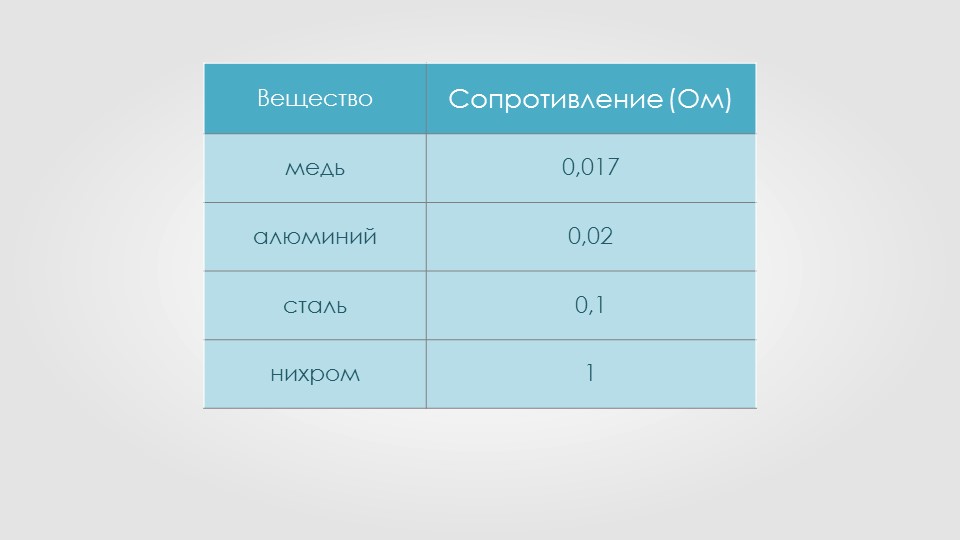
При повышенных плотностях тока может происходить пассивация анодов за счет образования на их поверхности труднорастворимой оксидной или солевой пленки. Введение в электролит NH4OH, Nа2HPO4·12H2O, NH4NO3, сегнетовой соли, лимонной кислоты и других добавок улучшает работу анодов и повышает допустимую анодную плотность тока [1, 2]. Катодный потенциал меди в пирофосфатных электролитах имеет более отрицательное значение, чем в кислых электролитах.
Большая катодная поляризация объясняется пассивированием поверхности катода вследствие адсорбции ионов Р2О74‒ или образования оксидных (Сu2О8) и труднорастворимых соединений (Сu2Р2О7) в виде фазовой пленки.
Предполагают, что выделение меди на катоде из пирофосфатных растворов происходит в результате восстановления двухзарядных комплексов:
CuP2O72- + 2e– → Cu + Р2О74-,
образующихся при диссоциации шестизарядных комплексов:
Cu(P2O7)26‒ → CuP2O72‒ + Р2О74‒.
Повышение температуры ускоряет выделение меди, что связано как с ускорением диффузии комплексных анионов к катоду, так и с облегчением их разряда.
Анодный выход по току в этих электролитах несколько выше катодного, поэтому при корректировке нет необходимости добавлять медные соли. Анодную плотность тока рекомендуется поддерживать в пределах 2‒4 А/дм2. При более низкой плотности тока растворение идет недостаточно быстро, при более высокой – на поверхности анодов образуется труднорастворимая оксидная пленка.
Для предотвращения пассивации анодов необходимо достаточное количество свободных анионов Р2О74‒ и достаточно высокое значение рН раствора. Повышение температуры способствует отводу продуктов реакции и, следовательно, уменьшению пассивации анодов. Для этой же цели в электролиты вводят депассиваторы, которые способствуют снижению активности ионов Cu2+ в прианодном пространстве.
При работе пирофосфатных ванн меднения рекомендуется проводить фильтрацию электролита: для полублестящих осадков – периодически или непрерывно, для блестящих – непрерывно.
Таблица 1 – Составы растворов электролитов и технологические режимы процесса гальванического медненияspan>
|
Тип |
Номер состава |
Состав электролита |
Режим обработки |
Дополнительные указания |
||
|
Компонент |
Коли-чество, г/дм3 |
Темпе-ратура, °С |
Плотность тока, А/дм2 |
|||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Кислые электролиты |
1 |
CuSO4∙5H2O H2SO4 |
150-250 50-70 |
18-25 |
1-3 |
При плотности тока более 2 А/дм2 обработку проводят барботажом сжатым воздухом |
|
Кислые электролиты |
2 |
CuSO4∙5H2O H2SO4 NаCl Блескообразователь |
180-220 45-65 0,05-0,15 4-6 |
20-30 |
0,8-9 |
Обработку проводят перемешиванием электролита сжатым воздухом и фильтрацией электролита; iа=0,4-5 А/дм2; аноды – медные с фосфором |
|
3 |
Cu(BF4) HBF4 H3BO3 |
200-225 5-20 20-35 |
15-30 |
2-6 |
||
|
Щелочные электролиты |
4 |
CuCN NаCN NаOH |
20-30 5-10 5-10 |
15-55 |
0,3-2 |
Допускается наличие углекислого натрия до 80 г/дм3 |
|
5 |
CuSO4∙5H2O K4P2O7 NH4OH 25%p-p H4P2O7 Аммоний лимонно-кислый |
75-100 300-375
2-15 1-10 15-25 |
50-75 |
0,5-5 |
||
|
6 |
CuSO4∙5H2O Этилендиамин (NH4)2SO4 |
180-250 90-125 60 |
20-40 |
0,5-3 |
||
Особенностью этилендиаминовых электролитов меднения является возможность непосредственного меднения стальных деталей. Детали в ванну загружают под током плотностью в 5 раз превышающей рабочую. Составы большинства электролитов меднения приведены в таблице.
Детали в ванну загружают под током плотностью в 5 раз превышающей рабочую. Составы большинства электролитов меднения приведены в таблице.
3. Подготовка поверхности перед гальваническим осаждением металлов.
Подготовка поверхности является неотъемлемой и весьма существенной операцией всего технологического процесса нанесения металлических покрытий. Основное требование ‒ прочность сцепления между основой и металлическим покрытием ‒ может быть удовлетворено только в том случае, если между ними нет посторонних загрязнений, чаще всего в виде жиров и окислов. Она включает: механическую обработку, обезжиривание моющими растворами, электрохимическую обработку и травление.
3.1. Подготовка металлической поверхности.
Механическая обработка детали выбирается с тем расчетом, что после нанесения покрытия класс чистоты поверхности снизится на 1‒2 единицы в зависимости от металла покрытия и его толщины. Особое внимание следует обратить на резьбовые соединения, которые могут потребовать дополнительной обработки после покрытия.
После тщательной промывки в горячей проточной воде детали отправляют в ванну электрохимического обезжиривания, где анодно (за счет подтравливания) или катодно (под током выделяющегося водорода) снимаются остатки загрязнений. Поверхность считается чистой, если после окунания вода стекает сплошной пленкой, т.е. при достижении полной смачиваемости поверхности.
Процесс травления зависит от материала деталей, конструкции и наносимого покрытия. Большие проблемы возникают при наличии окалины, возникающей в процессе механической обработки. Недопустимо обрабатывать сборочные узлы, паяные соединения, т.к. возможны подтравливание поверхности.
В зависимости от назначения покрытий, метода их нанесения и операций, предшествующих процессу нанесения покрытий, подготовку поверхности основного металла ведут различными способами. При горячем методе нанесения защитных покрытий подготовка поверхности сводится к обезжириванию и травлению. Если перед покрытием изделия подвергались отжигу, при котором жиры сгорают, то можно ограничиться одним травлением. Такая же подготовка поверхности необходима перед нанесением антикоррозионных (недекоративных) покрытий гальваническим путем, если изделия предварительно подвергались термической обработке.
Такая же подготовка поверхности необходима перед нанесением антикоррозионных (недекоративных) покрытий гальваническим путем, если изделия предварительно подвергались термической обработке.
Если перед гальваническим покрытием изделия подвергались обработке резанием или давлением в присутствии смазки, то поверхность их становится гидрофобной ‒ не смачивается водными растворами солей и кислот. В этих случаях подготовка поверхности начинается с растворения минеральных жиров в органических растворителях, после чего удаляют окислы.
Более сложная подготовка поверхности перед нанесением защитно-декоративных покрытий (медных, никелевых, хромовых, серебряных). В этом случае недостаточно удаления жиров и окислов. Необходима тщательная механическая обработка с применением тонких абразивов с целью получения максимально гладкой поверхности. Такая подготовка необходима главным образом потому, что в процессе нанесения защитно-декоративных покрытий дефекты поверхности не только не исчезают, но часто становятся более рельефными, так как плотность тока и толщина покрытий на макровыступах больше, чем в макроуглублениях.
3.2 Подготовка поверхности диэлектрика.
Механическая подготовка крупных и средних деталей, осуществляемая для получения микрошероховатости поверхности часто заключается в мокрой или сухой абразивной обдувке сжатым воздухом давлением 0,1‒0,6 Мпа или обработке абразивными кругами и лентами на шлифовально-полировальных станках. Мелкие детали массового производства галтуют с абразивом во вращающихся барабанах или колоколах, а также в виброустановках.
Удаление различных загрязнений, образующихся на поверхности диэлектриков в процессе механической или иной обработки, при хранении и транспортировании, удаляются в щелочных растворах или органических растворителях. Обработку проводят путем погружения деталей в раствор, в парах органических растворителей, струйным методом. Их выбор, а также выбор состава раствора и оборудования производится в зависимости от вида, степени загрязнения поверхности и природы диэлектрика. При этом подбирают такие составы и режимы обработки, при которых легко удаляются жировые загрязнения, а обрабатываемый материал не растворяется, не набухает и не растрескивается. Используемые для обезжиривания щелочные растворы в основном те же, что и для металлов.
Используемые для обезжиривания щелочные растворы в основном те же, что и для металлов.
Непосредственно перед травлением в некоторых случаях выполняют операцию предтравления, которая включает обработку поверхности диэлектрика органическими растворителями, их смесями или эмульсиями, растворами кислот, щелочей, солей. К предтравлению также относят термообработку, облучение, обработку ультразвуком, и другие виды воздействия. Кондиционирование снимает или разрыхляет поверхностный слой, способствуя улучшению травимости диэлектрика. Одновременно снижаются продолжительность и температура травления, удлиняется период эксплуатации раствора.
Травление представляет собой химический процесс, в результате которого изменяются структура и химические свойства поверхности диэлектрика. При этом ей придают требуемые шероховатость, гидрофильность и способность к реакции при выполнении последующих операций нанесения покрытия.
4. Рассеивающая способность.
Качество и свойства электрохимических покрытий определяются не только структурой, но и равномерностью распределения металла по толщине слоя на поверхности покрываемых изделий. На практике ток распределяется по поверхности электрода неравномерно, поэтому фактическая плотность тока и толщина покрытия на различных участках катода различны: на одних больше среднего значения, на других меньше. Это может отрицательно сказаться на свойствах покрытия, поскольку на отдельных участках его толщина может быть меньше минимально допустимой.
На практике ток распределяется по поверхности электрода неравномерно, поэтому фактическая плотность тока и толщина покрытия на различных участках катода различны: на одних больше среднего значения, на других меньше. Это может отрицательно сказаться на свойствах покрытия, поскольку на отдельных участках его толщина может быть меньше минимально допустимой.
Распределение тока и металла по поверхности катода зависит:
1) от геометрических факторов размера и формы электродов и ванны, расположения электродов относительно друг друга и стенок ванны;
2) от электрохимических факторов электропроводимости электролита, характера изменения катодной поляризации и выхода по току металла с изменением плотности тока.
Различают первичное и вторичное распределение тока.
Первичное зависит только от соотношения геометрических параметров электролитической ванны. Оно наблюдается при отсутствии зависимости катодной поляризации от плотности тока и одинаково для геометрически подобных систем любого масштаба.
Вторичное, или действительное, распределение тока отклоняется от первичного, как правило, в сторону большей равномерности.
Оно зависит от поляризуемости катода , удельной электропроводимости раствора х и геометрических размеров системы. Параметром, обобщающим действие геометрических и электрохимических факторов на распределение тока, является критерий электрохимического подобия.
В геометрически подобных системах, чем больше критерий электрохимического подобия, тем более равномерно распределение тока.
Способность электролита изменять первичное распределение тока называют рассеивающей способностью электролита. Обычно этот термин употребляют и для оценки способности электролита давать равномерные по толщине покрытия на изделиях сложного профиля. Поэтому принято различать соответственно рассеивающую способность по току (РСТ ) и рассеивающую способность по металлу (РСМ ).
Современные представления о механизме перераспределения тока в электролитах основываются на теории полей поляризации. При прохождении тока через электролитическую ванну в ней возникает электрическое поле. Обычно функцию распределения потенциала в электрическом поле называют просто потенциалом данного поля. При отсутствии зависимости поляризации от плотности тока в электролитической ванне реализуется первичное поле, потенциал которого обозначается Ut и определяется только соотношением геометрических параметров ванны.
При прохождении тока через электролитическую ванну в ней возникает электрическое поле. Обычно функцию распределения потенциала в электрическом поле называют просто потенциалом данного поля. При отсутствии зависимости поляризации от плотности тока в электролитической ванне реализуется первичное поле, потенциал которого обозначается Ut и определяется только соотношением геометрических параметров ванны.
Появление на электродах поляризации, зависящей от плотности тока, можно рассматривать как появление так называемого поля поляризации, потенциал которого обозначается Uo. На значение Uo влияют геометрические параметры электролитической ванны и электрохимические характеристики электролита: электропроводимость и поляризуемость. Это поле Uo , суммируясь с первичным полем, дает в результате реально существующее на практике вторичное поле, потенциал которого обозначается U 2 .
Если поляризуемость стремится к бесконечности, то поле поляризации называют предельным полем поляризации, потенциал его равен. Вторичное поле в этом случае называют предельным полем.
Вторичное поле в этом случае называют предельным полем.
Чтобы оценить рассеивающую способность электролитов, применяют ячейки различных конструкций, в которых экспериментально определяют распределение тока и металла и полученные с исследуемыми электролитами результаты сопоставляют. Иногда распределение тока и металла определяют расчетным путем.[14] По этим данным обычно приводят качественную характеристику рассеивающей способности; считают, что она выше у того электролита , у которого вторичное распределение тока или металла в данной ячейке более равномерное.
5. Выводы по литературному обзору
В производстве ПП создание проводников электрического тока на поверхности и в отверстиях диэлектрического материала осуществляется путем нанесения меди гальваническим способом.
Нанесение медного покрытия возможно в кислых и щелочных электролитах. К кислым электролитам относятся сульфатные и фторборатные электролиты. Их основные достоинства – простота состава и устойчивость в эксплуатации, но они обладают низкой рассеивающей способностью.
К щелочным электролитам относятся цианидные, пирофосфатные и этилендиаминовые электролиты. Основные достоинства: высокая рассеивающая способность, получение мелкокристаллических осадков, возможность непосредственно меднить стальные детали
Для практических целей в гальванике в основном используют сернокислые и пирофосфатные электролиты меднения.
Подготовка поверхности является неотъемлемой и весьма существенной операцией всего технологического процесса нанесения металлических покрытий. Основное требование ‒ прочность сцепления между основой и металлическим покрытием. Подготовка поверхности включает в себя механическую обработку, обезжиривание и травление. Критерием оценки качественной подготовки служит полная смачиваемость металлизируемой поверхности.
Качество и свойства электрохимических покрытий определяется структурой и равномерностью распределения металла по толщине слоя на поверхности покрываемых изделий. Способность электролита изменять первичное распределение тока называют рассеивающей способностью электролита.
Рассеивающая способность электролита (РС) — это способность электролита давать равномерные по толщине покрытия на деталях сложного профиля или способность электролита изменять первичное распределение тока.
Распределение тока и металла по поверхности катода зависит: от размера и формы электродов и ванны, расположения электродов относительно друг друга и стенок ванны; от электрохимических факторов электропроводимости электролита, характера изменения катодной поляризации и выхода по току металла с изменением плотности тока.
Для осуществления быстрого исследования и тестирования работоспособности различных электролитов, применяемых в гальваническом производстве, используется электрохимическая ячейка с угловым катодом – ячейка Хулла.
Конец статьи
Понравилась статья? Оцените статью. Всего 1 клик!
Нажмите на звезду
Средняя оценка:
5,00
Всего оценок: 3
Данная статья является интеллектуальной собственностью ООО “НПП Электрохимия”. Любое копирование информации возможно только с разрешения владельца сайта. Размещение активной индексируемой ссылки на https://zctc.ru обязательно.
Любое копирование информации возможно только с разрешения владельца сайта. Размещение активной индексируемой ссылки на https://zctc.ru обязательно.
Какова проводимость меди?
Обновлено 08 декабря 2018 г.
Автор J. Dianne Dotson
Металлическая медь лучше всего знакома вам по старым пенни, которые сделаны из меди и других металлов. Но медь играет важную роль во всем мире благодаря своим уникальным свойствам. Одним из таких свойств является его проводимость или способность проводить электричество. Высокая проводимость меди делает ее идеальной для электрических целей.
TL;DR (слишком длинный; не читал)
Медь — недрагоценный металл красно-золотистого цвета с высокой электропроводностью. На самом деле проводимость меди настолько высока, что она считается эталоном, по которому сравнивают другие неблагородные металлы и сплавы. На проводимость меди влияет добавление других металлов для изготовления сплавов.
Свойства меди
Медь представляет собой привлекательный металл красно-золотистого цвета. Он назван медью в честь древнеанглийского слова «coper», которое произошло от «Cyprium aes», латинского слова, обозначающего металл с Кипра. Атомный символ меди — «Cu», а ее атомный номер — 29.. Медь была первым металлом, который когда-либо обрабатывали люди. В конце концов, люди обнаружили, что если соединить медь с металлическим оловом, то можно получить новый вид металла под названием бронза. Это положило начало тому, что мы называем бронзовым веком, в котором цивилизация совершила скачок вперед с помощью металлической меди. Бронза использовалась в валюте и инструментах, которые помогли изменить общество.
Он назван медью в честь древнеанглийского слова «coper», которое произошло от «Cyprium aes», латинского слова, обозначающего металл с Кипра. Атомный символ меди — «Cu», а ее атомный номер — 29.. Медь была первым металлом, который когда-либо обрабатывали люди. В конце концов, люди обнаружили, что если соединить медь с металлическим оловом, то можно получить новый вид металла под названием бронза. Это положило начало тому, что мы называем бронзовым веком, в котором цивилизация совершила скачок вперед с помощью металлической меди. Бронза использовалась в валюте и инструментах, которые помогли изменить общество.
Медь часто встречается вместе с серой. Важные источники меди включают халькопирит и борнит. Медь извлекают из добытой сульфидной руды плавлением, а затем очищают электролизом.
Полезным свойством меди является ее пластичность или способность растягиваться. Медь можно тянуть и скручивать, но она не сломается. Это делает его идеальным для использования в качестве проволоки. Медь является податливым металлом, а это означает, что ей можно легко придавать форму и манипулировать ею. Поэтому он несколько мягкий. Еще одним свойством меди является ее отличная способность проводить тепло. Медь не подвержена коррозии, как некоторые другие металлы, а также не окисляется и не ржавеет, как железо. Медь на самом деле устойчива ко многим органическим соединениям, и, пожалуй, самым ценным ее свойством является высокая проводимость.
Медь является податливым металлом, а это означает, что ей можно легко придавать форму и манипулировать ею. Поэтому он несколько мягкий. Еще одним свойством меди является ее отличная способность проводить тепло. Медь не подвержена коррозии, как некоторые другие металлы, а также не окисляется и не ржавеет, как железо. Медь на самом деле устойчива ко многим органическим соединениям, и, пожалуй, самым ценным ее свойством является высокая проводимость.
Медь — отличный металл для механической обработки и соединения, так как ее легко формовать и паять. Кроме того, отличным и ценным свойством меди является ее способность к переработке. Неважно, находится ли источник меди в шахте или из вторичного сырья. Его многие полезные свойства сохраняются независимо от его источника.
Сплавы представляют собой смеси металлов, такие как смесь меди и олова для получения бронзы, которая является более твердым металлом, чем медь. Металлические сплавы обладают некоторыми из тех же свойств, что и исходные металлы, но их поведение также может сильно отличаться. Например, смеси сплавов могут влиять на электропроводность металлов. Сочетание различных металлов с медью приводит к уникальным свойствам каждого сплава. Когда медь соединяется с серебром, полученный сплав обладает многими свойствами чистой меди. Но если медь соединить с фосфором, то полученный сплав ведет себя совсем иначе.
Например, смеси сплавов могут влиять на электропроводность металлов. Сочетание различных металлов с медью приводит к уникальным свойствам каждого сплава. Когда медь соединяется с серебром, полученный сплав обладает многими свойствами чистой меди. Но если медь соединить с фосфором, то полученный сплав ведет себя совсем иначе.
Различные медные сплавы используются по-разному. Довольно часто сплавы изготавливают либо для упрочнения меди, либо для повышения ее электропроводных качеств.
Проводимость меди
Проводимость металлов относится к способности металлов проводить электричество. Проводимость может измениться при добавлении других металлов, например, при изготовлении сплавов. Металл с наибольшей проводимостью – драгоценный металл серебро. Стоимость серебра делает его экономически нецелесообразным для широкомасштабного использования в электротехнике. Среди неблагородных металлов проводимость меди или Cu самая высокая. Это означает, что медь может проводить больший электрический ток, чем другие недрагоценные металлы. На самом деле проводимость других неблагородных металлов сравнивают с медью, потому что медь стала высшим стандартом.
На самом деле проводимость других неблагородных металлов сравнивают с медью, потому что медь стала высшим стандартом.
Стандарт электропроводности называется Международным стандартом на отожженную медь или IACS. Процент IACS вещества относится к его электропроводности, а процент IACS чистой меди считается 100%. Напротив, проводимость алюминия составляет 61 процент IACS. На проводимость Cu влияет добавление различных металлов для образования сплавов. Медные сплавы с содержанием меди более 99,3% называются «медью». Некоторые сплавы содержат очень высокий процент меди, и они называются «сплавами с высоким содержанием меди». В то время как процентное содержание меди влияет на проводимость Cu, наиболее сильно на нее влияет то, с какими материалами она сочетается. Компромисс обычно происходит, когда медные сплавы делают более прочными. Как правило, эти сплавы имеют более низкую проводимость.
Cu-ETP (Electronic Touch Pitch) имеет 100% IACS и является обозначением типа меди, используемой в проводах, кабелях и шинах. Литая медь, или Cu-C, на 98 процентов состоит из IACS, поэтому она также обладает высокой проводимостью. Когда для получения сплавов с медью добавляют олово, магний, хром, железо или цирконий, прочность металла повышается, но его проводимость падает. Например, медь-олово или CuSnO.15 имеет проводимость Cu до 64 процентов по шкале IACS. В зависимости от функции сплава проводимость меди может значительно снизиться. Все еще существуют сплавы, которые сочетают в себе хорошую обрабатываемость и высокую проводимость. Примеры его включают медно-теллуровые (CuTep) и медно-серные (CuSP) сплавы. Их электропроводность колеблется от 64 до 98 процентов МАКО. Эти сплавы оказались весьма полезными для крепления полупроводников и наконечников для контактной сварки. Иногда материалы на основе меди требуют высокой твердости и прочности при умеренной проводимости Cu; примером является смесь меди, никеля и кремния, которая дает проводимость Cu от 45 до 60 процентов IACS. На конце шкалы с низкой электропроводностью латуни представляют собой медные сплавы, которые отлично подходят для литья.
Литая медь, или Cu-C, на 98 процентов состоит из IACS, поэтому она также обладает высокой проводимостью. Когда для получения сплавов с медью добавляют олово, магний, хром, железо или цирконий, прочность металла повышается, но его проводимость падает. Например, медь-олово или CuSnO.15 имеет проводимость Cu до 64 процентов по шкале IACS. В зависимости от функции сплава проводимость меди может значительно снизиться. Все еще существуют сплавы, которые сочетают в себе хорошую обрабатываемость и высокую проводимость. Примеры его включают медно-теллуровые (CuTep) и медно-серные (CuSP) сплавы. Их электропроводность колеблется от 64 до 98 процентов МАКО. Эти сплавы оказались весьма полезными для крепления полупроводников и наконечников для контактной сварки. Иногда материалы на основе меди требуют высокой твердости и прочности при умеренной проводимости Cu; примером является смесь меди, никеля и кремния, которая дает проводимость Cu от 45 до 60 процентов IACS. На конце шкалы с низкой электропроводностью латуни представляют собой медные сплавы, которые отлично подходят для литья. Их процент IACS колеблется около 20. Одним из примеров этих сплавов с низкой медной проводимостью является медно-цинковый. Иногда сбалансированный сплав обеспечивает проводимость Cu от низкой до умеренной, что полезно для электрических нужд. В эту категорию попадают медно-цинковые латуни, и их проводимость колеблется от 28 до 56 процентов IACS. Невероятная универсальность меди и ее способность образовывать полезные сплавы с таким количеством различных металлов.
Их процент IACS колеблется около 20. Одним из примеров этих сплавов с низкой медной проводимостью является медно-цинковый. Иногда сбалансированный сплав обеспечивает проводимость Cu от низкой до умеренной, что полезно для электрических нужд. В эту категорию попадают медно-цинковые латуни, и их проводимость колеблется от 28 до 56 процентов IACS. Невероятная универсальность меди и ее способность образовывать полезные сплавы с таким количеством различных металлов.
Поскольку проводимость меди очень высока, ее способность передавать тепло также довольно высока. Изготовление медных сплавов с высокой электропроводностью требует изготовления сплавов, устойчивых к перегреву при пропускании через них электрического тока. Это имеет решающее значение для передачи энергии, так как более высокая температура влияет на сопротивление.
Использование меди
Медь используется по-разному, как в физическом, так и в биологическом отношении. Он также используется в сельском хозяйстве в качестве яда.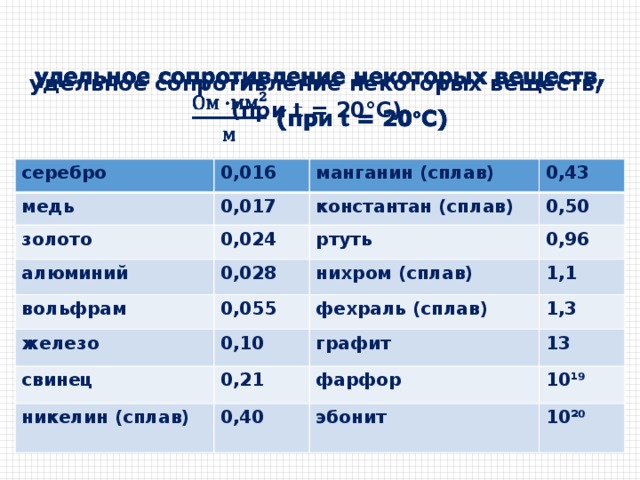 Растворы меди обычно используются как часть химических тестов. В организме медь играет роль эссенциального элемента, необходимого для передачи энергии в клетках. Некоторые ракообразные даже используют медь вместо железа в качестве основного переносчика кислорода.
Растворы меди обычно используются как часть химических тестов. В организме медь играет роль эссенциального элемента, необходимого для передачи энергии в клетках. Некоторые ракообразные даже используют медь вместо железа в качестве основного переносчика кислорода.
Медь, конечно же, используется для изготовления монет; старые пенни являются одним из примеров. На самом деле, большинство монет содержат хотя бы немного меди.
Медь в основном используется для передачи и доставки электроэнергии ко всем повседневным вещам, которыми вы пользуетесь. Медь широко используется в электропроводке, строительстве, машиностроении, телекоммуникациях, передаче электроэнергии, транспорте и других промышленных целях. Его можно использовать для кабелей, трансформаторов и соединительных деталей. Медь также используется в компьютерах и микросхемах.
По мере роста рынка экологически чистой энергии растет и спрос на медь. Медь чрезвычайно полезна во многих областях, а также может быть переработана снова и снова. Поэтому он является ключевым компонентом систем возобновляемой энергии. Фактически, солнечная, ветровая и электротранспортная промышленность полагаются на медь для подключения к энергосистеме. Электромобилям требуется гораздо больше меди, чем автомобилям, работающим на газу. Высокая проводимость меди делает ее очень эффективной. Кажется уместным, что самый старый металл, используемый людьми, будет продолжать приносить пользу и в будущем.
Поэтому он является ключевым компонентом систем возобновляемой энергии. Фактически, солнечная, ветровая и электротранспортная промышленность полагаются на медь для подключения к энергосистеме. Электромобилям требуется гораздо больше меди, чем автомобилям, работающим на газу. Высокая проводимость меди делает ее очень эффективной. Кажется уместным, что самый старый металл, используемый людьми, будет продолжать приносить пользу и в будущем.
Факторы, влияющие на электропроводность меди: влияние примесей
. Одним из свойств меди, которое во многом обеспечило ей ее нынешнее выдающееся место среди полезных металлов, является ее электропроводность — свойство, ставшее теперь главным критерием ценности товарного продукта. Во исполнение этого типично американского принципа, что «лучшее не бывает слишком хорошим», обычно требуется металл с самой высокой электропроводностью, даже когда такая исключительная чистота не дает никаких преимуществ; например, при изготовлении латуни и других сплавов. Средний литейщик из латуни нервничает, если его медь не настолько чиста, что ее проводимость равна 99 или 100 процентов, в то время как характер используемого цинка обычно упускается из виду при беспокойстве.
Средний литейщик из латуни нервничает, если его медь не настолько чиста, что ее проводимость равна 99 или 100 процентов, в то время как характер используемого цинка обычно упускается из виду при беспокойстве.
Электролитическое рафинирование позволяет производить медь очень высокой степени чистоты, при этом содержание металлических примесей составляет в среднем лишь несколько тысячных долей процента; кислород, обычно присутствующий в форме закиси меди, доводя общее количество примерно до одной десятой процента. Однако опубликованные данные о взаимосвязи между химической чистотой и электропроводностью очень скудны, почти все работы, которые были выполнены, касались сплавов, содержащих значительные количества посторонних элементов. В этой статье я собрал воедино результаты экспериментов, длившихся несколько лет, которые проводились с идеей определения количества различных элементов, снижающих электропроводность на 3 или 4 %. меди, а не сплавов.
Существует множество мер предосторожности, необходимых для сохранения одинаковых условий в различных экспериментах, поскольку расплавленная медь химически очень чувствительна к окружающей среде, а количество многих веществ, необходимых для снижения ее проводимости на несколько процентов, чрезвычайно незначительно. Процедура, принятая после длительных экспериментов, была следующей:
Процедура, принятая после длительных экспериментов, была следующей:
Используемая медь была в форме отожженной проволоки № 12 B. & S., спрессованной вместе и помещенной в круглый тигель Баттерси, размер H, 500 г. составляющая заряд. Примесь добавляли одним из трех способов, в зависимости от ее температуры плавления: 1. Если высокая, то сбрасывалась навеской прямо на дно тигля. 2. Если медная проволока была сравнительно низкой, часть медной проволоки сворачивали в фольгу, а примеси заключали в нее, и все это помещали на дно тигля; и 3. Если содержание очень низкое (например, фосфора), его, как и прежде, заворачивали в фольгу, но подсовывали под поверхность расплавленной меди непосредственно перед заливкой образцов. После того, как проволока была утрамбована в тигле, сверху был помещен слой битого древесного угля толщиной около дюйма, который полностью заполнил тигель. На тигель надевали крышку, которую затем подвергали сильному дутью в газовой печи. Образец заливали 25 мин. после включения дутья, которого как раз хватило, чтобы полностью расплавить шихту, не перегревая ее, и заметно не изменить «шаг» меди. Не было никаких проблем с получением элементов, температура плавления которых намного ниже их температуры плавления при этой температуре, для растворения в расплавленной меди. Отливки производились в нагретой чугунной форме в виде слегка сужающихся цилиндров со средним диаметром 0,5 дюйма и длиной 7 дюймов. Эти отливки были обжаты в горячем состоянии на наковальне до диаметра 3/8 дюйма, а затем вытянуты в холодном состоянии на проволоку № 12 B. & S. Затем, чтобы устранить последствия волочения, провода подвергали электрическому отжигу, заставляя их нести ток в 110 ампер. Электрический метод отжига — очень простой способ точного воспроизведения результатов, при этом температура отжига оказывает заметное влияние на проводимость. Провода были измерены на проводимость, а затем проанализированы на наличие меди и посторонних элементов. Сумма меди плюс примесь была общей проверкой анализа и «смолы».
Не было никаких проблем с получением элементов, температура плавления которых намного ниже их температуры плавления при этой температуре, для растворения в расплавленной меди. Отливки производились в нагретой чугунной форме в виде слегка сужающихся цилиндров со средним диаметром 0,5 дюйма и длиной 7 дюймов. Эти отливки были обжаты в горячем состоянии на наковальне до диаметра 3/8 дюйма, а затем вытянуты в холодном состоянии на проволоку № 12 B. & S. Затем, чтобы устранить последствия волочения, провода подвергали электрическому отжигу, заставляя их нести ток в 110 ампер. Электрический метод отжига — очень простой способ точного воспроизведения результатов, при этом температура отжига оказывает заметное влияние на проводимость. Провода были измерены на проводимость, а затем проанализированы на наличие меди и посторонних элементов. Сумма меди плюс примесь была общей проверкой анализа и «смолы».
Таблица I. дает общую сводку данных, элементы расположены в алфавитном порядке. Данные также представлены графически на рис. 1-16. Легирующие элементы были получены в максимально чистом виде, и не предполагается, что на результаты сильно влияют примеси в них. Это были: пробное серебро 1000 пробы; золото в виде гранул из анализов слитков, не содержащих примесей, но незначительное количество серебра; тест-лид; электролитическое железо без углерода; и сера в виде сульфида меди. Остальные элементы были химически чистыми (CP), доступными на рынке.
1-16. Легирующие элементы были получены в максимально чистом виде, и не предполагается, что на результаты сильно влияют примеси в них. Это были: пробное серебро 1000 пробы; золото в виде гранул из анализов слитков, не содержащих примесей, но незначительное количество серебра; тест-лид; электролитическое железо без углерода; и сера в виде сульфида меди. Остальные элементы были химически чистыми (CP), доступными на рынке.
При рассмотрении результатов естественно сгруппировать элементы по порядку в периодической системе. Это сделано в Таблице II. Столбец, озаглавленный «коэффициент», дает отношение снижения электропроводности к количеству присутствующей примеси. При получении этого соотношения касательные к кривым на рис. от 1 до 16, так что отношения строго верны только в случае бесконечно малого понижения. Видно, что этот фактор имеет общее отношение к периодическому расположению, уменьшаясь с увеличением атомного веса внутри любой группы, хотя очевидной связи между одной группой и другой нет. Этот фактор полезен при анализе меди, которая показывает низкую проводимость, как средство определения вероятной причины неисправности. Данные не дают даже приблизительной константы молекулярного понижения проводимости, т. е.
Этот фактор полезен при анализе меди, которая показывает низкую проводимость, как средство определения вероятной причины неисправности. Данные не дают даже приблизительной константы молекулярного понижения проводимости, т. е.
— это «коэффициент», умноженный на атомный вес — даже в рамках отдельных периодических групп.
Форма кривой состав-проводимость бинарного сплава может быть одной из четырех различных типов.
- Когда компоненты взаимно растворимы во всех пропорциях
ций. График состав-проводимость для такого случая дает плавную кривую на всем протяжении.
2. Когда составляющие взаимно нерастворимы в любых пропорциях, и в этом случае кривая проводимости становится прямой линией, так называемый сплав представляет собой не что иное, как механическую смесь.
3. Когда взаимная растворимость ограничена, на каждом конце кривой имеется растворимый ряд, а в середине – эвтектоносный ряд. Поскольку двух веществ, абсолютно нерастворимых друг в друге, вероятно, не существует, случай 2 не может быть жестко применен, такие вещества образуют крайнюю область применения случая 3.
Поскольку двух веществ, абсолютно нерастворимых друг в друге, вероятно, не существует, случай 2 не может быть жестко применен, такие вещества образуют крайнюю область применения случая 3.
4. Наконец, бывают случаи, когда образуются определенные химические соединения, которые могут давать кривую с растворимым рядом на одном конце и полностью эвтектическим рядом на другом.
Результаты, приведенные в этой статье, относятся исключительно к первой очень короткой части кривой проводимости, и поэтому следует ожидать, что в каждом случае будет проявляться некоторая кривизна. Однако некоторые из используемых элементов настолько почти нерастворимы в меди, что кривая мало отличается от прямой линии, соединяющей проводимости двух чистых веществ в смеси.
Полезные сплавы меди включают смеси с цинком, оловом, алюминием, кремнием и фосфором. Цинк и олово добавляются в относительно больших количествах для образования латуни и бронзы. Алюминий, кремний и фосфор добавляются в сравнительно небольших количествах, и их способность раскислять медь, подвергшуюся ненужному воздействию воздуха при плавке, вероятно, проявляется гораздо чаще при изготовлении отливок, чем это может себе представить литейщик. При надлежащих условиях вполне возможно изготавливать медные отливки идеальной прочности и проводимости без использования флюсов. Но, взглянув на таблицу множителей, видно, что с электрической точки зрения нельзя было подобрать худших элементов, чем упомянутые выше. С другой стороны, элементы, мало влияющие на электропроводность, — свинец, висмут и теллур — делают металл чрезвычайно хрупким. Этот эффект, по-видимому, связан с растворимостью последних элементов, которые практически нерастворимы в меди. Тогда мы имеем механическую смесь, в которой проводимость изменяется только в соответствии с пропорциями смеси, в то время как механические свойства самого постороннего элемента выдвигаются на первый план.
При надлежащих условиях вполне возможно изготавливать медные отливки идеальной прочности и проводимости без использования флюсов. Но, взглянув на таблицу множителей, видно, что с электрической точки зрения нельзя было подобрать худших элементов, чем упомянутые выше. С другой стороны, элементы, мало влияющие на электропроводность, — свинец, висмут и теллур — делают металл чрезвычайно хрупким. Этот эффект, по-видимому, связан с растворимостью последних элементов, которые практически нерастворимы в меди. Тогда мы имеем механическую смесь, в которой проводимость изменяется только в соответствии с пропорциями смеси, в то время как механические свойства самого постороннего элемента выдвигаются на первый план.
С другими классами веществ дело обстоит совсем по-другому, сплав представляет собой медь, внедренную в матрицу из сплава меди и примеси. Электропроводность этой матрицы, как правило, низка, и ее количество несоизмеримо с количеством добавленной примеси, и отсюда резкое снижение электропроводности в целом. Металлографическая работа с микроскопом подтверждает это; 0,1% висмута, например, вызывает лишь тонкую оболочку вокруг кристаллов меди, в то время как такое же количество мышьяка образует толстую стенку. Часто можно противодействовать пагубному механическому воздействию одной примеси, добавляя другую, как в случае, когда относительно безвредная примесь может растворять нерастворимую в других отношениях примесь, такую как свинец.
Металлографическая работа с микроскопом подтверждает это; 0,1% висмута, например, вызывает лишь тонкую оболочку вокруг кристаллов меди, в то время как такое же количество мышьяка образует толстую стенку. Часто можно противодействовать пагубному механическому воздействию одной примеси, добавляя другую, как в случае, когда относительно безвредная примесь может растворять нерастворимую в других отношениях примесь, такую как свинец.
Результаты, приведенные в Таблице I, показывают, насколько жестким требованием является обычная 97- или 98-процентная удельная проводимость, тем более что медь обычно связана с мышьяком; и если учесть, что средний электролитический рафинировочный завод ежедневно выполняет это требование с запасом в 2 или 3 %, часто используя аноды, содержащие 1 % или более мышьяка, становится понятным, что электролиз должен был стать рафинированием. даже медь никогда не содержала ни золота, ни серебра.
by David Рубрики Электрометаллургия, Плавка-плавка-рафинирование Теги 906Инновации: Знакомство с медью: информационные бюллетени
Вин Калькатт
| Свойство | Значение | Единицы | Значение | Единицы |
|---|---|---|---|---|
| Атомный номер | 29 | |||
| Атомный вес | 63,54 | |||
| Решетчатая структура: гранецентрированная кубическая | ||||
| Плотность | ||||
| Стандартное значение МЭК (1913) | 8,89 | г/см 3 | 0,321 | фунтов/дюйм 3 |
| Типичное значение при 20°C | 8,92 | г/см 3 | 0,322 | фунтов/дюйм 3 |
| при 1083°C (твердый) | 8,32 | г/см 3 | 0,300 | фунтов/дюйм 3 |
| в 1083 (жидкость) | 7,99 | г/см 3 | 0,288 | фунтов/дюйм 3 |
| Температура плавления | 1083 | °С | 1981 | °F |
| Точка кипения | 2595 | °С | 4703 | °F |
| Коэффициент линейного теплового расширения при: | ||||
| -253°C, -423°F | 0,3 х 10 -6 | °С | 0,17 х 10 -6 | °F |
| -183°C, -297°F | 9,5 х 10 -6 | °С | 5,28 х 10 -6 | °F |
| от -191°C до 16°C, от -312 до 61°F | 14,1 x 10 -6 | °С | 7,83 х 10 | °F |
| от 25°C до 100°C, 77-212°F | 16,8 x 10 -6 | °С | 9,33 x 10 -6 | °F |
| от 20°C до 200°C, 68-392 °F | 17,3 х 10-6 | °С | 9,61 х 10 -6 | °F |
| от 20°C до 300°C, 68-572 °F | 17,7 x 10 -6 | °С | 9,83 x 10 -6 | °F |
| Удельная теплоемкость (теплоемкость) при: | ||||
-253°C. -425°F -425°F | 0,013 | Дж/г°С | 0,0031 | БТЕ/фунт°F |
| -150°C, -238°F | 0,282 | Дж/г°С | 0,0674 | БТЕ/фунт°F |
| -50°C, -58°F | 0,361 | Дж/г°С | 0,0862 | БТЕ/фунт°F |
| 20°С, 68°F | 0,386 | Дж/г°С | 0,0921 | БТЕ/фунт°F |
| 100°С, 212°F | 0,393 | Дж/г°С | 0,0939 | БТЕ/фунт°F |
| 200°С, 392°F | 0,403 | Дж/г°С | 0,0963 | БТЕ/фунт°F |
| Теплопроводность при: | ||||
| -253°C, -425 °F | 12,98 | Вт-см/см 2 ·°C | 750 | БТЕ/фут/фут 2 ч°F |
| -200°C, -328°F | 5,74 | Вт-см/см 2 ·°C | 330 | БТЕ/фут/фут 2 ч°F |
| -183°C, -297°F | 4,73 | Вт-см/см 2 ·°C | 270 | БТЕ/фут/фут 2 ч°F |
| -100°C, -148°F | 4,35 | Вт-см/см 2 ·°C | 252 | БТЕ/фут/фут 2 ч°F |
| 20°C, 68°F | 3,94 | Вт-см/см 2 ·°C | 227 | БТЕ/фут/фут 2 ч°F |
| 100°C, 212°F | 3,85 | Вт-см/см 2 ·°С | 223 | БТЕ/фут/фут 2 ч°F |
| 200°C, 392°F | 3,81 | Вт-см/см 2 ·°C | 220 | БТЕ/фут/фут 2 ч°F |
| 300°C, 572°F | 3,77 | Вт-см/см 2 ·°C | 217 | БТЕ/фут/фут 2 ч°F |
| Электропроводность (объемная) при: | ||||
| 20°C, 68°F (отожженный) | 58,0-58,9 | МС/м (мОммм 2 ) | 100,0-101,5 | % МАКО |
| 20°C, 68°F (полностью холодная обработка) | 56,3 | МС/м (мОм·мм 2 ) | 97,0 | % МАКО |
| Удельное электрическое сопротивление (объемное) при: | ||||
| 20°C, 68 °F (отожженный) | 0,017241-0,0170 | Ом·мм 2 /м | 10.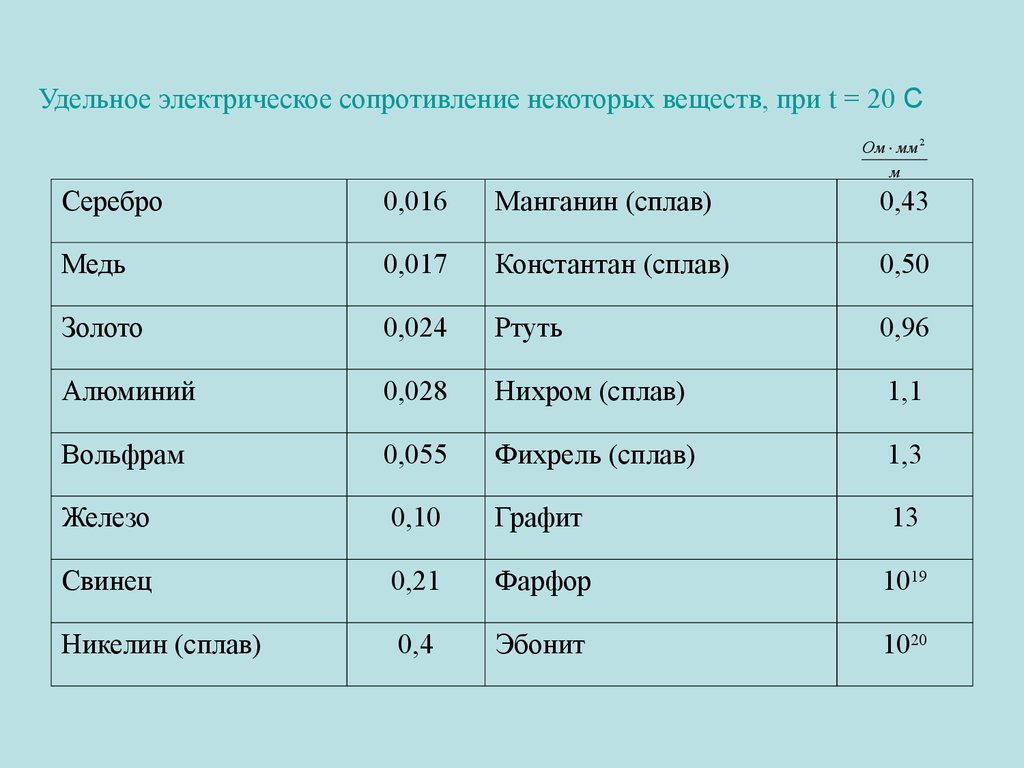 371-10.2 371-10.2 | Ом (окрмил/фут) |
| 20°C, 68°F (отожженный) | 1,7241-1,70 | мкОм·см | 0,6788-0,669 | мкОм-в |
| 20°C, 68°F (полностью холодная обработка) | 0,0178 | Ом·мм 2 /м | 10,7 | Ом (окрмил/фут) |
| 20°C, 68°F (полностью холодная обработка) | 1,78 | мкОм·см | 0,700 | мкОм-вход |
| Удельное электрическое сопротивление (масса) при 20 °C, 68 °F (отожженный) | ||||
| Обязательный максимум | 0,15328 | Ом·г/м 2 | 875,4 | Ом·фунт/миля 2 |
| Температурный коэффициент электрического сопротивления (a) при 20°C °F: Отожженная медь из 100% IACS (применимо от от -100°C до 200°C, от 212°F до 392°F) | 0,00393 | °С | 0,00218 | °F |
| Полностью холоднодеформированная медь с содержанием 97% IACS (применимо от 0°C до 100°C, 68-212°F) | 0,00381 | °С | 0,00238 | °F |
| Модуль упругости (растяжение) при 20°C:, 68 °F | ||||
| Отожженный | 118 000 | МПа | 17 х 103 | КСи |
| Холодная обработка | 118 000–132 000 | МПа | 17-19 х 10 3 | КСи |
| Модуль жесткости (кручение) при 20°C, 68°F | ||||
| Отожженный | 44 000 | МПа | 6,4 x 10 3 | КСи |
| Холодная обработка | 44 000–49 000 | МПа | 6,4-7 х 10 3 | КСи |
| Скрытая теплота плавления | 205 | Дж/г | ||
| Электрохимический эквивалент для: | ||||
| Cu ++ | 0,329 | Мг/Кл | ||
| Медь + | 0,659 | Мг/Кл | ||
| Нормальный электродный потенциал (водородный электрод) для: | ||||
| Cu ++ | -0,344 | В | ||
| Медь + | -0,470 | В |
| Свойство | Единицы | Медь (высокая проводимость) | Алюминий (1350) |
|---|---|---|---|
| Электропроводность (отожженный) | %IACS | 101 | 61 |
| Удельное электрическое сопротивление (отожженный) | мкОм-см | 1,72 | 2,83 |
| Теплопроводность при 20°C | Вт/м·К | 397 | 230 |
| Коэффициент расширения | °С °F | 17 x 10 -6 9,4 x 10 -6 | 23 x 10 -6 12,8 x 10 -6 |
| Прочность на растяжение (отожженный) | KSi МПа | 29,0-36,2 200-250 | 7,2-8,7 50-60 |
| Прочность на растяжение (полутвердый) | KSi МПа | 37,7-43,5 260-300 | 12,3-14,5 85-100 |
| предел текучести 0,2 % (отожженный) | KSi МПа | 7,25-7,98 50-55 | 2,9-4,3 20-30 |
| 0,2% предел текучести (полутвердый) | KSi МПа | 24,6-29,0 170-200 | 8,7–9,4 60–65 |
| Модуль упругости | KSi МПа | 16,8-18,8 116-130 | 10,1 70 |
| Усталостная прочность (отожженный) | KSi МПа | 9,0 62 | 5,07 35 |
| Усталостная прочность (полутвердый) | KSi МПа | 16,9 117 | 7,25 50 |
| Удельная теплоемкость | БТЕ/фунт 0 F Дж/кг·K | 0,092 385 | 0,215 900 |
| Плотность | г/см 3 фунт/дюйм 3 | 8,91 0,322 | 2,70 0,0975 |
| Точка плавления | °С °F | 1083 1981 | 660 1220 |
Примечание : Указанные значения являются типичными для электролитической меди с высокой проводимостью (ETP). Значения для других марок могут отличаться от указанных (см. «Медь с высокой проводимостью — Технические данные». Полный и доступный для поиска список физических и механических свойств кованой и литой меди и медных сплавов можно найти в разделе «Свойства кованой и литой меди»). Поиск сплавов) Значения для других марок могут отличаться от указанных (см. «Медь с высокой проводимостью — Технические данные». Полный и доступный для поиска список физических и механических свойств кованой и литой меди и медных сплавов можно найти в разделе «Свойства кованой и литой меди»). Поиск сплавов) | |||
- Знакомство с медью: применение
- Знакомство с медью: типы меди
- Введение в медь: добыча и добыча
- Знакомство с медью: информационные бюллетени
- Phelps Dodge Morenci перевела все производство меди на добычу для выщелачивания
- Как гидрометаллургия и процесс SX/EW сделали медь «зеленым» металлом
- Введение в медь: горячие ссылки и дополнительная литература





 В качестве катодов используют тонкие листы чистой меди, на которые во время электролиза осаждается чистая медь. На аноде происходит растворение меди. Ионы меди передвигаются к катоду, принимают от катода электроны и переходят в атомы: Cu+2+2e=>Cu. Чистая медь оседает на катоде.
В качестве катодов используют тонкие листы чистой меди, на которые во время электролиза осаждается чистая медь. На аноде происходит растворение меди. Ионы меди передвигаются к катоду, принимают от катода электроны и переходят в атомы: Cu+2+2e=>Cu. Чистая медь оседает на катоде. 5-2%, их подвергают обогащению, т.е. отделяют соединения меди от пустой породы, применяя флотационный метод. Для этого руду размалывают до тончайшего порошка и смешивают его с водой, добавив в неё предварительно флоторагенты – сложные органические вещества. Они покрывают мельчайшие крупинки соединений меди и сообщают им несмачиваемость. В воду добавляют ещё вещества, создающие пену. Затем через взвесь пропускают сильный поток воздуха. Поскольку частички (крупинки соединений меди) водой не смачиваются, они прилипают к пузырькам воздуха и всплывают наверх. Всё это происходит во флотационных аппаратах. Пену, которая содержит крупинки соединений меди, собирают, отфильтровывают, отжимают от воды и высушивают. Так получают концентрат, из которого выделяется медь. В зависимости от состава руды существует несколько методов её переработки.
5-2%, их подвергают обогащению, т.е. отделяют соединения меди от пустой породы, применяя флотационный метод. Для этого руду размалывают до тончайшего порошка и смешивают его с водой, добавив в неё предварительно флоторагенты – сложные органические вещества. Они покрывают мельчайшие крупинки соединений меди и сообщают им несмачиваемость. В воду добавляют ещё вещества, создающие пену. Затем через взвесь пропускают сильный поток воздуха. Поскольку частички (крупинки соединений меди) водой не смачиваются, они прилипают к пузырькам воздуха и всплывают наверх. Всё это происходит во флотационных аппаратах. Пену, которая содержит крупинки соединений меди, собирают, отфильтровывают, отжимают от воды и высушивают. Так получают концентрат, из которого выделяется медь. В зависимости от состава руды существует несколько методов её переработки. В последнее время начали применять обжиг в кипящем слое. Продукты обжига затем переплавляют совместно с флюсами в отражательной печи. При этом протекает множество химических процессов, например
В последнее время начали применять обжиг в кипящем слое. Продукты обжига затем переплавляют совместно с флюсами в отражательной печи. При этом протекает множество химических процессов, например При последующей переплавке на поду отражательной печи содержание меди может быть повышено до 99,7%. Дальнейшая очистка меди проводится электролизом.
При последующей переплавке на поду отражательной печи содержание меди может быть повышено до 99,7%. Дальнейшая очистка меди проводится электролизом.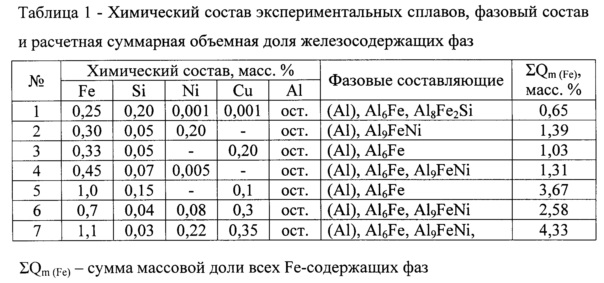 Выделение металлической меди из раствора проводят электролизом.
Выделение металлической меди из раствора проводят электролизом.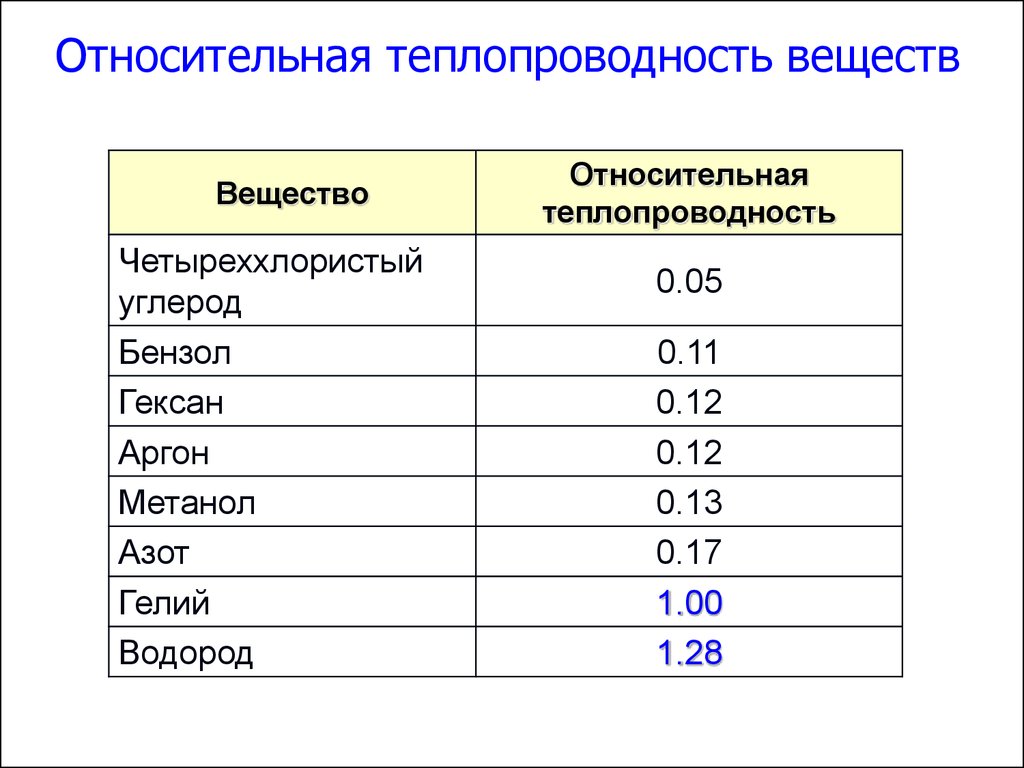
 Катодприменяют обычно из чистой электролитной меди. Электролит содержит 40–60 г/л меди, 10–20 г/л H2SО4.
Катодприменяют обычно из чистой электролитной меди. Электролит содержит 40–60 г/л меди, 10–20 г/л H2SО4.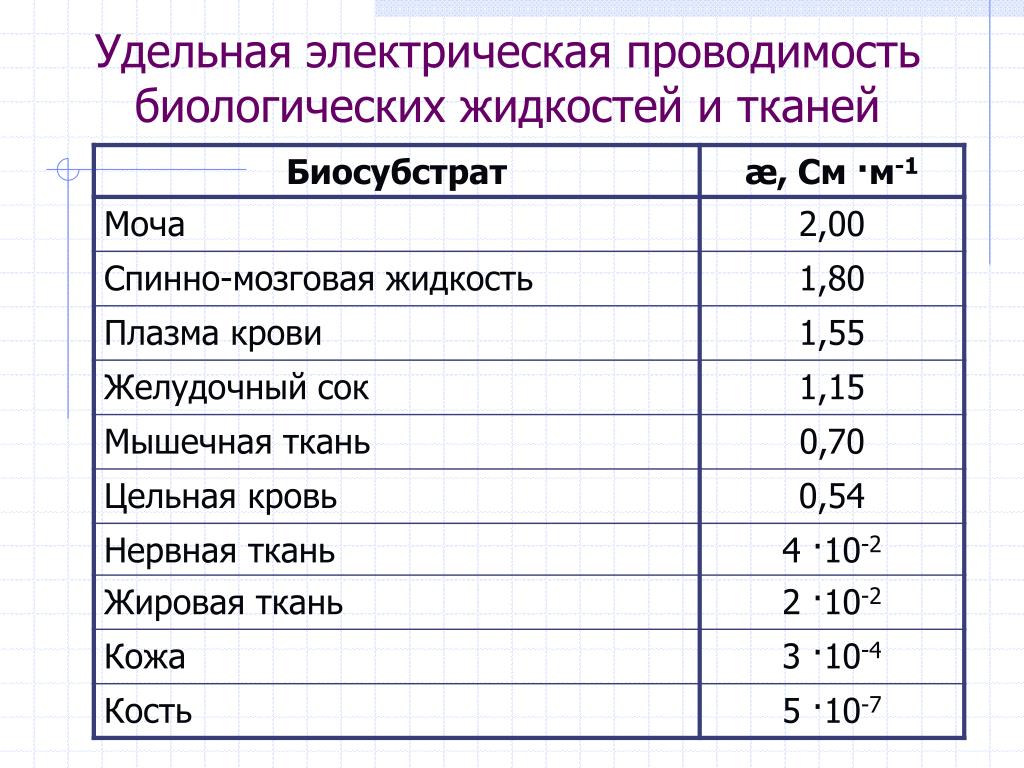 Электропроводность меди в твердом состоянии зависит в первую очередь от чистоты металла. Примеси и легирующие элементы уменьшают электропроводность меди и повышают ее удельное электросопротивление.
Электропроводность меди в твердом состоянии зависит в первую очередь от чистоты металла. Примеси и легирующие элементы уменьшают электропроводность меди и повышают ее удельное электросопротивление.
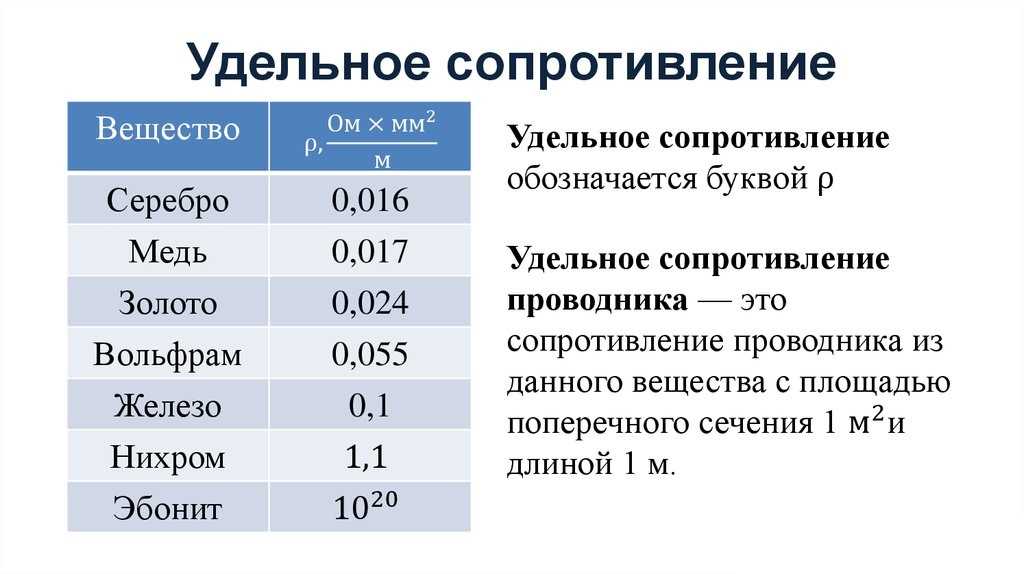 Физические и механические свойства электрических сортов меди и алюминия (тип 1350) по сравнению с
Физические и механические свойства электрических сортов меди и алюминия (тип 1350) по сравнению с