Как в химии обозначается медь: Медь, свойства, соединения, сплавы, производство, применение
alexxlab | 07.03.2023 | 0 | Разное
Химия и ток
В современной жизни химические источники тока окружают нас повсюду: это батарейки в фонариках, аккумуляторы в мобильных телефонах, водородные топливные элементы, которые уже используются в некоторых автомобилях. Бурное развитие электрохимических технологий может привести к тому, что уже в ближайшее время вместо машин на бензиновых двигателях нас будут окружать только электромобили, телефоны перестанут быстро разряжаться, а в каждом доме будет свой собственный электрогенератор на топливных элементах. Повышению эффективности электрохимических накопителей и генераторов электроэнергии посвящена одна из совместных программ Уральского федерального университета с Институтом высокотемпературной электрохимии УрО РАН, в партнерстве с которыми мы публикуем эту статью.
На сегодняшний день существует
множество разных типов батареек, среди
которых все сложнее ориентироваться.
Далеко не каждому очевидно, чем аккумулятор
отличается от суперконденсатора и почему
водородный топливный элемент можно
использовать, не опасаясь нанести
вред окружающей среде.
Химия как источник электричества
Сначала разберемся, почему химическую энергию вообще можно использовать для получения электричества. Все дело в том, что при окислительно-восстановительных реакциях происходит перенос электронов между двумя разными ионами. Если две половины химической реакции разнести в пространстве, чтобы окисление и восстановление проходили отдельно друг от друга, то можно сделать так, чтобы электрон, который отрывается от одного иона, не сразу попадал на второй, а сначала прошел по заранее заданному для него пути. Такую реакцию можно использовать как источник электрического тока.
Впервые эта концепция была реализована еще в XVIII
веке итальянским физиологом Луиджи
Гальвани. Действие традиционного
гальванического элемента основано на реакциях восстановления и окисления металлов с
разной активностью. Например, классической ячейкой является
гальванический элемент, в котором
происходит окисление цинка и восстановление
меди. Реакции восстановления и окисления
проходят, соответственно, на катоде
и аноде. А чтобы ионы меди и цинка
не попадали на «чужую территорию»,
где они могут прореагировать друг
с другом непосредственно, между
анодом и катодом обычно помещают
специальную мембрану. В результате
между электродами возникает разность
потенциалов. Если соединить электроды,
например, с лампочкой, то в получившейся
электрической цепи начинает течь ток
и лампочка загорается.
Например, классической ячейкой является
гальванический элемент, в котором
происходит окисление цинка и восстановление
меди. Реакции восстановления и окисления
проходят, соответственно, на катоде
и аноде. А чтобы ионы меди и цинка
не попадали на «чужую территорию»,
где они могут прореагировать друг
с другом непосредственно, между
анодом и катодом обычно помещают
специальную мембрану. В результате
между электродами возникает разность
потенциалов. Если соединить электроды,
например, с лампочкой, то в получившейся
электрической цепи начинает течь ток
и лампочка загорается.
Помимо материалов анода и катода, важной составляющей химического источника тока является электролит, внутри которого движутся ионы и на границе которого с электродами протекают все электрохимические реакции. При этом электролит не обязательно должен быть жидким — это может быть и полимерный, и керамический материал.
Основным недостатком гальванического
элемента является ограниченное время
его работы. Как только реакция пройдет
до конца (то есть будет полностью
израсходован весь постепенно растворяющийся
анод), такой элемент просто перестанет
работать.
Возможность перезарядки
Первым шагом к расширению возможностей химических источников тока стало создание аккумулятора — источника тока, который можно перезаряжать и поэтому использовать многократно. Для этого ученые просто предложили использовать обратимые химические реакции. Полностью разрядив аккумулятор в первый раз, с помощью внешнего источника тока прошедшую в нем реакцию можно запустить в обратном направлении. Это восстановит исходное состояние, так что после перезарядки батарею можно будет использовать заново.
На сегодня создано много различных типов аккумуляторов, которые отличаются типом происходящей в них химической реакции. Наиболее распространенными типами аккумуляторов являются свинцово-кислотные (или просто свинцовые) аккумуляторы, в основе которых лежит реакция окисления-восстановления свинца. Такие устройства обладают довольно длительным сроком службы, а их энергоемкость составляет до 60 ватт-часов на килограмм. Еще более популярными в последнее время являются литий-ионные аккумуляторы, основанные на реакции окисления-восстановления лития. Энергоемкость современных литий-ионных аккумуляторов сейчас превышает 250 ватт-часов на килограмм.
Энергоемкость современных литий-ионных аккумуляторов сейчас превышает 250 ватт-часов на килограмм.
Основными проблемами литий-ионных аккумуляторов являются их небольшая эффективность при отрицательных температурах, быстрое старение и повышенная взрывоопасность. А из-за того, что металлический литий очень активно реагирует с водой с образованием газообразного водорода и при горении аккумулятора выделяется кислород, самовозгорание литий-ионного аккумулятора очень тяжело поддается традиционным способам пожаротушения. Для того чтобы повысить безопасность такого аккумулятора и ускорить время его зарядки, ученые предлагают модифицировать материал катода, воспрепятствовав образованию дендритных литиевых структур, а в электролит добавить вещества, которые блокируют образование взрывоопасных структур, и компоненты, подавляющие возгорание на ранних стадиях.
Твердый электролит
В качестве другого менее очевидного способа повышения эффективности и безопасности батарей, химики предложили не ограничиваться в химических источниках тока жидкими электролитами, а создать полностью твердотельный
источник тока.
Водородные топливные элементы
Возможность перезарядки и специальные меры безопасности делают аккумуляторы значительно более перспективными источниками тока, чем обычные батарейки, но все равно каждый аккумулятор содержит внутри себя ограниченное количество реагентов, а значит, и ограниченный запас энергии, и каждый раз аккумулятор необходимо заново заряжать для возобновления его работоспособности.
Чтобы сделать батарейку «бесконечной», в качестве источника энергии можно использовать не те вещества, которые находятся внутри ячейки, а специально прокачиваемое через нее топливо. Лучше всего в качестве такого топлива подойдет вещество, максимально простое по составу, экологически чистое и имеющееся в достатке на Земле.
Лучше всего в качестве такого топлива подойдет вещество, максимально простое по составу, экологически чистое и имеющееся в достатке на Земле.
Наиболее подходящее вещество такого типа — газообразный водород. Его окисление кислородом воздуха с образованием воды (по реакции 2H2 + O2 → 2H2O) является простой окислительно-восстановительной реакцией, а транспорт электронов между ионами тоже можно использовать в качестве источника тока. Протекающая при этом реакция является своего рода обратной реакцией к реакции электролиза воды (при котором под действием электрического тока вода разлагается на кислород и водород), и впервые такая схема была предложена еще в середине XIX века.
Но несмотря на то, что схема выглядит
довольно простой, создать основанное
на этом принципе эффективно работающее
устройство — совсем не тривиальная задача. Для этого надо развести в пространстве потоки кислорода и водорода, обеспечить транспорт нужных ионов через электролит и снизить возможные потери энергии на всех этапах работы.
Схема работающего водородного топливного элемента очень похожа на схему химического источника тока, но содержит в себе дополнительные каналы для подачи топлива и окислителя и отвода продуктов реакции и избытка поданных газов. Электродами в таком элементе являются пористые проводящие катализаторы. К аноду подается газообразное топливо (водород), а к катоду — окислитель (кислород из воздуха), и на границе каждого из электродов с электролитом проходит своя полуреакция (окисление водорода и восстановление кислорода соответственно). При этом, в зависимости от типа топливного элемента и типа электролита, само образование воды может протекать или в анодном, или в катодном пространстве.
Если электролит является протонпроводящей
полимерной или керамической мембраной,
раствором кислоты или щелочи, то носителем
заряда в электролите являются ионы
водорода. В таком случае на аноде
молекулярный водород окисляется до ионов
водорода, которые проходят через
электролит и там реагируют с кислородом. Если же носителем заряда является
ион кислорода O2–, как в случае
твердооксидного электролита, то на катоде
происходит восстановление кислорода
до иона, этот ион проходит через
электролит и окисляет на аноде
водород с образованием воды и свободных
электронов.
Если же носителем заряда является
ион кислорода O2–, как в случае
твердооксидного электролита, то на катоде
происходит восстановление кислорода
до иона, этот ион проходит через
электролит и окисляет на аноде
водород с образованием воды и свободных
электронов.
Кроме реакции окисления водорода для топливных элементов предложено использовать и другие типы реакций. Например, вместо водорода восстановительным топливом может быть метанол, который кислородом окисляется до углекислого газа и воды.
Эффективность топливных элементов
Несмотря на все преимущества водородных топливных элементов (такие как экологичность, практически неограниченный КПД, компактность размеров и высокая энергоемкость), они обладают и рядом недостатков. К ним относятся, в первую очередь, постепенное старение компонентов и сложности при хранении водорода. Именно над тем, как устранить эти недостатки, и работают сегодня ученые.
Повысить эффективность топливных
элементов в настоящее время предлагается
за счет изменения состава электролита,
свойств электрода-катализатора,
и геометрии системы (которая
обеспечивает подачу топливных газов
в нужную точку и снижает побочные
эффекты).
В результате удается добиться повышения стабильности работы топливного элемента и времени жизни его отдельных компонентов. Сейчас коэффициент преобразования химической энергии в электрическую в таких элементах достигает 80 процентов, а при определенных условиях может быть и еще выше.
Огромные перспективы водородной энергетики связывают с возможностью объединения топливных элементов в целые батареи, превращая их в электрогенераторы с большой мощностью. Уже сейчас электрогенераторы, работающие на водородных топливных элементах, имеют мощность до нескольких сотен киловатт и используются как источники питания транспортных средств.
Альтернативные электрохимические накопители
Помимо
классических электрохимических
источников тока, в качестве накопителей
электроэнергии используют и более необычные системы. Одной из
таких систем является суперконденсатор
(или ионистор) — устройство, в котором
разделение и накопление заряда происходит за счет
образования двойного слоя вблизи
заряженной поверхности. На
границе электрод-электролит в таком
устройстве в два слоя выстраиваются
ионы разных знаков, так называемый
«двойной электрический слой», образуя
своеобразный очень тонкий конденсатор.
Емкость такого конденсатора, то есть
количество накопленного заряда, будет
определяться удельной площадью
поверхности электродного материала,
поэтому в качестве материала для
суперконденсаторов выгодно брать
пористые материалы с максимальной
удельной площадью поверхности.
Одной из
таких систем является суперконденсатор
(или ионистор) — устройство, в котором
разделение и накопление заряда происходит за счет
образования двойного слоя вблизи
заряженной поверхности. На
границе электрод-электролит в таком
устройстве в два слоя выстраиваются
ионы разных знаков, так называемый
«двойной электрический слой», образуя
своеобразный очень тонкий конденсатор.
Емкость такого конденсатора, то есть
количество накопленного заряда, будет
определяться удельной площадью
поверхности электродного материала,
поэтому в качестве материала для
суперконденсаторов выгодно брать
пористые материалы с максимальной
удельной площадью поверхности.
Ионисторы являются рекордсменами
среди зарядно-разрядных химических
источников тока по скорости заряда, что
является несомненным преимуществом
данного типа устройств. К сожалению,
они также являются рекордсменами
и по скорости разряда. Энергоплотность
ионисторов в восемь раз меньше по сравнению
со свинцовыми аккумуляторами и в 25 раз
меньше по сравнению с литий-ионными. Классические «двойнослойные» ионисторы
не используют электрохимическую реакцию
в своей основе, и к ним наиболее точно
применим термин «конденсатор». Однако
в тех вариантах исполнения ионисторов,
в основе которых используется
электрохимическая реакция и накопление
заряда распространяется в глубину
электрода, удается достичь более высоких
времен разрядки при сохранении быстрой
скорости заряда. Усилия разработчиков
суперконденсаторов направлены на
создание гибридных с аккумуляторами
устройств, сочетающих в себе плюсы
суперконденсаторов, в первую очередь
высокую скорость заряда, и достоинства
аккумуляторов — высокую энергоемкость
и длительное время разряда. Представьте
себе в ближайшем будущем аккумулятор-ионистор,
который будет заряжаться за пару минут
и обеспечивать работу ноутбука или
смартфона в течение суток или более!
Классические «двойнослойные» ионисторы
не используют электрохимическую реакцию
в своей основе, и к ним наиболее точно
применим термин «конденсатор». Однако
в тех вариантах исполнения ионисторов,
в основе которых используется
электрохимическая реакция и накопление
заряда распространяется в глубину
электрода, удается достичь более высоких
времен разрядки при сохранении быстрой
скорости заряда. Усилия разработчиков
суперконденсаторов направлены на
создание гибридных с аккумуляторами
устройств, сочетающих в себе плюсы
суперконденсаторов, в первую очередь
высокую скорость заряда, и достоинства
аккумуляторов — высокую энергоемкость
и длительное время разряда. Представьте
себе в ближайшем будущем аккумулятор-ионистор,
который будет заряжаться за пару минут
и обеспечивать работу ноутбука или
смартфона в течение суток или более!
Несмотря на то, что сейчас плотность энергии суперконденсаторов пока в несколько раз меньше плотности энергии аккумуляторов, их используют в бытовой электронике и для двигателей различных транспортных средств, в том числе и в самых современных разработках.
* * *
Таким образом, на сегодня существует большое количество электрохимических устройств, каждое из которых перспективно для своих конкретных приложений. Для повышения эффективности работы этих устройств ученым необходимо решить ряд задач как фундаментального, так и технологического характера. Большинством этих задач в рамках одного из прорывных проектов занимаются в Уральском федеральном университете, поэтому о ближайших планах и перспективах по разработке современных топливных элементов мы попросили рассказать директора Института высокотемпературной электрохимии УрО РАН, профессора кафедры технологии электрохимических производств химико-технологического института Уральского федерального университета Максима Ананьева.
N + 1: Ожидается ли в ближайшем будущем какая-то альтернатива наиболее популярным сейчас литий-ионным аккумуляторам?
Максим Ананьев: Современные усилия разработчиков
аккумуляторов направлены на замену
типа носителя заряда в электролите
с лития на натрий, калий, алюминий. В результате замены лития можно будет
снизить стоимость аккумулятора, правда
при этом пропорционально возрастут
массо-габаритные характеристики. Иными
словами, при одинаковых электрических
характеристиках натрий-ионный аккумулятор
будет больше и тяжелее по сравнению
с литий-ионным.
В результате замены лития можно будет
снизить стоимость аккумулятора, правда
при этом пропорционально возрастут
массо-габаритные характеристики. Иными
словами, при одинаковых электрических
характеристиках натрий-ионный аккумулятор
будет больше и тяжелее по сравнению
с литий-ионным.
Кроме того, одним из перспективных развивающихся направлений совершенствования аккумуляторов является создание гибридных химических источников энергии, основанных на совмещении металл-ионных аккумуляторов с воздушным электродом, как в топливных элементах. В целом, направление создания гибридных систем, как уже было показано на примере суперконденсаторов, по-видимому, в ближайшей перспективе позволит увидеть на рынке химические источники энергии, обладающие высокими потребительскими характеристиками.
Уральский федеральный университет совместно с академическими и индустриальными партнерами России и мира сегодня реализует шесть мегапроектов, которые сфокусированы на прорывных направлениях научных исследований. Один из таких проектов — «Перспективные технологии электрохимической энергетики от химического дизайна новых материалов к электрохимическим устройствам нового поколения для сохранения и преобразования энергии».
Один из таких проектов — «Перспективные технологии электрохимической энергетики от химического дизайна новых материалов к электрохимическим устройствам нового поколения для сохранения и преобразования энергии».
Группа ученых стратегической академической единицы (САЕ) Школа естественных наук и математики УрФУ, в которую входит Максим Ананьев, занимается проектированием и разработкой новых материалов и технологий, среди которых — топливные элементы, электролитические ячейки, металлграфеновые аккумуляторы, электрохимические системы аккумулирования электроэнергии и суперконденсаторы.
Исследования и научная работа ведутся в постоянном взаимодействии с Институтом высокотемпературной электрохимии УрО РАН и при поддержке партнеров.
Какие топливные элементы разрабатываются сейчас и имеют наибольший потенциал?
Одними из наиболее перспективных
типов топливных элементов являются
протонно-керамические элементы. Они
обладают преимуществами перед полимерными
топливными элементами с протонно-обменной
мембраной и твердооксидными элементами,
так как могут работать при прямой подаче
углеводородного топлива. Это существенно
упрощает конструкцию энергоустановки
на основе протонно-керамических
топливных элементов и систему
управления, а следовательно, увеличивает
надежность работы. Правда, такой тип
топливных элементов на данный момент
является исторически менее проработанным,
но современные научные исследования
позволяют надеяться на высокий
потенциал данной технологии в будущем.
Это существенно
упрощает конструкцию энергоустановки
на основе протонно-керамических
топливных элементов и систему
управления, а следовательно, увеличивает
надежность работы. Правда, такой тип
топливных элементов на данный момент
является исторически менее проработанным,
но современные научные исследования
позволяют надеяться на высокий
потенциал данной технологии в будущем.
Какими проблемами, связанными с топливными элементами, занимаются сейчас в Уральском федеральном университете?
Сейчас ученые УрФУ совместно с Институтом
высокотемпературной электрохимии
(ИВТЭ) Уральского отделения Российской
академии наук работают над созданием
высокоэффективных электрохимических
устройств и автономных генераторов
электроэнергии для применений в
распределенной энергетике.
Создание энергоустановок для распределенной
энергетики изначально подразумевает
разработку гибридных систем на основе
генератора электроэнергии и накопителя,
в качестве которых выступают аккумуляторы.
При этом топливный элемент работает
постоянно, обеспечивая нагрузку в
пиковые часы, а в холостом режиме заряжает
аккумулятор, который может сам выступать
резервом как в случае высокого
энергопотребления, так и в случае
внештатных ситуаций.
Наибольших успехов химики УрФУ и ИВТЭ достигли в области разработки твердо-оксидных и протонно-керамических топливных элементов. Начиная с 2016 года на Урале вместе с ГК «Росатом» создается первое в России производство энергоустановок на основе твердо-оксидных топливных элементов. Разработка уральских ученых уже прошла «натурные» испытания на станции катодной защиты газотрубопроводов на экспериментальной площадке ООО «Уралтрансгаз». Энергоустановка с номинальной мощностью 1,5 киловатта отработала более 10 тысяч часов и показала высокий потенциал применения таких устройств.
В рамках совместной лаборатории
УрФУ и ИВТЭ ведутся разработки
электрохимических устройств на основе
протонпроводящей керамической мембраны.
Это позволит в ближайшем будущем снизить
рабочие температуры для твердо-оксидных
топливных элементов с 900 до 500
градусов Цельсия и отказаться
от предварительного риформинга
углеводородного топлива, создав, таким
образом, экономически эффективные
электрохимические генераторы, способные
работать в условиях развитой в России
инфраструктуры газоснабжения.
Александр Дубов
Металл вокруг нас: интересные факты о металлах
Металл вокруг нас
- Образование и карьера
- Металлургия и общество
Интересные факты
Рассмотрены следующие аспекты:
- факты, обзоры и новости
- занимательная информация о свойствах металлов и сплавов
- неизвестное об уникальных металлических изделиях
- роль металлов в космических, геологических, социальных и биологических процессах
Интересные факты о золоте
18 октября 2016
15186
0
( Голосов: 17 )
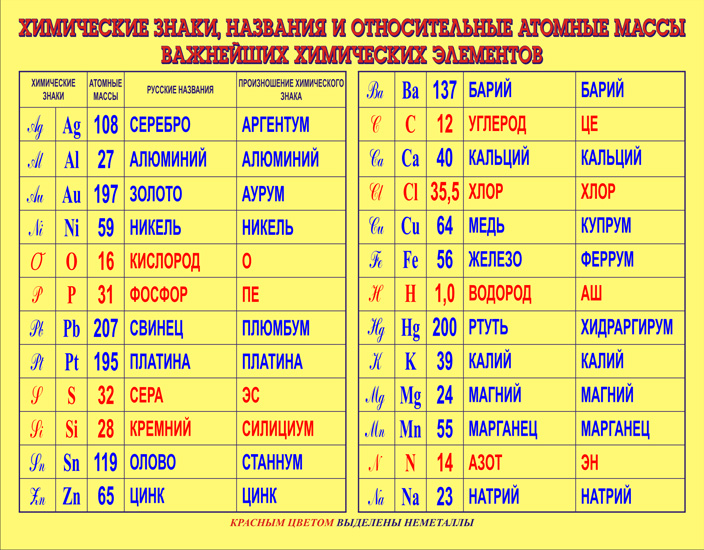
Факт 1: В переводе с прото-индо-европейских корней термин «золото» означал «желтый», «зеленый» или, возможно, «яркий». Золото было одним из первых металлов, открытых человеком. Золото –это химический элемент, в таблице Д.И. Менделеева обозначается «AU», что в переводе с латинского языка Aurum — «сияющий свет». Согласно археологическим данным, золото и медь стали первыми металлами, обнаруженными людьми около 5000 лет до нашей эры. Декоративные золотые изделия, найденные в Болгарии относятся к 4 000 г. до н.э.
Золото было одним из первых металлов, открытых человеком. Золото –это химический элемент, в таблице Д.И. Менделеева обозначается «AU», что в переводе с латинского языка Aurum — «сияющий свет». Согласно археологическим данным, золото и медь стали первыми металлами, обнаруженными людьми около 5000 лет до нашей эры. Декоративные золотые изделия, найденные в Болгарии относятся к 4 000 г. до н.э.
Интересные факты о серебре
17 октября 2016
9080
0
( Голосов: 9 )
Факт 1: Серебро (евр. кэсэф; греч. аргирион) — благородный металл, ковкий, пластичный серебристо-белого цвета. Имеет гранецентрированную кубическую кристаллическую решетку, температуру плавления — 960 °C и плотность — 10,5 г/см*3. Кроме того, этот металл обладает наибольшей отражательной способностью и самой высокой электро- и теплопроводностью. Серебро открыли приблизительно 4000 лет до н.э. Первые украшения стали появляться в Египте.
кэсэф; греч. аргирион) — благородный металл, ковкий, пластичный серебристо-белого цвета. Имеет гранецентрированную кубическую кристаллическую решетку, температуру плавления — 960 °C и плотность — 10,5 г/см*3. Кроме того, этот металл обладает наибольшей отражательной способностью и самой высокой электро- и теплопроводностью. Серебро открыли приблизительно 4000 лет до н.э. Первые украшения стали появляться в Египте.
Интересные факты о никеле
16 октября 2016
11254
0
( Голосов: 11 )
Факт 1: С немецкого слово “nickel” переводится как “озорник”. Никель был открыт в 1751 году, а заслуга получения никеля принадлежит шведскому ученому А.Ф. Кронстедт. По другой версии название никеля происходит от слова «kupiernickel», которое в переводе с немецкого означает «дьявольская медь». Своё название никель получил в честь злого духа гор немецкой мифологии. Никелю приписали дурную славу, так как при выплавлении руд никеля выделялись мышьяковые газы. В тоже время, ничего дьявольского серебристо-белый, пластичный и блестящий металл не имеет. Ученые тогда считали его сплавом. И споры велись вплоть до начала 19-го века, пока никель не выделили безо всяких примесей в чистом виде.
Никель был открыт в 1751 году, а заслуга получения никеля принадлежит шведскому ученому А.Ф. Кронстедт. По другой версии название никеля происходит от слова «kupiernickel», которое в переводе с немецкого означает «дьявольская медь». Своё название никель получил в честь злого духа гор немецкой мифологии. Никелю приписали дурную славу, так как при выплавлении руд никеля выделялись мышьяковые газы. В тоже время, ничего дьявольского серебристо-белый, пластичный и блестящий металл не имеет. Ученые тогда считали его сплавом. И споры велись вплоть до начала 19-го века, пока никель не выделили безо всяких примесей в чистом виде.
Интересные факты об олове
15 октября 2016
16223
0
( Голосов: 7 )
Факт 1: Олово в переводе с латинского это значит «прочный, стойкий». При комнатной температуре олово устойчиво к воздействию воздуха или воды (но при температурах выше 150 °C начинается заметное окисление этого металла). При температуре −33 °C, олово трескается и превращается в порошок (в старые времена рассыпание оловянных изделий называли «оловянной чумой»).
При комнатной температуре олово устойчиво к воздействию воздуха или воды (но при температурах выше 150 °C начинается заметное окисление этого металла). При температуре −33 °C, олово трескается и превращается в порошок (в старые времена рассыпание оловянных изделий называли «оловянной чумой»).
Интересные факты об алюминии
14 октября 2016
33817
0
( Голосов: 14 )
Факт 1: Алюминий является самым распространенным металлом в земной коре среди других металлов и третий по распространённости химический элемент в земной коре после кислорода и углерода. В недрах земли его содержится восемь процентов, в то время как золота — всего 5 миллионных частей процента. Однако люди долго не знали алюминия: первый слиток его был выплавлен во Франции только в 1885 году, и металл этот считался тогда драгоценным.
В недрах земли его содержится восемь процентов, в то время как золота — всего 5 миллионных частей процента. Однако люди долго не знали алюминия: первый слиток его был выплавлен во Франции только в 1885 году, и металл этот считался тогда драгоценным.
Интересные факты о бронзе
13 октября 2016
12127
0
( Голосов: 6 )
Факт 1: Бронза – это сплав меди с разными химическими элементами, главным образом металлами (олово, алюминий, бериллий, свинец, кадмий, хром и другие). Соответственно, бронза называется оловянной, алюминиевой, бериллиевой и т. д. На юге России (Кубань, Адыгея) находят бронзовые изделия майкопской культуры, которые датируются ещё серединой 4 тысячелетия до н. э. Примечательно, что именно в эпоху бронзы преобладающее значение получила монументальная архитектура.
Соответственно, бронза называется оловянной, алюминиевой, бериллиевой и т. д. На юге России (Кубань, Адыгея) находят бронзовые изделия майкопской культуры, которые датируются ещё серединой 4 тысячелетия до н. э. Примечательно, что именно в эпоху бронзы преобладающее значение получила монументальная архитектура.
Интересные факты о платине
12 октября 2016
12398
0
( Голосов: 6 )
Факт 1: Платина в переводе с испанского значит «серебришко». Старинное русское название платины — «серебрец». Такое пренебрежительное название объясняется исключительной тугоплавкостью платины, которая не поддавалась переплавке. Долгое время платина оставалась природным казусом, не находила практического применения и ценилась вдвое ниже, чем серебро. Первыми «ценность» металла поняли в середине XVIII века фальшивомонетчики. Так плотность платины выше, чем у золота, и соответственно она тяжелее, стали подмешивать платину к золоту и серебру, сначала в украшениях, а затем и в монетах. Золото с примесью платины прозвали гнилым, или «испанским». Сейчас на мировых биржах платина дороже серебра примерно в 100 раз.
Старинное русское название платины — «серебрец». Такое пренебрежительное название объясняется исключительной тугоплавкостью платины, которая не поддавалась переплавке. Долгое время платина оставалась природным казусом, не находила практического применения и ценилась вдвое ниже, чем серебро. Первыми «ценность» металла поняли в середине XVIII века фальшивомонетчики. Так плотность платины выше, чем у золота, и соответственно она тяжелее, стали подмешивать платину к золоту и серебру, сначала в украшениях, а затем и в монетах. Золото с примесью платины прозвали гнилым, или «испанским». Сейчас на мировых биржах платина дороже серебра примерно в 100 раз.
Интересные факты о меди
11 октября 2016
19953
0
( Голосов: 9 )
Факт 1: Предметы, изготовленные из такого металла как медь, а также из ее сплавов, не могут создавать искры. Это свойство меди применяется в производстве инструментов для проведения огнеопасных работ. В Японии, подверженной частым землетрясениям, медь применяют для производства газовых трубопроводов, которые отличаются высокой сейсмоустойчивостью.
Это свойство меди применяется в производстве инструментов для проведения огнеопасных работ. В Японии, подверженной частым землетрясениям, медь применяют для производства газовых трубопроводов, которые отличаются высокой сейсмоустойчивостью.
Интересные факты о металлах
10 октября 2016
14597
0
( Голосов: 6 )
1 место: Платина в переводе с испанского буквально означает «серебришко». Такое пренебрежительное название платине дали конкистадоры. Дело в том, что будучи исключительно тугоплавкой, платина не поддавалась переплавке и ценилась вдвое ниже, чем серебро. Сейчас на мировых биржах платина дороже серебра примерно в 100 раз.
Такое пренебрежительное название платине дали конкистадоры. Дело в том, что будучи исключительно тугоплавкой, платина не поддавалась переплавке и ценилась вдвое ниже, чем серебро. Сейчас на мировых биржах платина дороже серебра примерно в 100 раз.
Золотые слитки в форме плитки шоколада
01 сентября 2016
7694
0
( Голосов: 5 )
Швейцарская фирма Valcambi SA («Валкамби») выпускает золотые слитки CombiBar в форме, напоминающей плитку шоколада. Золотая «плитка» компании Valcambi SA весит 50 грамм она изготовлена из золота 999,99 пробы.
Золотая «плитка» компании Valcambi SA весит 50 грамм она изготовлена из золота 999,99 пробы.
Металлургия и общество
Культурные, социально-политические и технические взаимосвязи современной индустриальной цивилизации, в основе которой лежат металлургические технологии.
АНАЛИТИКА
Научные статьи и методические материалы о природных и вторичных ресурсах металлов, а также металлургических технологиях
Производство и наука
- Эколого-экономическая эффективность реновации технических изделий июль 22, 2019
- Сжиженный природный газ март 19, 2018
- Ветроэнергетика в России, развитие технологии в ветроэнергетике янв 23, 2018
Методические материалы
- Модернизация барабанных летучих ножниц – Дипломный проект дек 03, 2020
- Схема рециклинга автомобильных катализаторов, содержащих металлы платиновой группы авг 15, 2018
- Историко-реконструкторское движение в России фев 04, 2017
Интерактивный учебник
- Как правильно согнуть металлический квадрат апр 01, 2020
- Сталь с полимерным покрытием янв 04, 2019
- Топливо из ТБО дек 17, 2018
Потенциал Забайкальского .
 ..
..Обработка металлов …
Пластическая деформация …
Металлургические технологии …
Основоположники отечественной …
Основоположники отечественной …
Русская средневековая .
 ..
..Русская средневековая …
ИНТЕРАКТИВ
Интерактивная картина мира металлов на ключевых этапах истории цивилизации
Энциклопедия «Металлургия и время»
- «Дредноуты» и «крупповские пушки» март 10, 2014
- Преимущества получения ферромарганца в электропечах март 09, 2014
- Проблемы производства доменных ферросплавов март 08, 2014
Металлургические объекты
- Музей истории МИСиС.
 Металлургия – кузница победы
апр 20, 2020
Металлургия – кузница победы
апр 20, 2020 - Доменная печь Лиенсхютте (Lienshytte blast-furnace) авг 28, 2014
- Железоделательный завод Энгельсберг (Engelsbergs bruk) авг 27, 2014
Обучающие игры
- Маша и компания – Таланты дек 07, 2014
- Маша и компания – Игры на природе дек 06, 2014
- Легенды огня и металла Часть 3.
 Мушкет
июнь 19, 2014
Мушкет
июнь 19, 2014
Copyright © 2011 – 2022 MetalSpace
Определение очищенной меди | Law Insider
означает судно, построенное или приспособленное главным образом для перевозки нефти наливом в его грузовых помещениях, и включает комбинированные суда и любой «танкер-химовоз», как он определен в Приложении II к настоящей Конвенции, когда оно перевозит груз или часть груза. нефти оптом.
означает корпорацию, товарищество, компанию с ограниченной ответственностью или другую хозяйственную единицу, занимающуюся производством качественной продукции и зарегистрированную секретарем штата Арканзас для ведения бизнеса в Арканзасе;
означает предельный коэффициент полезного действия.

означает любую организацию, предоставляющую собственные или арендованные транспортные средства для перевозки или оказывающую транспортно-экспедиторские услуги или авиаэкспресс.
означает судно, которое не является самоходным или приспособленным для движения под парусом, веслом, веслом или подобным устройством.
означает в системе электроснабжения отсрочку конечного использования электроэнергии до момента, когда она была произведена, или преобразование электрической энергии в форму энергии, которая может быть сохранена, хранение такой энергии, и последующее обратное преобразование такой энергии в электрическую энергию или использование в качестве другого энергоносителя;
означает сжиженный нефтяной газ.
означает предприятие, использующее
означает ШФЛУ, химическая формула которого C3H8, используемая для отопления, сушки урожая, моторного топлива и в качестве сырья для нефтехимической промышленности при производстве этилена и пропилена ;
означает дизельное топливо с содержанием серы не более пятнадцати частей на
означает судно, построенное или приспособленное и используемое для перевозки наливом любых жидких продуктов, перечисленных в главе 17 Международного кодекса по химовозам , в его актуальной версии;
означает любую печь, котел, аппарат, дымовую трубу и все связанное с ними оборудование, используемое в процессе сжигания топлива.

означает сжиженный природный газ.
означает весовую долю песка, ила и глины в почве.
означает систему, которая хранит энергию и высвобождает ее в той же форме, в которой она была введена.
означает различимый компонент предприятия, занимающийся поставкой отдельных товаров или услуг или группы связанных товаров или услуг, подверженный рискам и доходам, которые отличаются от рисков и доходов других вертикалей бизнеса.
означает здание, часть здания или внешнюю территорию, примыкающую к зданию, используемую для хранения любых химических или химически активных продуктов.
означает любую трубу, трубы или трубопроводы, используемые для внутриштатной транспортировки или передачи любого твердого, жидкого или газообразного вещества, кроме воды.
означает газообразное топливо, произведенное из биомассы;
средство для производства
означает дистиллятное масло, которое можно использовать в качестве топлива для работы двигателя с воспламенением от сжатия и которое имеет приблизительную температуру кипения от 150 °C до 400 °C;
означает субстехиометрическое окисление или паровую конверсию вещества с получением газообразной смеси, содержащей два или более из следующих компонентов: (i) оксиды углерода; (ii) метан; и (iii) водород;
означает то же, что и в разделе 214A.
 1 Кодекса штата Айова.
1 Кодекса штата Айова.означает природный газ, нефть, уголь или любую форму твердого, жидкого или газообразного топлива, полученного из такого материала.
означает землю, используемую или управляемую для долгосрочного производства древесины, древесного волокна или продукции из древесины.
означает в отношении единицы:
Электролитическое рафинирование меди
Электролитическое рафинирование меди используется для очистки металла с помощью электролиза.
В этом методе анод изготавливается из нечистой меди, а катод из чистой меди. Электролит готовят из подкисленного раствора медного купороса. При пропускании электричества нечистая медь с анода растворяется в электролите, а чистая медь осаждается на катоде.
Таким образом из катода получают чистую медь.
Что такое переработка?
Аффинаж — это процесс удаления примесей для получения чистого металла. Для удаления примесей из металлов используются различные процессы; они основаны на природе металла и примесей.
Различные методы, используемые для рафинирования металлов:
- Дистилляция
- Ликвация
- Зонное рафинирование
- Парофазное рафинирование
- Электролитическое рафинирование
Чаще всего используется электролитическая очистка.
Помимо меди, такие металлы, как серебро и цинк, очищаются с помощью электролиза.
В 1847 году Максимилиан, герцог Лейхтенбергский, впервые экспериментально продемонстрировал электролитическое рафинирование меди.
Электролиз
Термин «электролиз», введенный Майклом Фарадеем, относится к процессу, при котором электрический ток проходит через химическое вещество, чтобы вызвать химическое изменение.
При электролизе через электролит пропускают постоянный электрический ток. В результате на электродах происходят химические реакции, и материалы разлагаются.
Основными компонентами электролиза являются:
- Электролит
- Электроды
- Внешний источник питания
- Солевой мостик
Химическое вещество, содержащее свободные ионы и проводящее электрический ток, известно как электролит.
Электрический проводник, используемый для контакта с неметаллической частью цепи, называется электродом.
Электроды погружены в электролит и находятся на расстоянии друг от друга. Ток течет между ними через электролит. Электроды также подключаются к источнику питания, замыкая электрическую цепь.
Электролиз включает обмен ионами и атомами, который происходит в результате добавления или удаления электронов из-за приложенного тока.
Процесс электролитического рафинирования
Электрорафинирование также известно как электрорафинирование. В этом методе металлы, такие как медь, очищают с помощью электролиза.
В качестве анода используется полоска нечистого металла, а в качестве катода – полоска чистого металла. В качестве электролита используется водный раствор соли металла.
На отрицательно заряженном электроде или катоде катионы металлов приобретают электроны и восстанавливаются. Таким образом, они осаждаются на катоде в виде чистых нейтральных атомов металла.
При электролитическом рафинировании анодом является нечистый металл, и примеси теряются при переносе металла с анода на катод.
После завершения процесса на катоде образуется чистый металл путем растворения нечистого металла на аноде.
При пропускании электрического тока через раствор электролита происходят следующие реакции:
Реакция на катоде
Mn+ + ne- → M
Реакция на аноде:
M → Mn+ + ne-
Электролитическое рафинирование медь
Примесная или черновая медь имеет чистоту около 99% при извлечении из руды. Медные металлы могут быть очищены до 99,99% электролитическим рафинированием. Анод (положительный электрод) сделан из нечистой меди, а катод (отрицательный электрод) из чистой меди. В качестве электролита в этом процессе используется сульфат меди, подкисленный серной кислотой. При пропускании электрического тока нечистый металл растворяется с анода в растворе электролита. В этой фазе сульфат меди диссоциирует на ионы Cu++ и (SO4)2-. Положительные ионы меди, также известные как катионы, движутся к катоду, состоящему из чистой металлической меди. Катионы металлов поглощают электроны с катода и осаждаются на катоде в виде атомов Cu. Таким образом, на катоде образуется чистая медь.
Положительные ионы меди, также известные как катионы, движутся к катоду, состоящему из чистой металлической меди. Катионы металлов поглощают электроны с катода и осаждаются на катоде в виде атомов Cu. Таким образом, на катоде образуется чистая медь.
При пропускании электрического тока через раствор электролита происходят следующие реакции:
На катоде:
Cu2+ + 2e- → Cu
На аноде:
Cu → Cu2+ + 2e-
Растворимые примеси растворяются в растворе электролита, а нерастворимые примеси могут находиться на дне анода. Эта нерастворимая примесь известна как анодный шлам.
В этом методе катод покрывают графитом, так как это облегчает отделение чистой меди.
Значение электролитического рафинирования меди
Загрязненная медь имеет меньшую проводимость, чем чистая медь. Примеси снижают электропроводность меди. Как мы знаем, медь используется для изготовления электрических проводов из-за ее проводящей природы. При получении меди она имеет чистоту 99%; после электролитической очистки становится почти 99,99% чистоты.