Как в промышленности получают ацетилен – Урок №19. Получение и применение ацетилена.
alexxlab | 07.01.2020 | 0 | Разное
Ацетилен
Для газопламенных работ необходимо осуществить передачу тепла из пламени в металл в количестве, достаточном для конкретных условий работ. Горючие газы сгорают, как правило, в смеси с кислородом. Наибольшей температурой обладает ацетилено-кислородное пламя (3200°С), что позволяет использовать ацетилен при любых видах газопламенной обработки металлов. Интенсивность горения пламени определяется произведением нормальной скорости горения на теплоту сгорания смеси. Ацетилен обладает наивысшей «интенсивностью горения», которая для смеси стехиометрического состава составляет 27 700 ккал/(м2*с).
Ацетилен
Ацетилен относится к группе непредельных углеводородов ряда СnН2n-2.. Это бесцветный горючий газ со специфическим запахом; благодаря наличию в нем примесей – фосфористого водорода, сероводорода и пр. плотность ацетилена при 20°С и 760 мм рт. ст. равна 1,091 кг/м
Ацетилен – единственный широко используемый в промышленности газ, относящийся к числу немногих соединений, горение и взрыв которых возможны в отсутствии кислорода или других окислителей. Ацетилен высокоэндотермическое соединение; при разложении 1 кг ацетилена выделяется более 2000 ккал, т. е. примерно в 2 раза больше, чем при взрыве 1 кг твердого ВВ тротила. Температура самовоспламенения ацетилена колеблется в пределах 500 – 600°С при давлении 2 кгс/см2 и заметно снижается с увеличением давления; так, при давлении 22 кгс/см2
температура самовоспламенения ацетилена равна 350°С, а при наличии катализаторов, таких, как железный порошок, силикагель, активный уголь и др. разложение ацетилена начинается при 280 – 300°С. Присутствие окиси меди снижает температуру самовоспламенения до 246°С. При определенных условиях ацетилен реагирует с медью, образуя взрывоопасные соединения; поэтому при изготовлении ацетиленового оборудования запрещается применять сплавы, содержащие более 70% Cu.Взрывчатый распад ацетилена, как правило, начинается при интенсивном нагреве со скоростью 100 – 500°С/с. При медленном нагреве происходит реакция полимеризации ацетилена, идущая с выделением тепла, которая, как правило, при температуре свыше 530°С влечет за собой взрывчатый распад ацетилена. Нижнее предельное давление, при котором возможно разложение ацетилена, равно 0,65 кгс/см2. Пределы взрываемости для ацетилена широки (табл. 2). Наиболее опасными являются смеси ацетилена с кислородом стехиометрического состава (~30%). Скорости распространения пламени и детонации достигают наибольшего значения при соотношении ацетилена и кислорода 1:2,5 и соответственно равны 13,5 и 2400 м/с при нормальных условиях. Давление, образующееся при взрыве ацетилена, зависит от начальных параметров и характера взрыва. Оно может возрасти примерно в 10 – 12 раз по сравнению с начальным при взрыве в небольших сосудах и может быть увеличено в 22 раза при детонации чистого ацетилена и в 50 раз при детонации ацетилено-кислородной смеси.
При газопламенной обработке металлов ацетилен используют либо в газообразном состоянии при получении его в переносных или стационарных ацетиленовых генераторах, либо в растворенном состоянии. Растворенный ацетилен представляет собой раствор ацетилена в ацетоне, распределенный равномерно в пористом наполнителе под давлением. Растворимость ацетилена зависит от температуры и давления. Пористая масса в баллоне обеспечивает рассосредоточение ацетилена по всему объему и локализацию взрывчатого распада ацетилена. При отсутствии пористой массы в баллоне инициированный взрывной распад ацетилена, растворенного в ацетоне, происходит при давлении ниже 5 кгс/см 2. В качестве пористых наполнителей могут быть использованы не только насыпные пористые массы, но и литые пористые массы, которые нашли применение за рубежом.
Физико-химические показатели газообразного и растворенного технического ацетилена оговорены ГОСТ 5457 – 75. По содержанию допустимого количества примесей различают ацетилен растворенный, растворенный и газообразный; допустимое содержание примесей (в объемных долях) соответственно равно:
- воздуха и других малорастворимых в воде газов – не более 0,9, 1,0, 1,5;
- фосфористого водорода – 0,01; 0,04; 0,08;
- сероводорода – 0,005; 0,05; 0,15;
- водяных паров при 20°С и 760 мм рт. ст. – 0,5; 0,6.
Для газопламенной обработки металлов, наряду с ацетиленом, полученным из карбида кальция, применяют пиролизный ацетилен, получаемый из природного газа термоокислительным пиролизом метана с кислородом. Пиролизный ацетилен также хранят и транспортируют в баллонах в растворенном виде. Наполнитель и растворитель для пиролизного ацетилена тот же, что и для ацетилена из карбида кальция.
При применении растворенного ацетилена по сравнению с газообразным обеспечиваются наибольший коэффициент использования карбида, чистота рабочего места сварщика, устойчивая работа аппаратуры и безопасность в работе. Основным сырьем для получения ацетилена, используемого при газопламенной обработке металлов, является карбид кальция. Карбид кальция получают в электрических печах при взаимодействии обожженной извести с коксом или антрацитом. Расплавленный карбид кальция разливают в изложницы, где он застывает; затем его дробят в кусковых дробилках и сортируют по размерам кусков согласно ГОСТ 1460. Ацетилен получают в результате разложения (гидролиза) карбида кальция водой. Действительный «литраж» ацетилена из 1 кг технического карбида при 20°С и 760 мм рт. ст. не превышает 285 л и зависит от грануляции карбида. С увеличением размеров кусков карбида «литраж» увеличивается, однако скорость разложения его уменьшается, т. е. увеличивается длительность разложения карбида (табл. 1).
Содержание фосфористого водорода в ацетилене по объему не более 0,08%, содержание сульфидной серы не более 1,2%. В ГОСТ 1460 оговаривается также допустимое количество кусков карбида кальция других размеров в партиях указанной грануляции. Большой тепловой эффект реакции разложения карбида создает опасность сильного перегрева. Без отвода тепла при взаимодействии стехиометрического количества карбида кальция и воды реакционная масса разогревается до 700 – 800°С. Разложение карбида при недостаточном охлаждении и особенно в присутствии воздуха может привести к взрыву, поэтому необходимо процесс осуществлять при значительном избытке воды. Для разложения 1 кг карбида необходимо 5 – 20 л воды. Особое внимание необходимо обращать на наличие карбидной пыли в карбиде. Пыль разлагается почти мгновенно; за счет мгновенного разогрева может возникнуть взрыв ацетилена. Поэтому переработка пыли в обычных генераторах, не приспособленных для использования пыли, не допускается. Если содержание пыли значительно, карбид кальция перед загрузкой в генератор просеивают через сито с ячейками диаметром 2 мм. Накопившуюся пыль следует разложить на открытом воздухе в специальном сосуде вместимостью не менее 800 – 1000 л при интенсивном помешивании, одновременно высыпая не более 250 г карбидной пыли. Воду следует менять после разложения пыли в количестве до 100 кг.
Карбид кальция транспортируют и хранят в железных барабанах с толщиной стенки не менее 0,51 мм и массой 50 – 130 кг. Боковую поверхность барабанов делают гофрированной для большей жесткости. Карбид кальция интенсивно поглощает влагу даже из воздуха, поэтому при плохой герметичности тары возможно образование ацетилена непосредственно в барабане. Герметичность барабанов следует тщательно проверять; при перевозке барабанов на открытых машинах необходимо покрывать барабаны брезентом. При обнаружении повреждения барабана, карбид должен быть пересыпан в другую герметичную тару.
При обслуживании стационарных генераторов карбид из барабанов пересыпают в специальные приемники-бункеры. Вскрытие барабанов на станции, как правило, механизировано. Для этих целей применяют станки, в которых верхняя крышка вырезается специальным режущим роликом или клиновыми ножами. Ножи и ролик изготовляют из неискрящегося материала. Кроме того, к месту реза подается масло или азот.
Транспортировка карбида кальция в барабанах для стационарных генераторов производительностью свыше 20 м3/ч экономически не оправдана, так как раскупорка барабанов занимает значительное время; накапливается большое количество порожней тары, которая вторично не может быть использована; потери карбида за счет его дробления при перекатывании барабанов и последующего отсева от пыли значительны. Поэтому можно считать наиболее перспективным контейнерный способ перевозки и хранения карбида для стационарных установок. При газопламенной обработке алюминия, латуни, свинца и других металлов, имеющих температуру плавления ниже температуры плавления стали, в качестве горючего газа целесообразно применять не ацетилен, а газы – заменители ацетилена или жидкие горючие. Основные физические и тепловые свойства горючих газов приведены в табл. 2.
Таблица 1. Физико-химические показатели карбида кальция
Размеры кусков, мм | Обозначение | «Литраж», л/кг, не менее | |
Первый сорт | Второй сорт | ||
25 – 80 | 25/80 | 285 | 265 |
15 – 25 | 15/25 | 275 | 255 |
8 – 15 | 8/15 | 250 | |
2 – 8 | 2/8 | 255 | 240 |
Для кусков смешанного размера |
| 275 | 255 |
Таблица 2. Основные физические и тепловые свойства горючих газов
Наименование горючего газа и химическая формула | Низшая теплота сгорания при 20°С и 760 мм рт. ст., ккал/мз | Температура пламени смеси с кислородом, °С | Коэффициент замены ацетилена | Плотность при 20°С и 760 мм рт. ст., кг/м3 | Критическое давление, кгс/см2 | Температура,°С | Пределы взрываемости, % содержания горючего в смеси | Оптимальное соотношение между кислородом и другим горючим в смеси | Относительная скорость распространения пламени с воздухом | |||
критическая*1 | плавления | кипения | с воздухом | с кислородом | ||||||||
Ацетилен С2Н2 | 12000 | 3100-3200 | 1,0 | 1,09 | 61,65 | +35,54 | -81,0 | -83,6 | 2,1-100 | 2,3-100 | 1,7 | 1,0 |
Водород Н2 | 2400 | 2100-2500 | 5,2 | 0,084 | 12,8 | -239,8 | -259,2 | -252,8 | 3,3-81,5 | 2,6-95 | 0,4 | 1,2 |
Метан СН4 | 8000 | 2000-2200 | 1,6 | 0,67 | 45,7 | -82,5 | -182,5 | -161,7 | 4,8-16,7 | 5-59, | 2,0 | – |
Этан С2Н6 | 14400 | 2200 | 1,27 | – | – | – | -172,1 | -88,5 | 3,1-15,0 | 4,1-50,1 | – | – |
Пропан С3Н8 | 20800 | 2600-2750 | 0,65 | 1,88 | 42 | +96,8 | -189,9 | -42,6 | 2,0-11 | 2,0-48 | 3,5-4,0 | 0,3 |
Бутан С4Н10 | 27800 | 2400-2500 | 0,45 | 2,54 | 36 | -152 | -139 | -0,6 | 1,5-8,5 | 3,0-45 | 3,5-4,0 | – |
Пропан-бутан | 20600 | 2000-2100 | 0,6 | 1,867 | – | – | – | – | 2,17-9,5 | – | 3,5-4,0 | – |
Этилен С2Н4 | 14200 | 2900 | 0,9 | 1,17 | – | – | – | – | 2,7-36 | 2,6-80 | – | – |
Окись углерода СО | 2800 | 2600-2800 | 4,5 | 1,16 | 34,5 | -140,2 | -205 | -191,5 | 11,4-77,5 | 15,5-93,9 | – | – |
Сланцевый газ *2 | 3000–3400 | 1500-2000 | 4,0 | 0,74-1,0 | – | – | – | – | – | – | 0,7 | 0,5 |
Коксовый газ *2 | 3500–4400 | 2000-2200 | 3,2 | 0,4-0,55 | – | – | – | – | 7-21 | – | 0,8-0,9 | 0,7 |
Природный газ*2 (метан 98%) | 7500 – 9000 | 2000-2200 | 1,8 | 0,68-0,9 | – | – | – | – | 4,8-14,0 | – | 1,7-2,1 | 0,4 |
Нефтяной (попутный) газ | 8700–14800 | 2000-2400 | 1,2 | 0,87-1,37 | – | – | – | – | 3,5-16,3 | — | 1,9-2,9 | 0,5 |
Городской газ*2 | 4100–9000 | 2000-2300 | 3,0 | 0,84-1,05 | – | – | – | – | 3,8-40 | 8,5-73,6 | 1,2 | 0,5 |
Пиролизный газ | 7500 – 9000 | 2000-2400 | 1,8 | 0,65-0,85 | – | – | – | – | – | – | – | – |
МАПП или МАФ | 21 200 | 2800-2900 | 0,55 | 1,76 | – | – | – | – | 3,4-108 | 2,5-60 | – | – |
Пары бензина (~С7Н15) | 10 тыс. ккал/кг | 2400 | – | 0,7-0,74 кг/л | – | – | – | – | 0,7-6,0 | 2,1-28,4 | – | – |
Пары керосина (~С7Н14) | 10 тыс. ккал/кг | 2300 | – | 0,79-0,82 кг/л | – | – | – | – | 1,4-5,5 | – | – | – |
*1 Критической температурой называется такая температура, выше которой газ не переходит в жидкое состояние ни при каком давлении.
*2 Для горючих газовых смесей приводимые данные относятся к средним составам этих газов.
Широкие пределы изменения плотности, температуры пламени и теплоты сгорания объясняются изменяющимся химическим составом указанных газов, зависящим от месторождения или места производства.
Метилацетилен-пропадиен МАПП (широко применяемый в США) – смесь горючих газов; по физическим свойствам близок к пропану. Пределы взрываемости МАПП в смеси с воздухом 3,4 – 10,8%, в смеси с кислородом 2,5 – 60%. Смеси метилацетилена и пропадиена термодинамически нестойки, поэтому в состав МАППа вводят стабилизатор. Распад метилацетилена, аналогично ацетилену, происходит с большим выделением тепла. Температура пламени МАПП (2900°С) близка к температуре ацетилена. МАПП используют для кислородной резки и сварки и других газопламенных процессов.
Горючее МАФ – метилацетиленовая пропадиеновая фракция является отходом олифинового производства, а также отходом производства этилена и моновинилацетилена. Эта фракция содержит 48 – 75% смеси метилацетилена и пропадиена и стабилизаторы: 3% пропилена, 15% пропана, 7% других углеводородов. Пределы взрываемости для МАФа те же, что и для МАППа. МАФ нечувствителен к удару. Баллоны с МАФом не взрываются, находясь рядом с горящим баллоном. Смесь инертна при температуре до 215°С и давлении до 20 кгс/см2. При соприкосновении с медью образуются взрывоопасные соединения – ацетилениды меди. Скорость распространения пламени МАФ равна 470 см/с. Вместимость баллонов для сжиженных газов 40 или 55 дм3; толщина стенки 3 мм. Предельное рабочее давление (кгс/см2)в баллонах для сжиженных газов различно: для пропана не более 16, для пропилена 20, для бутана и бутилена 3,8. Коэффициент наполнения баллонов сжиженными газами (в кгс/м3) соответственно будет равен: 425 для пропана, 445 – пропилена, 448 – бутана и 526 – бутилена. Коэффициент наполнения обозначает массу газа в кг на 1 м3 вместимости баллона и не должен превышать значений, указанных для каждого газа.
oitsp.ru
Ацетилен: применение в медицине, промышленности
Ацетилен относится к углеводородам ненасыщенного ряда. Это соединение, а также его различные гомологи служат сырьем для синтеза большого количества химических продуктов.
Свойства и получение ацетилена
В условиях атмосферного давления и нормальной температуры ацетилен представляет собой бесцветный газ. Если температура опускается до значения -85 градусов и ниже, то это соединение переходит в другое состояние – твердое. При этом образуются кристаллы. Следует отметить, что в жидком и твердом состоянии ацетилен может легко взрываться под воздействием трения или при ударе (гидравлическом или механическом). Именно это свойство во многом обусловливает его область применения. Реакции горения ацетилена происходят в присутствии кислорода. В результате данного процесса возникает пламя, характеризующееся самыми высокими показателями температуры (3150 градусов) по сравнению с другими видами горючего.
Основным способом получения ацетилена является реакция, в которой взаимодействуют карбид кальция и вода. Данный процесс протекает при показателях температуры около 2000 градусов и является эндотермическим.
Существует такое понятие, как выход ацетилена. Это такое его количество, которое выделяется в результате разложения 1 кг карбида кальция. ГОСТ 1460-56 устанавливает конкретные значения данной величины, которая находится в прямой зависимости от степени грануляции исходного вещества. Таким образом, следствием относительно небольшого размера частиц карбида кальция является снижение выхода ацетилена.
Данная закономерность является следствием наличия в мелких частицах карбида посторонних примесей, например оксида кальция.
Существуют и другие, менее громоздкие, дорогие и энергозатратные способы получения ацетилена. Например, реакция термоокислительного пиролиза метана из природного газа; разложение нефти, керосина и других видов горючего путем электропиролиза.
Хранение и транспортировка
Все способы хранения и транспортировки предусматривают использование баллонов. Они заполняются специальной массой пористой консистенции. Ее пропитывают ацетоном, который хорошо растворяет ацетилен. Применение данного способа позволяет значительно увеличить наполняемость баллона ацетилена и, что немаловажно, понижает его взрывоопасность.
Длительное соприкосновение ацетилена с такими металлами, как медь и серебро, может привести к повышению его взрывоопасности. Следовательно, недопустимо использование материалов, которые могут содержать эти металлы, например в вентилях.

Как правило, баллоны должны иметь специальные вентили, предназначенные именно для хранения ацетилена.
Полного использования всей емкости баллона можно достигнуть, храня пустые емкости так, чтобы ацетон был распределен по всему объему баллона. А это возможно только в горизонтальном положении. Наполнение баллона должно происходить очень медленно, что важно для соблюдения условий химической реакции растворения ацетилена в ацетоне, а в частности ее скорости.
Преимущества растворенного ацетилена
Основное преимущество растворенного ацетилена перед тем, который получают с использованием переносных генераторов из карбида кальция, состоит в том, что при применении баллонов происходит повышение труда сварщика примерно на 20 %, а потери ацетилена при этом снижаются на 25 %. Также следует отметить повышение оперативности и маневренности сварочного поста, безопасность. В отличие от газа, полученного из карбида кальция, растворенный ацетилен содержит значительно меньше посторонних веществ, то есть примесей, что позволяет использовать его в особо ответственных сварочных работах.
Основные области применения ацетилена
- Сварка и резка металлов.
- Использование в качестве источника яркого, белого света. В данном случае речь идет об ацетилене, получаемом путем взаимодействия карбида кальция и воды. При этом используются автономные светильники.
- Производство взрывчатых веществ.
- Получение других соединений и материалов, которыми являются уксусная кислота, этиловый спирт, растворители, пластические массы, каучук, ароматические углеводороды.
Автогенные и сварочные работы сопровождают практически все этапы строительства. Именно в этих видах работ применяется ацетилен. В специальном устройстве под названием горелка происходит смешивание газов и непосредственно сама реакция горения. Наивысшая температура данной реакции достигается при содержании ацетилена 45 % от всего объема баллона.

Баллоны с этим газом маркируют следующим образом: окрашивают в белый цвет и большими красными буквами наносят надпись: «Ацетилен»
Строительные работы проводятся в основном на открытом воздухе. Применение ацетилена и его гомологов в этих условиях не должно проходить под воздействием прямых солнечных лучей. Небольшие перерывы должны сопровождаться перекрыванием вентилей на горелке, а длительные – перекрыванием вентилей на самих баллонах.
В химической промышленности очень востребован ацетилен. Применение его заключается в использовании данного вещества в процессе получения продуктов органического синтеза. Это синтетический каучук, пластмассы, растворители, уксусная кислота и т.д.
Ацетилен, являясь универсальным горючим, часто используется в процессах, сопровождающихся газопламенной обработкой. Важно, что применение ацетилена в промышленности возможно только при соблюдении мер безопасности, так как он является взрывоопасным газом.
Карбидные лампы
Название «карбидная лампа» обусловлено использованием в качестве источника света открытого пламени струи сжигаемого ацетилена. Он, соответственно, получен в результате взаимодействия карбида кальция с водой.
Такие лампы были широко распространены в прошлом. Их можно было увидеть на каретах, автомобилях и даже велосипедах. В современное время карбидные лампы используют только в случае острой необходимости в мощном автономном светильнике. Так, спелеологи часто пользуются ими. Отдаленные маяки снабжают именно такими лампами, ведь такой тип освещения намного выгоднее, нежели подведение линий электропередач. Достаточно распространенным является использование таких ламп на судах дальнего плавания.
Ацетилен: применение в медицине
Как используется вещество в этой сфере? Общая анестезия предполагает применение алкинов. Ацетилен является одним из тех газов, которые используются при ингаляционном наркозе. Но повсеместное его применение в этом качестве осталось в прошлом. Сейчас появились более современные и безопасные способы анестезии.
Хотя следует отметить, что и применение ацетилена не представляло большой опасности, так как прежде чем значение его концентрации во вдыхаемом воздухе дойдет до опасного предела, нижний порог горючести будет пройден.
Самым главным условием использования данного газа является соблюдение мер безопасности. Сложно переоценить, насколько опасен ацетилен. Применение его возможно только после проведения всех необходимых инструктажей с работниками различных сфер, в которых он используется.
fb.ru
Применение ацетилена. Сварка ацетиленом
Чтобы понять, где применяется ацетилен, необходимо изучить и понять, что же это такое. Данное вещество представляет собой горючий бесцветный газ. Его химическая формула – С2Н2. Газ обладает атомной массой, равной 26,04. Он немного легче воздуха и обладает резким запахом. Получение и применение ацетилена осуществляется лишь в промышленных условиях. Получают данное вещество из карбида кальция путем разложения компонента в воде.

Чем опасен ацетилен
Применение ацетилена ограничено его необычайными свойствами. Этот газ самовоспламеняется. Происходит это при температуре 335°С, а его смесь с кислородом – при температуре от 297 до 306°С, с воздухом – при температуре от 305 до 470°С.
Стоит отметить, что ацетилен технический взрывоопасен. Это было происходит при:
- Повышении температуры до 450-500°С, а также при давлении в 150-200 кПа, что равно 1,5-2 атмосферам.
- Смесь ацетилена и кислорода при атмосферном давлении также опасна, если ацетилена в ней содержится 2,3-93%. Взрыв может произойти от сильного нагрева, открытого пламени и даже от искры.
- При подобных же условиях происходит взрыв смеси воздуха с ацетиленом, если в ней содержится 2,2-80,7 % ацетилена.
- Если газ долго соприкасается с медным или серебряным предметом, то может образоваться ацетиленистое взрывчатое серебро или же медь. Это вещество очень опасно. Взрыв может произойти от сильного удара или же в результате повышения температуры. Работать с газом следует осторожно.
Особенности вещества
Ацетилен, свойства и применение которого до конца не изучены, в результате взрыва может привести к несчастному случаю и сильнейшим разрушениям. Вот некоторые данные. При взрыве одного килограмма данного вещества выделяется в 2 раз больше тепловой энергии, чем при взрыве такого же количества тротила, а также в полтора раза больше, чем при взрыве одного килограмма нитроглицерина.

Области применения ацетилена
Ацетилен – это горючий газ, который используется при газовой сварке. Нередко его используют для кислородной резки. Стоит отметить, что температура горения смеси кислорода и ацетилена может достигать 3300°С. Благодаря этому свойству вещество чаще других используется при сварке. Ацетиленом обычно заменяют природный газ и пропан-бутан. Вещество обеспечивает производительность и высокое качество сварки.
Снабжение постов газом для резки и сварки может осуществляться от ацетиленового генератора или же от баллонов с ацетиленом. Для хранения данного вещества обычно используют емкости белого цвета. Как правило, на них присутствует надпись «Ацетилен», нанесенная красной краской. Стоит учесть, что существует ГОСТ 5457-75. Согласно данному документу для обработки металлов применяется технический растворенный ацетилен марки Б или же вещество в газообразном виде.

Сварка ацетиленом: проверка
Технология сварки данным газом достаточно проста. Однако при работе с веществом требуется терпение и внимательность. Для сварки обычно используют специальные горелки, с маркировкой 0-5. Ее выбор зависит от того, какой толщиной обладают свариваемые детали. Следует учесть, что чем больше размер горелки, тем больше расход.
Сварка ацетиленом осуществляется только после того, как оборудование будет проверено и отрегулировано. При этом следует обратить внимание на номер наконечника и номер подающей газ форсунки, которая располагается около рукоятки горелки под гайкой. Также следует проверить все уплотнения.

Процесс сварки
Применение ацетилена при сварке должно осуществляться аккуратно и в соответствии с определенными правилами. Для начала горелку следует продуть газом. Это нужно делать до тех пор, пока не появится запах ацетилена. После этого газ поджигается. При этом следует добавлять кислород, пока пламя не станет более устойчивым. Из редуктора на выходе давление ацетилена должно быть от 2 до 4 атмосфер, а кислорода – от 2 атмосфер.
Для сварки черных металлов требуется нейтральное пламя. Оно обладает четко очерченной короной и условно его можно разделить на три яркие части: ядро – ярко-голубой окрас с зеленоватым отливом, восстановленное пламя – бледно-голубого оттенка, факел пламени. Последние две зоны являются рабочими.
Перед началом работы все детали нужно очистить, а затем подогнать друг к другу. При работе с горелкой также применяют левый и правый способ. В последнем случае происходит медленное остывание шва. Присадочный материал, как правило, перемещается за горелкой. При левом способе повышается эластичность и прочность шва. В данном случае пламя направляется от места сварки. Присадочный материал следует вносить в сварочную ванну только после того, как переместится на следующую позицию горелка.

Правила безопасности
Применение ацетилена без навыков и опыта запрещено. Существует несколько правил, которые следует соблюдать при работе с веществом:
- Содержание ацетилена в помещении в воздухе необходимо постоянно контролировать. Для этого следует использовать специальные автоматические приборы, которые способны оповещать о превышении концентрации газа. Этот показатель не должен быть более 0,46 %.
- Области применения ацетилена совершенно разные, но чаще всего его используют при сварке. При работе с баллонами, наполненными именно этим газом, следует соблюдать осторожность. Запрещено размещать емкости вблизи открытого огня или же около отопительных систем. Помимо этого, запрещено работать с баллонами, которые находятся в горизонтальном положении, а также, если они не закреплены и неисправны.
- При работе с ацетиленом следует использовать исключительно неискрящиеся инструменты, электрическое оборудование и освещение во взрывобезопасном исполнении.
- Если происходит утечка ацетилена из баллона, то следует быстро закрыть вентиль емкости. Для этого можно использовать неискрящийся специальный ключ. Определить утечку можно лишь по звуку или же запаху.

Что делать, если возник пожар
Неправильное применение ацетилена может привести к печальным последствиям. Этот газ взрывается и приносит сильное разрушение. Что же делать, если возник пожар?
- При возникновении пожара следует незамедлительно убрать из опасной зоны все емкости, наполненные ацетиленом. Те баллоны, которые остались, следует постоянно охлаждать обычной водой или же специальным составом. Емкости должны полностью остыть.
- Если воспламенился газ, который выходит из баллона, то следует незамедлительно закрыть емкость. Для этого следует использовать неискрящийся ключ. После этого емкость необходимо остудить.
- При сильном возгорании тушение огня следует осуществлять только с безопасного расстояния. В такой ситуации стоит использовать огнетушители, наполненные составом, содержащим флегматизирующую концентрацию азота 70 % по объему, также диоксид углерода 75 % по объему, песок, струи воды, сжатый азот, полотно асбестовое и так далее.
fb.ru
Ацетилен в промышленности органического синтеза
В отличие от промышленности органического синтеза США, базирующейся главным образом на парафиновых и олефиновых углеводородах нефти, основным сырьем этой промышленности в Германии явился уголь и синтезируемые на его основе водяной газ и ацетилен. Производство на базе ацетилена пластических масс, синтетического каучука и заменителей смазочных масел из природной нефти, конечно, диктовалось принципами автар- [c.476]Почему именно ацетилен Всю первую половину нашего века в учебниках по органической химии можно бьшо увидеть ацетиленовое дерево — схему, на которой от ствола-ацетилена отходили многочисленные сучья, делившиеся затем на ветви и веточки различных синтезов. В общей сложности их число переваливало за 300. Практически всю промышленность органического синтеза [c.105]
Ацетилен служит сырьем для синтезов многочисленных органических соединений. На основе карбидного ацетилена возникла большая промышленность органического синтеза в тех странах, которые богаты углем — в первую очередь речь идет о Германии и Англии. Поскольку ацетилен довольно дорогое сырье, то в настоящее время всюду, где это возможно, его стремятся заменить этиленом, получаемым из нефти. [c.254]
Как видно из таблицы, пирогаз содержит значительные количества водорода и окиси углерода, которые можно перерабатывать в аммиак или метанол. Кроме них в пирогазе имеются такие ценные компоненты, как ацетилен и этилен, являющиеся важнейшим сырьем в промышленности органического синтеза. [c.453]
Сырьевая база промышленности органического синтеза тесно связана со структурой топливно-энергетического баланса отдельных регионов и стран. Преобладание угля в этом балансе создало в свое время сырьевую основу для производства химической продукции на коксохимических заводах и на базе ацетилена. С переходом энергетики и транспорта на преимуш,е-ственное использование нефти и газа ацетилен в большинстве промышленных процессов был вытеснен нефтехимическим этиленом, а источником получения ароматических углеводородов, помимо коксохимического производства, стала нефтепереработка. Современный этап развития промышленности органического синтеза определяется обычно как нефтехимический однако его можно называть и олефиновым . При мировом объеме производства продуктов в процессах тяжелого органического синтеза, равном 100 млн. т в год, мош ности по этилену достигают 50 млн. т в год [2]. [c.6]
Сроки и темпы перехода промышленного органического синтеза с угольного сырья на нефтегазовое и с ацетилена на низшие олефины в разных странах были не одинаковы. В странах Западной Европы, Японии и СССР преобладание низших олефинов в сырьевой базе отрасли стало заметным с 60-х гг. В США этилен и пропилен, полученные из газов крекинга при переработке нефти, применяли наряду с ацетиленом в химической промышленности уже в 20—30-е гг. [3], а современный процесс производства низших олефинов — термический пиролиз углеводородов с водяным паром — выделился из процессов нефтепереработки и превратился в основной промышленный метод получения этилена и пропилена в период 1920—1940 гг. Работы в области производства и химического использования нефтяного и газового сырья проводились в эти же годы и в СССР. Вскоре после окончания войны вступили в строй нефтехимические заводы в гг. Сумгаите, Грозном, Куйбышеве, Уфе, Саратове, Орске и других городах. На этих предприятиях синтетический этанол, изопропанол и ацетон вырабатывались на основе этилена и пропилена, полученных в процессе пиролиза углеводородного сырья [4]. [c.6]
В настоящее время комплексный процесс пиролиза бензина правомерно рассматривать как источник получения не только этилена, пропилена и фракции углеводородов С4, но целой гаммы первичных продуктов, представляющих большой интерес для промышленности органического синтеза. Известно, что в условиях жесткого пиролиза в относительно больших количествах образуются ацетилен, аллен (пропадиен) и метилацетилен, К качеству этилена сегодня предъявляются весьма высокие требования, в том числе — к содержанию в нем ацетилена. Очистить этилен от ацетилена можно, в принципе, двумя путями селективным гидрированием ацетилена или выделением его с помощью экстрактивной дистилляции. [c.368]
Выдающийся вклад в разработку многочисленных промышленных технологических процессов на основе ацетилена внес В Реппе Разработанные им способы получения разнообразных органических продуктов сделали ацетилен в 30-50-е годы XX столетия основным сырьевым источником промышленности органического синтеза На основе ацетилена получают в больших количествах уксусный альдегид, уксусную кислоту, уксусный ангидрид, этилацетат, хлористый винил, винилацетат, акрилонитрил, акрилаты, хлоропрен и др (см выше) [c.326]
Среди исходных алифатических продуктов, вырабатываемых в США из нефти и природного газа, первое место занимают этилен и пропилен. Значение их как сырья для промышленности органического синтеза непрерывно увеличивается. Ацетилен (54% которого в 1969 г. получали уже нефтехимическими методами), будучи дороже этилена и других [c.5]
Ацетилен ныне стал важнейшим исходным сырьем в промышленном органическом синтезе. [c.17]
Ацетилен является универсальным горючим для газопламенной обработки металлов и незаменим при выполнении многих работ ПО газовой сварке стали и др. Неуклонно расширяется также использование ацетилена в качестве исходного сырья для промышленного органического синтеза. В связи с этим за последние годы значительна увеличилось количество действующих ацетиленовых станций а во многих из них устаревшее оборудование заменено новым. [c.3]
Значение парафинов для промышленного органического синтеза еще более возрастает оттого, что из них получают ценные исходные вещества низшие олефины и ацетилен — методом пиролиза [c.31]
Даже этот краткий обзор дает представление о громадном значении, которое ацетилен как исходный материал приобретает в области промышленного органического синтеза. [c.414]
Этот способ применяют как в лабораториях, так и в промышленности, где он освоен еще в прошлом веке. Карбидный ацетилен послужил сырьем для промышленности органического синтеза в странах, богатых углем (Германия, Англия). Однако получение его требует больших затрат электроэнергии, вследствие чего карбидный ацетилен дорог и в последнее время он вытесняется другими способами получения ацетилена. [c.83]
Известен еще ряд реакций полимеризации ацетилена, в результате которых получается много технически ценных высокомолекулярных производных. Все это делает ацетилен одним из важнейших промежуточных продуктов для промышленности органического синтеза, особенно теперь, когда в результате создания мощных гидроэлектростанций стоимость карбида кальция стала низкой. [c.67]
Для промышленности органического синтеза важнейшими видами сырья являются
www.chem21.info
Газ ацетилен, физические свойства ацетилена, химические свойства ацетилена.
Продажа Производство ДоставкаГазообразный
Жидкий
Ацетилен — ненасыщенный углеводород C2H2. Имеет тройную связь между атомами углерода, принадлежит к классу алкинов.
Физические свойства
При нормальных условиях — бесцветный газ, малорастворим в воде, легче воздуха. Температура кипения −83,8 °C. При сжатии разлагается со взрывом, хранят в баллонах, заполненных кизельгуром или активированным углем, пропитанным ацетоном, в котором ацетилен растворяется под давлением в больших количествах.Взрывоопасный. Нельзя выпускать на открытый воздух. Частицы C2H2 есть на Уране и Нептуне.
Химические свойства
Ацетилено-кислородное пламя(температура «ядра» 3300 °C)
Для ацетилена (этина) характерны реакции присоединения:
HC≡CH + Cl2 -> СlСН=СНСl
Ацетилен с водой, в присутствии солей ртути и других катализаторов, образует уксусный альдегид (реакция Кучерова). В силу наличия тройной связи, молекулавысокоэнергетична и обладает большой удельной теплотой сгорания — 14000 ккал/м³. При сгорании температура пламени достигает 3300°С. Ацетилен можетполимеризироваться в бензол и другие органические соединения (полиацетилен, винилацетилен). Для полимеризации в бензол необходим графит и температура в 400 °C.
Кроме того, атомы водорода ацетилена относительно легко отщепляются в виде протонов, то есть он проявляет кислотные свойства. Так ацетилен вытесняет метаниз эфирного раствора метилмагнийбромида (образуется содержащий ацетиленид-ион раствор), образует нерастворимые взрывчатые осадки с солями серебра иодновалентной меди.
Ацетилен обесцвечивает бромную воду и раствор перманганата калия.
Основные химические реакции ацетилена (реакции присоединения, сводная таблица 1.):
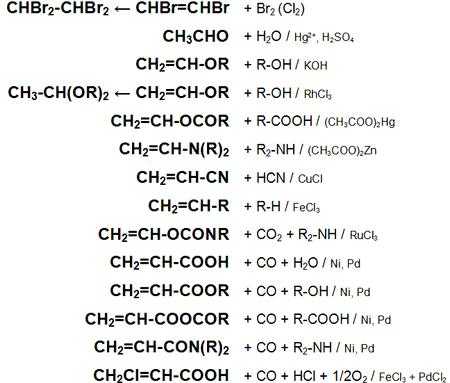
История
Открыт в 1836 г. Э. Дэви, синтезирован из угля и водорода (дуговой разряд между двумя угольными электродами в атмосфере водорода) М. Бертло (1862 г.).
Способ производства
В промышленности ацетилен часто получают действием воды на карбид кальция см. видео данного процесса (Ф. Вёлер, 1862 г.), а также при дегидрировании двух молекул метана при температуре свыше 1400° Цельсия.
Применение
Ацетиленовая лампа
Ацетилен используют:
- для сварки и резки металлов,
- как источник очень яркого, белого света в автономных светильниках, где он получается реакцией карбида кальция и воды (см. карбидка),
- в производстве взрывчатых веществ (см. ацетилениды),
- для получения уксусной кислоты, этилового спирта, растворителей, пластических масс, каучука, ароматических углеводородов.
Безопасность
Поскольку ацетилен растворим в воде и его смеси с кислородом могут взрываться в очень широком диапазоне концентраций, его нельзя собирать в газометры. Ацетилен взрывается при температуре около 500 °C или давлении выше 0,2 МПа; КПВ 2,3-80,7 %, температура самовоспламенения 335 °C. Взрывоопасность уменьшается при разбавлении ацетилена другими газами, например N2, метаном или пропаном. При длительном соприкосновении ацетилена с медью или серебром образуется взрывчатая ацетиленистая медь или ацетиленистое серебро, которые взрываются при ударе или повышении температуры. Поэтому при хранении ацетилена не используются материалы, содержащие медь (например, вентили баллонов). Ацетилен обладает слабым токсическим действием. Для ацетилена нормирован ПДКм.р. = ПДК с.с. = 1,5 мг/м3 согласно гигиеническим нормативам ГН 2.1.6.1338-03 “Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населенных мест”. ПДКр.з. (рабочей зоны) не установлен (по ГОСТ 5457-75 и ГН 2.2.5.1314-03), т.к. концентрационные пределы распределения пламени в смеси с воздухом составляет 2,5-100%. Хранят и перевозят его в заполненных инертной пористой массой (например, древесным углем) стальных баллонах белого цвета (с красной надписью «А») в виде раствора в ацетоне под давлением 1,5-2,5 МПа.
tgko.ru
Ацетилен в промышленности органического синтеза
из “Органическая химия Издание 3”
Ацетилен — эндотермическое соединение, для его образовани требуется затратить большое количество энергии при сжигани ацетилена выделяется много тепла (1300 кДж/моль). Температур кислородно-ацетиленового пламени 3000°С, т. е. выше температуры горения этилена и этана. При этой температуре часть ацетилена разлагается на элементы, образуя мельчайшие ярко светящиеся частицы. В XIX веке карбидные фонари использовали для освещения улиц, площадей. Фонари экипажей, велосипедов также работали на ацетилене. Кислородно-ацетиленовые горелки в настоящее время используют для сварки и резки металлов. При недостатке кислорода пламя ацетилена сильно коптит. [c.89]Ацетилен получают в промышленности в огромных количествах. Сырьевые источники ацетилена — уголь, природный газ нефть. [c.89]
Этот способ применяют как в лабораториях, так и в промышленности, где он освоен еще в прошлом веке. Карбидный ацетилен послужил сырьем для промышленности органического синтеза в странах, богатых углем (Германия, Англия). Однако получение его требует больших затрат электроэнергий, вследствие чего карбидный ацетилен дорог. [c.89]
В более новом способе исходят из метана, который превращают в ацетилен термическим крекингом или электрокрекингом-. [c.89]
Водород и оксид углерода используют для получения спиртов. Сырьем для крекинга и пиролиза служит природный газ или нефть. Получаемый таким образом ацетилен дешевле карбидного, однако очистка его — сложная, еще не решенная до конца задача. [c.91]
Ацетилен образуется при сухой перегонке многих органических веществ, всегда содержится в светильном газе каменноугольного происхождения (коксовый газ). На основе ацетилена развились многие отрасли промышленности органического синтеза. [c.91]
Большое значение в развитии химии ацетилена имеют работы советских ученых. Выдающаяся роль принадлежит здесь А. Е. Фаворскому (1860—1945 гг.) и его школе разработан новый (без-ртутный) способ получения уксусного альдегида, новые способы получения высокомолекулярных соединений — синтетического каучука, пластмасс, универсального клея (клей Назарова), лекарственных веществ (бальзам Шостаковского). Большой вклад в химию ацетилена внесли также работы Н. Д. Зелинского и Б. А. Казанского. [c.91]
Большой интерес представляют реакции ацетилена и ацетиленовых углеводородов с кетонами. Например, реакцией ацетилена с ацетоном можно получить изопрен, который является исходным продуктом для получения синтетического каучука. [c.91]
На схеме 2 (см. с. 90) приведены важнейшие промышленные синтезы на основе ацетилена. Необходимо отметить, что ряд химических продуктов, получаемых из ацетилена, можно синтезировать также из этилена, причем часто этот путь более экономичен. [c.91]
Вернуться к основной статье
www.chem21.info
Сфера и область применения ацетилена. Где применяется ацетилен.

Открыт несколько веков назад – ацетилен – остается одним из самых популярных органических соединений и сегодня. В быту его начали использовать еще в 20 веке, а сегодня этот углеводород востребован в разных отраслях промышленности и даже в медицине.
Что собой представляет ацетилен?
В нормальных условиях ацетилен представляет собой газ без запаха и цвета. При наличии примесей его запах становится неприятным и резким. Это вещество может находиться в твердом и жидком состоянии (если понизить температуру до – 85 градусов Цельсия, ацетилен становиться твердым). Сферы и области применения ацетилена настолько обширны благодаря его уникальным и ценным свойствам. К таким свойствам можно отнести то, что он способен взрываться. При попадании ацетилена на воздух и при наличии искры это происходит мгновенно. Именно поэтому ацетилен хранят в специальных баллонах.
Применение ацетилена в обработке металлов
Сегодня чаще всего ацетилен используется при газовой и автогенной сварке. Сварку совершают с помощью горячего пламени, образованного при работе ацетилено-кислородной горелки. Температура такого пламени может достигать 3000 градусов Цельсия и плавить даже листы стали. Такую сварку применяют и для пластмасс, в том числе и при ремонте автомобильных пластмассовых бамперов.
Огневая чистка ацетиленом позволяет получить металлическую поверхность без грязи и коррозии. Такой способ отлично очищает металл перед последующей обработкой. Пайка твердым припоем, при которой также используется данное соединение, позволяет соединять между собой материалы различной структуры.
Другие сферы применение ацетилена
Помимо сварки и обработки металлов ацетилен имеет множество других сфер применения, например, в различных отраслях промышленности. Химическая промышленность активно применяет ацетилен в органическом синтезе для производства таких веществ как уксусная кислота, технический углерод, этиловый спирт, каучук, пластмассы, растворители, лаки, взрывчатые вещества, органическое стекло. Помимо этого, раствор ацетилена в аммиаке используют в ракетной промышленности как ракетное топливо.
На протяжении всего прошлого века большой популярностью пользовались карбидные лампы, которые работали на основе ацетиленового пламени. Такими лампами оснащали кареты, автомобили и велосипеды. На сегодняшний день карбидные лампы утратили былую полярность, но их по-прежнему используют на кораблях дальнего плаванья и маяках, так как они работают без электричества и очень экономичны.
Статьи на схожую тематику:
– вес ацетилена
– вес пропан бутана
Ацетилен применяется даже в медицинских целях при ингаляционном наркозе. Применяют его не часто, так как на данный момент существуют более современные способы анестезии. Кроме этого, ацетилен обладает небольшой токсичностью и поэтому более безопасно стало использовать другие методы наркоза.
naruservice.com




