Кальция карбид структурная формула: Карбид кальция
alexxlab | 10.03.2023 | 0 | Разное
Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит)
Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит)
- ГОСТ 1460-81
- ТУ 6-01-1347-87
- Химическая формула: СаС2
- Описание Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит): Информация отсутствует.
Применение Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит): Карбид кальция применяется для получения цианамида, из которого получают удобрения, цианистые соединения, меламин, изанидин. Используют для получения карбидно-карбамидного регулятора роста растений, изготовления реагента карбидного порошкового. Карбид кальция используется для получения ацетилена. На основе ацетилена производят синтез многих важных органических продуктов: синтетический каучук, винилхлорид, акрилонитрил, этилен, стирол.
Купить в интернет-магазине
Упаковка Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит): Карбид кальция упаковывают в стальные барабаны массой нетто 120, 125 кг.
Хранение Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит): Карбид кальция хранят на открытых площадках под навесом или в несгораемых, хорошо проветриваемых складах, исключающих попадание влаги, в вертикальном положении, не более чем в три яруса. Совместное хранение с другими веществами и материалами не допускается. Гарантийный срок хранения продукта – 6 месяцев со дня изготовления.
Транспортирование Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит): Информация отсутствует.
Безопасность Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит): При взаимодействии с водой карбид кальция разлагается с выделением ацетилена и гидрата окиси кальция, при контакте с окислителями также выделяет ацетилен и разогревается.
Цена Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит): Низкая стоимость, а также скидки в зависимости от объема закупаемого товара.
Оформление и отгрузка Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит) : Благодаря отлаженной работе офиса и складов, мы предоставляем быстрое оформление и отгрузку товаров.
Доставка Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит): Мы предлагаем доставку товаров по России:
- автотранспортом;
- железнодорожными контейнерами, вагонами;
- через транспортные компании.
Для получения подробной информации о ценах на товары и условиях поставки звоните нашим специалистам по телефонам: (383) 279-12-43, 279-17-37, 279-16-30.
Также вы можете купить Карбид кальция (Углеродистый Кальций, Ацетиленид Кальция, Карбит) через интернет-магазин компании ОАО Реактив:
Заказать в интернет-магазине
Карбід кальцію – купити за найвигіднішою ціною в Києві від компанії “ТОВ Преміум Корк”
Визначення
Карбіди – хімічні сполуки які получаеются в результаті лужних реакцій вуглецю з металами. У більшості випадків виходять надтверді сплави, порівнянні за своїм твердостным характеристиками з алмазом.
У більшості випадків виходять надтверді сплави, порівнянні за своїм твердостным характеристиками з алмазом.
Найбільш широку популярність і поширення отримав сплав, званий карбід кальцію – хімічна формула сполуки CaC2
Коротко про історію
Карбід кальцію був вперше синтезований німецьким хіміком Фрідріхом Велером в 1862 р. Вчений намагався відокремити кальцій від вапна методом безперервного нагрівання суміші з вугіллям. А в результаті отримав масу блідо-сірого кольору без ознак металу. На початку двадцятого століття карбід кальцію був основним джерелом виробництва ацетилену у великих обсягах, тому виникла гостра необхідність в організації процесу масового виробництва.
Склад CaC2 (технічного) використовується для зварювальних робіт.
| ||||||||||||
| ||||||||||||
| ||||||||||||
| ||||||||||||
| ||||||||||||
| ||||||||||||
| ||||||||||||
| ||||||||||||
|
Особливості
Карбід кальцію, ацетилен – міцний елемент з кристалічною структурою. Від якості вихідної сировини залежить кінцевий тон: може варіюватися від блакитного до фіолетового, чорного. А також можлива присутність неприємного запаху з нотками часнику. Процес злиття з водою, розчинами мінеральних кислот, лугів протікає з виділенням великої кількості тепла, що має виробничу важливість.
Від якості вихідної сировини залежить кінцевий тон: може варіюватися від блакитного до фіолетового, чорного. А також можлива присутність неприємного запаху з нотками часнику. Процес злиття з водою, розчинами мінеральних кислот, лугів протікає з виділенням великої кількості тепла, що має виробничу важливість.
Техніка безпеки
Як вже зазначалося раніше, кальцій карбід – це вибухонебезпечну речовину і для дотримання безпеки в роботі з ним потрібно слідувати декільком обов’язковим умовам:
- створити герметичне місце зберігання і обробки;
- не допускати доступу джерела вогню;
- дрібні частинки (карбідна пил) викликають роздратування шкірних покривів, органів дихання, тому обов’язкова захисна одяг, респіратори;
- генератори ацетилену повинні розміщуватися в суворо ізольованих місцях;
- після закінчення зварювальних робіт обов’язково потрібно утилізувати невідпрацьовані шлаки в спеціальних місцях;
- при транспортировке и хранении нужно исключить возможность столкновения баллонов, емкостей, так как это несет смертельную опасность.

Карбид кальция – источник производства многих органических и неорганических соединений, которые широко используются в разных сферах жизни человека. Многие из них не имеют аналогов. Но, наряду с неисчерпаемой пользой этого вещества, не стоит забывать и о вреде, который он может нанести человечеству и экологии, ведь он относится к первому классу опасности, обладает взрыво и пожароопасными действиями.
Карбид кальция – определение, структура, формула, использование с часто задаваемыми вопросами
Здесь, в этой статье, мы обсудим карбиды, использование карбида, формулу карбида, что такое карбид кальция, использование карбида кальция, структуру карбида кальция. , реакция карбида кальция и воды, химическая формула карбида кальция и карбида алюминия и некоторые часто задаваемые вопросы, связанные с карбидами, будут обсуждаться здесь.
Карбид кальция Структура показана ниже.
Формула карбида кальция
Формула карбида кальция CaC 2 .
Читайте также –
- Решения NCERT для 11 класса по химии
- NCERT Решения для 12 класса по химии
- NCERT Решения для всех предметов
Что такое carb?
Карбид — один из наиболее важных терминов, который используется как в органической, так и в неорганической химии. Это химическое соединение, состоящее из углерода и металлических или полуметаллических элементов. Это ионная или ковалентная связь, которая соединяет карбидную группу с металлическими или полуметаллическими элементами.
Формула карбид-иона (C 4-), а дикарбид-иона (C -2 2 ). Он существует в ионной форме и означает, что ионы дикарбида состоят из двух атомов «С». Формула дикарбида (C -2 2 ) показывает, что он существует в дианионной форме. Среди различных карбидов значительную роль играют карбиды кремния, карбиды вольфрама из-за их физических свойств, таких как прочность, твердость и способность противостоять химическим воздействиям при высоких температурах.
Карбид алюминия (Al 4 C 3 ), карбид бериллия (Be 2 C), карбид кальция (CaC 2 ) и т. д. являются некоторыми примерами карбида. Карбид железа или также называемый (цементит) является важным компонентом стали и чугуна.
Общие свойства карбидов
Карбиды обычно обладают очень высокой температурой плавления.
Карбиды проводят тепло и электричество.
Карбиды представляют собой соединения с металлическим блеском.
Карбиды щелочных металлов обычно мягкие и прозрачные в чистом состоянии. Они легко разлагаются водой или кислотами с образованием алифатических углеводородов. Они не будут проводить электрический ток в твердом состоянии.
Все карбиды металлов чеканки оказались окрашенными и взрывоопасными порошками. Примеры: Cu 2 C 2 (темно-коричневый), Ag 2 C 2 (белый), Au 2 C 2 (желтый).

Карбиды щелочноземельных металлов разлагаются разбавленными кислотами или водой с образованием газообразного ацетилена и реагируют с N 2 .
Оксид магния восстанавливается такими карбидами до магния. Они также реагируют с NH 3 и Br 2 .
Получение карбидов
Различные типы карбида
В зависимости от связи между ионом карбида и металлическим элементом обычно выделяют следующие типы.
Ионные карбиды- Сочетание щелочных или щелочноземельных металлов с ионами карбидов приводит к образованию ионных карбидов. Сила электростатического притяжения связывает эти ионы. В этом типе карбидов существует огромная разница в электроотрицательности. CaC 2 является примером.

Ковалентные карбиды- Низкоэлектроположительные элементы, такие как «Si» и «B», объединяются с ионами карбида с образованием ковалентных карбидов. В карбидах этого типа существует небольшая разница в электроотрицательности. «SiC» (карборунд), B 4 C являются примерами.
Карбиды внедрения- Комбинация переходных металлов и молекул карбида образует карбиды внедрения. В этом типе карбида ионы карбида занимают междоузлия металлической решетки. ТиК тому пример.
Промежуточный карбид переходного металла – Эти типы карбидов также состоят из переходного металла и карбид-иона, и их размеры одинаковы. Карбид железа или известный как цементит (Fe 3 C) является примером.
Использование карбидов
Большинство карбидов очень твердые. Поэтому они используются в качестве абразивных инструментов, сверлильных и режущих инструментов.

Используются в качестве восстановителей в металлургии.
Al 4 C 3 используется для синтеза метана, тогда как CaC 2 используется для производства ацетилена.
Твердые сплавы также используются в качестве футеровки печей.
Карбид бора обычно используется для резки алмазов, изготовления ламп накаливания, а также для сверления отверстий в скалах.
Карбид вольфрама в настоящее время используется в ювелирном деле, а также в производстве различных хирургических инструментов.
Что такое карбид кальция?
Важное химическое соединение с формулой CaC 2 известно как карбид кальция или ацетилид кальция. Одним из его промышленных применений является то, что он используется для синтеза ацетилена и цианамида кальция.
В чистом виде оказывается бесцветным, но в любом случае куски технического сорта CaC 2 имеют серый или коричневый цвет и содержат CaC 2 . Остальная часть состоит из CaO, Ca 3 P 2 , CaS, Ca 3 N 2 , SiC и т. д.
CaC 2 в основном используется в производят ацетилен в карбидных лампах. Он также используется для синтеза различных химикатов и удобрений, а также участвует в производстве стали.
Приготовление
Карбид кальция синтезируют в промышленных масштабах с использованием электродуговой печи путем смешивания смеси кокса и извести при температуре . Это эндотермическая реакция, требующая 110 килокалорий на моль и очень высокой температуры для удаления CO.
Высокотемпературные условия, необходимые для производства CaC 2 , не могут быть достигнуты путем традиционного сжигания. Следовательно, эту реакцию следует проводить в электрической печи с использованием графитовых электродов.
Следовательно, эту реакцию следует проводить в электрической печи с использованием графитовых электродов.
Кроме того, учащиеся могут обратиться,
- Решения NCERT для класса 12 по химии Глава 10 Элементы S-блока
- NCERT Примеры решений для класса 12 по химии Глава 10 Элементы S-блока
- Глава 1 NCERTm0 примечания по химии Элементы S-Block
Применение карбида кальция
- Производство ацетилена: CaC 2 реагирует с водой с образованием ацетилена и гидроксида кальция.
Производство стали: CaC 2 используется при десульфурации железа, а также в качестве топлива в сталеплавильном производстве для увеличения доли брака в жидком чугуне.
Раскислитель: При ковшевой обработке действует как сильный раскислитель.

В качестве агента созревания: CaC 2 используется в качестве источника газообразного ацетилена, который действует как альтернативный агент созревания, как и этилен.
CaC 2 также используется для определения влажности почвы.
CaC 2 в настоящее время продается как средство от кротов.
Структура карбида кальция
Обычная кристаллическая форма CaC 2 при комнатной температуре представляет собой искаженную структуру каменной соли, в которой единицы C -2 2 лежат параллельно. Это может быть показано как:
Также проверьте-
- NCERT IMEMPLAR CLASS 11TH DELITUTIONS
- NCERT IMEPRAR CLASS 12th Chemistry Solutions
- NCERT Примечание.

- NCERT Примечания для всех субъектов
Карбид кальция – структура, производство, применение и часто задаваемые вопросы
Перейти к содержимому
Что такое карбид кальция?
Карбид кальция – Структура: Карбид кальция представляет собой неорганическое соединение с химической формулой CaC2. Это бесцветное твердое вещество, мало растворимое в воде. Его получают реакцией извести и сажи. Это бесцветное твердое вещество, которое используется в производстве газообразного ацетилена и различных других химических веществ. Он образуется в результате реакции оксида кальция и углерода.
Зарегистрируйтесь, чтобы получить бесплатные тестовые и учебные материалы
+91
Подтвердите OTP-код (обязательно)
Я согласен с условиями и политикой конфиденциальности.
Структура и связь CaC2
Молекула карбоната кальция (CaCO3) состоит из одного атома кальция и трех ионов карбоната.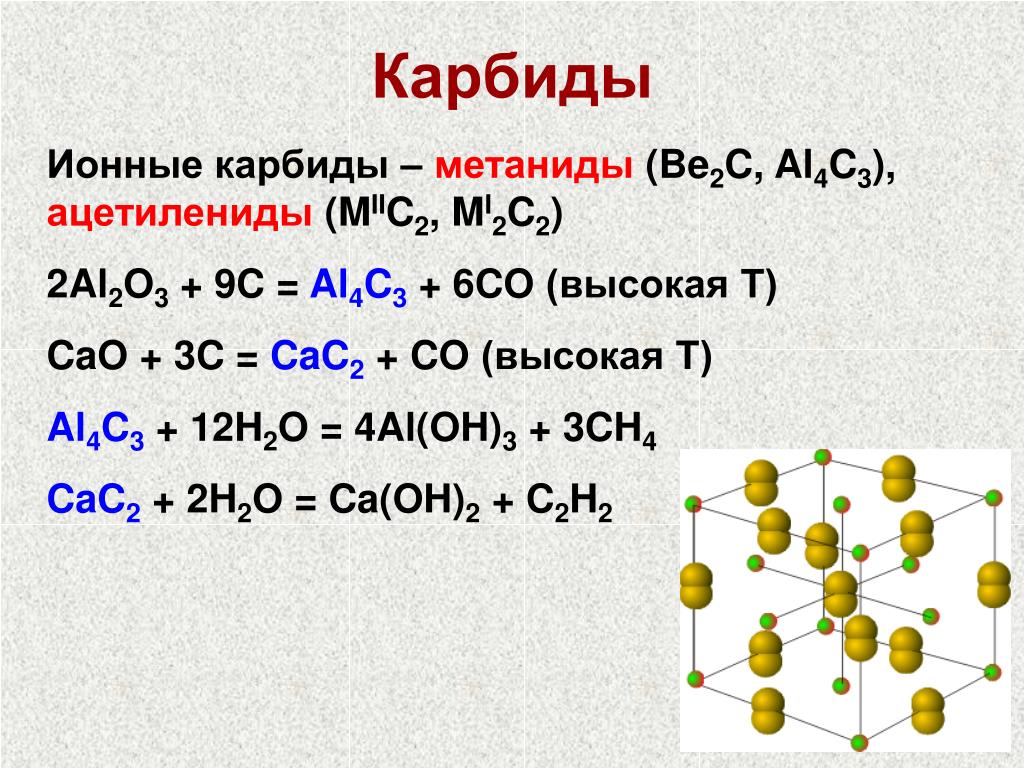 Атом кальция окружен шестью атомами кислорода в октаэдрической геометрии. Каждый карбонат-ион окружен четырьмя атомами кислорода в тетраэдрической геометрии. Атом кальция и ионы карбоната удерживаются вместе ковалентными связями.
Атом кальция окружен шестью атомами кислорода в октаэдрической геометрии. Каждый карбонат-ион окружен четырьмя атомами кислорода в тетраэдрической геометрии. Атом кальция и ионы карбоната удерживаются вместе ковалентными связями.
Производство карбида кальция
Карбид кальция представляет собой химическое соединение с химической формулой CaC2. Это серый, твердый, легковоспламеняющийся материал, который получают путем нагревания оксида кальция и углерода в печи.
Карбид кальция представляет собой неорганическое соединение с химической формулой CaC2. Это бесцветный газ без запаха, легковоспламеняющийся. Это полезный материал в производстве газообразного ацетилена.
Карбид кальция получают реакцией оксида кальция и углерода.
2CaO(т) + 3C(т) → CaC2(г) + CO2(г)
Затем карбид кальция реагирует с водой с образованием газообразного ацетилена.
CaC2(г) + 2h3O(ж) → C2h3(г) + Ca(OH)2(водн.)
Производство цианамида кальция
- Цианамид кальция получают из оксида кальция и аммиака.
 Оксид кальция реагирует с аммиаком с образованием цианамида кальция и воды.
Оксид кальция реагирует с аммиаком с образованием цианамида кальция и воды. - Цианамид кальция представляет собой неорганическое соединение с химической формулой CaCN2. Это бесцветное твердое вещество, растворимое в воде. Он производится в промышленных масштабах путем реакции карбида кальция с газообразным азотом.
- Реакция карбида кальция с газообразным азотом приводит к образованию цианамида кальция и карбидного шлака. Карбидный шлак представляет собой отходы, содержащие карбонат кальция и карбид кремния.
- Цианамид кальция используется в качестве удобрения и нетоксичного пестицида. Он также используется в производстве азотной кислоты.
Использование карбида кальция (CaC2)
Карбид кальция используется в производстве газообразного ацетилена, который является топливом, используемым при сварке и резке металлов. Он также используется в производстве других химических веществ, в том числе цианамида кальция, который используется в сельском хозяйстве для производства удобрений.

