Карбид вода: Что такое карбид кальция и какой газ он выделяет?
alexxlab | 20.06.1984 | 0 | Разное
Школьные и дворовые игры Брянска. Часть 4. Опасные игры
Здесь преимущественно даже не игры, а всякие пацанские забавы. Иногда потенциально опасные, но о-о-очень заманчивые!
Автор: Дмитрий Радченко, Шеф-редактор
Отдых и развлечения
Карбид
Карбид, как много в этом звуке… Многие до сих пор проходя мимо работающего ацетиленового сварочного генератора и уловив ноздрями знакомый до боли запах, испытывают непреодолимое желание подождать, когда мужики будут вытряхивать корзинку с остатками карбида.
Два основных способа применения карбида:
Карбид клали в баллончик из-под Дихлофоса. Баллончик аккуратно освобождали от верхушки — нужно было разогнуть завальцовку, сзади пробивали гвоздём дырку. В баллон клали карбид. Сзади, через дырочку, поджигаешь, а спереди — пламя и ба-бах!
Обычная стеклянная бутылка. Туда немного воды. Сверху напихивается трава. На траву засыпаются кусочки карбида. Важно, чтобы карбид не упал в воду. Бутылку затыкаем пробкой максимально плотно (можно использовать винтовую от водки). После этого бутылку бросают или просто заваливают на бок и прячутся. Карбид приходит во взаимодействие с водой — ба-бах! Что характерно, винные и водочные бутылки обычно разрывались, осколки летели в разные стороны. А вот бутылки от шампанского были многоразовыми. Из них только пробка вылетала.
Важно, чтобы карбид не упал в воду. Бутылку затыкаем пробкой максимально плотно (можно использовать винтовую от водки). После этого бутылку бросают или просто заваливают на бок и прячутся. Карбид приходит во взаимодействие с водой — ба-бах! Что характерно, винные и водочные бутылки обычно разрывались, осколки летели в разные стороны. А вот бутылки от шампанского были многоразовыми. Из них только пробка вылетала.
Крякалка (Пугач)
Альтернатива сегодняшним петардам. Трубка медная (из форсунок или холодильника) с одной стороны плющилась и загибалась, туда заливалось немного свинца. С другой стороны вставлялся затупленный гвоздь соответствующей толщины, он с одной стороны тоже загибался. На загнутые края трубки и гвоздя надевалась резинка желательно от камеры велосипеда. О края трубки нарезали серу от спичек, тромбовали гвоздём. Натягивали резинкой гвоздь под небольшим углом относительно трубки, потом снизу пальцем нажимали на резинку или слегка ударяли шляпкой гвоздя о подоконник и ба-бах!
Ракетки
Газета пропитывалась в насыщенном растворе селитры, сушилась, туго сворачивалась, заматывалась в фольгу. Дырочку в торце, туда такой же фитиль. Поджигалось, запускалось. Задача была вовремя ее кинуть, чтобы в руках не долбанула. Особо крутые делали ракету из картонной трубки с обтекателем из пробки от шампанского или вина, запускали с рейки.
Дырочку в торце, туда такой же фитиль. Поджигалось, запускалось. Задача была вовремя ее кинуть, чтобы в руках не долбанула. Особо крутые делали ракету из картонной трубки с обтекателем из пробки от шампанского или вина, запускали с рейки.
Некоторые ходили на «Цветмет», выносили оттуда кусок самолётного пропеллера, истирали напильником, покупали в аптеке еще один ингредиент… Тогда марганец копейки стоил. На старом аэропорту (вход под забором со стороны областного ГАИ) можно было найти много подходящих деталек. А селитруха использовалась только как фитиль. Как вспоминает один из испытателей, «Я однажды захотел супер-ракету сделать, и всю трубку, до обтекателя (не из пробки — конус из бумаги клеил) забил смесью. Жахнуло так, что полдня перед глазами зеленый круг стоял».
Примечание: Почему-то лучше всего для изготовления «селитрухи» подходила «Пионерская правда». Бумага у неё была специфическая. Благо, проблем с сырьём не было – газету должен был выписывать каждый пионер СССР.
Ножички
Одним названием назывались как минимум три совершенно разные игры.
Ножички на земле (Землерез, Земельки):
Чертили на земле большой круг, который делили на секторы. Хозяин каждого сектора должен стоя на своей земле так метнуть ножичек в сектор соседа, чтобы прямая, проведённая по линии входа лезвия в землю, разделила соседский сектор на 2 части, одна из которых переходила к метавшему. Таким образом, если у тебя всё время отрезают землю, а ты себе ничего не завоёвываешь, в конце концов ты не сможешь стоять на своём секторе — не поместишься. Значит — проиграл!
Ножички на деревянной скамейке:
Игра идёт на очки. Перочинный нож складывешь вполовину. Острие втыкаешь в лавку, а рукоять подсекаешь снизу. Ножик должен крутнуться в воздухе и воткнуться. Если в результате броска рукоятка не упиралась в лавку, что стоило 10 очков, а повисала в воздухе — это было круто. Тогда расстояние от плоскости до рукояти мерили пальцами. Каждый палец — 10 очков. А уж если ножик лёг на рукоять лезвием вверх — это уже почти победа.
Ножички с коленки:
Этот, пожалуй, самый технически сложный вариант, запечатлён на фото. Игроки должны воткнуть нож в землю не просто так, а с коленки, с локтя, с плеча, с носа, с макушки… Требует особого мастерства и длительных тренировок.
Игроки должны воткнуть нож в землю не просто так, а с коленки, с локтя, с плеча, с носа, с макушки… Требует особого мастерства и длительных тренировок.
Мертвец
Становишься к стенке, набираешь воздух в легкие и задерживаешь. В это время пара корешей тебе со всей силы давят на грудь. Секунд на 10 теряешь сознание и сползаешь по стене.
Термитники
Перфорированная трубочка из тонкой-тонкой жести, а на конце — маленькая твёрдая чёрная шайбочка. Долго греешь её на спичке, и, наконец, она сама загорается, делается яркой-яркой, слепяще-яркой. И тогда — бац об стену, и мелкие брызги — что твои звезды — в разные стороны!
Мы, уже взрослые, так и не смогли выяснить изначальное предназначение этих штук. Известно только, что брянские пацаны их воровали на «Чермете». Они там связками валялись.
* * *
Читайте также:Дворовые игры Брянска. Старые, но не забытые
Из соображений безопасности наших юных неподготовленных читателей мы не приводим весь известный нам перечень способов взорвать этот беззащитный мир с помощью подручного материала.
Основной материал (часть 1)
Часть 2. Игры с реквизитом
Часть 3. Игры для большой толпы
Часть 5. Азартные игры
Часть 6. Идиотские игры
Карбид алюминия, химические свойства, получение
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
KrКриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t° кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИрридийИрридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Новый пористый материал помогает получить возобновляемую энергию из воды
2086
Добавить в закладки
Одним из перспективных источников возобновляемой энергии является газообразный водород, получаемый из воды с помощью солнечного света. Исследователи из Университета Линчёпинга (Швеция) разработали материал – нанопористый кубический карбид кремния, – который может впитывать солнечную энергию и расщеплять молекулы воды для получения газообразного водорода, передает пресс-служба вуза. Статья с результатами исследования опубликована в журнале ACS Nano.
Плотность энергии водорода в три раза выше, чем у бензина. Его
можно использовать для выработки электроэнергии с помощью
топливных элементов. К тому же, на рынке уже есть автомобили,
работающие на водороде. Тем не
менее, производство водорода – процесс не очень
экологичный: в результате образуется диоксид углерода,
поскольку технология для его получения, которую используют
сегодня, зависит от ископаемого топлива. Так, при производстве
одной тонны газообразного водорода выделяется 9-12 тонн
углекислого газа.
Тем не
менее, производство водорода – процесс не очень
экологичный: в результате образуется диоксид углерода,
поскольку технология для его получения, которую используют
сегодня, зависит от ископаемого топлива. Так, при производстве
одной тонны газообразного водорода выделяется 9-12 тонн
углекислого газа.
Производство газообразного водорода путем расщепления молекул воды с помощью солнечной энергии – экологически более безопасный подход: в данном случае не выделяется углекислый газ. При этом, полученные топливо можно хранить.
«Обычные солнечные элементы производят энергию в дневное время, и эту энергию необходимо либо использовать немедленно, либо накапливать, например, в батареях. Водород является многообещающим источником энергии, который можно хранить и транспортировать так же, как традиционные виды топлива, такие как бензин и дизельное топливо», – отмечают авторы работы.
Однако разделить воду, используя энергию солнечного света, для
получения газообразного водорода – непростая задача. Чтобы
добиться успеха, необходимо найти экономичные материалы, которые
обладают правильными свойствами для реакции, в которой вода (h3O)
расщепляется на водород (h3) и кислород (O2) посредством
фотоэлектролиза. Энергия солнечного света, которую можно
использовать для расщепления воды, поступает в основном в виде
ультрафиолетового излучения и видимого света. Следовательно,
требуется материал, который может эффективно поглощать такое
излучение для создания зарядов, которые могут быть разделены и
иметь достаточно энергии для разделения молекул воды на водород и
кислород. Большинство материалов, которые были исследованы до сих
пор, либо неэффективны в том, как они используют энергию видимого
солнечного света (например, диоксид титана поглощает только
ультрафиолетовый солнечный свет), либо не обладают свойствами,
необходимыми для разделения воды на газообразный водород
(например, кремний).
Чтобы
добиться успеха, необходимо найти экономичные материалы, которые
обладают правильными свойствами для реакции, в которой вода (h3O)
расщепляется на водород (h3) и кислород (O2) посредством
фотоэлектролиза. Энергия солнечного света, которую можно
использовать для расщепления воды, поступает в основном в виде
ультрафиолетового излучения и видимого света. Следовательно,
требуется материал, который может эффективно поглощать такое
излучение для создания зарядов, которые могут быть разделены и
иметь достаточно энергии для разделения молекул воды на водород и
кислород. Большинство материалов, которые были исследованы до сих
пор, либо неэффективны в том, как они используют энергию видимого
солнечного света (например, диоксид титана поглощает только
ультрафиолетовый солнечный свет), либо не обладают свойствами,
необходимыми для разделения воды на газообразный водород
(например, кремний).
Как альтернативу, ученые использовали карбид кремния (3C-SiC). Группа создала кубический карбид кремния с очень маленькими
порами. Материал обладает многообещающими свойствами,
которые позволяют предположить, что его можно использовать для
производства газообразного водорода из воды с помощью солнечного
света. Этот новый пористый материал может эффективно собирать
ультрафиолет и большую часть видимого солнечного света. Кроме
того, пористая структура помогает разделять заряды, обладающие
необходимой энергией, в то время как небольшие поры обеспечивают
большую активную площадь поверхности. Это улучшает перенос заряда
и увеличивает количество реакции, поэтому молекулы воды
разделяются на водород и кислород быстрее.
Группа создала кубический карбид кремния с очень маленькими
порами. Материал обладает многообещающими свойствами,
которые позволяют предположить, что его можно использовать для
производства газообразного водорода из воды с помощью солнечного
света. Этот новый пористый материал может эффективно собирать
ультрафиолет и большую часть видимого солнечного света. Кроме
того, пористая структура помогает разделять заряды, обладающие
необходимой энергией, в то время как небольшие поры обеспечивают
большую активную площадь поверхности. Это улучшает перенос заряда
и увеличивает количество реакции, поэтому молекулы воды
разделяются на водород и кислород быстрее.
[Фото: THOR BALKHED/LIU]
Автор Материал Оформила Татьяна Матвеева
альтернативное топливо альтернативные источники энергии вода водород возобновляемая энергетика карбид кремния нанопористый кубический карбид кремния солнечная энергия
Источник:
liu. se
se
Информация предоставлена Информационным агентством “Научная Россия”. Свидетельство о регистрации СМИ: ИА № ФС77-62580, выдано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций 31 июля 2015 года.
НАУКА ДЕТЯМ
На юго-западе Китая найдена древнейшая окаменелость гиббона
17:00 / Биология
«Черные лебеди» и «драконы»: изменение арктического климата ведет к экстремальным осадкам
16:20 / География, Климат
Ученые готовят стандарты отечественных сортов цитруса
14:10 / Биология
Встреча кандидата в президенты РАН академика Геннадия Красникова с учеными отделения медицинских наук РАН
14:00 / Здравоохранение, Медицина
Превосходство в квантовых технологиях выведет экономику РФ на качественно новый уровень, ― академик Г.Я. Красников
13:20 / Наука и общество, Новые технологии, Физика
Ученые создали материал для минерализации костей и зубов
13:10 / Медицина
14. 09.22. Пресс-конференция онколога академика Андрея Каприна
09.22. Пресс-конференция онколога академика Андрея Каприна
13:00 / Здравоохранение, Медицина
Исследование ученых ВИР: когда свекла краснее и какая?
12:07 / Биология
Урожаи Дальнего Востока. Лекция члена-корреспондента РАН Татьяны Асеевой
10:30 / Биология, История, Климат, Науки о земле
«Марсианской тройке» — 35 лет. В ИКИ РАН обсудили результаты работы российских ядерно-физических приборов ХЕНД, ДАН и ФРЕНД
10:05 / Космология, Космонавтика, Эксперименты
Памяти великого ученого. Наука в глобальном мире. “Очевиднное – невероятное” эфир 10.05.2008
04.03.2019
Памяти великого ученого. Нанотехнологии. “Очевидное – невероятное” эфир 3.08.2002
04.03.2019
Вспоминая Сергея Петровича Капицу
14.02.2017
Смотреть все
Карбид. Применение и безопасность. Особенности при сварки
Карбид кальция CaC2 – одно из самых узнаваемых химических веществ, знакомых каждому со школьных времен. Этот щелочной элемент всегда привлекал внимание исследователей своими необычными свойствами.
Этот щелочной элемент всегда привлекал внимание исследователей своими необычными свойствами.
Если опустить его в воду – начинается химическая реакция, в ходе которой в больших количествах выделяется ацетилен. Этот эффект применяется при проведении газосварочных работ, когда карбид используется как горючий материал. Дело в том, что ацетилен при его смешении с кислородом сгорает с выделением огромного количества энергии. При этом температура достигает 3150°C, что выше точки плавления большинства известных металлов и сплавов.
Материал позволяет сваривать не только обычную, но и нержавеющую сталь, а также многие другие цветные металлы, включая алюминий. Этим газовая сварка выгодно отличается от электродуговой, для проведения которой необходимы дорогие электроды.
Особенности химического планаПри знакомстве с карбидом также следует уделить внимание его химическим особенностям:
- Материал имеет свойство впитывать влагу (при этом наблюдается активная химическая реакция, сопровождающаяся разложением вещества).

- Летучие составляющие, образующиеся в результате взаимодействия с водой, способны вызвать раздражение кожи и слизистых.
- При сильном нагревании кристаллы карбида взаимодействуют с рядом других веществ, образуя карбонат кальция (например, при их соединении с азотом, получаем цианамид кальция).
В нагретом состоянии карбид вступает в реакцию с такими химическими элементами, как фосфор, мышьяк и хлор. Из-за активного выделения опасных для людей, составляющих при работе с ним используются средства защиты дыхательных путей.
Физические характеристикиПри выборе любого материала особое внимание уделяется его физическим свойствам. В данном случае такие характеристики:
- Хранится в виде кусков различного размера и имеет ярко выраженную кристаллическую структуру.
- Температура плавления карбида составляет около 2300°C, свойственна только чистому карбиду.
- Температура плавления зависит от наличия или отсутствия добавок.
 Добавление к нему ряда примесей существенно снижает этот показатель.
Добавление к нему ряда примесей существенно снижает этот показатель.
Также отмечается, что карбид кальция чаще всего встречается в твердом состоянии, а его цветовой оттенок варьируется от серого до коричневого. Перечисленные свойства карбида позволяют использовать его в различных отраслях промышленного производства.
Области примененияОбластей, в которых применяется этот сырьевой материал, достаточно много. Но самой важной из них считается синтез производных в промышленных масштабах. Чаще всего карбид кальция востребован при производстве следующих химических веществ:
- Каучук синтетический.
- Известная всем домохозяйкам уксусная кислота.
- Растворители (например, ацетон).
- Полимеры, включая винилхлорид
Это сырьевой материал используется и при изготовлении цианамида кальция, получаемого в результате нагрева смеси с азотом. Материал ценен также тем, что участвует в качестве составляющей при синтезе многих видов с/х удобрений.
Специалистам сельского хозяйства хорошо известен карбамидный регулятор, используемый для стимуляции роста многих растений. Одна из основных компонентов этого состава – карбид кальция. Без него практически невозможно обойтись и при восстановлении целого ряда щелочных металлов. И, наконец, этот уникальный компонент широко применяется при газосварке в качестве сырья, используемого для получения ацетилена.
Особенности применения при сваркеИспользуемый для сварки материал хранится в специальных емкостях из стали с рабочим объемом 100 или 130 литров. При его извлечении должны соблюдаться меры предосторожности, защищающие человека от отравления и ожогов. Перед применением вещества для сварки потребуется ознакомиться со следующими особенностями этих процедур:
- Ацетилен для сварки вырабатывается в специальных генераторах с фиксированным объемов загрузки карбида.
- Емкость баков ацетиленовых генераторов обеспечивает прием от 5 до 15 литров воды и 2-5 килограммов исходного сырья.
- Полезный выход ацетилена составляет около 260-280 литров, получаемых из килограмма CaC2.
Еще до начала сварочных работ потребуется ознакомиться с принципом использования карбида в заявленных целях.
Последовательность работПорядок проведения основных рабочих операций, позволяющий понять, что происходит с карбидом в генераторах ацетилена:
- Перед загрузкой карбид и вода подготавливаются в количествах, достаточных для получения нужного объема ацетилена.
- Затем он в автоматическом режиме в заранее просчитанных дозах загружается в газовую камеру.
- При поступлении очередной порции вещества в результате начавшейся реакции внутреннее давление в камере резко возрастает.
- Но со временем оно снижается, что объясняется активным выпуском готового ацетилена в рабочую камеру.
- Затем он через специальный отвод поступает в газовую горелку, установленную на значительном удалении от генератора (согласно требованиям ТБ – до 10 метров).

- На заключительном этапе образующаяся гашеная известь (порядка 1,2 кг), удаляется через разгрузочное отверстие.
В генераторах, используемых при проведении работ ненормируемых объемов, материал опускается в воду в корзинах особого типа. Важно отметить, что полезный «выход» получаемого ацетилена (его объем) регулируется путем изменения глубины погружения корзины.
Вес оборудования и транспортировкаОсновное достоинство исходного сырья, используемого для газовой сварки – низкий вес необходимого для его переработки оборудования и самого материала. Единственный минус этого процесса – слишком тяжелые баллоны под ацетилен, которые приходится перемещать на специальной тележке.
При небольших расстояниях до места складирования можно обойтись без нее (с привлечением одного или двух помощников). Типовой генератор ацетилена весит порядка 15-20 кг, что позволяет при необходимости без труда перемещать его в нужное место самостоятельно.
Техника безопасностиКак уже отмечалось, карбид относится к токсичным и взрывоопасным веществам, угрожающим здоровью человека.
 Избежать неприятных ситуаций при работе с ним поможет строгое соблюдение следующих требований ТБ:
Избежать неприятных ситуаций при работе с ним поможет строгое соблюдение следующих требований ТБ:- Работы с этим материалом проводятся на безопасных удалениях от открытого огня, способного стать причиной взрыва газа.
- Не допускается использовать сырье в небольших гранулах с размерами до 2 мм или в виде карбидной пыли.
- Запрещается работать с электроинструментом типа «болгарка«, а также со сварочным электрооборудованием вблизи от места хранения или применения карбида.
- Его допускается хранить в плотно закрываемых емкостях в местах, удаленных от водопроводных и газовых магистралей.
- Открывать баки разрешается только с помощью киянки или специального зубила из латуни, не образующих искр.
- Карбид, оставшийся после завершения реакции, обязательно закрывается крышкой, непроницаемой для воды.
- При работе в закрытых помещениях в них не должно находиться горючих материалов и подобных им веществ.
- В случае попадания мелких частиц в глаза или на слизистые нужно промыть их теплой водой, после чего останется удалить остатки с помощью влажного тампона.

Также оговаривается удаленное размещение имеющихся в комнате сварочных аппаратов и наличие эффективной системы вентиляции, обеспечивающей быстрый отвод горючих газов.
Требования ТБ, предъявляемые к оборудованиюПри обращении со специальным оборудованием по производству ацетилена обязательно выполняются следующие требования:
- Генератор ацетилена обязательно располагается в строго вертикальном положении, а установленный на нем манометр должен просматриваться из любого положения оператора.
- Раствор карбида, остающийся в бункерах генератора, обязательно вырабатывается до конца, а получившаяся в результате известь утилизируется.
- Повторная загрузка отсыревших кусков в бункеры оборудования не допускается.
- Категорически запрещается останавливать процесс и вскрывать генераторное устройство, если текущие реакции не завершены.
Добавим, что баллоны для ацетилена должны иметь в своем комплекте специальные предохранительные колпачки, защищающие клапаны. Соблюдение всех перечисленных требований позволит избежать серьезных травм и повреждений как у работающего персонала, так и у находящихся поблизости людей.
Соблюдение всех перечисленных требований позволит избежать серьезных травм и повреждений как у работающего персонала, так и у находящихся поблизости людей.
Сырье получения ацетилена рекомендуется покупать в специализированных магазинах, занимающихся продажей соответствующих материалов. Приобретение некачественного товара в других местах нередко приводит к ситуации, когда сварочные работы оказываются под угрозой срыва.
Карбид можно заказать и приобрести в Интернет магазинах, где его цена не слишком высока и устроит большинство покупателей. В заключение отметим, что если возникла необходимость в постоянном получении ацетилена – лучше всего заказывать оптовые партии этого вещества, что обойдется заметно дешевле разовых розничных закупок.
Похожие темы:
- Плазма. Свойства и получение. Применение и отличие. Особенности
особенности вещества и его применение в сварке
Многие люди не понаслышке знают, что такое карбид натрия или кальция. В 80-х годах даже крохотный кусок этой твердой коричневатой или серой субстанции считался огромным богатством, особенно для маленьких детей, которые так любили с ним играться. Все дело в том, что при контакте с водой вещество вступает в термическую реакцию, выделяя дым. Запах карбида напоминает аромат чеснока.
В 80-х годах даже крохотный кусок этой твердой коричневатой или серой субстанции считался огромным богатством, особенно для маленьких детей, которые так любили с ним играться. Все дело в том, что при контакте с водой вещество вступает в термическую реакцию, выделяя дым. Запах карбида напоминает аромат чеснока.
- Карбид кальция в сварке
- Особенности применения
- Требования безопасности
Карбид кальция в сварке
Для сварочных работ карбид является чуть ли не идеальным веществом, потому что при взаимодействии с водой выделяет в окружающее пространство летучий газ ацетилен, который служит основой металлизации, напайки, кислородной сварки и множества иных процессов, относящихся к обработке металлических сплавов.
Создается этот состав при очень высокой температуре (до 2400 градусов) посредством расплавления негашеной извести и кокса внутри электродуговой печки. Затем раскаленное жидкое вещество помещается в специальные формы (изложницы), где оно застывает и твердеет. Затем карбид раскалывают на кусочки размером не более 8 см. В итоге полученная субстанция будет состоять примерно на 78% из карбида кальция, а остальные 22% — это известковые окиси, примеси и иные вещества.
Затем карбид раскалывают на кусочки размером не более 8 см. В итоге полученная субстанция будет состоять примерно на 78% из карбида кальция, а остальные 22% — это известковые окиси, примеси и иные вещества.
Так как при воздействии воды карбид выделяет большое количество ацетиленового газа и тепловой энергии, это существенно затрудняет его хранение. Чтобы избежать порчи вещества, его нередко укладывают в герметичные стальные резервуары. При открытии этих металлических сосудов необходимо избегать открытого пламени и искр, иначе могут быть печальные последствия.
Карбидная пыль (частички до 2 мм) непригодна для применения, потому что растворяется в воде практически моментально. Кроме того, при хранении большого количества пыли увеличивается риск, что применение состава в итоге приведет к взрыву резервуара. Специалисты отмечают, что килограмм рассматриваемого вещества способен выделить при взаимодействии с водой более 260 кубических дюймов ацетилена.
Карбид часто используется для газовой резки и сварки. При горении ацетилен контактирует с кислородом и достигает температуры 3150, что делает этот газ совершенно незаменимым при обработке тугоплавких металлических сплавов. В целях безопасности ацетилен делают в особых генераторах на основе угля, нефти, природного газа или карбида кальция.
Особенности применения
В сварке это вещество используют везде. Делают это по следующей схеме:
- Кусочки карбида помещаются в корзинку. Оптимальный размер элементов — 8 см. Такие «камешки» смогут обеспечить оптимальную выработку ацетиленового газа. Специалисты не советуют насыпать в генератор карбидную пыль. Частички менее 2 мм в диаметре почти мгновенно выделяют ацетилен, что может привести к взрыву оборудования.
- Корзину ставят в специальный резервуар с водой. Его горловину нужно закрыть плотной крышкой с винтовым креплением.
- Посредством вращения винтового маховика корзина с кусками вещества погружаются в воду, начинается генерация ацетиленового газа.
 Уменьшая/увеличивая глубину погружения корзины можно регулировать интенсивность выработки ацетилена, поддерживая в горелке устройства для сварки оптимальную интенсивность.
Уменьшая/увеличивая глубину погружения корзины можно регулировать интенсивность выработки ацетилена, поддерживая в горелке устройства для сварки оптимальную интенсивность.
Карбид при сварочных работах выполняет функции топлива, насыщающего генератор газа. И без его применения будет трудно применять ацетиленовую горелку. Ведь газовый баллон очень нелегко перемещать. А карбидные кусочки достаточно положить в герметичный сосуд и транспортировать на совершенно любые расстояния, предотвратив появление влаги.
Требования безопасности
В связи с тем, что это опасный материал, работать с ним нужно, строго соблюдая правила безопасности. Основные правила, которые обязательно должны выполнять при сварке с помощью карбида:
- Не забывайте, что карбид очень активно реагирует на воздействие воды и воздуха.

- Хранить вещество необходимо исключительно в герметичном и сухом месте.
- Вещество является очень взрывоопасным, потому открытое пламя и искры возле него категорически запрещены.
- Карбидная пыль может вызвать раздражение слизистых и кожного покрова, потому при работе с ней нужно обязательно пользоваться защитными очками, перчатками и респиратором.
- Монтаж ацетиленовых генераторов запрещено в подвалах.
- После окончания сварки с помощью карбидных кусочков, нужно «доработать» остатки вещества в генераторы. Полученные шлаки следует помещать в специальный бункер или яму.
- Также запрещено курить при работе с этим материалом.
- Точки и удары при перевозке баллонов с газом крайне опасны и могут привести к трагическим последствиям.
Соблюдая эти правила, можно безопасно пользоваться карбидом для сварки. Кроме того, это вещество позволяет сэкономить и сократить расход ацетилена.
Какие эксперименты проводили и какие опыты ставили дети в советские времена, июль 2022 | msk1.ru
Пусть сделает шаг вперед тот, кто не пытался в детстве повторить этот эксперимент!
Иллюстрация: Дмитрий Гладышев / Городские порталы
Поделиться
Редакция MSK1.RU решила удариться в детство и рассказать о проделках в юные годы. Мы вспомнили и спросили наших читателей, что делали советские дети и какие эксперименты проводили на своем опыте в то время, когда не было онлайн-игр, планшетов, соцсетей и игрушечного монстра Хаги Ваги. На ум пришло и лизание трубы зимой, и «секретики» в земле, и марганцовка с магнием, и многое другое. Впрочем, читайте сами — и возможно, текст и у вас вызовет ностальгические чувства. Однако редакция настоятельно предупреждает: не повторять.
Парадоксально, но почти каждый человек из поколения 40+ в детстве считал чуть ли не своим личным долгом проверить, что будет, если языком лизнуть на морозе металлическую трубу или ручку двери. И почти все — кто сильнее, кто не очень — прилипали и потом вряд ли решались повторять. Помню, соседская девочка Алеся в любознательном шестилетнем возрасте решила повторить этот эксперимент в мороз -20. Несмотря на все наши предупреждения, она смело высунула язык и, вполне ожиданно, прочно прилипла к воротам собственного же дома. При попытке отодрать себя она орала так, что повыскакивали чуть ли не все соседи, в итоге приклеилась губами напрочь и могла только мычать, размазывая по щекам жаркие слезы. Которые, надо сказать, тут же становились ледяными ручейками, а Алеся пыталась стереть их колючей шерстяной варежкой. В общем, когда ее родители с помощью теплой воды наконец-то отлепили от металла ворот, ее лицо было прекрасное (не в смысле красивое, а очень красное-прекрасное), а губы были такие, что сейчас бы позавидовала любая поклонница процедуры увеличения. После этого инцидента желающих повторять эксперимент почему-то больше не находилось.
И почти все — кто сильнее, кто не очень — прилипали и потом вряд ли решались повторять. Помню, соседская девочка Алеся в любознательном шестилетнем возрасте решила повторить этот эксперимент в мороз -20. Несмотря на все наши предупреждения, она смело высунула язык и, вполне ожиданно, прочно прилипла к воротам собственного же дома. При попытке отодрать себя она орала так, что повыскакивали чуть ли не все соседи, в итоге приклеилась губами напрочь и могла только мычать, размазывая по щекам жаркие слезы. Которые, надо сказать, тут же становились ледяными ручейками, а Алеся пыталась стереть их колючей шерстяной варежкой. В общем, когда ее родители с помощью теплой воды наконец-то отлепили от металла ворот, ее лицо было прекрасное (не в смысле красивое, а очень красное-прекрасное), а губы были такие, что сейчас бы позавидовала любая поклонница процедуры увеличения. После этого инцидента желающих повторять эксперимент почему-то больше не находилось.
Как потом мы узнали на уроках физики, слюна тут же замерзает от разности температур, а тепла тела недостаточно, чтобы растопить ее. К тому же, место соприкосновения металла с горячим языком почти не нагревается, и в итоге «экспериментатор» примерзает.
К тому же, место соприкосновения металла с горячим языком почти не нагревается, и в итоге «экспериментатор» примерзает.
У мальчишек были свои проказы, которые были нам, девчонкам, не совсем понятны, но порой приводили в восторг или в ужас.
— И карбид в воду кидали, и язык к железке, и стог поджигали, и по полыньям бегали, и со второго этажа стройки в песок прыгали. Непонятно, как выжили, — смеется Дима.
— Мы из карбида еще факелы делали. Там же ацетилен, а он горит хорошо. Бутылка, пробка, дырка, карбид, слюна, спички — вот тебе и факел. Зато кайф какой был! Просили: «Дядь, а дай карбида немного». Они остатки из ацетиленового генератора сливали в ливневку, но мы всегда находили, — вторит Андрей.
Такие «шалости» могли привести к трагическим последствиям
Иллюстрация: Дмитрий Гладышев / Городские порталы
Поделиться
Некоторые эксперименты и правда были крайне опасными. Современные родители, особенно «яжематери», и инстанции наподобие ПДН были бы в глубочайшем шоке от таких «шалостей».
Современные родители, особенно «яжематери», и инстанции наподобие ПДН были бы в глубочайшем шоке от таких «шалостей».
— У нас пацаны из класса так делали: брали фольгу, причем разноцветную, насыпали туда какую-то дрянь и поджигали, и быстро-быстро убегали. И она взрывалась. Бомбочки делали. Я не знаю, что они поджигали. Может, карбид, может, селитру. Для них было, наверное, особым таким извращенным удовольствием — бросать бомбочку зажженную в толпу девчонок и смотреть, как они разбегаются, визжат, пищат. А сами стояли ржали, — поделилась воспоминаниями Ксения.
— Бомбочки, карбид или селитру поджигали, по поездам ездили зайцами — мы недалеко от железнодорожной линии жили.
— В огонь баллончики кидали, — призналась Виктория.
— А еще дюбель, спички, кирпич. Или два болта, гайка, пакет, спички. Берешь дюбель, который гвоздь, кирпичиком его слегка вбиваешь в асфальт. Потом вытаскиваешь, сдираешь в ямку серу со спичек, вставляешь обратно дюбель и бросаешь кирпич. Получается бабах, — сказал Андрей.
Получается бабах, — сказал Андрей.
На уроках химии нам рассказали, что карбид — точнее, карбид кальция — при взаимодействии с водой разлагается с сильной тепловой реакцией и выделением ацетилена. Поэтому и происходит эффект наподобие взрыва, который нам так нравился.
Вряд ли даже миллениалы вспомнят, что такое пистоны. Это ленты с коричневатым веществом, которые должны были имитировать звук выстрела. Собственно, с этой задачей они справлялись просто превосходно!
— Еще были на бумажных листах такие — типа перфокарты, нанесены такие, как спички. И надо было их монеткой или гвоздиком чиркать, и они хлюпали. У папы в моем детстве тоже такое было, тоже так щелкали, — улыбается Ксения.
— Пистоны — только камушком. Если по ленте с пистонами камнем бахать, то можно было небольшой и неприятный ожог получить, — делится прошлым опытом Виктория.
Когда мне было лет так под 10 и я уже довольно неплохо, как мне казалось тогда, познала окружающий мир, я решила убедиться на своем опыте, что бывает, когда засовываешь что-то металлическое в электросеть. И однажды вечером воплотила свои задумки в жизнь: взяла тонкий плоский шампур и со всей дури вонзила его в розетку. Ощущение было, словно меня неожиданно кто-то тронул, я испугалась, затряслась всем телом и отпрыгнула. Честно — страшно в тот момент не было, а вот потом — очень! Но всё обошлось, и сейчас я пишу этот текст.
И однажды вечером воплотила свои задумки в жизнь: взяла тонкий плоский шампур и со всей дури вонзила его в розетку. Ощущение было, словно меня неожиданно кто-то тронул, я испугалась, затряслась всем телом и отпрыгнула. Честно — страшно в тот момент не было, а вот потом — очень! Но всё обошлось, и сейчас я пишу этот текст.
Опять же на уроках физики, чуть позже, нам рассказали, что любой металл прекрасно проводит электричество, и если держать, например, гвоздь в руке и засунуть его в розетку, то напряжение 220 В «ударит» по человеку. И это может быть смертельно опасно.
Еще одним не всегда безобидным развлечением молодых лет было подкладывание какого-то предмета перед идущим трамваем на рельсы. Мы начали с маленьких камешков, которыми щедро были усыпана земля вокруг шпал, а закончили довольно внушительными. Интересно было наблюдать, как тяжелый и звенящий трамвай просто превращает их в порошок. А вот однажды вагоновожатой пришлось выйти и убрать с рельсов препятствие.
— Монетку под трамвай, а не камушек, — пытается поправить меня наша читательница Виктория. — Она выходила длинная и плоская!
Впрочем, раскрошенный гравий иногда используют составители поездов: когда рельсы мокрые и скользкие, на него кладут тормозной башмак для лучшей фиксации.
И он смачно трескался. Главное было вовремя отскочить, чтобы не прилетело и не задело осколками. Веселее было разводить костер в старой ржавой огромной бочке, кидать шифер туда и накрывать всё это чугунной крышкой. Сейчас удивляюсь — как мы ее только сдвигали с места! А тогда было нипочем. В итоге в накрытой бочке шифер гулко взрывался, а мы, в свою очередь, взрывались звонким хохотом.
Опять же школьный курс физики: при нагревании шифера происходит расширение асбеста и цемента, который входит в его состав, а при его разрушении кинетическая энергия провоцирует взрыв — и, соответственно, осколки.
В детстве мы с друзьями ловили солнечных зайчиков, и это занятие оставалось невинным до тех пор, пока кого-то из ребят во дворе не предупредили родители, что из-за этого может случиться пожар. Вот уж где была дана пища для детского ума и простор для экспериментов! Мы специально достали где-то лупу и пытались поджигать с ее помощью всё, что могло гореть, при этом воображали себя спасшимися от кораблекрушения мореходами на необитаемом острове, конечно!
Вот уж где была дана пища для детского ума и простор для экспериментов! Мы специально достали где-то лупу и пытались поджигать с ее помощью всё, что могло гореть, при этом воображали себя спасшимися от кораблекрушения мореходами на необитаемом острове, конечно!
— Поджигали еще тополиный пух — он от линзы хорошо воспламенялся. Хотя чаще всего, конечно, поджигали спичками — когда могли их достать. Было у нас такое вредное «развлечение», — признаётся Ксения.
Еще мы любили играть в индейцев и готовили соответствующую атрибутику — впрочем, тогда мы еще не знали модного нынче слова «косплей». Насчет «настоящего оружия всех краснокожих», которые советские дети мастерили из подручных материалов, развернулась целая полемика среди читателей:
— Стрелялки делали из горлышка бутылки и напальчника, заряжали рябиной и стрелялись, больно было, однако! Еще стреляли из трубочек какого-то растения, рябиной и т. д. Сухой борщевик можно было так использовать, — тут же подхватывает Аленчик.
— Сначала мы его били, он высыхал, а потом уже шел в ход, — объясняет Аленчик.
Девочки хотели походить на мам и красивых женщин из советских фильмов, а вот с косметикой в те времена было не так всё хорошо. Про детскую и вовсе не слышали — и даже мечтать не могли, а в школе за такие «раскрашивания» можно было попасть на ковер к завучу или директору. В свободное от уроков время, особенно летом, если мамину помаду и тушь-«плевалку» достать украдкой не получалось, детвора шла на различные ухищрения.
— Тени из пыльцы цветов. Глаза красили. Чистотелом татушки делали на теле. А сережки из вишни-черешни? — вспоминает Люда.
— И из гроздей смородины! Красная смотрелась лучше всего. А как же цветной маникюр из малины? Надеть на палец и ходить задаваться. И из фольги от шоколада кольца такие делали, — подхватывает Аленчик.
— И из проволоки, — вторит Надя.
— Ногти делали из лепестков цветов, — говорит Мария.
— Из цветов ноги лепили на слюни. Гудрон жевали. Из песка кашу варили и продавали за листики, — вспоминает этапы своего взросления Юлия.
Гудрон жевали. Из песка кашу варили и продавали за листики, — вспоминает этапы своего взросления Юлия.
Советским детям, особенно кто помнит перестроечный дефицит, хотелось больше вкусняшек. И мы делали их сами: мазали хлеб маслом и сверху вареньем, или медом, или посыпали сахаром. Некоторые, впрочем, шли дальше.
— Газировку делали: сода, вода, сахар и лимонная кислота — рассказала Люда. — Получалась газировка типа «Спрайта». А пропорции не помню, там на глаз ложили: типа чайная ложка соды, литр воды, чайная ложка «лимонки» и сахар по вкусу.
— Я до сих пор так делаю, мне нравится, — признаётся Светлана. — В большую кружку или стакан лимонную кислоту примерно ¼ чайной ложки и сахар по вкусу, размешать до полного растворения, потом соду немного, на кончике чайной ложки, и быстро мешаешь и пьешь, пока газы не вышли.
— Соду с уксусом мешать любили, — добавляет Мария.
— А еще газировка из баллона была: воду наливаешь в специальный баллон, газовый баллончик вставляешь, в кружку варенья — и туда эту воду с газом, — вспоминает другая Мария.
Впрочем, гастрономические пристрастия у детей того времени были довольно специфическими.
— Ели что ни попадя! Березовый сок, смолу с деревьев, травинки пихали в муравейник. Я с двоюродным братом мух ловила и паукам в паутину… Вот это было зрелище! — делится опытом своих проказ Надя.
— Еще, гады, смолу жевать запрещали и заставляли колготки надевать. Изверги! — эмоционально отреагировал Миша.
Всем нам взрослые твердили: «Спички детям не игрушка». Однако на практике, когда родители не видели, спички оказывались еще каким развлечением!
— Мы еще спички к потолку кидали. Когда они горят, они приклеивались на потолке, — сказала Людмила.
— Не завидую вашей маме! Всё это потом отмывать, — ответила ей Лейла.
— Спички на известку клеили. Брали коробок, поджигали спичку и кидали в подъезде. Надо было, чтобы оно прилипло. Я сама таким не грешила, но пацаны в классе рассказывали, чем они развлекались. Это у них такое соревнование было, — вспомнила Ксения.
— Да, и в спичках уточнение. Нужно было поплевать на побеленную стену, потом на конец спички набрать побелки, спичку поджечь и кинуть на потолок. Она тогда приклеивалась, — поделился опытом из детства Андрей.
А вы что вспомните из своего детства? Какие шалости и эксперименты проводили лично вы? Напишите об этом в комментариях.
Карбид кальция для производства ацетилена
Карбид кальция для производства ацетилена – Rexarc
Ацетилен представляет собой горючий газ с характерным запахом. Он используется в качестве сырья для производства ряда органических химикатов, а также в качестве компонента топлива при резке металлов и кислородно-ацетиленовой сварке. Сегодня ацетилен также используется в производстве некоторых пластиков. Обычно ацетилен производится одним из следующих способов:
- Инициирование реакции карбида кальция с водой в ацетиленовом генераторе
- Использование различных типов углеводородов
Каждый метод имеет свои преимущества, и выбор будет полностью зависеть от пользователя. В этом посте мы обсудим производство ацетилена с использованием карбида кальция в ацетиленовом генераторе.
В этом посте мы обсудим производство ацетилена с использованием карбида кальция в ацетиленовом генераторе.
Введение в процесс производства ацетилена с использованием карбида кальция
В различных промышленных условиях производство ацетилена начинается в генераторах, производящих ацетилен. Это оборудование продается различной вместимости от 8 м 3 до более чем 200 м 3 в час. Карбид кальция вводится сверху корпуса генератора в воду. Химическая формула этой реакции может быть выражена как:
CAC 2 + 2 H 2 O → C 2 H 2 + CA(OH) 2
3 Эта реакция должна быть только проводится в контролируемых условиях. Технологический блок должен быть оборудован датчиками давления и температуры, а также обратными клапанами в целях безопасности.
Генератор ацетилена и производство ацетилена с использованием карбида кальция
Компоненты установки для производства ацетилена и их индивидуальный вклад описаны здесь:
Генератор : Здесь карбид кальция смешивается с большим количеством воды для производства ацетилена.
 газ. Генератор оснащен следующими аксессуарами:
газ. Генератор оснащен следующими аксессуарами:
a. Датчики автоматического управления
b. Кормушка
в. Бункер(ы)
d. Мешалка
e. Разрядник
Конденсатор : Помогает охладить газообразный ацетилен, образующийся в генераторе.
Скруббер для аммиака : Этот сосуд удаляет аммиак из потока ацетилена перед очисткой.
Осушитель среднего давления : Как следует из названия, осушитель среднего давления помогает осушать газообразный ацетилен. Он также используется для контроля содержания влаги в потоке ацетилена, поступающего в очиститель. Для этой цели используют безводный хлорид кальция.
Очиститель : в основном состоит из очищающего материала, который помогает отделить фосфин и сероводород, образующиеся при производстве ацетилена.

Скруббер очистителя : Этот компонент предотвращает попадание любого очищающего материала в компрессор.
Компрессор : Ацетилен является горючим газом. В нем используется компрессор для ацетилена, окруженный водой, которая охлаждает теплоту сжатия после каждой ступени.
Правила техники безопасности при обращении с карбидом кальция при производстве ацетилена
Ниже приведены некоторые рекомендации, которые следует соблюдать при обращении с карбидом кальция при производстве ацетилена.
Максимально допустимый размер и вес карбида для одной загрузки должны соответствовать спецификации производителя оборудования.
Карбид кальция следует хранить в воздухонепроницаемой и водонепроницаемой металлической упаковке с маркировкой «Карбид кальция – опасен, если не сухой».
Масса карбида кальция в бочках не должна превышать 250 кг.
 Он должен храниться там, где вода не может попасть. Контейнеры следует регулярно проверять, чтобы убедиться, что в них не попала вода.
Он должен храниться там, где вода не может попасть. Контейнеры следует регулярно проверять, чтобы убедиться, что в них не попала вода.Бочки с карбидом кальция следует открывать только во время заполнения карбидом бункеров.
Карбид с концентрацией пыли более 15% не должен заряжаться в генераторе.
Остатки карбида в воде не должны сбрасываться напрямую в окружающую среду.
Оптимальный размер карбида кальция для получения газа
Размер карбида кальция является важным фактором при производстве газа. Следующая информация даст вам представление о лучших оценках.
Размер класса | Количество A | LITRE на кг.0164 | ||
| 15-80 | 311 | 288 | 4. | 4.60 |
| 7-15 | 301 | 275 | 4.81 | 4.42 |
| 4-7 | 287 | 267 | 4.59 | 4.28 |
| 2-4 | 273 | 251 | 4.36 | 4.01 |
| 1-2 | 257 | 236 | 4.25 | 3,77 |
Вышеупомянутая информация о наилучших размерах для выхода газа собрана из нескольких промышленных исследований. Вы всегда можете обратиться к отраслевому эксперту, такому как Rexarc, чтобы понять, какие размеры лучше всего подходят для вашего приложения. Компания производит промышленные ацетиленовые установки различных спецификаций и размеров. Урожайность может быть разной у разных производителей.
Компания производит промышленные ацетиленовые установки различных спецификаций и размеров. Урожайность может быть разной у разных производителей.
Новое сообщение >>
Похожие сообщения в блоге
Соответствующая запись не найдена
Пользовательские
Мы являемся универсальным магазином от производства судов на заказ до полной трелевки, сантехники и контрольно-измерительных приборов.
Связь
Мы поддерживаем наши процессы и сообщаем вам о статусе вашего проекта так много или так мало, как вы хотите.
Обязательства
Мы постоянно реинвестируем в наших сотрудников, бизнес и технологии оборудования, чтобы своевременно поставлять качественную продукцию.
WebWISER – Дом
WISER — это система, предназначенная для оказания помощи аварийно-спасательным службам при инцидентах с опасными материалами.
WISER предоставляет широкий спектр информации об опасных веществах, в том числе
поддержка идентификации, физические характеристики, информация о здоровье человека и
советы по сдерживанию и подавлению. Известные вещества Поиск вещества в базе данных известных веществ WISER. Помогите определить химическое вещество Определите неизвестное химическое вещество на основе его физических свойств, симптомов воздействия, окружающей среды и других критериев. Инструменты Ознакомьтесь с общими инструментами и справочными материалами. Последние новости
WebWISER лучше всего просматривать в следующих браузерах (указанная версия или выше): Internet Explorer 9, Firefox 26, Safari 7 или Google Chrome 30. WISER также доступен как отдельное приложение для ПК и различных мобильных платформ. включая устройства iOS и Android. Посетите домашнюю страницу WISER для бесплатных загрузок и получения дополнительной информации о WISER. | Другие ресурсы для чрезвычайных ситуаций с химическими веществами в NLM
Other Chemical Emergency Resources
|
Обработка воды Как она заслуживает того, чтобы ее обрабатывали с помощью кремниевых карбид -мембран
Вы здесь
Журнал Smart Water. 0261
0261
Автор контента: Sebastian Andreassen
Автор контента: Mike Snodgrass
Большинство населения мира не имеет доступа к чистой воде, и большая часть сточных вод не сбрасывается безопасным образом в природные водоемы. Существующие запасы пресной воды испытывают растущую нагрузку из-за роста населения, промышленного использования и загрязнения. Как часть жизнеспособного водоснабжения, сточные воды не используются полностью из-за ограничений и высокой стоимости традиционных технологий. В некоторых случаях сточные воды практически не очищаются в виде сбросов ливневой канализации. Мембраны из карбида кремния (SiC) устраняют многие ограничения, связанные с традиционной очисткой воды , создавая глобальную возможность безопасной очистки и регенерации воды с меньшими затратами времени, занимаемой площади и стоимости.
Современный ландшафт очистки воды обычно состоит из длинных, сложных и индивидуально разработанных схем очистки, включающих многочисленные этапы очистки, прежде чем воду можно будет повторно использовать, сбрасывать или безопасно потреблять. Этот подход часто имеет ограниченное рабочее окно и может иметь проблемы, если качество воды на входе отклоняется от исходной основы проекта. Это приводит к простою установки, незапланированному техническому обслуживанию и снижению количества и качества очищенной воды. По этой причине часто требуются дополнительные резервные мощности в дополнение к и без того чрезмерным затратам и размерам завода.
Этот подход часто имеет ограниченное рабочее окно и может иметь проблемы, если качество воды на входе отклоняется от исходной основы проекта. Это приводит к простою установки, незапланированному техническому обслуживанию и снижению количества и качества очищенной воды. По этой причине часто требуются дополнительные резервные мощности в дополнение к и без того чрезмерным затратам и размерам завода.
Способность мембран превращать сточные воды в безопасную, чистую воду, пригодную для повторного использования, широко признана во всем мире, но скорость адаптации медленнее, чем должна быть. Это связано с тем, что обычные мембраны не всегда были самыми надежными, в результате чего реальные затраты на расширенное повторное использование оказались выше, чем предполагалось. Многие из наших проблем с нехваткой воды могут быть решены при наличии надежной и устойчивой технологии, позволяющей легко превращать сточные воды в питьевую воду.
Внедрение технологии SiC было чрезвычайно быстрым во всех частях мира благодаря широким возможностям очистки, которые она может обеспечить.
По-настоящему эластичная мембрана может быть получена только путем полной замены самого материала мембраны. Обычные мембраны получают из нефтяного масла. SiC получают из песка Северного моря . Не нужно быть экспертом по мембранам, чтобы понять разницу между этими материалами. С пошаговым изменением материала мембраны может быть достигнуто гораздо более широкое рабочее окно, позволяющее системе быть по-настоящему устойчивой.
Мембраны SiC обеспечивают полное восстановление после очистки, бессрочное хранение в сухом состоянии, высокая устойчивость к твердым веществам, устойчивость к грубому материалу и возможность промывки под давлением — вот лишь некоторые из многих особенностей, облегчающих жизнь пользователю. SiC также является одним из немногих мембранных материалов, которые являются естественно и постоянно гидрофильными, что означает, что органические загрязнения, включая масло, отталкиваются мембраной, в то время как вода естественным образом втягивается.
площадь мембраны по сравнению с обычными мембранами .
Карбид кремния позволяет по-новому взглянуть на очистку воды и сточных вод. Дни больших, сложных очистных поездов, использующих грузовики с химикатами для кондиционирования воды с резервной мощностью, теперь могут уйти в прошлое. И во многих случаях, используя SiC, традиционные схемы очистки могут быть сокращены до 10 % занимаемой площади, 10 % использования химикатов и, по крайней мере, половины потребления энергии.
Карбид кремния также является единственной технологией, которая может мгновенно очищать и дезинфицировать в начале шторма. Это гарантирует, что независимо от времени года или интенсивности шторма SiC может обеспечить физический барьер для бактерий, патогенов и твердых частиц, обеспечивая чистоту и безопасность наших водных путей.
Вся вода, которая у нас есть, это вся вода, которая у нас будет. Мы несем ответственность за ее очистку, восстановление и повторное использование с умом. Внедрение технологии SiC было чрезвычайно быстрым во всех частях мира благодаря широким возможностям лечения, которые она может предоставить.
Всего за пять лет по всему миру было доставлено более 500 миллионов литров чистой и безопасной воды, но впереди еще долгий путь .
Избранные новости
09.14.2022 · Изменение климата · 9
Сокращение запасов воды на Тибетском нагорье угрожает водной безопасности в районах нижнего течения
14/09/2022 · Управление · 14
Пуэрто-Рико объявляет новые тендеры на инфраструктуру водоснабжения на сумму 48 миллионов долларов
7 2022 · Экономика замкнутого цикла · 95
Изучение возможностей использования сточных вод в экономике замкнутого цикла
13/09/2022 · Бизнес · 20
Консультационная служба Бахрейна EWA получает заявки на участие в тендере IWPPancy, этап
09.13.2022 · Бизнес · 25
Багдад потратит 172 миллиона долларов на обслуживание канализационных систем
09.12.2022 · Засуха · 26
Меры по адаптации к нехватке воды в северной Мексике
09/09/2022 · Качество воды · 38
Вредные цветы водорослей угрожают калифорнийским водам
09/09/2022 · Business Adview For Pfesshy.
08/09/2022 · Biodiversity · 57 1
Drought and overexploitation of aquifers dry up Spain’s Doñana National Park completely
08/09/2022 · Water quality · 47
Shrinking Alpine glaciers повлияет на водные ресурсы Европы
09.07.2022 · Цифровой · 44
Китай борется с засухой с помощью технологий, поскольку нехватка воды угрожает экономике
09.06.2022 · Бизнес · 441
DOOSAN выигрывает 640 миллионов долларов США на строительство завода для опреснения в Саудовской Аравии
06/09/2022 · Ирригация · 59
Проекты Проект. /09/2022 · Бизнес · 154
Катар запускает первый проект по очистке сточных вод в рамках государственно-частного партнерства вода
01/09/2022 · Изменение климата · 141
Изменение является нашим единственным устойчивым вариантом
азой-легированного фрагбидного карбиде. один из наиболее многообещающих электрокатализаторов для реакции выделения водорода, хотя он демонстрирует вялую кинетику из-за сильной связи вольфрам-водород.
Кроме того, еще не сообщалось о каталитической активности карбида вольфрама в отношении реакции выделения кислорода. Здесь мы представляем супераэрофобный электрод из карбида вольфрама, легированный азотом, обладающий высокой стабильностью и активностью в отношении реакции выделения водорода, а также эффективно управляющий выделением кислорода в кислоте. Легирование азотом и структура наноматрицы ускоряют выделение газообразного водорода из электрода, обеспечивая плотность тока −200 мА см -2 при потенциале -190 мВ по сравнению с обратимым водородным электродом, которые представляют собой один из лучших катализаторов из неблагородных металлов для реакции выделения водорода. В кислых условиях (0,5 M серная кислота) расщепление воды, катализируемое наноматрицей карбида вольфрама, легированного азотом, начинается примерно с 1,4 В и превосходит большинство других катализаторов расщепления воды.
Введение
Газообразный водород долгое время считался чистым и устойчивым энергоносителем для замены традиционных ископаемых видов топлива.
Экономически эффективное производство газообразного водорода является одним из ключевых моментов, которые еще предстоит решить для успешной водородной экономики 1,2,3 . Электролиз воды с использованием электричества из устойчивых источников энергии (например, ветра или солнца) представляет собой экологически безопасную схему производства газообразного водорода высокой чистоты 4,5,6,7,8,9,10,11 . По сравнению со щелочным электролизом производство водорода в кислотах, например, при электролизе с мембраной из полимерного электролита, имеет преимущества простоты, высокой плотности тока и совместимости с высоким давлением. Однако высокоэффективные катализаторы для HER и OER в кислых средах в основном ограничиваются благородными металлами (например, платиной (Pt), иридием (Ir) и рутением (Ru)). Высокая стоимость и ограниченный запас благородных металлов ограничивают их широкое применение. Были предприняты замечательные усилия по разработке катализаторов неблагородных металлов для HER в кислоте 9.
0027 12 , такие как сульфиды металлов 13,14,15,16,17 , карбиды металлов 5,18,19,20 и фосфиды металлов 21,22,23 . К сожалению, большинство катализаторов, не содержащих благородных металлов, для HER в кислоте имеют либо большое начальное перенапряжение 24,25,26,27 , либо отсутствие рабочей стабильности, особенно при высоких плотностях тока 11,16,17,18,19 . Что касается OER в кислом электролите, эффективные катализаторы по-прежнему ограничиваются катализаторами на основе благородных металлов 28,29 , в то время как лишь несколько катализаторов на основе неблагородных металлов (например, Co 3 O 4 30 , MnO x 31 и CoMnO x 32 ), но с большими начальными потенциалами и плохой стабильностью.
Карбид вольфрама (WC) представляет собой распространенный в земле и недорогой катализатор, который стабилен в кислоте и ведет себя как Pt в гидрогенолизе благодаря своей электронной конфигурации вокруг уровня Ферми 33,34 .
Эти свойства делают WC многообещающим кандидатом для применения в качестве электрокатализатора неблагородных металлов для HER в кислоте 9.0027 5,18,35,36 . Несмотря на его популярность, наши теоретические расчеты показывают, что адсорбированные атомы водорода сильно связываются с WC, способствуя восстановлению H + , но препятствуя десорбции водорода. Поэтому важно исследовать материалы на основе WC с лучшими характеристиками. Наностержни карбида вольфрама были синтезированы без шаблона 37,38 . В 2013 году Хашимото и соавт. синтезировал электрокатализатор Fe-WCN 39 . Они предположили, что электронная плотность атомов W снижается за счет связи W-N и, следовательно, улучшает каталитическую активность HER. Далее Чен и соавт. сообщил об электрокатализаторе, сочетающем карбид-нитрид вольфрама и графеновые нанопластинки, показывая, что синергетические эффекты между W 2 Фазы C и WN способствуют выдающейся каталитической активности выделения водорода 40 .
Однако эффект ограничивался только низкой плотностью тока, а лежащие в его основе механизмы оставались неоднозначными. В результате ни один из материалов не показал плотности тока, равной -200 мА см -2 . Кроме того, помимо собственной активности катализатора, для эффективного газовыделения важно быстрое удаление пузырьков газа с поверхности электрода. Сильное прилипание пузырьков к поверхности электрода препятствует переносу заряда и массы между катализатором и электролитом. Катализаторы также могут отслаиваться при выходе пузырьков из-за сильной адгезии. Таким образом, активность катализаторов реакций газовыделения можно значительно повысить с помощью супераэрофобных электродов 20,21 . Таким образом, конструкция электродов, основанная на наноструктурировании и модуляции на атомном уровне, является многообещающим подходом к ускорению активности и стабильности реакции выделения водорода.
Здесь мы сообщаем о супераэрофобном каталитическом электроде как для HER, так и для OER в кислоте на основе структур наномассивов WC, легированных N.
Стратегия дизайна многогранна. N-допинг модулирует уровень поверхностной энергии для оптимизации связывания водорода и, таким образом, способствует кинетике HER. Структура наноматрицы не только обнажает больше активных участков для электрохимической реакции, но также способствует выделению газа, предлагая супераэрофобный интерфейс под водой. Следовательно, поверхность раздела имеет слабую адгезию пузырьков, отрывая маленькие пузырьки с небольшой площадью контакта, что способствует выделению газа на гетерогенных каталитических поверхностях. Как и ожидалось, электрод наноматрицы N-WC обеспечивает превосходную HER-активность и стабильность до -200 мА см9.0027 -2 , превосходя подавляющее большинство зарегистрированных электрокатализаторов из неблагородных металлов. Кроме того, наноматрица N-WC также демонстрирует отличные общие характеристики расщепления воды в кислоте, функционируя как катод и анод с достаточной стабильностью.
Результаты.
Теоретические расчеты.
Результат расчета HBE на Pt (111) составляет −0,47 эВ, как показано на рис. 1a, что очень похоже на опубликованный результат −0,46 эВ 41 , что подтверждает правильность нашего метода расчета. Далее мы сосредоточимся на связывании водорода с поверхностью (001) WC, поскольку, согласно более раннему исследованию 42 , она оказалась наиболее стабильной поверхностью. Как показано на рис. 1b, атомы водорода прочно связываются между двумя атомами W, при этом расчетное значение HBE на атом H равно −1,05 эВ, что значительно более отрицательно, чем у Pt (111) (−0,47 эВ). Поэтому связанные с поверхностью атомы водорода не так легко отрываются от поверхности, как H 2 с поверхности WC (001), что согласуется с наблюдаемой низкой HER-активностью WC. Примечательно, что HBE на поверхности N-WC (001) уменьшается до -0,72 эВ (рис. 1c) при легировании WC N, становясь намного ближе к связыванию H на Pt (111). Следовательно, рассчитанные HBE предполагают, что HER-активность WC может быть значительно улучшена за счет N-допирования.
Также было исследовано изменение HBE с различным количеством легирования N, и было продемонстрировано, что 6,25 ат.% N-легирования в N-WC является оптимальным значением (дополнительный рисунок 1). Рис. 1
Геометрия связи водорода и энергии связи DFT. Геометрия связывания водорода и энергия связи a WC (001) поверхность, b N-WC (001) поверхность, c Pt (111) поверхность и d расчетная парциальная плотность состояния (DOS) WC (001) и N-WC (001). Вертикальной пунктирной линией показано положение уровня Ферми. Цветовая схема: черные, коричневые, белые, синие и серые шарики обозначают атомы C, W, H, N и Pt соответственно
Изображение в натуральную величину
Парциальные плотности состояний (DOS) на отдельных поверхностных атомах WC показаны на рис. 1d по сравнению с таковыми в N-WC для анализа влияния N-легирования на электронную структуру WC. Отметим, что плотность 5d-состояний атомов W на поверхностях N-WC (001) сдвинута вниз по сравнению с плотностью на поверхностях WC (001), что предполагает более отрицательный центр d-зоны атомов W на N-WC (001).
Действительно, центр d-полосы W на WC (001) рассчитан как -1,12 эВ, а на N-WC (001) рассчитан как -1,50 эВ, что близко к таковому на поверхностях Pt (111). Нижний центр d-полосы приводит к более слабой адсорбции H на каталитической поверхности (дополнительный рисунок 2) 43 . Эти результаты дают ценную информацию о влиянии легирования N на электронную структуру и предполагают более подходящую адсорбцию H на поверхности N-WC для повышения активности HER.
Синтез электрода наноматрицы N-WC
Электроды наноматрицы WC, легированные N, были приготовлены с помощью последовательного двухэтапного подхода (рис. 2a). На первом этапе использовали контролируемую гидротермальную реакцию вольфрамовой кислоты для выращивания наномассива WO 3 на бумаге из углеродного волокна (CFP). Впоследствии WO 3 наноматрицу подвергали восстановлению и одновременно карбонизации и легированию N при высокой температуре с использованием меламина в качестве источника как C, так и N.
Рис. 2Условия химического осаждения из паровой фазы были оптимизированы для достижения высокой активности HER. Плотность тока для приложенного потенциала -200 мВ по сравнению с RHE измеряли как индексы. Было обнаружено, что оптимальные условия, обеспечивающие максимальную плотность каталитического тока, составляют 850 ° C в течение 3 часов (дополнительный рисунок 3). Порошок WC без наноматрицы, легированный азотом (N-WC), наноматрица WC без примеси N (наноматрица WC) и порошок WC (WC) также были приготовлены при оптимизированной температуре и времени для использования в качестве контрольных образцов (подробности см. раздел «Методы»).
Изготовление электродов наноматрицы N-WC для HER. a Схематическая иллюстрация: WO 3 наноматрицы на CFP были синтезированы с помощью нематричной самособирающейся гидротермальной реакции вольфрамовой кислоты; затем наноматрицу WO 3 восстанавливали, карбонизировали и легировали N меламином при высокой температуре, чтобы получить наноматрицу N-WC, которую использовали непосредственно в качестве высокоэффективного каталитического электрода HER или OER.
b SEM из WO 3 наноматрица. c СЭМ наноматрицы N-WC. Масштабная линейка в b и c : слева вверху 20 мкм, слева внизу 5 мкм, справа 200 нм
Полноразмерное изображение
который демонстрирует структуру наноматрицы, состоящую из тонких лент длиной около 5 мкм, шириной ~ 400 нм и толщиной ~ 10 нм. Морфология WO 3 хорошо сохранилась после преобразования в наноматрицу N-WC (рис. 2c), за исключением того, что она стала тоньше на 2–3 нм. Идеальное сохранение структуры наноматрицы можно объяснить морфологией тонкого пояса, в которой большинство атомов кислорода находится вблизи поверхности, поэтому атомы кислорода можно было легко извлечь и заменить атомами углерода или азота без повреждений. На рис. 3а показаны данные рентгеновской дифракции (XRD) CFP, WO 9.наноматрица 0034 3 и наноматрица N-WC. На профиле XRD CFP пики при 26,4° и 42,5° характерны для графита (PDF#41–1487). Рентгенограмма наноматрицы WO 3 хорошо совпадает с гексагональной WO 3 (PDF № 75–2187).
Рис. 3После восстановления и карбонизации WO 3 была успешно получена гексагональная фаза WC (PDF № 51–0939), как показано на рентгенограмме наноматрицы N-WC, на которой пик при 42,5° относится к экстратетрагональному углероду (PDF № 54–0501). Изображения просвечивающей электронной микроскопии (ПЭМ) на рис. 3b показывают, что каждый пояс N-WC состоит из параллельных узких поясов, расположенных рядом друг с другом. На поверхности много наночастиц диаметром около 3 нм. Изображение ПЭМ высокого разрешения (HRTEM) показывает полосы решетки наночастиц. Расстояние d 0,25 нм соответствует плоскостям (100) гексагонального WC. Дифракционные кольца WC (001) и WC (100) можно было ясно увидеть на изображении SAED (дополнительный рисунок 4). Судя по карте SEM-энергодисперсионного спектрометра (EDS), показанной на дополнительном рисунке 5, вольфрам и углерод являются основными компонентами наноматрицы N-WC с очень небольшим количеством азота. Для сравнения на дополнительном рисунке 6 показаны рентгенограммы CFP, наномассива N-WC, наномассива N-WC и WC.
Все они ведут себя как чистые фазы WC (PDF#51–0939). EDS наномассива WC на дополнительном рисунке 7 показывает отсутствие азота.
Характеристика электрода с наноматрицей N-WC. a Рентгенограммы CFP и синтезированного наномассива WO3 и наномассива N-WC. b HRTEM наноматрицы N-WC. c XPS-обзор наноматрицы N-WC и XPS с высоким разрешением d N 1s и e W 4f. f Распределение элементов TEM-EDS наноматрицы N-WC. Масштабная линейка в b 909:25 : слева 200 нм, справа 2 нм. Масштабная линейка в f 1 мкм
Полноразмерное изображение
Данные рентгеновской фотоэлектронной спектроскопии (XPS) были выполнены, чтобы получить больше информации о химическом окружении наномассива N-WC. По данным XPS на рис. 3c можно идентифицировать элемент N, а его содержание на поверхности образца составляет около 8,0 ат.%. На рис. 3d показан профиль XPS с высоким разрешением N 1s. Подгоночные пики при 399,7 и 401,3 эВ можно отнести к особенностям связей N–C, а пик при 39Сообщалось, что 8,7 эВ представляет собой связь N-W 44 .
Наличие связи N–W также подтверждается РФЭС W 4f на рис. 3e. Пик при более высокой энергии связи 41,3 эВ возникает в результате неизбежного окисления поверхности наномассива N-WC при воздействии воздуха. Энергия связи при 35,5 и 38 эВ предположительно соответствует связям W–N 45 , а пики с центром при 32,5 и 34,6 эВ относятся к связям WC 18,46 .
На рисунке 3f и в дополнительной таблице 1 показаны результаты TEM-EDS и соответствующее распределение элементов в наноматрице N-WC. Как показано на картировании элементов, N равномерно распределен вдоль нанопоясов N-WC. Спектр TEM-EDS наномассива N-WC показан на дополнительном рисунке 8. Согласно результату TEM-EDS, содержание N составляет около 6,6 ат.%, что близко к результату исследования XPS, что указывает на то, что элемент N равномерно легирован внутри образца.
Электрокаталитическое выделение водорода
Электрокаталитические характеристики наномассивных электродов N-WC для HER были измерены с трехэлектродной конфигурацией в 0,5 M H 2 SO 4 .
Рис. 4На рисунке 4а показаны кривые линейной сканирующей вольтамперограммы (LSV) для различных электрокатализаторов с ИК-коррекцией. Содержание металлов в катализаторах на основе WC составляет все 10 мг см -2 . Электрод WC проявляет каталитическую эффективность с перенапряжением -193 мВ при -10 мА см -2 и -513 мВ при -200 мА см -2 , что сопоставимо с катализатором WC, о котором обычно сообщается 18,39 . После легирования азотом электрод N-WC демонстрирует значительно улучшенные каталитические свойства с перенапряжением -113 мВ для управления каталитическим током -10 мА см -2 и перенапряжением -310 мВ для -200 мА см -2 . Эффект легирования N подтвердил предположение расчетов DFT, показывающих, что N в N-WC может сделать энергию связи W – H более подходящей для кинетики HER.
Характеристики HER и сравнение. a LSV коммерческого наномассива Pt/C, WC, WC, N-WC и N-WC в 0,5 M H 2 SO 4 с ИК-коррекцией при скорости сканирования 1 мВ/с.
b Графики Тафеля, рассчитанные по a . c Сопротивление переменному току WC, наноматрицы WC, N-WC, наномассивы N-WC и коммерческих катализаторов Pt/C. d Тест на стабильность наноматрицы N-WC при перенапряжении -0,144 В в течение 10 ч, а затем -0,156 В в течение еще 10 ч с ИК-коррекцией
Изображение в полный размер
Кроме того, наноструктурирование также положительно влияет на каталитическую активность. Наноматрица WC демонстрирует -200 мА см -2 при -320 мВ, демонстрируя улучшенные каталитические характеристики по сравнению с аналогом WC (-513 мВ). Что наиболее важно, наноматрица N-WC демонстрирует наиболее впечатляющую активность HER с небольшим перенапряжением -89 мВ при плотности тока -10 мА см -2 и перенапряжением -190 мВ при -200 мА см -2 (дополнительная таблица 2). ). Такая каталитическая активность превосходит ранее сообщавшиеся электроды на основе карбида (дополнительная таблица 3). Производительность наномассива N-WC также является выдающейся среди лучших электрокатализаторов HER на основе неблагородных металлов в кислоте (дополнительная таблица 4).
Данные об электрохимически активной площади поверхности (ECSA) были получены из кривых CV в нефарадеевской области (подробности см. В разделе «Методы» и на дополнительном рисунке 9).). Оба образца наномассива демонстрируют значительно больший ECSA, чем образцы порошка (дополнительный рисунок 10). После нормализации ECSA превосходство образцов N-WC по-прежнему заметно, что еще раз демонстрирует улучшение внутренней активности за счет N-допинга (дополнительный рисунок 11). Кроме того, образцы наноматриц демонстрируют гораздо более высокую активность, чем их порошковые аналоги, что означает, что структура наноматрицы благоприятствует HER не только из-за увеличенной площади поверхности, но и из-за ускоренного выхода пузырьков газа.
Как показано на рис. 4b, наклон Тафеля для наноматрицы N-WC для HER составляет −75 мВ dec −1 , что является наименьшим среди всех электрокатализаторов на основе WC, демонстрируя более благоприятный процесс HER для N -WC наноматричный электрод.
Быстрая кинетика реакции HER N-WC также отражается небольшим сопротивлением переносу заряда 0,5 Ом при потенциале -0,5 В по сравнению с обратимым водородным электродом (рис. 4c).
Стабильность наноматрицы N-WC была протестирована при перенапряжении -0,144 В (~-20 мА см -2 ) в течение первых 10 часов, а затем -0,156 В (~-50 мА см -2 ) в течение следующих 10 часов, как показано на рис. 4d. Плотность тока увеличилась на 2,9 % на первом этапе, а затем снизилась на 1,9 % при более высоком перенапряжении в последующие 10 ч электролиза. Для карбида вольфрама 18,35,36 никогда не сообщалось о превосходной стабильности при −50 мА см −2 . Увеличение плотности тока при -0,144 мВ означает, что электрод сначала активируется во время HER. Затем в следующем периоде появляется спад каталитического тока. Чтобы проверить этот процесс, мы дополнительно проверили стабильность свежего образца при температуре около -60 мА см9.0027 −2 . Как показано на дополнительном рисунке 12, плотность тока увеличилась в первые 6 часов, а затем немного уменьшилась до равновесного состояния, при котором ток оставался неизменным в течение остальных 12 часов.
Плотность тока снизилась примерно на 0,5% после общего 22-часового испытания при -60 мА см -2 . Чтобы смоделировать промышленное производство H 2 при большой плотности тока с перерывами, мы провели испытание на стабильность с прерыванием при −100 мА см −2 (дополнительный рисунок 13). Плотность тока уменьшилась примерно на 14% после 30-часового электролиза воды. Выдающуюся каталитическую стабильность можно объяснить ее высокой химической стабильностью и надежностью структуры наноматрицы для высвобождения пузырьков. Из посмертного XPS-анализа (дополнительный рисунок 14) превосходная стабильность наномассива N-WC дополнительно подтверждается незначительными структурными различиями до и после длительного электролиза воды.
Поведение пузырьков
Поведение пузырьков во время электрокаталитической реакции при -200 мВ по сравнению с RHE было зарегистрировано с помощью системы высокоскоростной камеры. Хорошо видно, что наноматрица WC и WC демонстрирует меньшую и более медленную эволюцию H 2 , чем электроды наноматрицы N-WC и N-WC (дополнительный фильм 1 и снимки на рис.
Рис. 55a). Наблюдаемая значительная разница показывает, что N-допирование увеличивает внутреннюю каталитическую активность за счет модуляции электронной структуры WC, как это предполагается нашими расчетными предсказаниями. В то же время на поверхности электродов WC и N-WC можно было видеть большие площади светоотражающих газовых пленок, которые образуются в результате H 2 Газ сильно прилип к поверхности электрода. Как только активные центры изолированы от водного электролита прилипшими пузырьками или газовыми пленками, электрокаталитическая реакция замедляется. Напротив, на поверхности наноматрицы WC или наноматрицы N-WC не было очевидной газовой пленки или крупных пузырьков, поэтому каталитическая HER продолжается без перерыва. Кроме того, пузырьки на наномассиве N-WC намного меньше и исчезают намного быстрее, чем пузырьки на других электродах.
Исследование поведения пузырьков. a Моментальные снимки пузырьков, отрывающихся от разных электродов при −200 мВ по сравнению с RHE.
b краевые углы пузырьков, c силы адгезии пузырьков и d распределения размеров пузырьков на различных электродах из WC, наномассивов WC, N-WC и наномассивов N-WC. Масштабная линейка в a : 100 мкм
Полноразмерное изображение
Существенные различия в поведении пузырьков свидетельствуют о более слабой адгезии пузырьков на электроде с наноматрицей, чем на плоском электроде, что количественно описывается краевым углом (CA) и сила сцепления (AF). Как показано на рис. 5b и c, ненаноструктурированные электроды показывают CA = 146° и AF = 19.мкН для WC, тогда как CA = 148° и AF = 12 мкН для N-WC. Напротив, два электрода наноматрицы демонстрируют значительное увеличение CA (156 ° для наноматрицы WC и 163 ° для наноматрицы N-WC) и снижение AF (5 мкН для наноматрицы WC и почти не обнаруживаемое для наноматрицы N-WC). Эти данные подтверждают тот факт, что придание шероховатости поверхности может улучшить каталитическую активность HER за счет ослабления взаимодействия пузырьков с поверхностью электрода, что способствует быстрому высвобождению пузырьков H 2 .
Кроме того, WC-электроды, легированные азотом, демонстрируют немного большую CA и более слабую AF, чем их нелегированные азотом аналоги WC той же структуры, демонстрируя дополнительные доказательства того, что N-легирование ослабляет силу взаимодействия между H 2 пузыри и поверхность электрода.
Распределение размеров пузырьков, оторвавшихся от электродов, количественно определено статистически на рис. 5d. Средние размеры пузырьков на наномассиве WC и наномассиве N-WC существенно не отличаются, и аналогичные наблюдения применимы к электродам WC и N-WC. Однако при сравнении электродов с наноматрицей с их неструктурированными аналогами преимущества очевидны: меньший размер пузырьков, а также более крупная CA и более слабая AF. Соответственно, наноматрица WC проявляет гораздо лучшую каталитическую активность, чем WC, тогда как наноматрица N-WC превосходит N-WC. Следовательно, ускоряющий эффект структурирования наномассивов по отношению к HER еще раз подтверждается.
Электрокаталитическое выделение кислорода
In 0,5 M H 2 SO 4 , характеристики OER наноматрицы N-WC были измерены с использованием Pt-фольги в качестве противоэлектрода по сравнению с коммерческими 20 мас.
Рис. 6% Ir/C и IrO 2 Катализатор. Нагрузка металла на все три электрода составляет 10 мг см -2 . Как показано на рис. 6а, OER начинается примерно при 1,35 В на электроде с наноматрицей N-WC и примерно при 1,5 В на коммерческом катализаторе Ir/C и IrO 2 . Плотность тока на наномассиве N-WC очень быстро увеличивается с потенциалом. При напряжении около 1,7 В относительно RHE плотность тока достигает до 60 мА см −2 . Концентрация O 2 в электролите определялась измерителем растворенного кислорода (DOM) во время электрохимического испытания, когда на наномассив N-WC периодически подавались потенциалы 1,35, 1,4 и 1,45 В. На рис. 6б концентрация O 2 повышается до 1,5, 1,6 и 1,7 млн соответственно при приложении к электроду напряжения 1,35, 1,4 и 1,45 В и падает каждый раз, когда напряжение выключено. Синхронизированное изменение между напряжением и O 2 9Концентрация 0035 указывает на то, что OER действительно возникает при напряжении около 1,35 В относительно RHE.
Хотя OER-активность наномассива N-WC впечатляет, стабильность наномассива N-WC для OER в кислоте все еще нуждается в улучшении, как показано на рис. 6c. Потенциал увеличивается с 1,35 до 1,54 В по сравнению с RHE через 1 ч непрерывного расщепления воды при 10 мА см -2 . Чтобы выяснить причину нестабильности наномассива N-WC, мы записали рентгенограммы наномассива N-WC до и после теста OER, показывающие, что небольшое количество оксидов вольфрама образовалось на наномассиве N-WC во время теста OER (рис. 6d). ). Хотя наноматрица N-WC на данный момент недостаточно стабильна для практического применения, анод на основе N-WC может представлять собой важное направление исследований неблагородного катализатора OER в кислоте.
Производительность OER и сравнение. a Кривые поляризации OER, протестированные в 0,5 M H 2 SO 4 наноматрицы N-WC, IrO 2 и 20 мас.% Ir/C при скорости сканирования 5 мВ/с с ИК-коррекцией.
b O 2 концентрация в 0,5 M H 2 SO 4 при периодическом приложении к электроду наноматрицы N-WC различных потенциалов. c Тест на стабильность наноматрицы N-WC для OER при 10 мА см −2 . d Рентгенограммы наноматрицы N-WC до и после теста OER
Изображение в полный размер
Электрокаталитическое расщепление воды
) или коммерческий электрод Ir/C (загрузка 5 мг см -2 ) (электролизная ячейка, отмеченная как набор W-IrC) в качестве анода, была измерена общая эффективность расщепления воды. При комнатной температуре (20 °C) эксперимент проводили в 0,5 M H 2 SO 4 , а соответствующие вольт-амперные кривые показаны на рис. 7а. Что касается набора W – IrC, общая реакция расщепления воды начинается примерно при 1,5 В. Мы провели тест хроноамперометрии при 1,5 В без компенсации iR и записали видео электродов (дополнительный фильм 2). На снимке, показанном на рис.
Рис. 77b, отчетливо видны пузырьки как на аноде, так и на катоде, что соответствует расщеплению воды, начиная примерно с 1,5 В. Таким образом, наноматрица N-WC обещает практическое применение в качестве HER-катода. Удивительно, но общее расщепление воды комплекта W–W начинается примерно при 1,4 В.До 1,7 В относительно ОВЭ плотность тока достигает до 30 мА см −2 . Эти результаты имеют важное значение, поскольку никогда не сообщалось о таких превосходных характеристиках каталитического электролиза воды в кислоте с катализаторами, не содержащими благородных металлов. Был проведен хроноамперометрический тест установки W–W на уровне 1,4 В без компенсации iR. Записанное видео электродов (дополнительный фильм 3) показывает сильное пузырение на электродах (снимок на рис. 7c), подтверждая высокоэффективное каталитическое расщепление воды с помощью наномассивов N-WC в качестве бифункционального каталитического электрода как для анода, так и для катода. . Кроме того, мы протестировали характеристики разделения воды набора W – IrC и набора W – W, питаемого от коммерческой батареи AA, как показано на рис.
7d и соответствующих видеороликах (дополнительные фильмы 4 и 5). Пузыри развиваются на электродах набора W – IrC (дополнительный фильм 6, рис. 7e) и более интенсивно на электродах набора W – W (дополнительный фильм 7, рис. 7f).
Полное разделение воды. a Вольт-амперные кривые общего расщепления воды с наномассивом N-WC в качестве катода при использовании наномассива Ir/C (обозначается как набор W-IrC) или наномассива N-WC (обозначается как набор W-W) в качестве анода . б Видеофрагмент электролиза воды на установке В–ИрК с напряжением 1,5 В в Видеофрагмент электролиза воды на установке В–В с напряжением 1,4В г Установка общего разделения воды с питанием от коммерческую батарейку АА и соответствующие снимки барботирования газа с электролизом воды набора W–IrC ( e ) или набор W-W ( f )
Увеличенное изображение
Обсуждение
Таким образом, мы разработали, сконструировали и продемонстрировали супераэрофобный N-WC наномассив катализатора для расщепления воды на H 2 и O 2 путем контролируемого синтеза наноматрицы WO 3 с последующим одновременным восстановлением, карбонизацией и легированием N меламином при высокой температуре.
Чтобы внести ясность, N-допирование играет наиболее важную роль в повышении активности HER наномассива N-WC за счет улучшения внутренней активности на атомном уровне. В то же время наноструктурирование также повышает активность и стабильность HER, предлагая большую эффективную площадь поверхности и способствуя выделению газа в наноразмерной конструкции. В результате катализатор наноматрицы N-WC достигает плотности каталитического тока -10 мА см -2 при перенапряжении -89 мВ и -200 мА см -2 при -190 мВ, отличающийся выдающейся каталитической активностью HER и рабочей стабильностью для длительного электролиза воды. Наблюдаемые каталитические характеристики HER нашего наномассива N-WC являются одними из лучших катализаторов HER на основе неблагородных металлов в кислоте. Что еще более важно, общая реакция расщепления воды начинается примерно при 1,4 В, при этом наноматрица N-WC работает как катодный, так и анодный электроды, демонстрируя низкое перенапряжение и высокую активность для OER в кислоте.
Методы
Материалы
Вольфрамовая кислота была приобретена у Aladdin Industrial Corporation. Безводный сульфат натрия, перекись водорода и соляная кислота были приобретены у Beijing Chemical Works. 5 мас.% дисперсии Nafion D-521, 20 мас.% Pt/C, IrO 2 , нанографит, камфора, 20 мас.% Ir/C и CFP были приобретены у Alfa Aesar. Меламин был получен из Тяньцзиньского научно-исследовательского института тонкой химии Гуан Фу. Все растворы в данной работе были приготовлены на деионизированной воде.
Синтез WO
3 наноматрицWO 3 наноматриц на CFP синтезированы гидротермальным методом. При магнитном перемешивании порошок вольфрамовой кислоты (0,625 г) растворяли в 20 мл 12 мас.% раствора перекиси водорода при нагревании при 95 °С в течение 3 часов. Затем раствор переносили в тефлоновый реакционный сосуд с 0,2 г безводного сульфата натрия, 115 мкл соляной кислоты и добавляли кусок CFP размером 2 см × 2 см. 180 °С. ВО 9Порошок 0034 3 без наноматрицевой структуры также был синтезирован тем же методом без CFP.
Восстановление, карбонизация и легирование азотом
WO 3 наноматрицы на лодочке для сжигания, содержащей меламин, нагревали при различных температурах ( T ) и времени ( t ) периодов, с потоком газа Ar в трубке печь. Для оптимизации каталитических характеристик мы пробовали T = 650, 750, 850 и 950 °C, а t = 0,5, 1, 3 и 6 ч. В качестве индексов измеряли плотности тока (без коррекции iR) при перенапряжении -200 мВ. Было обнаружено, что оптимальные условия для обеспечения максимальной плотности каталитического тока составляют 850 ° C в течение 3 часов (дополнительный рисунок 3). Порошок N-WC без структуры наноматрицы был изготовлен с использованием WO 9.0034 3 порошок в качестве прекурсора, карбонизированный и легированный N в тех же условиях, что и наноматрицы N-WC с лучшими характеристиками. Наномассивы WC и WC изготавливали при той же температуре и времени с наномассивами N-WC отдельно, за исключением использования камфоры в качестве источника углерода.
Характеристика материалов
Морфологию исследовали с помощью JEOL JEM 2100, работающего при 200 кВ, и Zeiss SUPRA-55, работающего при 20 кВ. XPS проводили с использованием Thermo Electron ESCALAB-250. Рентгенограммы были получены с помощью Shimadzu XRD-6000 при 10°/мин.
Электрохимические измерения
Электрохимические измерения проводились в 0,5 M растворе H 2 SO 4 с помощью прибора CH (CHI660E) с эталоном Ag/AgCl и графитовым стержневым противоэлектродом во время теста HER. Электрод Ag/AgCl корректировали обратимым водородным электродом и промывали деионизированной водой перед использованием. Наноматрицы WC (20 мг см -2 ) и наноматрицы N-WC (16 мг см -2 ) использовались непосредственно в качестве электродов. Электроды на основе порошковых образцов были изготовлены с помощью следующих этапов: 16 мг порошка N-WC (или 20 мг порошка WC) и 10 мкл дисперсии Nafion смешивали с 1 мл изопропанола с образованием каталитических чернил, которые затем наносили на кусок CFP.
по каплям под инфракрасной лампой. Содержание металла в катализаторах на основе WC составляет 10 мг см 9 .0027 −2 . Электрод Pt/C был изготовлен по той же процедуре, за исключением того, что 2 мкл дисперсии нафиона и 0,4 мг 20 мас.% Pt/C смешивали с 0,5 мл изопропанола для образования каталитической краски. Загрузка электрода Pt/C составляла 0,4 мг см -2 . По той же методике были изготовлены электроды Ir/C и IrO 2 . 50 мг 20 вес.% Ir/C и 100 мкл дисперсии Nafion смешивали с 5 мл изопропанола для получения каталитической краски Ir/C. Каталитическая краска IrO 2 была изготовлена из 11,7 мг IrO 2 и 20 мкл дисперсии нафиона, смешанного с 5 мл изопропанола. Металлические нагрузки Ir/C и IrO 2 электрод 10 мг см -2 . LSV для HER выполняли при 1 мВ с -1 . LSV для OER выполняли при 5 мВ с -1 . Данные ECSA были получены из CV-кривых катализаторов на основе WC в нефарадеевской области с различными скоростями сканирования.
При -0,5 В относительно RHE, EIS измерялся от 100 кГц до 0,005 Гц с амплитудой 10 мВ. Загрузка всех катализаторов указана в дополнительной таблице 5.
Исследование поведения пузырьков
При комнатной температуре СА пузырьков водорода на разных электродах в 0,5 M H 2 SO 4 были измерены в окружающем воздухе с помощью метода с закрытыми пузырьками 47 , а размер пузырьков контролировался на уровне 2 мкл. АФ между пузырьками водорода и электродами в 0,5 M H 2 SO 4 была протестирована Dataphysics DCAT21, Германия 20. Видео процесса выделения водорода было записано с помощью Microscope (SZ-CTC, OLYMPUS) с X-Motion, AOS Technologies.
O
2 тест на концентрациюO 2 концентрация в 0,5 M H 2 SO 4 был протестирован DOM (лабораторный измеритель растворенного кислорода TP351). Перед использованием РОМ включали на 8 часов для достижения баланса в воздухе.
0,5 M H 2 SO 4 перед испытанием продували газообразным аргоном в течение 1 часа.
Статистика
На рис. 5d 50 пузырьков, отрывающихся от поверхности каждого электрода, были случайным образом зарегистрированы и использованы непосредственно в ящичковых диаграммах.
Расчеты DFT
Все периодические расчеты границ выполнялись с помощью пакета моделирования Vienna ab initio 48,49,50,51 . Для описания электрон-ионных взаимодействий использовались метод плоской волны с проектором 52,53 и обменно-корреляционный функционал PBE 54 . Для базиса плоских волн во всех расчетах было выбрано пороговое значение 450 эВ. Для оптимизации объемных Pt и WC была выбрана сетка k-точек типа 7 × 7 × 7 Монкхорста-Пака. Для расчета плит Pt (111) и WC (001) была выбрана сетка k-точек типа 5 × 5 × 1 Monckhorst-Pack. Метод Метфесселя-Пакстона второго порядка использовался для интегрирования по зоне Бриллюэна 29 , а значение σ- было выбрано равным 0,1 эВ.
Для оптимизации структуры использовался силовой критерий сходимости 0,01 эВ Å -1 . Критерий сходимости по энергии был установлен равным 10 -4 эВ на элементарную ячейку. Для моделирования поверхности Pt (111) использовались пять слоев атомов Pt и по четыре атома Pt на каждый слой. Нижние три слоя были исправлены во время оптимизации. Для моделирования поверхности WC (001) использовались четыре слоя W и четыре слоя атомов C, по четыре атома на слой. Чтобы смоделировать поверхность N-WC (001), мы заменили половину подповерхностных атомов C атомами N, что соответствует атомному проценту атомов N 6,25%, что близко к экспериментальному атомному проценту 6,61%. Два нижних слоя атомов W и C были зафиксированы во время оптимизации геометрии для поверхностей WC (001) и N-WC (001). Вакуумная пластина около 15 Å была вставлена между поверхностной пластиной. Для расчета H0034 2 . Только один атом водорода был включен в расчет поверхностей, поглощаемых водородом, что соответствует заполнению поверхности ¼.
HBE = E total –0,5 E h3 – E Surf . E total – полная энергия поглощенной системы, E surf – оптимизированная энергия голой поверхности, E ads – энергия адсорбата (H 2 ) в вакууме.
Доступность данных
По обоснованному запросу дополнительные данные доступны у соответствующего автора.
Ссылки
Бокрис, Дж. О. Водородная экономика. Наука 176 , 1323–1323 (1972).
ОБЪЯВЛЕНИЯ КАС Статья пабмед Google ученый
- “>
Тернер, Дж. А. Устойчивое производство водорода. Наука 305 , 972–974 (2004).
ОБЪЯВЛЕНИЯ КАС Статья пабмед Google ученый
Schlapbach, L. & Zuttel, A. Материалы для хранения водорода для мобильных приложений. Природа 414 , 353–358 (2001).
ОБЪЯВЛЕНИЯ КАС Статья пабмед Google ученый
Лю, Дж. и др. Усиление фотохимического выделения водорода в иерархическом фотонном кристалле диоксида титана, нагруженном Pt. Энергетика Окружающая среда. науч. 3 , 1503–1506 (2010).
КАС Статья Google ученый
Гонг, К. и др. Сверхмалые и фазово-чистые наночастицы W 2 C для эффективного электрокаталитического и фотоэлектрохимического выделения водорода. Нац. коммун. 7 , 13216 (2016).
ОБЪЯВЛЕНИЯ КАС Статья пабмед ПабМед Центральный Google ученый
Лю, М., Цзин, Д., Чжоу, З.
и Го, Л. Одномерные гомопереходы, индуцированные близнецами, обеспечивают высокую квантовую эффективность для генерации солнечного водорода. Нац. коммун. 4 , 2278 (2013).
ОБЪЯВЛЕНИЯ пабмед Google ученый
Моралес-Гио, К. Г., Тилли, С. Д., Врубель, Х., Гретцель, М. и Ху, X. Выделение водорода из фотокатода из оксида меди (i), покрытого аморфным катализатором из сульфида молибдена. Нац. коммун. 5 , 3059 (2014).
ОБЪЯВЛЕНИЯ Статья пабмед Google ученый
- “>
Креспо-Кесада, М. и др. Инкапсулированный металлом свинцово-органический фотокатод на основе перовскита для выделения водорода в воде за счет солнечной энергии. Нац. коммун. 7 , 12555 (2016).
ОБЪЯВЛЕНИЯ КАС Статья пабмед ПабМед Центральный Google ученый
Pinhassi, R. I. et al. Гибридные биофотоэлектрохимические элементы для расщепления солнечной воды. Нац. коммун. 7 , 12552 (2016).
ОБЪЯВЛЕНИЯ КАС Статья пабмед ПабМед Центральный Google ученый
Ран, Дж. и др. Ti 3 C 2 мксеновый сокатализатор на фотопоглотителях из сульфида металла для повышенного фотокаталитического производства водорода в видимом свете. Нац. коммун. 8 , 13907 (2017).
ОБЪЯВЛЕНИЯ КАС Статья пабмед ПабМед Центральный Google ученый
- “>
Ши, Дж. и др. Новый Sn 2 Sb 2 O 7 нанофотокатализатор для эволюции H 2 , управляемой видимым светом. Нано рез. 5 , 576–583 (2012).
КАС Статья Google ученый
Lu, S. & Zhuang, Z. Электрокатализаторы для реакций окисления и выделения водорода. Науч. Китай Матер. 59 , 217–238 (2016).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Се, Дж. и др. Богатые дефектами сверхтонкие нанолисты MoS 2 с дополнительными активными краевыми центрами для усиленного электрокаталитического выделения водорода. Доп. Матер. 25 , 5807–5813 (2013).
КАС Статья пабмед Google ученый
Li, Y. et al. MoS 2 наночастицы, выращенные на графене: передовой катализатор для реакции выделения водорода. Дж. Ам. хим. соц. 133 , 7296–7299 (2011).
КАС Статья пабмед Google ученый
Cheng, L. et al. Ультратонкие нанохлопья WS 2 в качестве высокоэффективного электрокатализатора реакции выделения водорода.
Ангью. хим. Междунар. Эд. 53 , 7860–7863 (2014).
КАС Статья Google ученый
Кибсгаард, Дж., Джарамилло, Т. Ф. и Безенбахер, Ф. Создание соответствующего мотива активного центра в катализаторе выделения водорода с тиомолибдатными кластерами [Mo 3 S 13 ] 2− . Нац. хим. 6 , 248–253 (2014).
КАС Статья пабмед Google ученый
Корниенко Н. и др. Оперативный спектроскопический анализ электрокатализатора выделения водорода из аморфного сульфида кобальта. Дж. Ам. хим. соц. 137 , 7448–7455 (2015).
КАС Статья пабмед Google ученый
Fan, X., Zhou, H. & Guo, X. Нанокристаллы WC, выращенные на вертикально ориентированных углеродных нанотрубках: эффективный и стабильный электрокатализатор для реакции выделения водорода.
ACS Nano 9 , 5125–5134 (2015).
КАС Статья пабмед Google ученый
млн лет, Р. и др. Сверхтонкие наночастицы карбида молибдена в сочетании с углеродом в качестве высокоактивного электрокатализатора выделения водорода. Анжю. хим. Междунар. Эд. 54 , 14723–14727 (2015).
КАС Статья Google ученый
Сюй, Ю.-Т. и другие. Путь пиролиза в клетке к сверхмалым наночастицам карбида вольфрама для эффективного электрокаталитического выделения водорода. Дж. Ам. хим. соц. 139 , 5285–5288 (2017).
КАС Статья пабмед Google ученый
Лю, К. и др. Углеродные нанотрубки, украшенные нанокристаллами CoP: высокоактивный наногибридный электрокатализатор, не содержащий благородных металлов, для выделения водорода.
Ангью. хим. Междунар. Эд. 53 , 6710–6714 (2014).
КАС Статья Google ученый
McEnaney, J.M. et al. Наночастицы аморфного фосфида молибдена для электрокаталитического выделения водорода. Хим. Матер. 26 , 4826–4831 (2014).
КАС Статья Google ученый
Xiao, P. et al. Фосфид молибдена как эффективный электрокатализатор реакции выделения водорода. Энергетика Окружающая среда. науч. 7 , 2624–2629 (2014).
КАС Статья Google ученый
- “>
Лу, З. и др. Сверхвысокие характеристики выделения водорода подводными «супераэрофобными» наноструктурированными электродами MoS 2 . Доп. Матер. 26 , 2683–2687 (2014).
ОБЪЯВЛЕНИЯ КАС Статья пабмед Google ученый
Ли, Ф. и др. Разработан синтез многослойных углеродных нанотрубок@Cu@MoS 2 гибрида в качестве перспективного электрокатализатора для высокоэффективной реакции выделения водорода. J. Источники питания 300 , 301–308 (2015).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Ян, Л. и др. Пористые металлические нанолисты MoO 2 на подложке MoS 2 для повышенной электрокаталитической активности в реакции выделения водорода. Nanoscale 7 , 5203–5208 (2015).
ОБЪЯВЛЕНИЯ КАС Статья пабмед Google ученый
- “>
Zhou, H. et al. Одностадийный синтез самонесущей пористой гибридной пены NiSe 2 /Ni: эффективный трехмерный электрод для реакции выделения водорода. Nano Energy 20 , 29–36 (2016).
КАС Статья Google ученый
Smith, R.D.L., Sporinova, B., Fagan, R.D., Trudel, S. & Berlinguette, C.P. Легкая фотохимическая подготовка пленок аморфного оксида иридия для катализа окисления воды. Хим. Матер. 26 , 1654–1659 (2014).
КАС Статья Google ученый
Reier, T. et al. Молекулярный анализ структуры и активности высокоэффективных оксидных Ir-Ni катализаторов с низким содержанием иридия для электрохимического расщепления воды (OER). Дж. Ам. хим. соц. 137 , 13031–13040 (2015).
КАС Статья пабмед Google ученый
- “>
Mondschein, J.S. et al. Кристаллические пленки оксида кобальта для устойчивого электрокаталитического выделения кислорода в сильнокислых условиях. Хим. Матер. 29 , 950–957 (2017).
КАС Статья Google ученый
Huynh, M., Shi, C., Billinge, SJL & Nocera, DG. Природа активированного оксида марганца для выделения кислорода. Дж. Ам. хим. соц. 137 , 14887–14904 (2015).
КАС Статья пабмед Google ученый
Huynh, M., Ozel, T., Liu, C., Lau, E.C. & Nocera, D.G. Разработка стабилизированных темплатом активных катализаторов выделения кислорода, содержащих большое количество земли, в кислоте. Хим. науч. 8 , 4779–4794 (2017).
КАС Статья пабмед ПабМед Центральный Google ученый
- “>
Хьюстон, Дж. Э., Ларамор, Г. Э. и Парк, Р. Л. Поверхностные электронные свойства вольфрама, карбида вольфрама и платины. Наука 185 , 258–260 (1974).
ОБЪЯВЛЕНИЯ КАС Статья пабмед Google ученый
Леви, Р. Б. и Будар, М. Платиноподобное поведение карбида вольфрама в поверхностном катализе. Science 181 , 547–549 (1973).
ОБЪЯВЛЕНИЯ КАС Статья пабмед Google ученый
Никифоров А.В. и др. WC в качестве неплатинового электрокатализатора выделения водорода для высокотемпературных электролизеров воды PEM. Междунар. Дж. Гидрог. Энергия 37 , 18591–18597 (2012).
КАС Статья Google ученый
- “>
Томас-Гарсия, А.Л., Ли, К., Дженсен, Дж.О. и Бьеррум, Н.Дж. Карбиды вольфрама с большой площадью поверхности: синтез, характеристика и каталитическая активность в отношении реакции выделения водорода в фосфорной кислоте при повышенных температурах. Междунар. Дж. Электрохим. науч. 9 , 1016–1032 (2014).
Google ученый
Ян Ю. и др. Бестемплатный псевдоморфный синтез наностержней карбида вольфрама. Маленький 8 , 3350–3356 (2012).
КАС Статья пабмед Google ученый
Ли, Н., Ян, Ю., Ся, Б.-Ю., Ван, Ж.-Ю. & Wang, X. Новые наностержни из карбида вольфрама: собственный миметик пероксидазы с высокой активностью и стабильностью в водных и органических растворителях. Биосенс. Биоэлектрон. 54 , 521–527 (2014).
КАС Статья пабмед Google ученый
- “>
Чжао Ю., Камия К., Хашимото К. и Наканиши С. Выделение водорода с помощью наноэлектрокатализаторов карбонитрид вольфрама, синтезированных путем образования гибрида вольфрамовая кислота/полимер in situ. Анжю. хим. Междунар. Эд. 52 , 13638–13641 (2013).
КАС Статья Google ученый
Чен, В.-Ф. и другие. Карбид-нитрид вольфрама на графеновых нанопластинках как прочный электрокатализатор выделения водорода. ChemSusChem 7 , 2414–2418 (2014).
КАС Статья пабмед Google ученый
Уотсон, Г.В., Уэллс, Р.П.К., Уиллок, Д.Дж. и Хатчингс, Г.Дж. Сравнение адсорбции и диффузии водорода на {111} поверхностях Ni, Pd и Pt из расчетов теории функционала плотности. J. Phys. хим. B 105 , 4889–4894 (2001).
КАС Статья Google ученый
Михальский Р., Чжан Ю.-Дж. и Петерсон, А.А. Тенденции в активности катализаторов на основе карбидов металлов по выделению водорода. ACS Катал. 4 , 1274–1278 (2014).
КАС Статья Google ученый
Китчин, Дж. Р., Норсков, Дж. К.
, Барто, М. А. и Чен, Дж. Г. Модификация поверхностных электронных и химических свойств Pt(111) подповерхностными 3d-переходными металлами. J. Chem. физ. 120 , 10240–10246 (2004).
ОБЪЯВЛЕНИЯ КАС Статья пабмед Google ученый
Ян Х. и др. Мелкоразмерные и высокодисперсные кластеры WN из [SiO 4 (W 3 O 9 ) 4 ] 4-, загружаемые на графен, полученный из GO, в качестве перспективных носителей для электроокисления метанола. Энергетика Окружающая среда. науч. 7 , 1939–1949 (2014).
КАС Статья Google ученый
Ян Х. и др. Модифицированный фосфором нитрид вольфрама/восстановленный оксид графена в качестве высокоэффективного электрокатализатора, не содержащего благородных металлов, для реакции выделения водорода. Анжю.
хим. Междунар. Эд. 54 , 6325–6329 (2015).
КАС Статья Google ученый
Zellner, M.B. & Chen, J.G. Синтез, характеристика и поверхностная реакционная способность пленок PVD из карбида вольфрама (WC). Прибой. науч. 569 , 89–98 (2004).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Jiang, M. et al. Супераэрофобный наноструктурированный электрод на основе RuO 2 для высокоэффективной реакции выделения хлора. Малый 13 , 1602240 (2017).
Артикул Google ученый
Kresse, G. & Hafner, J. Ab initio. физ. Rev. B 47 , 558–561 (1993).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Kresse, G.
& Hafner, J. Ab initio. Физ. Ред. B 49 , 14251–14269 (1994).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Крессе, Г. и Фуртмюллер, Дж. Эффективность расчетов полной энергии ab-initio для металлов и полупроводников с использованием базисного набора плоских волн. Вычисл. Матер. науч. 6 , 15–50 (1996).
КАС Статья Google ученый
Крессе, Г. и Фуртмюллер, Дж. Эффективные итерационные схемы для неэмпирических расчетов полной энергии с использованием базисного набора плоских волн. Физ. Ред. B 54 , 11169–11186 (1996).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
- “>
Blöchl, P. E. Метод дополненной волны проектора. физ. Ред. B 50 , 17953–17979 (1994).
ОБЪЯВЛЕНИЯ Статья Google ученый
Кресс, Г. и Жубер, Д. От ультрамягких псевдопотенциалов к проекторному методу дополненной волны. Физ. Ред. B 59 , 1758–1775 (1999).
ОБЪЯВЛЕНИЯ КАС Статья Google ученый
Пердью, Дж. П., Берк, К. и Эрнзерхоф, М. Упрощенное приближение обобщенного градиента. физ. Преподобный Летт. 77 , 3865–3868 (1996).
ОБЪЯВЛЕНИЯ КАС Статья пабмед Google ученый
Скачать ссылки
Благодарности
Эта работа была поддержана Программой для чанцзянских ученых и исследовательской группы по инновациям в Университете, Фондом естественных наук Китая и фондами фундаментальных исследований для центральных университетов, а также срок механизма субсидирования от Министерства финансов и Министерства образования КНР. В.С.Б. признает время суперкомпьютеров от NERSC и финансирование в рамках Аргоннско-Северо-западного центра исследований солнечной энергии (ANSER), исследовательского центра Energy Frontier, финансируемого Министерством энергетики США, Управлением науки, Управлением фундаментальных энергетических наук, под номером награды DE- SC0001059.
Авторы благодарны профессору Хайляну Вану за содержательное обсуждение и предложения.
Информация об авторе
Авторы и филиалы
Государственная ключевая лаборатория инженерии химических ресурсов, Колледж энергетики и Пекинский передовой инновационный центр науки и техники о мягких веществах, Пекинский химико-технологический университет, 100029, Пекин, Китай
Нана Хань, Чжии Лу, Инцзе Ли, Вэньвэнь Сюй, Тэнфэй Гао, Чжао Цай, Ин Чжан, Вэнь Лю и Сяомин Сунь
Институт химии и энергетики, Йельский университет, 810 West Campus Drive, West Haven, CT, 06516, USA
Ke R. Yang, Victor S. Batista и Wen Liu
2 Авторы
Нана Хан
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Ke R. Yang
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Zhiyi Lu
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Yingjie Li
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Wenwen Xu
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Tengfei Gao
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Zhao Cai
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Ying Zhang
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Victor S.
Batista
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Wen Liu
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Xiaoming Sun
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Contributions
XS, WL, NH и ZL разработал этот проект и эксперименты. NH провел большинство экспериментов. К.С.Ю. и В.С.Б. провел теоретические расчеты. Ю.Л. проводили СЭМ-исследования. З.К. выполнили HRTEM-исследования. Т.Г. проводили исследования ЭДС. W.X. провел тест XPS. Ю.З. провел тесты CA и AF. Х.С., В.Л. и NH написали статью в соавторстве. Результаты и рукопись комментируются и обсуждаются всеми авторами.
Авторы переписки
Переписка с Вэнь Лю или Сяомин Сунь.
Заявление об этике
Конкурирующие интересы
Авторы не заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Примечание издателя: Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Электронный дополнительный материал
Дополнительная информация
Description of Additional Supplementary Files
Supplementary Movie 1
Supplementary Movie 2
Supplementary Movie 3
Supplementary Movie 4
Supplementary Movie 5
Supplementary Movie 6
Дополнительный фильм 7
Права и разрешения
Открытый доступ при условии, что вы укажете первоначальных авторов и источник, предоставите ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons для статьи, если иное не указано в кредитной строке материала.
Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/.
Перепечатка и разрешения
Об этой статье
Дополнительная литература
Аморфизация катализаторов на основе халькогенидов благородных металлов на пределе однослойности в отношении производства водорода
- Юнмин Хе
- Лижэнь Лю
- Чжэн Лю
Природный катализ (2022)
Безлинкерная химическая подготовка наночастиц палладия на электродах из оксида цинка, легированного алюминием, для электрохимического окисления воды
- Исмаил А.
Булиямину
- Мд.Абдул Азиз
- Заин Хассан Ямани
Journal of Materials Science: Materials in Electronics (2022)
Разработка интерфейса гетероструктур карбид/фосфид вольфрама, закрепленных на углероде, легированном N,P, для высокоэффективной реакции выделения водорода
- Хунфан Ду
- Чжужу Ду
- Вэй Хуан
Материалы науки Китая (2022)
Фемтосекундная лазерная микро-нанообработка для ускорения высвобождения пузырьков в реакциях газовыделения
- Шуай Чжан
- Лишуан Сюй
- Сянтин Донг
Исследования в области нанотехнологий (2022)
Включение фосфора активирует базисную плоскость дисульфида вольфрама для эффективного катализа выделения водорода.
- Фань Ван
- Шувен Ню
- Минхуа Чен
Исследования в области нанотехнологий (2022)
Комментарии
Отправляя комментарий, вы соглашаетесь соблюдать наши Условия и Правила сообщества. Если вы обнаружите что-то оскорбительное или не соответствующее нашим условиям или правилам, отметьте это как неприемлемое.
Эффективные уплотнения из карбида кремния для проверенных водяных насосов
Перейти к содержимомуПредыдущий Следующий
- Посмотреть увеличенное изображение
О различных частях, из которых состоит водяной насос Dolz, в этом посте мы сосредоточимся на компоненте, отвечающем за защита от любой возможной утечки и загрязнения : динамическое уплотнение.
Наряду с подшипником сальник является важнейшим элементом водяного насоса, так как от них зависит его герметичность. Таким образом, его основная функция заключается в защите подшипника путем предотвращения утечек и загрязнения охлаждающей жидкостью, получающей герметичный водяной насос .
Задача в этом процессе состоит в том, чтобы позволить вращающемуся валу войти во «влажную» зону насоса , не допуская утечки охлаждающей жидкости. И по этой причине необходимо, чтобы между насосом и корпусом было уплотнение, поддерживающее давление процесса и трение, вызванное вращением вала.
Традиционно это достигалось за счет набивки: шнур, пропитанный гидроизоляционной смазкой , который обматывался вокруг вала за турбиной.
Метод, который развивался по мере разработки новых двигателей в автомобильной промышленности. Поэтому необходимо было создать более надежные и долговечные конфигурации для получения максимально возможных характеристик прочности уплотнения.
Уплотнения новейшей технологии
В Industrias Dolz у нас есть самосмазывающихся уплотнений из карбида кремния , с каучуком HNBR и синтетическими графическими контактными кольцами. Продукт высочайшего качества для оптимальной работы водяного насоса.
Благодаря своей инновационной конструкции и качественной охлаждающей жидкости эти уплотнения полностью предотвращают утечки , что обеспечивает долгий срок службы водяного насоса.
Компоненты динамического уплотнения:
- Углерод
- Уплотнения из карбида кремния
- Пружина из нержавеющей стали
- Каучуки (NBR и HBNR)
- Корпус из нержавеющей стали (фиксированный)
- Трубка из окрашенной стали (бесплатно)
Современные материалы, характеризующиеся высокой твердостью, низким тепловым расширением, высокой жесткостью и хорошим сопротивлением носить.
Уплотнения из карбида кремния состоят из двух отдельных частей, одна из которых закреплена на корпусе, а другая вращается вокруг оси подшипника. Все это в единой детали, которая монтируется независимо от турбины с помощью устройства т, обеспечивающего точную регулировку высоты характеристики и сохранение ее сопротивления.
Продолжайте читать: 3 причины для одновременной замены ремня ГРМ и водяного насоса
Революция в уплотнениях из карбида кремния
Карбид кремния (SiC) представляет собой материал со свойствами высокой твердости , подобными алмазу, что делает его идеальным для использования в процессах изготовления компонентов, подвергающихся экстремальным нагрузкам. температуры, напряжения и частоты.
Этот полупроводниковый и тугоплавкий материал устойчив к истиранию и износу , что дает множество преимуществ, таких как высокая теплопроводность, высокое механическое сопротивление и низкий коэффициент трения.
В результате вы продлеваете срок службы водяного насоса.
Dolz, внедряет инновации с 1934 г.
Помимо поставки самых опытных водяных насосов на рынке, компания Dolz обеспечивает герметичность всех производимых деталей с помощью строгого процесса, в ходе которого калибрует и обнаруживает любые возможные утечки.
Оставаясь впереди рынка послепродажного обслуживания, мы выполняем свое твердое обязательство развиваться с точки зрения дизайна, производства и доставки, предоставляет нашим клиентам лучшие решения и обеспечивает превосходное качество , сервис и инновации. Есть вопросы? Мы будем рады помочь Вам!
Поиск
Поиск:
Последние записи
- Расширение ассортимента: 9 новых ссылок на комплекты вспомогательного привода Dolz. 8 сентября 2022 г.
- Повреждение и выход из строя подшипника водяного насоса 25 августа 2022 г.
- Дольц вернется в следующем выпуске Automechanika Frankfurt 23 августа 2022 г.
- Какие автозапчасти самые важные 22 августа 2022 г.
- 10 вопросов, которые нужно задать при выборе марки водяного насоса 18 августа 2022 г.
Архив по дате
Архив по датеВыберите месяц Сентябрь 2022 г. (1) Август 2022 г. (8) Июль 2022 г. (5) Июнь 2022 г. (5) Май 2022 г. (8) Апрель 2022 г. (5) Март 2022 г. (5) Февраль 2022 г. (9) январь 2022 г. (4) декабрь 2021 г. (5) ноябрь 2021 г. (7) октябрь 2021 г. (4) сентябрь 2021 г. (7) август 2021 г. (7) июль 2021 г. (6) июнь 2021 г. (5) май 2021 г. (8) апрель 2021 г. (4) март 2021 г. (6) февраль 2021 г. (1) декабрь 2020 г. (1) июнь 2020 г. (1) март 2020 г. (1) апрель 2019 г.(1) февраль 2019 г. (1) декабрь 2018 г. (1) август 2018 г. (1) июль 2018 г. (1) декабрь 2017 г. (1) сентябрь 2017 г. (1) июль 2017 г. (1) ноябрь 2016 г. (1) август 2016 г. (2) март 2016 г. (1) Сентябрь 2015 г.
(2)
Категории
КатегорииВыберите категориюПослепродажное обслуживание (1)Dolz (113)Notas de Prensa (23)Комплекты ремня ГРМ (3)Комплекты цепи привода ГРМ (2)Без категории (4)Водяные насосы (5)Перейти к началу
Коррозионная стойкость марок карбида вольфрама от Federal Carbide
Главная / О нас / Что нового / Условия продажи / Возможности трудоустройства / Свяжитесь с нами
- Карбид вольфрама
- Недвижимость из цементированного карбида вольфрама
- Коррозия Сопротивление карбида вольфрама класса
- Дизайн Соображения
- Приложения для работы с жидкостями и управления потоком
- Компоненты из карбида вольфрама для пайки
Таблица марок карбида вольфрама- Руководство по применению карбида вольфрама
- Режимы отказа изнашиваемых деталей из карбида
- Паспорт безопасности материала
Таблица марок тяжелых сплавов вольфрама
- Руководство по применению тяжелых сплавов вольфрама
Сравнительная таблица марок вольфрамовых тяжелых сплавов- Коррозионная стойкость карбида вольфрама марок
Таблица марок карбида вольфрама- Руководство по применению карбида вольфрама
Сравнительная таблица марок карбида вольфрамаКобальт на сегодняшний день является наиболее широко используемым связующим металлом или «цементом» в цементированных карбидах вольфрама, поскольку он наиболее эффективно смачивает зерна карбида вольфрама во время жидкофазного спекания.
По этой причине считается, что кобальт превосходит другие связующие металлы с точки зрения устранения остаточной пористости и достижения высоких показателей прочности и ударной вязкости в спеченных изделиях. Однако разрушение цементированных карбидов в агрессивных средах обычно происходит из-за химической реакции кобальта с коррозионными агентами. Процесс коррозии включает растворение связующего кобальта на открытых поверхностях, оставляя рыхлый скелет из зерен карбида вольфрама, имеющий небольшую структурную целостность. Этот механизм часто называют «выщелачиванием» кобальта, и обычно он сопровождается отслаиванием карбидных зерен без носителя на пораженных участках поверхности.
Хотя сорта WC + Co имеют довольно хорошую стойкость к воздействию ацетона, этанола, бензина и других органических растворителей, а также аммиака, большинства оснований, слабых кислот и водопроводной воды. Однако воздействие муравьиной, соляной, фтористоводородной, азотной, фосфорной, серной и других сильных кислот может привести к относительно быстрому разрушению связующей фазы.
На скорость коррозии также влияют температура, концентрация и электропроводность коррозионного агента, а также другие факторы окружающей среды. Легирование кобальта хромом, молибденом и/или никелем может значительно улучшить стойкость связующего к коррозии, но полная замена кобальта никелем оказалась наиболее эффективным средством продления срока службы твердых сплавов в высококоррозионных средах. Поэтому марки WC + Ni и другие специальные составы, разработанные для защиты от коррозии без ущерба для прочности или других характеристик, идеально подходят для таких применений, как уплотнительные кольца, компоненты управления потоком, дроссельные клапаны, форсунки и подшипники.
Приведенные ниже таблицы предназначены только для использования в качестве общих показателей коррозионной стойкости марок цементированного карбида. В Таблице 1 показаны общие показатели коррозии для Co и Ni марок связующего в зависимости от значения pH. В Таблице 2 показана относительная коррозионная стойкость выбранных марок Federal Carbide на основе потери веса испытательных образцов, погруженных в различные растворы в течение определенного периода времени.
Таблица 1 Стойкость к коррозии Связующие Co и Ni в зависимости от значения pH
РН
WC + кобальтовое связующее
WC + никелевое связующее
12
Очень хорошо Очень хорошо 11
10
9
Хороший 8
7
Ярмарка
6
Бедные
5
От очень плохой до нулевой устойчивости
к коррозииХороший
4
3
Ярмарка
2
1
Бедные
0
Таблица 2 Относительная коррозионная стойкость выбранных марок карбида
VG = очень хорошо; Г = Хорошо; F = Удовлетворительно; П = Плохо; VP = Очень плохо
Тип раствора и темп.

Жидкий агент
Концентрация (%)FC3
(6% Co)FC10
(9% Co)FC3N
(6% Ni)FC8N
(никель-хром-молибден)Кислоты при 50°C.
Уксусная кислота
10
Г
Г
Г
ВГ
50
Г
Г
ВГ
ВГ
100
Г
Г
ВГ
ВГ
Борная кислота
10
Г
Г
ВГ
ВГ
Хромовая кислота
10
Г
Г
Г
Г
Лимонная кислота
10
Г
Г
ВГ
ВГ
Муравьиная кислота
10
Ф
Ф
Г
Г
Плавиковая кислота
20
Г
Г
Г
ВГ
Соляная кислота
5
Ф
Ф
Г
Ф
35
Г
Г
ВГ
Г
Азотная кислота
5
Р
ВП
Г
Г
50
ВГ
ВГ
ВГ
ВГ
Фосфорная кислота
10
Р
Р
Г
Г
50
Р
ВП
Ф
Ф
Серная кислота
10
Р
ВП
Г
Г
50
Г
Ф
ВГ
Г
90
Г
Г
ВГ
Г
Щелочи при 50°C.
Гидроксид калия
10
Г
Г
ВГ
ВГ
Гидроксид натрия
10
Г
Г
Г
ВГ
Солевые растворы при 50°C.
Хлорид аммония
10
Г
Г
Г
ВГ
Аммиачная селитра
10
Ф
Ф
Ф
ВГ
Сульфат аммония
10
Г
Г
Г
ВГ
Перекись водорода
10
ВП
ВП
ВП
Ф
Гидроксид калия
10
Г
Г
ВГ
ВГ
Силикат калия
10
ВГ
ВГ
ВГ
ВГ
Хлорид натрия
10
ВГ
Г
ВГ
ВГ
Гидроксид натрия
10
Г
Г
Г
ВГ
Вода при 50°C.
Морская вода
100
Г
Г
ВГ
ВГ
Чистая вода
100
ВГ
ВГ
ВГ
ВГ
Federal Carbide предлагает полное семейство стандартных марок карбида вольфрама на никелевой связке для применений, требующих устойчивости к коррозии. Кроме того, компания Federal разработала множество нестандартных марок для использования в чрезвычайно агрессивных средах, в ситуациях, требующих как высокой прочности, так и коррозионной стойкости, а также там, где должны соблюдаться строгие требования к оборудованию для пищевой промышленности.


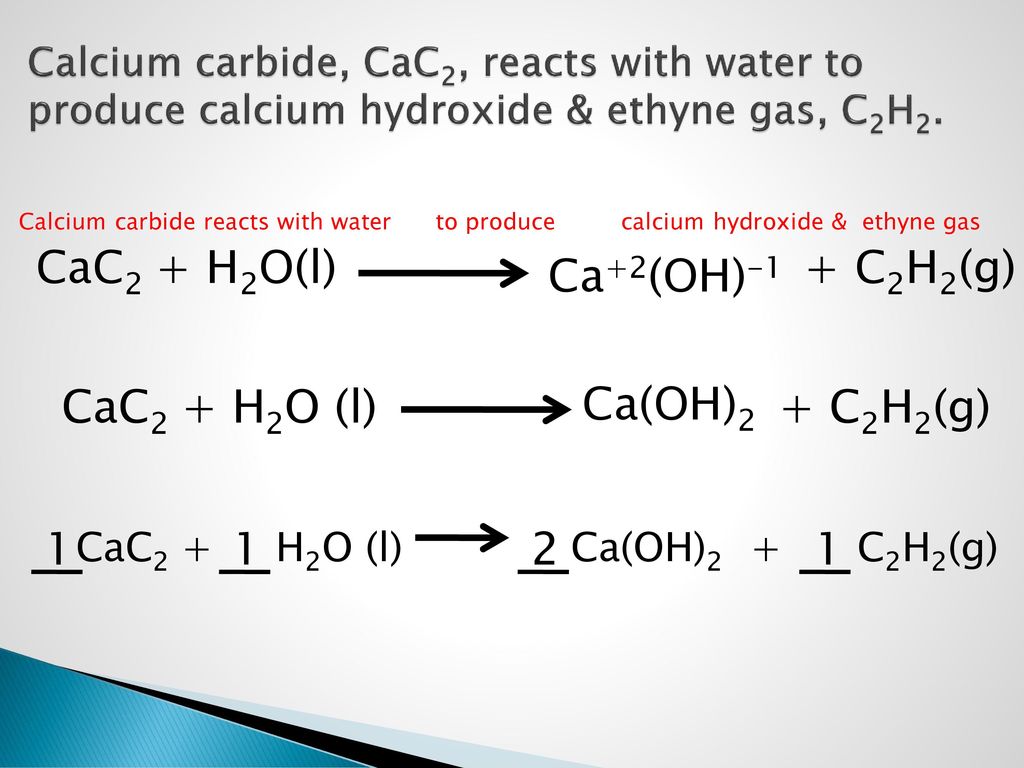
 Для начала настройте свой профиль и
выберите элемент ниже.
Для начала настройте свой профиль и
выберите элемент ниже.

 Эта экспериментальная функция ограничена только данными ERG. Испанские переводы будут добавлены позже.
Эта экспериментальная функция ограничена только данными ERG. Испанские переводы будут добавлены позже. ниже.
ниже.
 Будьте в курсе последней информации из следующего:
Будьте в курсе последней информации из следующего:



 ..
..


