Корродирование металла: Коррозия металлов — урок. Химия, 9 класс.
alexxlab | 29.11.1985 | 0 | Разное
Коррозия металлов — что это такое? Виды и примеры
Коротко о главном
Коррозия металлов или ржавление в химии — это явление, которое возникает из-за взаимодействия металлической пластинки с веществами окружающей среды (кислородом воздуха или кислотами, с которыми может реагировать металлическое изделие).
Обычно окисляются металлы, включая железо, которые находятся левее водорода в ряду напряжений.
Чаще всего встречаются химическая и электрохимическая коррозии. Чтобы понять, чем они отличаются друг от друга, давайте сравним их по нескольким критериям в таблице ниже.
Таблица 1. Сравнение химической и электрохимической коррозии металлов | ||
|---|---|---|
Признаки сравнения | Химическая коррозия | Электрохимическая коррозия |
Определение | Разрушение металлов в из-за взаимодействия с газами или растворами, которые не проводят электрический ток | Разрушение металла, при котором возникает электрический ток в воде или среде другого электролита |
Агрессивные реагенты | O2, пары H2O, CO2, SO2, Cl2 | Растворы электролитов |
Примеры | 3Fe + 2O2 → Fe3O4 | 4Fe + 3O2 + 6H2O = 4 Fe(OH)3 При контакте железа с цинком коррозии подвергается цинк: А (+) на цинке: Zn0 – 2e– = Zn2+. К (–) на железе: 2H+ + 2e– = H2. |
Защитить металл от коррозии можно по-разному: покрытием защитными материалами, электрохимическими методами, шлифованием и т. д. Далее — подробно обо всем этом.
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Что такое коррозия
Коррозия — это самопроизвольное разрушение элементов, чаще всего металлов, под действием химического или физико-химического влияния окружающей среды.
Иными словами, из-за химического воздействия железо начинает ржаветь. Это весьма сложный процесс, который состоит из несколько этапов. Но суммарное уравнение коррозии выглядит так:
4Fe + 6H2O (влага) + 3O2 (воздух) = 4Fe(OH)3.
Часто под коррозией понимают химическую реакцию между материалом и средой либо между их компонентами, которая протекает на границе раздела фаз. Обычно это окисление металла. Например:
Обычно это окисление металла. Например:
3Fe + 2О2 = Fe3O4;
Fe + H2SO4 = FeSО4 + Н2.
Некоторые металлы, даже активные, покрываются плотной оксидной пленкой при коррозии. Это одна из их характерных черт. Оксидная пленка не дает окислителям проникнуть в более глубокий слой и поэтому защищает металл от коррозии. Алюминий обычно устойчив при контакте с воздухом и водой, даже горячей. Тем не менее, если поверхность алюминия покрыть ртутью, то образуется амальгама. Она разрушает оксидную пленку, и алюминий начинает быстро превращаться в белые хлопья метагидроксида алюминия:
Коррозии подвергаются и многие малоактивные металлы. Например, поверхность медного изделия покрывается патиной — зеленоватым налетом. Это происходит потому, что на ней образуются смеси основных солей.
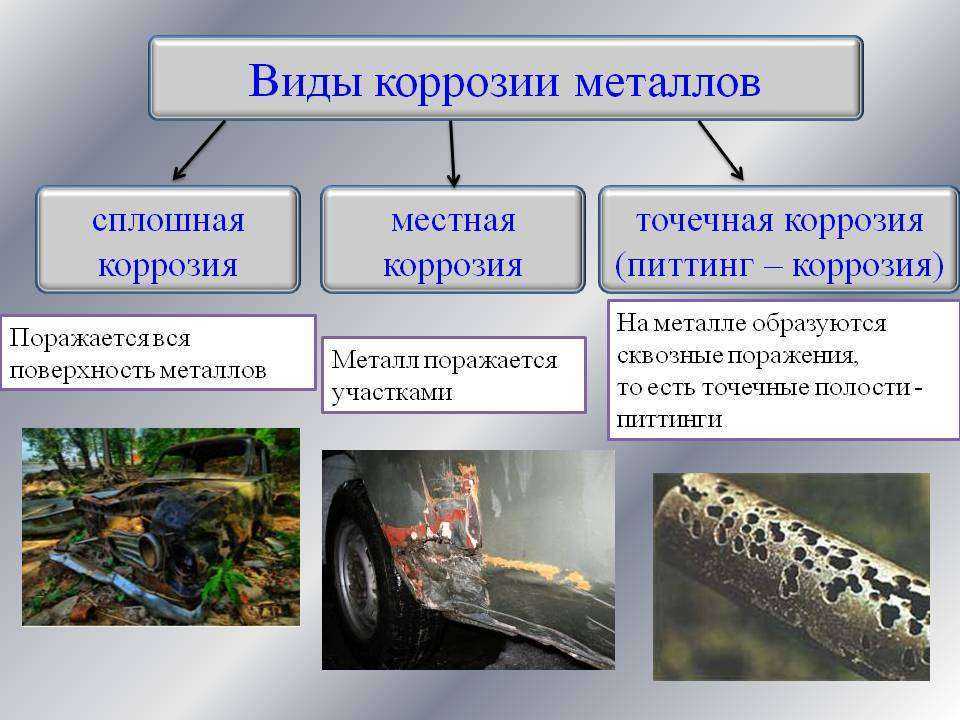
Виды коррозии металлов
Химическая коррозия
Химическая коррозия — это процесс разрушения металла, который связан с реакцией между металлом и коррозионной средой.
Химическая коррозия протекает без воздействия электрического тока, и в результате этой реакции металлы окисляются. Этот вид коррозии можно разделить на два подвида:
Их них более распространенной считают газовую коррозию. Она протекает во время прямого контакта твердого тела с активным газом воздуха. Чаще всего это кислород. В результате на поверхности тела образуется пленка продуктов химической реакции между веществом и газом. Дальше эта пленка мешает контакту корродирующего материала с газом. При высоких температурах газовая коррозия развивается интенсивно. Возникшая при этом пленка называется окалиной, которая со временем становится толще.
Важную роль в процессе коррозии играет состав газовой среды. Но для каждого металла он индивидуален и изменяется с переменой температур.
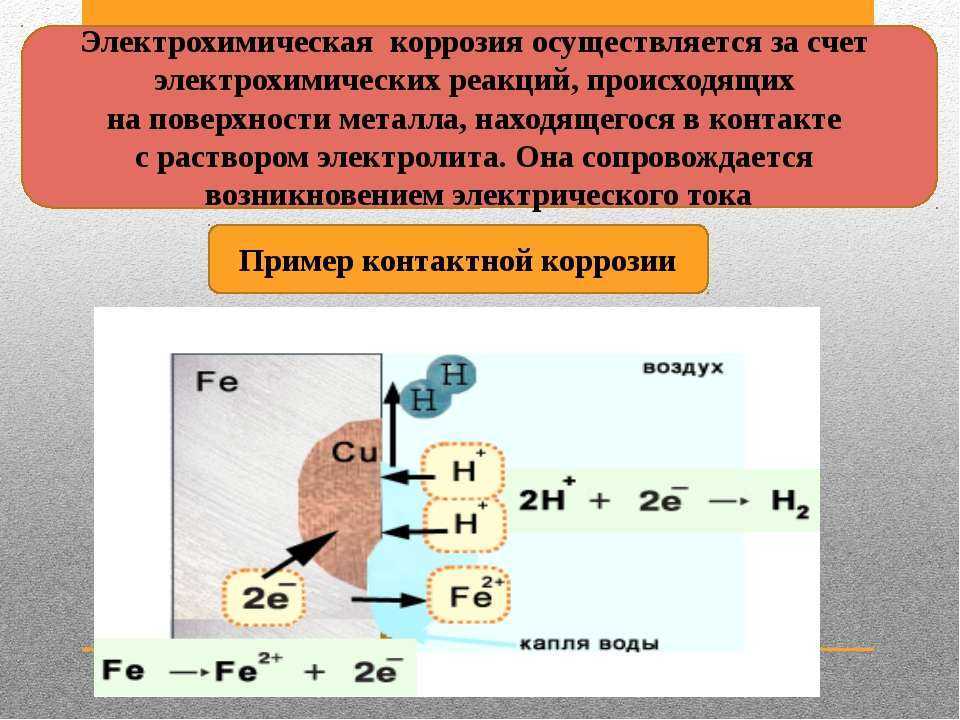
Электрохимическая коррозия
Электрохимическая коррозия — это разрушение металла, которое протекает при его взаимодействии с окружающей средой электролита.
Этот вид коррозии считают наиболее распространенным. Самым важным происхождением электрохимической коррозии является то, что металл неустойчив в окружающей среде с точки зрения термодинамики. Вот несколько ярких примеров этой реакции: ржавчина в трубопроводе, на обшивке днища морского судна и на различных металлоконструкциях в атмосфере.
Самым важным происхождением электрохимической коррозии является то, что металл неустойчив в окружающей среде с точки зрения термодинамики. Вот несколько ярких примеров этой реакции: ржавчина в трубопроводе, на обшивке днища морского судна и на различных металлоконструкциях в атмосфере.
В механизме электрохимической коррозии обычно выделяют два направления: гомогенное и гетерогенное. Разберем их подробнее в таблице ниже.
Гетерогенный механизм электрохимической коррозии | |
|---|---|
Поверхность металла рассматривается как однородный слой. | У твердых металлов поверхность неоднородна из-за структуры сплава, в котором атомы по-разному расположены в кристаллической решетке. |
Растворение металла происходит из-за термодинамической возможности для катодного или анодного процессов. | Неоднородность можно наблюдать при наличии в сплаве каких-либо включений. |
Скорость, с которой протекает электрохимическая коррозия, зависит от времени протекания процесса. |
В электрохимической коррозии протекает одновременно два процесса на аноде и на катоде, которые зависят друг от друга. Растворение основного металла происходит только на анодах. Анодный процесс заключается в том, что ионы металла отрываются и переходят в раствор:
Fe → Fe2+ + 2e.
В результате происходит реакция окисления металла. В данном случае анод заряжается отрицательно.
При катодном процессе избыточные электроны переходят в молекулы или атомы электролита, которые, в свою очередь, восстанавливаются. На катоде идет реакция восстановления. Он носит заряд положительного электрода.
O2 + 2H2O + 4e → 4OH–
2H+ + 2e → H2
Торможение одного процесса приводит к торможению и другого процесса. Окисление металла может происходить только в анодном процессе.
Окисление металла может происходить только в анодном процессе.
Учёба без слёз (бесплатный гайд для родителей)
Пошаговый гайд от Екатерины Мурашовой о том, как перестать делать уроки за ребёнка и выстроить здоровые отношения с учёбой.
Как защитить металлы от коррозии
От коррозии можно и нужно защищаться. Чтобы уберечь металлы от этой реакции, их покрывают защитными материалами, обрабатывают электрохимическими методами, шлифованием и т. д. Рассмотрим все эти способы подробнее.
Способ № 1. Защитные покрытия.
Для защиты от коррозии металлические изделия покрывают другим металлом, т. е. производят никелирование, хромирование, цинкование, лужение и т. д. Еще один вариант защиты — покрыть поверхность металла специальными лаками, красками, эмалями.
Способ № 2. Легирование.
Легирование — это введение добавок, которые образуют защитный слой на поверхности металла. Например, при легировании железа хромом и никелем получают нержавеющую сталь.
Способ № 3. Протекторная защита.
Протекторная защита — это способ уберечь металл от коррозии, при котором металлическое изделие соединяют с более активным металлом. Этот второй металл в итоге и разрушается в первую очередь.
Способ № 4. Электрохимическая защита.
Чтобы защитить металлы от электрохимической коррозии, нейтрализуют ток, который возникает при ней. Это делают с помощью постоянного тока, который пропускают в обратном направлении.
Способ № 5. Изменение состава среды путем добавления ингибиторов.
Для защиты от коррозии используют специальные средства, которые ее замедляют — ингибиторы. Они изменяют состояние поверхности металла — образуют труднорастворимые соединения с катионами металла. Защитные слои, образованные ингибиторами, всегда тоньше наносимых покрытий.
Способ № 6. Замена корродирующего металла на другие материалы: керамику и пластмассу.
Способ № 7. Шлифование поверхностей изделия.
Шлифование поверхностей изделия.
Проверьте себя
Что такое коррозия?
Где в повседневной жизни можно встретить ржавление железа и других металлов? Приведите примеры.
Гидроксид железа Fe(OH)3 называют:
а ржавчина;
б) окалина;
в) патина.
Что является причиной возникновения коррозии?
Чем отличаются химический и электрохимический типы коррозии?
Что такое коррозионная среда?
Узнайте все о коррозии металлов и разберитесь в других темах за 9 класс на онлайн-курсах по химии в Skysmart! Наши преподаватели помогут выяснить, где скрываются пробелы в знаниях, и восполнить их. Никаких скучных задач и сухих лекций — только интерактивные упражнения, опыты и теория простым языком. Все это поможет разобраться даже в тех темах, которые не давались в школе. Ждем на бесплатном вводном уроке!
Типы и виды коррозий металла — Короли Воды и Пара на vc.
 ru
ru175 просмотров
Коррозии металла
Сегодня мы с вами разберемся, узнаем многое про типы и виды коррозии металла. Изучим тему, узнав, откуда и из-за чего берётся коррозия на металле.
Откуда берётся, коррозия металла
Коррозия появляется из-за воздействия на него окружающей среды. Учёные выяснили, что это саморазрушение металлов и сплавов в ходе химических и физико-химических и электрохимических процессов. Так же есть практически аналогичный процесс, это разрушение металла методом физического воздействия, не надо его путать с коррозией, этот процесс называют: «эрозия» или же «износ».
Также стоит сказать, что на появление ржавчины сильнее всего содействует влажная среда. На появление ржавчины, как и на все химические процессы, влияет температура окружающей среды, даже если температура воздуха будет различаться всего на 5-10 градусов, то разница в скорости уже будет видна. Таким образом, появляется ржавчина, она бывает разных видов и ниже мы расскажем именно про это.
Типы и виды коррозии
Коррозию в основном различают на четыре основных типа, а именно: электрохимическая, химическая, водородная и кислородная.
Электрохимическая коррозия
Электрохимической коррозией называют разрушение металла, вследствие взаимодействия с коррозионной средой гальванических элементов. Для появления электрохимической коррозии обязательна наличие электролита, с которыми будут соприкасаться электроды и другие элементы. Если процесс проходит в воде и в нем растворены соли, то процесс идет намного быстрее.
Водородная и кислородная коррозия
Когда случается Восстановление ионов Н3О+ или же молекулы воды Н2О, это называют коррозией с водородной деполяризацией или же проще водородной коррозией. Такую коррозию чаще всего называют ржавчиной. Коррозия такого типа возникает во влажных местах либо же в водопроводных трубах (при скоплении конденсата). Каждый из нас видел коррозии такого типа, если не дома, то на улице уж точно.
Также коррозия может возникать, не только при прикосновении нескольких разных металлов. Элементы коррозии могут возникать и в случаи, если металл один. Если структура металла неоднородна, то она возникает также, так случается чаще ведь сейчас практически всегда в любом металле есть примеси в виде других металлов, это делается для экономии.
Химическая коррозия (при воздействии пара)
Химической коррозией считается ржавчина возникшая из-за касания и взаимодействия металла с средой которая полна активной коррозией, в отличии от электрохимической, процесс не идет совместно с электрохимическими реакциями и стоит на границе фаз. В отличии от остальных в этом виде есть и другие типы. Например жидкостная коррозия, газовая коррозия, атмосферная коррозия и так далее.
- Газовая коррозия (при воздействии пара) – Это коррозия, которая возникает из-за взаимодействия с активными газами, которые находятся в среде, где находится, металл. Для хода газовой коррозии обязательна высокая температура среды.
 Такими газами могут быть: Кислород, пары воды, пары серы и другие.
Такими газами могут быть: Кислород, пары воды, пары серы и другие. - Жидкостная коррозия – Ржавчина этого типа может появится из-за соприкосновения с активными жидкостями, например нефть, керосин, бензин или почти со всеми маслами.
Защита от появления коррозии
Вы, наверное, задаетесь вопросом: «Если есть такое множество видов коррозии и если ржавчина может возникнуть практически везде, то мы не придумали как защитить металлы?» И это логичный вопрос, ведь люди постоянно придумывают, как облегчить свою жизнь. Наш ответ да, люди всё таки придумали, как защищать металлы от коррозии, и этих методов великое множество, ниже мы расскажем про нескольких из них.
Металлическое покрытие
Это самый простой метод защиты, металл, покрывают защитным слоем, другого уже заведомо обработанного металлом, уж простите за тавтологию. Таким тонким слоем можно защитить металл от возникновения ржавчины, таких покрытии есть великое множество, например анодное покрытие и катодное покрытие. К сожалению, покрытие такого типа не защищает от коррозии, которая возникает водородным методом, то есть от пара, от воды и так далее.
К сожалению, покрытие такого типа не защищает от коррозии, которая возникает водородным методом, то есть от пара, от воды и так далее.
Химическое покрытие
Так же есть неметаллические покрытия для защиты металлов от ржавчины, химическое покрытие один из этих методов защиты, вот несколько из этих покрытий:
- Оксидирование;
- Фосфатирование;
- Азотирование;
- Воронение стали;
- Цементация.
Электрохимическая защита
В этом случае защита создаётся при помощи постоянного обеспечения током. Так же есть и другой метод электрохимической защиты, его называют Протекторной, при этой схеме К поверхности прицепляются другие куски металла уже обеспеченным защитой и это называют протектором.
Наши специалисты проконсультируют Вас и помогут в правильном подборе оборудования в паровые и пароконденсатные системы, во избежание появления коррозий.
Если у Вас остались вопросы, мы будем рады Вам помочь. С нами можно связаться любым удобным способом:
По почте: [email protected]
По телефону: +7 (343) 288-35-54 или WhatsApp
Подписывайтесь на наш Телеграм канал, там всегда много полезного и интересного.
Электрохимическая коррозия: причины, типы, скорость протекания
Электрохимическая коррозия относится к наиболее часто встречающимся процессам постепенного разрушения металла.
Как мы знаем, наше окружение наполнено электричеством.
В зависимости от среды, меняются показатели проводимости. Не отличается то, что при контакте с такой средой сталь начинает постепенно портиться.
У процесса есть несколько важных отличий.
В первую очередь – неодновременное протекание восстановления окислительного процесса и ионизации атомов металла.
На интенсивность распространения при этом влияет такой параметр, как электродный потенциал металла.
Главная причина электрохимической коррозии в том, что большинство металлов проявляют термодинамическую неустойчивость.
Примеры распространения коррозии такого типа встречаются в воде, почве, на открытом воздухе.
Она часто становится причиной потери прочности и постепенного разрушения металла на днище судов, трубопроводов, опор ЛЭП и других объектов.
Если говорить о типах электрохимической коррозии, то называют 3 разновидности:
- щелевые поражения;
- питтинги;
- межкристаллическое повреждение.
Повреждаться могут разные типы металлов в зависимости от их расположения. Ржавчина появляется при контакте со стоячей и текущей водой, в местах соединения разных металлов, а также на сварных швах.
Какие механизмы отвечают за протекание электрохимической коррозии
Такое повреждение металла проводится двумя механизмами – гомогенным и гетерогенным. Рассмотрим каждый из них подробно.
- Гомогенный. Первоначально затрагивается поверхностный слой металлического изделия. Постепенно металл начинает растворяться под действием актов – катодного или анодного.
 На протяжении определенного времени происходит миграция катода и анода. Со временем процесс ускоряется. Особенность гомогенного механизма в том, что затрагивает как твердые, так и жидкие металлы. Меняется только скорость течения.
На протяжении определенного времени происходит миграция катода и анода. Со временем процесс ускоряется. Особенность гомогенного механизма в том, что затрагивает как твердые, так и жидкие металлы. Меняется только скорость течения. - Гетерогенный. У большинства твердых металлов не наблюдается гомогенной поверхности. Это связано с тем, что в самом материале состав кристаллической решетки может отличаться. Также как и в описанном выше случае, формируется анодный и катодный процессы, металл начинает постепенно разрушаться.
У такого вида процесса есть несколько особенностей.
В первую очередь – четкое деление на катодный и анодный процесс. Один из основных факторов, влияющих на их скорость протекания относительно друг друга – это время.
Схема электрохимической коррозии
В зависимости от типа металла, коррозия может быть локализована на отдельных участках. Также наблюдается растворение поверхностного слоя на анодах, что позволяет поражению затронуть обширные площади.
Здесь появляется еще одна особенность протекания процесса – формирование гальванических элементов. Это происходит из-за специфики структуры поверхности, на которой присутствуют микроэлектроды.
Из-за чего начинает развиваться коррозия
После того, как мы рассмотрели суть электрохимической коррозии, пришло время обратить внимание на причины распространения коррозии.
Среди них три распространенные:
- Сплав имеет неоднородную структуру. В большинстве сплавов поверхность негомогенная, потому что в кристаллической решетке присутствуют посторонние включения. Ухудшает ситуацию и присутствие пор макро и микротипа. Это приводит к тому, что продукты коррозии также начинают образовываться неравномерно.
- Неоднородная среда, в которой находится металл. Чтобы коррозия протекла быстрее, важен фактор доступа окислителя. Электрохимическая реакция может быть ускорена.
- Отличие физических условий.
 Коррозия усиливается в том случае, если происходит облучение, в среде присутствуют блуждающие тока. Негативно влияет и температура, особенно при перепадах. В таком случае разница между холодными и теплыми местами становится причиной появления анода.
Коррозия усиливается в том случае, если происходит облучение, в среде присутствуют блуждающие тока. Негативно влияет и температура, особенно при перепадах. В таком случае разница между холодными и теплыми местами становится причиной появления анода.
Именно по причине различия в критических факторах, скорость электрохимической коррозии может сильно меняться.
Главные внутренние факторы протекания электрохимической коррозии
На интенсивность распространения коррозийного поражения влияют две группы факторов – внешние и внутренние.
Текущее состояние поверхности металла
Когда поверхность металла неровная, коррозийный процесс протекает намного интенсивнее. Если на поверхности присутствуют небольшие выступы, они начинают накапливать воду.
Это может негативно повлиять на интенсивность распространения.
Чтобы не допустить такого фактора, важно использовать отшлифованный или отполированный металл.
Когда сталь гладкая, вода не так сильно повреждает ее, потому что постепенно происходит формирование равномерной пленки по всей поверхности.
Также хорошим средством для уменьшения поражения становится применение пассивирования, а также ряд других способов.
Степень термодинамической стойкости металла
Разные виды материалов отличаются разными показателями термодинамической устойчивости.
Наиболее стойкие разновидности материала не разрушаются при помещении в агрессивную среду.
Чтобы понять, есть ли у металла склонность к коррозии под действием термодинамических факторов, измеряют потенциал анодного и катодного процесса, а также изобарно-изотермического.
Именно такой фактор оказывает большое влияние на потенциальное воздействие среды на постепенное развитие коррозии.
К сожалению, у большинства представленных в продаже марок металлов стойкость невысокая. Есть и неустойчивые разновидности, у которых этот риск нивелируется благодаря склонности к образованию пассивных пленок на поверхности.
Кристаллографическая структура
Оказывает прямое воздействие на металл.
Как известно, атомы в кристаллической решетке располагаются по-разному. Лучше защищены те разновидности, у которых атомы упакованы неплотно.
Особенности решетки также учитывают при планировании защиты материала методом создания на нем специальных пленок. И пленка и сам основной материал должны четко соответствовать по составу друг другу или быть максимально приближенными.
В этом случае исключается появление напряжения, которое негативно отражается на текущем состоянии заготовки. Если контакт с агрессивной средой все-таки происходит, материал начинает разрушаться слой за слоем.
ГетерогенностьЭтот фактор рассматривается в непосредственной связи с величиной зерна металла.
Если в сплаве есть выраженные анодные включения, они сильно влияют на ускорение протекания коррозии.
Катодные включения не столь опасны, потому что на интенсивности процесса не отражаются. Величина зерна как фактор риска рассматривается не так часто и этим показателем можно пренебречь.
Не стоит сбрасывать со счетов и механические факторы
Важно понимать, что многие конструкции из металла используются под постоянным напряжением.
К этой категории относится повышенное внутреннее напряжение, когда сильно увеличивается риск деформации.
Негативно влияют на качество металла также воздействие истирания, периодические контакты с другими металлическими изделиями.
Такой фактор оказывает значительное влияние на интенсивность распространения повреждения.
Даже если само сырье первоначально обладало стойкостью к потенциальным повреждениям, в таком случае она уменьшится – формируемые пленки просто не будут закрепляться на поверхности.
Потому лучше сразу исключить это условие электрохимической коррозии – постараться не использовать металлоконструкции под пиковыми сильными нагрузками, не допускать возникновения трения и соприкосновения между собой стальных деталей.
Основные внешние факторы электрохимической коррозии
Кроме внутренних, на металл также влияют и внешние факторы.
Они могут не только ускорять, но и замедлять процесс, а также влиять на характер его протекания.
К ним относятся следующие:
- Температура. Температура сильно влияет на то, как себя ведет металл в разных условиях. От нее сильно зависит то, насколько быстро будут растворяться вторичные продукты коррозии. Среди других особенностей – запуск и стимуляция диффузионных процессов в металле, создание перенапряжения на электродах и другие проявления. Когда металлическое изделие помещается в растворы с кислородной деполяризацией, по мере прогрева электролита диффузия окислителя ускоряется. На фоне этого наблюдается сильное снижение перенапряжения ионизации кислорода.
Если деталь помещается в растворы неокисляющихся кислот, наблюдается коррозия с водородной деполяризацией.
Повышение температуры уменьшает скорость распространения повреждений, потому что сильно снижается перенапряжение водорода.
Отдельно стоит отметить ситуацию, когда металл уже покрывается специальной защитной пленкой. В этом случае сам тип пленки будет влиять на то, как именно она поведет себя при контакте с разными видами внешних угроз, в том числе, с повышением температуры.
В этом случае сам тип пленки будет влиять на то, как именно она поведет себя при контакте с разными видами внешних угроз, в том числе, с повышением температуры.
Нагрев и охлаждение могут отразиться на состоянии катодов и анодов через их внутренние процессы.
В некоторых случаях полярность электродов значительно меняется.
Как мы уже отмечали выше, проблемы могу возникать из-за того, что разные участки детали нагреты до отличающихся друг от друга температур.
В этом случае стремительно увеличивается количество термогальванических пар, стимулирующих распространение коррозии на новые участки.
- Уровень рН раствора, в который помещен металл. Такой показатель как рН указывает, насколько в растворе будут активными ионы водорода, и как быстро коррозия будет распространяться по материалу. Это опасно, потому что может непредсказуемо менять потенциал катодных процессов, формирование окисных пленок. Также создается значительное перенапряжение реакции на электродах.
 Рекомендуется не допускать контакта металла со средами, у которых показатель рН высокий.
Рекомендуется не допускать контакта металла со средами, у которых показатель рН высокий.
Если по каким-то причинам металлическая заготовка оказалась помещена в раствор, большое значение будет иметь скорость, с которой он движется, а также само наличие внутренних колебаний.
Заранее определить точное воздействие будет сложно по той причине, что всегда непросто предсказать, как поведут себя нейтральные электролиты.
Cчитается, что при смешении электролита, меняются показатели диффузии кислорода, что значительно отражается на процессе протекания коррозии.
Можно уделять меньше внимания скорости движения электролита в том случае, если вы имеете дело со средами повышенной кислотности.
На них подобное поражение оказывает минимум влияния.
Чем отличаются анодный и катодный процессы
Если вы внимательно проследите за тем, как работает гальванический элемент, то увидите, что в нем протекают сразу два связанных друг с другом процесса – анодный и катодный.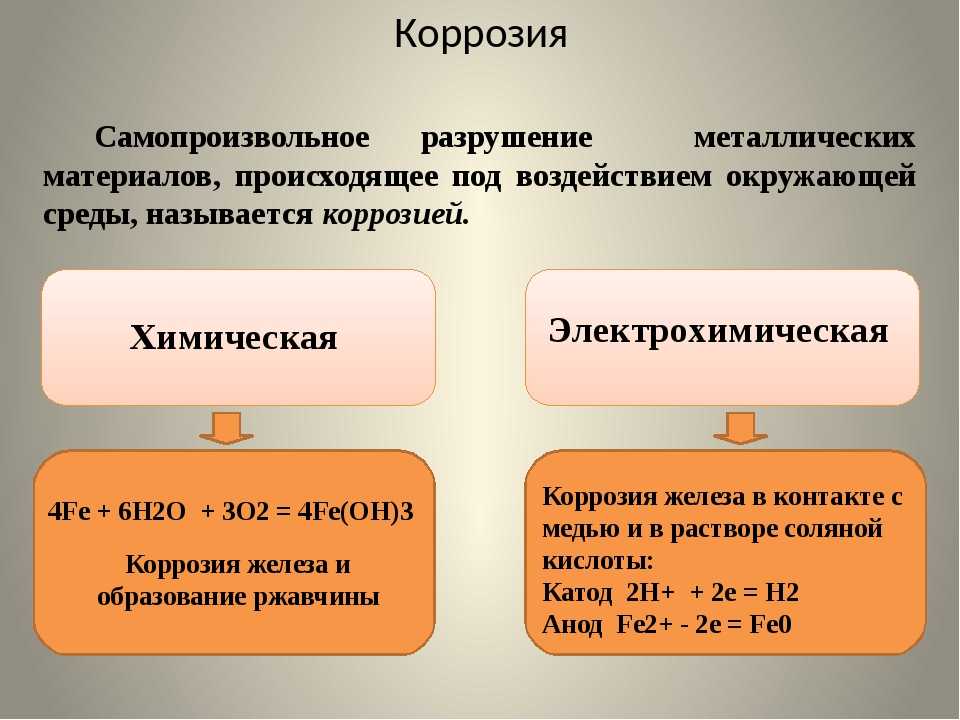
Рассмотрим их более подробно.
Анодный процесс
В химии показывается формулой Fe → Fe2+ + 2e. Она показывает, что постепенно запускается окисление, ионы металла начинают переход в раствор.
Катодный процесс
Может протекать по-разному.
В частности, переизбыток электронов решается ассимиляцией атомами электролита и его молекул. На фоне этого происходит восстановительная реакция непосредственно на самом катоде.
Формула будет зависеть от того, в каких условиях протекает реакция.
Так при наличии водородной деполяризации можно записать процесс как 2 H+ + 2e → h3.
Важно понимать, что оба процесса сильно связаны друг с другом под влиянием кинетического фактора.
С течением времени может происходить взаимное замедление или ускорение анодного или катодного процесса. При этом сам анод всегда будет оставаться тем местом, на котором формируется коррозия металла.
Во время анализа протекания процесса коррозии часто обращают внимание на электропроводящие фазы и момент после их соприкосновения.
Обычно одна фаза имеет положительный заряд, в то время как другая – отрицательный. Это приводит к появлению разности потенциалов.
Таким образом возникает ДЭС или как его часто называют ученые – двойной электрический слой с ассиметричным расположением частиц в местах, где фазы разделяются.
Опасным для металла становится скачок потенциалов. Он может стимулироваться двумя центральными причинами:
- Большая накопленная энергия гидратации. В таком случае наблюдается отрыв ионов металла и постепенное перетекание их в раствор. На поверхности в результате остается аналогичное число электронов, заряд становится отрицательным. Далее, в соответствии с законами физики, наблюдается перетекание катионов из раствора, формируется ДЭС на границе, как мы уже описывали выше.
- Разряжение катионов электролита. В результате металл начинает стремительно принимать положительный заряд. ДЭС появляется из-за активности анионов раствора в контакте с катионами электролита.

Что происходит в том случае, если поверхностный слой металла совсем не имеет определенного заряда?
В таком случае ДЭС наблюдаться не будет, возникнет явление нулевого заряда.
Его потенциал будет отличаться в зависимости от того, с каким металлом вам приходится работать.
Описанный процесс значительно отражается на том, как протекает коррозия и как быстро она захватывает все новые и новые участки металла.
В современной науке нет средств, которые могли бы точно измерить величину скачка потенциала, значит и процесс формирования электродвижущей силы оказывается на таким интенсивным.
Если рассматривать вопросы, связанные с процессом поляризации, можно написать отдельную статью на эту тему.
Потому далее мы рассмотрим другой важный показатель – поляризацию.
Поляризация и ее влияние на скорость протекания коррозии
Процесс поляризации связан с интенсивностью распространения электрохимической коррозии.
Этот показатель отражает, насколько сильное перенапряжение наблюдается на определенном участке.
Принято выделять три вида поляризации:
- Электрохимическая. Чаще всего наблюдается в ситуации, когда катодный и анодный процессы начинают замедляться.
- Фазовая. Возникает в том случае, если на поверхности материала формируется новая фаза.
- Концентрационная. Этот процесс появляется в том случае, если есть очень малые показатели скорости отвода продуктов коррозии, а также подхода деполяризатора.
Особенности поляризации также стоит учитывать в том случае, если вы заинтересованы в дополнительной защите металлов от постепенного разрушения.
Обеспечиваем эффективную защиту от коррозии
Наша компания предлагает заказчикам защиту металлоконструкций разных типов от коррозии.
Мы используем методику горячего цинкования.
В пользу работы с нами говорит сразу несколько факторов:
- Опыт работы с 2007 года, есть постоянные заказчики.

- Большие производственные площади. Три цеха для горячего цинкования, мощность 120 тысяч тонн в год.
- Универсальность. Работаем со множеством видов изделий благодаря установленной на предприятии самой глубокой ванны в ЦФО – 3,43 метра.
Мы используем в процессе проверенное европейское оборудование. Даем гарантию соответствия качества товаров требованиям ГОСТ 9.307-89.
Чтобы получить дополнительные консультации и ответы на интересующие вас вопросы, звоните нам или оставляйте заявку на сайте.
Вернуться к статьям
Поделиться статьей
Коррозия металла
Черный металл
- Статьи
Отправить заявку 24/7
Коррозия металла, в простонародье называемая ржавчиной, – это распад металла на химические соединения, которые входят в его состав. Чаще всего это происходит под воздействием неблагоприятных условий окружающей среды.
В мире не существует такого металла, который не может быть подвержен коррозии. Даже такие металлы как золото и серебро, при определенных условиях, распадаются на составляющие. Например, при воздействии на них высоких температур или некоторых видов кислот.
Даже такие металлы как золото и серебро, при определенных условиях, распадаются на составляющие. Например, при воздействии на них высоких температур или некоторых видов кислот.
От коррозии страдают не только металлоконструкции зданий и сооружений, но и изделия из металла, с которыми человек каждый день сталкивается в быту. Например, ВГП трубы. Какую бы качественную очистку не проходила вода, попадая в дома и квартиры через старый водопровод, она может нанести существенный вред здоровью человека. Вместе с водой в организм могут попасть тяжелые металлы, с которыми она соприкасалась. Поэтому так важен своевременный ремонт и замена водопровода.
Несмотря на то, что для обычного человека ржавчина всегда одинакова, коррозия металла может быть нескольких видов.
- Химическая коррозия. Разнообразные газы, которые часто встречаются в окружающей среде, могут вступать во взаимодействие с металлом. Так происходит химическая коррозия. Яркий пример, это потемнение серебра.
 Если в окружающей среде избыток серного газа, то он вступает в реакцию с серебром, изменяя его структуру и цвет.
Если в окружающей среде избыток серного газа, то он вступает в реакцию с серебром, изменяя его структуру и цвет. - Электрохимическая коррозия. Этот вид коррозии встречается чаще всего. В его образовании повинно сразу несколько факторов. Под действием перепада температур и разных атмосферных факторов, прочность металла ухудшается. Появляются микро трещинки и пористость. При попадании в трещинки влаги, в порах скапливается вода. При воздействии с газами она превращается в некое подобие электролита. Таким образом, происходит электрохимическая коррозия.
Такой вид коррозии наиболее опасен, так как разрушение происходит изнутри, и протекает незаметно. Очень часто, именно благодаря этому виду коррозии неожиданно разрушаются дома и ломаются технические детали.
Защита от коррозии
Самым распространенным способом защиты от коррозии металлопроката в промышленности являются цинкование и порошковая окраска.
Цинкование
Технология цинкования заключается в нанесении равномерного тонкого слоя цинка на поверхность изделия. Цинк, благодаря своим химическим свойствам, препятствует контакту основного металла со средами, способными привести к его разрушению. Оцинкованный лист гораздо более устойчив к коррозии, чем лист из черного металла.
Цинк, благодаря своим химическим свойствам, препятствует контакту основного металла со средами, способными привести к его разрушению. Оцинкованный лист гораздо более устойчив к коррозии, чем лист из черного металла.
В зависимости от формы изделия и его использования различают два способа нанесения:
- горячее цинкование,
- холодное.
При горячем цинковании поверхность тщательно очищается от загрязнений и окалины, а затем обезжиривается, чтобы обеспечить максимально прочный контакт. После подготовительного этапа прокат или готовая деталь опускается в расплавленный цинк на 3-10 минут, после чего вынимается и просушивается.
Холодное цинкование также начинается с этапа очистки, но в дальнейшем производится за счет нанесения специального цинксодержащего состава с помощью краскопульта или валика/кисти. Несмотря на то, что этот способ не может обеспечить такого же высокого качества покрытия, горячий метод в ряде случаев использовать не представляется возможным. При этом, папример, нанести цинковое покрытие холодным способом на различные металлоконструкции можно без их демонтажа.
При этом, папример, нанести цинковое покрытие холодным способом на различные металлоконструкции можно без их демонтажа.
Главным недостатком цинкования как такового является невозможность дальнейшего использования обработанного изделия для сварки, так как из-за воздействия высоких температур защитное покрытие разрушается и перестает выполнять свои функции.
Порошковая окраска
Также является достаточно популярным методом защиты, дополнительно позволяющим улучшить эстетические качества изделия или конструкции.
В отличие от лакокрасочного защитного покрытия, нанесение порошковой краски требует соблюдения более сложной техники. Так для распыления используется специальный электростатический распылитель, позволяющий добиться равномерного распределения красящего порошка по металлической поверхности.
Для закрепления краски деталь поступает в камеру полимеризации, где под действием температуры в 150-200 градусов Цельсия синтетический красящий состав сплавляется в прочное защитное покрытие. Наиболее простым примером его использования является цветной профнастил.
Наиболее простым примером его использования является цветной профнастил.
Как и цинкование метод порошковой покраски способен надежно защитить обрабатываемую поверхность от коррозии, но выбирать используемый способ защиты, прежде всего, следует, сходя из дальнейшего использования обрабатываемого металлоизделия.
- Сравнение стальной и композитной арматуры
С появлением более современных синтетических материалов металлическ…
ЧИТАТЬ ДАЛЕЕ
- Сортамент гладкой арматуры и ее применение
Сталь…
ЧИТАТЬ ДАЛЕЕ
- Выбор профнастила для кровли
В одной из предыдущих публикации мы детально рассказали о том, как …
ЧИТАТЬ ДАЛЕЕ
- Виды и использование сварной сетки
Сварная сетка – это «полотно», сформированное из …
ЧИТАТЬ ДАЛЕЕ
- Расчет веса стального шестигранника
Стальной шестигранник – одна из разновидностей сортового прок…
ЧИТАТЬ ДАЛЕЕ
- Виды труб для водопровода.
 Какие выбрать? Что учесть при монтаже?
Какие выбрать? Что учесть при монтаже?Широкий ассортимент – палка о двух концах. С одной стороны он…
ЧИТАТЬ ДАЛЕЕ
- Сталь профнастила и варианты защитных покрытий
Профнастил, он же профлист, пользуется достаточно высоким спросом в…
ЧИТАТЬ ДАЛЕЕ
- Правильное крепление профлиста на крышу
Профлист, он же профилированный лист или профнастил, в последние го…
ЧИТАТЬ ДАЛЕЕ
- Что лучше, швеллер или двутавр? Какой прокат прочнее?
Двутавр и швеллер можно считать одними из самых популярных разновид…
ЧИТАТЬ ДАЛЕЕ
- Стальная полоса как элемент заземляющего контура
С ростом количества разнообразной потребительской электроники в каж…
ЧИТАТЬ ДАЛЕЕ
- Метизы на все случаи жизни
Строго говоря, термин «метизы» (аббревиатура от «…
ЧИТАТЬ ДАЛЕЕ
- Расчет веса вязальной проволоки
Расчет веса проволоки, в основном, может потребоваться в двух ситуа.
 ..
..ЧИТАТЬ ДАЛЕЕ
- Проверка качества и герметичности сварного шва труб и конструкций
К монтажу металлопроката предъявляются достаточно жесткие требовани…
ЧИТАТЬ ДАЛЕЕ
- Особенности использования швеллера при обвязке фундамента
Швеллер – это одна из разновидностей фасонного проката, отлич…
ЧИТАТЬ ДАЛЕЕ
- Гнутый стальной уголок: ГОСТ, виды, применение
Гнутый стальной уголок – не самый популярный, но все же доста…
ЧИТАТЬ ДАЛЕЕ
- Коррозия металла
Коррозия металла, в простонародье называемая ржавчиной, – это распа…
ЧИТАТЬ ДАЛЕЕ
- Когда и зачем нужно использовать металлические трубы для прокладки кабелей и проводов
Трубный прокат имеет достаточно обширное применение, в том числе ис…
ЧИТАТЬ ДАЛЕЕ
- Доставка, приемка и правильное хранение арматуры
Стальная арматура является незаменимым атрибутом практически любого…
ЧИТАТЬ ДАЛЕЕ
- Технология резки металла лазером
.
 ..
..ЧИТАТЬ ДАЛЕЕ
- Профнастил для всех
Профнастил…
ЧИТАТЬ ДАЛЕЕ
- Инструкция о порядке приемки продукции по количеству П-6
Утверждена постановлением Госарбитража при Совете Министров СССР от…
ЧИТАТЬ ДАЛЕЕ
- Колючая проволока для войны и мира
Для современного человека колючая проволока — предмет накрепко ассо…
ЧИТАТЬ ДАЛЕЕ
- Металлоконструкции
Современный индустриальный пейзаж нево…
ЧИТАТЬ ДАЛЕЕ
- Стальной рифленый лист: стандарты, виды, размеры, вес, использование
Рифленый лист – разновидность листового металлопроката, отлич…
ЧИТАТЬ ДАЛЕЕ
- Металлопрокат – материалы и технологии
Металлопрокат — это строго говоря, тот самый материал который опред…
ЧИТАТЬ ДАЛЕЕ
- Бесшовные трубы – производство и применение
…
ЧИТАТЬ ДАЛЕЕ
- Характеристики и применение просечно-вытяжного листа
Ассортимент производимых металлоизделий, даже без учета типоразмеро.
 ..
..ЧИТАТЬ ДАЛЕЕ
- Сварочные электроды УОНИ: особенности, характеристики, использование
Современный рынок предлагает широкий выбор различной продукции для …
ЧИТАТЬ ДАЛЕЕ
- Порошковая окраска металлических изделий
Окраска для металлических изделий — процедура совершенно необходима…
ЧИТАТЬ ДАЛЕЕ
- Пробивка отверстий в металле: особенности технологии
Пробивка отверстий в металле является одним из методов перфорации. …
ЧИТАТЬ ДАЛЕЕ
- Спецсталь: состав, изготовление, обработка
Новые отрасли промышленности, бурно развившиеся во второй половине …
ЧИТАТЬ ДАЛЕЕ
- Проволока гост 3282-74
Стальная проволока – самое простое и широко известное изделие из м…
ЧИТАТЬ ДАЛЕЕ
- Рубка металла: от зубила до станка
Рубка металла – один из основных способов металлообработки, п…
ЧИТАТЬ ДАЛЕЕ
- Соединение швеллеров: способы и методика
За счет своей формы, имеющей перпендикулярные ребра жесткости, швел.
 ..
..ЧИТАТЬ ДАЛЕЕ
- Металлическая сетка – виды и производство
Металлические сетки — один из наиболее востребованных видов стальны…
ЧИТАТЬ ДАЛЕЕ
- Монтаж профильной трубы: способы и необходимые принадлежности
Профильная труба – один из самых удобных вариантов металлоп…
ЧИТАТЬ ДАЛЕЕ
- Инструкция о порядке приемки продукции по качеству П-7
Утверждена постановлением Госарбитража при Совете Министров СССР от…
ЧИТАТЬ ДАЛЕЕ
- Зачем нужна стальная двутавровая балка?
…
ЧИТАТЬ ДАЛЕЕ
- Как марка стали бесшовных труб влияет на их применение
Использование любой разновидности металлоизделий зависит сразу от н…
ЧИТАТЬ ДАЛЕЕ
- Катанка и проволока — производство и использование
Проволока — один из самых востребованных видов изделий из металла. …
ЧИТАТЬ ДАЛЕЕ
- Что такое сортовой металл, и чем он отличается от других
Всю массу выпускаемого производителями металлопроката можно раздели.
 ..
..ЧИТАТЬ ДАЛЕЕ
- Профильная труба – материалы, производство, применение
Трубный металлопрокат предназначен не только для создания трубопров…
ЧИТАТЬ ДАЛЕЕ
- Технология соединения двутавров
Двутавр, он же …
ЧИТАТЬ ДАЛЕЕ
- Типы и марки сварочных электродов
Сварка металлов при помощи вольтовой дуги появилась в XIX веке и ст…
ЧИТАТЬ ДАЛЕЕ
- Производство и характеристики двутавровой балки
…
ЧИТАТЬ ДАЛЕЕ
- Способы цинкования металла
Железо и сталь — это материал из которого изготовлен скелет совреме…
ЧИТАТЬ ДАЛЕЕ
- Сварные трубы – технология, применение, достоинства
ХХI век – это век трубопроводов. Труб для нефте- и газотранспортных…
ЧИТАТЬ ДАЛЕЕ
- Сортамент металлопроката: основные виды, определения и ГОСТы
Сортамент металлопроката, выпускаемого современной промышленностью …
ЧИТАТЬ ДАЛЕЕ
- Швеллер — использование и нагрузка
Швеллер — это один из видов фасонного стального проката.
 В поперечн…
В поперечн…ЧИТАТЬ ДАЛЕЕ
- Назад
- Вперёд
Недостаточно прав для комментирования
Спасибо за обращение! Заявка отправлена.
Коррозия металлов | Статья в журнале «Молодой ученый»
Библиографическое описание:Чепкасова, О. А. Коррозия металлов / О. А. Чепкасова, А. А. Селезнева, А. И. Садилов, С. В. Хмелев. — Текст : непосредственный // Молодой ученый. — 2015. — № 23 (103). — С. 260-261. — URL: https://moluch.ru/archive/103/23845/ (дата обращения: 25.09.2022).
В статье рассмотрены основные вопросы процесса коррозионного повреждения металла, виды коррозии и коррозионных разрушений, способы защиты от коррозии.
Ключевые слова: остаточный ресурс, коррозия металлов, защита от коррозии.
Основным критерием оценки остаточного ресурса технического устройства (далее ТУ) являются прочностные характеристики, определяемые расчётами. Расчёт прочностных характеристик зависит от марки материала, геометрических параметров, толщины элементов ТУ. При проектировании ТУ учитываются все эти параметры с учётом допусков, проектной скорости коррозии, сроков и условий эксплуатации. Однако в процессе эксплуатации ключевым фактором, влияющим на пригодность ТУ является коррозионное повреждение металла, скорость которого может отличаться от проектной в несколько раз. Для определения прогнозируемых сроков эксплуатации ТУ необходима оценка скорости коррозии в конкретных условиях эксплуатации, а так же возможность влиять на неё с целью увеличения этих сроков. Для решения этих вопросов необходимо понимание самих процессов протекания коррозии, природы и сути процесса.
Коррозия — это разрушение металла под действием окружающей среды. По механизму протекания различают два типа коррозии — химическую и электрохимическую. Химическая коррозия начинает влиять на металл сначала его происхождения. Окалина ее продукт. Взаимодействие металла и окружающей среды протекает постоянно, химические процессы, проходящие при этом взаимодействии можно назвать борьбой за выживание, наша задача свести потери металла в этой борьбе к минимуму.
По механизму протекания различают два типа коррозии — химическую и электрохимическую. Химическая коррозия начинает влиять на металл сначала его происхождения. Окалина ее продукт. Взаимодействие металла и окружающей среды протекает постоянно, химические процессы, проходящие при этом взаимодействии можно назвать борьбой за выживание, наша задача свести потери металла в этой борьбе к минимуму.
По характеру агрессивной среды различают атмосферную коррозию, подземную и подводную.
Виды коррозионных разрушений разнообразны — равномерная коррозия, неравномерная, коррозия пятнами, коррозия язвами, подповерхностная коррозия, точечная или питтинговая, структурно-избирательная коррозия, межкристаллитная коррозия (этот самый опасный вид коррозии, обусловленный сложностью выявления). Последствия скрытно протекающих коррозионных процессов зачастую приводят к авариям, которых могло бы и не быть.
Химическая коррозия — это процесс разрушения металла под действием внешней среды, не сопровождаемая образованием электрического тока. Ее разновидность газовая коррозия, представляет собой процесс взаимодействия газов при высокой температуре с металлом. При таком взаимодействии образуется оксидная пленка, на железе она рыхлая, легко отскакивает и не защищает от разрушения.
Ее разновидность газовая коррозия, представляет собой процесс взаимодействия газов при высокой температуре с металлом. При таком взаимодействии образуется оксидная пленка, на железе она рыхлая, легко отскакивает и не защищает от разрушения.
В отличии от химической — электрохимическая коррозия протекает при контакте металла с раствором электролита. При этом электролитом может являться любая жидкость или газ. Примером электрохимической коррозии может быть атмосферная коррозия. Электрохимическая коррозия, более трудно прогнозируемая, чем химическая, ввиду необходимости учёта множества факторов, зачастую изменяющихся в процессе эксплуатации ТУ. При этом скорость протекания процессов электрохимической коррозии на порядок больше чем при химической коррозии.
В одних случаях на поверхности металла может образоваться плотная оксидная пленка, выполняющая роль защитного слоя. Образовавшаяся оксидная пленка предохраняет металл от разрушения. Это явление широко используется в современной технике, как способ защиты от коррозионных процессов.
Существует немало способов защиты от коррозии. Самый лучший из них создание такого металла, который бы вообще не корродировал. Один из путей создания коррозионностойкого металла — получение особых сплавов, в которые добавляют хром, никель, молибден, титан и другие компоненты. Так называемое легирование. Технология создания таких сплавов трудоемка, и связана с повышенными экономическими затратами. Цена таких материалов выше и не всегда целесообразно применение их в конкретных условиях.
Ингибирование — способ, при котором скорость коррозии снижается, если в агрессивную среду ввести соединения, значительно замедляющие коррозионный процесс. Одним из механизмов ингибирования является адсорбция ингибитора на поверхности защищаемого изделия. Ингибируемые бумаги и пленки применяются при долговременном хранении.
Различают металлические и неметаллические защитные покрытия, изолирующие металл от агрессивной среды. Большие детали или трубы защищают методом металлизации. Плакирование — метод защиты металла от коррозии другим металлом, который устойчив к агрессивной среде.
Плакирование — метод защиты металла от коррозии другим металлом, который устойчив к агрессивной среде.
Трубы газо- и нефтепроводов защищаются комбинированным способом, мазутно-битумное покрытие, ингибированная бумага и одновременно с этим катодная защита. Сущность электрозащиты состоит в том что, на катод, которым является сам трубопровод, накачиваются электроны от внешнего источника тока, и это тормозит коррозию. Анодом в этом случае может служить любой ненужный металл. Так же широко сейчас применяются различные плёнки на основе полиэтилена, внутренняя поверхность так же защищается различными покрытиями на основе керамики. Сварные стыки также защищаются от взаимодействия с перекачиваемой средой различными способами.
При защите ТУ применяется метод протекторной защиты. Протектор — активный металл, с более отрицательным потенциалом, например цинк, который разрушаясь сам, защищает объект.
Надежным способом зашиты от коррозии, являются гальванические покрытия, которые получают электролизом в водных растворах.
Неметаллические покрытия — это покрытия лаками, красками, различными силикатными эмалями и полимерными материалами. Покрытие силикатными эмалями широко применяется в химической промышленности. Кислотостойкие эмали применяют для покрытия вакуумных аппаратов, резервуаров, реакторов.
Затраты на защиту металла от коррозии оправданы и дают хороший экономический эффект, с учётом снижения затрат на замену непригодного ТУ. Где то, например подземные трубопроводы с агрессивной средой, она просто необходима для безопасной эксплуатации.
При проведении экспертизы промышленной безопасности технических устройств, применяемых на опасных производственных объектах, одной из важнейших задач является определение скорости коррозии и прогнозирование этой скорости на планируемый период эксплуатации. Мероприятия по антикоррозионной защите могут значительно увеличить срок эксплуатации и, как следствие, снизить затраты на замену ТУ.
Литература:
-
Материаловедение и технология металлов.
 / Ф. Гарифуллин, Г. Фетисов. — Издательство: Оникс. 2009. 624 с.
/ Ф. Гарифуллин, Г. Фетисов. — Издательство: Оникс. 2009. 624 с.
- Коррозия и защита от коррозии. / Семенова И. В., Флорианович Г. М., Хорошилов А. В. — Издательство: М.: Физматлит. 2002. 335 с.
Основные термины (генерируются автоматически): агрессивная среда, электрохимическая коррозия, коррозия, способ защиты, химическая коррозия, атмосферная коррозия, коррозионное повреждение металла, остаточный ресурс, процесс эксплуатации, скорость коррозии.
Методы защиты коррозии | Статья в журнале «Молодой ученый»Коррозия – это самопроизвольный процесс разрушения материалов и изделий из них под химическим воздействием окружающей среды. Коррозия металлов – разрушение металлов вследствие физико-химического воздействия внешней среды. ..
..
Влияние
коррозии на прочность оборудования | Статья в журнале…Коррозией металлов называют самопроизвольное разрушение металлических материалов вследствие химического или электрохимического взаимодействия их с окружающей средой. Коррозионный процесс протекает на границе раздела двух сред металла и окружающей…
Методы борьбы с коррозией. Плазменное электролитическое…осадком, газовая коррозия, коррозионная эрозия, щелевая коррозия и т.д. [4]. Все это приводит к необходимости защиты оборудования от воздействия агрессивных сред, созданию новых и совершенствованию старых способов защиты.
К вопросу оценки
скорости коррозии технических устройств…В данной работе рассмотрены методы оценки и определения скорости коррозии технологического оборудования в зависимости от условий его эксплуатации при осуществлении технического диагностирования оборудования в нефтеперерабатывающей и нефтехимической…
Способы изменения конструкции устройства для снижения…Обработка коррозионной среды. В случае электрохимической коррозии она сводится к уменьшению содержания деполяризаторов
Основные термины (генерируются автоматически): металл, коррозионная среда, слой, материал, коррозия, окружающая среда, схема строения. ..
..
Электрохимическая коррозия. Коррозионный процесс, разрушающий металл, в следствие
Электрохимическая коррозия наблюдается при протекании следующих процессов: − анодного, образование ионов металла в электролите и некомпенсированных электронов
Ингибирование
коррозии стали 20Л в хлоридсодержащих средахКлючевые слова: коррозионная стойкость, ингибиторы коррозии, скорость коррозии, ингибирующий эффект.
Об эффективной защите сталей в различных агрессивных средах ингибированием коррозионного процесса органическими гетероциклическими соединениями. ..
..
Лабораторные
методы измерения и приборы контроля коррозииСреднее значение глубины коррозионного поражения при равномерной коррозии можно вычислить с помощью массометрического показателя скорости коррозии ; . Где плотность металла, г/см3; 8,76- переводной коэффициент.
Защита кузова легкового автомобиля от коррозии с помощью…Коррозия — это процесс разрушения твердых тел в результате химических и электрохимических реакций, развивающихся на поверхности предмета при его взаимодействии с окружающей средой.
Скорость коррозийной реакции зависит от ряда причин
Защита кузова автомобиля от коррозии | Статья в журнале. ..
..«Коррозия, ржавление, ржа — это самопроизвольное разрушение металлов и сплавов в результате химического, электрохимического или физико-химического взаимодействия с окружающей средой.
Коррозия Металла в Apple Music
Коррозия Металла в Apple MusicКаковы наиболее распространенные формы коррозии металлов?
Коррозия — это природное явление, затрагивающее почти все металлические предметы, которые мы используем в повседневной жизни. Автомобили, самолеты, медицинские инструменты, здания, инфраструктура, бытовая техника и системы распределения энергии — все они состоят из металла, и поэтому все они подвержены коррозии.
Автомобили, самолеты, медицинские инструменты, здания, инфраструктура, бытовая техника и системы распределения энергии — все они состоят из металла, и поэтому все они подвержены коррозии.
У всех нас была такая машина. Да, автомобильного воплощения Корабля Тесея, которого мы почти уверены, больше не существует. Спасибо большое, коррозия!
Коррозия проявляется в различных формах, и, как правило, корродирующие компоненты, изготовленные из металла, подвержены более чем одной форме одновременно. Сочетание металлов, используемых в компоненте, и широкий спектр сред, которым он подвергается, часто дают возможность для более чем одной формы атаки. В определенных условиях металлы могут подвергаться различным типам местной коррозии, включая точечную, щелевую, межкристаллитную, стрессовую и гальваническую коррозию. Даже один сплав может подвергаться более чем одной форме коррозии в зависимости от воздействия на него различных сред в разных точках системы.
Продолжительность времени, общие условия и уровень воздействия агрессивных сред могут влиять на скорость, тяжесть и тип возникающей в результате коррозии.
Что такое коррозия металлов?
Коррозия – это повреждение материала в результате химических реакций между ним и окружающей средой. Хотя коррозия затрагивает не только металлы, но и другие материалы, включая полимеры и керамику, этот термин чаще всего ассоциируется с разрушением металлов.
Почему металлы подвергаются коррозии?
Большинство металлов не встречаются в природе в металлическом состоянии, требуется энергия (в доменной печи), чтобы отделить эти металлические элементы от соединений, которые они содержат в природе. Поскольку энтропия увеличивается, а свободная энергия должна уменьшаться, атомы, составляющие металл в его метастабильном состоянии, хотят вернуться в стабильное состояние, для поддержания которого требуется минимальная энергия. Коррозия – это возврат энергии, использованной для извлечения их из исходного низкоэнергетического (рудного) состояния путем окисления.
Это достигается за счет обмена электронами между металлом и окружающей средой.
При коррозии металл обычно теряет электроны, окисляясь, а воздействующие на него вещества окружающей среды приобретают электроны, восстанавливаясь.
Эта реакция является самопроизвольной и электрохимически благоприятной.
К сожалению, для металлов почти все среды вызывают коррозию в той или иной степени, потому что коррозия является более стабильным состоянием.
Какие виды коррозии металлов наиболее распространены?
Коррозия классифицируется по способу ее проявления. Различные его формы сгруппированы по внешнему виду корродированного металла с формами коррозии, идентифицированными при визуальном наблюдении. В большинстве случаев достаточно невооруженного глаза, но иногда полезно или требуется увеличение. NACE, орган по коррозии, разделяет коррозию на 3 группы. Это следующие группы:
- Группа 1: Коррозия, определяемая визуальным наблюдением
- Группа 2: Коррозия, требующая дополнительных методов исследования
- Группа 3: Коррозия, требующая проверки под микроскопом
Внутри этих групп существует много конкретных типов коррозии, которые могут возникнуть. Ниже приведены некоторые из наиболее распространенных.
Ниже приведены некоторые из наиболее распространенных.
1. Коррозионное растрескивание под напряжением
Глядя на свою деталь через ушко, вы замечаете небольшие, тонкие трещины, видимые на углах. Это явный признак заведомо плохой формы коррозии, коррозии под напряжением.
Коррозия под напряжением возникает, когда материал находится в коррозионной среде и присутствуют растягивающие напряжения. Все металлы имеют разные пределы/диапазоны растяжения, и чем ближе к высоте этого предела, тем больше вероятность возникновения коррозии под напряжением. Пример включает любые процессы, которые включают в себя изменения/циклы высокой/низкой температуры. Очень важно убедиться, что это учтено на этапе исследований и разработок при выборе правильного сплава для вашего применения.
2. Точечная коррозия
При осмотре специалист по качеству также замечает небольшие полости в материале. Хотя коррозионное растрескивание под напряжением также присутствует, оно указывает на явные признаки гораздо более опасного типа коррозии: точечной коррозии.
Эти небольшие глубокие полости могут быть вызваны множеством различных факторов. Несколько примеров: плохое нанесение покрытия, повреждение пленки или инородные отложения внутри самого металла. Тем не менее, точечная коррозия может привести к очень быстрым и разрушительным отказам, если ее не обнаружить на ранних этапах жизненного цикла производственного процесса. В местах, где эта пленка (пассивность) была нарушена, влага может попасть внутрь и вызвать коррозию клеток. Это создает повышенный риск разрушения самого материала, так как во многих местах зерна материала не обладают структурной жесткостью.
3. Эрозионная коррозия
Одна из наиболее часто встречающихся записей в списке, эрозионная коррозия возникает, когда коррозионная жидкость проходит по металлу, что приводит к ускоренному износу поверхности этого металла. Этот тип износа металлов обычно виден невооруженным глазом, образуя канавки, кратеры или впадины на поверхности материала.
Как это работает? Ионы на поверхности материалов буквально сметаются силой бегущей по ней агрессивной жидкости. Это приводит к тому, что материал становится гораздо более восприимчивым к повреждениям из-за удаления пленки и проникновения в сам металл. Как и при многих других формах коррозии, временная шкала этой поломки зависит от многих факторов.
Это приводит к тому, что материал становится гораздо более восприимчивым к повреждениям из-за удаления пленки и проникновения в сам металл. Как и при многих других формах коррозии, временная шкала этой поломки зависит от многих факторов.
Если у вас есть вопросы о ваших уникальных потребностях в материалах или процессах, которые вы выполняете с металлом, который вы покупаете, и вы хотите понять наиболее вероятные факторы, которые могут вызвать этот тип коррозии в вашем приложении, команда металлургов Ульбриха может помочь.
4. Щелевая коррозия
Как следует из названия, этот тип коррозии образуется внутри зазоров или щелей на поверхности металла. Щелевая коррозия также может повлиять на все, с чем «соединен» металл; приваренный металл к металлу или даже металл, прикрепленный к неметаллическим объектам.
Эти щели чаще всего заполняются загрязнениями, которые ускоряют процесс коррозии. Вода (обычно стоячая) — самый большой подозреваемый, на который стоит обратить внимание. Эта вода является катализатором электрохимических реакций, которые в конечном итоге приведут к разрушению материала.
Эта вода является катализатором электрохимических реакций, которые в конечном итоге приведут к разрушению материала.
5. Селективное выщелачивание
Представьте себе: вы собираетесь построить новый инструмент для своего цеха и используете валяющийся поблизости кусок нержавеющей стали, чтобы сделать воронку для жидкости. Эта жидкость постоянно течет по воронке. Со временем вы заметите, что в жидкости, выходящей с другой стороны, есть небольшие хлопья металлического материала. Заглянув внутрь воронки, вы понимаете, что жидкость, протекающая через воронку, оставляет канавки и бороздки на внутренней поверхности. Это пример деникелирования; форма селективного выщелачивания, при которой никель специально отделяется от других элементов в сплаве.
Избирательная коррозия с выщелачиванием возникает, когда изнашивается только один (или более) элемент в сплаве. Когда начинается это ухудшение, сплавы начинают отделяться друг от друга на молекулярном уровне. Из-за истории и условий использования ваша воронка начала проявлять признаки выборочного выщелачивания. В этом случае никель из нержавеющей стали удаляется, а другие металлы сплава остаются. Подобную ситуацию можно предотвратить путем термической обработки материала, чтобы сделать его более упругим, а также путем проведения дальнейших исследований того, как жидкость может вызывать химические реакции на нержавеющей стали. Это может быть важным фактором, который следует учитывать при работе с дуплексными сплавами.
В этом случае никель из нержавеющей стали удаляется, а другие металлы сплава остаются. Подобную ситуацию можно предотвратить путем термической обработки материала, чтобы сделать его более упругим, а также путем проведения дальнейших исследований того, как жидкость может вызывать химические реакции на нержавеющей стали. Это может быть важным фактором, который следует учитывать при работе с дуплексными сплавами.
6. Равномерная коррозия
Очень распространенный пример равномерной коррозии, который может распознать большинство, особенно те из вас, кто купил Mazda6 в период с 2005 по 2008 год, — это ржавчина! Этот тип однородной коррозии поражает всю площадь поверхности (или большую часть) указанного материала. Его очень хорошо видно невооруженным глазом.
Эта коррозия приведет к тому, что металл будет медленно терять свою «толщину» и разрушаться, постепенно растворяясь. Это в конечном итоге приведет к тому, что металл станет хрупким и сломается.
Подумайте о колесных арках и переднем крае капота вашей старой Mazda6 2008 года выпуска. Если вы живете где-нибудь, где с 2008 модельного года не раз шел дождь, вы теперь увидите коричневый и хрупкий отслаивающийся металл. У вас есть реальный пример равномерной коррозии! Как правило, это вызвано химическими или электрохимическими реакциями. Равномерная коррозия известна как один из НАИБОЛЕЕ распространенных видов коррозии.
Если вы живете где-нибудь, где с 2008 модельного года не раз шел дождь, вы теперь увидите коричневый и хрупкий отслаивающийся металл. У вас есть реальный пример равномерной коррозии! Как правило, это вызвано химическими или электрохимическими реакциями. Равномерная коррозия известна как один из НАИБОЛЕЕ распространенных видов коррозии.
7. Межкристаллитная коррозия
Как известно многим инженерам, металлургам и другим людям, тесно связанным с химией металлов, металл состоит из миллиардов «зерен». Именно эти зерна влияют на жесткость и прочность самого металла. Если возникает межкристаллитная коррозия, то физическая структура, удерживающая металл вместе (зерна), подвергается риску.
Например, аустенитные нержавеющие стали обычно подвержены межкристаллитной коррозии при термообработке. Эти границы, которые образуются при неправильной термообработке, могут привести к тяжелым последствиям в будущем, поэтому важно знать данные о механических свойствах при выборе сплавов для вашего применения. Это состояние приводит к предпочтительной или неприемлемой коррозии границ зерен, снижающей объемную прочность материала, что может привести к преждевременному разрушению материала.
Это состояние приводит к предпочтительной или неприемлемой коррозии границ зерен, снижающей объемную прочность материала, что может привести к преждевременному разрушению материала.
8. Гальваническая/биметаллическая коррозия
При длительном контакте двух разнородных металлов возникает биметаллическая коррозия. Разница электродных потенциалов между металлами вызывает ячейку, называемую биметаллической парой. Биметаллическая парная ячейка заставляет один металл действовать как катод, а другой – как анод.
Чем дальше друг от друга находятся два металла в гальваническом ряду, тем больше потенциальное влияние биметаллической коррозии двух материалов.
Что можно сделать, чтобы предотвратить коррозию металлов?
Наука предотвращения и контроля коррозии очень сложна. Эта сложность только усугубляется тем фактом, что существует множество различных форм коррозии, на которые влияет широкий спектр внешних факторов. Для обеспечения длительной и бесперебойной работы продукции, которую производит ваша организация, крайне важно работать с опытными в металлургии партнерами, которые хорошо осведомлены о коррозии и ее влиянии на материалы на месте в рабочей среде. Отказ компонентов и значительное количество повреждений материала, вызванных коррозией, можно исключить, выбрав соответствующий сплав и характеристики для данного применения.
Отказ компонентов и значительное количество повреждений материала, вызванных коррозией, можно исключить, выбрав соответствующий сплав и характеристики для данного применения.
Основными участниками коррозийных эффектов жидкостей и металлов являются:
- Кислород, хлорид и/или содержание сульфида
- Температура
- PH – значение
Предотвращение CROROSION. КРОЗИОН Включает в себя CORROSION. Следующие стратегии:
. Предотвращение CROROSION. Следующие стратегии:
. Коррозион. Следующие стратегии: . Коррозион. Выбор правильного сплава с идеальным химическим составом для вашей работы является ключом к предотвращению коррозии. Здесь, в Ульбрихе, наша команда опытных металлургов повидала все это. Связь между инженерами и инженерами между производителями и их партнерами по перекатке или поставщиками металла является ключом к преодолению проблем, связанных с коррозией металла. Если вы работаете над деталью или изделием, для которых стойкость к коррозии имеет решающее значение, и хотели бы обратиться к нам за помощью, мы здесь для вас! Мы помогли бесчисленным партнерам, производящим детали для самых сложных применений, определить правильный сплав для работы. На нашем веб-сайте также есть листы технических данных, в которых содержится подробная информация, которая поможет вам расширить свои знания о нашем широком ассортименте сплавов. Майкл Пфайфер, доктор философии, ЧП. Оставить комментарий В предыдущей статье я обсуждал источники факторов стресса, которые могут вызвать деградацию материалов в компонентах и соединениях. В этой статье я расскажу об основах коррозии металлов — электрохимической ячейке, семи распространенных формах коррозии, а также примерах подходов к разработке металлов и механическому проектированию для борьбы с коррозией. Коррозия представляет собой электрохимическую реакцию, которая включает изменения как в металле, так и в окружающей среде, контактирующей с металлом. Реакция происходит при создании электрохимической ячейки. Электрохимическая ячейка состоит из анода, катода, электролита и электрического контакта между анодом и катодом. Когда электрохимическая ячейка установлена, анод окисляется — коррозирует — и катод получает электроны. На катоде могут протекать различные реакции. Во многих случаях катодная реакция приводит к образованию газообразного водорода. Существуют различные способы создания электрохимической ячейки, что приводит к различным формам коррозии. Семь распространенных форм коррозии металлов: Равномерная коррозия происходит по всей открытой поверхности металла. Ржавчина на стальной конструкции или зеленый налет на медной кровле являются примерами однородной коррозии. Коррозия происходит равномерно по всей поверхности оголенного металла. Движущей силой равномерной коррозии является электрохимическая активность металла в окружающей среде, воздействию которой подвергается металл. Электрохимическую активность определяют путем измерения электродного потенциала металла, подвергающегося воздействию интересующего водного раствора. Металлы с положительным электродным потенциалом обладают малой электрохимической активностью и называются благородными, с повышением коррозионной стойкости по мере увеличения потенциала. Металлы с отрицательным потенциалом электрода обладают более высокой электрохимической активностью и называются активными, коррозионная стойкость которых снижается по мере того, как потенциал становится более отрицательным. Например, в морской воде активна углеродистая сталь, а золото благородно. Гальваническая коррозия возникает вблизи соединения двух разнородных металлов, находящихся в электрическом контакте. Движущей силой коррозии является разница электродных потенциалов между двумя металлами, при этом коррозия металла более активна. Например, если углеродистая сталь находится в контакте с медью и подвергается воздействию дождя, сталь подвергается коррозии. Чем больше разность потенциалов между металлами, тем быстрее будет происходить коррозия. Щелевая коррозия возникает в щелях между компонентами и под полимерными покрытиями и клеями. Когда контактирующая жидкость попадает в щель, она со временем застаивается, что приводит к уменьшению количества растворенных ионов или кислорода по сравнению с жидкостью вне щели. В результате создается электрохимическая ячейка, в которой металл в щели становится анодом, а металл снаружи становится катодом. Точечная коррозия возникает в металлах, обычно пассивных, таких как алюминий и нержавеющая сталь. Пассивные металлы имеют очень тонкий оксидный поверхностный слой, который защищает нижележащий металл от окружающей среды. Питтинг возникает, когда оксидный слой разрушается из-за воздействия окружающей среды. Точечная коррозия представляет собой проблему, если она приводит к ослаблению или перфорации металла. Кроме того, точечная коррозия представляет собой проблему для применений, где внешний вид важен, так как будут признаки коррозии, такие как пятна ржавчины на нержавеющей стали. Межкристаллитная коррозия включает коррозию по границам зерен пораженного металла. В результате зерна металла отпадают, а металл ослабевает. Аустенитные нержавеющие стали, такие как 304 и 316, являются примерами металлов, которые могут страдать от межкристаллитной коррозии. Коррозионное растрескивание под напряжением связано с комбинированным действием напряжения и воздействия агрессивной среды. В большинстве случаев стресс или окружающая среда сами по себе недостаточны, чтобы вызвать деградацию металла. То есть напряжение ниже предела текучести металла, и металл не подвергается коррозии в конкретной среде при отсутствии напряжения. В совокупности напряжение и коррозионная среда вызывают растрескивание металла. Есть случаи, когда остаточное напряжение было достаточным, чтобы вызвать коррозионное растрескивание под напряжением. Делегирование — селективное выщелачивание одного элемента из сплава. Скорость коррозии металла и конкретный механизм коррозии зависят от нескольких факторов, включая состав металла, микроструктуру металла, окружающую среду, геометрию компонента, нагрузку на компонент, контакт между металлами и способ соединения компонентов. С точки зрения технологии металлов следующие подходы являются примерами способов предотвращения и контроля коррозии: С точки зрения механического проектирования, следующие подходы являются примерами способов предотвращения и контроля коррозии: В следующей статье я расскажу об испытаниях на коррозию, включая испытания на уровне материалов. Тестирование надежности на уровне материалов — это мощный подход к одновременной оценке нескольких материалов, компонентов и конструкций соединений. Примечание. Для этого содержимого требуется JavaScript. Задайте вопрос или отправьте комментарий.
Пожалуйста, войдите, чтобы просмотреть и использовать контактную форму. Рубрика: Статьи, Металлургия и надежность продукции, о надежности продукции В случае марки нержавеющей стали, содержащей не менее 11% хрома, когда этот металл подвергается воздействию насыщенной кислородом среды, хром будет реагировать с воздухом, образуя пассивный оксидный слой на поверхности металла. Это замедляет дальнейшее окисление и помогает металлу сопротивляться равномерной и локальной коррозии. Другие элементы также обеспечивают антикоррозионный эффект. Например, никель помогает стабилизировать микроструктуру, повышая устойчивость к коррозионному растрескиванию под напряжением. Марганец в умеренных количествах и в сочетании с никелем помогает предотвратить точечную коррозию. Добавление молибдена повышает устойчивость к точечной и щелевой коррозии.
В случае марки нержавеющей стали, содержащей не менее 11% хрома, когда этот металл подвергается воздействию насыщенной кислородом среды, хром будет реагировать с воздухом, образуя пассивный оксидный слой на поверхности металла. Это замедляет дальнейшее окисление и помогает металлу сопротивляться равномерной и локальной коррозии. Другие элементы также обеспечивают антикоррозионный эффект. Например, никель помогает стабилизировать микроструктуру, повышая устойчивость к коррозионному растрескиванию под напряжением. Марганец в умеренных количествах и в сочетании с никелем помогает предотвратить точечную коррозию. Добавление молибдена повышает устойчивость к точечной и щелевой коррозии. Если вам нужна помощь в выборе коррозионностойкого сплава и вы хотите узнать больше о характеристиках, на которые следует обратить внимание, чтобы он выдерживал условия, которым он будет подвергаться, свяжитесь с одним из наших инженеров сегодня!
Если вам нужна помощь в выборе коррозионностойкого сплава и вы хотите узнать больше о характеристиках, на которые следует обратить внимание, чтобы он выдерживал условия, которым он будет подвергаться, свяжитесь с одним из наших инженеров сегодня! Коррозия металла — Accendo Reliability
 В ходе реакции атомы металла теряют электроны – окисляются, а окружающая среда приобретает электроны – восстанавливается. В результате окисления атом становится положительно заряженным ионом и отрывается от металла.
В ходе реакции атомы металла теряют электроны – окисляются, а окружающая среда приобретает электроны – восстанавливается. В результате окисления атом становится положительно заряженным ионом и отрывается от металла.

 Во многих случаях движущей силой коррозии является разница между концентрацией кислорода внутри щели и снаружи щели.
Во многих случаях движущей силой коррозии является разница между концентрацией кислорода внутри щели и снаружи щели. Эти сплавы подвержены межкристаллитной коррозии при воздействии температур в диапазоне от 800 до 1600 F. Это происходит во время сварки и других процессов. Восприимчивость к межкристаллитному разрушению является результатом изменений микроструктуры, в результате которых участки зерен, прилегающие к границам зерен, имеют пониженную коррозионную стойкость.
Эти сплавы подвержены межкристаллитной коррозии при воздействии температур в диапазоне от 800 до 1600 F. Это происходит во время сварки и других процессов. Восприимчивость к межкристаллитному разрушению является результатом изменений микроструктуры, в результате которых участки зерен, прилегающие к границам зерен, имеют пониженную коррозионную стойкость. Это приводит к образованию пористой структуры, недостаточно прочной, чтобы выдерживать приложенные механические нагрузки. Одним из распространенных примеров является удаление цинка из латунных сплавов, используемых для сантехники, когда цинк выщелачивается из сплава.
Это приводит к образованию пористой структуры, недостаточно прочной, чтобы выдерживать приложенные механические нагрузки. Одним из распространенных примеров является удаление цинка из латунных сплавов, используемых для сантехники, когда цинк выщелачивается из сплава. Борьба с коррозией
Испытания на коррозию  Настройка тестирования требует времени и усилий, но затраты времени и средств, когда продукты проходят валидацию и проверочное тестирование с первого раза, впечатляют.
Настройка тестирования требует времени и усилий, но затраты времени и средств, когда продукты проходят валидацию и проверочное тестирование с первого раза, впечатляют. Этот сайт использует файлы cookie, чтобы предоставить вам лучший опыт, проанализировать трафик сайта и получить представление о продуктах или предложениях, которые могут вас заинтересовать. Продолжая, вы соглашаетесь на использование файлов cookie. Узнайте, как мы используем файлы cookie, как они работают и как настроить параметры браузера, прочитав нашу Политику использования файлов cookie.
Примечание. Для этого контента требуется JavaScript.
Грандиозные задачи в области исследований коррозии и защиты металлов
Стремление к разработке технологий, отвечающих растущим потребностям общества, устойчивости, экологической безопасности и рентабельности, постоянно растет. Пригодность этих технологий для исследования новых ресурсов в крайне неблагоприятных условиях, таких как глубоководные и космические, придала больший импульс исследованиям коррозии. Взгляд на периодическую таблицу элементов показывает, что подавляющее большинство элементов, используемых для изготовления инженерных конструкций и устройств, которые являются неотъемлемой частью нашей жизни, термодинамически благоприятны для коррозии в химических средах, в которых они обитают. Кроме того, миниатюризация устройств и легкие инженерные конструкции обеспечивают меньшую свободу действий для коррозии для удовлетворительной работы этих компонентов. Иногда материалы, изготавливаемые для таких компонентов, не соответствуют их способности противостоять коррозионным разрушениям. Поэтому исследования коррозии должны включать поиск путей и средств защиты этих материалов от таких отказов. Хотя им суждено (термодинамически) подвергаться коррозии в типичных химических средах, они должны служить (Pourbaix, 19).
Пригодность этих технологий для исследования новых ресурсов в крайне неблагоприятных условиях, таких как глубоководные и космические, придала больший импульс исследованиям коррозии. Взгляд на периодическую таблицу элементов показывает, что подавляющее большинство элементов, используемых для изготовления инженерных конструкций и устройств, которые являются неотъемлемой частью нашей жизни, термодинамически благоприятны для коррозии в химических средах, в которых они обитают. Кроме того, миниатюризация устройств и легкие инженерные конструкции обеспечивают меньшую свободу действий для коррозии для удовлетворительной работы этих компонентов. Иногда материалы, изготавливаемые для таких компонентов, не соответствуют их способности противостоять коррозионным разрушениям. Поэтому исследования коррозии должны включать поиск путей и средств защиты этих материалов от таких отказов. Хотя им суждено (термодинамически) подвергаться коррозии в типичных химических средах, они должны служить (Pourbaix, 19). 74). Следовательно, эффективный контроль коррозионных повреждений не может заключаться только в использовании «правильных материалов», поскольку это может быть практически невозможно. Укрощение окружающей среды с помощью ингибиторов и нанесения покрытий, электрохимических средств, таких как катодная и анодная защита, и инженерных средств, таких как конструкция конструкции, помогают эффективно сдерживать коррозию. Особое внимание также уделяется мониторингу коррозии, осмотру, прогнозированию срока службы и упреждающему управлению активами. Во всех этих случаях важно понимать коррозионные явления, связанные с взаимодействием металла и окружающей среды.
74). Следовательно, эффективный контроль коррозионных повреждений не может заключаться только в использовании «правильных материалов», поскольку это может быть практически невозможно. Укрощение окружающей среды с помощью ингибиторов и нанесения покрытий, электрохимических средств, таких как катодная и анодная защита, и инженерных средств, таких как конструкция конструкции, помогают эффективно сдерживать коррозию. Особое внимание также уделяется мониторингу коррозии, осмотру, прогнозированию срока службы и упреждающему управлению активами. Во всех этих случаях важно понимать коррозионные явления, связанные с взаимодействием металла и окружающей среды.
Мультидисциплинарный характер коррозии сопряжен с более серьезными проблемами и предоставляет широкие возможности для исследователей коррозии (NAP, 2011). Здесь выделены некоторые критические области.
Механизмы коррозии
Поскольку термодинамической устойчивости к коррозии для подавляющего большинства элементов не существует, путь увеличения срока их службы заключается в повышении их кинетической устойчивости к коррозии. Повышение кинетической стойкости металлов и сплавов зависит от понимания механизмов коррозии на макроскопическом, микроскопическом и атомном уровнях (Marcus, 2012). В настоящее время у нас есть проблемы, связанные с определением и количественной оценкой химических, электрохимических и механических, включая экологические аспекты коррозии на этих уровнях. Решение этих проблем будет иметь большое значение для разработки сплавов, защищающих от различных типов коррозии, а также для прогнозирования и упреждающего контроля коррозии.
Повышение кинетической стойкости металлов и сплавов зависит от понимания механизмов коррозии на макроскопическом, микроскопическом и атомном уровнях (Marcus, 2012). В настоящее время у нас есть проблемы, связанные с определением и количественной оценкой химических, электрохимических и механических, включая экологические аспекты коррозии на этих уровнях. Решение этих проблем будет иметь большое значение для разработки сплавов, защищающих от различных типов коррозии, а также для прогнозирования и упреждающего контроля коррозии.
Разработка коррозионно-стойких сплавов
Энергоэффективные и экологически безопасные технологии в целом и технологии, включающие использование нетрадиционных источников энергии, таких как солнечная энергия и водород, глубоководные исследования и использование ископаемого топлива бедного качества, в частности, чаще чем не затрагивают инженерные сооружения, подвергающиеся воздействию крайне агрессивных сред. Поэтому для этих технологий требуются высокоэффективные сплавы и материалы. Разработка сплавов включает, помимо прочего, изучение коррозионного поведения наноматериалов, аморфных, высокоэнтропийных сплавов, биоматериалов и т. д.
Разработка сплавов включает, помимо прочего, изучение коррозионного поведения наноматериалов, аморфных, высокоэнтропийных сплавов, биоматериалов и т. д.
Обработка и изготовление сплавов Коррозия
Как правило, на металлургическую структуру типичных сплавов влияет способ их обработки и изготовления, что, в свою очередь, влияет на коррозионные свойства сплавов. С появлением аддитивного производства, также известного как 3D-печать, этот аспект становится еще более важным (Bourell et al., 2020). Кроме того, на металлургию изготовленных металлов, таких как металлы, подвергающиеся соединению металлов и металлообработке, влияют условия изготовления, такие как температура и давление. В результате технологии изготовления влияют на коррозию металлов. Поэтому такие исследования, касающиеся обработки сплавов, изготовления, металлургии и коррозии, важны.
Обработка поверхности и покрытие
Не все технические сплавы, обладающие желаемыми свойствами, устойчивы к коррозии. Также невозможно улучшить присущую им коррозионную стойкость до желаемого уровня. Обработка поверхности и покрытия позволяют использовать такие металлы для желаемых целей. В то же время растущая забота об окружающей среде сделала некоторые процессы обработки поверхности и покрытия устаревшими. Поэтому необходимо развивать науку и технологии экологически безопасных многофункциональных и умных покрытий. Например, покрытия должны обладать не только коррозионной стойкостью, но и другими свойствами, такими как износостойкость, биосовместимость, а в случае фотоэлементов светопроницаемость и теплоизоляция. В местах, где необходимо предотвратить коррозию из-за локального повреждения покрытий, эти покрытия должны быть умными, чтобы обнаруживать и лечить поврежденное место. Разработка металлических и неметаллических покрытий, обладающих одним или несколькими из вышеперечисленных свойств, может значительно улучшить защиту от коррозии устройств и инженерных сооружений.
Также невозможно улучшить присущую им коррозионную стойкость до желаемого уровня. Обработка поверхности и покрытия позволяют использовать такие металлы для желаемых целей. В то же время растущая забота об окружающей среде сделала некоторые процессы обработки поверхности и покрытия устаревшими. Поэтому необходимо развивать науку и технологии экологически безопасных многофункциональных и умных покрытий. Например, покрытия должны обладать не только коррозионной стойкостью, но и другими свойствами, такими как износостойкость, биосовместимость, а в случае фотоэлементов светопроницаемость и теплоизоляция. В местах, где необходимо предотвратить коррозию из-за локального повреждения покрытий, эти покрытия должны быть умными, чтобы обнаруживать и лечить поврежденное место. Разработка металлических и неметаллических покрытий, обладающих одним или несколькими из вышеперечисленных свойств, может значительно улучшить защиту от коррозии устройств и инженерных сооружений.
Вычислительное материаловедение, анализ данных, машинное обучение и искусственный интеллект
Ожидается, что эти инструменты преодолеют ограничения экспериментального и детерминированного подходов к пониманию явлений коррозии. Эти инструменты способны оказать большое влияние на развитие науки и техники о коррозии, особенно на разработку новых коррозионно-стойких сплавов для применения материалов в высококоррозионных условиях и прогнозирования срока службы конструкций от коррозии. Однако для успешного применения этих инструментов в науке и технике о коррозии необходимы согласованные исследования (Coelho et al., 2022).
Эти инструменты способны оказать большое влияние на развитие науки и техники о коррозии, особенно на разработку новых коррозионно-стойких сплавов для применения материалов в высококоррозионных условиях и прогнозирования срока службы конструкций от коррозии. Однако для успешного применения этих инструментов в науке и технике о коррозии необходимы согласованные исследования (Coelho et al., 2022).
Усовершенствованные/новые экспериментальные методы исследования коррозии
Понимание механизмов коррозии включает исследование металлических систем в различных масштабах. Поэтому необходимы исследования по разработке методов, позволяющих разрешить процессы коррозии в различных масштабах.
Таким образом, большинство материалов, особенно металлических сплавов, применяемых для изготовления инженерных конструкций и устройств, имеют термодинамическую склонность к коррозии при воздействии на них химических сред. Только за счет повышения кинетической коррозионной стойкости этих материалов можно увеличить срок службы деталей. Для этого необходимо понимать механизмы коррозии. С одной стороны, с ростом технического прогресса возникает необходимость в разработке сплавов, устойчивых к высокоагрессивным коррозионным средам. С другой стороны, при использовании новых производственных технологий, таких как аддитивное производство, нам необходимо понимать коррозионное поведение материалов, изготовленных с использованием новых технологий и способов. Поскольку покрытия остаются одним из наиболее широко используемых методов предотвращения коррозии, меняющиеся экологические нормы и передовые технологии требуют покрытий нового поколения. Необходимо преодолеть ограничения экспериментальных исследований. В этом заключается потребность в вычислительных материаловедениях, аналитике данных, машинном обучении и искусственном интеллекте.
Для этого необходимо понимать механизмы коррозии. С одной стороны, с ростом технического прогресса возникает необходимость в разработке сплавов, устойчивых к высокоагрессивным коррозионным средам. С другой стороны, при использовании новых производственных технологий, таких как аддитивное производство, нам необходимо понимать коррозионное поведение материалов, изготовленных с использованием новых технологий и способов. Поскольку покрытия остаются одним из наиболее широко используемых методов предотвращения коррозии, меняющиеся экологические нормы и передовые технологии требуют покрытий нового поколения. Необходимо преодолеть ограничения экспериментальных исследований. В этом заключается потребность в вычислительных материаловедениях, аналитике данных, машинном обучении и искусственном интеллекте.
Авторские вклады
VR предоставил концептуальный вклад в работу и написал документ.
Конфликт интересов
Автор заявляет, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Примечание издателя
Все утверждения, изложенные в этой статье, принадлежат исключительно авторам и не обязательно представляют претензии их дочерних организаций или издателя, редакторов и рецензентов. Любой продукт, который может быть оценен в этой статье, или претензии, которые могут быть сделаны его производителем, не гарантируются и не поддерживаются издателем.
Ссылки
Coelho, L.B., Zhang, D., Ingelgem, Y.V., and Steckelmacher, D. (2022). Обзор машинного обучения прогнозирования коррозии с точки зрения данных, Npj Mater. Деград. . 6. 8. doi:10.1038/s41529-022-00218-4
CrossRef Full Text | Google Scholar
DL Bourell, W Frazier, H Kuhn и M Seifi (редакторы) (2020). Аддитивные производственные процессы (Огайо: ASM International).
Google Scholar
NAP, (2011). Возможности исследований в области науки о коррозии и техники, подготовленный Национальным исследовательским советом национальных академий, Отдел инженерных и физических наук . Вашингтон, округ Колумбия: Издательство национальных академий. Доступно на: www.nap.edu.
Вашингтон, округ Колумбия: Издательство национальных академий. Доступно на: www.nap.edu.
Google Scholar
P Маркус (редактор) (2012). Механизмы коррозии в теории и на практике . 3-е издание (Бока-Ратон, Флорида: CRC Press).
Google Scholar
Pourbaix, M. (1974). Атлас электрохимических равновесий в водных растворах . Хьюстон: Национальная ассоциация инженеров по коррозии.
Google Scholar
Распространенные виды коррозии | Astro Pak
Когда слышишь слова «металл» и «коррозия» вместе, то чаще всего на ум приходит образ чего-то сделанного из стали или железа, покрытого оранжево-красной ржавчиной. И это совершенно точно и приемлемо, учитывая, насколько обычным явлением в нашем мире является медленное окисление железа. Старая металлическая вывеска, крыло битой машины перед вами, которое выглядит так, будто оно развалится в любой момент, или даже китчевое произведение искусства, на котором была применена настоящая или поддельная коррозия, чтобы придать объекту «характер». Но коррозия — это гораздо больше, чем простой случай Fe 9.0338 2 O 3 , он же «оксид железа» или, как мы все его называем, «ржавчина».
Но коррозия — это гораздо больше, чем простой случай Fe 9.0338 2 O 3 , он же «оксид железа» или, как мы все его называем, «ржавчина».
Ржавчина относится только к коррозии железа или стали. Другие металлы могут подвергаться коррозии, и существует 10 распространенных типов коррозии. Хотя их причина, цвет и конкретный процесс могут различаться, все они являются общими в том, что они вызывают возможное ухудшение состояния металла.
Общая атака Коррозия является наиболее распространенной формой. На железе это то, что мы называем «ржавчиной». Это химическая или электрохимическая реакция. В случае с железом и многими другими металлами это больше, чем взаимодействие металла с кислородом в атмосфере, для начала химической реакции требуется некоторый уровень влаги. Другие металлы, конечно, подвержены коррозии. Возможно, самым удивительным является то, что алюминий очень подвержен коррозии, но образующийся оксид алюминия представляет собой очень твердый материал, который фактически защищает основной металл от дальнейшей коррозии, часто называемый пассивной оксидной пленкой.
В целом общая коррозия является причиной потери большей части металла в результате коррозии, но в то же время она считается управляемой, поскольку она наиболее изучена и, следовательно, предсказуема и часто предотвратима.
Локальная коррозия , как следует из названия, представляет собой коррозию, происходящую в определенной области металла. Существует три подтипа: Точечная, щелевая и нитевидная:
- Точечная коррозия – возникает при образовании на поверхности металла одного или нескольких небольших отверстий в результате механического воздействия или химической реакции. Это создает небольшой электрический ток, при этом ямка является анодом (генерирующим отрицательные ионы), а оставшийся металл служит катодом в гальванической реакции. Из-за своего размера такую коррозию трудно обнаружить. Если его не обработать, он может проникнуть в металл, что приведет к поломке.
- Щель – как и точечная коррозия, возникает в определенном месте и часто возникает в зоне постоянного контакта с влагой, например, под прокладкой, шайбой, между слоями металла и т.
 п. Если условия создают кислую среду или если кислород истощен в этой области, то, вероятно, произойдет коррозия.
п. Если условия создают кислую среду или если кислород истощен в этой области, то, вероятно, произойдет коррозия. - Нитевидная форма . Возможно, ее труднее всего обнаружить на начальном этапе, она возникает под окрашенными или покрытыми металлом поверхностями, когда разрушение покрытия приводит к накоплению влаги. Коррозия начинается в месте дефекта и распространяется на окружающий металл, что часто приводит к образованию пузырей на краске или металлическом покрытии.
Гальваническая коррозия , также известная как коррозия разнородных металлов, очень похожа на описанную выше точечную электрохимическую реакцию, но в гораздо большем масштабе. Это происходит, когда два разнородных металла, таких как латунь и железо, находятся в непосредственном контакте и подвергаются воздействию электролита, который может быть таким же простым, как вода. Два элемента образуют гальваническую пару, в которой один металл служит анодом, разъедая его, когда его ионы текут к другому металлу, который действует как катод. В конечном итоге анодная часть будет изнашиваться быстрее, а катодная часть будет подвергаться коррозии гораздо медленнее. Гальваническая коррозия представляет особый риск для океанских судов, и в корпус индуцируется ток, чтобы противодействовать этому процессу и защитить корпус.
В конечном итоге анодная часть будет изнашиваться быстрее, а катодная часть будет подвергаться коррозии гораздо медленнее. Гальваническая коррозия представляет особый риск для океанских судов, и в корпус индуцируется ток, чтобы противодействовать этому процессу и защитить корпус.
В Растрескивание под воздействием окружающей среды химическая реакция в сочетании с одним из ряда условий окружающей среды вызывает коррозию металла. Температура и напряжение могут способствовать ускорению износа металла в четырех основных ситуациях:
- Коррозионное растрескивание под напряжением (SCC ) — это рост образования трещин в металле в агрессивной среде. Некоторые сплавы могут подвергаться SCC в очень специфических химических средах (например, при воздействии хлоридов), которые в противном случае обладают лишь слабой коррозионной активностью. Это может привести к неожиданному и внезапному разрушению металлических сплавов под нагрузкой и, как правило, при повышенных температурах.

- Коррозионная усталость также требует коррозионной среды с добавлением механической деградации из-за циклической нагрузки, также известной как переменное напряжение. Это вызывает особую озабоченность у планеров.
- Водородное растрескивание (HIC) , также известное как водородное охрупчивание (HE) и водородное растрескивание (HAC), представляет собой сложный процесс, который до конца не изучен из-за разнообразия и сложности факторов, которые могут его вызывать. Сталь может стать хрупкой под воздействием водорода при высоких температурах, поскольку этот элемент соединяется с углеродом в металле с образованием метана в его пустотах. Медные сплавы, содержащие включения кислорода, также поглощают водород, который затем связывается с кислородом, образуя воду. Эта вода образует пузырьки пара под давлением на границах зерен и заставляет зерна отталкиваться друг от друга. Точно так же сплавы ванадия, никеля и титана также могут поглощать водород, что может вызвать расширение и повреждение их кристаллической структуры.
 Однако аустенитная нержавеющая сталь не подвержена этому охрупчиванию.
Однако аустенитная нержавеющая сталь не подвержена этому охрупчиванию. - Охрупчивание жидким металлом вызвано воздействием определенных жидких металлов. И ртуть, и галлий могут вызвать этот отказ, при этом алюминий особенно чувствителен к ртути.
Фреттинг-коррозия аналогична коррозионному растрескиванию под напряжением тем, что для его возникновения требуется механическая сила. В случае фреттинг-коррозии соответствующий элемент подвергается многократному износу, весу и/или вибрации на шероховатой поверхности. Примером того, где это может произойти, является шариковый подшипник. Механические повреждения также дополнительно увеличивают шероховатость поверхности, делая ее еще более восприимчивой к дальнейшим повреждениям. Это также может привести к точечной коррозии одной или обеих поверхностей. Недавно открытый металл вместе с любым мусором, образовавшимся в результате первоначального повреждения, окислится. В некоторых случаях окисленный металл даже тверже, чем исходный материал, но, тем не менее, окисленный мусор может действовать на поверхность как абразив, ускоряя износ металла.
Высокотемпературная коррозия обычно имеет место в машинах, работающих на топливе. Когда двигатель или газовая турбина сжигает топливо, содержащее примеси, он может оставить осадок, который очень агрессивен при высоких температурах, при которых он работает. Одним из распространенных примеров является судовое топливо, которое естественным образом содержит ванадий. Другим примером является сера в дизельном топливе, которое, хотя и улучшает экономию топлива и смазывающую способность топлива, вызывает ряд проблем с окружающей средой и здоровьем. Сульфатные соединения, образующиеся при сгорании топлива, способны воздействовать даже на нержавеющую сталь. Кроме того, кислород, сульфиды, пар и углерод также могут разрушать некоторые металлы при высокой температуре.
Коррозия под действием потока (FAC) возникает, когда защитный слой металла, такой как пассивный слой нержавеющей стали, разрушается под действием газа или воды, подвергая нижележащий металл химической или механической коррозии. Это особенно распространено в трубопроводах из углеродистой стали, по которым проходит сверхчистая деоксигенированная вода или влажный пар.
Это особенно распространено в трубопроводах из углеродистой стали, по которым проходит сверхчистая деоксигенированная вода или влажный пар.
- Коррозия соударения предполагает обтекание твердой поверхности жидкостью с высокой скоростью, создающей картину локальной коррозии.
- Коррозия, вызванная эрозией Коррозия имеет место, когда жидкость содержит твердые абразивные частицы, такие как суспензия.
- Кавитация возникает в результате быстрого изменения давления жидкости, вызывающего образование пузырьков. Эти пузырьки схлопываются и создают ударные волны, которые могут повредить близлежащие металлические поверхности. Это часто происходит с рабочими колесами насосов и крутыми изгибами труб.
Межкристаллитная коррозия часто возникает в металлах с примесями. Эти примеси обычно располагаются вблизи границ зерен. Границы зерен представляют собой двумерные дефекты в кристаллической структуре металла, и они имеют тенденцию снижать как его электрические, так и термические свойства, делая эти области более уязвимыми для химических или электрохимических реакций, чем объемный металл.
Делегирование, , как следует из названия, происходит в металлических сплавах. В этом случае корродирует только один из металлов, образующих сплав, в то время как другой металл остается в основном неповрежденным. Цинк, углерод, никель и кобальт являются четырьмя наиболее распространенными элементами, которые выщелачиваются из их сплавов. Обычно требуется химическая реакция или сварка, хотя цинк и никель можно удалить из их сплавов с медью после длительного воздействия воды. Оставшаяся медная структура пористая и подвержена разрушению.
Как видно, коррозия принимает различные формы. Однако, даже при различных причинах и методах, все они представляют серьезную угрозу целостности любой металлической конструкции, на которую они воздействуют. Независимо от того, видна ли коррозия на поверхности или для ее обнаружения требуется специальное оборудование, абсолютно необходимо иметь план защиты и предотвращения коррозии.
Об автореДэрил Ролл
Консультант Astro Pak, Дэрил, является главным старшим техническим консультантом по вопросам коррозии, химии поверхности и пассивации нержавеющей стали. Имея более чем 40-летний опыт работы в области химической обработки, Дэрил опубликовал в журналах MICRO, UltraPure Water Journal и Chemical Engineering свои статьи о пассивации и борьбе с помутнением. Он является участником подкомитетов ASME BPE по требованиям к отделке поверхности и конструкционным материалам, а также ведущим участником рабочих групп по окрашиванию и пассивации. Дэрил имеет степень бакалавра искусств. получил степень бакалавра химии и наук о Земле в Калифорнийском государственном университете Фуллертона и лицензию профессионального инженера штата Калифорния.
Имея более чем 40-летний опыт работы в области химической обработки, Дэрил опубликовал в журналах MICRO, UltraPure Water Journal и Chemical Engineering свои статьи о пассивации и борьбе с помутнением. Он является участником подкомитетов ASME BPE по требованиям к отделке поверхности и конструкционным материалам, а также ведущим участником рабочих групп по окрашиванию и пассивации. Дэрил имеет степень бакалавра искусств. получил степень бакалавра химии и наук о Земле в Калифорнийском государственном университете Фуллертона и лицензию профессионального инженера штата Калифорния.
Основы теории коррозии металлов
Коррозия представляет собой электрохимический процесс, при котором должны присутствовать четыре (4) условия, иначе коррозии не будет:
- Должна быть положительная или анодная область, называемая «анодом».
- Должна быть отрицательная или катодная область, называемая «катодом».
- Должен быть влагосодержащий электролит для протекания ионного тока между анодом и катодом.
 Важно отметить, что анод и катод должны быть погружены в один и тот же электролит. Атмосфера не электролит. Два куска металла, соприкасающиеся друг с другом во влажной среде, создают отличные условия для протекания тока.
Важно отметить, что анод и катод должны быть погружены в один и тот же электролит. Атмосфера не электролит. Два куска металла, соприкасающиеся друг с другом во влажной среде, создают отличные условия для протекания тока. - Должен быть обратный путь для протекания электронного тока, который называется «металлическим путем» между анодом и катодом.
В гальванической реакции разница электрических потенциалов (напряжений) между анодом и катодом вызывает протекание тока коррозии. Анод – это область, которая страдает от потери металла или коррозии. Это результат разряда тока с поверхности металла. Количество металла, который подвергнется коррозии (ржавчине), прямо пропорционально величине протекающего тока. Например, разряд постоянного тока в один ампер в почву или водный электролит может удалить приблизительно двадцать (20) фунтов стали за один (1) год. В этом примере скорость коррозии стали составляет 20 фунтов/ампер-год. Каждый металл имеет свою собственную скорость коррозии и имеет единицу измерения «фунтов на ампер-год». В почвенных электролитах фактическое количество металла, подвергающегося коррозии за год, измеряется в граммах. Причина этого в том, что в почвах очень низкий ток разряда. Разряжаемый ток измеряется в тысячных долях ампера или миллиамперах (1000 мА = 1 Ампер). Зная несколько фактов, расчетное количество потребляемого тока можно легко рассчитать с помощью «Закона Ома», который гласит, что напряжение равно произведению ампер на сопротивление (E = IR). Следовательно, можно легко понять, что величина тока, который будет разряжаться, обратно пропорциональна величине сопротивления в цепи. С нематематической точки зрения, при постоянной разности напряжений между анодом и катодом величина анодного тока увеличивается по мере уменьшения сопротивления цепи. Следовательно, верно и обратное: величина анодного тока уменьшается по мере увеличения сопротивления цепи. Величина тока, который разряжается в электролит, напрямую связана с тем, насколько сильно металл будет подвергаться коррозии (ржавчине).
В почвенных электролитах фактическое количество металла, подвергающегося коррозии за год, измеряется в граммах. Причина этого в том, что в почвах очень низкий ток разряда. Разряжаемый ток измеряется в тысячных долях ампера или миллиамперах (1000 мА = 1 Ампер). Зная несколько фактов, расчетное количество потребляемого тока можно легко рассчитать с помощью «Закона Ома», который гласит, что напряжение равно произведению ампер на сопротивление (E = IR). Следовательно, можно легко понять, что величина тока, который будет разряжаться, обратно пропорциональна величине сопротивления в цепи. С нематематической точки зрения, при постоянной разности напряжений между анодом и катодом величина анодного тока увеличивается по мере уменьшения сопротивления цепи. Следовательно, верно и обратное: величина анодного тока уменьшается по мере увеличения сопротивления цепи. Величина тока, который разряжается в электролит, напрямую связана с тем, насколько сильно металл будет подвергаться коррозии (ржавчине).
Если одно из четырех условий, упомянутых выше, может быть устранено, процесс коррозии и/или потеря металла могут быть предотвращены или уменьшены. В большинстве ситуаций это невозможно сделать экономически; следовательно, используется система «катодной защиты» (CP), которая сегодня является одним из наиболее распространенных методов снижения коррозии в коррозионной машиностроительной промышленности. Система CP уменьшает коррозию, устраняя все анодные области на металлической конструкции, погруженной в электролит. Это достигается за счет превращения конструкции в чистый приемник тока, а не в разрядник тока. Это похоже на установку электрического щита (плотины) вокруг сооружения и высказывание «вы (сооружение) не можете отводить ток, потому что вы являетесь чистым приемником тока». Помните, любой металл, который пропускает ток, подвергается коррозии; и любой металл, который получает ток, защищен.
Катодная защита обычно осуществляется одним из двух методов: Первый метод включает подключение гальванического анода к защищаемой конструкции с использованием металлического проводника, такого как изолированный медный провод. Анод в этом случае сделан из металла, который имеет более высокий естественный потенциал (напряжение), чем естественный потенциал конструкции. Магний является одним из наиболее распространенных материалов для гальванических анодов, используемых в наземных системах CP, из-за его высокого природного потенциала. Этот тип системы CP полностью основан на разнице «естественных» гальванических потенциалов между двумя металлами, вызывающей протекание тока катодной защиты; следовательно, было создано название «Гальваническая система CP». Когда два металла погружены в один и тот же электролит и между ними есть металлическая дорожка, металл с более низким потенциалом становится катодным по отношению к другому металлу, который становится анодным. Причина этого явления заключается в том, что два металла имеют разность или дисбаланс потенциалов, в результате чего один из них является чистым приемником тока и становится катодным (защищенным). Другой металл с более высоким потенциалом становится анодным, потому что он является чистым разрядником тока и подвергается коррозии (ржавеет), переходя в оксидное состояние.
Анод в этом случае сделан из металла, который имеет более высокий естественный потенциал (напряжение), чем естественный потенциал конструкции. Магний является одним из наиболее распространенных материалов для гальванических анодов, используемых в наземных системах CP, из-за его высокого природного потенциала. Этот тип системы CP полностью основан на разнице «естественных» гальванических потенциалов между двумя металлами, вызывающей протекание тока катодной защиты; следовательно, было создано название «Гальваническая система CP». Когда два металла погружены в один и тот же электролит и между ними есть металлическая дорожка, металл с более низким потенциалом становится катодным по отношению к другому металлу, который становится анодным. Причина этого явления заключается в том, что два металла имеют разность или дисбаланс потенциалов, в результате чего один из них является чистым приемником тока и становится катодным (защищенным). Другой металл с более высоким потенциалом становится анодным, потому что он является чистым разрядником тока и подвергается коррозии (ржавеет), переходя в оксидное состояние. Чем больше разница потенциалов между двумя металлами, тем больше будет течь ток, когда все остальные переменные остаются постоянными. Поскольку напряжения, связанные с гальваническими системами CP, относительно низкие, небольшая разность потенциалов, существующая между двумя металлами, приводит к относительно низкому выходному току (миллиампер). Этот тип системы CP обычно связан с очень маленькими и/или хорошо покрытыми структурами, которые погружены в проводящий электролит (с низким удельным сопротивлением). Второй распространенный тип системы CP — это система импульсного тока. Этот тип системы CP основан на внешнем источнике постоянного тока, таком как выпрямитель, солнечная панель, батарея, топливный элемент и т. д., для подачи тока в защищаемую конструкцию. Ток форсируется или направляется по фиксированному пути; однако это определяется тем, как выполнены соединения с источником питания. Все, что подключено к положительной клемме источника питания, станет анодом, а все, что подключено к отрицательной клемме, станет катодом.
Чем больше разница потенциалов между двумя металлами, тем больше будет течь ток, когда все остальные переменные остаются постоянными. Поскольку напряжения, связанные с гальваническими системами CP, относительно низкие, небольшая разность потенциалов, существующая между двумя металлами, приводит к относительно низкому выходному току (миллиампер). Этот тип системы CP обычно связан с очень маленькими и/или хорошо покрытыми структурами, которые погружены в проводящий электролит (с низким удельным сопротивлением). Второй распространенный тип системы CP — это система импульсного тока. Этот тип системы CP основан на внешнем источнике постоянного тока, таком как выпрямитель, солнечная панель, батарея, топливный элемент и т. д., для подачи тока в защищаемую конструкцию. Ток форсируется или направляется по фиксированному пути; однако это определяется тем, как выполнены соединения с источником питания. Все, что подключено к положительной клемме источника питания, станет анодом, а все, что подключено к отрицательной клемме, станет катодом. Следовательно, легко понять, насколько важно соединить защищаемую структуру с отрицательным выводом, а не с положительным выводом, который сделал бы ее анодом. Поскольку эта система включает в себя внешний источник питания, ее размеры позволяют генерировать любое напряжение, необходимое для получения соответствующего тока для защиты конструкции. Это единственное основное функциональное различие, которое отделяет две системы друг от друга: низкое напряжение — низкий ток (гальванические системы CP) по сравнению с высоким напряжением — большой ток (системы импульсного тока).
Следовательно, легко понять, насколько важно соединить защищаемую структуру с отрицательным выводом, а не с положительным выводом, который сделал бы ее анодом. Поскольку эта система включает в себя внешний источник питания, ее размеры позволяют генерировать любое напряжение, необходимое для получения соответствующего тока для защиты конструкции. Это единственное основное функциональное различие, которое отделяет две системы друг от друга: низкое напряжение — низкий ток (гальванические системы CP) по сравнению с высоким напряжением — большой ток (системы импульсного тока).
Свойства металла: коррозионная стойкость
Коррозия является общей проблемой, затрагивающей поверхность большинства металлических деталей. В то время как коррозия часто влияет только на внешний вид металлической детали, сильная коррозия может повлиять на производительность и даже привести к отказу оборудования. Коррозия является настолько широко распространенной проблемой, что глобальные затраты на коррозию оцениваются в 2,5 триллиона долларов в год, согласно исследованию, проведенному Национальной ассоциацией инженеров-коррозионистов (NACE).
Здесь мы исследуем многие способы проявления коррозии в материале, а также методы, которые производители используют для предотвращения воздействия коррозии на рабочие характеристики деталей.
Коррозия и коррозионная стойкость
Коррозия — это естественный процесс, который происходит, когда химическая реакция с окружающей средой постепенно разрушает поверхность материала. Если не остановить коррозию, она будет распространяться глубже в материал, пока не повлияет на целостность самой детали. Сопротивление коррозии , с другой стороны, это способность материала сопротивляться коррозионным силам. Различные материалы способны сопротивляться коррозии с разной скоростью
Формы коррозии
По данным Национальной ассоциации инженеров по коррозии (NACE), коррозия любого металла проявляется одним из восьми способов.
1. Равномерное воздействие
Равномерное воздействие является наиболее распространенным типом коррозии. Это происходит посредством электрохимической реакции и распределяется равномерно по всей поверхности металла. В результате корродированный материал становится тоньше и со временем может выйти из строя.
Это происходит посредством электрохимической реакции и распределяется равномерно по всей поверхности металла. В результате корродированный материал становится тоньше и со временем может выйти из строя.
2. Гальваническая коррозия или коррозия двух металлов
Гальваническая коррозия или коррозия двух металлов относится к коррозионным повреждениям, возникающим при соединении двух разнородных материалов и их контакте с электричеством в проводящем растворе. Типичным примером являются подводные трубопроводы, изготовленные путем сварки стальных и медных труб. Что запускает эту реакцию, так это несходство электродных потенциалов между двумя разными металлами, что в конечном итоге приводит к тому, что один металл корродирует заметно быстрее, чем другой
3. Межкристаллитная коррозия
Межкристаллитная коррозия предполагает локальную коррозию исключительно по границам пораженного металла, а не на внутренних поверхностях. Этот тип коррозии может затронуть даже аустенитные нержавеющие стали , которые, как правило, устойчивы к коррозии, если они не обработаны должным образом и подвергаются воздействию агрессивных сред.
4. Щелевая коррозия
Как следует из названия, щелевая коррозия чаще всего возникает в щелях, а также под полимерными покрытиями и клеями. Механизм этого типа коррозионного воздействия основан на разнице между концентрациями кислорода внутри и снаружи щели или области покрытия.
5. Селективное выщелачивание
Селективное выщелачивание представляет собой удаление одного из металлов-компонентов твердого сплава в результате коррозионных процессов. Децинкификация (селективное удаление цинка из латунных сплавов) и деникелирование (селективное удаление никеля из труб из медно-никелевого сплава) являются примерами селективного выщелачивания. Однако этот процесс может происходить и со сплавами, содержащими алюминий, железо, хром или другие металлы.
6. Эрозионная коррозия
Эрозионная коррозия возникает, когда оксиды и гидроксиды металлов с корродированной металлической поверхности удаляются жидкостями, обнажая и воздействуя на свежий некорродированный металл. Этот тип коррозии обычно наблюдается в металлических трубах, где движущиеся жидкости переносят коррозию на не подвергшийся воздействию металл.
Этот тип коррозии обычно наблюдается в металлических трубах, где движущиеся жидкости переносят коррозию на не подвергшийся воздействию металл.
7. Коррозионное растрескивание под напряжением
Коррозионное растрескивание под напряжением относится к растрескиванию, вызванному напряжением и воздействием агрессивной среды. В этих ситуациях напряжения или условий окружающей среды самих по себе недостаточно, чтобы вызвать коррозию, но они работают вместе, вызывая растрескивание.
8. Точечная коррозия
Точечная коррозия – это еще одна разрушительная форма коррозии, которая приводит к образованию локальных отверстий в металле. Небольшие отверстия бывает трудно обнаружить, даже если они становятся глубже и угрожают целостности детали.
Предотвращение коррозии металлических деталей
Коррозия является серьезной проблемой для клиентов, занимающихся литьем, поэтому литейные предприятия (и другие производители металлов) используют различные методы для производства деталей, устойчивых к коррозии.
- Правильное планирование
Хотя ни один металл не является полностью устойчивым к коррозии во всех средах, тщательное планирование на этапе проектирования продукта обеспечивает максимальную коррозионную стойкость каждой детали в условиях эксплуатации. Помимо используемого материала, конструкции изделий могут также включать дренажные каналы и элементы, улучшающие поток воздуха. Дизайнеры также знают, что щели, зазоры и глухие отверстия могут привести к коррозии. - Легирование
Легирование включает смешивание металлических элементов, часто для улучшения таких качеств, как прочность, пластичность и коррозионная стойкость. Например, сочетание железа с не менее чем 12-13% хрома позволяет получить нержавеющую сталь, широко используемый коррозионно-стойкий сплав. - Анодирование
Анодирование означает окисление поверхности металла с целью получения защитного оксидного слоя. Анодирование может добавить цвет и улучшить эстетику и обычно используется для алюминиевых изделий.
- Термическая обработка
Надлежащая термическая обработка отливок играет большую роль в том, как материал будет вести себя в определенных условиях, включая его коррозионную стойкость. Для большинства аустенитных сплавов нержавеющей стали требуется этап отжига на твердый раствор для растворения любых присутствующих карбидов и предотвращения межкристаллитной коррозии. Термическая обработка после сварки также очень важна для предотвращения аналогичной десенсибилизации нержавеющих сплавов и межкристаллитного разрушения во время эксплуатации. - Азотирование и карбидирование
Азотирование и карбидирование — это виды специальной термической обработки, при которых поверхность металла подвергается воздействию химической среды, образующей защитный слой на поверхности детали. Оба метода в основном используются для упрочнения компонентов, а дополнительным преимуществом является небольшое повышение коррозионной стойкости. - Регулярное техническое обслуживание
Визуальный осмотр является ключом к предотвращению влияния коррозии на работу деталей. Регулярное техническое обслуживание для удаления видимой коррозии может значительно увеличить срок службы деталей в агрессивных средах.
Регулярное техническое обслуживание для удаления видимой коррозии может значительно увеличить срок службы деталей в агрессивных средах. - Гальванизация
Гальванизация включает в себя покрытие поверхности металлического предмета слоем цинка. Этот слой цинка действует как расходуемый анод , помогая предотвратить окислительную коррозию от повреждения исходного металла. - Окраска и порошковое покрытие
Окраска часто является наиболее экономичным способом защиты от коррозии. Краски и порошковые покрытия, часто на основе акрила, нейлона, винила или уретана, образуют защитный барьер между металлом и агрессивными элементами, такими как вода и кислород.
Стойкость металлов к естественной коррозии
Поскольку различные металлические элементы и сплавы подвергаются воздействию агрессивных сред, их внешний вид часто меняется. Красновато-коричневая ржавчина (оксид железа) является одним из наиболее распространенных видимых типов коррозии в материалах на основе железа. Ржавчина также является очень разрушительным типом коррозии и может легко привести к поломке детали, если ее не обслуживать должным образом.
Ржавчина также является очень разрушительным типом коррозии и может легко привести к поломке детали, если ее не обслуживать должным образом.
Другие изменения поверхности, хотя и тесно связанные с коррозией, на самом деле служат для защиты некоторых металлов от разрушительной коррозии. Например, потускнение , которое образуется на светлых металлах, таких как серебро, представляет собой самоограничивающийся коррозионный слой. Патина , представляющая собой зеленый слой, покрывающий многие медные предметы, состоит из карбоната меди и защищает эти предметы от дальнейшей коррозии. Точно так же ряд металлов естественным образом образуют оксидные слои при воздействии воздуха или воды. Эти слои включают оксид меди, оксид алюминия и оксид хрома.
Коррозия является неизбежным фактом в процессе производства. При заказе, сборке или производстве литых металлических деталей производители должны учитывать коррозию. Во многих случаях металлурги на литейных предприятиях, таких как Eagle Group, дают рекомендации по идеальному сплаву для каждой детали с учетом функциональной среды детали.




