Критические точки на диаграмме железо углерод: Критические точки на диаграмме “Железо-углерод”
alexxlab | 14.05.2023 | 0 | Разное
Металловедение (Гуляев А. П.)
Металловедение (Гуляев А. П.)
ОглавлениеПРЕДИСЛОВИЕ ТЕОРИЯ СПЛАВОВ ТЕОРИЯ СПЛАВОВГлава I. КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ 2. Классификация металлов 3. Кристаллическое строение металлов 4. Кристаллические решетки металлов 5. Реальное строение металлических кристаллов 6. Анизотропия свойств кристаллов 7. Методы изучения строения металлов Глава II. КРИСТАЛЛИЗАЦИЯ 1. Три состояния вещества 2. Энергетические условия процесса кристаллизации 3. Механизм процесса кристаллизации 4. Форма кристаллических образований 5. Строение слитка 6. Превращения в твердом состояние. Полиморфизм 7. Магнитные превращения 8. Закалка из жидкого состояния. Аморфное состояние Глава III. МЕХАНИЧЕСКИЕ СВОЙСТВА. НАКЛЕП И РЕКРИСТАЛЛИЗАЦИЯ 2. Упругая и пластическая деформация. Несовершенства решетки и прочность металлов 3. Сверхпластичность 4. Разрушение 5. Методы определения механических свойств 6. Наклеп 7. Влияние нагрева на строение и свойства деформированного металла (рекристаллизационные процессы) Глава IV. 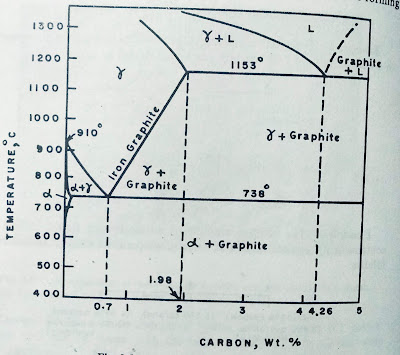 СТРОЕНИЕ СПЛАВОВ СТРОЕНИЕ СПЛАВОВ2. Химическое соединение 3. Твердый раствор на основе одного из компонентов сплава 4. Твердый раствор на основе химического соединения 5. Упорядоченные твердые растворы 6. Электронные соединения (фазы Юм-Розери) 7. Фазы Лавеса 8. Фазы внедрения Глава V. ДИАГРАММА СОСТОЯНИЯ 2. Общие замечания о построении диаграмм состояния 3. Экспериментальное построение диаграмм 4. Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов (I рода) 5. Правило отрезков 6. Диаграмма состояния для сплавов с неограниченной растворимостью в твердом состоянии (II рода) 7. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии (III рода) 9. Диаграмма состояния для сплавов, испытывающих полиморфные превращения 10. Кристаллизация сплавов в неравновесных условиях 11. Системы с тремя компонентами 12. 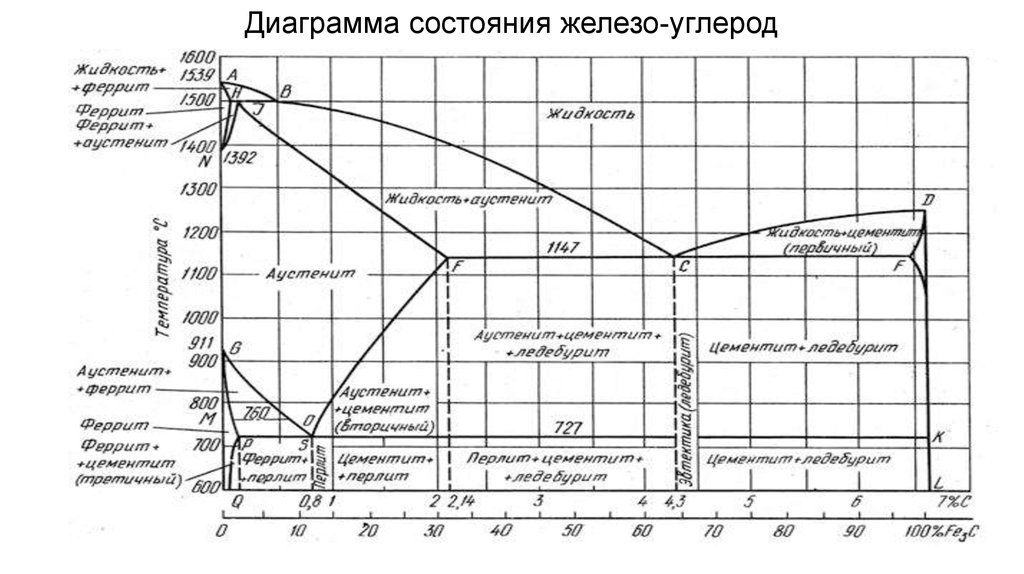 Упрощенные методы изучения многокомпонентных систем Упрощенные методы изучения многокомпонентных систем13. Связь между свойствами сплавов и типом диаграммы состояния Часть вторая. ЖЕЛЕЗОУГЛЕРОДИСТЫЕ СПЛАВЫ Глава VI. ДИАГРАММА ЖЕЛЕЗО—УГЛЕРОД 2. Железо 3. Цементит 4. Диаграмма состояния Глава VII. УГЛЕРОДИСТЫЕ СТАЛИ 1. Влияние углерода на свойства стали 2. Влияние постоянных примесей на свойства стали 3. Сталь различных способов производства. Чистая сталь 4. Углеродистая сталь общего назначения 5. Нагартованная сталь 6. Листовая сталь для холодной штамповки 7. Обрабатываемость резанием. Автоматные стали Глава VIII. ЧУГУН 2. Структура чугуна. Формы графита 3. Структура и свойства чугуна 4. Примеси в чугуне 5. Марки серых и высокопрочных чугунов 6. Ковкий чугун Часть третья. ТЕРМИЧЕСКАЯ ОБРАБОТКА Глава IX. ОБЩИЕ ПОЛОЖЕНИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ 2. Классификация видов термической обработки 3. Термическая обработка и диаграмма состояния 4 Основные виды термической обработки стали 5.  Четыре основных превращения в стали Четыре основных превращения в сталиГлава X. ТЕОРИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ 2. Рост аустенитного зерна 3. Распад аустенита 4. Мартенситное превращение 5. Бейнитное превращение 6. Превращения при отпуске 7. Влияние термической обработки на свойства стали 8. Термомеханическая обработка Глава XI. ПРАКТИКА ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ 2. Время нагрева 3. Химическое воздействие нагревающей среды 4. Закалочные среды 5. Прокаливаемость 7. Способы закалки 8. Обработка стали холодом 9. Дефекты, возникающие при закалке 10. Отжиг и нормализация Глава XII. ПОВЕРХНОСТНАЯ ЗАКАЛКА СТАЛИ 2. Высокочастотная закалка Глава XIII. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ 2. Цементация стали 3. Азотирование стали 4. Цианирование стали 5. Диффузионная металлизация Часть четвертая. ЛЕГИРОВАННЫЕ СТАЛИ И СПЛАВЫ Глава XIV. ВЛИЯНИЕ ЛЕГИРУЮЩИХ ЭЛЕМЕНТОВ 2. Влияние элементов на полиморфизм железа 3.  Распределение легирующих элементов в стали Распределение легирующих элементов в стали4. Влияние легирующих элементов на феррит 5. Карбидная фаза в легированных сталях 6. Влияние легирующих элементов на превращения в стали Глава XV. КЛАССИФИКАЦИЯ И МАРКИРОВКА ЛЕГИРОВАННЫХ СТАЛЕЙ 2. Маркировка легированных сталей Глава XVI. КОНСТРУКЦИОННЫЕ СТАЛИ 1. Механические свойства стали, влияние структуры и легирующих элементов 2. Термическая обработка конструкционных сталей 3. Цементуемые (низкоуглеродистые) стали 4. Улучшаемые (среднеуглеродистые) стали 5. Высокопрочные стали 6. Свариваемость стали 7. Строительная сталь 8. Арматурная сталь 9. Пружинная сталь 10. Шарикоподшипниковая сталь 11. Дефекты легированных сталей Глава XVII. ИНСТРУМЕНТАЛЬНЫЕ СТАЛИ 2. Инструментальные стали пониженной прокаливаемости 3. Инструментальные стали повышенной прокаливаемости (легированные инструментальные стали) 4. Быстрорежущие стали 5. Штамповые стали 6. Твердые сплавы Глава XVIII. 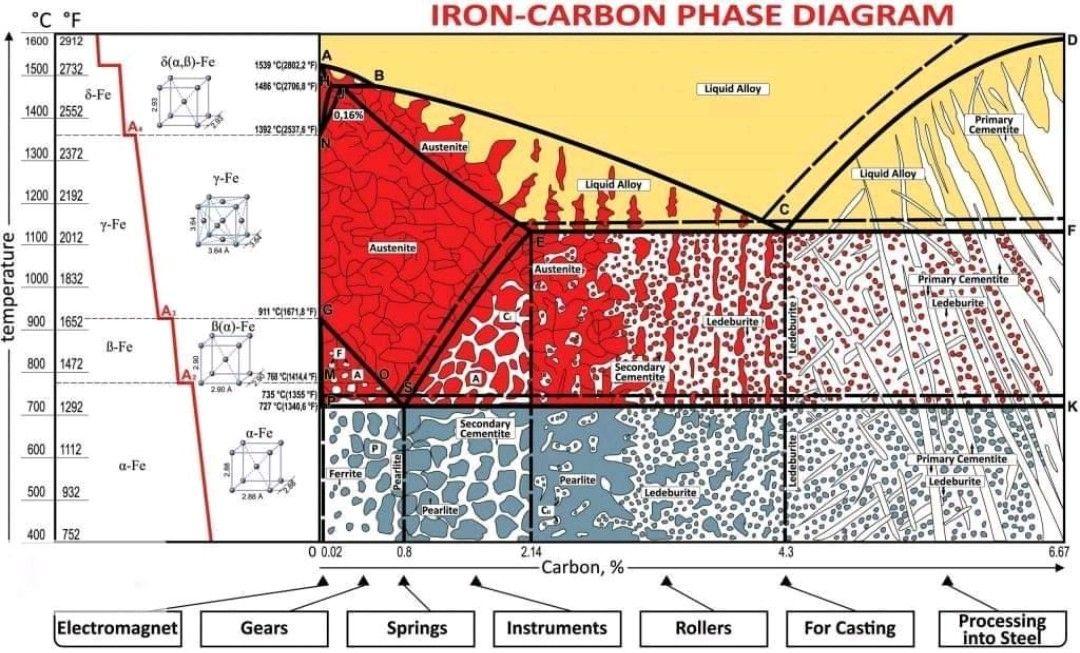 ЖАРОСТОЙКИЕ И ЖАРОПРОЧНЫЕ СТАЛИ И СПЛАВЫ ЖАРОСТОЙКИЕ И ЖАРОПРОЧНЫЕ СТАЛИ И СПЛАВЫ2. Жаропрочность 3. Оценка жаропрочных свойств 4. Влияние структуры и состава на жаропрочность 5. Классификация жаропрочных материалов 6. Перлитные и мартенситные жаропрочные стали 8. Никелевые и кобальтовые жаропрочные сплавы Глава XIX. КОРРОЗИОННОСТОЙКИЕ (НЕРЖАВЕЮЩИЕ) СТАЛИ И СПЛАВЫ 2. Хромоникелевые нержавеющие стали 3. Кислотостойкие стали и сплавы 4. Криогенные стали и сплавы Глава XX. ИЗНОСОСТОЙКИЕ СТАЛИ И СПЛАВЫ 2. Графитизированная сталь 3. Высокомарганцовистая сталь 4. Наплавочные материалы Глава XXI. ТИТАН И ЕГО СПЛАВЫ 2. Легирование титана 3. Фазовые превращения в титановых сплавах 5. Термическая обработка титановых сплавов 6. Примеси в титановых сплавах 7. Коррозионная стойкость титана Глава XXII. ТУГОПЛАВКИЕ МЕТАЛЛЫ 2. Взаимодействие тугоплавких металлов с другими элементами и между собой 3. Механические свойства и жаропрочность 4.  Хладноломкость тугоплавких металлов Хладноломкость тугоплавких металлов5. Сопротивление окислению и защита от окисления 6. Коррозионная стойкость Глава XXIII. СПЛАВЫ С ОСОБЫМИ ТЕПЛОВЫМИ И УПРУГИМИ СВОЙСТВАМИ 2. Сплавы с постоянным модулем упругости Глава XXIV. МАГНИТНЫЕ СТАЛИ И СПЛАВЫ 2. Стали и сплавы для постоянных магнитов (магнитнотвердые сплавы) 3. Магнитномягкие сплавы 4. Немагнитные стали 5. Электротехнические сплавы Глава XXV. СПЛАВЫ АТОМНОЙ ЭНЕРГЕТИКИ 2. Конструкционные материалы. Теплоносители 3. Ядерное горючее (уран, плутоний, торий) Часть пятая. Цветные металлы и сплавы Глава XXVI. ЛЕГКИЕ МЕТАЛЛЫ И ИХ СПЛАВЫ 1. Свойства алюминия 2. Постоянные примеси алюминия (железо и кремний) 3. Термическая обработка сплавов Al-Cu 4. Влияние состава алюминиевых сплавов на процессы, происходящие при термической обработке 5. Классификация алюминиевых сплавов 6. Деформируемые сплавы, не упрочняемые термической обработкой 7. Дюралюминий и другие деформируемые сплавы, упрочняемые термической обработкой 8. 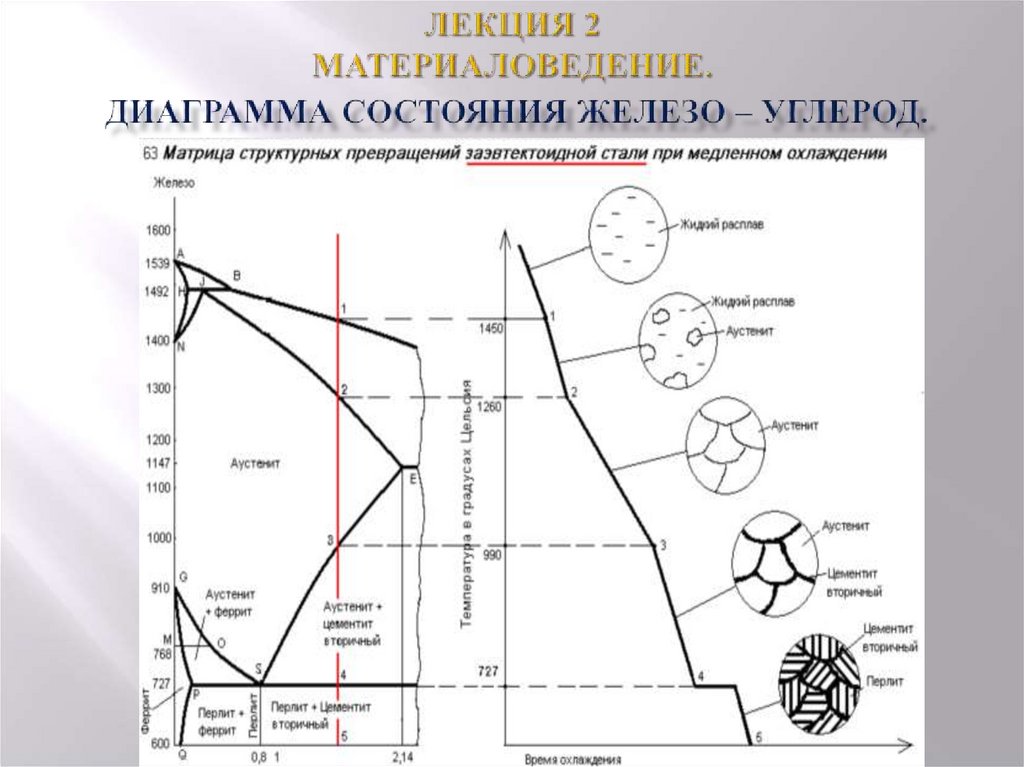 9. Силумины и другие алюминиевые сплавы для фасонного литья 10. Жаропрочные алюминиевые сплавы 11. Магний 12. Сплавы магния 13. Бериллий 14. Сплавы бериллия Глава XXVII. МЕДЬ И ЕЕ СПЛАВЫ 2. Сплавы меди с цинком (латуни) 3. Сплавы меди с оловом (оловянистые бронзы) 4. Сплавы меди с алюминием, кремнием, бериллием и другими элементами ГЛАВА XXVIII. ПОДШИПНИКОВЫЕ СПЛАВЫ И ПРИПОИ 2. Легкоплавкие подшипниковые сплавы (баббиты) 3. Припои 4. Легкоплавкие сплавы Глава XXIX. НЕКОТОРЫЕ СПЛАВЫ ЦВЕТНЫХ МЕТАЛЛОВ 2. Типографские сплавы 3. Благородные металлы |
Диаграмма состояния сплавов железо-углерод
Главная › Новости
Опубликовано: 03.09.2018
Диаграмма состояний железо-углерод
Современную промышленность сложно представить без использования различного вида металлических сплавов, в том числе и стальных.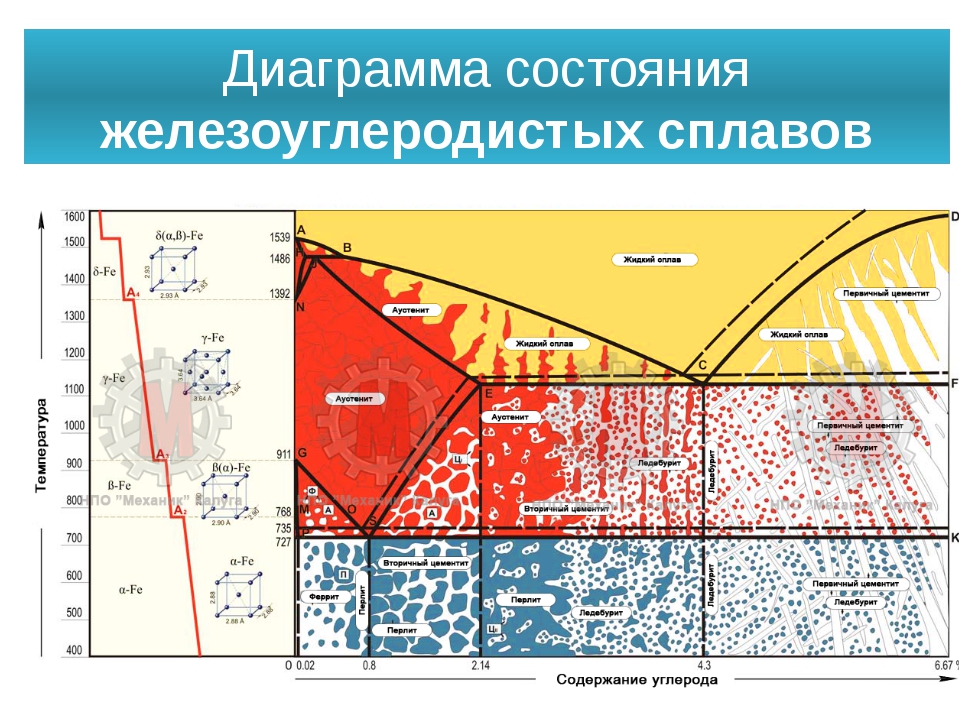 Разработкой их составов занимаются ученые – металлурги в разных странах, но для прогнозирования свойств будущих сплавов, большая часть специалистов руководствуется диаграммой железо – углерод. Она дает четкое представление о том, как устроено большинство стальных сплавов и чугунов.
Разработкой их составов занимаются ученые – металлурги в разных странах, но для прогнозирования свойств будущих сплавов, большая часть специалистов руководствуется диаграммой железо – углерод. Она дает четкое представление о том, как устроено большинство стальных сплавов и чугунов.
Диаграмма состояния
Диаграмма содержит в себе некоторое количество линий и критичных точек, обозначающих состояние расплава при определенном нагреве.
Классификация железоуглеродистых сплавов
Различные комбинации этих элементов приводят к получению большого количества сплавов, которые можно разделить на три большие группы:
кристаллизация сплавов
Техническое железо. Стали. Чугуны.
Техническое железо
К техническому железу относят материалы, в которых содержится менее 0,02% углерода. К сталям относят, материалы, в которых углерод находится в пределах от 0,02 до 2,14%. И в группу чугунов входят материалы, количество углерода в которых превышает 2,14%.
К сталям относят, материалы, в которых углерод находится в пределах от 0,02 до 2,14%. И в группу чугунов входят материалы, количество углерода в которых превышает 2,14%.
Материаловедение. Диаграмма сплавов.
Компоненты в системе железо углерод
АустенитАтомы размещается в гранецентрированной ячейке. Твердость аустенита имеет твердость 200 … 250 единиц по Бринеллю. Кроме того у него хорошая пластичность и он отличается парамагнитностью.
Железо
Железо – это материал, относящийся к металлам. Его натуральный цвет – серебристо-серый. В чистом виде он очень пластичен. Его удельный вес составляет 7,86 г/куб. см. Температура плавления составляет 1539 °C. На практике чаще всего применяют техническое железо, в составе которого присутствуют следующие примеси – марганец, кремний и многие другие. Массовая доля примесей не превышает 0,1%.
Железо
У железа есть такое свойство как полиформизм. То есть, при одном и том же химическом составе, это вещество может иметь разную структуру кристаллической решетки и соответственно разные свойства. Модификации железа называют соответственно – Б, Г, Д. Все эти модификации существуют при разных условиях. Например, тип Б, может существовать только при температуре 911 °С. Тип Г может существовать в диапазоне от 911 до 1392 °С. Тип Д существует в диапазоне от 1392 до 1539 °С.
Каждый из типов обладает своей формой кристаллической решеткой, например, у типа Б решетка представляет собой куб, решетка типа Г имеет гранецентрированную кубическую форму. Решетка типа Д, имеет форму объемно центрированного куба.
Еще одно свойство состоит в том, что при температуре ниже 768 железо ферримагнитно, а при ее повышении это свойство теряется.
Точки полиморфной и магнитной трансформации называют критическими. На таблице они обозначены следующим образом – А2, А3, А4. Цифровые индексы показывают тип трансформации. Для более полного различия превращения железа из одного вида в другой к обозначению добавляют индексы с и r. Первый говорит о нагреве, второй об охлаждении.
Для более полного различия превращения железа из одного вида в другой к обозначению добавляют индексы с и r. Первый говорит о нагреве, второй об охлаждении.
Полиморфные модификации железа
При высоких параметрах пластичности, железо не обладает высокой твердостью, по шкале Бринелля она равна 80 единиц.
Железо имеет возможность образовывать твердые растворы. Их можно разделить на две группы – раствор замещения и внедрения. Первые состоят их железа и других металлов, вторые из железа и углерода, водорода и азота.
Углерод
Другой компонент системы – углерод. Это – неметалл и он обладает тремя модификациями в виде алмаза, графита и угля. Он плавится при 3500 °С.
Аллотропные модификации углерода
В сплаве железа, этот элемент находится в виде твердого раствора, его называют цементит или в виде графита. В таком виде он присутствует в сером чугуне. Графит, не отличается ни пластичностью, ни прочностью.
Цементит
Доля углерода составляет 6,67%.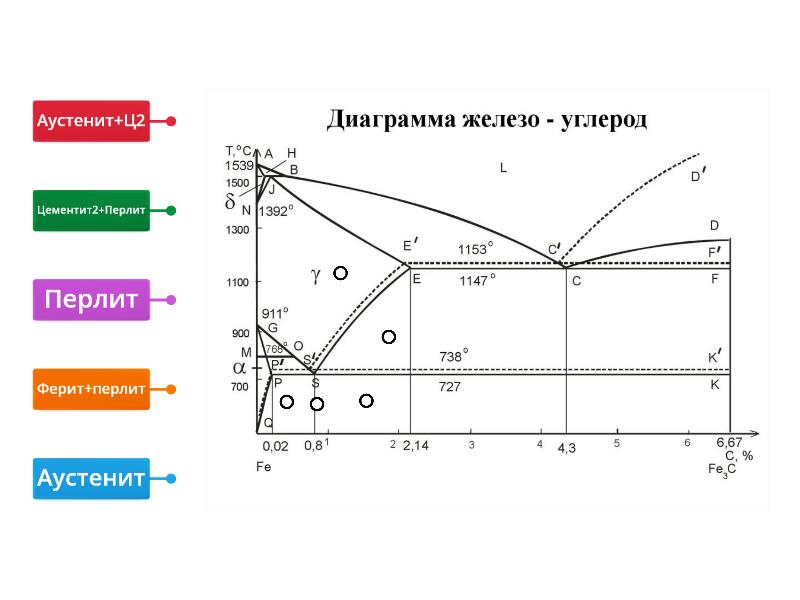 Он обладает высокой твердостью – 800 НВ, но при этом у него отсутствует пластичность. Полиморфными свойствами не обладает.
Он обладает высокой твердостью – 800 НВ, но при этом у него отсутствует пластичность. Полиморфными свойствами не обладает.
Он обладает следующим свойством – при формировании раствора замещения, углерод может быть заменен на атомы других веществ, например, на хром или никель. Такой раствор получил название легированного раствора.
Цементит
Он не обладает устойчивостью, при наличии некоторых условий он может разлагаться, при этом происходит трансформация углерода в графит. Это свойство нашло применение при образовании чугунов.
Кстати, в жидком состоянии, железо может растворять в себе примеси, при этом образуя, однородная масса.
Феррит
Так называют твердый раствор, при котором происходит внедрение углерода в железо.
Он растворяется с определенной переменностью, при нормальной (комнатной) температуре объем углерода лежит в пределах 0,006%, при 727 °С, то концентрация углерода составит 0,02%. По достижении 1392 °С образуется феррит.
Феррит
Содержание углерода составит 0,1%. Его атомы размещаются в дефектных узлах решетки.
Его атомы размещаются в дефектных узлах решетки.
Феррит по своим параметрам близок к железу.
Аустенит в сталях
Наличие аустенита в стальных сплавах придает им определенные свойства. Детали и узлы, произведенные из подобных сталей, предназначаются для работы в средах, содержащие агрессивные компоненты, например, на предприятиях, перерабатывающих разные кислоты.
Стали этого класса отличаются высоким уровнем легирования, во время кристаллизации формируется гранецентрированная решетка. Такая структура не подвержена изменению даже под воздействием глубокого холода.
Стали этого типа можно разделить на два типа отличающиеся друг от друга составом. В первых, содержатся такие вещества как железо, никель, хром. При этом общее количество добавок не может превышать 55%. Ко второй группе относят никелевые и железоникелевые композиции. В никелевых композициях, его содержание превышает 55%. В железоникелевых составах соотношение никеля и железа составляет 1:5, а количество никеля начинается от 65%.
Такое количество никеля обеспечивает повышенную пластичность, а хром, в свою очередь обеспечивает высокую коррозионную стойкость и жаропрочность. Применение других легирующих материалов позволяет выплавлять сплавы с уникальными эксплуатационными свойствами. Металлурги, составляя рецептуру сплавов, руководствуются будущим назначением сталей.
Для получения легированный сталей применяют ферритизаторы, которые придают постоянство аустенитам, к таким веществам относят ниобий, кремний и некоторые другие. Кроме них применяют углерод, марганец – их называют аустенизаторами.
Цементит: формы существования
Так называют соединение углерода и железа. Это компонент чугуна и некоторых сталей. В него входит 6,67% углерода.
В его кристалл входит несколько октаэдров, они расположены друг по отношению к другу с некоторым углом. Внутри каждого из них расположен атом углерода. В результате такого построения получается следующая картина – один атом вступает в связь с несколькими атомами железа, а железо в свою очередь связано с тремя атомами этого элемента.
Кристаллическая решетка цементита
У этого вещества имеются все свойства, которые присущи металлам – электропроводность, своеобразным блеском, высокая теплопроводность. То есть, смесь железа и углерода, ведет себя как металл. Этот материал обладает определенной хрупкостью. Большая часть его свойств определена сложным строением кристаллической решетки.
Этот материал плавится при 1600 градусах Цельсия. Но на этот счет существует несколько мнений, одни исследователи считают, что его температура плавления лежит в диапазоне от 1200 до 1450, другие определяют, что верхний уровень равен 1300 °С.
Первичный цементит
Металлурги разделяют три типа этого вещества – первичный, вторичный, третичный.
Диаграмма железо-цементит
Первичный, получается из жидкости при закалке сплавов, которые содержат в себе 5,5% углерода. Первичный имеет форму в виде крупных пластин.
Вторичный
Этот элемент получается из аустенита при охлаждении последнего. На диаграмме этот процесс этот процесс можно видеть по диаграмме Fe – C.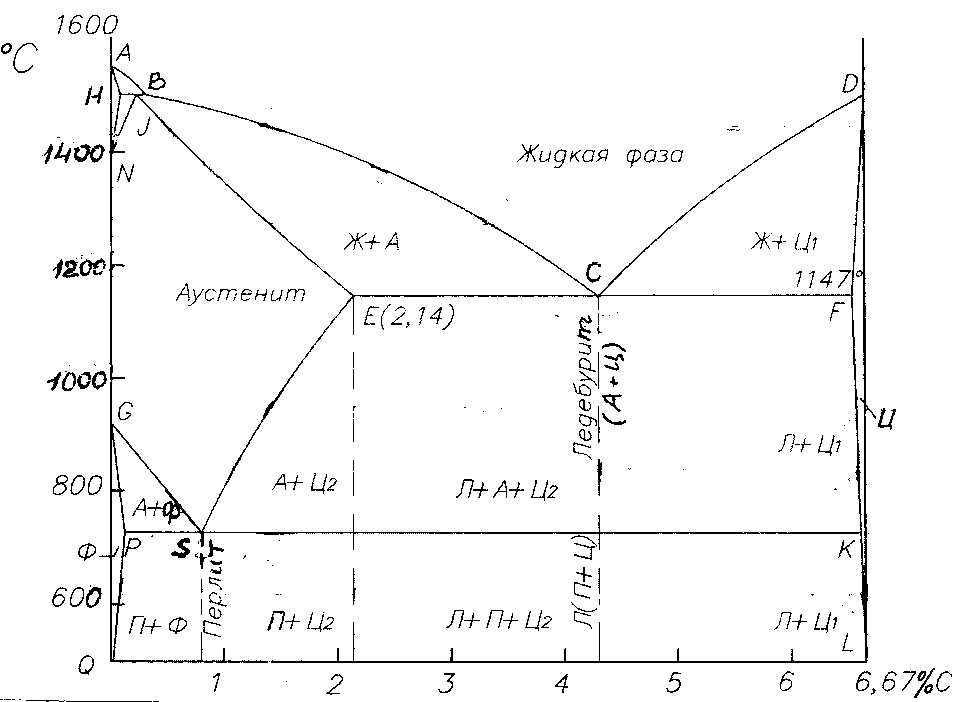 Цементит представлен в виде сетки, размещенной по границам зерен.
Цементит представлен в виде сетки, размещенной по границам зерен.
Третичный
Этот тип, является производным от феррита. Он имеет форму иголок.
В металлургии существуют и другие формы цементита, например, цементит Стеда и пр.
Другие структурные составляющие в системе железо углерод
Перлит
Перлит – это механическая смесь, которая состоит из феррита и цементита. Ледебурит представляет собой переменный раствор.
Перлит
При температуре от 1130 и до 723 °С в его состав входят аустенит и цементит. При более низких температурах он состоит из аустенит заменяет феррит.
Ледебурит в сталях
Стали, в основании которых лежит ледебурит относят к легированным. В процессе кристаллизации происходит образование ледебурита. На диаграмме состояния железо углерод этот процесс указан в точке Е, которая расположена на линии Fe – Fe3C.
Использование таких элементов, как хром, вольфрам и некоторых других, приводят к образованию таких сплавов как Р6М5. Эту сталь и ее аналоги применяют при изготовлении инструментов, например, металлорежущих.
Эту сталь и ее аналоги применяют при изготовлении инструментов, например, металлорежущих.
Узловые критические точки диаграммы состояния системы железо углерод
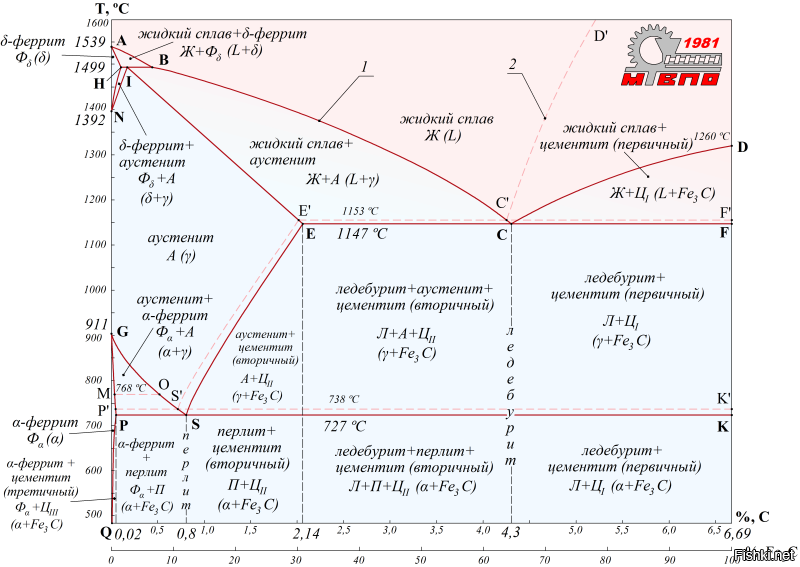
На диаграмме железо углерод отмечено некоторое количество точек, называемых критичными. Каждая точка несет в себе информацию о температуре, долевом содержании углерода и описанием того, что именно происходит в этом месте.
Всего существует 14 этих критичных точек.
Например, А, говорит о том, что при температуре 1539 °С и при нулевом содержании углерода происходит плавление чистого железа. D говорит о том, что при температуре 1260 возможно плавление Fe3c.
Точки расположены на пересечении линий, размещенных на диаграмме.
Значение линий диаграммы состояния системы железо углерод
Каждая линия, расположенная на диаграмме, так же несет в себе смысловую нагрузку. Например, линия PQ показывает выделение третичного цементита из феррита.
Все расшифровки значений точек и линий всегда есть в приложениях к диаграмме состояния углерод железо.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Объяснение диаграммы фаз железа-углерода » BorTec
Углерод является наиболее важным легирующим элементом в железе. По этой причине даже самые незначительные изменения в содержании углерода могут привести к значительным изменениям в характеристиках материала. Однако важность фазовой диаграммы железо-углерод быстро снижается, если материал быстро охлаждается или нагревается. Диаграмма также менее информативна, если увеличивается доля других легирующих элементов .
Углерод встречается в двух различных формах: во-первых, в связанной форме и, во-вторых, в виде элементарного углерода в форме графита. Вот почему фазовая диаграмма железо-углерод представлена в двух формах . Стабильная система с диаграммой Fe-Графит и метастабильная с диаграммой Fe-Fe 3 C. Обе системы можно представить на одной диаграмме, хотя на практике в основном используется метастабильная система Fe-Fe 3 C.
Как представлены фазы на фазовой диаграмме железо-углерод?
AG Caesar, CC BY-SA 4.0, через Wikimedia Commons
Ось X на диаграмме представляет массовый процент углерода. Температура отложена по оси Y. Чтобы сделать диаграмму более наглядной, показано только технически интересное содержание углерода от 0 до 6,67%. Сплавы, содержащие более 6,67% углерода, образуют фазу 100% цементита
Поля фаз ограничены линиями, представляющими точки излома, сдвинутые в сторону других температур. Для лучшего понимания соответствующие точки отмечены буквами . Обратите внимание, что на некоторых диаграммах точка I обозначена как J. Одной из наиболее важных линий является линия ликвидуса , представленная ломаной ABCD. Выше этой линии сплав находится в жидкой форме. Полилиния AHIECF называется линией солидуса . Ниже этой линии сплав полностью тверд. Если температура находится между ними, сплав имеет кашицеобразную консистенцию. Сплав состоит из остаточного расплава, δ-железа, γ-железа и цементита (Fe 3 С). Пропорции текучие и меняются в зависимости от температуры. Как только при охлаждении сплава температура падает ниже линии ликвидуса, начинается первичная кристаллизация из расплава.
Сплав состоит из остаточного расплава, δ-железа, γ-железа и цементита (Fe 3 С). Пропорции текучие и меняются в зависимости от температуры. Как только при охлаждении сплава температура падает ниже линии ликвидуса, начинается первичная кристаллизация из расплава.
Железо имеет различные аллотропные модификации . Таким образом, в зависимости от содержания углерода и температуры образуются разные фазы. Интеркаляционные смешанные кристаллы, образованные δ-, γ- и α-твердыми растворами железа, обладают различной растворимостью углерода. Вариации вызваны различными пространственными решетками и постоянными решетки.
Какое металлографическое обозначение?
В металлографии смешанные кристаллы называются δ-ферритом, аустенитом для γ-смешанных кристаллов и ферритом для α-смешанных кристаллов. Here is an overview of the carbon content of the individual phases :
Designation | Max C-content | Metallographic designation |
δ-solid solution | 0. | δ-Ferrite |
γ-solid solution | 2.06 % at 1147° C | |
| α-solid solution | 0,02 % при 723°C | Феррит |
Цементит (Fe 3 C) представляет собой соединение железа с углеродом, которое также является фазой. Однако цементит представляет собой промежуточную фазу , которую не следует путать со смешанными кристаллами железа. Химический состав цементита всегда одинаков, хотя он встречается в трех различных формах :
- Первичный цементит: первичная кристаллизация из расплава (соответствует линии CD)
- Вторичный цементит: выделение из аустенита (соответствует линии ES)
- Третичный цементит: выделение из расплава феррит (соответствует линии PQ)
Вторичный цементит присутствует при содержании углерода от 2,06 до 4,3 % C, но не показан на диаграмме. Это связано с тем, что его нельзя обнаружить металлографически.
Это связано с тем, что его нельзя обнаружить металлографически.
В дополнение к фазам также встречаются фазовые смеси:
Обозначение | состоит из | PEREADENDIENS 995599555 | . | 0,02 % – 6,67 % при T ≤ 723 ° C |
| Ledeburite I | 51,4 % Austenite / 48,6 % Cemetit | |||
| Ledeburite II | 51,4 % Perlite / 48,6 % цементит | 2,06 % – 6,67 % при T ≤ 723 ° C |
What Athermal Reactive.
Три изотермические реакции показаны на фазовой диаграмме железо-углерод. Линия HIB представляет собой перитектику, линия ECF — эвтектику, а левая PSK — эвтектоидную реакцию.
При нагреве или охлаждении стали на линиях происходят превращения. Они отмечены точками останова. Вот самые важные из них:
- На линии P-S-K аустенит распадается на перлит , если содержание углерода составляет менее 0,02 % (A 1 ).
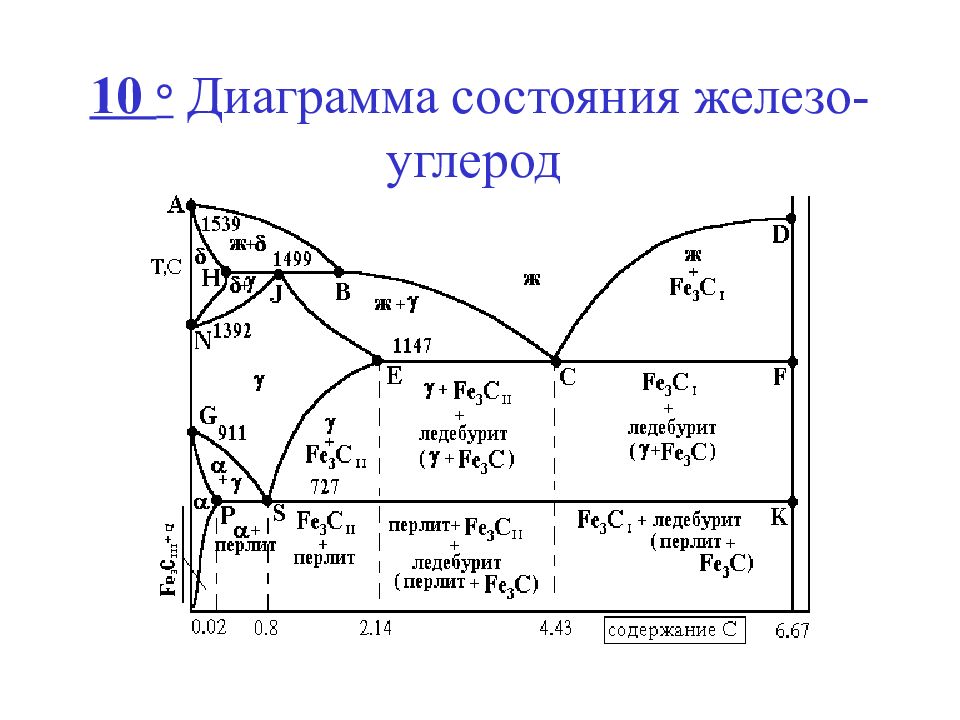
- Феррит теряет ферромагнетизм на линии M-O при нагреве выше 769°C (A 2 )
- Если температура падает ниже линии G-O-S при охлаждении, образуется низкоуглеродистый феррит . В ходе этого процесса аустенит накапливается с выделяющимся углеродом до тех пор, пока температура не поднимется до 723 °С, и он не достигнет эвтектоидной концентрации (А 3 ).
Как применяется диаграмма железо-углерод?
Фазовая диаграмма железо-углерод помогает лучше понять поведение чугуна и стали. Сталь, например, легко формуется в диапазоне аустенита и поэтому может быть кована. С другой стороны, чугун имеет более высокую долю углерода, который присутствует в форме графита и ледебурита. Это значительно ограничивает пластичность.
По этой причине диаграмма железо-углерод становится важным инструментом для оценка стали и чугуна .
Диаграмма равновесия железа и углерода с объяснением [Фазовая диаграмма]
В этой статье мы обсудим диаграмму равновесия железа и углерода , использование диаграммы равновесия, типы диаграммы равновесия железа и углерода, а также различные фазы и термины, связанные с железом и углеродом.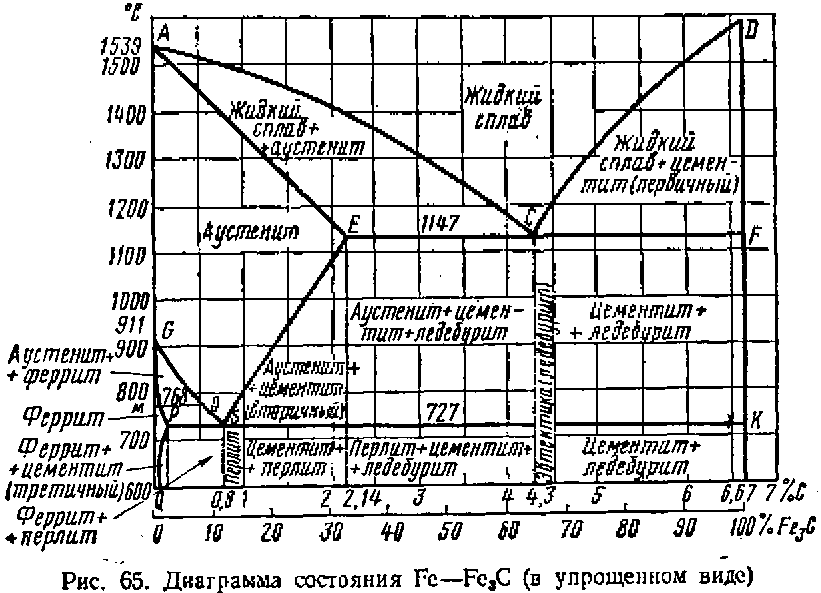 фазовая диаграмма.
фазовая диаграмма.
Содержание
Что такое фазовые диаграммы?Фазовые диаграммы представляют собой графическое представление фаз, присутствующих в сплаве, при различных условиях температуры, давления и химического состава.
Затвердевание металлических сплавов легко понять с помощью диаграмм равновесия. Это графические изображения изменений состояния из-за изменений температуры и концентрации. Поскольку эта диаграмма показывает природу и состав сплавов, а также количество и состав фаз в данной системе, она также известна как диаграмма состава или фазовая диаграмма.
Диаграмма равновесия Характеристики и применение Равновесие означает, что изменения, происходящие в системе в результате протекания процесса в одном направлении, полностью компенсируются изменениями вследствие реверсирования процесса в системе. Таким образом, это рассматривается как динамическое состояние баланса между движениями атомов, где равнодействующая равна нулю.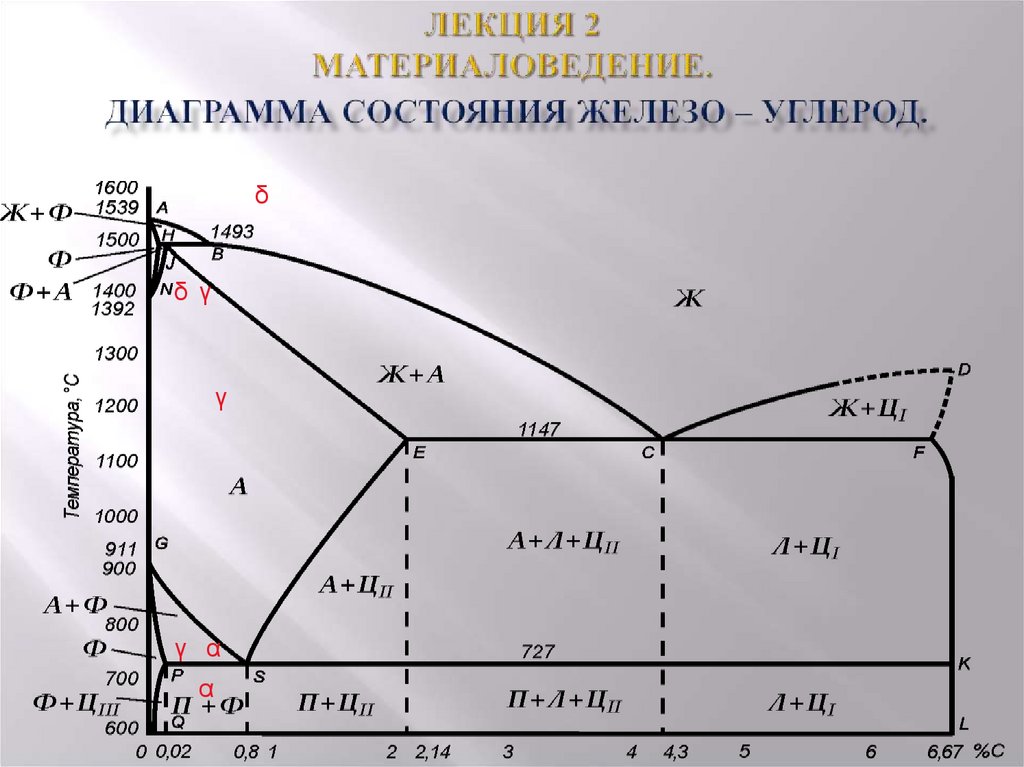
Скорость изменения температуры или состава была чрезвычайно низкой во время экспериментальной работы, так что сплав «останавливался» до того, как переменная, такая как температура, снова изменялась. Состояние, таким образом, является состоянием покоя, а не изменения.
Диаграмма равновесия показывает следующее:
1. Температура, при которой твердый сплав начнет плавиться и закончит плавиться.
2. Возможные фазовые изменения, которые произойдут в результате изменения состава или температуры.
Диаграмма описывает подходящие условия для существования равновесия двух или более фаз. Например, диаграмма состояния воды описывает точку (тройную точку), в которой вода может сосуществовать в трех разных фазах одновременно. Это происходит при температуре чуть выше точки замерзания (0,01°C) и давлении 0,006 атм.
Использование диаграммы равновесия в металлургии- Разработка новых сплавов на основе требований применения.
- Производство этих сплавов.
- Разработка и внедрение соответствующих процедур термообработки для улучшения химических, физических и механических свойств этих новых сплавов.
- Устранение неполадок, возникающих при использовании этих новых сплавов, что в конечном итоге повышает предсказуемость продукта.
Диаграмма равновесия железа и углерода (также называемая фазовой диаграммой железа и углерода) представляет собой графическое представление соответствующих состояний микроструктуры сплава железо-углерод (Fe-C) в зависимости от температуры и содержание углерода.
Фазовая диаграмма железо-углерод обычно используется для полного понимания различных фаз стали и чугуна. Сталь и чугун представляют собой сплавы как железа, так и углерода. Кроме того, оба сплава содержат микроэлементы в небольших количествах.
График довольно сложный, но поскольку мы ограничиваем наше исследование Fe3C, мы будем рассматривать только до 6,67 весовых процентов углерода.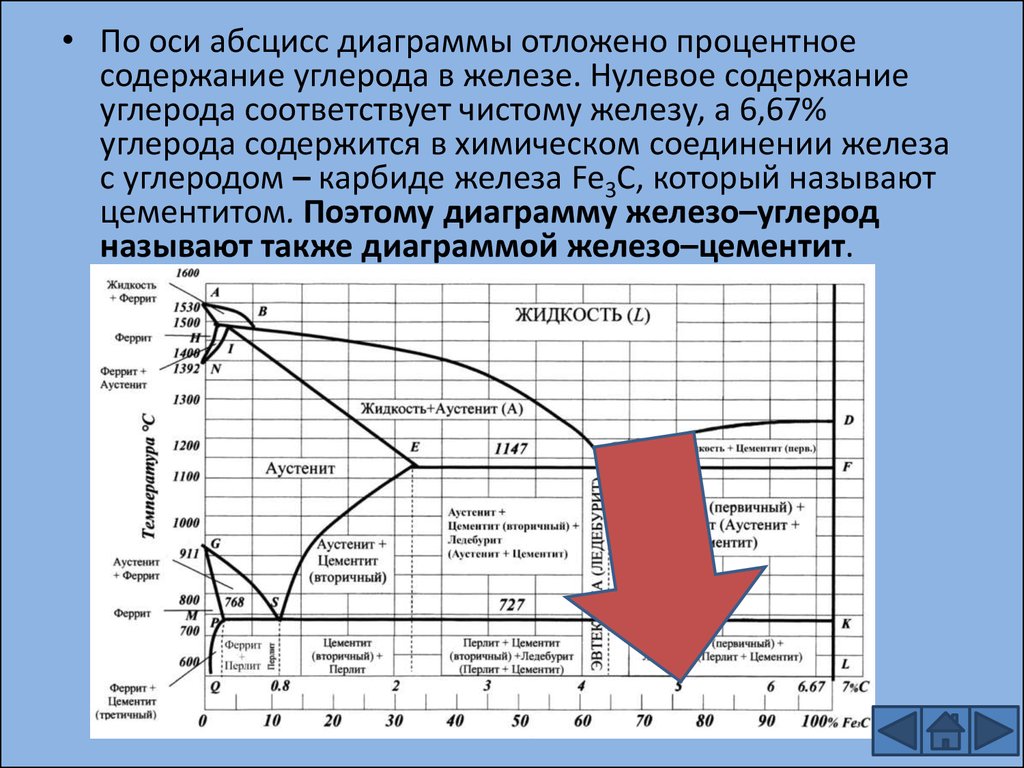
Бинарная диаграмма равновесия железо-углерод лежит в основе стали и чугуна. Речь идет о превращениях, происходящих в сплавах состава от чистого железа до цементита (6,67% углерода). Есть две версии диаграммы равновесия железа и углерода:
1. Железоцементитная система. 2. Железо-графитовая система.
Эти две системы зависят от скорости охлаждения. При быстром охлаждении образуется цементит, и эта система известна как система железо-цементит . В этой системе структуры, образующиеся в затвердевших фазах, не достигают достаточно полного равновесия. Таким образом, железоцементитная система является метастабильной .
При медленном охлаждении образуется графит, и система известна как железо-графитовая система . Структуры, образующиеся в затвердевшей фазе, достигают достаточно полного равновесия.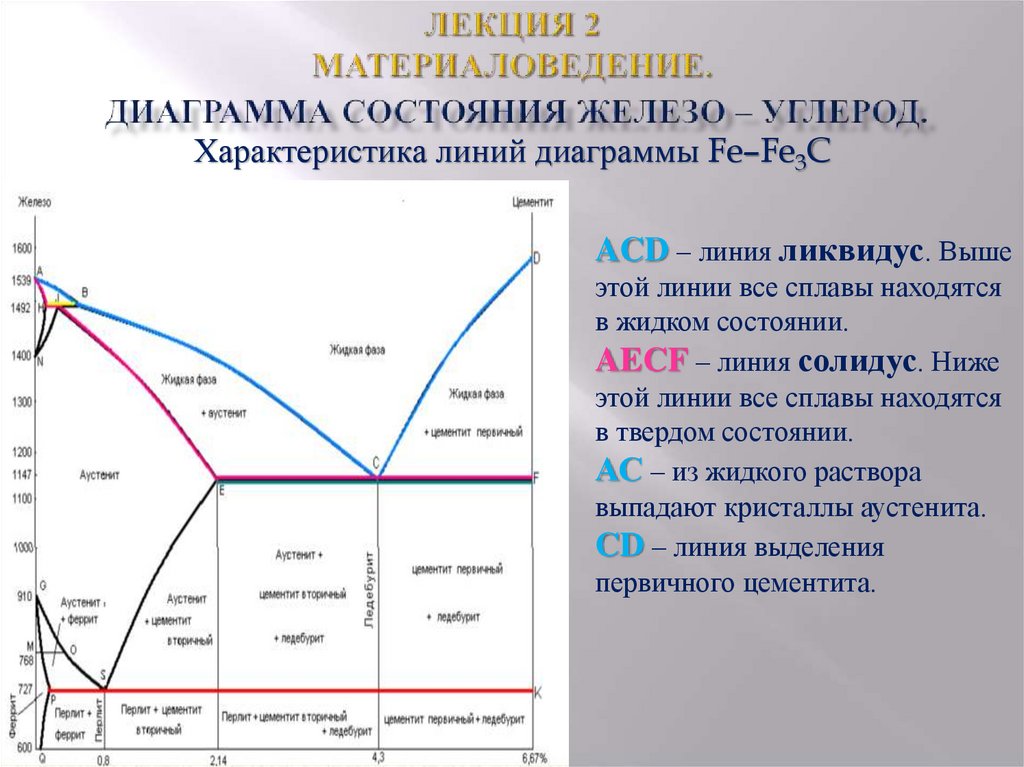 Итак, это стабильная версия .
Итак, это стабильная версия .
Масштаб в процентах по оси X фазовой диаграммы железо-углерод находится в диапазоне от 0% до 6,67% Углерод. Металл известен просто как железо или чистое железо с максимальным содержанием углерода 0,008 процентов по массе углерода. При комнатной температуре он существует в феррит гос.
Сталь представляет собой железоуглеродистый сплав с содержанием углерода от 0,008 до 2,14 процентов. Марки стали в этом диапазоне известны как низкоуглеродистая сталь (или мягкая сталь), среднеуглеродистая сталь и высокоуглеродистая сталь .
Когда содержание углерода превышает 2,14 процентов, мы достигаем стадии чугуна . Чугун чрезвычайно тверд, но его хрупкость сильно ограничивает его применение и методы формования.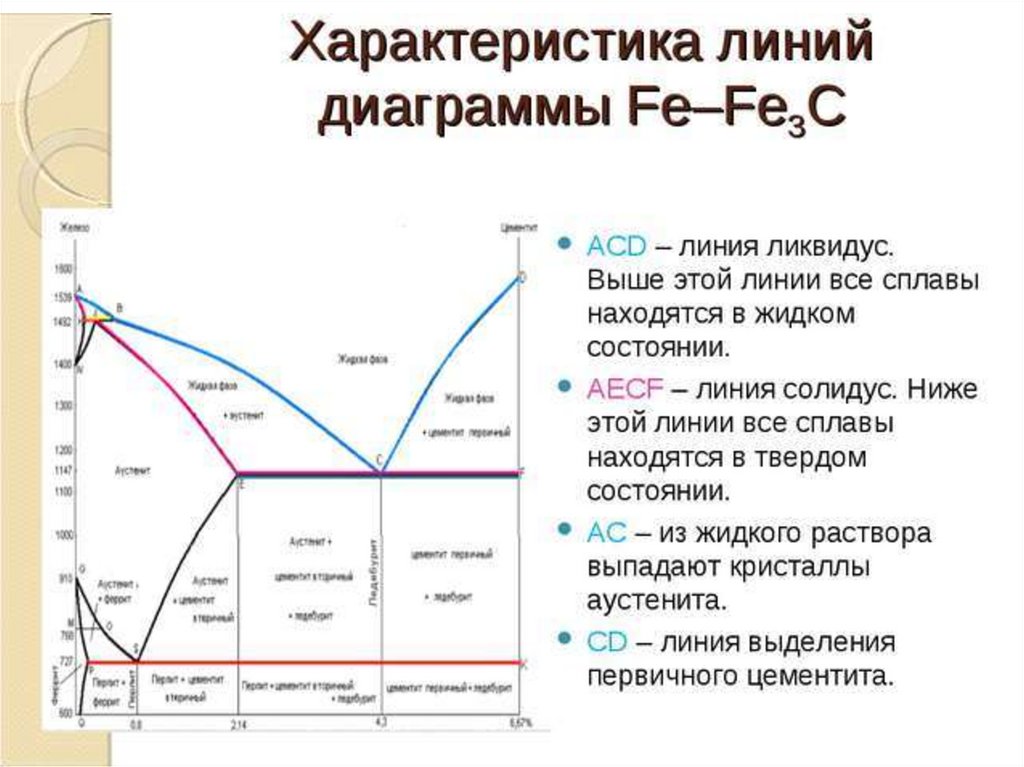
Если построить серию кривых нагрева время-температура для сталей с различным содержанием углерода и нанести соответствующие критические точки, то получится диаграмма, подобная рис. 2.14. Эта диаграмма, которая применяется только в условиях медленного охлаждения, известна как частичная фазовая диаграмма железо-углерод . Обращаясь к этой диаграмме, можно легко определить надлежащие температуры закалки для любой углеродистой стали. Критические точки на рис. 2.14 на линии PSK обозначены A1, на линии GS — A3, а на линии SE — Acm
Диаграмма равновесия железа и углерода с объяснением Аустенит Аустенит , твердый раствор углерода и других компонентов в особой форме железа, известной как γ (гамма) железо. Возьмем в качестве примера кусок 0,20-процентной углеродистой стали, нагретый до температуры около 850°С. Выше точки Ar3 (линия GS) эта сталь представляет собой твердый раствор (тип внедрения) углерода в гамма-железе и называется аустенитом 9. 0004 . Он имеет гранецентрированную кубическую решетку и немагнитен.
0004 . Он имеет гранецентрированную кубическую решетку и немагнитен.
Обычный аустенит может содержать примерно до 2% углерода при температуре 1130°C. При охлаждении этой стали атомы железа начинают образовывать объемно-центрированную кубическую решетку ниже точки Ar3 (линия GS). Эта новая формирующаяся структура называется ферритом или альфа-железом и представляет собой твердый раствор углерода в альфа-железе, содержащий до 0,008% углерода при комнатной температуре.
При охлаждении стали до Ar1 (линия ПСК) образуется дополнительный феррит. На линии Ари оставшийся аустенит трансформируется в новую структуру, называемую 9.0003 перлит . Название перлита связано с его перламутровым блеском. Он состоит из чередующихся пластин из феррита и цементита и содержит около 87% феррита. Перлит может быть мелкопластинчатой или крупнозернистой структуры. Это прочное вещество, и его можно достаточно хорошо разрезать режущими инструментами, т. Е. Перлитная составляющая стали поддается механической обработке.
Когда содержание углерода в стали превышает 0,20 %, температура, при которой феррит впервые отделяется от аустенита, падает до тех пор, пока при содержании углерода около 0,80 % (точка S) свободный феррит не исчезнет. отторгается от аустенита. Эта сталь называется эвтектоидная сталь и 100-процентный перлит .
Эвтектоидная точка Что такое Эвтектоидная точка?Эвтектоидная точка в любом металле, как было сказано ранее, является самой низкой температурой, при которой происходят изменения в твердом растворе.
Если содержание углерода в стали превышает эвтектоидное (0,8% углерода), на диаграмме состояния железа и углерода наблюдается новая линия, обозначаемая Acm (линия S). Линия обозначает температуру, при которой карбид железа впервые отделяется от аустенита вместо феррита.
Карбид железа (Fe3C) известен как цементит .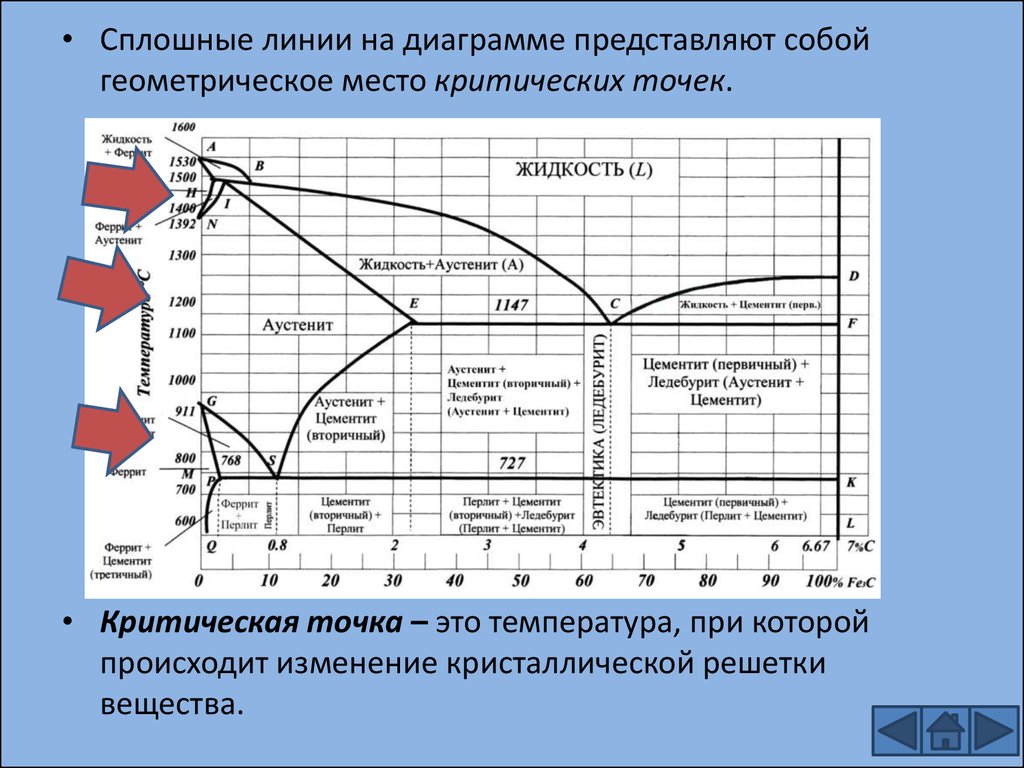 Он чрезвычайно твердый, хрупкий и выглядит как параллельные пластинки (пластинчатые слои), округлые частицы (сфероиды) или оболочки вокруг зерен перлита. В точке С эвтектическая смесь, содержащая 4,3% углерода, известна как ледебурит . Это редко наблюдается в медленно охлаждаемых сплавах, поскольку они распадаются из-за своей нестабильной природы на другие фазы во время охлаждения после затвердевания.
Он чрезвычайно твердый, хрупкий и выглядит как параллельные пластинки (пластинчатые слои), округлые частицы (сфероиды) или оболочки вокруг зерен перлита. В точке С эвтектическая смесь, содержащая 4,3% углерода, известна как ледебурит . Это редко наблюдается в медленно охлаждаемых сплавах, поскольку они распадаются из-за своей нестабильной природы на другие фазы во время охлаждения после затвердевания.
Стали, содержащие менее 0,80% углерода, называются доэвтектоидными сталями , а те, которые содержат более 0,8% углерода, называются заэвтектоидными сталями . Эта терминология применима только к простым и низколегированным сталям. В высоколегированных сталях эвтектоидный состав изменяется, и структура может даже не существовать.
Прежде всего следует отметить, что диаграмма нормального равновесия действительно представляет собой метастабильное равновесие между железом и карбидом железа (цементитом).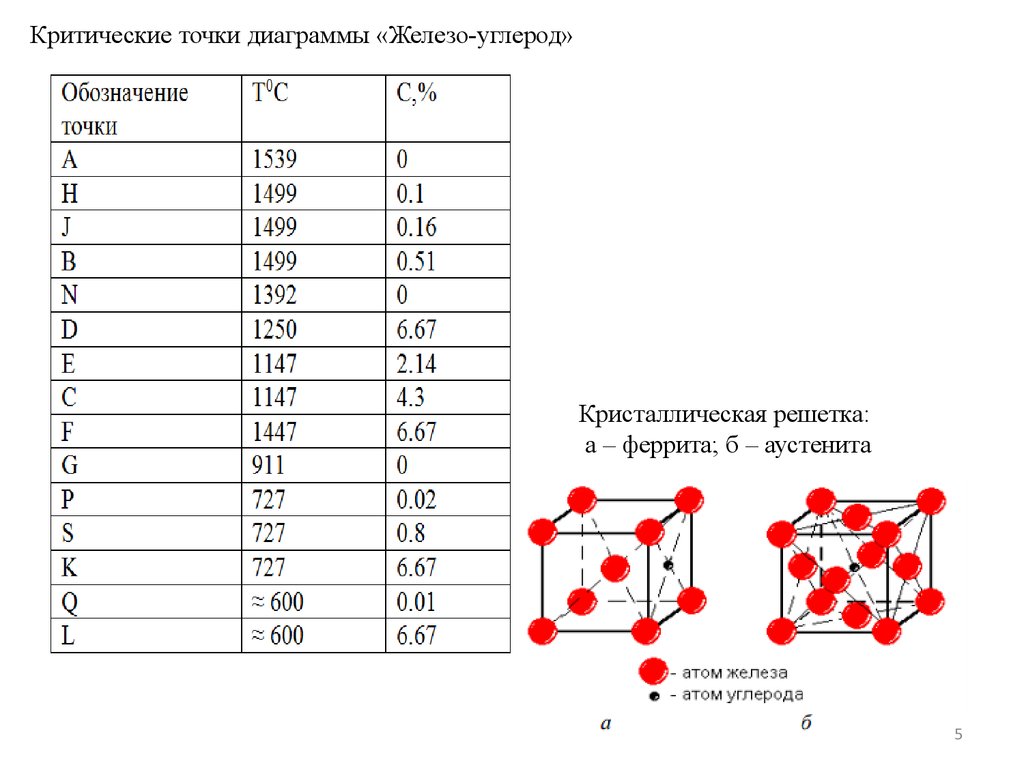 Цементит метастабилен, и истинное равновесие должно быть между железом и графитом.
Цементит метастабилен, и истинное равновесие должно быть между железом и графитом.
Хотя графит широко встречается в чугунах (2-4 мас.% С), обычно трудно получить эту равновесную фазу в сталях (0,03-1,5 мас.% С). Следовательно, следует учитывать метастабильное равновесие между железом и карбидом железа, поскольку оно имеет отношение к поведению большинства сталей на практике.
Железо-графитовая системаЖЕЛЕЗНО-ГРАФИТНАЯ СИСТЕМА
Уже было сказано, что карбид железа или цементит является метастабильным, хотя при нормальных условиях он имеет тенденцию сохраняться неопределенное время. Когда цементит разлагается, это происходит в соответствии с реакцией:
Fe3C <——–> 3Fe + C
В стабильной фазе вместо фазы, известной как цементит , встречается свободный углерод или графит . При небольшой степени переохлаждения графит образуется при затвердевании чугуна из жидкого состояния. Медленное охлаждение способствует графитизации . Быстрое охлаждение частично или полностью подавляет графитизацию и приводит к образованию цементита.
Медленное охлаждение способствует графитизации . Быстрое охлаждение частично или полностью подавляет графитизацию и приводит к образованию цементита.
Система железо-графит (пунктирная линия) показана на рис. 2.14. Случай углеродного сплава, содержащего 3,5 процента углерода по весу, взят в качестве иллюстрации 9.0009
В точке 1 сплав находится в жидком состоянии. В точке 2 на линии охлаждения реакция, которая происходит, может быть выражена как:
Изображение
> Между точками 2 и 3 избыток углерода в аустените осаждается в виде свободного графита, а не в виде цементита. В точке 3 протекает эвтектоидная реакция. Это выражается как:
Image
Механизм эвтектоидного превращения должен превращать одну твердую фазу в две другие, обе с составом, отличающимся от исходного.
На примере эвтектоидного распада железа аустенит, содержащий 0,8 % углерода, превращается в феррит (железо, почти не содержащее углерода) и цементит (Fe3C, содержащий 25 ат. % углерода). Следовательно, атомы углерода должны диффундировать вместе, чтобы образовать Fe3C, оставив феррит. Зародыши небольших пластин феррита и цементита формируются на границах зерен аустенита, а диффузия углерода происходит в очень локальном масштабе непосредственно перед границей раздела (схема ниже).
% углерода). Следовательно, атомы углерода должны диффундировать вместе, чтобы образовать Fe3C, оставив феррит. Зародыши небольших пластин феррита и цементита формируются на границах зерен аустенита, а диффузия углерода происходит в очень локальном масштабе непосредственно перед границей раздела (схема ниже).
Таким образом пластины растут, поглощая аустенит на своем пути, образуя перлит. Процесс графитизации контролируется изменением скорости охлаждения и надлежащим легированием металлической матрицы.
Термины, используемые в диаграмме равновесия железа и углерода Эвтектическая точкаЭвтектоидная точка любого металла представляет собой самую низкую температуру, при которой происходят изменения в твердых растворах.
В этих точках происходят эвтектические реакции, когда жидкая фаза замерзает в смесь двух твердых фаз. Это происходит, когда жидкий сплав эвтектического состава полностью охлаждается до эвтектической температуры.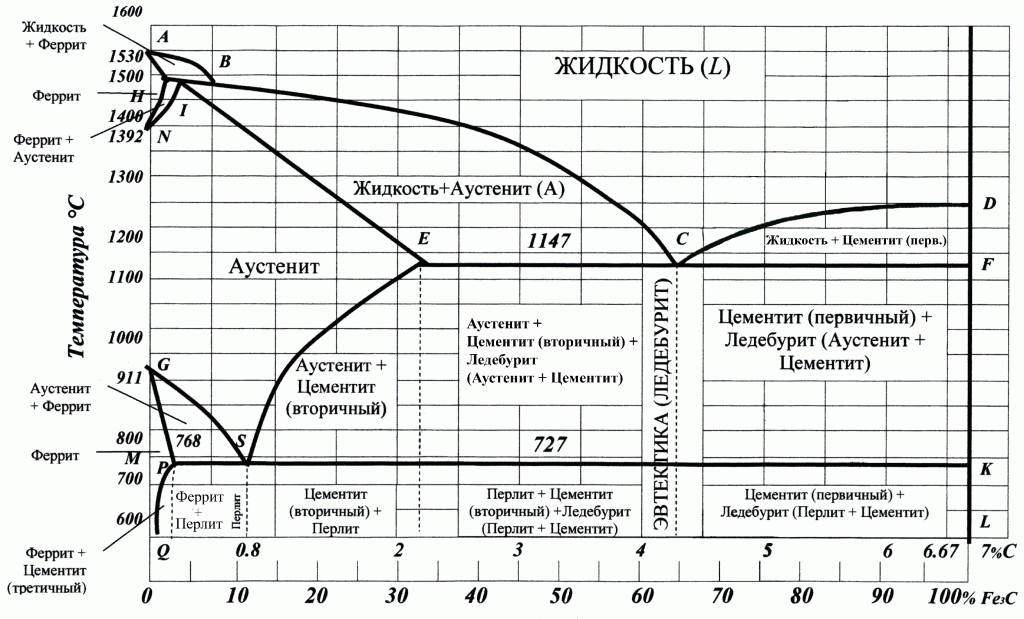
Эвтектические сплавы – это сплавы, образующиеся в этой точке. Сплавы слева и справа от этой точки известны как доэвтектические сплавы и заэвтектические сплавы («гипо» по-гречески означает «меньше», «гипер» — больше).
АустенитАустенит, твердый раствор углерода и других компонентов в особой форме железа, известной как γ (гамма) железо.
Эта фаза представляет собой твердый раствор углерода в ГЦК Fe с максимальной растворимостью 2,14% С. При дальнейшем нагреве она превращается в ОЦК феррит при 1395°С. γ-аустенит нестабилен при температурах ниже температуры эвтектики (727°C), если его не охладить быстро.
Альфа-железо или феррит Существующий при низких температурах и низком содержании углерода, альфа-феррит представляет собой твердый раствор углерода в ОЦК Fe. Эта фаза стабильна при комнатной температуре. На графике это можно увидеть в виде полоски на левом краю с осью Y слева и A2 справа. Эта фаза является магнитной ниже 768°C.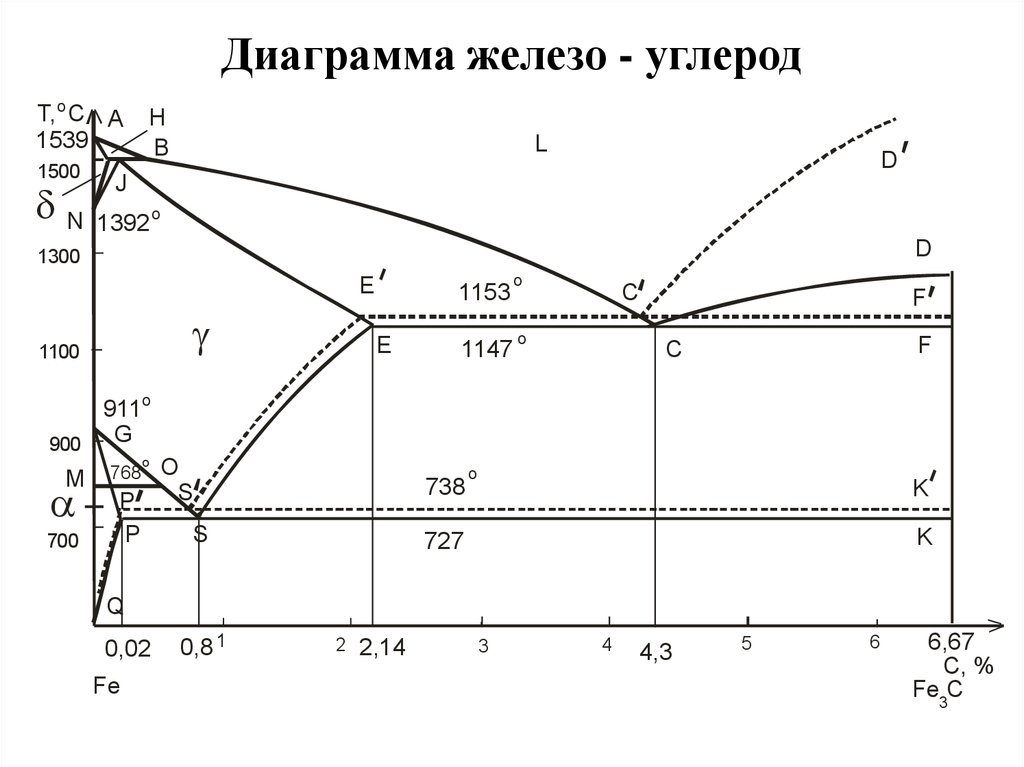
Он имеет максимальное содержание углерода 0,022 % и превращается в γ-аустенит при 912°C, как показано на графике.
ЦементитЦементит, метастабильная фаза этого сплава с фиксированным составом Fe3C, является метастабильной фазой этого сплава. При комнатной температуре очень медленно разлагается на железо и углерод (графит).
Это длительное время разложения, и оно займет намного больше времени, чем срок службы приложения при комнатной температуре. Другие факторы, такие как высокие температуры и добавление определенных легирующих элементов, могут влиять на это разложение, способствуя образованию графита.
Цементит твердый и хрупкий, что делает его идеальным для армирования стали. Его механические свойства определяются его микроструктурой, которая определяется тем, как он смешивается с ферритом.
Мы попытались охватить все термины, связанные с фазовой диаграммой железа и углерода, включая различные фазы и термины, используемые в ней, чтобы лучше понять.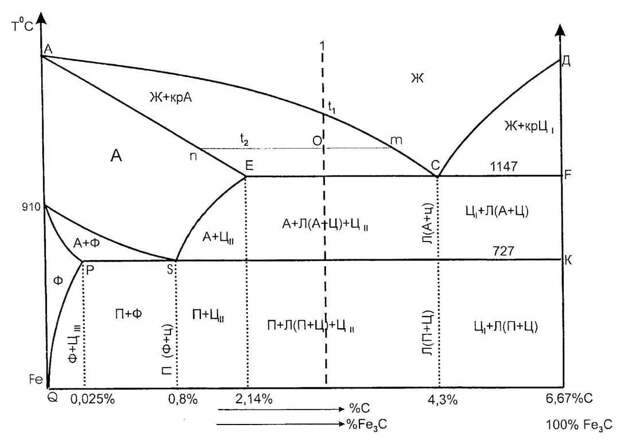


 10 % at 1493° C
10 % at 1493° C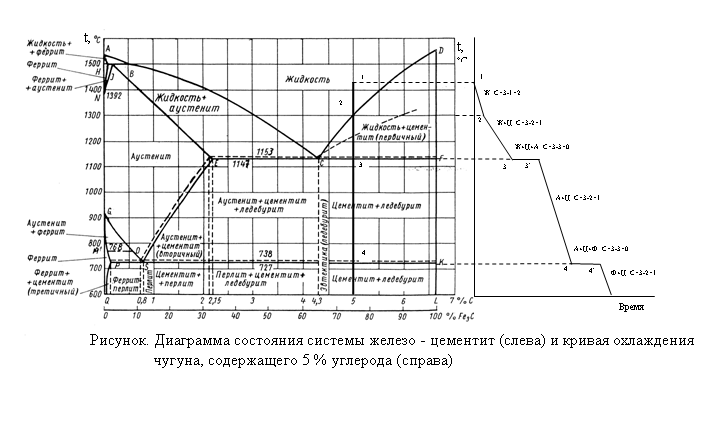 / 12 % цементит
/ 12 % цементит