Масса углекислого газа – Молярная масса углекислого газа (CO2), все формулы
alexxlab | 28.05.2020 | 0 | Разное
Углекислый газ и его физические свойства — объем, плотность, масса, формула
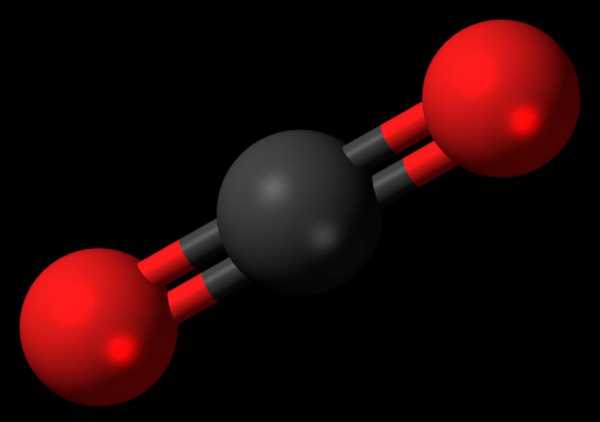
Молекула углекислого газа
Углекислый газ представляет собой бесцветный газ, без запаха,который относится к неорганическим веществам. Другие названия вещества — диоксид углерода, двуокись углерода, углекислота, диоксид карбона, угольный ангидрид. Молекула углекислого газа состоит из атома углерода, соединенного двойной ковалентной связью с двумя атомами кислорода.

Электронная формула диоксида углерода
Химическая формула — CO2. Молярная масса углекислоты равна 44,01 г/моль. Расстояние от центра центрального атома углерода до каждого центра атома кислорода равно 116,3 пикометров (10 в -12 степени).
Структурная формула молекулы
CO2 при низких температурах и нормальном давлении замерзает и кристаллизуется в белую массу, похожую на снег — «Сухой лед». При превышении температуры (-78.5 °C) начинается его испарение (кипение), минуя фазу жидкостного состояния.
В жидкостное состояние газ преобразуется при высоком давлении (73.8 атм.) и средних температурах (+31.1 °C). Это критическая точка углекислоты. Подъем температуры или давления после нее приводит к образованию сверхкритической жидкости (Отсутствует различие между жидкостной и газовой фазой). При снижении температуры до -56.6 °C и давления до 5.2 атм. он остается в жидкостной фазе. Это предельные значения, при изменении которых углекислота переходит в газообразную или твердую фазу (тройная точка состояний).
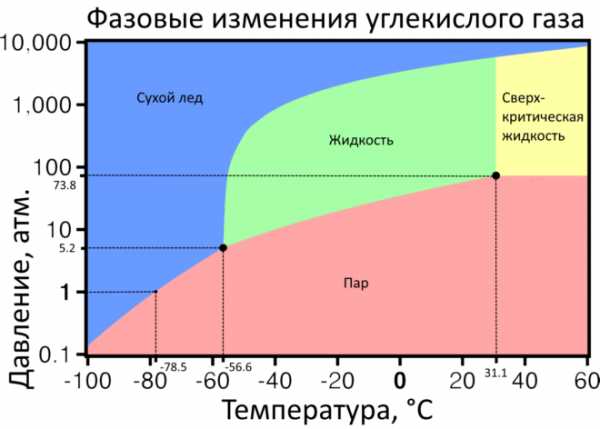
CO2 не ядовит, но при превышении концентрации в десятки раз, он оказывает удушающее воздействие на живые организмы и вызывает кисловатый вкус и запах (реакция CO2 со слюной и слизистыми образует угольную кислоту).
Читайте также: Углекислый газ в помещении.
Двуокись углерода превышает по плотности кислород на 37 процентов и равна 1,96 кг/м3 при нормальных условиях среды (температура — 273 К, давление — 101 кПа). Этим физическим свойством объясняется потеря сознания у животных в «Собачьей пещере», расположенной рядом с городом Поццуоли, Италия. Диоксид углерода скапливался из трещин кратеров в нижних слоях пещеры, тем самым достигая больших концентраций. Туристов приводили туда обычно с собакой, которая в пещере с течением времени теряла сознание. Человек обычно не подвергался воздействию CO2, так как дышал воздухом с более высокого уровня.
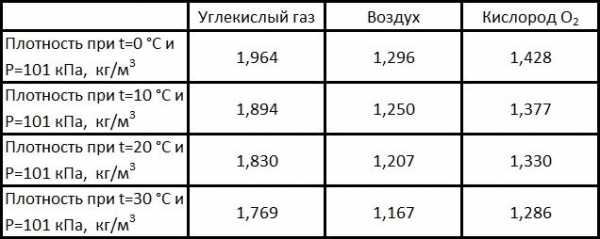
Плотность углекислоты, воздуха и кислорода.
Объем углекислого газа в окружающем нас воздухе, составляет 0,04% (406 ppm – 406 частиц на миллион).
Как вычислить массу газа 🚩 вес углекислого газа 🚩 Естественные науки
Автор КакПросто!
Довольно часто встает вопрос: как можно вычислить массу какого-либо газа, содержащегося в определенном объеме при определенных условиях (давлении, температуре)? Произвести эти вычисления несложно, надо лишь знать несколько правил.

Статьи по теме:
Инструкция
Предположим, перед вами поставлена задача: надо определить массу углекислого газа, занимающего при нормальном давлении и комнатной температуре объем в 0,18 м^3. Прежде всего вспомните универсальное правило, согласно которому 1 моль любого газа при нормальных условиях занимает объем, равный 22,4 литра. (Точнее – 22, 414 литра, но для упрощения расчетов эту величину можно округлить). Потом переведите данный вам объем в литры. 0,18м^3 – это 180 литров. Соответственно, в нем содержится 180/22,4 = 8,036 молей углекислого газа. А теперь остается последний шаг. Формула углекислого газа – СО2. Его молярная масса: 12 + 16*2 = 44 грамма/моль. То есть в одном моле углекислого газа содержится примерно 44 грамма этого вещества. Сколько же его в 8,036 молях? Произведите умножение: 44*8,036 = 353, 58 грамма или округленно 353,6 грамма. Задача решена.Если вам надо найти массу того же углекислого газа, но находящегося при условиях весьма отличающихся от нормальных? Например, какое-то количество этого газа поместили в герметичный сосуд объемом V, нагрели до температуры Т, измерили его давление, оказавшееся равным P. Вопрос: какая масса углекислого газа содержится в сосуде при таких условиях?
И эта задача также очень простая. Для ее решения надо всего лишь вспомнить про уравнение Менделеева-Клапейрона, названное в честь двух выдающихся ученых. Оно было выведено ими для описания состояний так называемого «идеального газа». Его формула такова: PV = MRT/m. Или в слегка видоизмененной форме: PVm = МRT, где З – давление в паскалях, V – объем в кубических метрах, m – молярная масса газа, M – его фактическая масса, T – температура в градусах Кельвина, R – универсальная газовая постоянная, примерно равная 8,31.
Легко можно видеть, что фактическая масса газа М вычисляется по формуле: М = PVm / RT. Подставив в эту формулу все известные данные, и помня, что молярная масса углекислого газа m равна 44 грамма/моль, вы легко получите ответ.
Конечно же, ни углекислый газ, ни какой-либо другой не является идеальным газом. Поэтому, уравнение Менделеева-Клапейрона не вполне точно описывает его состояние. Но, если условия не очень сильно отличаются от нормальных, погрешности вычислений малы, и ими можно пренебречь.
Источники:
- формула углекислого газа
Совет полезен?
Статьи по теме:
Не получили ответ на свой вопрос?
Спросите нашего эксперта:
www.kakprosto.ru
Молекулярный вес, определение углекислого газа
Определение молекулярной массы углекислого газа. Для [c.49]
РАБОТА 2. ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОЙ МАССЫ УГЛЕКИСЛОГО ГАЗА [c.38]
Зная вес углекислого газа в определенном объеме при нормальных условиях, можно найти его плотность по водороду или воздуху и подсчитать его молекулярный вес. [c.63]
ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОГО ВЕСА УГЛЕКИСЛОГО ГАЗА [c.35]
Определение молекулярного веса углекислого газа. [c.69]
Для определения молекулярного веса углекислого газа им наполняют плоскодонную колбу с узким горлом емкостью 250 мл. Колбу предварительно моют, высушивают и подбирают пробку, плотно входящую в нее. Колбу с пробкой взвешивают на технохимических весах (с точностью до 0,01 г). Затем в колбу до дна вставляют газоотводную трубку и заполняют колбу углекислым газом из аппарата Киппа или из баллона. Для очистки и высушивания газа его пропускают последовательно через склянки с водой и серной кислотой. Колбу закрывают пробкой, взвешивают, снова пропускают в нее углекислый газ и еще раз взвешивают. По достижении постоянного веса (расхождение не более чем на 0,01 г) записывают этот вес и определяют объем колбы, заполнив ее водой и измерив затем объем воды мерным цилиндром. Отмечают температуру и давление воздуха и вычисляют мо- [c.70]
Для определения молекулярного веса углекислого газа собрать прибор по рис. 50. [c.63]
Для определения молекулярного веса углекислого газа взять сухую плоскодонную колбу емкостью 500 мл с хорошо пригнанной резиновой пробкой. При помоши резинового кольца или карандаша по стеклу сделать отметку на горлышке колбы в том месте, где кончается пробка. Взвесить с точностью до 0,01 г колбу с пробкой. При заполнении колбы углекислым газом газоотводную трубку аппарата Киппа или баллона с углекислым газом опустить до дна колбы. Когда колба заполнится углекислым газом (как это определить ), медленно вынуть газоотводную трубку, закрыть отверстие колбы пробкой и взвесить. Заполнение колбы углекислым газом производить несколько раз, до тех пор пока не будет получен постоянный вес. Определить объем колбы, наполнив ее водой до метки. Отметить температуру и давление. Вычислить молекулярный вес углекислого газа.
Определение молекулярного веса углекислого газа Получение карбонатов и бикарбонатов и их взаимные [c.228]
Определение молекулярного веса хлора. Сущность метода та же, что и при определении молекулярного веса углекислого газа. Некоторое отличие заключается в том, что хлор собирают не в колбе, а в газовой пипетке. Газовая пипетка (рис. 17) представляет собой стеклянный баллон объемом 150—200 мл, снабженный двумя кранами для впуска и выпуска газа. К пипетке прикрепляется проволока с петлей на конце, которая позволяет подвешивать пипетку к крючку серьги весов при взвешивании. [c.33]
Определение молекулярного веса углекислого газа…………….34 [c.3]
ИЗ крови выделяются газы, которые проходят через осушительную трубку и вносятся в колонку потоком газа-носителя. Такая система позволяет за 5—6 мин разделить и определить кислород, азот и углекислый газ. Для разделения газов используют две последовательно включенные колонки, одна из которых заполнена силикагелем 950 (28/200 мейл), а другая — молекулярным ситом 13-Х (см. раздел Б, II, в, 2). Воспроизводимость метода более 1%, а результаты, полученные при определении углекислого газа и кислорода, совпадают с результатами, полученными по методу Ван-Слайка, с точностью 1% (по Объему). Когда мы писали настоящую книгу, еще не был известен состав гемолизирующего агента, и поэтому методика извлечения газов не включена в экспериментальную часть данной главы.
Определение молекулярного веса углекислого газа. На техно-химических весах взвесить сухую колбу с воздухом, заключенным в ней, и с пробкой (вес вг). Пробка должна быть вдвинута в горло колбы до метки (резиновое кольцо). Опустить в колбу стеклянную трубочку, подводящую углекислый газ из аппарата Киппа через промывные склянки (с раствором соды и с концентрированной серной кислотой). Открыть кран аппарата Киппа и медленно пропускать углекислый газ в течение 7—8 мин. Закрыть колбу пробкой до метки и взвесить (вг). Вновь пропускать углекислый газ 3—4 мин., а затем взвесить (вз). Если два последних веса равны или отличаются друг от друга не более чем на 0,01 г, то наполнение колбы следует считать законченным. В противном случае повторить наполнение и добиться постоянного веса колбы. Отметить температуру по комнатному термометру и давление — по барометру. [c.27]
Знания газовых законов учащихся молопределения молекулярного веса
www.chem21.info
Удельный вес углекислого газа – Справочник химика 21
Подсчитать мощность мотора, работающего на компрессоре, который сжимает 10 м углекислого газа в I час до 70 ата. Температура Oj перед сжатием —15° С, я давление 23,5 ага х для СО2 1,28 удельный объем СО2 0,0167 м /кг- к. п. д. передачи 0,75 и запас мощности мотора 15%- [c.151]При вытеснении нефти оторочкой углекислого газа нефтеотдача может быть на 50—100% больше, чем при обычном заводнении, если удельный расход углекислого газа составлял не менее [c.119]
С, удельным объемом твердой фазы 0,661 дм кг и жидкой фазы 0,849 дм /кг. В критической точке давление равно 7,528 МПа, температура 31,04 °С, удельный объем 2,14 дм кг. При 0°С и 101,325 кПа удельный объем углекислого газа составляет 506 дм кг, а относительная плотность по воздуху 1,529.
Разноречивы мнения о роли твердых частиц в механизме перемешивания газа. Одни [6, 22 считают, что порции газа чисто механически захватываются частицами, движущимися навстречу основному потоку газа, другие [23, 24] указывают на преимущественно адсорбционный характер переноса газа пористыми частицами. Такие выводы сделаны но результатам экспериментов с непористыми материалами. Вероятно, в зависимости от гидродинамического режима (пузырчатый и агрегатный) удельный вес того и другого механизма различен, а в общем рассмотрении оба они имеют место. Так же, как и для твердых частиц, при описании перемешивания газа применяют диффузионную модель, когда степень перемешивания характеризуется через коэффициент осевой эффективной диффузии Величину этого коэффициента определяют опытами с трассирующим газом. При этих опытах на какой-то высоте над газораспределительной решеткой по оси аппарата вводят газ-трассер, например, гелий или углекислый газ. По высоте и радиусу слоя ниже и выше точки ввода трассера отбирают и анализируют пробы газовой смеси. Характер распределения концентраций трассера по разным сечениям иллюстрируют [25] кривые рис. 22. [c.35]
Удельная теплоемкость [в ккал кг-град)]-, топочных газов —0,24, сырого бикарбоната — 0,44, соды — 0,26, углекислого газа — 0,21, мазута — 0,16, пара — 0,47. [c.534]
Обычная дистиллированная вода обладает электропроводимостью порядка 2-10 ом -см , что объясняется присутствием в ней растворенного аммиака, углекислого газа, органических веществ и других примесей. Поэтому удельная электропроводимость входящая в уравнения (4) и [c.53]
Варгафтик для графического обобщения теплопроводности углекислого газа [Л. 4-12] использовал координатную систему (X—Яо)=/(7), где А, — теплопроводность при р и Хо — теплопроводность при той же и давлении, равном 1 кГ/см у — удельный вес. В указанной координатной системе получается единая зависимость в виде кривой, выходящей из начала координат. Экспериментальные точки, полученные при различных температурах и давлениях, ложатся около этой кривой в пределах точности опытов.
На фиг. 29 представлен график зависимости износа образцов от изменения скорости скольжения в пределах от 0,005 до 12 м/сек при постоянной удельной нагрузке 50 кг/см , при испытании в газовых средах — кислороде (кривая 1), аргоне (кривая 2), углекислом газе (кривая износа валов и образцов в среде аргона (кривая 5) и воздуха (кривая 5). [c.51]
Условия работы исследуемых сопряженных деталей — плиты и опорного кольца (малые скорости относительного перемещения деталей, вызванного изменением их температуры, большие удельные давления 1000—1200 кг см , очень высокая пластичность металлов, из которых изготовлены детали, среда — углекислый газ) способствуют возникновению и развитию процесса схватывания металлов. [c.159] Для устранения процесса схватывания первого рода в деталях машин, изготовленных из мягких сталей, работающих в условиях сухого трения при больших удельных нагрузках, малых скоростях относительного перемещения, вwww.chem21.info
Масса углекислого газа
Ф: Какова масса 500 моль углекислого газа?Ф: Какова масса 500 моль углекислого газа? Рымкевич 455.
Углекислый газ для растений, Система Углекислого газа Co2 в аквариум, Баллон с Со2
аквариум #аквариумныеРастения #углекислота #Со2вАквариуме #аквариумистика #рыбки Углекислый газ для расте…
№35 Углекислый газ для растений. Как обеспечить растение углекислым газом.
Углекислый газ для растений это второе удобрение. Растение растет благодаря фотосинтезу. Для него нужны…
Физика Чему равны молярные массы кислорода и углекислого газа (CO2)?
Физика Чему равны молярные массы кислорода и углекислого газа (CO2)? Поддержать проект можно так yandex 410013539261355…
Физика Какова масса 50 моль углекислого газа?
Физика Какова масса 50 моль углекислого газа? Поддержать проект можно так yandex 410013539261355 Основные положения…
Оптимизатор ДМ
Предприниматель (в машиностроительной отрасли) Бацуца Владимир Иванович рассказывает о своем опыте исполь…
Когда Воздух выбивает СО2 из Воды. Углекислый Газ в Аквариуме
Подписаться: https://www.youtube.com/channel/UCSlDT4AIPCuUsYnmNdxhW7g?sub_confirmation=1 – Представители ТМ АКВАБИОС в России …
Полезная хитрость для механизма подачи проволоки сварочного полуавтомата
Как продлить срок службы механизма подачи проволоки сварочного полуавтомата.
Бодитюнинг. День 1.3. От чего растут мышцы? Статика и углекислый газ…
СПАСИБО ЗА ПОДПИСКУ! Приобрести курс тренировок на силу и массу “Переформатирование” https://bbright.club/?page_id=796…
🍅ПОДКОРМКА ТОМАТОВ ВОДКОЙ для огромного и вкусного урожая!
Приобретая растения в магазинах Procvetok вы помогаете развитию канала ***** https://procvetok.ru/ (Россия) ***** https://procvetok.by/…
Свойства углекислого газа
http://paramitacenter.ru / Центр довузовской подготовки ПАРАМИТА.
Физика . Молярная масса , введение в молекулярно-кинетическую теорию
На этом уроке мы рассмотрим введение в молекулярно-кинетическую теорию. Узнаем такие понятия как : Атомная…
пропускание углекислого газа через воду раствор гидроксида кальцияБодитюнинг. День 1.4. От чего растут мышцы? ММВ. Углекислый газ. Гормон роста. Статика.
СПАСИБО ЗА ПОДПИСКУ! Приобрести курс тренировок на силу и массу “Переформатирование” https://bbright.club/?page_id=796…
Как добиться Фотосинтеза в Аквариуме. Углекислый Газ СО2, Удобрения, Свет для Аквариумных Растений
Подписаться: https://www.youtube.com/channel/UCSlDT4AIPCuUsYnmNdxhW7g?sub_confirmation=1 – Представители ТМ АКВАБИОС в России …
avtoclubvideo.ru
Какова масса 50 моль углекислого газа: подробное решение
В данной статье приводится решение типичной задачи из школьного курса химии, которую можно сформулировать следующим образом: “Имеются 50 моль углекислого газа. Какова масса его?”. Рассмотрим подробнее этот вопрос и приведем решение с развернутыми выкладками.
Углекислый газ
Прежде чем переходить к ответу на вопрос о том, какова масса углекислого газа в 50 моль, познакомимся с этим соединением.
Как следует из названия, это вещество представляет собой газ при стандартных внешних условиях (давление воздуха – 101325 Па и температура – 0 oC). Его химическая формула CO2, поэтому его часто называют диоксидом углерода. Он не имеет цвета и запаха.
Углекислый газ в атмосфере Земли присутствует в концентрации около 0,04 объемных процентов. Без него жизнь бы на нашей планете была невозможна, поскольку все зеленые растения используют его в процессе фотосинтеза, результатом которого является кислород.
Человечество применяет углекислый газ во многих областях: при изготовлении охлаждающих напитков, поскольку он хорошо растворяется в воде; в качестве создания нейтральной среды, которая защищает поверхность предметов от окисления кислородом; в качестве жидкого охлаждающего агента.
Используют этот газ в химической промышленности при добыче экстрактов растений, также он является рабочем веществом некоторых лазеров.

Что необходимо знать для решения задачи?
Познакомившись с химическим соединением ближе, вернемся к задаче: “Какова масса углекислого газа в 50 моль?”
Необходимо понимать, что “моль” – это единица измерения количества молекул рассматриваемого соединения. 1 моль любого вещества содержит 6,022*1023 частиц, это значение называется числом Авогадро. Таким образом, зная, сколько весит 1 моль CO2, мы сможем ответить на вопрос о том, какова масса углекислого газа в 50 моль.
Молярную массу любого атома можно найти в Периодической таблице химических элементов. Из нее выпишем нужные цифры:
- M(C) = 12,0107 г/моль;
- M(O) = 15,999 г/моль.
Какова масса углекислого газа в 50 моль: решение
Теперь перейдем непосредственно к решению задачи. Молекула CO2 содержит 1 атом углерода и 2 атома кислорода. Это означает, что в 1 моле молекул CO2 будет находиться 1 моль атомов C и в два раза больше атомов O. Подставляя выписанные из таблицы Д. И. Менделеева цифры, получаем: M(CO2) = M(C) + 2 * M(O) = 12,0107 + 2 * 15,999 = 44,0087 г/моль.
Таким образом, 1 моль молекул диоксида углерода имеет массу 44,0087 грамма. Какова масса углекислого газа в 50 моль? Конечно же, в 50 раз больше полученного значения. Она равна: m = 50 * M(CO2) = 50 * 44,0087 = 2200,435 грамм, или 2,2 килограмма.
При отмеченных стандартных условиях плотность этого газа составляет ρ = 1,977 кг/м3. Это означает, что 50 моль CO2 займут объем: V = m/ρ = 2,2/1,977 = 1,11 м3.
autogear.ru

