Медь железо сходства и различия: Сходство и различия меди и железа
alexxlab | 18.06.2023 | 0 | Разное
Что будет, если сплавить все металлы вместе?
Люди издавна любили проводить самые разные опыты с материалами, чтобы понять свойства материй. Химиков, например, волнует вопрос – что будет, если сплавить все металлы вместе? При этом некоторые из них все-таки проводили несколько испытаний с плавлением нескольких видов металлов. Всего металлов в таблице Менделеева насчитывается около 100 позиций.
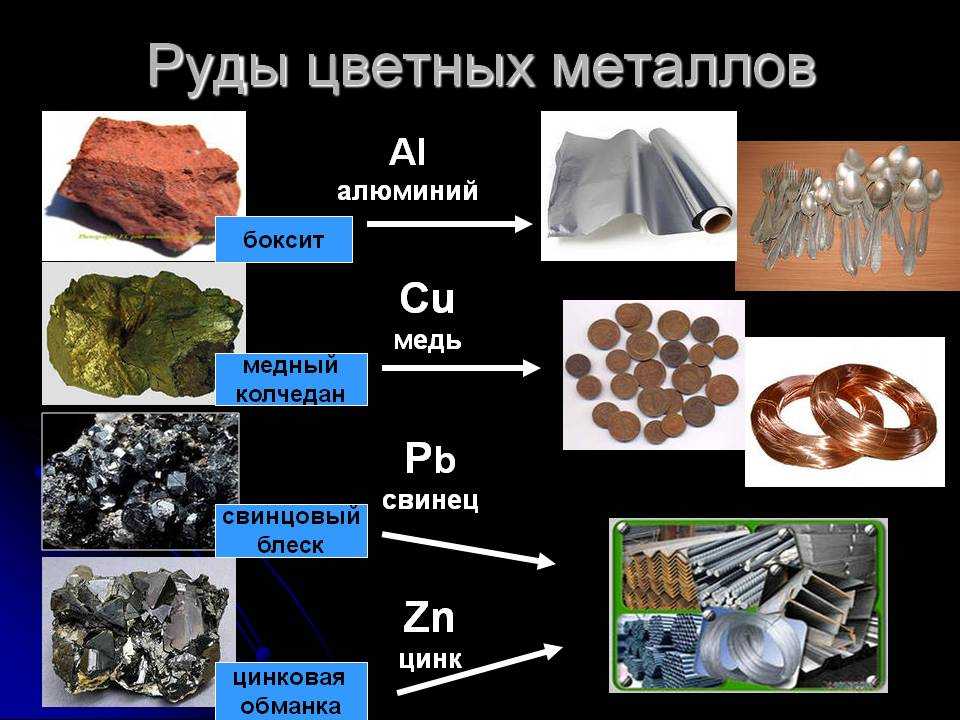
Сходства и отличия металлов
Можно ли получить путем общего плавления суперсплав на подобие вымышленного Вибраниума, который будет выдерживать высокие нагрузки или, наоборот, получится материал, быстро разрушающийся? Этот вопрос до сих пор волнует химиков.
Металлы, которые содержатся в таблице Менделеева, обладают некоторыми схожими свойствами, которые характерны для этого класса веществ. Они обладают следующими характеристиками:
- высокая твердость;
- высокая теплопроводность;
- высокая электропроводность;
- металлический блеск.

Также существуют и отличия между ними – уровень прочности, плавкости, окисляемости и ценности. Например, железо обладает высочайшей твердостью и прочностью, но очень быстро окисляется на воздухе. А медь, наоборот, имеет высокую теплопроводность, но является довольно мягким металлом. Поэтому еще с древних времен люди начали соединять несколько металлов воедино, чтобы получить более универсальные свойства нового суперсплава. К настоящему времени химики смогли придумать более 5 тысяч сплавов путем плавления нескольких исходных металлов. А есть ли возможность получить один сплав из всех металлов?
Особенности сплавления металлов
Плавка металла – это завораживающее зрелище, которое приводит в восторг не только химиков, но и обычных людей. Сплав – это смесь двух или более химических элементов с преобладанием металлических компонентов.
Интересные факты:
- Первым плавным металлом в истории стала медь, которая часто встречается в природе.
 Поэтому получить медь было проще всего;
Поэтому получить медь было проще всего; - Первым сплавом в истории стала бронза, которая содержала в себе медь и металлический мышьяк. Мышьяк придавал материалу повышенную прочность и твердость. Но из-за чрезмерной токсичности, его со временем заменили оловом;
- Один блогер-химик решил получить медь в домашних условиях. Он взял кусочек чистой меди и 9-процентное олово. Он взял 215 г чистой меди и 15 г олова. Опыт проводился в специальной плавильне, где температура достигает 1150ºС. Также была добавлена часть буры в качестве флюса. Это было сделано для того, чтобы сплав получился более чистым. После перемешивания массы в тигле ее помещают в камеру плавления, а затем в графитовую форму, чтобы получить слиток правильной структуры. Кстати, к графиту не прилипает ни один металл, поэтому именно графитовая форма является идеальной для проведения опытов;
- На основе меди можно сделать еще один сплав, который называется латунь. Это сплав меди и цинка. При этом, если медь обладает пластичностью и мягкостью, то латунь – высокой хрупкостью, поэтому с легкостью раскалывается при малейшем ударе.
 При сплавлении меди и цинка, последний начинает быстро выгорать, но добавление буры позволяет снизить этот процесс;
При сплавлении меди и цинка, последний начинает быстро выгорать, но добавление буры позволяет снизить этот процесс; - Чтобы придать слитку завершенный вид, его полируют и удаляют окись. В таком виде можно заметить, что слитки отличаются по цвету. По техническим характеристикам наиболее прочным является сплав бронзы, из-за чего он плохо поддается механической обработке. А вот латунь, наоборот, легко поддается любой механической обработке, поэтому ее часто используют при производстве мелких деталей. Именно поэтому тонкие механизмы начали изготавливать из латуни. Но все же, бронза не идет ни в какое сравнение с железом и его сплавами. Именно поэтому за бронзовым веком идет железный. На протяжении многих лет на основе железа придумано более 1000 сплавов, используемых в разных отраслях производств для самых разных нужд человечества.
Сплавы на основе железа
Наиболее прочным сплавом из железа считается сплав Гадфильда, из которого производятся гусеницы для танков или тракторов. Кроме железа в составе содержится до 14% металлического марганца, который придает полученному материалу невероятную прочность и износостойкость. Блогеру-химику удалось сделать этот сплав в своей домашней плавильне. Получился прочный, но окисленный кусок материала, который не реагирует на магнит. Кстати, магнит делается из сплава Альнико (AlNiCo).
Кроме железа в составе содержится до 14% металлического марганца, который придает полученному материалу невероятную прочность и износостойкость. Блогеру-химику удалось сделать этот сплав в своей домашней плавильне. Получился прочный, но окисленный кусок материала, который не реагирует на магнит. Кстати, магнит делается из сплава Альнико (AlNiCo).
Состав магнита:
- 53% железа;
- 10% алюминия;
- 19% никеля;
- 18% кобальта.
Одного процесса плавления металлов для получения полноценного магнита недостаточно. Для того, чтобы магнит притягивал металл, его необходимо подвергать нагреванию и пропускать через него ток. То есть, это очень сложный технологический процесс.
Что будет, если сплавить воедино все известные металлы?
Помимо традиционных сплавов, используемых в производствах, химики не раз пытались соединить в один материал большое количество металлов. Для получения такого материала они брали 22 металла и сплавляли воедино. В качестве основы выступало железо, в котором способны растворяться все остальные металлы. Основными легирующими компонентами выступили хром, никель, кобальт и марганец. В состав сплава также вошли серебро, золото и платина. Щелочные металлы отсутствовали в составе.
В качестве основы выступало железо, в котором способны растворяться все остальные металлы. Основными легирующими компонентами выступили хром, никель, кобальт и марганец. В состав сплава также вошли серебро, золото и платина. Щелочные металлы отсутствовали в составе.
Что же получилось из этого опыта? На самом деле получился достаточно текучий сплав, который горит при выливании в форму. После остывания образовался легкий кусочек металла, обладающий достаточно прочными свойствами и поддающийся механической обработке. При этом сплав очень выраженно реагировал на магнит.
Практика многокомпонентных сплавов может послужить прекрасной альтернативой для получения совершенно новых материалов, которые обладают неизвестными до сегодняшнего дня свойствами. Возможно, они будут использоваться при производстве автомобилей или космических кораблей.
Цена на медь, появление, добыча и использование
Медь (латинский Cuprum) представляет собой химический элемент с символом элемента Cu и атомным номером 29. Это переходный металл, в периодической таблице он находится в 4. Период и 1. Подгруппа (после новой группы отсчетов 11) или группа меди. Латинское название cuprum происходит от (aes) cyprium “руда с греческого острова Кипр”, в которой медь добывалась в древние времена.
Это переходный металл, в периодической таблице он находится в 4. Период и 1. Подгруппа (после новой группы отсчетов 11) или группа меди. Латинское название cuprum происходит от (aes) cyprium “руда с греческого острова Кипр”, в которой медь добывалась в древние времена.
Как относительно мягкий металл, медь легка в форме и прочна. Являясь отличным проводником тепла и электричества, он находит универсальное применение. Кроме того, он также относится к группе монет металлов.
Как слабореактивный тяжелый металл, медь является одним из полудрагоценных металлов.
история
Медь, золото, серебро и олово были первыми металлами, которые человечество узнало в своем развитии. Поскольку медь легко обрабатывается, она уже использовалась древнейшими известными культурами около 10.000 лет назад. Время его длительного использования 5. Тысячелетие до нашей эры К 3. Тысячелетие до нашей эры В зависимости от региона Британская Колумбия также называется медным веком. У Худжайрата аль-Гузлана в Иордании уже был 4. 000 v. Chr. Массовое производство меди. В алхимии медь ассоциировалась с Венерой / Женственностью ♀ (планетарные металлы) и считалась соединением серы и ртути. Первые зеркала были сделаны из этого металла. Во время позднего восточного средиземноморского бронзового века медь в основном добывалась на Кипре и экспортировалась оттуда в основном в толстых медных слитках весом около 30 в виде бычьих шкур (так называемых слитков быка). Фрагменты кипрских бычьих шкур слитков времен 16. и 11. До н.э. Хр. Встречаются в значительной части Средиземного моря, вплоть до Сардинии, на Балканах и даже к северу от Альп (Фонд депо Обервильфлинген). Крупнейшим доиндустриальным производителем меди была Римская империя с предполагаемым годовым объемом производства 15.000 т.
000 v. Chr. Массовое производство меди. В алхимии медь ассоциировалась с Венерой / Женственностью ♀ (планетарные металлы) и считалась соединением серы и ртути. Первые зеркала были сделаны из этого металла. Во время позднего восточного средиземноморского бронзового века медь в основном добывалась на Кипре и экспортировалась оттуда в основном в толстых медных слитках весом около 30 в виде бычьих шкур (так называемых слитков быка). Фрагменты кипрских бычьих шкур слитков времен 16. и 11. До н.э. Хр. Встречаются в значительной части Средиземного моря, вплоть до Сардинии, на Балканах и даже к северу от Альп (Фонд депо Обервильфлинген). Крупнейшим доиндустриальным производителем меди была Римская империя с предполагаемым годовым объемом производства 15.000 т.
Позднее медь была легирована оловом и свинцовыми компонентами до бронзы. Этот более твердый и технически стойкий сплав стал названием бронзового века. Различие между свинцом и оловом было введено только с ростом знаний о металле, поэтому термин «бронза» с сегодняшней точки зрения применяется только к сплавам с высоким содержанием меди и олова и меди.
Золотисто-желтый медно-цинковый сплав «латунь» был известен еще в Древней Греции. Он был расплавлен путем совместной переработки соответствующих руд, но только римляне интенсивно использовали эту процедуру. В древней Колумбии часто использовался золото-медный сплав Тумбага.
Вхождение
Медь находится в земной коре с содержанием около 0,006% и, следовательно, зависит от частоты элементов в земной коре на 23. Место. Часто медь выглядит твердой, то есть в элементарной форме. В настоящее время (2017) 3000 известен во всем мире благодаря твердой меди, в том числе в Афганистане, Аргентине, Австралии, Бельгии, Боливии, Бразилии, Болгарии, Чили, Китае, Демократической Республике Конго, Германии, Финляндии, Франции, Греции, Индия, Иран, Ирландия, Италия, Япония, Канада, Казахстан, Марокко, Мексика, Монголия, Намибия, Новая Зеландия, Норвегия, Австрия, Перу, Филиппины, Польша, Португалия, Румыния, Россия, Замбия, Швеция, Швейцария , Зимбабве, Словакии, Испании, ЮАР, Чехии, Турции, Украины, Венгрии, Соединенных Штатов Америки (США) и Великобритании (Великобритания).
В нескольких образцах горных пород из Срединно-Атлантического хребта и Луны, которые принесли зонд миссии Luna 24 Mare Crisium, можно было обнаружить достойную медь.
Основные производители медной руды Источник: Википедия
Медь как минерал
Медный самородок
Природные месторождения твердой меди, то есть в ее элементарной форме, были известны задолго до основания Международной минералогической ассоциации (IMA). Поэтому медь признана так называемым «добытым» минералом как самостоятельный минеральный вид.
Согласно классификации минералов по Струнзу (издание 9) меди по системе №. «1.AA.05» (Элементы – металлы и интерметаллические соединения – семейство медных купалитов – медная группа) соответственно в устаревшем 8. Издание перечислено под I / A.01 (медная серия). Классификация минералов по Дане, которая преимущественно используется в англоязычных странах, приводит элемент минерал по системе №. 01.01.01.03 (Золотая группа).
Медь дендриты
В природе медь обычно образуется в базальтовых лавах либо в форме «медно-красных», блестящих металлических самородков (затвердевших из расплава), либо в разветвленных структурах, так называемых дендритах. Иногда можно найти кристаллическое обучение. Медь встречается в парагенезисе с различными, в основном вторичными, минералами меди, такими как борнит, халькоцит, корнуоллит, куприт, азурит и малахит, а также тенорит, но также может быть связана со многими другими минералами, такими как кальцит, клиноклас, пренит, пумпеллит, кварц и серебро.
Иногда можно найти кристаллическое обучение. Медь встречается в парагенезисе с различными, в основном вторичными, минералами меди, такими как борнит, халькоцит, корнуоллит, куприт, азурит и малахит, а также тенорит, но также может быть связана со многими другими минералами, такими как кальцит, клиноклас, пренит, пумпеллит, кварц и серебро.
Dicey медные кристаллы
Медные руды распространены. Например, медь изготавливается из халькопирита (халькопирит, CuFeS2), халькоцита (халькоцит, Cu2S), реже также из борнита (халькопирит меди, Cu5FeS4), атакамита (CuCl2 · CuX (CO) (CO) (CO) (CO) (CO) (CO) (CO) XUMX (CO) (CO) (CO) XUMX (CO) (CO) (CO) XUMX (CO)) ) и другие руды. В 2 2 были известны минералы меди. Минералы с самой высокой концентрацией меди в соединении – это куприт (до 2%) и альгодонит (до 3%), а также паралаконит, тенорит и халькоцит (до 2019%).
продвижение по службе
Наиболее важным производителем меди является Чили, за которым следуют Перу и США. В Европе заслуживают внимания Польша, Португалия и Швеция. Основные экспортеры были организованы из 1967 в 1988 в CIPEC. В CIPEC входили Чили, Перу и Папуа-Новая Гвинея, на острове Бугенвиль которых одна из крупнейших в мире медных шахт 1988 привела к гражданской войне.
В Европе заслуживают внимания Польша, Португалия и Швеция. Основные экспортеры были организованы из 1967 в 1988 в CIPEC. В CIPEC входили Чили, Перу и Папуа-Новая Гвинея, на острове Бугенвиль которых одна из крупнейших в мире медных шахт 1988 привела к гражданской войне.
Исторически значимыми были медные рудники на полуострове Кьюнау в Верхнем озере (США). Здесь было крупнейшее в мире месторождение твердой меди. Деградация произошла там уже в доколумбовые времена. В Германии медный сланец добывался на Земле Мансфельдер до 1990, а в Корнуолле – в основном на 18. и 19. Век дал значительную добычу меди.
восстановление
Извлечение меди после левитационного плавления
Различные процедуры
| 1. | Чили | 5.330 | 170.000 | 360.000 |
| 2. | Перу | 2. 390 390 | 81.000 | 120.000 |
| 3. | Китайская Народная Республика | 1.860 | 27.000 | 63.000 |
| 4. | Соединённые Шта́ты | 1.270 | 45.000 | 70.000 |
| 5. | Австралия | 920 | 88.000 | 88.000 |
| 6. | ДР Конго | 850 | 20.000 | k. А. |
| 7. | Мексика | 755 | 46.000 | 50.000 |
| 7. | Замбия | 755 | 20.000 | 35.000 |
| 9. | Индонезия | 650 | 26.000 | 38.000 |
| 10 | Канада | 620 | 11.000 | 20.000 |
| Другие страны | 4.300 | 260.000 | 110.000 | |
| Мир | 19. 700 700 | 790.000 | 1.000.000 |
|---|
Наиболее важными печами для производства меди являются пламенная печь и, начиная с 1980, печь мгновенной плавки.
Процесс извлечения меди
Для производства меди вначале из халькопирита (CuFeS2) получают так называемый медный камень (Cu2S с различным содержанием FeS, содержание Cu около 70%). Для этого исходный материал обжаривают с добавлением кокса и содержащихся в нем оксидов железа, зашлакованных кремнистыми заполнителями. Этот шлак из силиката железа плавает на матовой поверхности и может быть легко слит.
Röstarbeit:
Таяние работы:
Полученный таким образом медный штейн затем перерабатывают в сырую медь (также черную медь). Для этого его заливают в конвертер с жидким свечением, а в этот расплав вдувают воздух. На первой стадии (продувка шлаком), в то время как содержащийся в нем сульфид железа обжаривается до оксида железа, и это связывается хлопьевидным кварцем со шлаком, который можно сливать. На втором этапе (Garblasen) две трети оставшихся Cu2S окисляются до Cu2O. Затем оксид реагирует с оставшимся сульфидом с образованием неочищенной меди.
На втором этапе (Garblasen) две трети оставшихся Cu2S окисляются до Cu2O. Затем оксид реагирует с оставшимся сульфидом с образованием неочищенной меди.
Пузырьки Шлак:
Garblasen:
Сырая медь имеет содержание меди 98%. Оставшийся 2% содержит драгоценные металлы, такие как серебро и золото, а также основные металлы, такие как железо и цинк. Электролитическое рафинирование меди проводят в сульфатсодержащем растворе сульфата меди (II) с неочищенным медным анодом и чистым медным катодом. Во время электролиза все металлы, которые менее благородны, чем медь, окисляются и растворяются в виде катионов, в то время как благородные металлы тонут в виде анодного шлама.
Уравнение реакции электролитического рафинирования:
Анод
катод
В то время как анод медленно растворяется с образованием катионов, только медь, электролитическая медь, осаждается на катоде при восстановлении ионов меди с массовой долей w (Cu) = 99,99%.
Анодный шлам, полученный в качестве побочного продукта, позднее рециркулируется и используется в качестве исходного материала для извлечения драгоценных металлов.
Добыча меди происходит в Affinerien. В Европе Aurubis AG (ранее Norddeutsche Affinerie) со штаб-квартирой в Гамбурге, ранее это также был медеплавильный завод в Дуйсбурге (сейчас DK Recycling).
Медь также может быть получена в виде так называемой цементной меди путем осаждения из раствора сульфата меди с железом. Процесс осаждения называется цементацией. Получающаяся медь часто загрязнена. Осаждение меди на железо из природных растворов солей металлов практикуется в Китае с 1086 нашей эры.
Медь также может быть представлена алюмотермической реакцией. Термит служит смесью оксида меди (II) и манной крупы алюминия. Использование агента потока (например, фторида кальция) может увеличить выход, потому что элементарные металлы не могут растворить полученный шлак в агенте потока. Алюминотермическая экстракция неэкономична из-за необходимого алюминия.
Добыча меди после Schweehmmelzverfahren, источник Википедия
Eigenschaften
Физические свойства
При плотности 8920 кг / м³ медь является одним из тяжелых металлов, который кристаллизуется гранецентрированным кубом и, следовательно, имеет кубическую ближайшую упаковку с пространственной группой Fm3m (номер пространственной группы 225). Параметр решетки для чистой меди равен 0,3615 нм (соответствует 3,615 Å) для формульных единиц 4 на элементарную ячейку.
Параметр решетки для чистой меди равен 0,3615 нм (соответствует 3,615 Å) для формульных единиц 4 на элементарную ячейку.
Медь является очень хорошим проводником тепла. Его температура плавления составляет 1083,4 ° C. Точно так же медь – очень хороший электрический проводник с электропроводностью 58 · 106 S / m. Его проводимость лишь немного хуже, чем у серебра, и намного лучше, чем у золота. Поскольку все примеси, растворенные в меди, особенно примеси, такие как фосфор и железо, значительно снижают электропроводность, для проводниковых материалов часто ищут самые высокие уровни чистоты.
Твердость по шкале Мооса для меди составляет от 2,5 до 3, что соответствует твердости по Виккерсу (VHN) 77-99 при испытательном усилии 100 g. Холодная штамповка увеличивает прочность 150 … 200 MPa (состояние отливки) до значений около 450 MPa. Удлинение при разрыве составляет 4,5% со значениями твердости около 100 HB. Деформированная и впоследствии отожженная медь с прочностью 200 … 240 МПа имеет относительное удлинение при разрыве более 38% и значения твердости вокруг 50 HB.
Ковка очень возможна при температурах от 700 до 800 ° C. Холодные деформации можно проводить без промежуточного отжига.
Поскольку голая металлическая медь имеет ярко-красный цвет, цвет линии – розовый. Красный цвет связан с тем, что он поглощает дополнительный зеленый и синий свет немного больше при нормальной температуре. Это начинается в воздухе и становится красновато-коричневым. При дальнейшем выветривании и коррозии гладкая поверхность теряется очень медленно (часто в течение столетий), а цвет меняется от красновато-коричневого до сине-зеленого из-за образования патины.
Химические свойства
Медь встречается в состояниях окисления 0, + 1, + 2, + 3 и + 4, чаще всего + 1 и + 2, где + 2 – наиболее стабильное состояние окисления в водных растворах; Уровень + 4 встречается крайне редко (например, в Cs2CuF6). Соли меди (II) (например, сульфат меди) в основном имеют синий или зеленый цвет. Медь имеет некоторые химические свойства, сходные с серебром и золотом в той же группе. Слой металлической меди наносится на железный гвоздь, погруженный в раствор сульфата меди, для которого железо растворяется в виде сульфата железа, поскольку железо менее благородно, чем медь (см. Также серию напряжений). Медь обычно не подвергается воздействию соляной кислоты, но она сильно подвергается воздействию кислорода и растворяется горячей серной кислотой. Он также растворяется в азотной кислоте и царской водке. Смесь соляной или серной кислоты с перекисью водорода растворяет медь очень быстро. Металл также подвергается воздействию органических кислот. Против щелочей ведет себя стабильно. При красном нагревании он реагирует с кислородом, образуя толстый слой оксида меди. Медь пассивируется фтором и его соединениями. В зависимости от размера зерна, медный порошок является легковоспламеняющимся или горючим. Металл в компактной форме не воспламеняется и не подвергается дальнейшему воздействию образования тонкого оксидного слоя воздуха и воды, поэтому он устойчив к чистому воздуху и воде.
Слой металлической меди наносится на железный гвоздь, погруженный в раствор сульфата меди, для которого железо растворяется в виде сульфата железа, поскольку железо менее благородно, чем медь (см. Также серию напряжений). Медь обычно не подвергается воздействию соляной кислоты, но она сильно подвергается воздействию кислорода и растворяется горячей серной кислотой. Он также растворяется в азотной кислоте и царской водке. Смесь соляной или серной кислоты с перекисью водорода растворяет медь очень быстро. Металл также подвергается воздействию органических кислот. Против щелочей ведет себя стабильно. При красном нагревании он реагирует с кислородом, образуя толстый слой оксида меди. Медь пассивируется фтором и его соединениями. В зависимости от размера зерна, медный порошок является легковоспламеняющимся или горючим. Металл в компактной форме не воспламеняется и не подвергается дальнейшему воздействию образования тонкого оксидного слоя воздуха и воды, поэтому он устойчив к чистому воздуху и воде.
В жидкой меди растворяются кислород и водород, которые могут превращаться в пар при затвердевании расплава и, таким образом, формировать газовую пористость в отливке.
В кислородсодержащих видах меди могут образовываться трещины и пустоты при контакте с водородсодержащими газами, что приводит к так называемому водородному охрупчиванию меди.
Биологические свойства
По сравнению со многими другими тяжелыми металлами медь относительно слаба для высших организмов. Таким образом, человек может ежедневно принимать 0,04 грамм меди, не причиняя вреда своему здоровью. В свободной форме, не связанной с белком, медь обладает антибактериальными свойствами; здесь говорят, как и с серебром, об олигодинамическом эффекте, почему z. Б. Цветочная вода, которая хранится в медных сосудах или в которой помещена медная монета, не так быстро становится нечистой.
Бактерицидные свойства
Медь токсична для многих микроорганизмов даже при низких концентрациях. Поэтому (но также и потому, что легко установить) водопроводные трубы часто содержат медь. Из-за бактерицидных свойств меди, она тестируется в крупномасштабных испытаниях, чтобы определить, имеет ли экономический смысл оснащать палаты для больниц медными дверными ручками. Например, клиническое исследование 2008 / 2009 показывает, что в клинике Асклепиос в Вандсбеке, Гамбург, после замены дверных ручек / накладок 50 и выключателей освещения количество микробов MRSA было снижено до 63%. Чилийское исследование показало, что влажность воздуха от 7,2 до 19,7% снижает количество меди на целых 92%. Многоцентровое исследование 2010 / 2011 из США показывает, что уровень заражения в «медных комнатах» падает почти на 60%, а на самих медных объектах – более чем на 80%. 2013 преобразовал отделение педиатрии в Нидерберге, Северный Рейн-Вестфалия, в медные сплавы.
Поэтому (но также и потому, что легко установить) водопроводные трубы часто содержат медь. Из-за бактерицидных свойств меди, она тестируется в крупномасштабных испытаниях, чтобы определить, имеет ли экономический смысл оснащать палаты для больниц медными дверными ручками. Например, клиническое исследование 2008 / 2009 показывает, что в клинике Асклепиос в Вандсбеке, Гамбург, после замены дверных ручек / накладок 50 и выключателей освещения количество микробов MRSA было снижено до 63%. Чилийское исследование показало, что влажность воздуха от 7,2 до 19,7% снижает количество меди на целых 92%. Многоцентровое исследование 2010 / 2011 из США показывает, что уровень заражения в «медных комнатах» падает почти на 60%, а на самих медных объектах – более чем на 80%. 2013 преобразовал отделение педиатрии в Нидерберге, Северный Рейн-Вестфалия, в медные сплавы.
Токсический эффект заключается в том, что ионы меди связываются с тиоловыми группами белков и перекисляют липиды клеточной мембраны, что приводит к образованию свободных радикалов, которые повреждают ДНК и клеточные мембраны. Например, у людей в случае болезни Вильсона (болезнь накопления меди) это приводит к повреждению органов с высоким избытком меди.
Например, у людей в случае болезни Вильсона (болезнь накопления меди) это приводит к повреждению органов с высоким избытком меди.
Медные сплавы с содержанием меди не менее 60% также проявляют токсическое действие в отношении норовирусов.
Действие против улиток
Слизь улитки окисляет медь в медной проволоке или медной фольге, которая служит барьером для исчезающих растений. Это создает раздражающее вещество, которое препятствует дальнейшему ползанию улитки.
Потребности в органической меди
В большинстве многоклеточных организмов медь является компонентом многих ферментов (металлоферментов) и, следовательно, жизненно важным микроэлементом. Медь входит в состав голубого гемоцианина, который служит кровяным красителем у моллюсков и членистоногих для транспорта кислорода.
Суточная потребность взрослого человека составляет миллиграммы 1,0-1,5. В организме человека медь в основном хранится в печени.
Медь в основном содержится в шоколаде, печени, злаках, овощах и орехах. Дефицит меди редко встречается у людей, главным образом при длительной диарее, у недоношенных детей, после продолжительного недоедания или мальабсорбции такими заболеваниями. Спру, болезнь Крона или муковисцидоз. Потребление высоких доз цинка, железа или молибдата также может привести к снижению количества меди в организме. Синдром Менкеса является редким врожденным нарушением обмена меди.
Дефицит меди редко встречается у людей, главным образом при длительной диарее, у недоношенных детей, после продолжительного недоедания или мальабсорбции такими заболеваниями. Спру, болезнь Крона или муковисцидоз. Потребление высоких доз цинка, железа или молибдата также может привести к снижению количества меди в организме. Синдром Менкеса является редким врожденным нарушением обмена меди.
Избыток меди поступает в пищеварительную систему с желчью для выведения.
Сульфат меди (медный купорос) является сильным рвотным средством и поэтому используется для лечения многих интоксикаций, таких как белый фосфор, который в данном конкретном случае также обладает преимуществом одновременного связывания фосфора в виде труднорастворимого фосфида меди.
При редком наследственном заболевании экскреция меди по Вильсону нарушается, и происходит увеличение накопления меди, сначала в печени, а затем, когда это выделяет медь в кровоток, в другие органы. Другим не менее редким заболеванием обмена меди является синдром Менкеса. Несмотря на то, что медь может поглощаться клетками, они не могут в дальнейшем транспортироваться упорядоченным образом, так что некоторые органы имеют повышенное содержание меди, а другие – более низкое содержание меди.
Несмотря на то, что медь может поглощаться клетками, они не могут в дальнейшем транспортироваться упорядоченным образом, так что некоторые органы имеют повышенное содержание меди, а другие – более низкое содержание меди.
Медь и болезнь Альцгеймера
Снова и снова обсуждалась связь между медью и развитием болезни Альцгеймера. Уже исследователи 2003 предположили, что медь замедляет выработку амилоида А и что недостаток меди способствует развитию болезни Альцгеймера. Однако последующее пилотное исследование с участием пациентов с болезнью Альцгеймера 70 не показало какого-либо защитного эффекта от повышенного потребления меди, даже несмотря на то, что отходы Abeta42 стабилизировались в спинномозговой жидкости, маркере болезни Альцгеймера.
Другие исследования показали, что медь может быть вредна для мозга. Таким образом, исследование с ионофором PBT2 в качестве активного ингредиента против болезни Альцгеймера показало хорошие результаты в исследовании фазы II. Активный ингредиент связывает не только цинк, но и медь и тем самым снижает концентрацию меди в мозге.
Активный ингредиент связывает не только цинк, но и медь и тем самым снижает концентрацию меди в мозге.
Новое исследование показывает, что медь накапливается в мозговых капиллярах при длительном высоком потреблении и может повредить там гематоэнцефалический барьер. В результате удаление бета-амилоида затрудняется, а накопление вещества вызывает болезнь Альцгеймера.
Использовать
Медь используется исключительно или в качестве сплава в электроустановках, для трубопроводов (отопление, вода, газы), для прецизионных деталей, монет, столовых приборов, произведений искусства, музыкальных инструментов и многого другого.
При использовании в контакте с другими металлами он вызывает контактную коррозию при воздействии влаги.
Электрический кабель (многожильный провод)
После серебра медь обладает второй по величине электропроводностью среди всех веществ даже до золота и поэтому используется среди прочего для:
электрические кабели, перемычки и силовые кабели малого сечения, воздушные линии
Следы печатных плат на печатных платах и частично в интегральных микросхемах
Электрические машины: проводные обмотки в трансформаторах, катушках индуктивности / катушках и электродвигателях
Компоненты: анодные корпуса магнетронов, зажимы, соединительные ножки компонентов, держатели контактов, пресс-гильзы
Хотя алюминий дешевле и по массе на длину лучше электрический проводник, чем медь. Это однако объемно. U. a. Следовательно, и поскольку медь может лучше контактировать и имеет более высокое сопротивление изгибу, она обычно предпочтительна в качестве проводника для алюминия, за исключением случаев, когда речь идет о весе или цене.
Это однако объемно. U. a. Следовательно, и поскольку медь может лучше контактировать и имеет более высокое сопротивление изгибу, она обычно предпочтительна в качестве проводника для алюминия, за исключением случаев, когда речь идет о весе или цене.
Провода и жилы, изготовленные из так называемой бескислородной меди (OFC, англ. Бескислородная медь с чистотой> 99,99%), имеют очень мелкозернистую кристаллическую структуру и особенно высокую усталостную прочность. Они используются для кабелей и проводов, которые подвергаются высоким механическим нагрузкам.
Для воздушных линий используются сплавы меди и магния. Должен быть найден компромисс между увеличением прочности на разрыв и снижением проводимости.
Медь обладает высокой отражательной способностью в инфракрасном диапазоне и поэтому используется в качестве зеркала для излучения лазера на углекислом газе и для покрытия стекла (изоляционное стекло).
Благодаря высокой теплопроводности и коррозионной стойкости, он хорошо подходит в качестве материала для теплообменников, радиаторов и монтажных пластин силовых полупроводников.
«Брюнингталер» – медная или бронзовая курсовая монета за 4 рейхспфеннига 1932 года – изображение Википедия
В декоративно-прикладном искусстве медный лист приводят в движение, который деформируется ударом, что легко возможно благодаря его мягкости. В изобразительном искусстве медь до сих пор используется для производства печатных форм для гравировки и офорта.
Даже крыши покрыты медным листом, который затем образует устойчивую зеленоватую патину, которая состоит из различных основных карбонатов меди или меди. Эту патину, которую часто ошибочно называют вердигрисом (см. Ацетат меди), хорошо защищает нижележащий металл от дальнейшей коррозии, поэтому медные кровли могут прослужить несколько веков. Медные гвозди используются в традиционной шиферной кровле.
сплавы
Медная крыша для Dresden Residenzschloss, изображение: Википедия
Медь также входит в состав многих таких сплавов. Как латунь (с цинком), бронза (с оловом) и никель серебро (с цинком и никелем). Эти медные сплавы широко используются из-за их хороших свойств, таких как цвет, коррозионная стойкость и технологичность. Кованые сплавы (латунь и никель-серебро) и литейные материалы (бронзовый металл, бронза). Кованые сплавы приводятся в желаемую форму с помощью пластического формования (горячая штамповка: прокатка, ковка и т. Д. Или холодная штамповка: волочение проволоки, ковка, холодная прокатка, глубокая вытяжка и т. Д.), В то время как литые материалы обычно трудно или невозможно пластически формуемых.
Кованые сплавы (латунь и никель-серебро) и литейные материалы (бронзовый металл, бронза). Кованые сплавы приводятся в желаемую форму с помощью пластического формования (горячая штамповка: прокатка, ковка и т. Д. Или холодная штамповка: волочение проволоки, ковка, холодная прокатка, глубокая вытяжка и т. Д.), В то время как литые материалы обычно трудно или невозможно пластически формуемых.
В зависимости от добавления никеля цвет меди исчезает и образуются коррозионно-стойкие сплавы от желтоватого до белого (мельхиор).
Многие материалы для монет изготовлены из меди, поэтому «северное золото», называемое металлом золотых частей монет евро, представляет собой сплав меди, цинка, алюминия и олова. Металлы монет монет 2001-DM действительны до 1, а яркие части монет евро сделаны из сплавов мельхиора.
Соединения меди используются в цветных пигментах, в качестве тонеров, в медицинских препаратах и гальванических покрытиях.
Цена истории
Медь является относительно дорогим металлом. Его цена в значительной степени обусловлена основными товарными биржами и биржами товарных фьючерсов в мире. Лидером в торговле медью является Лондонская биржа металлов (LME).
Его цена в значительной степени обусловлена основными товарными биржами и биржами товарных фьючерсов в мире. Лидером в торговле медью является Лондонская биржа металлов (LME).
Цена на медь на мировом рынке подвержена сильным колебаниям: самое большое колебание, которое он испытал за последние 10 года в году 2008, как и цена на медь в 2. Торгуется на LME на промежуточном максимуме 8.940 USD / т в июле и до 23. Декабрь 2008 упал до годового минимума 10 в размере 2.825 USD [55]. После этого цена на медь, восстановленная менее чем за 4 месяцев (15, апрель 2009), вернулась к 4.860 USD / т. Его максимум 10 за год был цен на медь на 14. Февраль 2011 с 10.180 USD / т.
С марта 2012 по март 2013 цена на медь выросла в верхней части (2, апрель 2012), за исключением 8.619,75 USD и 2. Август 2012 снизился до 7.288,25 USD. Аналогичный спрэд был также замечен с октября 2012 до марта 2013 между 8.350 USD / т и 7.577 USD / т.
В августе 2014 цена на медь на мировом рынке была около 7. 000 USD / т. По курсу на тот момент это были 6.199 EUR / т.
000 USD / т. По курсу на тот момент это были 6.199 EUR / т.
Высокая цена на медь также вызывает увеличение краж медьсодержащих предметов. Особенно пострадали здесь кабели заземления железных дорог. Например, в год 2015 Deutsche Bahn AG понес убытки в размере около 14 миллионов евро.
Один из крупнейших финансовых скандалов в новейшей истории – дело Сумитомо. Он был основан на торговле медью. В результате раскрытия, цена на медь 1996 упала на 27% в течение одного дня.
Медь против железа: в чем разница?
Основное различие между Медью и Железом заключается в том, что Медь — это химический элемент с атомным номером 29 , а Железо — это химический элемент 26 или простое вещество, состоящее из него.
Медь
Медь — это химический элемент с символом Cu (от латинского: cuprum) и атомным номером 29. Это мягкий, ковкий и пластичный металл с очень высокой тепло- и электропроводностью. Свежая открытая поверхность чистой меди имеет красновато-оранжевый цвет.
 Медь используется как проводник тепла и электричества, как строительный материал и как составная часть различных металлических сплавов, таких как стерлинговое серебро, используемое в ювелирных изделиях, мельхиор, используемый для изготовления морского оборудования и монет, и константан, используемый в тензодатчиках и термопарах. для измерения температуры.
Медь используется как проводник тепла и электричества, как строительный материал и как составная часть различных металлических сплавов, таких как стерлинговое серебро, используемое в ювелирных изделиях, мельхиор, используемый для изготовления морского оборудования и монет, и константан, используемый в тензодатчиках и термопарах. для измерения температуры.Медь является одним из немногих металлов, встречающихся в природе в металлической форме, пригодной для непосредственного использования (самородные металлы), в отличие от извлечения из руды. Это привело к очень раннему использованию человеком, начиная с ок. 8000 г. до н.э. Это был первый металл, выплавленный из руды, c. 5000 г. до н.э., первый металл, отлитый в форму, c. 4000 г. до н.э. и первый металл, который был специально сплавлен с другим металлом, оловом, для создания бронзы, c. 3500 г. до н.э.
В римскую эпоху медь в основном добывалась на Кипре, происхождение названия металла от aes cyprium (кипрский металл), позднее измененного на сuprum, от которого произошли слова Copper (англ.
 ), cuivre (франц.) , cobre (испанский), Koper (голландский) и Kupfer (немецкий) являются производными. Обычно встречающиеся соединения представляют собой соли меди (II), которые часто придают синий или зеленый цвет таким минералам, как азурит, малахит и бирюза, и исторически широко использовались в качестве пигментов. Медь, используемая в зданиях, обычно для кровли, окисляется с образованием зеленой зелени (или патины). Медь иногда используется в декоративно-прикладном искусстве как в форме элементарного металла, так и в соединениях в качестве пигментов. Соединения меди используются в качестве бактериостатических средств, фунгицидов и консервантов для древесины.
), cuivre (франц.) , cobre (испанский), Koper (голландский) и Kupfer (немецкий) являются производными. Обычно встречающиеся соединения представляют собой соли меди (II), которые часто придают синий или зеленый цвет таким минералам, как азурит, малахит и бирюза, и исторически широко использовались в качестве пигментов. Медь, используемая в зданиях, обычно для кровли, окисляется с образованием зеленой зелени (или патины). Медь иногда используется в декоративно-прикладном искусстве как в форме элементарного металла, так и в соединениях в качестве пигментов. Соединения меди используются в качестве бактериостатических средств, фунгицидов и консервантов для древесины.Медь необходима всем живым организмам в качестве пищевого микроэлемента, поскольку она является ключевым компонентом комплекса дыхательных ферментов цитохром-с-оксидазы. У моллюсков и ракообразных медь входит в состав пигмента крови гемоцианина, который у рыб и других позвоночных замещается железосодержащим гемоглобином.
 У человека медь содержится в основном в печени, мышцах и костях. В организме взрослого человека содержится от 1,4 до 2,1 мг меди на килограмм массы тела.
У человека медь содержится в основном в печени, мышцах и костях. В организме взрослого человека содержится от 1,4 до 2,1 мг меди на килограмм массы тела.Железо
Железо — химический элемент с символом Fe (от лат. ferrum) и атомным номером 26. Это металл первого переходного ряда. По массе это самый распространенный элемент на Земле, образующий большую часть внешнего и внутреннего ядра Земли. Это четвертый по распространенности элемент в земной коре. Его изобилие на каменистых планетах, таких как Земля, связано с его обильным производством в результате синтеза в звездах большой массы, где он является последним элементом, который будет произведен с выделением энергии перед сильным коллапсом сверхновой звезды, которая рассеет железо в космос.
Как и другие элементы группы 8, рутений и осмий, железо существует в широком диапазоне степеней окисления, от -2 до +7, хотя +2 и +3 являются наиболее распространенными. Элементарное железо встречается в метеороидах и других средах с низким содержанием кислорода, но вступает в реакцию с кислородом и водой.
 Свежие железные поверхности выглядят блестящими серебристо-серыми, но окисляются на обычном воздухе с образованием гидратированных оксидов железа, широко известных как ржавчина. В отличие от металлов, образующих пассивирующие оксидные слои, оксиды железа занимают больший объем, чем металл, и, таким образом, отслаиваются, открывая новые поверхности для коррозии.
Свежие железные поверхности выглядят блестящими серебристо-серыми, но окисляются на обычном воздухе с образованием гидратированных оксидов железа, широко известных как ржавчина. В отличие от металлов, образующих пассивирующие оксидные слои, оксиды железа занимают больший объем, чем металл, и, таким образом, отслаиваются, открывая новые поверхности для коррозии.Металлическое железо использовалось с древних времен, хотя медные сплавы, которые имеют более низкую температуру плавления, использовались еще раньше в истории человечества. Чистое железо относительно мягкое, но его невозможно получить плавлением, поскольку оно значительно упрочняется и упрочняется примесями, в частности углеродом, в процессе плавки. Определенная доля углерода (от 0,002% до 2,1%) дает сталь, которая может быть в 1000 раз тверже чистого железа. Металлическое сырое железо производится в доменных печах, где руда восстанавливается коксом до чугуна с высоким содержанием углерода. Дальнейшее рафинирование кислородом снижает содержание углерода до пропорции, необходимой для производства стали.
 Стали и сплавы железа, полученные из других металлов (легированных сталей), на сегодняшний день являются наиболее распространенными промышленными металлами, поскольку они обладают широким спектром желаемых свойств, а железосодержащие породы широко распространены.
Стали и сплавы железа, полученные из других металлов (легированных сталей), на сегодняшний день являются наиболее распространенными промышленными металлами, поскольку они обладают широким спектром желаемых свойств, а железосодержащие породы широко распространены.Химические соединения железа имеют множество применений. Оксид железа, смешанный с алюминиевым порошком, можно поджечь, чтобы создать термитную реакцию, используемую при сварке и очистке руд. Железо образует бинарные соединения с галогенами и халькогенами. Среди его металлоорганических соединений есть ферроцен, первое открытое многослойное соединение.
Железо играет важную роль в биологии, образуя комплексы с молекулярным кислородом в гемоглобине и миоглобине; эти два соединения являются обычными транспортными белками кислорода у позвоночных. Железо также является металлом в активном центре многих важных окислительно-восстановительных ферментов, отвечающих за клеточное дыхание, окисление и восстановление в растениях и животных.
 У мужчины среднего роста в организме около 4 граммов железа, у женщины около 3,5 граммов. Это железо распределяется по всему организму в гемоглобине, тканях, мышцах, костном мозге, белках крови, ферментах, ферритине, гемосидерене и транспортируется в плазме.
У мужчины среднего роста в организме около 4 граммов железа, у женщины около 3,5 граммов. Это железо распределяется по всему организму в гемоглобине, тканях, мышцах, костном мозге, белках крови, ферментах, ферритине, гемосидерене и транспортируется в плазме.
Википедия
Медь (существительное)
Красновато-коричневый, ковкий, пластичный металлический элемент с высокой электро- и теплопроводностью, символ Cu и атомный номер 29.
90 Медь (существительное)Медь (существительное)
Красновато-коричневый цвет/цвет меди.
«цветная панель|BB5836»
Медь (существительное)
Медная монета.
Медь (существительное)
Большой котел, часто используемый для нагревания воды или стирки одежды над огнем. По крайней мере, в Австралазии это также может быть стационарная установка из меди, с огнем под ней и собственным дымоходом. Вообще стало ненужным с появлением стиральной машины.

«Мама нагревала воду в котле на кухне и переливала в жестяную ванну».
«Объясняю, что носки нельзя кипятить в котле вместе с простынями и полотенцами, иначе они сожмутся».
Коппер (существительное)
Полицейский.
Медь (прилагательное)
Изготовлен из меди.
Медь (прилагательное)
Имеющий красновато-коричневый цвет/цвет меди.
Медь (глагол)
Обшить или покрыть медью.
Что-то из меди.
Железо (существительное)
Обычный недорогой металл, часто черного цвета, который ржавеет, притягивается магнитами и используется в производстве стали.
Железо (существительное)
Металлический химический элемент с атомным номером 26 и символом Fe.
Железо (существительное)
Любой материал, кроме стали, преимущественно состоящий из элементарного железа.
«кованое железо, ковкий чугун, чугун, чугун, серый чугун»
Железо (существительное)
Инструмент или устройство из металла, которое нагревается и затем используется для передачи тепла чему-то другому; чаще всего толстый кусок металла, снабженный ручкой и имеющий плоское, примерно треугольное дно, который нагревается и используется для разглаживания складок на одежде и теперь обычно содержит электрический нагревательный прибор.
Железо (существительное)
Кандалы.
Железо (существительное)
Пистолет.
Железо (существительное)
Темный оттенок цвета/цвет серебра.
Железо (существительное)
Мужчина-гомосексуал.
Железо (существительное)
Клюшка для гольфа, используемая для ударов со средней дистанции.
Железо (существительное)
Большая сила или мощь.
Железо (прилагательное)
Изготовлен из металлического железа.
Железо (прилагательное)
Сильный, как воля, несгибаемый.
«У нее была железная воля».
«Он держал железной хваткой».
«железная конституция»
«железные люди»
«адамант | адамант | латунь»
Железо (глагол) убрать складки.
Железо (глагол)
Заковать в кандалы; надеть кандалы или наручники.
Железо (глагол)
Обеспечить или вооружить железом.

«погладить повозку»
Викисловарь
Полное руководство по сравнению металлов
Металлы составляют более 75% таблицы Менделеева, и каждый из них классифицируется и используется по-разному. Это показывает, что о металле нужно знать многое, но знать все невозможно, если только вы не стали металлургом. Используйте это руководство, чтобы помочь вам сравнить и понять различия в металлах.
Какие существуют типы металлов?
Хотя многие типы металлов находятся в периодической таблице, большинство чистых металлов слишком мягкие и податливые, чтобы их можно было использовать только в промышленных целях. Вот почему образуются металлические сплавы.
Металлические сплавы представляют собой чистые металлы в сочетании с другими элементами для получения прочных материалов для изготовления деталей. При определении различных типов металлов и их использования все промышленные металлы имеют один общий элемент — железо.
Содержание железа является исходным показателем для определения типов металлов и сплавов, которые подразделяются на две категории; черных и цветных. Черные металлы – это те, которые содержат железо, тогда как цветные металлы не содержат железа.
Черные металлы – это те, которые содержат железо, тогда как цветные металлы не содержат железа.
Ниже приведен список распространенных черных и цветных металлов и сплавов.
Какие металлы самые прочные?
Объявить любой данный металл самым прочным металлом на земле сложнее, чем кажется. Сравнение металлов только по прочности не работает, потому что прочность зависит от контекста, в котором используется металл. Точно так же не существует универсальной шкалы прочности — есть четыре типа:
- Прочность на растяжение: Прочность на растяжение относится к способности металла сопротивляться растяжению.
- Прочность на сжатие : Прочность на сжатие относится к способности металла выдерживать сжатие.
- Предел текучести: Предел текучести относится к способности металла выдерживать постоянную деформацию или изгиб.
- Ударная вязкость: Ударная вязкость относится к способности металла выдерживать удар без разрушения или разрушения.

10 самых прочных металлов и сплавов перечислены ниже в алфавитном порядке:
- Углеродистая сталь
- Хром
- Инконель
- Железо
- Нержавеющая сталь
- сплав стали, железа и никеля
- Титан
- Алюминид титана
- Вольфрам
- Карбид вольфрама
Из чего состоит каждый металл
На фундаментальном уровне каждый металл состоит из атомарных материалов, таких как электроны, нейтроны и протоны. Как и другие атомы, чистые металлы отличаются друг от друга количеством протонов.
Чистые металлы в земной коре соединяются с металлическими и неметаллическими элементами, образуя сплавы. Добавление дополнительных элементов к чистым металлам изменяет их химические свойства и создает более твердые, прочные и устойчивые к коррозии сплавы.
Давайте посмотрим, из чего сделаны следующие сплавы металлов:
Латунь
Латунь — это сплав цветных металлов, состоящий из меди и цинка. Пропорции цинка и меди могут варьироваться, чтобы создать ассортимент латуни с уникальными свойствами. Латунь также можно комбинировать с другими элементами для создания латунных сплавов.
Бронза
Бронза представляет собой сплав цветных металлов, состоящий из меди и олова. Пропорции меди и олова могут варьироваться, но чистая бронза содержит до 90 процентов меди. Бронзу также можно комбинировать с другими элементами для создания бронзовых сплавов, таких как фосфористая бронза. Фосфористая бронза изготавливается из меди, олова и фосфора.
Углеродистая сталь
Углеродистая сталь представляет собой сплав черных металлов, состоящий из железа и углерода. Пропорции железа и углерода могут варьироваться, в результате чего получается три разных типа углеродистой стали; низкоуглеродистая сталь, среднеуглеродистая сталь и высокоуглеродистая сталь.
Чугун
Чугун представляет собой сплав черных металлов, состоящий из железа и углерода. Однако чугун также состоит из небольших количеств других сплавов, таких как марганец и кремний, которые изменяют его свойства в дальнейшем, чтобы называться чугуном.
Нержавеющая сталь
Нержавеющая сталь представляет собой сплав черных металлов, состоящий из железа и углерода с добавлением стали, хрома и никеля. Сочетание этих сплавов создает уникальный блеск нержавеющей стали и коррозионно-стойкие свойства.
Сталь
Сталь представляет собой сплав черных металлов, состоящий из железа и углерода с небольшим содержанием марганца, кремния, фосфора, серы и кислорода. Сталь является наиболее часто используемым в мире инженерным и конструкционным материалом, часто являющимся базовым компонентом для других металлических сплавов.
Какие бывают марки стали?
Марки стали
Четыре основные группы для классификации типов стали: углеродистые, легированные, нержавеющие и инструментальные.
- Углеродистая сталь: Черные металлы, содержащие железо и углерод с незначительными количествами других элементов. Это самая популярная из четырех марок стали, известная своей долговечностью и прочностью на растяжение. На его долю приходится 90% всего производства стали.
- Легированная сталь: Черные или цветные металлы, содержащие железо и углерод с дополнительными сплавами и элементами, такими как никель, медь, хром и алюминий. Эти дополнительные элементы повышают прочность стали, коррозионную стойкость и обрабатываемость.
- Нержавеющая сталь: Сплавы черных металлов, содержащие железо и углерод с добавками стали, хрома и никеля. Хром является основным ингредиентом для придания нержавеющей стали блеска, прочности и коррозионной стойкости.
- Инструментальная сталь: Металлические сплавы, содержащие железо и углерод с добавлением вольфрама, молибдена, кобальта и ванадия, повышающие прочность и термостойкость.
 Они используются для резки и сверления оборудования и машин.
Они используются для резки и сверления оборудования и машин.
Вы можете определить различные марки стали, измерив количество углерода, количество других сплавов и то, как производитель ее обрабатывает. Существуют две стандартные системы классификации марок стали:
- Система классификации ASTM: Каждому типу стали присваивается буквенный префикс, основанный на ее общей категории, и порядковый номер, соответствующий ее конкретным свойствам. Обозначение ASTM для железа и стали — «A». Примером может служить сталь A36, углеродистая конструкционная сталь, используемая в самых сложных условиях и применениях, включая мосты, двутавровые балки, лодочные рампы и многое другое.
- Система классификации SAE: Каждому типу стали присваивается четырехзначный номер для классификации. Первые две цифры обозначают тип стали и концентрацию легирующего элемента, а последние две – концентрацию в ней углерода.
 Примером может служить сталь 1060, обычная углеродистая сталь, используемая в приложениях общего назначения, где требуются высокая прочность и ударная вязкость.
Примером может служить сталь 1060, обычная углеродистая сталь, используемая в приложениях общего назначения, где требуются высокая прочность и ударная вязкость.
Какие металлы обладают магнитными свойствами?
Магнитные металлы
Металлы обладают магнитными свойствами, когда кристаллическая структура их атомов выровнена, поэтому все атомы обращены в одном направлении. Только ферромагнитные металлы и сплавы способны намагничиваться и относятся к одному из трех типов:
- Постоянные магниты — это обычно встречающиеся в природе элементы или химические соединения, которые нелегко теряют свой магнетизм.
- Временные магниты — намагничиваются при попадании в магнитное поле, но постепенно теряют свой магнетизм по мере удаления поля.
- Электромагнитные магниты — требуют, чтобы электрический ток проходил через проволочные катушки для создания магнитного притяжения.

Три элементарных металла, обладающих естественными ферромагнитными свойствами, — это железо, кобальт и никель. Соединения и сплавы также могут быть магнитными, если они содержат железо, кобальт или никель, например сталь и нержавеющая сталь. К немагнитным металлам относятся алюминий, медь, свинец, олово, титан, цинк и сплавы, такие как латунь и бронза.
Список магнитных металлов
- Кобальт
- Диспрозий
- Гадолиний
- Железо
- Никель
- Нержавеющая сталь (только железо)
- Сталь
Список немагнитных металлов
- Алюминий
- Латунь
- Бронза
- Медь
- Золото
- Серебро
- Цинк
Хотите узнать больше об основных свойствах магнитных металлов, различных типах, их обычном использовании, примерах и многом другом? Ознакомьтесь с нашим полным списком магнитных металлов.
Хотите приобрести магнитные металлические материалы? Мы можем предоставить вам различные материалы, в том числе холоднокатаную сталь, высокоуглеродистую пружинную сталь, варианты закаленной нержавеющей стали и многое другое различных марок, размеров и толщин.


