Определить вес металла: Калькулятор металлов – посчитать точный вес металлопроката
alexxlab | 26.03.2023 | 0 | Разное
рассчитать вес в метры по ГОСТ
Универсальный металлический калькулятор веса стали позволяет быстро и точно рассчитать вес металлопроката по ГОСТу в зависимости от материала и марки стали.
Онлайн калькулятор металлопроката |
К металлопрокату относится вся продукция, которая прошла горячий или холодный прокат на специальных станках. На сегодняшний день существует много видов с различными характеристиками. Запомнить плотность каждого металла и сплава невозможно. Поэтому и рассчитать тоннажность крайне сложно. Для этого используйте калькулятор металла на нашем сайте. Он быстро произведет расчеты исходя из особенностей изделия.
Почему лучше использовать калькулятор расчета металла
Металлопрокат используется повсеместно: в строительстве, ЖКХ и т.д. Часто требуется его транспортировка. Однако машины имеют определенную грузоподъемность, превышение которой недопустимо. Тут встает вопрос, как узнать тоннажность металла, если его нельзя разместить на весах из-за большого объема? Данный расчет выполняет специальный калькулятор, разработанный так, что способен учесть все особенности металлопроката, включая нестандартную форму.
Тут встает вопрос, как узнать тоннажность металла, если его нельзя разместить на весах из-за большого объема? Данный расчет выполняет специальный калькулятор, разработанный так, что способен учесть все особенности металлопроката, включая нестандартную форму.
Не рассчитав вес металлопроката вы рискуете переплатить за доставку груза. Если вызовете фуру, которая будет слишком большой для транспортировки, то вы однозначно переплатите. Стоимость доставки будет высокой. При решении сэкономить, рискуете оформить машину с меньшей грузоподъемностью. В результате вам придется либо заказывать еще один грузовик, либо оформлять более большой грузовой транспорт. Результат будет аналогичным — переплата и потеря времени.
Раньше люди самостоятельно занимались расчетом массы определенного количества металлопроката. Однако они были крайне сложными и часто приводили к ошибкам. С популяризацией интернета, рассчитать вес металлопроката не составит труда.
Преимущества онлайн расчёта
Калькулятор металла – это онлайн инструмент помощи инженерам по снабжению и не только в просчете нужной массы, объема, погонных метров нужного материала.
Основная формула расчета веса: m = ρ × V
- ρ – плотность материала, кг/м3 (см. таблицы ниже)
- V – объем, м3 (рассчитывается индивидуально по формулах для каждого изделия)
Когда необходимо купить металлопрокат, необходимо знать каким транспортом его будет удобнее перевозить. От того, какова будет общая масса металлических изделий, зависит тоннажность автомобилей или другого транспорта для доставки. Поэтому возникает вопрос как вычислить массу необходимого количества металлопроката.
Когда-то решение этого вопроса занимало массу времени даже у высококвалифицированных специалистов. Ведь для выполнения необходимых расчетов нужно было знать теоретическую массу веса различных металлов, формулы для вычисления объема различных прокатных форм и т.
Теперь при составлении любых строительных спецификаций применяется калькулятор металлопроката вместо множества таблиц, формул и кропотливых подсчетов. С помощью нашего сервиса калькулятор металлопроката онлайн можно рассчитать массу таких металлов:
- сталь;
- чугун;
- алюминий;
- бронза;
- латунь;
- магний;
- никель;
- медь;
- олово;
- свинец;
- титан;
- цинк.
Для того, чтобы произвести расчет нужно в выпадающем меню программы Бесплатный калькулятор металлопроката онлайн выбрать тип металла и тип проката. Расчет производится для таких типов проката:
- уголок;
- лист;
- труба;
- круг/проволока/катанка;
- труба квадратная;
- прокат;
- швеллер;
- лента/полоса;
- балка;
- шестигранник.
Для каждого типа металла есть возможность выбора конкретной марки. Например, когда в выпадающем меню «Тип металла» выбрана сталь, то в выпадающем меню «Марка», справа от поля с типом металла, можно выбрать любую из стандартных марок стали. Также в программу внесены все существующие марки металлов, из которых производится металлопрокат.
Например, когда в выпадающем меню «Тип металла» выбрана сталь, то в выпадающем меню «Марка», справа от поля с типом металла, можно выбрать любую из стандартных марок стали. Также в программу внесены все существующие марки металлов, из которых производится металлопрокат.
Далее, выбрав тип проката, тип металла и его марку, остается указать основные параметры самого изделия. В программе наглядно отображается какой именно параметр нужно внести для расчета. К каждому типу металлопроката прилагается графическое изображение его среза с отображением в виде букв названия каждой грани, полочки и т.п. Также изображен сам тип металлопроката. Вы наверняка не спутаете тип «лист» с типом «полоса», или «квадратную трубу» с «квадратом». Для удобства и простоты измерений на графическом изображении среза металлопроката обозначены названия каждой полочки, например, a, b, c. Например, если вы рассчитываете массу алюминиевого уголка, вам нужно указать высоту и ширину его полочек, а также толщину стенки (толщину листа металла).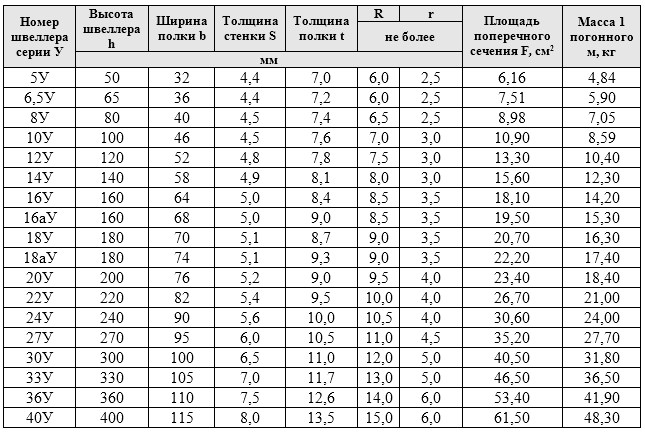
В калькулятор металла эти данные вносятся в миллиметрах. Кроме того, укажите длину конкретного металлоизделия в соответствующем поле, длина указывается в метрах. Теперь остается сделать клик на кнопке «Посчитать» и в поле «Масса» программа выдаст значение массы указанного металлопроката в килограммах, с точностью до грамма.
Для произведения расчета общей массы различных металлических изделий с разными габаритами, выполните расчет для каждого типа изделия отдельно. Затем просто сложите получившиеся результаты – и вы узнаете точную массу всего необходимого вам количества металлопроката.
Также есть возможность задать необходимую массу металлопроката (например, когда вы знаете, что можете перевезти металл с помощью грузовика с определенной грузоподъемностью) и, зная его основные промеры, определить общую длину изделия.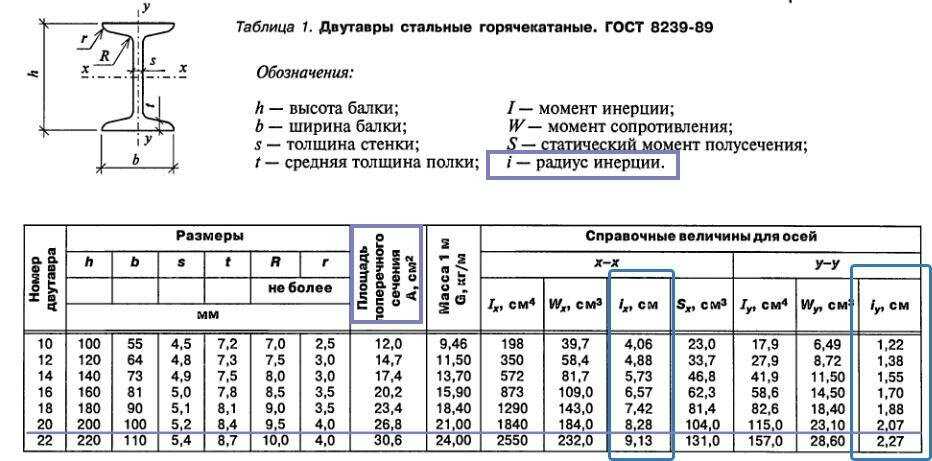
Таблица плотности металлов и сплавов
| Сталь | |
|---|---|
| марка | плотность, кг/м3 |
| 08X13 | 7760 |
| 08X17T | 7760 |
| 08X18h20 | 7850 |
| 08X18h20T | 7900 |
| 09Г2С | 7850 |
| 10 | 7850 |
| 10X17h23M2T | 7900 |
| 10X17h23M3T | 7900 |
| 10ХСНД | 7850 |
| 110Г13Л | 7820 |
| 12Х13 | 7720 |
| 12Х18Н10Т | 7900 |
| 12Х1МФ | 7800 |
| 14Х17Н2 | 7750 |
| 15Х25Т | 7700 |
| 15Х5М | 7750 |
| 15ХСНД | 7850 |
| 20 | 7850 |
| 20Л | 7850 |
| 20Х13 | 7670 |
| 20Х23Н18 | 7900 |
| 30Х | 7820 |
| 30Х13 | 7670 |
| 38ХН3МА | 7850 |
| 40Х | 7820 |
| 40Х13 | 7650 |
| 45 | 7820 |
| 5ХНМ | 7800 |
| 60Г | 7810 |
| 60С2А | 7680 |
| 65 | 7810 |
| 65Г | 7850 |
| 70 | 7810 |
| 95Х18 | 7750 |
| AISI 304 | 7850 |
| AISI 304L | 7850 |
| AISI 316L | 8000 |
| AISI 316Ti | 7950 |
| AISI 321 | 7900 |
| AISI 409 | 7760 |
| AISI 410 | 7720 |
| AISI 420 | 7650 |
| AISI 420S | 7670 |
| AISI 430 | 7720 |
| AISI 439 | 7700 |
| AISI 904L | 7960 |
| Р6М5 | 8300 |
| Ст1 | 7850 |
| Ст3кп | 7800 |
| Ст3пс | 7800 |
| Ст3сп | 7870 |
| У10 | 7810 |
| У10А | 7810 |
| У12А | 7810 |
| У7 | |
| У8 | 7840 |
| У8А | 7830 |
| Х15Н60 | 8500 |
| Х20Н80 | 8400 |
| Х23Ю5Т | 7210 |
| ШХ15 | 7810 |
| ШХ4 | 7850 |
| Чугун | |
|---|---|
| марка | плотность, кг/м3 |
| СЧ10 | 6800 |
| СЧ15 | 7000 |
| СЧ20 | 7100 |
| СЧ25 | 7200 |
| СЧ35 | 7400 |
| Алюминий | |
|---|---|
| марка | плотность, кг/м 3 |
| 1420 | 2470 |
| А5 | 2710 |
| А85 | 2700 |
| А97 | 2710 |
| А95 | 2710 |
| А99 | 2700 |
| А999 | 2710 |
| АВ | 2700 |
| АД | 2710 |
| АД0 | 2710 |
| АД1 | 2710 |
| АД31 | 2710 |
| АД33 | 2710 |
| АК4 | 2770 |
| АК4-1 | 2800 |
| АК5М7 | 2850 |
| АК6 | 2750 |
| АК8 | 2800 |
| АЛ1 | |
| АЛ19 | 2780 |
| АЛ2 | 2650 |
| АЛ3 | 2700 |
| АЛ32 | 2650 |
| АЛ4 | 2650 |
| АЛ5 | 2680 |
| АЛ7 | 2800 |
| АЛ8 | 2550 |
| АЛ9 | 2660 |
| АМг1 | 2670 |
| АМг2 | 2680 |
| АМг5 | 2650 |
| АМг3 | 2670 |
| АМг5П | 2650 |
| АМг6 | 2640 |
| АМц | 2730 |
АН-2. 5 5 | 7800 |
| В65 | 2800 |
| В93 | 2840 |
| В94 | 2850 |
| В95 | 2850 |
| ВАЛ10 | 2800 |
| Д1 | 2800 |
| Д16 | 2800 |
| Д18 | 2760 |
| Д19 | 2760 |
| Бронза | |
|---|---|
| марка | плотность, кг/м3 |
| БрА5 | 8200 |
| БрА7 | 7800 |
| БрА9Ж3Л | 7600 |
| БрА9Ж4 | 7600 |
| БрАЖ9-4 | 7600 |
| БрАЖМц10-3-1.5 | 7800 |
| БрАМц9-2 | 7600 |
| БрАЖН10-4-4 | 7500 |
| БрБ2 | 8200 |
БрБ2. 5 5 | 7800 |
| БрКМц3-1 | 8400 |
| БрКН1-3 | 8800 |
| БрО10 | 8800 |
| БрО10Ф1 | 8760 |
| БрО10Ц2 | 8500 |
| БрО5Ц5С5 | 8800 |
| БрО8С12 | 9100 |
| БрОФ6.5-0.15 | 7800 |
| БрОФ7-0.2 | 7800 |
| БрОЦ4-3 | 8800 |
| БрОЦС4-4-2.5 | 7800 |
| БрОЦС4-4-4 | 9100 |
| БрХ1 | 8900 |
| БрС30 | 9540 |
| Латунь | |
|---|---|
| марка | плотность, кг/м3 |
| Л59 | 8400 |
| Л60 | 8400 |
| Л63 | 8440 |
| Л66 | 8470 |
| Л68 | 8600 |
| Л70 | 8610 |
| Л75 | 8630 |
| Л80 | 8660 |
| Л85 | 8750 |
| Л90 | 8780 |
| Л96 | 8850 |
| ЛА77-2 | 8600 |
| ЛАЖ60-1-1 | 8200 |
| ЛЖМц59-1-1 | 8500 |
| ЛЖС58-1-1 | 8400 |
| ЛК80-3 | 8200 |
| ЛМц58-2 | 8400 |
| ЛО60-1 | 8500 |
| ЛО62-1 | 8500 |
| ЛО70-1 | 8600 |
| ЛС59-1 | 8450 |
| ЛС63-3 | 8500 |
| ЛС64-2 | 8500 |
| ЛЦ16К4 | 8300 |
| ЛЦ23А6Ж3Мц2 | 8500 |
| ЛЦ30А3 | 8500 |
| ЛЦ38Мц2С2 | 8500 |
| ЛЦ40С | 8500 |
| Магний | |
|---|---|
| марка | плотность, кг/м3 |
| МА1 | 1760 |
| МА11 | 1800 |
| МА14 | 1800 |
| МА15 | 1830 |
| МА2 | 1780 |
| Ма2-1 | 1790 |
| МА5 | 1800 |
| МА8 | 1780 |
| Мг95 | 1740 |
| МЛ10 | 1780 |
| МЛ12 | 1810 |
| МЛ19 | 1790 |
| МЛ2 | 1800 |
| МЛ3 | 1780 |
| МЛ4 | 1830 |
| МЛ5 | 1810 |
| МЛ6 | 1810 |
| МЛ9 | 1760 |
| Никель | |
|---|---|
| марка | плотность, кг/м3 |
| НХ9 | 8700 |
| Медь | |
|---|---|
| марка | плотность, кг/м3 |
| БрКд1 | 8940 |
| БрНБТ | 8830 |
| БрНХК | 8850 |
| БрХ | 8920 |
| БрХЦр | 8900 |
| М0 | 8940 |
| М00 | 8940 |
| М00б | 8940 |
| М0б | 8940 |
| М0к | 8940 |
| М1 | 8930 |
| М1к | 8940 |
| М1р | 8940 |
| М1ф | 8940 |
| М2 | 8940 |
| М3 | 8940 |
| М3р | 8940 |
| МК | 8920 |
| МН19 | 8900 |
| МНЖ5-1 | 8700 |
| МНМц3-12 | 8400 |
МНМц40-1. 5 5 | 7800 |
| МНМц43-0.5 | 7800 |
| МНЦ15-20 | 8700 |
| НМЖМц28-2.5-1.5 | 7800 |
| Олово | |
|---|---|
| марка | плотность, кг/м3 |
| О1 | 7300 |
| О1пч | 7300 |
| Свинец | |
|---|---|
| марка | плотность, кг/м3 |
| С0 | 11340 |
| С1С | 11340 |
| С1 | 11340 |
| С2 | 11340 |
| С3 | 11340 |
| Титан | |
|---|---|
| марка | плотность, кг/м3 |
| ВТ1-0 | 4510 |
| ВТ1-00 | 4510 |
| ВТ1-1 | 4510 |
| ВТ14 | 4520 |
| ВТ20 | 4450 |
| ВТ22 | 4600 |
| ВТ3-1 | 4500 |
| ВТ5 | 4400 |
| ВТ5-1 | 4460 |
| ВТ6 | 4430 |
| ОТ4-1 | 4550 |
| ПТ7М | 4490 |
| Цинк | |
|---|---|
| марка | плотность, кг/м3 |
| Ц0 | 7130 |
| Ц0А | 7130 |
| Ц1 | 7130 |
| ЦА4 | 6600 |
| ЦАМ4-1 | 6700 |
| ЦВ | 7130 |
Раньше было необходимо листать огромное количество таблиц, чтобы найти необходимый размер среди сортамента. Калькулятор же содержит все размеры для различных типов изделий, предусмотренных ГОСТ. Для нестандартных изделий и металлов, калькулятор автоматически вычислит объем изделия и определит его вес в соответствии с плотностью выбранного металла (стали, меди, алюминия и других).
Калькулятор же содержит все размеры для различных типов изделий, предусмотренных ГОСТ. Для нестандартных изделий и металлов, калькулятор автоматически вычислит объем изделия и определит его вес в соответствии с плотностью выбранного металла (стали, меди, алюминия и других).
Посчитать вес с онлайн калькулятором, проще простого!
Калькулятор металлопроката предоставлен сайтом calcus.ru
Загрузка…
Понравилось? Поделись с друзьями!
неорганическая химия – Как рассчитать эквивалентную массу металла в сульфате металла?
спросил
Изменено 1 год, 8 месяцев назад
Просмотрено 2к раз
$\begingroup$
Вопрос:
$\pu{2g}$ металла содержится в $\pu{4.
6g}$ его сульфата металла. Найдите эквивалентную массу металла.
Я понимаю, что эквивалентная масса элемента – это молекулярная масса, деленная на n-фактор (в данном случае это валентность), но не могу прийти к выводу.
Не могли бы вы также помочь мне понять, как эквивалентный вес металла связан с эквивалентным весом сульфата? В моем учебнике написано так:
$$\textrm{eq. вес. металла} = \textrm{экв. вес. сульфата металла(2-)}$$
, а затем продолжили расчеты.
PS Я знаю ответ, мне нужно знать, как концептуально к нему прийти!
- неорганическая химия
- стехиометрия
$\endgroup$
$\begingroup$
Я предполагаю, что если вы имеете дело с эквивалентными весами, то вы должны быть хорошо знакомы с понятиями эквивалентов.
Сейчас, $$ \textrm{эквивалент} = \textrm{вес} / \textrm{эквивалент. вес}$$
, и поскольку соединения объединяются в равных количествах эквивалентов, мы имеем
$$\frac{\textrm{вес металла}}{ \textrm{экв вес}} = \frac{\textrm{вес сульфата}}{ \ textrm{его эквивалентный вес}}$$
$$\rightarrow 2/x = 2,6/48$$
Следовательно, $x= 39,92$.
$\endgroup$
0
Зарегистрируйтесь или войдите в систему
Зарегистрируйтесь с помощью Google
Зарегистрироваться через Facebook
Зарегистрируйтесь, используя электронную почту и пароль
Опубликовать как гость
Электронная почта
Требуется, но никогда не отображается
Опубликовать как гость
Электронная почта
Требуется, но не отображается
Нажимая «Опубликовать свой ответ», вы соглашаетесь с нашими условиями обслуживания, политикой конфиденциальности и политикой использования файлов cookie
.
Определить идентичность элемента по бинарной формуле и процентному составу
ChemTeam: определение идентичности элемента по бинарной формуле и процентному составуОпределение идентичности элемента по бинарной формуле и процентному составу
Вернуться к кроту Содержание
Расчет эмпирической формулы при заданных данных массы
Расчет эмпирической формулы при наличии данных о процентном составе
Определение идентичности элемента по бинарной формуле и массовым данным
Определите формулу гидрата
Пример #1: Металл (М) образует оксид с формулой МО. Если оксид содержит 39,70% О по массе, какова идентичность М?
Решение:
1) Assme 100 г соединения присутствует:
39,70 г представляет собой О; 60,30 г М
2) Рассчитайте количество молей кислорода:
39,70 г / 16,00 г/моль = 2,48 моль
3) Определить количество молей М:
Молярное соотношение М:О 1:12,48 равно 1, как x равно 1
х = 2,48 моль М
4) Рассчитайте атомный вес M и определите его:
60,30 г/2,48 моль = 24,314 г/мольМ магний
Пример #2: Определенный сульфид металла, MS 2 , содержит 40,064% серы по массе. Какова идентичность металла М?
Какова идентичность металла М?
Решение №1:
1) Предположим, что присутствует 100 г соединения. Следовательно:
40,064 г — сера; 59,936 г М
2) Рассчитайте количество молей серы:
40,064 г / 32,065 г/моль = 1,249462 моль
3) Используйте молярное соотношение, чтобы получить моли M:
молярное соотношение М к S составляет 1 : 2x относится к 1, как 1,249462 моль к 2
х = 0,624731 моль М
4) Определите атомный вес М:
59,936 г / 0,624731 моль = 95,94 г/мольМ молибден
Решение №2:
1) Определить молярную массу МС 2
64,130 равно 0,40064, как х равно 1х = 160,069 г/моль
2) Вычесть вес серы:
160,069 − 64,130 = 95,94 г/моль
Примечание. значение 64,130 – это вес двух сер.
Пример #3: Установлено, что соединение имеет формулу XBr 2 , в которой X представляет собой неизвестный элемент. Установлено, что бром составляет 71,55% соединения. Установить личность Х.
Установлено, что бром составляет 71,55% соединения. Установить личность Х.
Решение №1:
1) Определить молярную массу XBr 2
159,808 к 0,7155, как х к 1х = 223,3515 г/моль
2) Вычтите массу двух бромов:
223,3515 – 159,808 = 63,543 г/мольЭлемент медь.
Решение №2:
Предположим, что присутствует 100 г соединения. Это означает, что в соединении находится 71,55 г Br.71,55 г / 79,904 г = 0,89545 моль
0,89545 моль к 2, как у к 1
Y = 0,4477725 Мол x присутствует в 100 г xbr 2
100 г – 71,55 г = 28,45 г x в 100 г xbr 2
28,45 g / 0,447725 = 63,544 G / g.
Х медный
Пример #4: Соединение, эмпирическая формула которого XF 3 , состоит из 64,8% F по массе. Какова атомная масса X?
Решение:
64,8 г / 19,0 г/моль = 3,4105 мольy равно 1, как 3,4105 равно 3
y = 1,137 моль X
35,2 г/1,137 моль = 30,96 г/моль
Пример #5: Элемент X образует пентабромид XBr 5 . Анализ XBr 5 показывает, что он содержит 92,81% Br по массе. Что такое элемент Х?
Анализ XBr 5 показывает, что он содержит 92,81% Br по массе. Что такое элемент Х?
Решение:
1) Предположим, имеется 100 г XBr 5 . Это означает следующее:
Присутствует 92,81 г Br и 7,19 г X
2) Рассчитайте количество молей Br:
92,81 г / 79,9 г/моль = 1,1616 моль
3) Определить количество молей X:
1,1616 моль равно 5, так как х равно 1х = 0,23232 моль
4) Определите атомный вес X:
7,19 г / 0,23232 моль = 30,95 г/мольЭлемент фосфор.
Пример #6: Элемент X образует тетрахлорид XCl 4 . Анализ XCl 4 показывает, что он содержит 40,63% Cl по массе. Определите Х.
Решение:
1) Предположим, что присутствует 100 г соединения. Это означает:
40,63 г хлорида на 100 г и 59,37 г Х
2) Определить количество молей хлорида:
40,63 г / 35,453 г/моль = 1,146 моль
3) Определить количество молей X:
1,146 моль равно 4, поскольку х равно 1x = 0,2865 моль X присутствует
4) Определите атомный вес X:
59,37 г/0,2865 моль = 207,2 г/мольX – свинец, PbCl 4
Пример #7: Металл M образует оксид M 2 O 3 , который содержит 68,4% металла по массе. Рассчитайте атомный вес металла.
Рассчитайте атомный вес металла.
Решение:
68,4 в 2 раза больше, чем 31,6 в 4848 получается из 16 умножить на 3, потому что есть 3 кислорода. Это 2x, потому что есть два атома M.
х = 51,95, атомный вес хрома.
Пример #8: Некоторый гидроксид металла, M(OH) 2 , содержит 32,80% кислорода по массе. Какова идентичность металла М?
Решение №1:
1) Напишите выражение для молярной массы соединения:
Пусть M = молярная масса металла.М + (2 х 16,00) + (2 х 1,01)
М + 34.02
2) Напишите выражение для данного массового процента кислорода:
[32,00 / (М + 34,02)] x 100% = 32,8%32,00 / (М + 34,02) = 0,328
3) Алгебра!
32,00 = (0,3280)(М + 34,02)32,00 = 0,3280М + 11,16
20,84 = 0,3280М
М = 63,54
Металл – медь.
Решение №2:
1) Определить массовую долю водорода:
от 32,80 до 32,00, как x до 2,02х = 2,07%
2) Определить массовую долю М:
100% – (32,80 + 2,07) = 65,13%
3) Определить атомный вес М:
ОДИН атом металла в (65,13/32,80) раз тяжелее ДВУХ атомов кислорода.масса атома металла = (65,13/32,80) (2 х 16,00) = 63,54 а.е.м.
Медь.
Решение №3:
1) Определите молярную массу M(OH) 2 :
32,00 равно 0,3280, поскольку x соответствует 1х = 97,56 г/моль
2) Вычтите массу двух гидроксидов:
97,56 – 34,02 = 63,54 г/мольМедь.
Пример #9: Оксид элемента с валентностью 6 содержит 48% кислорода. Какова атомная масса этого элемента? Определите элемент.
Решение:
Элемент M с валентностью +6 образует оксид с формулой MO 3 .Предположим, что присутствует 100 г соединения. Следовательно, 48 г кислорода и 52 г М.
Моль кислорода —> 48 г / 16 г/моль = 3 моль
При молярном отношении М к О 1:3 получаем следующее:
1 равно 3, так как x равно 3 молям
х = 1 моль (Это сколько молей М в 100 г МО 3 .
)
52 г/1 моль = 52 г/моль Элемент хром.
Пример #10: Проанализировано оксибромидное соединение KBrO x , где x неизвестно, и обнаружено, что оно содержит 59,19% Br. Каково значение х?
Решение:
1) Три элемента присутствуют в соединении в фиксированном соотношении:
К : Вг : О = 1 : 1 : х
2) Используя атомный вес, напишите выражение для процентного содержания брома:
59,19 = [(1) (79,9)] / { [(1) (39,1)] + [(1) (79,9)] + [(х) (16,0)] }59,19 = 79,9 / [119 + 16x]
3) Мы знаем, что x должно быть целым числом, поэтому попробуем x = 1:
59,19 = 79,9 / [119 + 16]79,9 / [119 + 16] = 59,185
4) Формула для KBrO x :
КБрО
Пример #11: Проанализировано оксибромидное соединение KBrO x , где x неизвестно, и обнаружено, что оно содержит 52,92% Br. Каково значение х?
Каково значение х?
Решение:
1) Три элемента присутствуют в соединении в фиксированном соотношении:
К : Вг : О = 1 : 1 : х
2) Используя атомный вес, напишите выражение для процентного содержания брома:
52,92 = (1 умножить на 79,9) / { [(1) (39,1)] + [(1) (79,9)] + [(х) (16,0)] }52,92 = 79,9 / [119 + 16x]
3) Мы знаем, что x должно быть целым числом, поэтому попробуем x = 1:
52,92 = 79,9 / [119 + (16) (1)]79,9 / [119 + 16] = 59,185 (что не равно 52,92)
4) Попробуем x = 2:
52,92 = 79,9 / [119 + (16) (2)]79,9 / [119 + 32] = 52,914
4) Формула для KBrO x :
KBrO 2
Пример #12: Некоторый гидроксид металла, M(OH) 2 , содержит 32,8% кислорода по массе. Какова идентичность металла М?
Решение:
1) Предположим, что присутствует 100,0 г соединения. Следовательно, масса кислорода в соединении:
Следовательно, масса кислорода в соединении:
(100,0 г) (0,328) = 32,8 г
2) Моль О в соединении:
32,8 г / 16,00 г/моль = 2,05 моль
3) Масса Н в соединении:
(2,05 моль) (1,01 г/моль) = 2,07 г
4) Масса металла в 100 г соединения:
100,0 г − 32,8 г − 2,07 г = 65,13 г
5) Из формулы:
моль M = моль O / 2 = 2,05 / 2 = 1,025 моль
6) Атомный вес M:
65,13 г/1,025 моль = 63,54 г/мольмедь
Пример #13: Металл М образует оксид М 2 O 3 , который содержит 81,9% металла по весу. Найдите атомный вес М.
Решение №1:
1) Предположим, что присутствует 100 г соединения.
Это означает, что 81,9 г соединения представляют собой М, а 18,1 г — О.
2) Определить количество молей O:
18,1 г / 15,9994 г/моль = 1,13129 моль
3) Молярное соотношение между М и О составляет 2:3. Используйте это отношение для определения молей M:
Используйте это отношение для определения молей M:
2 равно 3, а x равно 1,13129х = 0,7541933 моль
4) Определите атомный вес М:
81,9 г / 0,7541933 моль = 108,6 г/моль
Решение №2:
1) Молярная масса M 2 O 3 составляет:
2(М) + 3(О), что приводит к:2М + 48.0
2) Настройка расчета процента M:
2M / (2M + 48,0) = 0,819
3) Решить:
2М = 0,819(2М + 48,0)2М = 1,638 М + 39,312
0,362 М = 39,312
М = 108,6 г/моль
Пример #14: Ионное соединение, образованное алюминием и элементом группы VIA, содержит 18,55% Al по массе. Какова формула соединения?
Решение:
1) Соединение будет иметь общую формулу Al 2 Х 3 . Для решения задачи сначала предположим, что присутствует 100,0 г соединения. 18,55 г из них будет Al. Преобразуйте эту массу в моли:
18,55 г из них будет Al. Преобразуйте эту массу в моли:
18,55 г Al / 26,98 г/моль = 0,6875 моль Al
2) Используя формулу соединения, рассчитайте количество молей X:
(0,6875 моль Al) (3 моль X / 2 моль Al) = 1,031 моль X
3) Молярная масса Х:
(100,0 − 18,55 г) / 1,031 моль = 79,0,0 г/моль
4) Элемент группы VIA с молекулярной массой 79г/моль – это селен. Таким образом, соединение представляет собой Al 2 Se 3 , называемое селенидом алюминия.
Пример #15: Элемент X образует два оксида с формулами XO 3 и X 2 O 3 . Один из оксидов содержит 52% X по массе и имеет формульную массу 99,98 г/моль. Какова формула этого оксида?
(а) CrO 3
(б) Al 2 O 3
(в) Mg 2 O 3
(г) VO 3
Решение:
Предположим, что присутствует 100 г (или 99,98 г, если хотите) оксида.


 6g}$ его сульфата металла. Найдите эквивалентную массу металла.
6g}$ его сульфата металла. Найдите эквивалентную массу металла.