Основные свойства алюминия: свойства, применение, способы промышленного получения
alexxlab | 31.10.1991 | 0 | Разное
Основные свойства алюминия: области применения
30.04.2021 Автор: VT-METALL
Вопросы, рассмотренные в материале:
- Как был открыт алюминий и каковы его основные свойства
- Основные физические свойства алюминия
- Основные химические свойства алюминия
- Как применяют основные свойства алюминия
- Как используют основные свойства алюминия в строительстве
Основные свойства алюминия делают этот материал по-настоящему универсальным и ценным. Его используют во всех видах промышленного производства, в сельском хозяйстве, в быту, в коммерции. Обладает огромным количеством преимуществ по отношению к стали и другим видам металла.
Самые популярные сферы применения алюминия – изготовление металлоконструкций и металлообработка. О том, какие свойства металла и где конкретно они нашли свое применение, читайте далее.
Как был открыт алюминий и каковы его основные свойства
Алюминий представляет собой парамагнитный металл, достаточно легкий, имеющий серебристый цвет. Он хорошо поддается механической обработке и литью, просто формуется. В земной коре этот элемент третий по распространенности, впереди только кислород и кремний. Наши недра содержат целых 8 % данного металла, что значительно больше золота, количество которого составляет не более пяти миллионных долей процента.
Он хорошо поддается механической обработке и литью, просто формуется. В земной коре этот элемент третий по распространенности, впереди только кислород и кремний. Наши недра содержат целых 8 % данного металла, что значительно больше золота, количество которого составляет не более пяти миллионных долей процента.
Алюминий активно используется в большинстве сфер производства. Его сплавы применяются для изготовления бытовой техники, транспорта, в машиностроении и электротехнике. Капитальное строительство также не может обойтись без него.
Он чрезвычайно распространен в земной коре, являясь первым из металлов и третьим химическим элементом (первое место у кислорода, второе – у кремния). Доля алюминия в наших недрах – 8,8 %. Металл является частью большого количества горных пород и минералов, основной из которых – алюмосиликат.
В виде соединений алюминий находится в базальтах, полевых шпатах, гранитах, глине и пр. Однако в основном его получают из бокситов, которые достаточно редко встречаются в виде месторождений. В России такие залежи есть только на Урале и в Сибири. В промышленных масштабах алюминий можно также добывать из нефелинов и алунитов.
В России такие залежи есть только на Урале и в Сибири. В промышленных масштабах алюминий можно также добывать из нефелинов и алунитов.
Рекомендуем статьи по металлообработке
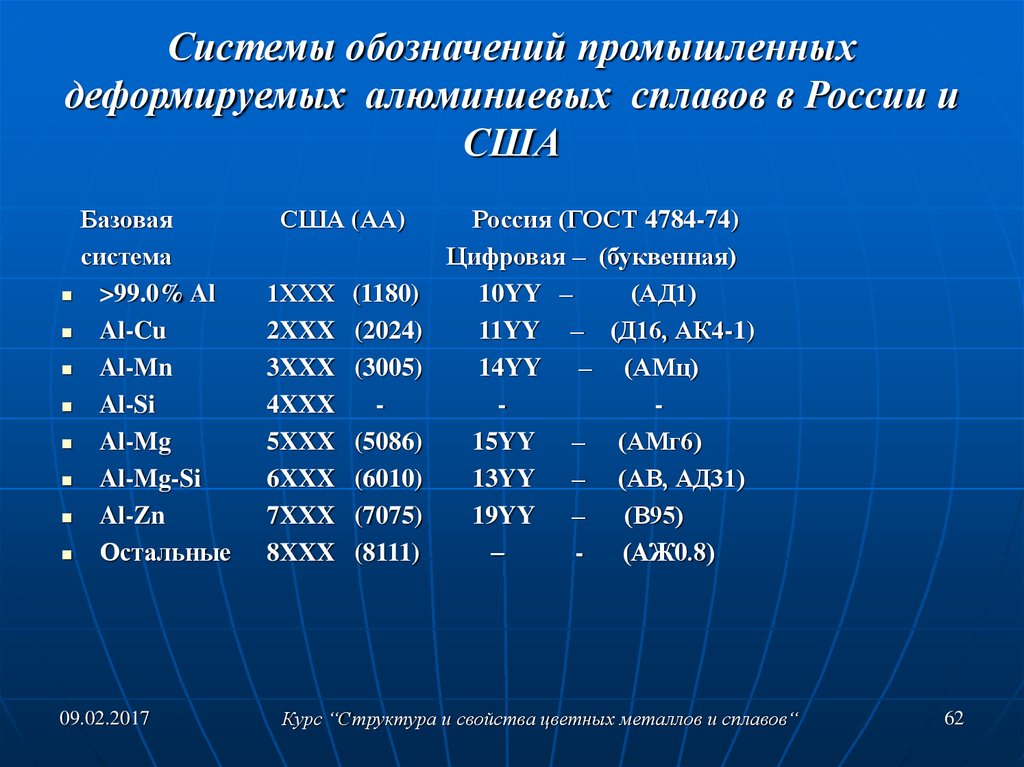
- Марки сталей: классификация и расшифровка
- Марки алюминия и области их применения
- Дефекты металлический изделий: причины и методика поиска
Ткани животных и растений содержат алюминий в виде микроэлемента. Некоторые организмы, например, моллюски и плауны, являются его концентраторами, накапливая в своих органах.
Человечеству с давних времен знакомо соединение алюминия под названием алюмокалиевые квасцы. Применялось оно в процессе выделки кожи, в качестве средства, которое, набухая, связывает различные компоненты смеси. Во второй половине XVIII в. ученые открыли оксид алюминия. А вот вещество в чистом виде получили значительно позже.
Впервые это удалось Ч. К. Эрстеду, который выделил алюминий из хлорида. Проводя опыт, он обрабатывал соли калия амальгамой, в результате чего выделился порошок серого цвета, признанный всеми чистым алюминием.
В дальнейшем, исследуя металл, ученые определили его химические свойства, проявляющиеся в высокой способности к восстановлению и активности. Именно поэтому с алюминием долгое время не работали.
Но уже в 1854 г. французский ученый Девиль, применив электролиз расплава, сумел получить металл в слитках. Данный метод используется и сейчас. В промышленных масштабах алюминий стали производить в начале XX в., когда предприятия смогли получить доступ к большому количеству электроэнергии.
Сегодня алюминий является одним из самых используемых в производстве бытовой техники и строительстве металлом.
Вред от принятия пищи из алюминиевой посуды
Отсекая огромный ворох страшилок об опасностях, связанных с алюминием, следует обратить внимание на официальное заявление Всемирной организации здоровья. Еще в 1998 году было сказано, чтобы нанести вред организму человека алюминием, его нужно принять внутрь более 50 мг одномоментно.
Для простого примера можно сказать, что даже кислые щи, простояв в алюминиевой кастрюле целую неделю, вбирают в себя не более 3 мг вещества. А поскольку вся окружающая человека среда имеет в своем составе алюминий, то он поступает в организм постоянно. Мало того. Он еще и вырабатывается организмом.
А поскольку вся окружающая человека среда имеет в своем составе алюминий, то он поступает в организм постоянно. Мало того. Он еще и вырабатывается организмом.
Но даже усиленный прием лекарств (содержащих алюминий) не может быть опасен. Если собрать все факторы воедино, то суточная норма вещества никогда не может быть превышена при естественном порядке. Для того, чтобы получить отравление алюминием вместе с пищей, в нее необходимо только добавить его в большом количестве намеренно.
В течение 20 лет с момента первого заявления, ВОЗ неоднократно выступала с различными докладами, пресекающими различные мифы. Одним из них выступает связь болезни Альцгеймера с принятием пищи из алюминиевой посуды. Медицинские исследования это не подтвердили.
Алюминий и Альцгеймер Источник Яндекс.Дзен
Основные физические свойства алюминия
Основные характеристики алюминия – высокая электро- и теплопроводность, пластичность, устойчивость к холоду и коррозии. Его можно обрабатывать посредством прокатки, ковки, штамповки, волочения. Алюминий прекрасно поддается сварке.
Алюминий прекрасно поддается сварке.
Примеси, присутствующие в металле в различных количествах, значительно ухудшают механические, технологические и физико-химические свойства чистого алюминия. Основными из них являются титан, кремний, железо, медь и цинк.
По степени очистки алюминий разделяют на технический металл и высокой чистоты. На практике различия данных типов – в стойкости к коррозии в различной среде. Стоимость напрямую зависит от чистоты алюминия. Технический металл подходит для производства проката, различных сплавов, кабельно-проводниковых изделий. Чистый используют для специальных целей.
Алюминий обладает высокой электропроводностью, уступая только золоту, серебру, меди. Однако сочетание данного показателя с малой плотностью позволяет использовать его при производстве кабельно-проводниковых изделий наравне с медью. Электропроводность металла может увеличиваться при длительном отжиге или ухудшаться при нагартовке.
Увеличивая чистоту алюминия, производители повышают его теплопроводность. Снизить данное свойство способны примеси меди, марганца и магния. Более высокую теплопроводность имеют исключительно медь и серебро. Именно благодаря данному свойству данный металл используют для производства радиаторов охлаждения и теплообменников.
Снизить данное свойство способны примеси меди, марганца и магния. Более высокую теплопроводность имеют исключительно медь и серебро. Именно благодаря данному свойству данный металл используют для производства радиаторов охлаждения и теплообменников.
Удельная теплоемкость алюминия, как и температура его плавления, достаточно высока. Данные показатели значительно превышают аналогичные значения большей части металлов. С повышением чистоты металла увеличивается и его способность отражать от поверхности световые лучи. Алюминий хорошо поддается полировке и прекрасно анодируется.
Металл близок по свойствам к кислороду, его поверхность на воздухе быстро затягивается пленкой из оксида алюминия – тонкой и прочной. Обладая антикоррозионными свойствами, она защищает металл от образования ржавчины и предупреждает дальнейшее окисление. Алюминий не взаимодействует с азотной кислотой (концентрированной и разбавленной) и органическими кислотами, он стоек к воздействию пресной, соленой воды.
Эти особенности алюминия придают ему устойчивость к коррозии, что и используется людьми. Именно поэтому его особенно широко применяют в строительстве. Интерес к нему увеличивается еще и по причине его легкости в сочетании с прочностью и мягкостью. Такие характеристики есть далеко не у всякого вещества.
Помимо вышеуказанных, алюминий имеет еще несколько интересных физических свойств:
- Ковкость и пластичность – алюминий стал материалом изготовления прочной и легкой тонкой фольги, а также проволоки.
- Плавление происходит при температуре +660 °С.
- Температура кипения +2 450 °С.
- Плотность – 2,7 г/см³.
- Наличие объемной гранецентрированной металлической кристаллической решетки.
- Тип связи – металлический.
Применение
Алюминий применяется в металлургии в качестве основы для сплавов (дуралюмин, силумин) и легирующего элемента (сплавы на основе меди, железа, магния, никеля). Сплавы алюминия используются в быту, в архитектуре и строительстве, в судостроении и автомобилестроении, а также в космической и авиационной технике. Алюминий применяется при производстве взрывчатых веществ. Анодированный алюминий (покрытый окрашенными плёнками из оксида алюминия) применяют для изготовления бижутерии. Также металл используется в электротехнике.
Алюминий применяется при производстве взрывчатых веществ. Анодированный алюминий (покрытый окрашенными плёнками из оксида алюминия) применяют для изготовления бижутерии. Также металл используется в электротехнике.
Основные химические свойства алюминия
С химической точки зрения алюминий является чрезвычайно сильным восстановителем, имеющим способность в чистом виде быть высоко активным веществом. Основное условие – убрать оксидную пленку.
Алюминий способен вступать в реакции с:
- щелочными соединениями;
- кислотами;
- серой;
- галогенами.
Алюминий не взаимодействует в обычных условиях с водой. Йод – единственный из галогенов, с которым у металла происходит реакция без нагревания. Для взаимодействия с прочими требуется увеличение температуры.
Рассмотрим несколько примеров, показывающих химические свойства данного металла. Это уравнения, иллюстрирующие взаимодействие с:
- щелочами: 2Al + 6h3O + 2NaOH = Na[Al(OH)4] + 3Н2;
- кислотами: AL + HCL = AlCL3 + h3;
- серой: 2AL + 3S = AL2S3;
- галогенами: AL + Hal = ALHal3.

Основным свойством алюминия считается его способность восстанавливать иные вещества из их соединений.
Реакции его взаимодействия с оксидами иных металлов хорошо показывают все восстановительные свойства вещества. Алюминий прекрасно выделяет металлы из различных соединений. Примером может служить: Cr2O3 + AL = AL2O3 + Cr.
Металлургическая промышленность активно использует эту способность алюминия. Методика получения веществ, которая основывается на данной реакции, называется алюминотермия. Химическая индустрия использует алюминий чаще всего для получения иных металлов.
СТРУКТУРА
Кубическая гранецентрированная структура. 4 оранжевых атома
Кристаллическая решетка алюминия — гранецентрированный куб, которая устойчива при температуре от 4°К до точки плавления. В алюминии нет аллотропических превращений, т.е. его строение постоянно. Элементарная ячейка состоит из четырех атомов размером 4,049596×10 -10 м; при 25 °С атомный диаметр (кратчайшее расстояние между атомами в решетке) составляет 2,86×10 -10 м, а атомный объем 9,999×10 -6 м 3 /г-атом. Примеси в алюминии незначительно влияют на величину параметра решетки. Алюминий обладает большой химической активностью, энергия образования его соединений с кислородом, серой и углеродом весьма велика. В ряду напряжений он находится среди наиболее электроотрицательных элементов, и его нормальный электродный потенциал равен -1,67 В. В обычных условиях, взаимодействуя с кислородом воздуха, алюминий покрыт тонкой (2-10 -5 см), но прочной пленкой оксида алюминия А123, которая защищает от дальнейшего окисления, что обусловливает его высокую коррозионную стойкость. Однако при наличии в алюминии или окружающей среде Hg, Na, Mg, Ca, Si, Си и некоторых других элементов прочность оксидной пленки и ее защитные свойства резко снижаются.
Примеси в алюминии незначительно влияют на величину параметра решетки. Алюминий обладает большой химической активностью, энергия образования его соединений с кислородом, серой и углеродом весьма велика. В ряду напряжений он находится среди наиболее электроотрицательных элементов, и его нормальный электродный потенциал равен -1,67 В. В обычных условиях, взаимодействуя с кислородом воздуха, алюминий покрыт тонкой (2-10 -5 см), но прочной пленкой оксида алюминия А123, которая защищает от дальнейшего окисления, что обусловливает его высокую коррозионную стойкость. Однако при наличии в алюминии или окружающей среде Hg, Na, Mg, Ca, Si, Си и некоторых других элементов прочность оксидной пленки и ее защитные свойства резко снижаются.
Как применяют основные свойства алюминия
Алюминий в чистом виде имеет слабые механические свойства. Именно поэтому наиболее часто применяют его сплавы.
Таких сплавов достаточно много, вот основные из них:
- алюминий с марганцем;
- дюралюминий;
- алюминий с магнием;
- алюминий с медью;
- авиаль;
- силумины.
В основе этих сплавов лежит алюминий, отличаются они исключительно добавками. Последние же делают материал прочным, легким в обработке, более стойким к износу, коррозии.
Есть несколько основных областей применения алюминия (чистого или в виде сплава). Из металла изготавливают:
- фольгу и проволоку для бытового использования;
- посуду;
- морские и речные суда;
- самолеты;
- реакторы;
- космические аппараты;
- архитектурные и строительные элементы и конструкции.
Алюминий является одним из самых важных металлов наравне с железом и его сплавами. Эти два элемента таблицы Менделеева наиболее широко применяются человеком в своей деятельности.
ПРИМЕНЕНИЕ
Широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — лёгкость, податливость штамповке, коррозионная стойкость. Электропроводность алюминия всего в 1,7 раза меньше, чем у меди, при этом алюминий приблизительно в 4 раза дешевле за килограмм, но, за счёт в 3,3 раза меньшей плотности, для получения равного сопротивления его нужно приблизительно в 2 раза меньше по весу. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при напылении проводников на поверхности кристаллов микросхем. Когда алюминий был очень дорог, из него делали разнообразные ювелирные изделия. Так, Наполеон III заказал алюминиевые пуговицы, а Менделееву в 1889 г. были подарены весы с чашами из золота и алюминия. Мода на ювелирные изделия из алюминия сразу прошла, когда появились новые технологии его получения, во много раз снизившие себестоимость. Сейчас алюминий иногда используют в производстве бижутерии.
Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при напылении проводников на поверхности кристаллов микросхем. Когда алюминий был очень дорог, из него делали разнообразные ювелирные изделия. Так, Наполеон III заказал алюминиевые пуговицы, а Менделееву в 1889 г. были подарены весы с чашами из золота и алюминия. Мода на ювелирные изделия из алюминия сразу прошла, когда появились новые технологии его получения, во много раз снизившие себестоимость. Сейчас алюминий иногда используют в производстве бижутерии.
Источник
Как используют основные свойства алюминия в строительстве
Строительство – одна из основных отраслей-потребителей алюминия. 25 % всего вырабатываемого металла используется именно в ней. Современный облик мегаполисов был бы невозможен без использования алюминия. Он дает возможность создавать функциональные и красивые здания, стремящиеся ввысь. Небоскребы офисных центров имеют фасады из стекла, закрепленные на прочных, легких рамах из алюминия.
Современные торговые, развлекательные и выставочные центры в основе своей имеют каркас из алюминия. Конструкции из данного металла используются для возведения бассейнов, стадионов и других спортивных строений. Алюминий – один из самых востребованных у архитекторов, строителей, дизайнеров металлов. Почему? Давайте разберемся.
Алюминий – прочный и легкий металл, не поддающийся коррозии, имеющий долгий срок службы и совершенно нетоксичный. Он легко поддается обработке, сварке, паянию, его просто сверлить, распиливать, связывать и соединять шурупами. Этот металл способен принять любую форму посредством экструзии. Алюминий поможет воплотить самый смелый замысел архитектора. Из него изготавливаются конструкции, которые невозможно сделать из иных материалов: пластика, дерева или стали.
Уход за алюминиевой посудой
Начать нужно с универсального совета. Посуду лучше мыть сразу после использования. Во-первых, это значительно легче. Во-вторых, так можно продлить срок службы у предмета. Единственная оговорка – необходимо дать время посуде на остывание. Ведь попадание даже капли холодной воды на раскаленный металл способно привести к его деформации.
Единственная оговорка – необходимо дать время посуде на остывание. Ведь попадание даже капли холодной воды на раскаленный металл способно привести к его деформации.
Удаление жира и гари
Блеск у алюминия возвращается даже после удаления многолетней гари:
- Понадобится большая емкость из металла, чтобы в ней полностью утопилась испорченная сковорода или кастрюля.
- Тара заполняется водой.
- Кусок хозяйственного мыла измельчается на терке.
- Порошок добавляется в воду.
- Туда же вливается 300 грамм силикатного клея.
- Раствор доводится до кипения, и в него погружается грязная посуда.
- Необходимо продержать ее на медленном огне не меньше одного часа.
- После этого с предосторожностями ее достают из кипятка.
- Мягкая фланель легко и быстро убирает размягченную гарь.
После завершения чистящей операции следует тщательно прополоскать изделие. Таким же способом удаляется и накипь с поверхности. Но можно попробовать приготовить раствор из нашатырного спирта (10 капель на литр) и мыла. Технология очистки такая же.
Технология очистки такая же.
Удаление нагара с алюминиевой сковороды Источник sdelai-lestnicu.ru
Возвращение блеска
Сделать алюминиевые предметы, как новыми, помогут следующие действия:
- Внутрь посуды нужно залить кислое молоко и оставить на 40 минут.
- Натереть стенки половинкой кислого яблока или лимона. Оставить посуду на пару часов.
- Замочить предмет в пищевом уксусе на несколько часов.
- Прокипятить 10 минут в посуде порезанную луковицу.
- Натереть мокрую поверхность зубным порошком и оставить на всю ночь.
После выполнения любой из операций всегда необходимо заканчивать тщательным полосканием в теплой воде.
Борьба с чернотой
Вернуть блеск алюминию после его закопчения на костре может винный уксус или лимонная кислота:
- Салфетка смачивается данными растворами. Затем ей протираются стенки.
- Внутрь посуды наливается вода. В нее добавляется или уксус, или кислота.
- Жидкость доводится до кипения.
 Огонь убавляется до минимума и выжидается не более 15 минут.
Огонь убавляется до минимума и выжидается не более 15 минут. - После остывания, раствор сливается.
- Стенки проходят мягкой губкой с теплой водой.
Обычно в походе для чистки используют песок для очистки котелка от копоти костра. Не нужно этого делать. Причины будут указаны ниже. Лучше принести закопченную посуду домой и воспользоваться вышеуказанным рецептом.
Предостережения
Все жесткие виды чистящих средств под строгим запретом. Даже если не прикладывать значительных усилий, поверхность все равно поцарапается. Нарушение защитной пленки приведет к тому, что алюминий будет контактировать с пищей.
Мытье посуды жесткой мочалкой Источник biolshop.com.ua
Вторая причина исключения жестких средств для чистки заключается в том, что сталь способна оставлять глубокие борозды. Они со временем забиваются грязью. Удалить ее из глубокой царапины не представляется возможным. По этой же причине лучше не использовать песок или любые абразивы.
Еще под запретом сода. Хоть она и считается универсальным чистящим средством, но для алюминия категорически не подходит. Ведь в ней находятся щелочи, а они будут губительны для наружного защитного слоя.
Хоть она и считается универсальным чистящим средством, но для алюминия категорически не подходит. Ведь в ней находятся щелочи, а они будут губительны для наружного защитного слоя.
Нельзя мыть предметы в посудомоечной машине. Во-первых, из-за этого блеск алюминий потеряет. Во-вторых, моющие средства для этих агрегатов все без исключения содержат щелочь. Производители даже специально увеличивают их количество для увеличения качества мытья. Посуда будет безнадежно испорчена.
Латунь.
Сплав меди с цинком. Различное соотношение этих двух составляющих позволяют получать сплавы с различными свойствами. Если цинка от 5 до 20 % – латунь называется красной, и желтой, если содержание цинка 20-36 %
Эти сплавы ковкие и имеют достаточно низкую температуру плавления. Внешне латунь напоминает золото, поэтому часто используется в прикладном искусстве и декоре . Мебельная фурнитура, замки, декоративные элементы. Из латуни делают музыкальные инструменты. Используется она и в военной промышленности.
Конструкционные стали.
Их классифицируют по характеристикам и по химическому составу сплавов. Если качественные и обыкновенные. И те и другие – углеродистые стали, хоть содержание углерода в них незначительное.
Предназначение обыкновенных конструкционных сплавов – изготовление промышленных изделий, которые должны подвергаться серьезным механическим нагрузкам: гвоздей, болтов, уголков, швеллеров, балок и т.п. Качественные конструкционные стали подходят для изготовления деталей, используемых в машиностроении. Конечно, выдерживаемые нагрузки у них гораздо ниже, такие марки стали гораздо мягче, их используют для изготовления деталей методом холодной штамповки. Кроме того есть особо-высококачественные марки, их называют криогенными. Они сохраняют прочностные характеристики при экстремально низких температурах. Из них делают емкости для транспортировки и хранения сжиженных газов, а так же применяют при строительстве объектов в условиях вечной мерзлоты.
Алюминий: свойства химические и физические
Одними из самых удобных в обработке материалов являются металлы. Среди них также есть свои лидеры. Так, например, основные свойства алюминия известны людям уже давно. Они настолько подходят для применения в быту, что данный металл стал очень популярным. Каковы же свойства алюминия как простого вещества и как атома, рассмотрим в данной статье.
Среди них также есть свои лидеры. Так, например, основные свойства алюминия известны людям уже давно. Они настолько подходят для применения в быту, что данный металл стал очень популярным. Каковы же свойства алюминия как простого вещества и как атома, рассмотрим в данной статье.
История открытия алюминия
Издавна человеку было известно соединение рассматриваемого металла – алюмокалиевые квасцы. Оно использовалось как средство, способное набухать и связывать между собой компоненты смеси, это было необходимо и при выделке кожаных изделий. О существовании в чистом виде оксида алюминия стало известно в XVIII веке, во второй его половине. Однако при этом чистое вещество получено не было.
Сумел же выделить металл из его хлорида впервые ученый Х. К. Эрстед. Именно он обработал амальгамой калия соль и выделил из смеси серый порошок, который и был алюминием в чистом виде.
Тогда же стало понятно, что химические свойства алюминия проявляются в его высокой активности, сильной восстановительной способности. Поэтому долгое время с ним никто больше не работал.
Поэтому долгое время с ним никто больше не работал.
Однако в 1854 году француз Девиль смог получить слитки металла методом электролиза расплава. Этот способ актуален и по сей день. Особенно массовое производство ценного материала началось в XX веке, когда были решены проблемы получения большого количества электроэнергии на предприятиях.
На сегодняшний день данный металл – один из самых популярных и применяемых в строительстве и бытовой промышленности.
Общая характеристика атома алюминия
Если характеризовать рассматриваемый элемент по положению в периодической системе, то можно выделить несколько пунктов.
- Порядковый номер – 13.
- Располагается в третьем малом периоде, третьей группе, главной подгруппе.
- Атомная масса – 26,98.
- Количество валентных электронов – 3.
- Конфигурация внешнего слоя выражается формулой 3s23p1.
- Название элемента – алюминий.
- Металлические свойства выражены сильно.

- Изотопов в природе не имеет, существует только в одном виде, с массовым числом 27.
- Химический символ – AL, в формулах читается как “алюминий”.
- Степень окисления одна, равна +3.
Химические свойства алюминия полностью подтверждаются электронным строением его атома, ведь имея большой атомный радиус и малое сродство к электрону, он способен выступать в роли сильного восстановителя, как и все активные металлы.
Алюминий как простое вещество: физические свойства
Если говорить об алюминии, как о простом веществе, то он представляет собой серебристо-белый блестящий металл. На воздухе быстро окисляется и покрывается плотной оксидной пленкой. Тоже самое происходит и при действии концентрированных кислот.
Наличие подобной особенности делает изделия из этого металла устойчивыми к коррозии, что, естественно, очень удобно для людей. Поэтому и находит такое широкое применение в строительстве именно алюминий. Свойства вещества также еще интересны тем, что данный металл очень легкий, при этом прочный и мягкий. Сочетание таких характеристик доступно далеко не каждому веществу.
Сочетание таких характеристик доступно далеко не каждому веществу.
Можно выделить несколько основных физических свойств, которые характерны для алюминия.
- Высокая степень ковкости и пластичности. Из данного металла изготовляют легкую, прочную и очень тонкую фольгу, его же прокатывают в проволоку.
- Температура плавления – 660 0С.
- Температура кипения – 2450 0С.
- Плотность – 2,7 г/см3.
- Кристаллическая решетка объемная гранецентрированная, металлическая.
- Тип связи – металлическая.
Физические и химические свойства алюминия определяют области его применения и использования. Если говорить о бытовых сторонах, то большую роль играют именно уже рассмотренные нами выше характеристики. Как легкий, прочный и антикоррозионный металл, алюминий применяется в самолето- и кораблестроении. Поэтому эти свойства очень важно знать.
Химические свойства алюминия
С точки зрения химии, рассматриваемый металл – сильный восстановитель, который способен проявлять высокую химическую активность, будучи чистым веществом. Главное – это устранить оксидную пленку. В этом случае активность резко возрастает.
Главное – это устранить оксидную пленку. В этом случае активность резко возрастает.
Химические свойства алюминия как простого вещества определяются его способностью вступать в реакции с:
- кислотами;
- щелочами;
- галогенами;
- серой.
С водой он не взаимодействует при обычных условиях. При этом из галогенов без нагревания реагирует только с йодом. Для остальных реакций нужна температура.
Можно привести примеры, иллюстрирующие химические свойства алюминия. Уравнения реакций взаимодействия с:
- кислотами – AL + HCL = AlCL3 + H2;
- щелочами – 2Al + 6H2O + 2NaOH = Na[Al(OH)4] + 3Н2;
- галогенами – AL + Hal = ALHal3;
- серой – 2AL + 3S = AL2S3.
В целом, самое главное свойство рассматриваемого вещества – это высокая способность к восстановлению других элементов из их соединений.
Восстановительная способность
Восстановительные свойства алюминия хорошо прослеживаются на реакциях взаимодействия с оксидами других металлов. Он легко извлекает их из состава вещества и позволяет существовать в простом виде. Например: Cr2O3 + AL = AL2O3 + Cr.
В металлургии существует целая методика получения веществ, основанная на подобных реакциях. Она получила название алюминотермии. Поэтому в химической отрасли данный элемент используется именно для получения других металлов.
Распространение в природе
По распространенности среди других элементов-металлов алюминий занимает первое место. Его в земной коре содержится 8,8 %. Если же сравнивать с неметаллами, то место его будет третьим, после кислорода и кремния.
Вследствие высокой химической активности он не встречается в чистом виде, а лишь в составе различных соединений. Так, например, известно множество руд, минералов, горных пород, в состав которых входит алюминий. Однако добывается он только из бокситов, содержание которых в природе не слишком велико.
Однако добывается он только из бокситов, содержание которых в природе не слишком велико.
Самые распространенные вещества, содержащие рассматриваемый металл:
- полевые шпаты;
- бокситы;
- граниты;
- кремнезем;
- алюмосиликаты;
- базальты и прочие.
В небольшом количестве алюминий обязательно входит в состав клеток живых организмов. Некоторые виды плаунов и морских обитателей способны накапливать этот элемент внутри своего организма в течение жизни.
Получение
Физические и химические свойства алюминия позволяют получать его только одним способом: электролизом расплава соответствующего оксида. Однако процесс этот технологически сложен. Температура плавления AL2O3 превышает 2000 0С. Из-за этого подвергать электролизу непосредственно его не получается. Поэтому поступают следующим образом.
- Добывают бокситы.
- Очищают их от примесей, оставляя лишь оксид алюминия.
- Затем плавят криолит.

- Добавляют туда оксид.
- Данную смесь элекролизуют и получают чистый алюминий и углекислый газ.
Выход продукта составляет 99,7 %. Однако возможно получение и еще более чистого металла, который используется в технических целях.
Применение
Механические свойства алюминия не столь хороши, чтобы применять его в чистом виде. Поэтому чаще всего используются сплавы на основе данного вещества. Таких много, можно назвать самые основные.
- Дюралюминий.
- Алюминиево-марганцевые.
- Алюминиево-магниевые.
- Алюминиево-медные.
- Силумины.
- Авиаль.
Основное их отличие – это, естественно, сторонние добавки. Во всех основу составляет именно алюминий. Другие же металлы делают материал более прочным, стойким к коррозии, износоустойчивым и податливым в обработке.
Можно назвать несколько основных областей применения алюминия как в чистом виде, так и в виде его соединений (сплавов).
- Для изготовления проволоки и фольги, используемой в быту.

- Изготовление посуды.
- Самолетостроение.
- Кораблестроение.
- Строительство и архитектура.
- Космическая промышленность.
- Создание реакторов.
Вместе с железом и его сплавами алюминий – самый важный металл. Именно эти два представителя периодической системы нашли самое обширное промышленное применение в руках человека.
Свойства гидроксида алюминия
Гидроксид – самое распространенное соединение, которое образует алюминий. Свойства химические его такие же, как и у самого металла, – он амфотерный. Это значит, что он способен проявлять двойственную природу, вступая в реакции как с кислотами, так и со щелочами.
Сам по себе гидроксид алюминия – это белый студенистый осадок. Получить его легко при взаимодействии соли алюминия с щелочью или гидроксидом аммония. При взаимодействии с кислотами данный гидроксид дает обычную соответствующую соль и воду. Если же реакция идет с щелочью, то формируются гидроксокомплексы алюминия, в которых его координационное число равно 4. Пример: Na[Al(OH)4] – тетрагидроксоалюминат натрия.
Пример: Na[Al(OH)4] – тетрагидроксоалюминат натрия.
Физические свойства алюминия | Всё о красках
Алюминий принадлежит основной группе III периодической системы, его атомное число 13, а атомный вес 26.9815. Алюминий характеризуется гранецентрированной кубической структурой кристалла. Основные физические свойства очищенного алюминия показаны в таблице.
Физические свойства алюминия
(Если иное не указано отдельно, все данные приведены для очищенного алюминия (чистота 99.99%) при температуре 20°C)
| Химический символ | Al | |
| Атомное число | 13 | |
| Относительная атомная масса (атомный вес) | 26.98154 | |
| Атомный объем | 9.996 106 | м3/моль |
| Конфигурация электрона (квантовое состояние) | Модель БораK shell 2eL shell 8eM shell 3e | Основная модель1s22s22p63s23p1 |
| Кристаллическая решетка | fсс | Структура типа A1 |
| Плотность упаковки | 74% | |
| Координационное число | 12 | |
| Постоянная кристаллической решетки | 0. 40496 40496 | нм |
| Энергия дефекта упаковки | 200 107 | Дж/см2 |
| Минимальное межатомное расстояние | 0.28635 | нм |
| Плотность | 2.6989 | г/cm3 или кг/дм3 |
| Изменение объема при переходе из жидкого состояния в твердое (усадка) | 6.5 | % |
| Линейная усадка при литье при температуре от 660°C (933 K) до 20°C (293 K) | 1.85 | % |
| Средний линейный коэффициент расширения при температуре от 20°C (293K) до 100°C (373K) | 236 106 | 1/K |
| модуль Юнга | 66.6 | ГПа или кН/мм2 |
| модуль сдвига | 25.0 | ГПа или кН/мм2 |
| коэффициент Пуассона | 0.35 | |
| Сжимаемость | 13.3 | мм2/MN |
| Точка плавления | 660. 2 2 | °C |
| Латентная теплота плавления | 390 | кДж/кг |
| Точка кипения | -2500 | °C |
| Латентная теплота испарения | 11 4 | МДж/кг |
| Давление пара при 660°C (933 K) при 1200°C (1473 K) | – 108-109~102 | мБармБар |
| Удельная теплота при постоянном давлении | 0.89 | кДж/кг K |
| Постоянная температуры (дебаевская температура) | 440 | K |
| Энергия активации самодиффузии | 120 | кДж/моль |
| Электропроводность | 37.67= 64.95% | м/W мм2% IACS |
| Электрическое удельное сопротивление | 26.55 | нW м |
| Температурный коэффициент электрического удельного сопротивления | + 0.115 | нW м/K |
| температура (фазового) перехода суперпроводимости | 1.2 | K |
| теплопроводность | 235 | Ватт/м K |
| Число Лоренца | 2. 1 108 1 108 | (Ватт W)/K2 |
| Удельная магнитная восприимчивость (определенная рационально) | 7.7 109 | м3/кг |
| Термоэлектрическая сила по отношению к платине | 4 | Дж В/K |
| Постоянная Холла | -35 1012 | м3/C |
| Поверхностное натяжение при температуре 660°C (933K) | 0.86 | Н/м |
| Динамическая вязкость при температуре 700°C (973K) | 1.1 | мН с/м2 |
| Теплота сгорания | 31 | МДж/кг |
| Стандартный потенциал электрода | -1.67 | В |
| Стандартный потенциал электрода в NaCI-H202 по отношению к электроду из каломели 0,1N | 0.87 | В |
| Электрохимический эквивалент AI3+ | 9.32 105 | г/С |
| Сечение захвата медленных нейтронов (2200м/сек) | 0. 20 1024 20 1024 | см2/атом |
Большинство данных свойств являются постоянными (например, атомный вес). Некоторые свойства зависят от внешних условий, например температуры (плотность и удельная теплота), многие свойства зависят от легирующих добавок и структурных изменений (например, теплопроводность). Рассмотрим более подробно те свойства, для которых такая зависимость имеет решающее значение.
Алюминий играет важную роль во многих отраслях промышленности именно благодаря его физическим свойствам. Одним из важнейших свойств является низкий уровень плотности, который делает алюминий наиболее подходящим материалом, который является экономичным и экологически чистым. Плотность серийно выпускаемых материалов на базе алюминия составляет от 2.6 до 2.8г/см3 (2.7г/см3 – беспримесный алюминий), это всего лишь третья часть плотности стали. Алюминий при этом еще более выигрывает по сравнению с тяжелыми металлами. Алюминий принадлежит к так называемым легким металлам, максимальная плотность которых составляет 4.
Низкая плотность позволяет значительно сократить вес оборудования для грузоперевозок, например, транспортных средств для наземных, морских и воздушных перевозок, контейнеров, которые постоянно используются для организации перевозок. В механическом машиностроении уменьшение веса приводит к значительному сокращению потребления энергии, а также затрат на организацию производства и технического обслуживания. Даже в стационарном оборудовании сокращение веса позволяет уменьшить требования к фундаменту и несущим структурам.
Плотность зависит от температуры, уменьшаясь при повышении температуры благодаря термическом расширению. При затвердении имеет место явление усадки в размере 6.5%, которое также вызывает повышение плотности от 2.37г/см3 в жидком состоянии при температуре 660°C до 2.55г/см3 в твердом состоянии при той же температуре. Усадка приводит к образованию пустот при затвердении алюминиевых литейных форм.
Коэффициент термического расширения очищенного алюминия (AI99.99) для различных диапазонов температур
| Температурный диапазон, °C | Средний линейный коэффициент термического расширения 106 1/K |
| 200- 20 | 180 |
| 150-20 | 199 |
| 100-20 | 210 |
| 50-20 | 218 |
| 20-100 | 236 |
| 20-200 | 245 |
| 20-300 | 255 |
| 20-400 | 264 |
| 20-500 | 274 |
| 20 – 600 | 285 |
Какой металл лучше всего подходит для вашего продукта?
Выбор основного материала для вашего проекта является жизненно важным решением, и вы должны тщательно взвесить варианты. Но с таким большим выбором поиск идеального материала может стать ошеломляющим.
Если вы находитесь в процессе разработки металлического изделия, сталь и алюминий, вероятно, приходили вам в голову в качестве возможных металлов для использования. Это неудивительно, поскольку это два наиболее широко производимых металла в мире.
Это неудивительно, поскольку это два наиболее широко производимых металла в мире.
В этой статье сравниваются некоторые основные свойства стали и алюминия и упоминаются некоторые типичные области применения каждого из них.
Содержание
Алюминий и сталь: факторы, которые следует учитывать
Несмотря на то, что существует множество различных сталей и алюминиевых сплавов, каждый из которых обладает своими специфическими свойствами, между этими двумя металлами есть некоторые ключевые различия. В этом разделе сравниваются некоторые из наиболее важных физических характеристик стали и алюминия.
Вес
Если вы спросите кого-нибудь, какой металл легче, большинство людей правильно ответят: алюминий. Высокая прочность стали достигается за счет гораздо более высокой плотности. На самом деле, для двух кусков одинакового объема сталь может быть в три раза тяжелее алюминия.
Прочность
Прочность часто является одним из первых свойств, учитываемых при выборе материала, особенно в условиях высоких нагрузок. Вообще говоря, сталь прочнее алюминия. Тем не менее, если учесть в уравнении более легкий вес алюминия, алюминий выходит на первое место с превосходным соотношением прочности к весу.
Вообще говоря, сталь прочнее алюминия. Тем не менее, если учесть в уравнении более легкий вес алюминия, алюминий выходит на первое место с превосходным соотношением прочности к весу.
Определение того, какой металл имеет лучшую прочность для вашего применения, будет зависеть от гибкости вашей конструкции. Например, более крупная алюминиевая деталь может обеспечить большую прочность при меньшем весе, чем стальная альтернатива.
Пластичность
Другим недостатком высокой прочности стали является то, что ей труднее придавать различные формы, чем алюминию, особенно сложной формы. Это можно в некоторой степени преодолеть, нагрев сталь до очень высоких температур, но это увеличивает стоимость и может ухудшить другие свойства. С другой стороны, алюминий относительно легко формуется как в холодном, так и в горячем состоянии, и он идеально подходит для производственных процессов, таких как экструзия и прокатка.
Теплопроводность
Алюминий, как правило, является гораздо лучшим проводником тепла, чем сталь, и часто используется в приложениях, где требуется рассеивание или распределение тепла, например, в радиаторах.
Коррозионная стойкость
Обычная углеродистая сталь имеет плохую коррозионную стойкость. Он легко ржавеет и будет продолжать разъедать при воздействии элементов. Алюминий, с другой стороны, образует на своей поверхности защитный оксидный слой, который действует как инертный барьер против дальнейшего окисления. Пока алюминий не подвергается воздействию окружающей среды, вызывающей его разрушение, он будет продолжать обеспечивать превосходную коррозионную стойкость.
Стоит отметить, что сталь можно сделать очень устойчивой к коррозии, если в ее легирующие элементы будет включено не менее 11% хрома, что делает ее «нержавеющей сталью». Однако нержавеющая сталь дороже, чем обычная углеродистая сталь, и это может повлиять на другие физические свойства стали.
Стоимость
Стоимость материала, естественно, будет важным фактором, который вы выберете для своего проекта. Поскольку цена на оба этих металла будет колебаться в зависимости от рынка и конкретного сплава, трудно сказать, что один из них будет дешевле другого в каждом контексте. Однако общепризнано, что углеродистая сталь в пересчете на фунт обычно дешевле, чем сопоставимый алюминиевый сплав.
Однако общепризнано, что углеродистая сталь в пересчете на фунт обычно дешевле, чем сопоставимый алюминиевый сплав.
Сравнение физических свойств
В следующей таблице сравниваются конкретные значения физических свойств стали и алюминия. Для этой цели мы сравнили среднеуглеродистую сталь и обычный алюминиевый сплав.
| Собственность | Среднеуглеродистая сталь | Общий алюминиевый сплав |
|---|---|---|
| Плотность | 7,75 – 7,89 г/куб.см | 0,0160 – 3,63 г/куб.см |
| Предел текучести при растяжении | 245 – 1740 МПа | 1,24 – 730 МПа |
| Коррозионная стойкость | Плохой | От хорошего до отличного |
| Теплопроводность | 21,9 – 52,0 Вт/м-К | 1,48 – 255 Вт/м-К |
| Пластичность | От умеренного до хорошего | От хорошего до отличного |
Применение для алюминия и стали
При выборе между сталью и алюминием для вашего конкретного проекта знание общих областей применения каждого из них может быть очень полезным.
| Промышленность | Сталь | Алюминий |
|---|---|---|
| Инфраструктура | • Стальная арматура в бетонных конструкциях, таких как мосты и парки • Стальные опоры и балки | • Архитектурные и отделочные работы, такие как боковые панели • Оконные и дверные рамы, желоба и перила |
| Механическое оборудование | • Тракторы, бульдозеры и краны • Прокатные станы • Ручные инструменты, такие как молотки и лопаты | • Трубопровод • Некоторые резервуары для хранения |
| Транспорт | • Рамы автомобилей • Приводы • Подвески | • Фюзеляж, крылья и опорная конструкция самолета • Кузов автомобиля и колеса • Автомобильные двигатели |
| Бытовая техника | • Стиральные машины и сушилки • Духовки | • Корпуса и рамы приборов • Кофеварки и миксеры |
| Спортивное оборудование | • Снаряжение для скалолазания • Головки клюшек для гольфа • Велосипедные цепи, зубья и тросы • Оборудование для тяжелой атлетики | • Велосипедные рамы, колеса и руль • Лыжные палки • Бейсбольные биты |
Что выбрать: сталь или алюминий для вашего проекта?
Выбор стали или алюминия для вашего проекта в конечном итоге будет зависеть от характеристик вашего проекта, процесса формования и вашего бюджета. Например, если прочность и долговечность являются наиболее важными атрибутами вашей конструкции, а форма не слишком сложна, возможно, лучшим вариантом будет стальной сплав. С другой стороны, если вам нужно хорошее соотношение прочности и веса, коррозионная стойкость и способность формировать уникальную форму, алюминий, вероятно, является лучшим выбором.
Например, если прочность и долговечность являются наиболее важными атрибутами вашей конструкции, а форма не слишком сложна, возможно, лучшим вариантом будет стальной сплав. С другой стороны, если вам нужно хорошее соотношение прочности и веса, коррозионная стойкость и способность формировать уникальную форму, алюминий, вероятно, является лучшим выбором.
Если вы хотите узнать больше о некоторых из наиболее широко используемых алюминиевых сплавов, ознакомьтесь с другими нашими статьями ниже:
- Алюминиевый сплав 6061
- Алюминиевый сплав 6063
- Алюминиевый сплав 2024
- Алюминиевый сплав 7075
Если вы хотите узнать больше о наиболее распространенных процессах производства алюминия, см. следующие материалы:
➨ Какой процесс производства алюминия лучше всего подходит для вашего проекта?
Общие свойства алюминия и алюминиевых сплавов
Алюминий
Алюминий является наиболее широко используемым цветным металлом, уступая в мировом потреблении только стали. Алюминий производится как в «чистом», так и в легированном виде. В продаже имеется алюминий с чистотой до 99,8%. Наиболее распространенными легирующими элементами являются медь, кремний, магний, марганец и цинк в различных количествах до примерно 5%. Основными преимуществами алюминия являются его низкая плотность, хорошее отношение прочности к массе (КСВ), пластичность, отличная обрабатываемость, литейность и свариваемость, коррозионная стойкость, высокая проводимость и разумная стоимость. По сравнению со сталью он на 1/3 плотнее (0,10 фунта/дюйм3 по сравнению с 0,28 фунта/дюйм3), примерно на 1/3 жестче (E = 10,3 МПа {71 ГПа} по сравнению с 30 МПа {207 ГПа}) и в целом менее прочен. . Если сравнить прочность низкоуглеродистой стали и чистого алюминия, сталь примерно в три раза прочнее. Таким образом, удельная прочность в этом сравнении примерно одинакова. Однако чистый алюминий редко используется в технике. Он слишком мягкий и слабый. Основными преимуществами чистого алюминия являются его блестящая отделка и хорошая коррозионная стойкость.
Алюминий производится как в «чистом», так и в легированном виде. В продаже имеется алюминий с чистотой до 99,8%. Наиболее распространенными легирующими элементами являются медь, кремний, магний, марганец и цинк в различных количествах до примерно 5%. Основными преимуществами алюминия являются его низкая плотность, хорошее отношение прочности к массе (КСВ), пластичность, отличная обрабатываемость, литейность и свариваемость, коррозионная стойкость, высокая проводимость и разумная стоимость. По сравнению со сталью он на 1/3 плотнее (0,10 фунта/дюйм3 по сравнению с 0,28 фунта/дюйм3), примерно на 1/3 жестче (E = 10,3 МПа {71 ГПа} по сравнению с 30 МПа {207 ГПа}) и в целом менее прочен. . Если сравнить прочность низкоуглеродистой стали и чистого алюминия, сталь примерно в три раза прочнее. Таким образом, удельная прочность в этом сравнении примерно одинакова. Однако чистый алюминий редко используется в технике. Он слишком мягкий и слабый. Основными преимуществами чистого алюминия являются его блестящая отделка и хорошая коррозионная стойкость. Используется в основном в декоративных целях.
Используется в основном в декоративных целях.
Алюминиевые сплавы обладают значительно большей прочностью, чем чистый алюминий, и широко используются в машиностроении, в частности в авиационной и автомобильной промышленности. Более высокопрочные алюминиевые сплавы имеют предел прочности при растяжении в диапазоне от 70 до 90 тысяч фунтов на квадратный дюйм (от 480 до 620 МПа) и предел текучести примерно в два раза выше, чем у мягкой стали. По удельной прочности они выгодно отличаются от среднеуглеродистых сталей. Алюминий успешно конкурирует со сталью в некоторых областях применения, хотя немногие материалы могут превзойти сталь, если требуется очень высокая прочность. На рис. 1 показаны кривые напряжения-деформации, полученные при испытаниях на растяжение для трех алюминиевых сплавов. Прочность алюминия снижается как при низких, так и при повышенных температурах.
| Рис. 1. Кривые напряжения-деформации при испытании на растяжение для трех алюминиевых сплавов |
Некоторые алюминиевые сплавы упрочняются термической обработкой, а другие – деформационным упрочнением или осаждением и старением. Высокопрочные алюминиевые сплавы примерно в 1,5 раза тверже мягкой стали, а обработка поверхности, такая как твердое анодирование, может сделать поверхность более твердой, чем самая твердая сталь.
Высокопрочные алюминиевые сплавы примерно в 1,5 раза тверже мягкой стали, а обработка поверхности, такая как твердое анодирование, может сделать поверхность более твердой, чем самая твердая сталь.
Алюминий является одним из наиболее легко обрабатываемых конструкционных материалов, хотя он имеет тенденцию к затвердеванию. Он отливает, обрабатывает, сваривает (тепло сварки вызывает локальный отжиг, который может устранить желательные эффекты упрочнения при холодной обработке или термической обработке любого металла) и легко формуется в горячем и холодном состоянии. Его также можно экструдировать. Сплавы специально разработаны как для литья в песчаные формы, так и для литья под давлением, а также для кованых и экструдированных профилей и кованых деталей.
АЛЮМИНИЕВЫЕ СПЛАВЫ ДЕФОРМАЦИИ доступны в широком ассортименте стандартных форм, таких как двутавровые балки, уголки, швеллеры, стержни, полосы, листы, круги и трубы. Экструзия также позволяет создавать относительно недорогие нестандартные формы. Система нумерации сплавов по алюминиевой ассоциации показана в таблице 1. Первая цифра указывает на основной легирующий элемент и определяет серию. Твердость обозначается суффиксом, содержащим букву и до 3 цифр, как указано в таблице. Наиболее распространенными и наиболее часто используемыми алюминиевыми сплавами в машиностроении являются сплавы серий 2000 и 6000.
Система нумерации сплавов по алюминиевой ассоциации показана в таблице 1. Первая цифра указывает на основной легирующий элемент и определяет серию. Твердость обозначается суффиксом, содержащим букву и до 3 цифр, как указано в таблице. Наиболее распространенными и наиболее часто используемыми алюминиевыми сплавами в машиностроении являются сплавы серий 2000 и 6000.
Самый старый алюминиевый сплав 2024, который содержит 4,5% меди, 1,5% магния и 0,8% марганца. Он является одним из наиболее поддающихся механической обработке алюминиевых сплавов и поддается термообработке. В более высоких состояниях, таких как -T3 и -T4, он имеет предел прочности при растяжении, приближающийся к 70 kpsi (483 МПа), что также делает его одним из самых прочных алюминиевых сплавов. Он также имеет высокую усталостную прочность. Однако он имеет плохую свариваемость и формуемость по сравнению с другими алюминиевыми сплавами.
Сплав 6061 содержит 0,6 % кремния, 0,27 % меди, 1,0 % марганца и 0,2 % хрома. Он широко используется в конструкционных приложениях из-за его превосходной свариваемости. Его прочность составляет от 40 до 45 килофунтов на квадратный дюйм (от 276 до 310 МПа) в более высоких состояниях. Он имеет более низкую усталостную прочность, чем алюминий 2024. Он легко обрабатывается и является популярным сплавом для экструзии, которая представляет собой процесс горячей штамповки. 98 циклов. Некоторые сплавы также доступны в форме alclad , которая связывает тонкий слой чистого алюминия с одной или обеих сторон для повышения коррозионной стойкости.
Его прочность составляет от 40 до 45 килофунтов на квадратный дюйм (от 276 до 310 МПа) в более высоких состояниях. Он имеет более низкую усталостную прочность, чем алюминий 2024. Он легко обрабатывается и является популярным сплавом для экструзии, которая представляет собой процесс горячей штамповки. 98 циклов. Некоторые сплавы также доступны в форме alclad , которая связывает тонкий слой чистого алюминия с одной или обеих сторон для повышения коррозионной стойкости.
| Некоторые из них поддаются закалке, но их прочность и пластичность меньше, чем у деформируемых сплавов. Доступны сплавы для литья в песчаные формы, литья под давлением или литья по выплавляемым моделям. Титан Несмотря на то, что он был открыт как элемент в 1791 году, серийно производимый титан стал доступен только с 1940-х годов, поэтому он является одним из новейших технических металлов. В некоторых случаях титан может стать ответом на молитву инженера.
Comparison стали с алюминием – IspatGuruСравнение стали с алюминием
Сравнение стали с алюминием Сталь представляет собой сплав железа и других элементов, прежде всего углерода. Чаще всего его получают путем восстановления железной руды. Рис. 1 Процесс производства стали Сталь широко используется в строительстве и других областях благодаря ее высокой прочности на растяжение и низкой стоимости. Различия в химическом составе сталей являются причиной большого разнообразия марок и свойств стали. Каждый элемент, который добавляется к основному составу стали, оказывает некоторое влияние на свойства стали и на то, как эта сталь реагирует на процессы обработки и изготовления сталей. Химический состав стали также определяет поведение стали в различных средах. Стандарты на сталь определяют пределы состава, качества и рабочих параметров для различных марок стали. Железо — химический элемент с символом Fe (от латинского: ferrum) и атомным номером 26. Это металл первой переходной серии. По массе это самый распространенный элемент на Земле, образующий большую часть внешнего и внутреннего ядра Земли. Алюминий, редкий и дорогой сто лет назад, с тех пор считается самым распространенным металлом на Земле, составляющим около 8 % земной коры. Это третий по распространенности известный элемент. Только кислород и кремний существуют в больших количествах. Алюминий — это элемент, который содержится в земной коре. Он не растворяется в воде и имеет цвет от серебристого до тускло-серого. Алюминий по своей природе мягкий, прочный, легкий, немагнитный и пластичный, а поскольку в чистом виде он обладает высокой реакционной способностью, в комбинированном виде он встречается более чем в 270 различных минералах. Наиболее распространенным минералом для алюминия является боксит. В настоящее время алюминий производят из минерального боксита (рис. 2). Бокситы превращаются в оксид алюминия (глинозем) с помощью процесса Байера. Затем глинозем преобразуется в металлический алюминий с использованием электролизеров по процессу Холла-Эру. Электролитический процесс производства алюминия был открыт в 1890 году. Рис. 2 Процесс производства алюминия Элемент алюминия, химический символ Al, имеет атомный номер 13. атом состоит из 13 электронов, каждый из которых имеет единичный отрицательный электрический заряд, расположенных на трех орбитах вокруг высококонцентрированного ядра, имеющего положительный заряд 13. Из-за своей низкой плотности и высокой коррозионной стойкости алюминий чаще всего используется в транспортных средствах, аэрокосмической промышленности и конструкционных материалах. Также из-за своей реактивной природы он используется в качестве катализатора или добавки во взрывчатые вещества. Алюминий также используется в предметах домашнего обихода, таких как посуда и упаковка (алюминиевая фольга). Использование алюминия также полезно при производстве автомобилей, поскольку считается, что он имеет лучшее соотношение веса и прочности. Алюминий также является хорошим отражателем и хорошим проводником электричества. Он также имеет примерно одну треть плотности и жесткости стали и может легко подвергаться механической обработке, литью, волочению и экструзии. Хотя алюминий широко используется в конструкциях планера и все чаще используется в автомобильных рамах для снижения веса и повышения эффективности использования топлива, он не нашел широкого применения в качестве гражданского конструкционного материала. Сталь и алюминий являются обычными веществами, которые используются в повседневной жизни и почти во всем, что используется сегодня. В то время как сталь является самым популярным сплавом, алюминий является самым распространенным металлом на земле. Ежегодно в мире производится алюминий, уступающий только стали. Хотя эти два используются в аналогичных приложениях, они полностью отличаются друг от друга. Сталь и алюминий являются универсальными металлами. Эти материалы имеют свои преимущества и недостатки. За последние несколько десятилетий были достигнуты успехи в производстве стали и алюминия. Сталь и алюминий – два самых популярных материала, используемых в различных областях. Сейчас они используются более широко, чем когда-либо. Они представлены в широком ассортименте продукции, от банок для напитков до транспортных средств и зданий. Каждый материал имеет определенный и отличный набор характеристик, которые делают его подходящим или неподходящим материалом для работы. Сравнение свойств стали и алюминия
В случае алюминия коэффициент теплового расширения является нелинейным в диапазоне от минус 200°С до плюс 600°С, но для практических целей считается постоянным в диапазоне температур от 20°С до 100°С C. На коэффициент теплового расширения сплавов влияет природа их компонентов. Присутствие кремния и меди уменьшает расширение, а магния увеличивает его. Для обычных алюминиевых сплавов, используемых в промышленности, коэффициент расширения варьируется от 0,0000235/K для алюминиевого сплава с 4,6 % Cu до 0,0000245/K для алюминиевого сплава с 4,5 % Mg, т. е. в два раза больше, чем у стали. Для стали это 0,000012/К. Дифференциальный коэффициент расширения необходимо учитывать, когда алюминий используется в сочетании с другими материалами, напр. большие алюминиевые/стальные конструкции. Однако возникающие напряжения сдерживаются низким модулем упругости алюминия, который составляет одну треть от модуля упругости стали. Только там, где размеры действительно велики, а элементы конструкции тонкие (нестабильные в боковом направлении), соединение со сталью создает проблему дифференциального расширения. Другой формой изменения размеров, которая не влияет непосредственно на пользователя алюминия, но важна при производстве отливок, является сжатие металла при затвердевании; это зависит от сплава и составляет от 1 % до 2 % (сравнительные данные для стали составляют 2 %). Исследование Массачусетского технологического института и соответствующие модели затрат показывают, что алюминий значительно дороже стали. Например, (i) производство алюминия в два-три раза дороже, чем стали, (ii) производство и сборка алюминия на 20–30 % дороже, чем стали, и (iii) снижение массы стали может быть достигнуто при почти нулевая стоимость, в то время как инженерные исследования показывают, что материалы с низкой плотностью, такие как алюминий, обходятся инженерам в определенные деньги за килограмм экономии веса. Годовой мировой спрос на алюминий примерно на 75 % удовлетворяется за счет свежевыплавленного алюминия и на 25 % за счет переработанного алюминиевого лома. Использование переработанного алюминия экономически и экологически выгодно. Для производства 1 тонны нового алюминия требуется 14 000 кВтч. И наоборот, для переплавки и переработки одной тонны алюминия требуется всего 5 %. Нет никакой разницы в качестве между первичным и переработанным алюминием и его сплавами. В случае стали более 33 % мирового спроса на сталь удовлетворяется за счет переработанной стали. Переработка стали обеспечивает значительную экономию сырья и энергии. На тонну используемого стального лома экономится более 1200 кг железной руды, 7 кг угля и 51 кг известняка. С экологической точки зрения переработка стали оказывает огромное влияние на сокращение выбросов CO2. Если 1 тонна горячекатаной стали производится из 100 % лома, а не из новых материалов, общая экономия CO2 составляет примерно 1,8 тонны. Чистый алюминий мягкий, пластичный и устойчивый к коррозии. Обладает высокой электропроводностью. Он широко используется для фольги и проводящих кабелей, но для обеспечения более высокой прочности, необходимой для других применений, необходимо легирование другими элементами. Алюминий – один из самых легких инженерных металлов, соотношение прочности и веса которого выше, чем у стали. Благодаря использованию различных комбинаций своих преимущественных свойств, таких как прочность, легкость, коррозионная стойкость, пригодность для повторного использования и формуемость, алюминий используется во все большем числе областей применения. Ассортимент продукции варьируется от конструкционных материалов до тонкой упаковочной пленки. Как и сталь, алюминий может быть сильно деформирован без разрушения. Это позволяет формовать алюминий прокаткой, экструзией, волочением, механической обработкой и другими механическими процессами. Сталь производится путем обработки железа в процессе, известном как плавка, при котором железо извлекается из железной руды и удаляется избыток кислорода, а железо соединяется с химическими компонентами, такими как углерод. Сталь по сравнению с чистым железом более устойчива к ржавчине и имеет лучшую свариваемость. Другие металлы добавляются в смесь железа и углерода, чтобы повлиять на свойства стали. Такие металлы, как никель и марганец, повышают прочность стали на растяжение и делают аустенитную форму железо-углеродистого раствора более химически стабильной, а хром может повышать твердость и температуру плавления. По сравнению с алюминием сталь очень пластична. Сталь – один из самых распространенных сплавов в современном мире. Он используется в различных областях, таких как инструменты, посуда, бытовая техника, транспорт, оружие, аэрокосмическая промышленность, здания, инфраструктура и т. Алюминий является основой аэрокосмической промышленности, используется для приготовления пищи и упаковки, помогает в производстве полностью спокойной стали и является основой для универсальной краски. Алюминий — легкий и привлекательный металл, демонстрирующий высокую степень коррозионной стойкости в обычных агрессивных средах. Он также мягкий, твердый, легко поддается сварке, трудно поддается сварке и имеет множество других, казалось бы, противоречивых характеристик. Если это звучит запутанно, это так. Свойства конкретного алюминиевого изделия зависят от выбранного сплава. Термин алюминий относится к семейству сплавов. Знание этих сплавов является ключом к эффективному использованию алюминия. Сталь тверже алюминия. Большинство закаленных сплавов и сплавов алюминия легче вмятины, вмятины или царапины по сравнению со сталью. Сталь прочна и с меньшей вероятностью деформируется, деформируется или изгибается под действием веса, силы или тепла. Алюминий – более легкий металл по плотности. Однако, поскольку он не может выдержать такое же напряжение, как сталь, обычно приходится использовать его больше, иногда до такой степени, что разница в стоимости сводится на нет. Иногда алюминий дешевле. Если кто-то ищет антикоррозионный металл, то алюминий дешевле нержавеющей стали. Однако по сравнению с базовой сталью она часто стоит дороже. Натуральные антикоррозионные свойства алюминия — одна из его лучших характеристик. Алюминий не гнется и не гнется так сильно, как сталь, а это означает, что он более склонен к поломке. Он также не поглощает вибрации так хорошо, как сталь, что может быть как хорошо, так и плохо в зависимости от ситуации. Сталь известна своей прочностью и весом. Из-за того, насколько он жесткий, часто можно использовать меньше, частично сводя на нет вес. С ним может быть немного сложнее работать, но как только он будет установлен на место и в форму, можно ожидать, что он останется таким. Как и большинство металлов, алюминий и сталь можно плавить, отливать, формовать и обрабатывать в различных формах. Сталь имеет преимущество перед алюминием в формуемости; алюминий имеет меньший диапазон деформации, чем сталь. Также, как и большинство металлов, алюминий и сталь могут проводить электричество. Алюминий не токсичен, что делает его идеальным для упаковки пищевых продуктов. Оба материала на 100 % подлежат вторичной переработке. Алюминий естественным образом образует защитное оксидное покрытие, которое делает его устойчивым к коррозии. Алюминий — хороший проводник тепла и электричества; он также в два раза лучший проводник, чем медь. Алюминий является хорошим отражателем света и тепла, что делает его идеальным для использования в производстве отражателей. Этот материал пластичен с низкой температурой плавления и плотностью. Материалы, на которые не воздействуют магнитные поля, считаются «немагнитными». Алюминий — это металл, который считается немагнитным; на него не действуют магнитные поля. Сталь, с другой стороны, является магнитной, поскольку на нее воздействуют магнитные поля. Оба материала пригодны для вторичной переработки, но магнитные свойства стали значительно облегчают ее отделение от других веществ в процессе переработки. Алюминий намного легче стали. Легкий вес алюминия делает его легче и эффективнее в обработке, чем сталь. Алюминий имеет более низкую температуру плавления, чем сталь, что также облегчает его обработку. Усталостные характеристики алюминия вдвое меньше, чем у стали, что является преимуществом стали перед алюминием в долговечности автомобиля. Оба типа металлов имеют бесчисленное множество применений. Сталь и алюминий используются в судостроении, автомобилестроении, производстве пресс-форм, машиностроении и многих других. Сходства алюминия и стали заключаются в том, что (i) конструкционные применения алюминия и стали в основном аналогичны, (ii) проблемы/процессы проектирования схожи, поэтому используется идентичный подход, (iii) правила проектирования для алюминия и стали одинаковы намеренно очень похожи. Однако существуют важные различия как в физических, так и в механических свойствах, которые необходимо учитывать в процессе проектирования. Различия в свойствах, последствия для поведения конструкции и способы решения этой проблемы при проектировании конструкции описаны ниже. Прежде всего, низкая плотность алюминия является основной причиной его использования во многих конструкциях. Высокое отношение прочности к весу является причиной номер один для развития авиационной промышленности. Хотя его небольшой вес является благоприятным свойством, в некоторых случаях он может быть недостатком; например, при циклическом нагружении отношение временной нагрузки к статической нагрузке невыгодно по сравнению со сталью, поэтому усталость необходимо учитывать на ранней стадии проектирования. Низкая плотность делает алюминиевую конструкцию склонной к вибрации, и в этих случаях необходимо учитывать динамическое поведение конструкции. Модуль Юнга важен для структурного поведения. Его стоимость составляет примерно одну треть от стоимости стали, но, в отличие от плотности, это недостаток по сравнению со сталью. Низкое значение модуля Юнга оказывает большое влияние на деформации алюминиевой конструкции. Хорошо известным примером является изгиб балок, где решающим фактором является жесткость. Вышеизложенное указывает на то, что при проектировании алюминиевых конструкций зачастую определяющим фактором является не прочность, а во многих случаях деформация. Таким образом, в строительстве и гражданском строительстве часто приходится учитывать сплав, который не обладает самой высокой прочностью. Низкий модуль Юнга также отвечает за более высокую чувствительность к проблемам устойчивости алюминиевых конструкций (выпучивание). Критическое напряжение для потери устойчивости линейно связано с модулем Юнга. |


 Он имеет верхний предел рабочей температуры от 1200 до 1400°F (от 650 до 750°C), весит в два раза меньше, чем сталь (0,16 фунта/дюйм3 {4429 кг/м3}), и по прочности не уступает стали средней прочности. (обычно 135 кфунтов на дюйм {930 МПа}). Его модуль Юнга составляет от 16 до 18 МПа (от 110 до 124 ГПа), или около 60% от модуля стали. Его удельная прочность приближается к прочности самых прочных легированных сталей и превышает удельную прочность сталей средней прочности в 2 раза. Его удельная жесткость больше, чем у стали, что делает его таким же или лучшим в отношении предельных прогибов. Он также немагнитен. Титан очень устойчив к коррозии и нетоксичен, что позволяет использовать его в контакте с кислыми или щелочными пищевыми продуктами и химическими веществами, а также в организме человека, например, в качестве замены сердечных клапанов и тазобедренных суставов. К сожалению, это дорого по сравнению с алюминием и сталью. Он находит широкое применение в аэрокосмической промышленности, особенно в конструкциях военных самолетов и реактивных двигателей, где требуются прочность, малый вес, устойчивость к высоким температурам и коррозии.
Он имеет верхний предел рабочей температуры от 1200 до 1400°F (от 650 до 750°C), весит в два раза меньше, чем сталь (0,16 фунта/дюйм3 {4429 кг/м3}), и по прочности не уступает стали средней прочности. (обычно 135 кфунтов на дюйм {930 МПа}). Его модуль Юнга составляет от 16 до 18 МПа (от 110 до 124 ГПа), или около 60% от модуля стали. Его удельная прочность приближается к прочности самых прочных легированных сталей и превышает удельную прочность сталей средней прочности в 2 раза. Его удельная жесткость больше, чем у стали, что делает его таким же или лучшим в отношении предельных прогибов. Он также немагнитен. Титан очень устойчив к коррозии и нетоксичен, что позволяет использовать его в контакте с кислыми или щелочными пищевыми продуктами и химическими веществами, а также в организме человека, например, в качестве замены сердечных клапанов и тазобедренных суставов. К сожалению, это дорого по сравнению с алюминием и сталью. Он находит широкое применение в аэрокосмической промышленности, особенно в конструкциях военных самолетов и реактивных двигателей, где требуются прочность, малый вес, устойчивость к высоким температурам и коррозии. В таблицах ниже показаны механические свойства некоторых алюминиевых сплавов.
В таблицах ниже показаны механические свойства некоторых алюминиевых сплавов. 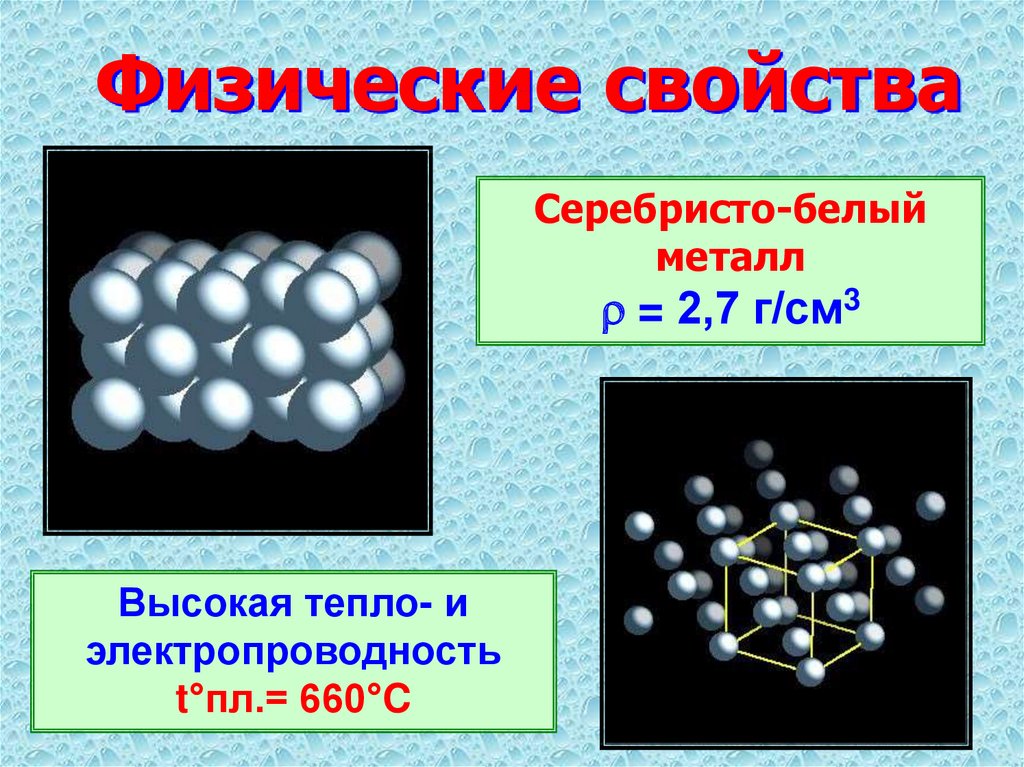 Углерод, наиболее распространенный легирующий материал в стали, действует как упрочняющий агент, предотвращая разделение и скольжение любых дислокаций в кристаллической решетке атомов железа друг относительно друга, что делает сталь более прочной. Варьируя количество легирующих элементов и форму их нахождения в стали, можно управлять такими качествами, как твердость, пластичность и предел прочности стали. Хотя известно, что сталь существует около 4000 лет назад, она не производилась широко до 17 века. Его массовое производство началось благодаря внедрению бессемеровского процесса в 1850-х годах. Этот процесс сделал производство стали более дешевым, эффективным и простым. Производство стали представляет собой двухэтапный процесс. Сначала железо получают путем восстановления железной руды. Это железо затем превращается в сталь путем окисления примесей. (Рис. 1)
Углерод, наиболее распространенный легирующий материал в стали, действует как упрочняющий агент, предотвращая разделение и скольжение любых дислокаций в кристаллической решетке атомов железа друг относительно друга, что делает сталь более прочной. Варьируя количество легирующих элементов и форму их нахождения в стали, можно управлять такими качествами, как твердость, пластичность и предел прочности стали. Хотя известно, что сталь существует около 4000 лет назад, она не производилась широко до 17 века. Его массовое производство началось благодаря внедрению бессемеровского процесса в 1850-х годах. Этот процесс сделал производство стали более дешевым, эффективным и простым. Производство стали представляет собой двухэтапный процесс. Сначала железо получают путем восстановления железной руды. Это железо затем превращается в сталь путем окисления примесей. (Рис. 1) Железо является основным компонентом стали. Состав стали в основном состоит из железа и других элементов, таких как углерод, марганец, кремний, фосфор, сера и легирующие элементы. Для легирования сталей используется большое количество элементов в широком диапазоне процентных соотношений.
Железо является основным компонентом стали. Состав стали в основном состоит из железа и других элементов, таких как углерод, марганец, кремний, фосфор, сера и легирующие элементы. Для легирования сталей используется большое количество элементов в широком диапазоне процентных соотношений. Это четвертый по распространенности элемент в земной коре. Железо обычно встречается в земной коре в виде руды, обычно оксида железа, такого как магнетит, гематит и т. д. Железо извлекается из железной руды путем удаления кислорода в сочетании с предпочтительным химическим партнером, таким как углерод, который теряется в атмосфере в виде углекислого газа.
Это четвертый по распространенности элемент в земной коре. Железо обычно встречается в земной коре в виде руды, обычно оксида железа, такого как магнетит, гематит и т. д. Железо извлекается из железной руды путем удаления кислорода в сочетании с предпочтительным химическим партнером, таким как углерод, который теряется в атмосфере в виде углекислого газа. Считалось, что алюминий использовался древними греками и римлянами в качестве красящих протрав и вяжущих средств. Только в 1808 году сэр Хамфри Дэви, британский электрохимик, установил существование алюминия, и только 17 лет спустя датский ученый Эрстед получил первую крошечную таблетку этого металла. Он был успешно извлечен в чистом виде Фридрихом Вёлером в 1827 году.0003
Считалось, что алюминий использовался древними греками и римлянами в качестве красящих протрав и вяжущих средств. Только в 1808 году сэр Хамфри Дэви, британский электрохимик, установил существование алюминия, и только 17 лет спустя датский ученый Эрстед получил первую крошечную таблетку этого металла. Он был успешно извлечен в чистом виде Фридрихом Вёлером в 1827 году.0003 Три электрона на внешней орбите придают атому алюминия валентную или химическую комбинированную способность + 3. Металл имеет атомный вес 26,9.8.
Три электрона на внешней орбите придают атому алюминия валентную или химическую комбинированную способность + 3. Металл имеет атомный вес 26,9.8.


 Сталь ферромагнитна, хотя ее магнитные свойства отличаются от железа. Железные вещества намагничиваются сравнительно быстро. Однако типы железа, включая мягкое железо, так же быстро теряют свой магнетизм. Эти характеристики особенно полезны, когда необходимы сильные, но временные магниты, такие как электромагниты. Стали требуется значительно больше времени, чтобы намагничиться, но она сохраняет свой магнетизм гораздо дольше. Это свойство, называемое высоким удерживанием, позволяет использовать сталь в качестве постоянных магнитов. Проницаемость в генри на метр углеродистой стали составляет 0,000126, а электротехнической стали – 0,005. Значения проницаемости в генри на метр для аустенитных нержавеющих сталей находятся в диапазоне 0,00000126-0,0000088, а для других нержавеющих сталей (ферритных и мартенситных) – в диапазоне 0,00005-0,00126.
Сталь ферромагнитна, хотя ее магнитные свойства отличаются от железа. Железные вещества намагничиваются сравнительно быстро. Однако типы железа, включая мягкое железо, так же быстро теряют свой магнетизм. Эти характеристики особенно полезны, когда необходимы сильные, но временные магниты, такие как электромагниты. Стали требуется значительно больше времени, чтобы намагничиться, но она сохраняет свой магнетизм гораздо дольше. Это свойство, называемое высоким удерживанием, позволяет использовать сталь в качестве постоянных магнитов. Проницаемость в генри на метр углеродистой стали составляет 0,000126, а электротехнической стали – 0,005. Значения проницаемости в генри на метр для аустенитных нержавеющих сталей находятся в диапазоне 0,00000126-0,0000088, а для других нержавеющих сталей (ферритных и мартенситных) – в диапазоне 0,00005-0,00126. Из-за низкого удельного веса массовая электропроводность чистого алюминия более чем в два раза выше, чем у отожженной меди, и выше, чем у любого другого металла. Значение электропроводности углеродистой стали (содержание углерода около 0,1 %) составляет около 12,1 % от IACS. Значение электропроводности для нержавеющей стали (18 Cr-8 Ni) составляет около 2,5 % от IACS.
Из-за низкого удельного веса массовая электропроводность чистого алюминия более чем в два раза выше, чем у отожженной меди, и выше, чем у любого другого металла. Значение электропроводности углеродистой стали (содержание углерода около 0,1 %) составляет около 12,1 % от IACS. Значение электропроводности для нержавеющей стали (18 Cr-8 Ni) составляет около 2,5 % от IACS. е. 921 Дж/кг при 100°С, что выше, чем у любого обычного металла, кроме магния. Однако в объемном отношении теплоемкость алюминия меньше, чем у любого из более тяжелых металлов. Удельная теплоемкость сталей 490-500 Дж/кг.
е. 921 Дж/кг при 100°С, что выше, чем у любого обычного металла, кроме магния. Однако в объемном отношении теплоемкость алюминия меньше, чем у любого из более тяжелых металлов. Удельная теплоемкость сталей 490-500 Дж/кг. Этот оксидный слой всегда присутствует на поверхности алюминия в атмосфере кислорода. Алюминий, однако, является очень реактивным химическим элементом, и его успешная устойчивость к коррозии зависит от полноты, с которой защитная пленка оксида алюминия предотвращает проявление этой основной активности. Сталь подвергается коррозии во многих средах, включая большинство наружных сред. Когда нелегированная или легированная сталь без защиты от коррозии подвергается воздействию атмосферы, поверхность через короткое время приобретает красновато-коричневый цвет. Этот красновато-коричневый цвет указывает на образование ржавчины и коррозию стали. При коррозии сталь окисляется с образованием ржавчины, которая занимает примерно в 6 раз больше объема исходного материала, израсходованного в процессе. Процесс коррозии начинается при воздействии на сталь агрессивной среды. Коррозия может быть либо химической коррозией, либо электрохимической коррозией. Хром обычно добавляют в сталь для повышения стойкости к окислению.
Этот оксидный слой всегда присутствует на поверхности алюминия в атмосфере кислорода. Алюминий, однако, является очень реактивным химическим элементом, и его успешная устойчивость к коррозии зависит от полноты, с которой защитная пленка оксида алюминия предотвращает проявление этой основной активности. Сталь подвергается коррозии во многих средах, включая большинство наружных сред. Когда нелегированная или легированная сталь без защиты от коррозии подвергается воздействию атмосферы, поверхность через короткое время приобретает красновато-коричневый цвет. Этот красновато-коричневый цвет указывает на образование ржавчины и коррозию стали. При коррозии сталь окисляется с образованием ржавчины, которая занимает примерно в 6 раз больше объема исходного материала, израсходованного в процессе. Процесс коррозии начинается при воздействии на сталь агрессивной среды. Коррозия может быть либо химической коррозией, либо электрохимической коррозией. Хром обычно добавляют в сталь для повышения стойкости к окислению.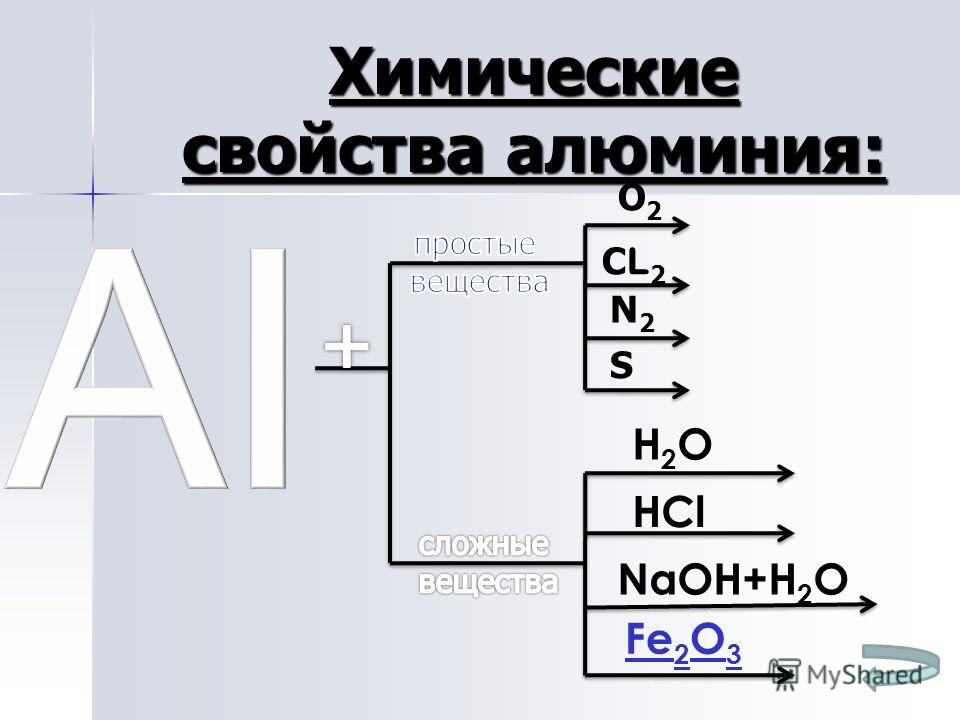 Коррозионная стойкость хромистых сталей резко возрастает при содержании хрома более 12 %. Хром образует прочный оксидный слой на поверхности стали, который предотвращает дальнейшее окисление и, таким образом, обеспечивает коррозионную стойкость сталей. Мягкие стали с содержанием меди около 0,25 % обладают улучшенной стойкостью к атмосферной коррозии. Это улучшение особенно заметно в промышленных средах, где скорость коррозии сталей, содержащих медь, может быть в два-четыре раза ниже, чем у сопоставимых углеродистых сталей. Медь также образует прочный оксидный слой на поверхности стали, который предотвращает дальнейшее окисление и, таким образом, обеспечивает коррозионную стойкость сталей.
Коррозионная стойкость хромистых сталей резко возрастает при содержании хрома более 12 %. Хром образует прочный оксидный слой на поверхности стали, который предотвращает дальнейшее окисление и, таким образом, обеспечивает коррозионную стойкость сталей. Мягкие стали с содержанием меди около 0,25 % обладают улучшенной стойкостью к атмосферной коррозии. Это улучшение особенно заметно в промышленных средах, где скорость коррозии сталей, содержащих медь, может быть в два-четыре раза ниже, чем у сопоставимых углеродистых сталей. Медь также образует прочный оксидный слой на поверхности стали, который предотвращает дальнейшее окисление и, таким образом, обеспечивает коррозионную стойкость сталей.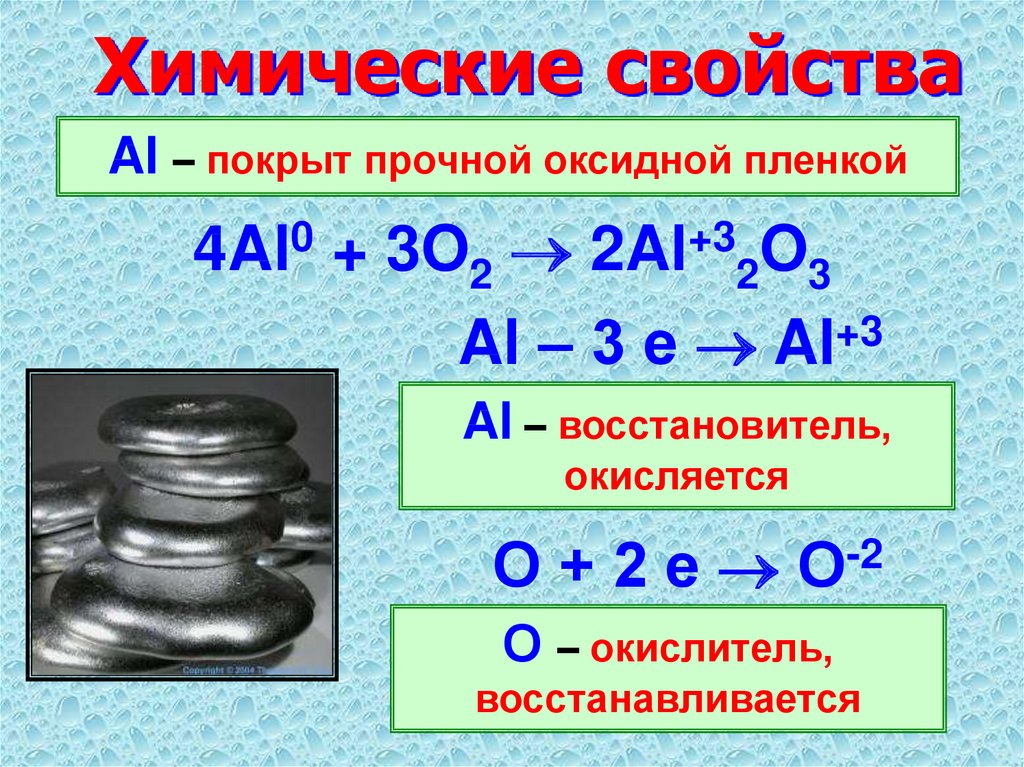
 Это применимо к навесным стенам для высотных зданий и парапетам для мостов, где длинные тонкие алюминиевые профили установлены на стальных каркасах. В этих случаях обычно необходимы скользящие швы, пластиковый герметик и другие приспособления для снятия напряжений. В случаях, когда конструкция является жесткой и маловероятной, например, алюминиевая надстройка на корабле со стальным корпусом, все соединения теперь делаются жесткими, а дифференциальное расширение принимается как сжимающее или растягивающее напряжение.
Это применимо к навесным стенам для высотных зданий и парапетам для мостов, где длинные тонкие алюминиевые профили установлены на стальных каркасах. В этих случаях обычно необходимы скользящие швы, пластиковый герметик и другие приспособления для снятия напряжений. В случаях, когда конструкция является жесткой и маловероятной, например, алюминиевая надстройка на корабле со стальным корпусом, все соединения теперь делаются жесткими, а дифференциальное расширение принимается как сжимающее или растягивающее напряжение.
 Нет никакой разницы в качестве между первичной и переработанной сталью.
Нет никакой разницы в качестве между первичной и переработанной сталью. Он также может быть отлит с высоким допуском. Легирование, холодная обработка и термическая обработка могут использоваться для изменения свойств алюминия, как это обычно делается для стали.
Он также может быть отлит с высоким допуском. Легирование, холодная обработка и термическая обработка могут использоваться для изменения свойств алюминия, как это обычно делается для стали. д. Это также наиболее часто производимый сплав, ежегодно производится почти более 1,66 миллиарда тонн.
д. Это также наиболее часто производимый сплав, ежегодно производится почти более 1,66 миллиарда тонн. Тем не менее, преимущество стали в том, что сталь намного тяжелее/намного плотнее, чем алюминий. Сталь обычно в 2,5 раза плотнее алюминия.
Тем не менее, преимущество стали в том, что сталь намного тяжелее/намного плотнее, чем алюминий. Сталь обычно в 2,5 раза плотнее алюминия. Прочность – самое большое преимущество стали. Алюминий — отличный выбор для многих ситуаций, но если вам абсолютно необходимо выбрать одно или другое, сталь предпочтительнее.
Прочность – самое большое преимущество стали. Алюминий — отличный выбор для многих ситуаций, но если вам абсолютно необходимо выбрать одно или другое, сталь предпочтительнее.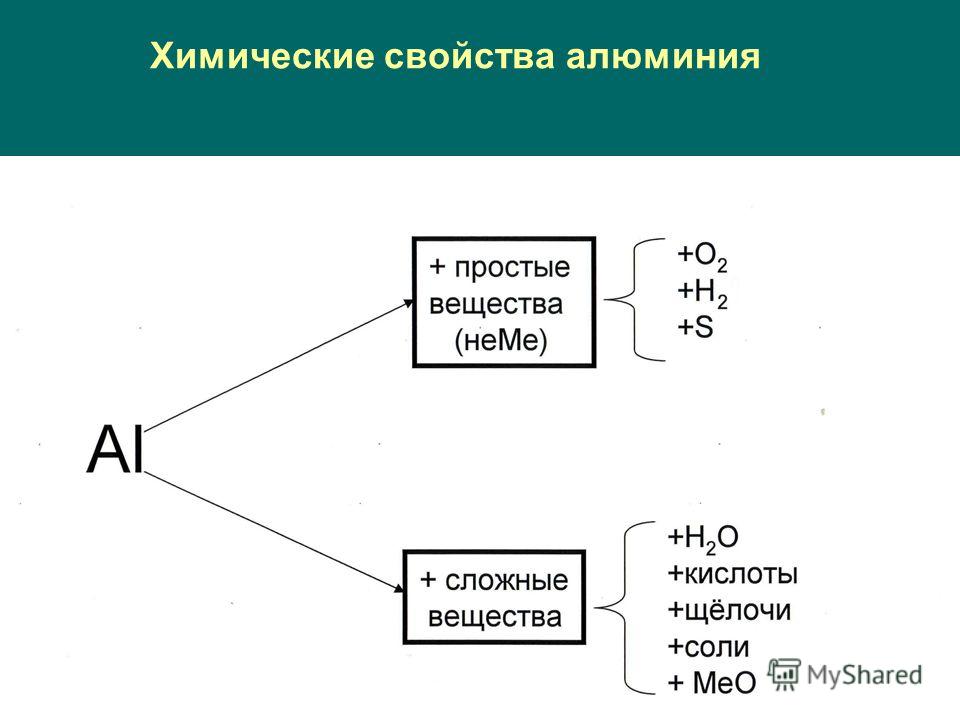 Преимуществом стали перед алюминием является твердость ее поверхности, которая намного тверже, чем у алюминия.
Преимуществом стали перед алюминием является твердость ее поверхности, которая намного тверже, чем у алюминия.

