Основные свойства металлов и сплавов: Свойства металлов и сплавов
alexxlab | 07.01.2023 | 0 | Разное
Свойства металлов и сплавов
Все свойства металлов и сплавов можно разделить на четыре группы:
Физические свойства. Физические свойства сплавов обуславливаются их составом и структурой. К ним относят:
- Цвет металла или сплава является одним из признаков, позволяющих судить о его свойствах.
- Температура плавления – температура, при которой металл переходит из твердого состояния в жидкое. У стали, например, температура плавления гораздо более высокая, чем у олова.
- Теплопроводность – способность тел проводить тепло при нагреве и охлаждении. Металлы имеют сравнительно высокую теплопроводность, чем она выше, тем равномернее распределяется температура по объему металла и тем быстрее он прогревается.
- Электропроводность – свойство металла проводить электрический ток.
- Магнитные свойства – способность металла намагничиваться (ферромагниты, парамагниты, диамагниты).

Химические свойства – это способность металла к взаимодействию с другими веществами: воздухом, водой, кислотами, щелочами и др. К химическим свойствам металлов и сплавов относят:
- Стойкость против коррозии на воздухе называют способность противостоять разрушающему действию кислорода, находящемуся в воздухе.
- Кислотостойкостью называют способность металлов и сплавов противостоять разрушающему действию кислот. Например, соляная кислота разрушает алюминий и цинк, а свинец не разрушает; серная кислота разрушает цинк и железо, но почти не действует на свинец, алюминий и медь.
- Щелочестойкостью металлов и сплавов называют способность противостоять разрушающему действию щелочей. Щелочи особенно сильно разрушают алюминий, олово и свинец.
- Жаростойкостью называют способность металлов и сплавов противостоять разрушению кислородом при нагреве. Для повышения жаростойкости вводят специальные примеси в металл, как, например, хром, вольфрам и т.
 д.
д.
Технологические свойства – способность металла подвергаться различным методам горячей и холодной обработки. К технологическим свойствам металлов и сплавов относят:
- Литейные свойства определяются жидкотекучестью, усадкой и склонностью к ликвации.
- Жидкотекучесть – способность металлов и сплавов заполнять полость литейной формы, точно воспроизводя ее конфигурацию.
- Усадкой называется сокращение объема и размеров металла отливки при затвердевании и последующем охлаждении.
- Ликвацией называется неоднородность химического состава твердого сплава по сечению слитка или заготовки.
- Ковкость – способность металлов и сплавов подвергаться обработке давлением. Это свойство связано с их пластической деформацией, особенно при нагревании. С ковкостью связаны такие важнейшие виды обработки металлов давлением, как прокатка, прессование, ковка, штамповка и волочение.

- Свариваемость – способность металлов и сплавов образовывать бездефектное сварное соединение, отвечающее необходимым эксплуатационным требованиям. Хорошая свариваемость у углеродистых, низкоуглеродистых и низколегированных сталей. Высокоуглеродистые и высоколегированные стали, некоторые цветные металлы и сплавы имеют худшую свариваемость. Чугун обладает плохой свариваемостью.
- Обрабатываемость материалов режущим инструментом – способность материала поддаваться обработке режущими инструментами. Обрабатываемость металлов резанием отражает способность металлов ограничивать производительность их обработки, вызывать затруднения в обеспечении требуемой точности и качества обработанной поверхности, требовать для обработки специальных приспособлений.
Механические свойства характеризуют отношение металла или сплава к действию на них внешних сил. Эти свойства обычно являются решающими показателями, по которым судят о пригодности металла к различным условиям работы. К этим свойствам относятся:
Эти свойства обычно являются решающими показателями, по которым судят о пригодности металла к различным условиям работы. К этим свойствам относятся:
- Прочность – свойство металла сопротивляться деформации и разрушению при действии на него нагрузки. Максимальная нагрузка, которую выдерживает металл в момент наступления разрушения, называется нагрузкой предела прочности, а напряжение, отвечающее этой максимальной нагрузке – пределом прочности.
- Упругость – свойство металла восстанавливать свою форму и размеры после прекращения действия нагрузки. Высокой упругостью должна обладать, например, рессоры и пружины, поэтому они изготовляются из специальных сплавов.
- Пластичность – способность металла изменять форму и размеры под действием внешней нагрузки и сохранять новую форму и размеры после прекращения действия сил. Пластичность – свойство, обратное упругости. Чем больше пластичность, тем легче металл куется, штампуется, прокатывается.

- Твердость – способность металла сопротивляться внедрению в его поверхность другого более твердого тела.
- Вязкость – способность металла оказывать сопротивление быстро возрастающим (ударным) нагрузкам. Вязкость – свойство, обратное хрупкости. Вязкие металлы применяются в тех случаях, когда детали при работе подвергаются ударной нагрузке.
- Усталость – процесс постепенного накопления повреждений в металле под длительным воздействием повторных или повторно-переменных напряжений, приводящий к образованию трещин и разрушению. Разрушение в результате усталости во многих случаях не сопровождается заметной макродеформацией образца или детали, поэтому такое разрушение чрезвычайно трудно предупредить.
- Ползучесть – свойство металла медленно и непрерывно пластически деформироваться при постоянной нагрузке, особенно при высокой температуре.
Оставить заявку на токарные работы Вы можете любым удобным способом:
- заполнить заявку на сайте
- написать: info@lasermeh.

- позвонить: +7(812)426-11-72
Полный список статей
Основные свойства металлов и сплавов
Основные свойства металлов и сплавов
Категория:
Изготовление форм
Основные свойства металлов и сплавов
Металлы и сплавы обладают определенными свойствами. Наиболее важными свойствами металлов и сплавов являются механические (твердость, прочность, пластичность, упругость) и технологические (жидкотекучесть, усадка, ликвация).
Твердость—способность металла противостоять проникновению в него другого, более твердого тела.
Прочность—способность металла сопротивляться разрушению под действием внешних сил.
Пластичность — способность металла деформироваться без разрушения под действием внешних сил и сохранять приданную форму после прекращения действия этих сил.
Упругость — свойство металла восстанавливать свою форму после прекращения действия внешних сил, вызывавших изменение формы.
Жид коте куч есть — способность расплавленного сплава заполнять литейную форму.
Усадка — уменьшение линейных размеров и объема отливок при охлаждении. Усадка выражается в процентах от первоначальных размеров полости формы (линейная усадка) или ее объема (объемная усадка).
Ликвация — свойство сплавов образовывать отливки с неоднородным химическим составом.
Контроль свойств металлов и сплавов в производственных условиях осуществляют путем проведения механических и технологических испытаний.
Испытание на растяжение (рис. 19) проводят с целью определения прочности и ‘пластичности материала, для чего из него вытачивают цилиндрические стандартные образцы, которые разрушают на разрывной машине.
Диаметр рабочей части нормального цилиндрического образца по ГОСТ 1497—61 10 мм, а длина равна пяти (для коротких образцов) или десяти (для длинных образцов) диаметрам. Головки образцов закрепляют в захватах разрывной машины, после чего машину приводят в действие. Растягивающее усилие создает напряжение в испытуемом образце и вызывает его удлинение, а когда напряжение превысит прочность образца — разрыв.
Величина наибольшего разрушающего растягивающего усилия, отнесенная к 1 мм2 поперечного сечения образца, определяет прочность материала 0В, а величина его удлинения по сравнению с первоначальной длиной образца — относительное удлинение, или вязкость.
Рис. 19. Схема основных методов контроля механических свойств металлов и сплавов:
а — схема контроля прочности и пластичности методом на растяжение, б — схема контроля твердости методом вдавливания шарика на приборе Бринелля, в — схема-контроля металла на изгиб
Испытание на твердость (рис. 19) чаще всего проводят на приборе Бринелля путем вдавливания на зачищенную поверхность отливки(или другого материала) с помощью оправки 3 стального закаленного шарика диаметром 10 или 5 мм силой Р 3000 или 1000 кГ. Показатель твердости определяется величиной, полученной от деления приложенного на приборе усилия на площадь отпечатка с диаметром d, оставленного на испытуемом материале шариком.
Испытание на изгиб применяют чаще всего для чугуна. Отлитый из серого чугуна образец 5 диаметром 30 мм и длиной, равной 300 или 600 мм подвергают разрушению. При этом определяют разрушающее усилие Р и величину (стрелу) прогиба средней части образца. Разделив разрушающее усилие на площадь поперечного сечения образца, можно определить прочность чугуна при изгибе
Отлитый из серого чугуна образец 5 диаметром 30 мм и длиной, равной 300 или 600 мм подвергают разрушению. При этом определяют разрушающее усилие Р и величину (стрелу) прогиба средней части образца. Разделив разрушающее усилие на площадь поперечного сечения образца, можно определить прочность чугуна при изгибе
Реклама:
Читать далее:
Понятие о структуре металлов и сплавов
Статьи по теме:
- Цветные металлы и их сплавы
- Понятие о научной организации труда
- Понятие о себестоимости отливок
- Новая система планирования и экономического стимулирования промышленного производства
- Оплата труда каркасника
Свойства металла | Металлургия для чайников
Металл — это химический элемент, который является хорошим проводником как электричества, так и тепла и образует катионы и ионные связи с неметаллами. В химии металл — это элемент, соединение или сплав, характеризующийся высокой электропроводностью. В металле атомы легко теряют электроны, образуя положительные ионы (катионы). Эти ионы окружены делокализованными электронами, которые отвечают за проводимость. Полученное таким образом твердое тело удерживается за счет электростатических взаимодействий между ионами и электронным облаком, которые называются металлическими связями.
В металле атомы легко теряют электроны, образуя положительные ионы (катионы). Эти ионы окружены делокализованными электронами, которые отвечают за проводимость. Полученное таким образом твердое тело удерживается за счет электростатических взаимодействий между ионами и электронным облаком, которые называются металлическими связями.Металл определяется как любой элемент, который теряет свои электроны внешней оболочки, чтобы стать стабильным. Так как нейтральные атомы имеют равное количество электронов (- заряд) и протонов (+ заряд). Поэтому, когда атом металла теряет электроны, он становится положительно заряженным. Эта заряженная частица называется ионом
Большинство элементов в периодической таблице представляют собой металлы, включая золото, серебро, платину, ртуть, уран, алюминий, натрий и кальций. Сплавы, такие как латунь и бронза, также являются металлами. Металлы расположены в левой части и в середине таблицы Менделеева. Группа IA и группа IIA (щелочные металлы) являются наиболее активными металлами.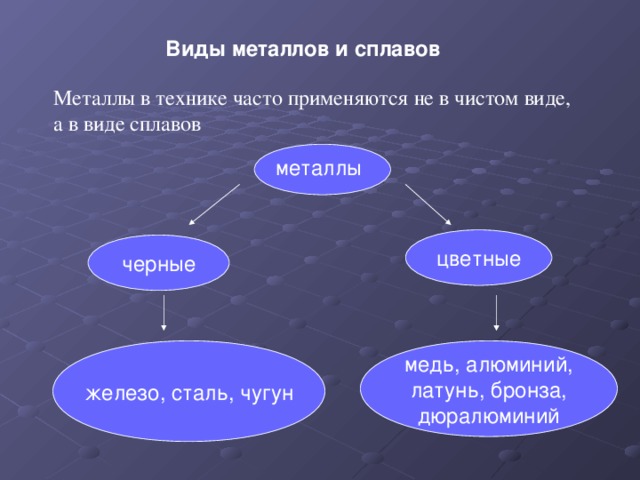 Переходные элементы групп с IB по VIIIB также считаются металлами. Основные металлы – это элемент справа от переходных металлов. Нижние два ряда элементов под основной частью таблицы Менделеева — это лантаноиды и актиниды, которые также являются металлами.
Переходные элементы групп с IB по VIIIB также считаются металлами. Основные металлы – это элемент справа от переходных металлов. Нижние два ряда элементов под основной частью таблицы Менделеева — это лантаноиды и актиниды, которые также являются металлами.
Металлы представляют собой блестящие твердые вещества комнатной температуры (кроме ртути, которая представляет собой блестящий жидкий элемент) с характерными высокими температурами плавления и плотностью. Многие свойства металлов, в том числе большой атомный радиус, низкая энергия ионизации и низкая электроотрицательность, обусловлены тем фактом, что электроны в валентной оболочке атомов металла могут быть легко удалены. Одной из характеристик металлов является их способность деформироваться без разрушения. Ковкость – это способность металла принимать форму. Пластичность – это способность металла вытягиваться в проволоку. Поскольку валентные электроны могут свободно двигаться, металлы являются хорошими проводниками тепла и электричества.
Свойства металлов
Металлы иногда описывают как совокупность положительных ионов, окруженных морем делокализованных электронов. Металлы занимают большую часть периодической таблицы, в то время как неметаллические элементы можно найти только в правой части периодической таблицы элементов. Диагональная линия, проведенная от бора (В) к полонию (Ро), отделяет металлы от неметаллов. Элементы в нижнем левом углу этой линии раздела называются металлами, а элементы в правом верхнем углу линии раздела называются неметаллами.
Свойства материалов
Альтернативное определение металла относится к ленточной теории. Если заполнить энергетические зоны материала доступными электронами и получить частично заполненную верхнюю полосу, то материал представляет собой металл. Солнце и Галактика Млечный Путь состоят примерно из 74% водорода, 24% гелия и 2% «металлов» (остальные элементы; атомные номера 3–118) по массе. Понятие металла в обычном химическом смысле не имеет отношения к звездам, поскольку химические связи, придающие элементам их свойства, не могут существовать при звездных температурах.
Металлы в целом обладают высокой электропроводностью, которая зависит от их валентности ионов, теплопроводности, блеска и плотности, а также способности деформироваться под напряжением без скалывания. Хотя есть несколько металлов с низкой плотностью, твердостью и температурой плавления, они (щелочные и щелочноземельные металлы) чрезвычайно реакционноспособны и редко встречаются в их элементарной металлической форме. С оптической точки зрения металлы непрозрачны, блестят и блестят. Большинство металлов имеют более высокую плотность, чем большинство неметаллов. Тем не менее, плотность металлов сильно различается: литий является наименее плотным твердым элементом, а осмий — самым плотным. Металлы групп I A и II A называются легкими металлами, потому что они являются исключениями из этого обобщения.
Высокая плотность большинства металлов обусловлена плотно упакованной кристаллической решеткой металлической структуры. Прочность металлических связей для различных металлов достигает максимума вокруг центра ряда переходных металлов, поскольку эти элементы имеют большое количество делокализованных электронов в металлических связях типа сильной связи. Большинство цветных металлов можно многократно перерабатывать в течение их жизненного цикла.
Большинство цветных металлов можно многократно перерабатывать в течение их жизненного цикла.
Электрическая и теплопроводность металлов обусловлена тем, что при металлической связи внешние электроны атомов металла образуют газ почти свободных электронов, движущихся как электронный газ на фоне положительного заряда, образованного ионными остовами . Хорошие математические предсказания для электропроводности, а также вклада электронов в теплоемкость и теплопроводность металлов могут быть рассчитаны на основе модели свободных электронов, которая не принимает во внимание детальную структуру ионной решетки.
Сплав представляет собой смесь двух или более элементов в твердом растворе, в котором основным компонентом является металл. Большинство чистых металлов либо слишком мягкие, либо хрупкие, либо химически активные для практического использования. Сочетание различных соотношений металлов в виде сплавов изменяет свойства чистых металлов для получения желаемых характеристик. Из всех используемых в настоящее время металлических сплавов сплавы железа (сталь, нержавеющая сталь, чугун, инструментальная сталь, легированная сталь) составляют наибольшую долю как по количеству, так и по товарной ценности. Железо, легированное различными пропорциями углерода, дает стали с низким, средним и высоким содержанием углерода, при этом повышение уровня углерода снижает пластичность и ударную вязкость. Другими важными металлическими сплавами являются сплавы алюминия, титана, меди и магния. Сплавы алюминия, титана и магния ценятся за их высокое отношение прочности к весу; магний также может обеспечивать электромагнитное экранирование.
Железо, легированное различными пропорциями углерода, дает стали с низким, средним и высоким содержанием углерода, при этом повышение уровня углерода снижает пластичность и ударную вязкость. Другими важными металлическими сплавами являются сплавы алюминия, титана, меди и магния. Сплавы алюминия, титана и магния ценятся за их высокое отношение прочности к весу; магний также может обеспечивать электромагнитное экранирование.
Сравнение металлов и полимеров
Сплавы, специально разработанные для особо требовательных применений, таких как реактивные двигатели, могут содержать более десяти элементов. В химическом отношении драгоценные металлы менее реакционноспособны, чем большинство элементов, обладают сильным блеском и высокой электропроводностью. Исторически драгоценные металлы были важны в качестве валюты, но теперь они рассматриваются в основном как инвестиционные и промышленные товары. Самыми известными драгоценными металлами являются золото и серебро. Другие драгоценные металлы включают металлы платиновой группы: рутений, родий, палладий, осмий, иридий и платину, из которых наиболее широко продается платина. Серебро значительно дешевле, чем эти металлы, но часто традиционно считается драгоценным металлом из-за его роли в чеканке монет и ювелирных изделиях.
Серебро значительно дешевле, чем эти металлы, но часто традиционно считается драгоценным металлом из-за его роли в чеканке монет и ювелирных изделиях.
СВОЙСТВА МЕТАЛЛОВ
Этот раздел посвящен главным образом терминам, используемым при описании различных свойств и характеристик металлов в целом. Первостепенное значение при обслуживании самолетов имеют такие общие свойства металлов и их сплавов, как твердость, хрупкость, ковкость, пластичность, упругость, ударная вязкость, плотность, плавкость, проводимость, сжатие и расширение. Вы должны знать определение включенных здесь терминов, потому что они формируют основу для дальнейшего обсуждения авиационных металлов.
Твердость
Твердость относится к способности металла сопротивляться истиранию, проникновению, резанию или постоянной деформации. Твердость можно повысить обработкой металла, а в случае стали и некоторых титановых и алюминиевых сплавов – термической обработкой и холодной обработкой (обсуждается позже). Конструктивные детали часто формируют из металлов в их мягком состоянии, а затем подвергают термообработке для их упрочнения, чтобы сохранить окончательную форму. Твердость и прочность являются тесно связанными свойствами всех металлов. Если у вас есть чистый кусок металла, вы можете контролировать размер зерен с помощью термической обработки или обработки металла.
Конструктивные детали часто формируют из металлов в их мягком состоянии, а затем подвергают термообработке для их упрочнения, чтобы сохранить окончательную форму. Твердость и прочность являются тесно связанными свойствами всех металлов. Если у вас есть чистый кусок металла, вы можете контролировать размер зерен с помощью термической обработки или обработки металла.
При нагревании металла атомы приобретают более правильное расположение, уменьшая количество границ зерен и делая металл более мягким. При ударах по металлу, когда он холодный, образуется много мелких зерен. Таким образом, холодная обработка делает металл тверже. Чтобы восстановить его работоспособность, вам нужно будет его снова нагреть.
Вы также можете нарушить правильное расположение атомов, вставив в структуру атомы немного другого размера. Такие сплавы, как латунь (смесь меди и цинка), тверже исходных металлов, потому что неравномерность структуры помогает предотвратить скольжение рядов атомов друг относительно друга.
Хрупкость
Хрупкость – это свойство металла, которое допускает небольшой изгиб или деформацию без разрушения. Другими словами, хрупкий металл может сломаться или треснуть без изменения формы. Поскольку конструкционные металлы часто подвергаются ударным нагрузкам, хрупкость не является очень желательным свойством. Чугун, литой алюминий и очень твердая сталь являются хрупкими металлами.
Плавкость
Металл, которому можно придать ковку, прокатке или прессованию различные формы без растрескивания, разрушения или других вредных воздействий, называется ковким. Это свойство необходимо для листового металла, из которого должны быть изготовлены криволинейные формы, такие как капоты, обтекатели и законцовки крыльев. Медь является одним из примеров ковкого металла.
Пластичность
Пластичность – это свойство металла, которое позволяет ему постоянно вытягиваться, изгибаться или скручиваться в различные формы без разрушения. Это свойство необходимо для металлов, используемых в производстве проволоки и труб. Пластичные металлы очень предпочтительны для использования в самолетах из-за их легкости формования и устойчивости к разрушению при ударных нагрузках. По этой причине алюминиевые сплавы используются для изготовления колец капота, фюзеляжа и обшивки крыла, а также формованных или штампованных деталей, таких как нервюры, лонжероны и переборки. Хромомолибденовая сталь также легко принимает желаемую форму. Пластичность аналогична пластичности.
Это свойство необходимо для металлов, используемых в производстве проволоки и труб. Пластичные металлы очень предпочтительны для использования в самолетах из-за их легкости формования и устойчивости к разрушению при ударных нагрузках. По этой причине алюминиевые сплавы используются для изготовления колец капота, фюзеляжа и обшивки крыла, а также формованных или штампованных деталей, таких как нервюры, лонжероны и переборки. Хромомолибденовая сталь также легко принимает желаемую форму. Пластичность аналогична пластичности.
Упругость
Упругость — это свойство, позволяющее металлу возвращаться к своей первоначальной форме при устранении силы, вызывающей изменение формы. Это свойство чрезвычайно ценно, потому что было бы крайне нежелательно иметь необратимую деформацию детали после снятия приложенной нагрузки. У каждого металла есть точка, известная как предел упругости, за которой его нельзя нагружать, не вызывая постоянной деформации. Когда металл нагружается за пределы его предела упругости и возникает необратимая деформация, это называется деформацией. В авиастроении элементы и детали проектируются таким образом, чтобы максимальные нагрузки, которым они подвергаются, никогда не превышали их предела упругости.
В авиастроении элементы и детали проектируются таким образом, чтобы максимальные нагрузки, которым они подвергаются, никогда не превышали их предела упругости.
Прочность
Материал, обладающий прочностью, выдерживает разрыв или сдвиг и может растягиваться или иным образом деформироваться без разрушения. Прочность является желательным свойством авиационных металлов.
Плотность
Плотность – это вес единицы объема материала. В авиастроении предпочтительнее фактический вес материала на кубический дюйм, поскольку этот показатель можно использовать для определения веса детали до фактического изготовления. Плотность является важным фактором при выборе материала, который будет использоваться в конструкции детали и при этом поддерживать надлежащий вес и баланс самолета.
Плавкость
Плавкость определяется как способность металла становиться жидким при нагревании. Металлы сплавляются при сварке. Стали плавятся примерно при 2500°F, а алюминиевые сплавы примерно при 1110°F.
Стали плавятся примерно при 2500°F, а алюминиевые сплавы примерно при 1110°F.
Проводимость
Проводимость — это свойство, позволяющее металлу переносить тепло или электричество. Теплопроводность металла особенно важна при сварке, потому что она определяет количество тепла, которое потребуется для правильного плавления. Проводимость металла в определенной степени определяет тип приспособления, используемого для контроля расширения и сжатия. В самолетах электропроводность также необходимо учитывать в сочетании с соединением, которое используется для устранения радиопомех. Металлы различаются по своей способности проводить тепло. Медь, например, обладает относительно высокой теплопроводностью и является хорошим проводником электричества.
Свободные электроны могут двигаться, поэтому, когда электроны вталкиваются с одного конца куска металла, другие выходят с другого конца. В металле нет пустых мест. Самый простой способ представить это как шланг, наполненный шариками, когда один входит в другой, немедленно выходит на другом конце. Таким образом, ток может течь через металлы. Именно наличие доступных электронов в металлах позволяет использовать их для выработки тока в батареях.
Таким образом, ток может течь через металлы. Именно наличие доступных электронов в металлах позволяет использовать их для выработки тока в батареях.
Вам также может понравиться
| Сверхпроводники Сверхпроводник – это элемент или… | Алюминиевый сплав Колесо из алюминиевого сплава Сплав – это материал… | Типы материалов Металлы: Металлы – элементы… | Полупроводниковые материалы Полупроводник – это вещество,… |
7.6: Металлы, неметаллы и металлоиды
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 21742
Цели обучения
- Понять основные свойства, отличающие металлы от неметаллов и металлоидов
Элемент — это простейшая форма материи, которая не может быть разделена на более простые вещества или построена из более простых веществ любым обычным химическим или физическим методом. Нам известно 118 элементов, из которых 92 встречаются в природе, а остальные получены искусственно. Элементы далее классифицируются на металлы, неметаллы и металлоиды на основе их свойств, которые коррелируют с их положением в периодической таблице.
Нам известно 118 элементов, из которых 92 встречаются в природе, а остальные получены искусственно. Элементы далее классифицируются на металлы, неметаллы и металлоиды на основе их свойств, которые коррелируют с их положением в периодической таблице.
| Металлические элементы | Неметаллические элементы |
|---|---|
| Отличительный блеск (блеск) | Неблестящий, различных цветов |
| Ковкий и пластичный (гибкий) в виде твердых тел | Хрупкий, твердый или мягкий |
| Проведение тепла и электричества | Плохие проводники |
| Оксиды металлов основные, ионные | Оксиды неметаллов кислотные, ковалентные |
| Катионы формы в водном растворе | Образуют анионы, оксианионы в водном растворе |
Металлы
За исключением водорода, все элементы, образующие положительные ионы за счет потери электронов в ходе химических реакций, называются металлами. Таким образом, металлы являются электроположительными элементами с относительно низкими энергиями ионизации. Они отличаются ярким блеском, твердостью, способностью резонировать звук и являются прекрасными проводниками тепла и электричества. Металлы в нормальных условиях являются твердыми телами, за исключением ртути.
Таким образом, металлы являются электроположительными элементами с относительно низкими энергиями ионизации. Они отличаются ярким блеском, твердостью, способностью резонировать звук и являются прекрасными проводниками тепла и электричества. Металлы в нормальных условиях являются твердыми телами, за исключением ртути.
Физические свойства металлов
Металлы блестящие, ковкие, пластичные, хорошо проводят тепло и электричество. Другие свойства включают:
- Состояние : Металлы являются твердыми при комнатной температуре, за исключением ртути, которая при комнатной температуре находится в жидком состоянии (галлий жидкий в жаркие дни).
- Блеск : Металлы обладают способностью отражать свет от своей поверхности и могут быть отполированы, например, золото, серебро и медь.
- Ковкость: Металлы обладают способностью выдерживать удары молотком и могут быть превращены в тонкие листы, известные как фольга.
 Например, кусок золота размером с кубик сахара можно растолочь в тонкий лист, который покроет футбольное поле.
Например, кусок золота размером с кубик сахара можно растолочь в тонкий лист, который покроет футбольное поле. - Пластичность: Металлы можно вытягивать в проволоку. Например, 100 г серебра можно вытянуть в тонкую проволоку длиной около 200 метров.
- Твердость: Все металлы твердые, кроме натрия и калия, которые мягкие и могут резаться ножом.
- Валентность: Металлы обычно имеют от 1 до 3 электронов на самой внешней оболочке их атомов.
- Проводимость : Металлы являются хорошими проводниками, потому что у них есть свободные электроны. Серебро и медь являются двумя лучшими проводниками тепла и электричества. Свинец — самый плохой проводник тепла. Висмут, ртуть и железо также являются плохими проводниками
- Плотность : Металлы имеют высокую плотность и очень тяжелые. Иридий и осмий имеют самую высокую плотность, тогда как литий имеет самую низкую плотность.

- Температуры плавления и кипения : Металлы имеют высокие температуры плавления и кипения. У вольфрама самые высокие температуры плавления и кипения, а у ртути самые низкие. Натрий и калий также имеют низкие температуры плавления.
Химические свойства металлов
Металлы представляют собой электроположительные элементы, которые обычно образуют основные или амфотерные оксиды с кислородом. Другие химические свойства включают:
- Электроположительный характер : Металлы, как правило, имеют низкую энергию ионизации, и обычно теряют электроны (т.е. окисляются ), когда подвергаются химическим реакциям Обычно они не принимают электроны. Например:
- Щелочные металлы всегда 1 + (теряют электрон в с подоболочкой)
- Щелочноземельные металлы всегда 2 + (теряют оба электрона за с подоболочка)
- Ионы переходных металлов не следуют очевидной схеме, 2 9{-}} \label{1.
 3} \]
3} \]Соединения металлов с неметаллами имеют тенденцию быть ионными по своей природе. Большинство оксидов металлов являются основными оксидами и растворяются в воде с образованием гидроксидов металлов :
\[\ce{Na2O(s) + h3O(l) \rightarrow 2NaOH(aq)}\label{1.4} \]
\[\ce{CaO(s) + h3O(l) \rightarrow Ca(OH)2(aq)} \label{1.5} \]
Оксиды металлов проявляют свою основную химическую природу, реагируя с кислоты 9{2-}\), таким образом, \(Al_2O_3\).
Пример \(\PageIndex{2}\)
Как вы думаете, будет ли он твердым, жидким или газообразным при комнатной температуре?
Растворы
Оксиды металлов обычно являются твердыми при комнатной температуре
Пример \(\PageIndex{3}\)
Напишите сбалансированное химическое уравнение реакции оксида алюминия с азотной кислотой:
Раствор
77 Оксид металла + кислота -> соль + вода\[\ce{Al2O3(s) + 6HNO3(aq) \rightarrow 2Al(NO3)3(aq) + 3h3O(l)} \nonumber \]
Неметаллы
Элементы, которые имеют тенденцию приобретать электроны с образованием анионов во время химических реакций, называются неметаллами.
 Это электроотрицательные элементы с высокими энергиями ионизации. Они неблестящие, хрупкие и плохо проводят тепло и электричество (кроме графита). Неметаллы могут быть газами, жидкостями или твердыми телами.
Это электроотрицательные элементы с высокими энергиями ионизации. Они неблестящие, хрупкие и плохо проводят тепло и электричество (кроме графита). Неметаллы могут быть газами, жидкостями или твердыми телами.Физические свойства неметаллов
- Физическое состояние : Большинство неметаллов существуют в двух из трех состояний вещества при комнатной температуре: газообразное (кислород) и твердое тело (углерод). Только бром существует в виде жидкости при комнатной температуре.
- Нековкий и пластичный : Неметаллы очень хрупкие, их нельзя свернуть в проволоку или растолочь в листы.
- Проводимость : Плохие проводники тепла и электричества.
- Блеск: Не имеют металлического блеска и не отражают свет.
- Точки плавления и кипения : Точки плавления неметаллов обычно ниже, чем у металлов, но сильно варьируются.
- Семь неметаллов существуют при стандартных условиях в виде двухатомных молекул : \(\ce{h3(g)}\), \(\ce{N2(g)}\), \(\ce{O2(g) }\), \(\ce{F2(g)}\), \(\ce{Cl2(g)}\), \(\ce{Br2(l)}\), \(\ce{I2( с)}\).

Химические свойства неметаллов
Неметаллы имеют тенденцию приобретать или делиться электронами с другими атомами. Они электроотрицательны по характеру. Неметаллы, реагируя с металлами, имеют тенденцию приобретать электроны (обычно приобретают электронную конфигурацию благородного газа) и становятся анионы:
\[\ce{3Br2(l) + 2Al(s) \rightarrow 2AlBr3(s)} \nonumber \]
Соединения, полностью состоящие из неметаллов, являются ковалентными веществами. Обычно они образуют кислотные или нейтральные оксиды с кислородом, которые растворяются в воде с образованием кислот:
\[\ce{CO2(g) + h3O(l)} \rightarrow \underset{\text{угольная кислота}}{\ce {h3CO3(aq)}} \nonumber \]
Как вы знаете, газированная вода слабокислая (угольная кислота).
Оксиды неметаллов могут соединяться с основаниями с образованием солей.
\[\ce{CO2(g) + 2NaOH(aq) \rightarrow Na2CO3(aq) + h3O(l)} \nonumber \]
Металлоиды
Металлоиды обладают промежуточными свойствами между металлами и неметаллами.
 Металлоиды используются в полупроводниковой промышленности. Все металлоиды твердые при комнатной температуре. Они могут образовывать сплавы с другими металлами. Некоторые металлоиды, такие как кремний и германий, при определенных условиях могут вести себя как электрические проводники, поэтому их называют полупроводниками. Кремний, например, выглядит блестящим, но имеет не ковкий и не пластичный (это хрупкий – характеристика некоторых неметаллов). Это гораздо худший проводник тепла и электричества, чем металлы. Физические свойства металлоидов имеют тенденцию быть металлическими, но их химические свойства имеют тенденцию быть неметаллическими. Степень окисления элемента этой группы может составлять от +5 до -2, в зависимости от группы, в которой он находится.
Металлоиды используются в полупроводниковой промышленности. Все металлоиды твердые при комнатной температуре. Они могут образовывать сплавы с другими металлами. Некоторые металлоиды, такие как кремний и германий, при определенных условиях могут вести себя как электрические проводники, поэтому их называют полупроводниками. Кремний, например, выглядит блестящим, но имеет не ковкий и не пластичный (это хрупкий – характеристика некоторых неметаллов). Это гораздо худший проводник тепла и электричества, чем металлы. Физические свойства металлоидов имеют тенденцию быть металлическими, но их химические свойства имеют тенденцию быть неметаллическими. Степень окисления элемента этой группы может составлять от +5 до -2, в зависимости от группы, в которой он находится.Таблица \(\PageIndex{2}\): Элементы, разделенные на металлы, неметаллы и металлоиды. Металлы Неметаллы Металлоиды Золото Кислород Кремний Серебро Углерод Бор Медь Водород Мышьяк Железо Азот Сурьма Меркурий Сера Германий Цинк Фосфор Тенденции металлических и неметаллических свойств
Металлический характер наиболее силен для элементов в крайней левой части периодической таблицы и имеет тенденцию к уменьшению по мере продвижения вправо в любой период (неметаллический характер увеличивается с увеличением электроотрицательности и ионизации).
 энергетические ценности). Внутри любой группы элементов (столбцов) металлический характер возрастает сверху вниз (значения электроотрицательности и энергии ионизации обычно уменьшаются по мере продвижения вниз по группе). Эта общая тенденция не обязательно наблюдается для переходных металлов.
энергетические ценности). Внутри любой группы элементов (столбцов) металлический характер возрастает сверху вниз (значения электроотрицательности и энергии ионизации обычно уменьшаются по мере продвижения вниз по группе). Эта общая тенденция не обязательно наблюдается для переходных металлов.
Неметаллический характер увеличивается снизу вверх и слева направо с наибольшим количеством неметаллических элементов в правом верхнем углу. металлический характер демонстрирует противоположную тенденцию: самый металлический элемент находится внизу слева.Участники и ссылки
Майк Блабер (Университет штата Флорида)
Бинод Шреста (Университет Лотарингии)
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 3,0
- Показать страницу Оглавление
- нет на стр.



