Особенности строения кристаллической решетки металлов пластичность: Строение металлов. Кристаллическая решетка металлов.
alexxlab | 14.03.2023 | 0 | Разное
Положения металлов в периодической таблице и особенности строения их атомов. | Методическая разработка по химии на тему:
Урок – лекция.
Тема. Положения металлов в периодической таблице и особенности строения их атомов.
Цель урока. Охарактеризовать положение металлов в периодической системе, дать понятие особенностей строения атомов металлов малых и больших периодов; обобщить знание видов химической связи и типов кристаллических решёток и зависимости свойств веществ от типа кристаллической решётки; познакомить учащихся с металлической связью, типами кристаллических решёток металлов и на основании этого объяснить особенности физических свойств металлов.
Оборудование. Периодическая таблица химических элементов, коллекция “Металлы”, диафильм “Общие свойства металлов”, таблицы “Виды химической связи”, прибор для демонстрации теплопроводности металлов, шаростержневые модели кристаллических решёток металлов.
Оформление класса. “Металлы отверзают недро земное к плодородию; металлы служат нам в ловлении земных и морских животных для пропитания нашего; металлы обличают купечество удобною к сему монетою . .. и кратко сказать, ни едино художество, ни едино ремесло простое употребления металлов миновать не может”.
.. и кратко сказать, ни едино художество, ни едино ремесло простое употребления металлов миновать не может”.
(М.В. Ломоносов)
Ход урока.
I. Организационная часть урока.
План лекции.
1. Значение металлов в истории человечества.
2. Положение металлов в периодической таблице.
3. Строение атомов металлов.
4. Особенности металлической связи. Кристаллические решётки металлов.
5. Физические свойства металлов.
II. Лекционное изложение нового материала.
С тех пор как каменный век сдал свои полномочия эпохе меди, металлы верно служат человеку, помогая ему строить и созидать, покорять стихию, овладевать тайнами природы, создавать замечательные машины и механизмы. Мир металлов необычайно богат и интересен. Среди них есть и давние друзья человека: медь, железо, золото, серебро, олово, ртуть, свинец. Эта дружба насчитывает уже тысячи лет. Но есть и такие, знакомство с которыми состоялось в последние десятилетия.
Семь металлов создал свет
По числу семи планет.
Дал нам космос на добро
Медь, железо, серебро, злато,
Олово, свинец …
Сын мой! Сера их отец!
И спеши, мой сын узнать:
Всем им ртуть родная мать.
(Н.А. Морозов)
2) Термин “металлы” относится и к простому веществу и к химическому элементу. (На экране с кодоскопа высвечиваем таблицу с вопросами.)
1. Где в периодической системе расположены металлы?
2. Чем объяснить значительное численное преимущество элементов-металлов в природе?
(Таблица “Распространённость металлов в земной коре”).
3. Что общего в строении атомов элементов, относящихся к металлам?
(Учащиеся отвечают на поставленные вопросы.)
Особенности строения атомов металлов таковы, что у них 1-3 ē на внешнем слое. Эти электроны атом сравнительно легко может отдавать.
Металлы обладают рядом общих свойств: тепло-, электро- проводностью, металлическим блеском. (Подумайте. Как это можно объяснить?)
Это связано со строением металлов. Особенности свойств заключаются в наличии свободных электронов и их движением по всему куску металла. Атомы металлов в отличие от неметаллов легко отдают наружные электроны, т.е. являются сильными восстановителями. Поэтому атомы металлов превращаются в положительно заряженные ионы. Электроны перемещаются между положительно заряженными ионами металла. Между этими частицами возникает связь, т.е. электроны как бы цементируют отдельные слои положительно заряженных ионов, которые находятся в узлах кристаллической решётки. Т.к. электроны находятся в постоянном движении они образуют “электронный газ”. Связь между частицами в металле называется металлической.
Атомы металлов в отличие от неметаллов легко отдают наружные электроны, т.е. являются сильными восстановителями. Поэтому атомы металлов превращаются в положительно заряженные ионы. Электроны перемещаются между положительно заряженными ионами металла. Между этими частицами возникает связь, т.е. электроны как бы цементируют отдельные слои положительно заряженных ионов, которые находятся в узлах кристаллической решётки. Т.к. электроны находятся в постоянном движении они образуют “электронный газ”. Связь между частицами в металле называется металлической.
Различное расположение ион-атомов в кристаллической решётке обуславливает различие видов металлических кристаллических решёток:
а) кубическая гранецентрированная;
б) гексагональная;
в) кубическая объёмноцентрированная
(демонстрируем шаростержневые модели кристаллических решёток, таблицу кристаллических решёток).
Mg, Be Cd | Cu, Ag, Au, Cr, Mo, W, Ca, Вa, Ni, Co |
гексагональная кубическая
Тип кристаллической решётки определяет особенности физических свойств веществ.
Характеризуем общие физические свойства металлов:
а) металлический блеск;
б) электропроводимость;
в) теплопроводность;
г) ковкость;
д) пластичность.
(Смотрим коллекцию “Металлы”.)
При обыкновенной температуре металлы – твёрдые вещества (кроме ртути).
Цвет: золото и цезий – жёлтый;
медь – светло-розовый;
висмут – красноватого цвета.
Плотность:
Легкие d < 5; тяжёлые d > 5.
Самый лёгкий металл литий (d = 0,53 г/см3)
Самый тяжёлый – осмий (d = 22,48 г/см3)
t° плавления:
t° пл. (Hg) = – 38,84°; t° пл. (Cs) = + 28,4°
t° пл. (W) = + 3387° t° пл. (Re) = + 3440°
Электропроводность:
Ag; Cu; Au; Cr; Al; Mg; Na; Ir; W; Be; Rh; Zn; Fe
Уменьшается →
Теплопроводность:
Ag; Cu; Au; Zn; Ni; Fe; Pt; Hg
Уменьшается →
(Опыт по теплопроводности).
Причины металлического блеска – способность отражать свет за счет плотной упаковки ион-атомов в кристаллической решётке.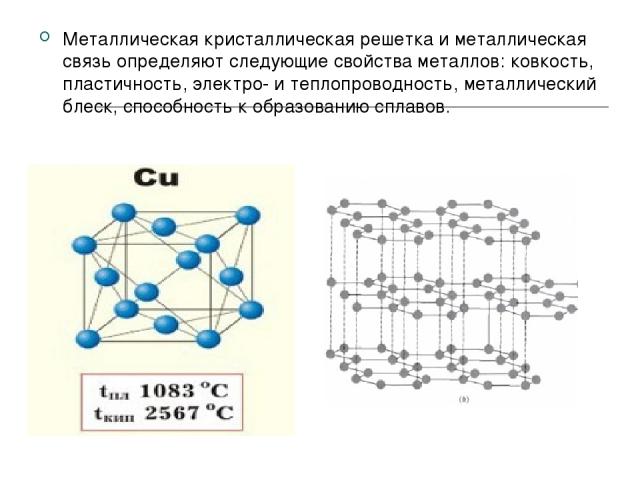 Первое место по блеску занимают серебро и палладий.
Первое место по блеску занимают серебро и палладий.
Ковкость – это прочность металлической связи. Самый ковкий металл – золото.
Благодаря металлической связи отдельные слои в кристаллах металлов могут смещаться относительно друг друга. Это придаёт металлам пластичность – способность изменять свою форму без разрыва химической связи.
По твёрдости металлы сравнивают с алмазом, твердость которого принята за 10. Самым мягким металлом является калий, самый твердый – хром.
Металлы смешиваются при расплавлении, образуя сплавы (см. таблички “Сплавы”).
III. Уяснение и запоминание лекционного материала.
Заполняем в тетрадях таблицу, отвечая на вопросы. (Положение металлов в периодической таблице, строение атомов металлов). Записываем особенности металлической связи (сходство и различие с ионной и ковалентной связью). Повторяем основные моменты лекции.
IV. Подведение итогов. Проверка усвоения лекционного содержания. Д/з.
1. Как расположены металлы в периодической системе Д.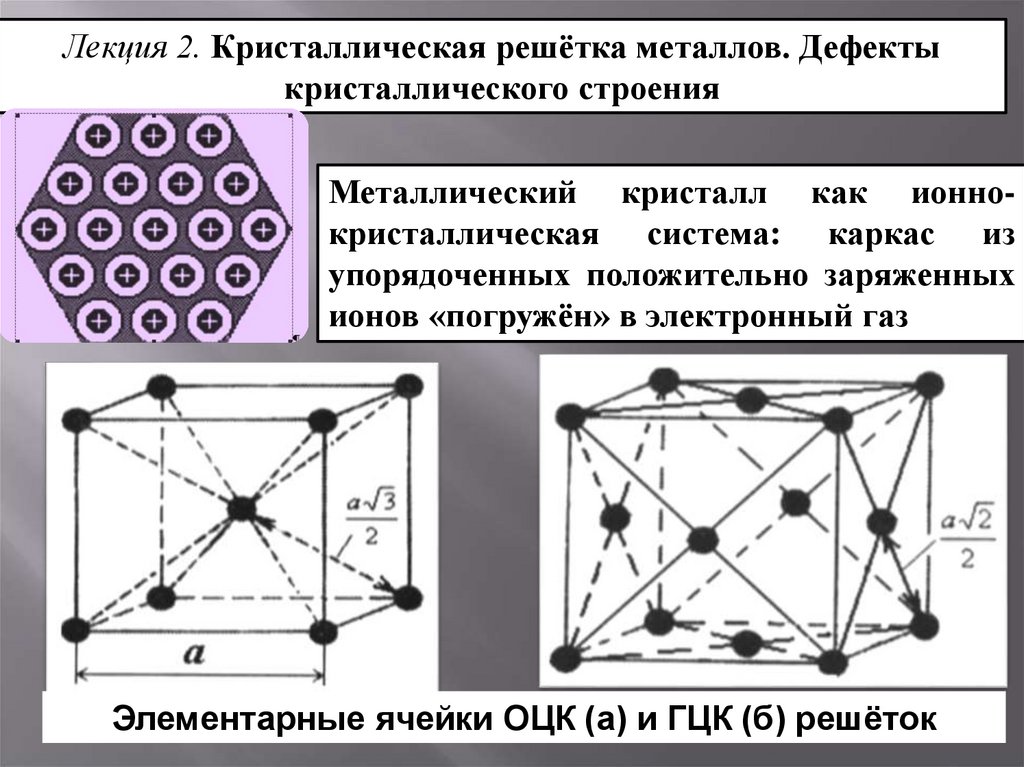 И. Менделеева? Почему?
И. Менделеева? Почему?
2. Какова сущность металлической связи?
3. Чем по строению и свойствам отличаются кристаллические решётки металлов от:
а) ионных; б) атомных?
4. Каковы общие физические свойства металлов? Поясните эти свойства, основываясь на представлениях о металлической связи.
5. Почему некоторые металлы пластичны (например, медь), а другие – хрупкие (например, сурьма)?
Д/з §40, 43. Упр. 1, 2, 3. с.119.
Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства. | Презентация по химии по теме:
государственное образовательное учреждение начального профессионального образования профессиональное училище № 39 |
Положение металлов в периодической системе Д.И. Менделеева |
Открытый урок по химии |
Преподаватель Борисенко И. А. |
17. |
Оглавление
Цель и задачи урока:
Форма урока:
Методы и приёмы:
Оборудование:
ХОД УРОКА
I. Организационный момент урока
II. Постановка и оглашение темы урока, его целей и задач.
III. Изучение нового материала.
IV. Закрепление изученного материала.
V. Подведение итогов урока
VI. Домашнее задание.
- На основе положения металлов в ПСХЭ подвести учащихся к пониманию особенностей строения их атомов и кристаллов (металлической химической связи и кристаллической металлической решетки), изучить общие физические свойства металлов. Повторить и обобщить знания о химической связи и металлической кристаллической решетке.
- Развивать умение анализировать, делать выводы о строении атомов исходя из положения металлов в ПСХЭ.
- Развивать умение владеть химической терминологией, чётко формулировать и высказывать свои мысли.

- Воспитывать самостоятельность мышления в ходе учебной деятельности.
- Формировать интерес к будущей профессии.
комбинированный урок с применением презентации
Рассказ, беседа, демонстрация видео типов кристаллических решеток металлов, тест, составление схем электронного строения атомов, демонстрация коллекции образцов металлов и сплавов.
- Таблица «Периодическая система химических элементов Д.И. Менделеева»;
- Презентация урока на электронном носителе.
- Коллекция образцов металлов и сплавов.
- Проектор.
- Карточки с таблицей «Характеристика строения атома по положению в ПСХЭ»
I. Организационный момент урока.
II. Постановка и оглашение темы урока, его целей и задач.
Слайд 1-2
III. Изучение нового материала.
Учитель: Человек использовал металлы с древних времён. Кратко об истории использования металлов.
Сообщение 1 учащегося. Слайд 3
В начале был век медный.
К концу каменного века человек открыл возможность использования металлов для изготовления орудий труда. Первым таким металлом была медь.
Период распространения медных орудий называют энеолитом или халколитом, что в переводе с греческого означает «медь». Медь обрабатывалась с помощью каменных орудий методом холодной ковки. Самородки меди превращались в изделия под тяжелыми ударами молота. В начале медного века из меди делали лишь мягкие орудия, украшения, предметы домашней утвари. Именно с открытием меди и других металлов стала зарождаться профессия кузнеца.
Позже появилось литьё, а потом человек стал добавлять к меди олово или сурьму, делать бронзу, более долговечную, прочную, легкоплавкую.
Сообщение 2 учащегося. Слайд 3
Далее идет век бронзовый.
Бронза – сплав меди и олова. Хронологические границы бронзового века датируются в начале 3-го тысячелетия до н.э. до начала 1-го тысячелетия до н.э.
Сообщение 3 учащегося. Слайд 4
Далее идет железный век.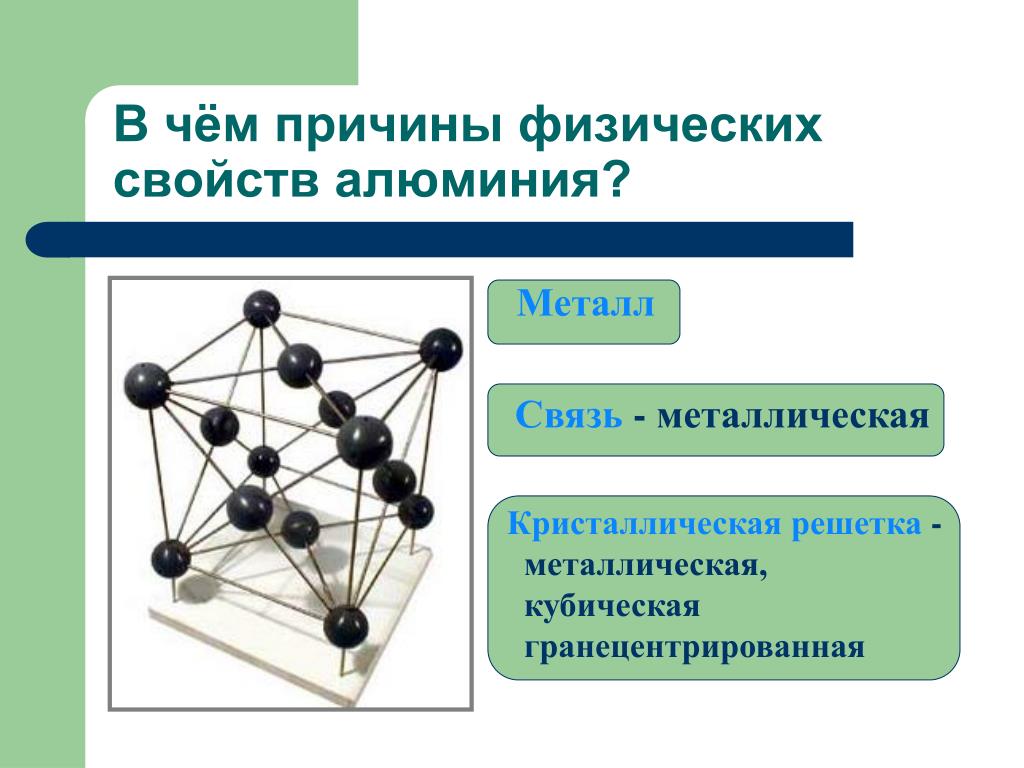
Третий и последний период первобытной эпохи характеризуется распространением железной металлургии и железных орудий и знаменует собой железный век. В современном значении этот термин был введен в употребление в середине IХ века датским археологом К. Ю. Томсоном и вскоре распространился в литературе наряду с терминами «каменный век» и « бронзовый век».
В отличие от других металлов железо, кроме метеоритного, почти не встречается в чистом виде. Ученые предполагают, что первое железо, попавшее в руки человека, было метеоритного происхождения, и не зря железо именуется « небесным камнем». Самый крупный метеорит нашли в Африке, он весил около шестидесяти тонн. А во льдах Гренландии нашли железный метеорит весом тридцать три тонны.
И настоящее время продолжается железный век. Ведь в настоящее время железные сплавы составляют почти 90 % всего металлов и металлических сплавов.
Учитель.
Золото и серебро – благородные металлы в настоящее время служат для изготовления ювелирных украшений, а также деталей в электронике, авиакосмической промышленности, в судостроении. Где в судоходстве могут применяться эти металлы? Исключительное значение металлов для развития общества обусловлено, конечно, их уникальными свойствами. Назовите эти свойства.
Где в судоходстве могут применяться эти металлы? Исключительное значение металлов для развития общества обусловлено, конечно, их уникальными свойствами. Назовите эти свойства.
Продемонстрировать учащимся коллекцию образцов металлов.
Учащиеся называют такие свойства металлов как электропроводность и теплопроводность, характерный металлический блеск, пластичность, твердость (кроме ртути) и др.
Учитель задает учащимся ключевой вопрос: а чем же обусловлены эти свойства?
Ожидаемый ответ: свойства веществ обусловлены строением молекул и атомов этих веществ.
Слайд 5. Итак, металлы – группа веществ с общими свойствами.
Демонстрация презентации.
Учитель: Металлами являются элементы 1-3 групп главных подгрупп, и элементы 4-8 групп побочных подгрупп.
Слайд 6. Задание 1. Самостоятельно, используя ПСХЭ, в тетради допишите представителей групп, являющиеся металлами.
I | II | III | IV | V | VI | VII | VIII |
Na | Mg | Al | Ti | V | Cr | Mn | Fe |
K | Ca | In | Sn | Ta | Mo | Tc | Pd |
Cs | Ba | Tl | Pb | Bi | W | Re | Ir |
Заслушивание ответов учащихся выборочно.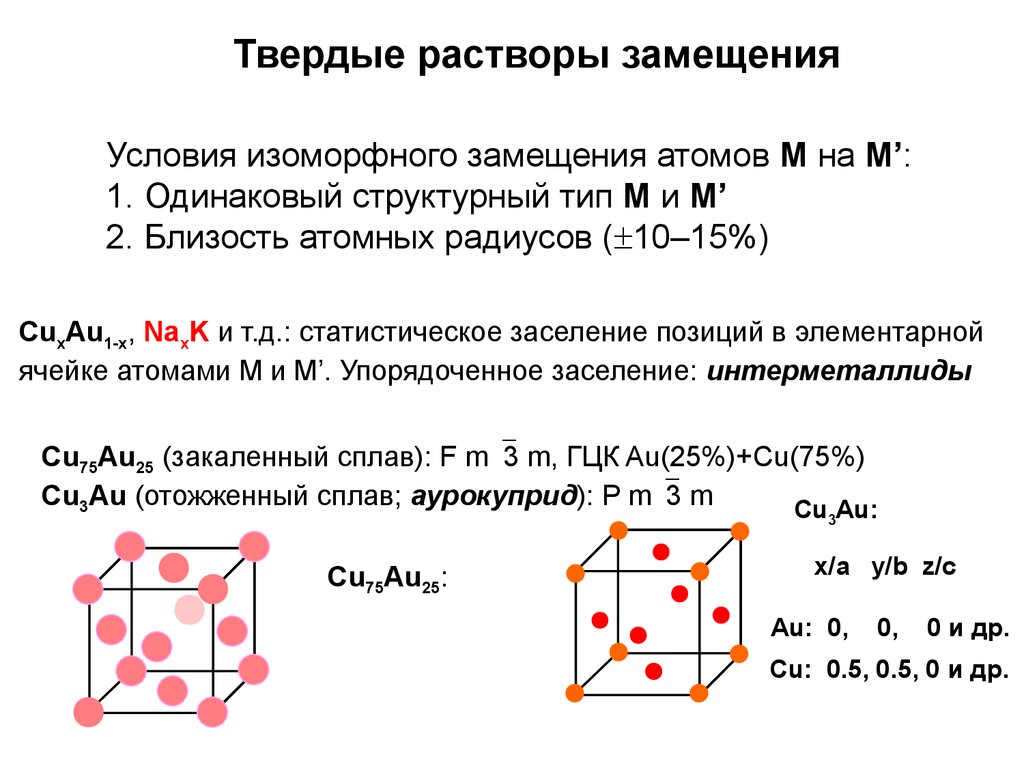
Учитель: металлами будут элементы, размещенные в левом нижнем углу ПСХЭ.
Учитель подчеркивает, что в ПСХЭ металлами будут все элементы, расположенные ниже диагонали В – Аt, даже те, у которых на внешнем слое 4 электрона (Gе, Sn, Рb), 5 электронов (Sb, Вi), 6 электронов (Ро), так как они отличаются большим радиусом.
Таким образом, из 109 элементов ПСХЭ 85 являются металлами. Слайд № 7
Учитель: положение элемента в ПСХЭ отражает строение атома элемента. С помощью таблиц, которые вы получили в начале урока, охарактеризуем строение атома натрия по его положению в ПСХЭ.
Демонстрация слайда 8.
Что представляет собой атом натрия? Посмотрите на приближенную модель атома натрия, в которой видны ядро и электроны, движущиеся по орбитам.
Демонстрация Слайда 9. Модель атома натрия.
Напомню вам, как составляется схема электронного строения атома элемента.
Демонстрация слайда 10. У вас должна получиться следующая схема электронного строения атома натрия.
Слайд 11. Задание 2. Составьте схему электронного строения атома кальция и алюминия в тетради самостоятельно по примеру с атомом натрия.
Учитель проверяет работу в тетради.
Какой вывод можно сделать об электронном строении атомов металлов?
– На внешнем энергетическом уровне 1-3 электрона. Мы помним, что вступая в химические соединения, атомы стремятся восстановить полную 8-электронный оболочку внешнего энергетического уровня. Для этого атомы металлов легко отдают 1-3 электрона с внешнего уровня, превращаясь в положительно-заряженные ионы. При этом проявляют восстановительные свойства.
Демонстрация слайда 12.Металлы – это химические элементы, атомы которых отдают электроны внешнего (а иногда предвнешнего) электронного слоя, превращаясь в положительные ионы. Металлы – восстановители. Это обусловлено небольшим числом электронов внешнего слоя, большим радиусом атомов, вследствие чего эти электроны слабо удерживаются с ядром.
Рассмотрим простые вещества – металлы.
Демонстрация слайда 13.
Сначала обобщим сведения о типе химической связи, образуемой атомами металлов и строении кристаллической решетки
- сравнительно небольшое количество электронов одновременно связывают множество ядер, связь делокализована;
- валентные электроны свободно перемещаются по всему куску металла, который в целом электронейтрален;
- металлическая связь не обладает направленностью и насыщенностью.
Демонстрация
Слайд 14 «Типы кристаллических решёток металлов»
Слайд 15 Видео кристаллической решетки металлов.
Учащиеся делают вывод, что в соответствие именно с таким строением металлы характеризуются общими физическими свойствами.
Учитель подчеркивает, что физические свойства металлов определяются именно их строением.
Слайд 16 Свойства металлов определяются строением их атомов
а) твердость – все металлы кроме ртути, при обычных условиях твердые вещества. Самые мягкие – натрий, калий. Их можно резать ножом; самый твердый хром – царапает стекло (демонстрация).
б) плотность – металлы делятся на лёгкие (5г/см) и тяжелые (больше 5г/см) (демонстрация).
в) плавкость – металлы делятся на легкоплавкие и тугоплавкие (демонстрация).
г) электропроводность, теплопроводность металлов обусловлена их строением. Хаотически движущиеся электроны под действием электрического напряжения приобретают направленное движение, в результате чего возникает электрический ток.
При повышении температуры амплитуда движения атомов и ионов, находящихся в узлах кристаллической решетки резко возрастает, и это мешает движению электронов, и электропроводность металлов падает.
Следует отметить, что у некоторых неметаллов, при повышении температуры электропроводность возрастает, например, у графита, при этом с повышением температуры разрушаются некоторые ковалентные связи, и число свободно перемещающихся электронов возрастает.
д) металлический блеск – электроны, заполняющие межатомное пространство отражают световые лучи, а не пропускают, как стекло.
Поэтому все металлы в кристаллическом состоянии имеют металлический блеск. Для большинства металлов в равной степени рассеиваются все лучи видимой части спектра, поэтому они имеют серебристо – белый цвет. Только золото и медь в большой степени поглощают короткие волны и отражают длинные волны светового спектра, поэтому имеют желтый свет. Самые блестящие металлы – ртуть, серебро, палладий. В порошке все металлы, кроме АI и Мg, теряют блеск и имеют черный или темно-серый цвет.
е) пластичность. Механическое воздействие на кристалл с металлической решеткой вызывает только смещение слоев атомов и не сопровождается разрывом связи, и поэтому металл характеризуется высокой пластичностью.
IV. Закрепление изученного материала.
Учитель: мы рассмотрели строение и физические свойства металлов, их положение в периодической системе химических элементов Д.И. Менделеева. Теперь для закрепления предлагаем выполнить тест.
Слайды 15-16-17.
1) Электронная формула кальция.
- а) 1S 2 2S2 2Р6 3S1
- б) 1S 2 2S 2 2Р6 3S 2
- в) 1S 2 2S 2 2Р6 3S 2 3S6 4S1
- г) 1S 2 2S 2 2Р6 3S 2 3Р6 4S 2
2) Электронную формулу 1S2 2S2 2Р6 3S2 3Р6 4S2 имеет атом:
- а) Nа
- б) Са
- в) Сu
- г) Zn
3) Электропроводность, металлический блеск, пластичность, плотность металлов определяются :
- а) массой металла
- б) температурой плавления металлов
- в) строением атомов металлов
- г) наличием неспареных электронов
4) Металлы при взаимодействии с неметаллами проявляют свойства
- а) окислительные;
- б) восстановительные;
- в) и окислительные, и восстановительные;
- г) не участвуют в окислительно-восстановительных реакциях;
5) В периодической системе типичные металлы расположены в:
- а) верхней части;
- б) нижней части;
- в) правом верхнем углу;
- г) левом нижнем углу
Проверяем работу соседа по парте по ключу Слайд 18
Номер вопроса | Правильный ответ |
1 | Г |
2 | Б |
3 | В |
4 | Б |
5 | Г |
V.
 Подведение итогов урока
Подведение итогов урокаКаждому ученику выставляется оценка.
VI. Домашнее задание.
Строение атомов металлов, их физические свойства
Пластичность | Энциклопедия MDPI
В физике и материаловедении пластичность, также известная как пластическая деформация, представляет собой способность твердого материала подвергаться постоянной деформации, необратимому изменению формы в ответ на приложенные силы. Например, твердый кусок металла, сгибаемый или растираемый в новую форму, проявляет пластичность, поскольку в самом материале происходят постоянные изменения. В технике переход от упругого поведения к пластическому называется текучестью. Пластическая деформация наблюдается в большинстве материалов, особенно в металлах, грунтах, горных породах, бетоне и пенопластах. Однако физические механизмы, вызывающие пластическую деформацию, могут сильно различаться. В кристаллическом масштабе пластичность металлов обычно является следствием дислокаций. Такие дефекты относительно редки в большинстве кристаллических материалов, но многочисленны в некоторых и являются частью их кристаллической структуры; в таких случаях может возникнуть пластическая кристалличность. В хрупких материалах, таких как камень, бетон и кость, пластичность обусловлена преимущественно скольжением по микротрещинам. В ячеистых материалах, таких как жидкие пены или биологические ткани, пластичность в основном является следствием пузырьковых или клеточных перестроек, особенно процессов Т1. Для многих пластичных металлов растягивающая нагрузка, приложенная к образцу, приводит к тому, что он ведет себя упруго. Каждое увеличение нагрузки сопровождается пропорциональным увеличением растяжения. При снятии нагрузки деталь возвращается к исходному размеру. Однако, как только нагрузка превышает пороговое значение — предел текучести — растяжение увеличивается быстрее, чем в упругой области; теперь, когда нагрузка будет удалена, некоторая степень растяжения останется. Упругая деформация, однако, является приближением, и ее качество зависит от рассматриваемого периода времени и скорости нагружения. Если, как показано на графике напротив, деформация включает в себя упругую деформацию, ее также часто называют «упруго-пластической деформацией» или «упруго-пластической деформацией».
В хрупких материалах, таких как камень, бетон и кость, пластичность обусловлена преимущественно скольжением по микротрещинам. В ячеистых материалах, таких как жидкие пены или биологические ткани, пластичность в основном является следствием пузырьковых или клеточных перестроек, особенно процессов Т1. Для многих пластичных металлов растягивающая нагрузка, приложенная к образцу, приводит к тому, что он ведет себя упруго. Каждое увеличение нагрузки сопровождается пропорциональным увеличением растяжения. При снятии нагрузки деталь возвращается к исходному размеру. Однако, как только нагрузка превышает пороговое значение — предел текучести — растяжение увеличивается быстрее, чем в упругой области; теперь, когда нагрузка будет удалена, некоторая степень растяжения останется. Упругая деформация, однако, является приближением, и ее качество зависит от рассматриваемого периода времени и скорости нагружения. Если, как показано на графике напротив, деформация включает в себя упругую деформацию, ее также часто называют «упруго-пластической деформацией» или «упруго-пластической деформацией». Совершенная пластичность – это свойство материалов подвергаться необратимой деформации без увеличения напряжений и нагрузок. Пластмассовые материалы, которые были закалены предварительной деформацией, такой как холодное формование, могут нуждаться во все более высоких напряжениях для дальнейшей деформации. Как правило, пластическая деформация также зависит от скорости деформации, т. е. обычно необходимо прикладывать более высокие напряжения для увеличения скорости деформации. Говорят, что такие материалы деформируются вязкопластически.
Совершенная пластичность – это свойство материалов подвергаться необратимой деформации без увеличения напряжений и нагрузок. Пластмассовые материалы, которые были закалены предварительной деформацией, такой как холодное формование, могут нуждаться во все более высоких напряжениях для дальнейшей деформации. Как правило, пластическая деформация также зависит от скорости деформации, т. е. обычно необходимо прикладывать более высокие напряжения для увеличения скорости деформации. Говорят, что такие материалы деформируются вязкопластически.
1. Способствующие свойства
Пластичность материала прямо пропорциональна его пластичности и пластичности.
2. Физические механизмы
Пластичность под сферическим наноиндентором в меди (111). Все частицы в идеальных положениях решетки опущены, а цветовой код относится к полю напряжений фон Мизеса. https://handwiki.org/wiki/index.php?curid=1952492
2.1. В Metals
Пластичность в кристалле чистого металла в первую очередь обусловлена двумя модами деформации в кристаллической решетке: скольжением и двойникованием. Скольжение — сдвиговая деформация, которая перемещает атомы на многие межатомные расстояния относительно их начального положения. Двойникование — это пластическая деформация, происходящая в двух плоскостях из-за набора сил, приложенных к данной металлической детали.
Скольжение — сдвиговая деформация, которая перемещает атомы на многие межатомные расстояния относительно их начального положения. Двойникование — это пластическая деформация, происходящая в двух плоскостях из-за набора сил, приложенных к данной металлической детали.
Большинство металлов более пластичны в горячем состоянии, чем в холодном. Свинец проявляет достаточную пластичность при комнатной температуре, в то время как чугун не обладает достаточной пластичностью для любой операции ковки даже в горячем состоянии. Это свойство имеет важное значение при штамповке, придании формы и экструзии металлов. Большинство металлов становятся пластичными при нагревании и, следовательно, подвергаются горячей обработке.
Системы скольжения
Кристаллические материалы содержат однородные плоскости атомов, организованные с дальним порядком. Самолеты могут проскальзывать друг мимо друга вдоль своих плотно упакованных направлений, как показано на странице систем скольжения. Результатом является постоянное изменение формы внутри кристалла и пластическая деформация. Наличие дислокаций увеличивает вероятность плоскостей.
Наличие дислокаций увеличивает вероятность плоскостей.
Обратимая пластичность
На наноуровне первичная пластическая деформация в простых гранецентрированных кубических металлах является обратимой, пока не происходит перенос материала в виде поперечного скольжения. [1] Сплавы с памятью формы, такие как нитиноловая проволока, также проявляют обратимую форму пластичности, которую правильнее называть псевдоупругостью.
Полосы сдвига
Наличие других дефектов в кристалле может запутывать дислокации или иным образом препятствовать их скольжению. Когда это происходит, пластичность локализуется в определенных областях материала. Для кристаллов эти области локализованной пластичности называются полосами сдвига.
Микропластичность
Микропластичность — локальное явление в металлах. Это происходит для значений напряжения, когда металл глобально находится в области упругости, а некоторые локальные области находятся в области пластичности. [2]
[2]
2.2. Аморфные материалы
Растрескивание
В аморфных материалах обсуждение «дислокаций» неприменимо, поскольку во всем материале отсутствует дальний порядок. Эти материалы все еще могут подвергаться пластической деформации. Поскольку аморфные материалы, такие как полимеры, плохо упорядочены, они содержат большое количество свободного объема или неиспользуемого пространства. Натяжение этих материалов при растяжении открывает эти области и может придать материалам нечеткий вид. Эта туманность является результатом растрескивание , при котором фибриллы образуются внутри материала в областях с высоким гидростатическим напряжением. Материал может превратиться из упорядоченного вида в «сумасшедший» рисунок деформации и растяжек.
2.3. Ячеистые материалы
Эти материалы пластически деформируются, когда изгибающий момент превышает полностью пластический момент. Это относится к пенам с открытыми порами, где изгибающий момент действует на стенки ячеек. Пенопласты могут быть изготовлены из любого материала с пластическим пределом текучести, включая жесткие полимеры и металлы. Этот метод моделирования пены в виде балок действителен только в том случае, если отношение плотности пены к плотности вещества меньше 0,3. Это связано с тем, что балки прогибаются в осевом направлении, а не изгибаются. В пенопластах с закрытыми порами предел текучести увеличивается, если материал находится под напряжением из-за мембраны, которая охватывает поверхность ячеек.
Пенопласты могут быть изготовлены из любого материала с пластическим пределом текучести, включая жесткие полимеры и металлы. Этот метод моделирования пены в виде балок действителен только в том случае, если отношение плотности пены к плотности вещества меньше 0,3. Это связано с тем, что балки прогибаются в осевом направлении, а не изгибаются. В пенопластах с закрытыми порами предел текучести увеличивается, если материал находится под напряжением из-за мембраны, которая охватывает поверхность ячеек.
2.4. Почвы и песок
Почвы, особенно глины, демонстрируют значительную неупругость под нагрузкой. Причины пластичности почв могут быть весьма сложными и сильно зависят от микроструктуры, химического состава и содержания воды. Пластическое поведение в почвах обусловлено в первую очередь перестройкой скоплений соседних зерен.
2.5. Горные породы и бетон
Неупругие деформации горных пород и бетона в первую очередь вызываются образованием микротрещин и скользящими движениями относительно этих трещин. При высоких температурах и давлениях на пластическое поведение может влиять и движение дислокаций в отдельных зернах микроструктуры.
При высоких температурах и давлениях на пластическое поведение может влиять и движение дислокаций в отдельных зернах микроструктуры.
3. Независимая от времени пластическая текучесть и пластическое течение в кристаллических материалах
[3]Независимая от времени пластическая текучесть как в монокристаллах, так и в поликристаллах определяется критическим/максимальным разрешенным напряжением сдвига ( τ CRSS ) , инициируя миграцию дислокаций вдоль параллельных плоскостей скольжения единой системы скольжения, тем самым определяя переход от упругого к пластическому деформационному поведению в кристаллических материалах.
3.1. Независимая от времени текучесть и пластическое течение в монокристаллах
Критическое разрешенное напряжение сдвига для монокристаллов определяется законом Шмида . Коэффициент Шмида состоит из двух переменных λ и φ, определяющих угол между направлением плоскости скольжения и приложенной растягивающей силой, а также угол между нормалью к плоскости скольжения и приложенной растягивающей силой соответственно. Примечательно, что м > 1, σ y > τ CRSS .
Примечательно, что м > 1, σ y > τ CRSS .
Зависимость критического разрешенного напряжения сдвига от температуры, скорости деформации и точечных дефектов
Три характерные области критического разрешенного напряжения сдвига в зависимости от температуры. https://handwiki.org/wiki/index.php?curid=1466661
Существуют три характерных области критического разрешенного напряжения сдвига в зависимости от температуры. В области низких температур 1 ( T ≤ 0,25 T m ), скорость деформации έ должна быть высокой для достижения высокого τ CRSS , необходимого для инициирования дислокационного скольжения и эквивалентного пластического течения. В области 1 критическое разрешенное касательное напряжение имеет две составляющие: атермическую ( τ a ) и тепловую ( В T = T *, область умеренных температур 2 (0,25 T м < T < 0,7 T м ) → 4 τ 4 компонента напряжения сдвига , представляющий устранение импеданса точечного дефекта миграции дислокаций. Таким образом, независимое от температуры критическое разрешенное напряжение сдвига τ CRSS = τ a остается таким до тех пор, пока не будет определена область 3. Примечательно, что в области 2 следует учитывать механизмы пластической деформации (ползучести), зависящие от времени при умеренной температуре, такие как сопротивление растворенного вещества. Кроме того, в области высоких температур 3 ( T ≥ 0,7 T m ) έ может быть низким, что способствует низкому τ CRSS , однако пластическое течение все равно будет происходить из-за термически активируемых высокотемпературных механизмов пластической деформации, зависящих от времени, таких как механизм Набарро–Херринга (NH ) и диффузионное течение Кобла через решетку и по поверхности монокристалла соответственно, а также ползучесть дислокаций.
В T = T *, область умеренных температур 2 (0,25 T м < T < 0,7 T м ) → 4 τ 4 компонента напряжения сдвига , представляющий устранение импеданса точечного дефекта миграции дислокаций. Таким образом, независимое от температуры критическое разрешенное напряжение сдвига τ CRSS = τ a остается таким до тех пор, пока не будет определена область 3. Примечательно, что в области 2 следует учитывать механизмы пластической деформации (ползучести), зависящие от времени при умеренной температуре, такие как сопротивление растворенного вещества. Кроме того, в области высоких температур 3 ( T ≥ 0,7 T m ) έ может быть низким, что способствует низкому τ CRSS , однако пластическое течение все равно будет происходить из-за термически активируемых высокотемпературных механизмов пластической деформации, зависящих от времени, таких как механизм Набарро–Херринга (NH ) и диффузионное течение Кобла через решетку и по поверхности монокристалла соответственно, а также ползучесть дислокаций.
Стадии независимого от времени пластического течения, последующая текучесть
Три стадии нестационарной пластической деформации монокристаллов. https://handwiki.org/wiki/index.php?curid=1162594
Во время этапа 1 легкого скольжения скорость упрочнения, определяемая изменением напряжения сдвига по отношению к деформации сдвига ( dτ / dγ ), является низкой, отражающей небольшое количество приложенного напряжения сдвига, необходимого для вызвать большую деформацию сдвига. Легкое скольжение дислокаций и соответствующее течение объясняются миграцией дислокаций только вдоль параллельных плоскостей скольжения (т.е. одной системы скольжения). Умеренное сопротивление миграции дислокаций вдоль параллельных плоскостей скольжения проявляется в связи со слабым взаимодействием полей напряжений между этими дислокациями, которое усиливается при уменьшении межплоскостного расстояния. В целом эти мигрирующие дислокации в рамках единой системы скольжения действуют как слабые препятствия для течения, и наблюдается умеренное повышение напряжения по сравнению с пределом текучести.
| Объемноцентрированные кубические переходные металлы | Гранецентрированные кубические металлы |
|---|---|
| Критическое разрешенное напряжение сдвига = высокое (относительно) и сильно зависящее от температуры | Критическое разрешенное напряжение сдвига = низкое (относительно) и слабо зависящее от температуры |
| Скорость упрочнения = не зависит от температуры | Скорость упрочнения = зависит от температуры |
| Деформация шейки увеличивается с температурой | Деформация шейки уменьшается с температурой |
3.2. Независимая от времени текучесть и пластическое течение в поликристаллах
Пластичность в поликристаллах существенно отличается от пластичности в монокристаллах из-за наличия планарных дефектов границ зерен (ЗЗ), которые действуют как очень сильные препятствия пластическому течению, препятствуя миграции дислокаций по всей длина активированной плоскости (плоскостей) скольжения. Следовательно, дислокации не могут переходить от одного зерна к другому через границу зерна. В следующих разделах исследуются особые требования GB к обширной пластической деформации поликристаллов до разрушения, а также влияние микроскопической текучести отдельных кристаллитов на макроскопическую текучесть поликристалла. Критическое разрешенное напряжение сдвига для поликристаллов также определяется законом Шмида (τ CRSS =σ y /ṁ), где σ y — предел текучести поликристалла, а ṁ — взвешенный коэффициент Шмида. Взвешенный фактор Шмида отражает наименее благоприятно ориентированную систему скольжения среди наиболее благоприятно ориентированных систем скольжения зерен, составляющих ГБ.
Следовательно, дислокации не могут переходить от одного зерна к другому через границу зерна. В следующих разделах исследуются особые требования GB к обширной пластической деформации поликристаллов до разрушения, а также влияние микроскопической текучести отдельных кристаллитов на макроскопическую текучесть поликристалла. Критическое разрешенное напряжение сдвига для поликристаллов также определяется законом Шмида (τ CRSS =σ y /ṁ), где σ y — предел текучести поликристалла, а ṁ — взвешенный коэффициент Шмида. Взвешенный фактор Шмида отражает наименее благоприятно ориентированную систему скольжения среди наиболее благоприятно ориентированных систем скольжения зерен, составляющих ГБ.
Ограничение границ зерен в поликристаллах
Ограничение границ зерен для поликристаллов можно объяснить, рассматривая границу зерен в плоскости xz между двумя монокристаллами A и B, идентичными по составу, структуре и системам скольжения, но разориентированными по отношению друг к другу .
 Примечательно, что для каждой из семи кристаллических систем существует максимум пять независимых систем скольжения, однако не все семь кристаллических систем достигают этого верхнего предела. Фактически, даже в пределах данной кристаллической системы состав и решетка Браве разнообразят количество независимых систем скольжения (см. таблицу ниже). В случаях, когда кристаллиты поликристалла не получают пяти независимых систем скольжения, условие ГЗ не может быть выполнено, и, таким образом, независимая от времени деформация отдельных кристаллитов приводит к образованию трещин и пустот в ГЗ поликристалла, и вскоре реализуется разрушение. . Следовательно, для данного состава и структуры монокристалл с менее чем пятью независимыми системами скольжения прочнее (проявляя большую степень пластичности), чем его поликристаллическая форма.
Примечательно, что для каждой из семи кристаллических систем существует максимум пять независимых систем скольжения, однако не все семь кристаллических систем достигают этого верхнего предела. Фактически, даже в пределах данной кристаллической системы состав и решетка Браве разнообразят количество независимых систем скольжения (см. таблицу ниже). В случаях, когда кристаллиты поликристалла не получают пяти независимых систем скольжения, условие ГЗ не может быть выполнено, и, таким образом, независимая от времени деформация отдельных кристаллитов приводит к образованию трещин и пустот в ГЗ поликристалла, и вскоре реализуется разрушение. . Следовательно, для данного состава и структуры монокристалл с менее чем пятью независимыми системами скольжения прочнее (проявляя большую степень пластичности), чем его поликристаллическая форма.| Решетка Браве | Класс основного материала: # Независимые системы скольжения |
|---|---|
| Гранецентрированный куб | Металл: 5, керамика (ковалентная): 5, керамика (ионная): 2 |
| Кубический центр по центру кузова | Металл: 5 |
| Простой куб | Керамика (ионная): 3 |
| Шестигранник | Металл: 2, керамика (смешанный): 2 |
Последствия ограничения границ зерен в поликристаллах
Хотя два кристаллита A и B, рассмотренные в предыдущем разделе, имеют идентичные системы скольжения, они разориентированы по отношению друг к другу и, следовательно, разориентированы по отношению к приложенной силе. Таким образом, микроскопическая текучесть внутри кристаллита может происходить в соответствии с правилами, определяющими независимую от времени текучесть монокристалла. В конце концов, активированные плоскости скольжения внутри зерен позволят дислокациям мигрировать к ГБ, где многие дислокации затем накапливаются как геометрически необходимые дислокации. Это скопление соответствует градиентам деформации по отдельным зернам, поскольку плотность дислокаций вблизи границ зерен больше, чем внутри зерен, что создает напряжение в соседнем контактирующем зерне. При рассмотрении бикристалла AB в целом наиболее благоприятно ориентированной системой скольжения в A будет не та, что в B, а значит, τ A CRSS ≠ τ B CRSS . Принципиальным является тот факт, что макроскопическая текучесть бикристалла продлевается до тех пор, пока не будет достигнуто более высокое значение τ CRSS между зернами A и B, в соответствии с ограничением ГБ. Таким образом, при заданном составе и структуре поликристалл с пятью независимыми системами скольжения прочнее (большая степень пластичности), чем его монокристаллическая форма.
Таким образом, микроскопическая текучесть внутри кристаллита может происходить в соответствии с правилами, определяющими независимую от времени текучесть монокристалла. В конце концов, активированные плоскости скольжения внутри зерен позволят дислокациям мигрировать к ГБ, где многие дислокации затем накапливаются как геометрически необходимые дислокации. Это скопление соответствует градиентам деформации по отдельным зернам, поскольку плотность дислокаций вблизи границ зерен больше, чем внутри зерен, что создает напряжение в соседнем контактирующем зерне. При рассмотрении бикристалла AB в целом наиболее благоприятно ориентированной системой скольжения в A будет не та, что в B, а значит, τ A CRSS ≠ τ B CRSS . Принципиальным является тот факт, что макроскопическая текучесть бикристалла продлевается до тех пор, пока не будет достигнуто более высокое значение τ CRSS между зернами A и B, в соответствии с ограничением ГБ. Таким образом, при заданном составе и структуре поликристалл с пятью независимыми системами скольжения прочнее (большая степень пластичности), чем его монокристаллическая форма. Соответственно, скорость деформационного упрочнения будет выше для поликристалла, чем для монокристалла, поскольку в поликристалле требуется большее напряжение для возникновения деформаций. Важно отметить, что, как и в случае напряжения течения монокристалла, τ расход ~ρ ½ , но также обратно пропорционален квадратному корню из среднего диаметра зерна (τ расход ~d -½ ). Следовательно, напряжение течения поликристалла и, следовательно, прочность поликристалла увеличиваются с малым размером зерна. Причина этого заключается в том, что более мелкие зерна имеют относительно меньшее количество плоскостей скольжения, которые необходимо активировать, что соответствует меньшему количеству дислокаций, мигрирующих к границам границ, и, следовательно, меньшему напряжению, вызываемому соседними зернами из-за скопления дислокаций. Кроме того, для данного объема поликристалла более мелкие зерна представляют собой более прочные границы зерен препятствия.
Соответственно, скорость деформационного упрочнения будет выше для поликристалла, чем для монокристалла, поскольку в поликристалле требуется большее напряжение для возникновения деформаций. Важно отметить, что, как и в случае напряжения течения монокристалла, τ расход ~ρ ½ , но также обратно пропорционален квадратному корню из среднего диаметра зерна (τ расход ~d -½ ). Следовательно, напряжение течения поликристалла и, следовательно, прочность поликристалла увеличиваются с малым размером зерна. Причина этого заключается в том, что более мелкие зерна имеют относительно меньшее количество плоскостей скольжения, которые необходимо активировать, что соответствует меньшему количеству дислокаций, мигрирующих к границам границ, и, следовательно, меньшему напряжению, вызываемому соседними зернами из-за скопления дислокаций. Кроме того, для данного объема поликристалла более мелкие зерна представляют собой более прочные границы зерен препятствия.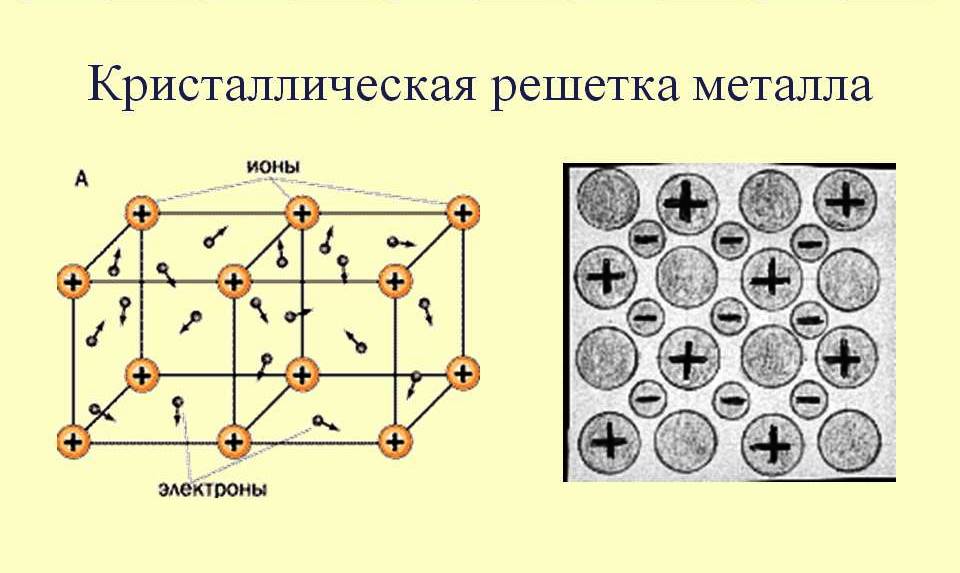 Эти два фактора позволяют понять, почему начало макроскопического течения в мелкозернистых поликристаллах происходит при больших приложенных напряжениях, чем в крупнозернистых поликристаллах.
Эти два фактора позволяют понять, почему начало макроскопического течения в мелкозернистых поликристаллах происходит при больших приложенных напряжениях, чем в крупнозернистых поликристаллах.
4. Математические описания
4.1. Теория деформации
Идеализированная кривая одноосного напряжения-деформации, показывающая режимы упругой и пластической деформации для теории деформации пластичности. https://handwiki.org/wiki/index.php?curid=2052089
Существует несколько математических описаний пластичности. [6] Одним из них является теория деформации (см., например, закон Гука), где тензор напряжений Коши (порядка d-1 в d измерениях) является функцией тензора деформации. Хотя это описание является точным, когда небольшая часть вещества подвергается возрастающей нагрузке (например, деформации), эта теория не может объяснить необратимость.
Пластичные материалы могут выдерживать большие пластические деформации без разрушения.
4.2. Flow Plasticity Theory
В 1934 году Эгон Орован, Майкл Поланьи и Джеффри Инграм Тейлор примерно одновременно поняли, что пластическую деформацию пластичных материалов можно объяснить с точки зрения теории дислокаций. Математическая теория пластичности, теория пластичности течения, использует набор нелинейных, неинтегрируемых уравнений для описания набора изменений деформации и напряжения по отношению к предыдущему состоянию и небольшому увеличению деформации.
5. Критерии доходности
Сравнение критерия Трески с критерием фон Мизеса. https://handwiki.org/wiki/index.php?curid=1999286
Если напряжение превышает критическое значение, как было сказано выше, материал подвергается пластической, или необратимой, деформации. Это критическое напряжение может быть растягивающим или сжимающим. Критерии Трески и фон Мизеса обычно используются для определения текучести материала. Однако эти критерии оказались недостаточными для большого диапазона материалов, и некоторые другие критерии текучести также широко используются.
Это критическое напряжение может быть растягивающим или сжимающим. Критерии Трески и фон Мизеса обычно используются для определения текучести материала. Однако эти критерии оказались недостаточными для большого диапазона материалов, и некоторые другие критерии текучести также широко используются.
5.1. Критерий Трески
Критерий Трески основан на представлении о том, что разрушение материала происходит при сдвиге, что является относительно хорошим предположением при рассмотрении металлов. Учитывая основное напряженное состояние, мы можем использовать круг Мора, чтобы определить максимальные напряжения сдвига, которые испытывает наш материал, и сделать вывод, что материал разрушится, если
- [математика]\displaystyle{ \sigma_1 – \sigma_3 \ge \sigma_0 }[ /математика]
где σ 1 — максимальное нормальное напряжение, σ 3 — минимальное нормальное напряжение, σ 0 — напряжение, при котором материал разрушается при одноосном нагружении. Можно построить поверхность текучести, которая обеспечивает визуальное представление этой концепции. Внутри поверхности текучести деформация упругая. На поверхности деформация носит пластический характер. Материал не может иметь напряженное состояние за пределами своей поверхности текучести.
Можно построить поверхность текучести, которая обеспечивает визуальное представление этой концепции. Внутри поверхности текучести деформация упругая. На поверхности деформация носит пластический характер. Материал не может иметь напряженное состояние за пределами своей поверхности текучести.
5.2. Критерий Хубера–Фон Мизеса 9.0013
Поверхности текучести фон Мизеса в координатах главных напряжений описывают цилиндр вокруг гидростатической оси. Также показана шестиугольная поверхность текучести Трески. https://handwiki.org/wiki/index.php?curid=2043554
Критерий Хубера-фон Мизеса [7] основан на критерии Трески, но учитывает предположение, что гидростатические напряжения не влияют на материал. отказ. М. Т. Хубер был первым, кто предложил критерий сдвиговой энергии. [8] 92)] }[/математика] Опять же, визуальное представление поверхности текучести может быть построено с использованием приведенного выше уравнения, которое принимает форму эллипса. Фильтр поиска панели навигации
Oxford AcademicУсиление механизмов пластичности кристалловФизика конденсированного состояния КристаллографияКнигиЖурналы
Термин поиска мобильного микросайта Закрыть Фильтр поиска панели навигации
Oxford AcademicУсиление механизмов пластичности кристалловФизика конденсированного состояния КристаллографияКнигиЖурналы
Термин поиска на микросайте Расширенный поиск Иконка Цитировать Цитировать Разрешения Argon, A. ‘4 СОПРОТИВЛЕНИЕ РЕШЕТКИ’ , Механизмы укрепления в кристаллической пластичности , OSMM ( Oxford, 2007; Online Edn, Oxford Academic , 1 сентяб .org/10.1093/acprof:oso/9780198516002.003.0004, , по состоянию на 15 января 2023 г. Выберите формат
Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks) Закрыть Фильтр поиска панели навигации
Oxford AcademicУсиление механизмов пластичности кристалловФизика конденсированного состояния КристаллографияКнигиЖурналы
Термин поиска мобильного микросайта Закрыть Фильтр поиска панели навигации
Oxford AcademicУсиление механизмов пластичности кристалловФизика конденсированного состояния КристаллографияКнигиЖурналы
Термин поиска на микросайте Advanced Search Одним из наиболее фундаментальных сопротивлений движению дислокаций является сопротивление дискретной решетки в чистом кристаллическом материале в диапазоне температур, где диффузия не играет никакой роли. Ключевые слова:
Дислокация Пайерлса-Набарро (P-N), энергия несоответствия ядра, P-N-модель, ГЦК-металлы, ГПУ-металлы, закон Шмидта, ОЦК-металлы, нешмидтовское поведение, перегибы в винтовых дислокациях, фононное увлечение Предмет Физика конденсированного состояния Кристаллография В настоящее время у вас нет доступа к этой главе. Получить помощь с доступом Доступ к контенту в Oxford Academic часто предоставляется посредством институциональных подписок и покупок. Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов: Как правило, доступ предоставляется через институциональную сеть к диапазону IP-адресов. Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией. Выберите этот вариант, чтобы получить удаленный доступ за пределами вашего учреждения. Технология Shibboleth/Open Athens используется для обеспечения единого входа между веб-сайтом вашего учебного заведения и Oxford Academic. Если вашего учреждения нет в списке или вы не можете войти на веб-сайт своего учреждения, обратитесь к своему библиотекарю или администратору. Введите номер своего читательского билета, чтобы войти в систему. Если вы не можете войти в систему, обратитесь к своему библиотекарю. Доступ члена общества к журналу достигается одним из следующих способов: Многие общества предлагают единый вход между веб-сайтом общества и Oxford Academic. Если у вас нет учетной записи сообщества или вы забыли свое имя пользователя или пароль, обратитесь в свое общество. Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам. Смотри ниже. Личную учетную запись можно использовать для получения оповещений по электронной почте, сохранения результатов поиска, покупки контента и активации подписок. Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам. Щелкните значок учетной записи в правом верхнем углу, чтобы: Oxford Academic предлагает широкий ассортимент продукции. Подписка учреждения может не распространяться на контент, к которому вы пытаетесь получить доступ. Если вы считаете, что у вас должен быть доступ к этому контенту, обратитесь к своему библиотекарю. Для библиотекарей и администраторов ваша личная учетная запись также предоставляет доступ к управлению институциональной учетной записью. Здесь вы найдете параметры для просмотра и активации подписок, управления институциональными настройками и параметрами доступа, доступа к статистике использования и т. Внутри поверхности материалы подвергаются упругой деформации. Достижение поверхности означает, что материал подвергается пластическим деформациям.
Внутри поверхности материалы подвергаются упругой деформации. Достижение поверхности означает, что материал подвергается пластическим деформациям. 4 СОПРОТИВЛЕНИЕ РЕШЕТКИ | Механизмы упрочнения пластичности кристаллов
Cite
 S.,
S., Abstract
 Это сопротивление будет рассмотрено с двух механистически различных точек зрения. Во-первых, рассматривается сопротивление Пайерлса-Набарро (ПН), возникающее в результате пульсирующих искажений ядра дислокации при его движении через дискретную решетку, часто влияющих на краевые и винтовые дислокации по-разному и на очень разных уровнях в разных кристаллических структурах. Подробно рассмотрены различные модели этого сопротивления, влияющего на винтовые дислокации, что привело к рассмотрению его зависимости от температуры и скорости деформации во многих ОЦК-металлах и, в меньшей степени, в нелегированных алмазно-кубических Si . Во-вторых, представлена форма повсеместного сопротивления, называемая фононным увлечением, которая возникает в результате взаимодействия движущихся дислокаций с тепловыми колебаниями решетки. Отмечено, что температурная зависимость фононного увлечения радикально отличается от зависимости сопротивления решетки.
Это сопротивление будет рассмотрено с двух механистически различных точек зрения. Во-первых, рассматривается сопротивление Пайерлса-Набарро (ПН), возникающее в результате пульсирующих искажений ядра дислокации при его движении через дискретную решетку, часто влияющих на краевые и винтовые дислокации по-разному и на очень разных уровнях в разных кристаллических структурах. Подробно рассмотрены различные модели этого сопротивления, влияющего на винтовые дислокации, что привело к рассмотрению его зависимости от температуры и скорости деформации во многих ОЦК-металлах и, в меньшей степени, в нелегированных алмазно-кубических Si . Во-вторых, представлена форма повсеместного сопротивления, называемая фононным увлечением, которая возникает в результате взаимодействия движущихся дислокаций с тепловыми колебаниями решетки. Отмечено, что температурная зависимость фононного увлечения радикально отличается от зависимости сопротивления решетки.
Войти
Получить помощь с доступом
Институциональный доступ
Доступ на основе IP
Войдите через свое учреждение

Войти с помощью читательского билета
Члены общества
Войти через сайт сообщества
 Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
Если вы видите «Войти через сайт сообщества» на панели входа в журнале: Вход через личный кабинет
Личный кабинет

Просмотр ваших зарегистрированных учетных записей
Выполнен вход, но нет доступа к содержимому
Ведение счетов организаций



 12.2010
12.2010
