Питтинговая коррозия: Питтинг – суть процесса, методы борьбы с питтинговой коррозией стали
alexxlab | 13.02.2023 | 0 | Разное
Питтинговая коррозия алюминия
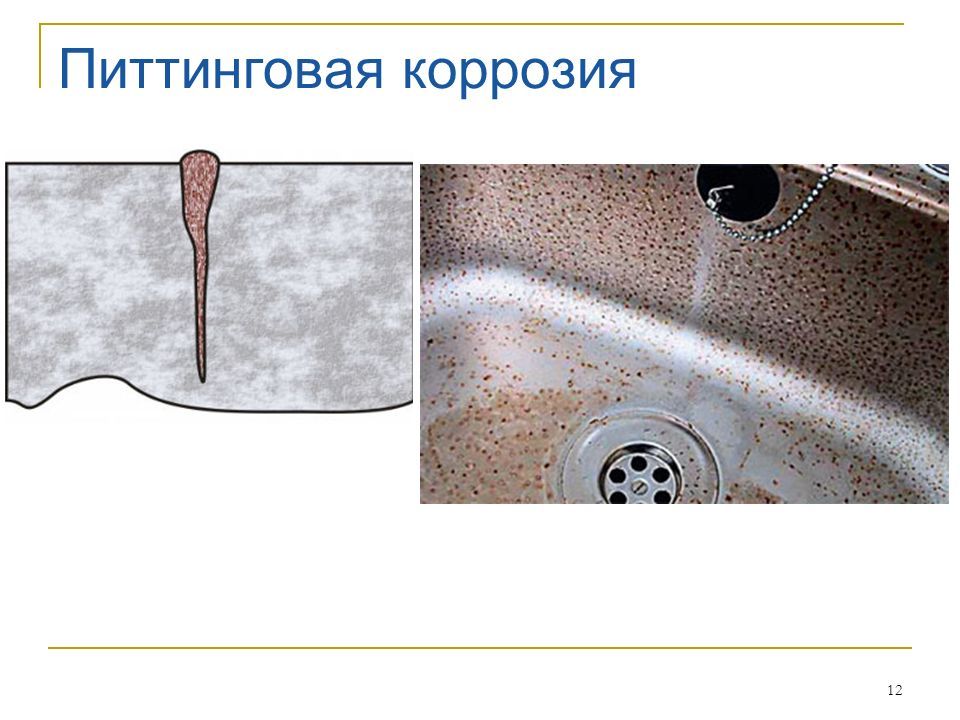
Питтинговая или точечная коррозия
Питтинговая коррозия является наиболее часто встречающимся видом коррозии алюминия и алюминиевых сплавов. Часто ее называют точечной коррозией. Язвы образуются в оксидной пленке алюминия, подверженной воздействию атмосферы, пресной или соленой воды и других нейтральных электролитов. Поскольку в растворах с высокой кислотностью или высокой щелочностью оксидная пленка обычно не устойчива, то питтинговая коррозия бывает только при интервале величины рН от 4,5 до 9,0.
Язвы могут быть мельчайшими и концентрированными или широко разбросанными и различными по размерам в зависимости от химического состава алюминиевого сплава, качества оксидной пленки и свойств корродирующей среды. Явление питтинга может усиливаться наличием щелей и контактов алюминия с другими металлами.
Морфология питтинговой коррозии алюминия
Известно, что хлоридные ионы способны «прорывать» оксидную пленку. Хлорид алюминия (AlCl3) обычно присутствуют в растворе внутри язвы и его концентрация увеличивается при развитии коррозии или при снижении влажности окружающего воздуха. Насыщенный раствор хлорида алюминия имеет величину рН около 3,5, поэтому на дне коррозионных язв коррозия продолжается до тех пор, пока туда еще могут мигрировать кислород и корродирующий электролит. Форма коррозионных язв может меняться от мелких блюдцеобразных до полусферических и далее – до глубоких круглых цилиндрических отверстий. Это отличает питтинговую коррозию от межкристаллитной коррозии, при которой образуются подповерхностные «туннели» вдоль границ зерен, обычно видимые только в микроскоп.
Насыщенный раствор хлорида алюминия имеет величину рН около 3,5, поэтому на дне коррозионных язв коррозия продолжается до тех пор, пока туда еще могут мигрировать кислород и корродирующий электролит. Форма коррозионных язв может меняться от мелких блюдцеобразных до полусферических и далее – до глубоких круглых цилиндрических отверстий. Это отличает питтинговую коррозию от межкристаллитной коррозии, при которой образуются подповерхностные «туннели» вдоль границ зерен, обычно видимые только в микроскоп.
Рисунок – Гальваническая химия точечной коррозии
Рейтинг стойкости к питтинговой коррозии
Сопротивление алюминиевых сплавов питтинговой коррозии существенно зависит от степени их чистоты. Чистый алюминий имеет максимальное сопротивление питтинговой коррозии, а сплавы различных серий по стойкости к питтинговой коррозии располагаются в следующем порядке (в европейских и международных обозначениях): 1ххх – 5ххх – 3ххх – 6ххх – 7ххх – 2ххх.
Технический алюминий
Чистый алюминий (99,00 % и чище) является более стойким к питтинговой коррозии, чем любой из алюминиевых сплавов. Быстрое растворение оксидной пленки происходит только в высоко кислотных или высоко щелочных растворах. В интервале величины рН от 4 до 9 на оксидной пленке могут лишь возникать пятна и легкая локальная питтинговая коррозия. Сверхчистый алюминий (99,999 % и чище) сопротивляется питтинговой коррозии намного более успешно, чем алюминий промышленной чистоты.
Быстрое растворение оксидной пленки происходит только в высоко кислотных или высоко щелочных растворах. В интервале величины рН от 4 до 9 на оксидной пленке могут лишь возникать пятна и легкая локальная питтинговая коррозия. Сверхчистый алюминий (99,999 % и чище) сопротивляется питтинговой коррозии намного более успешно, чем алюминий промышленной чистоты.
Алюминиево-магниевые сплавы
Из всех промышленных алюминиевых сплавов сплавы 5ххх (Al-Mg) с содержанием магния не более 3 % имеют наилучшее сопротивление питтинговой коррозии и самую низкую скорость распространения язв, особенно в морской воде и водных растворах с содержанием хлоридов. Повышение содержания меди всего лишь до 0,2 % резко снижает стойкость этих сплавов к питтинговой коррозии.
Алюминиево-марганцевые сплавы
Следующими по сопротивлению питтинговой коррозии стоят алюминиевые сплавы 3ххх (Al-Mn), такие как 3003 (АМц) и 3004 (Д12). Алюминиево-марганцевые частицы в этих сплавах имеют электрохимический потенциал аналогичный потенциалу алюминия.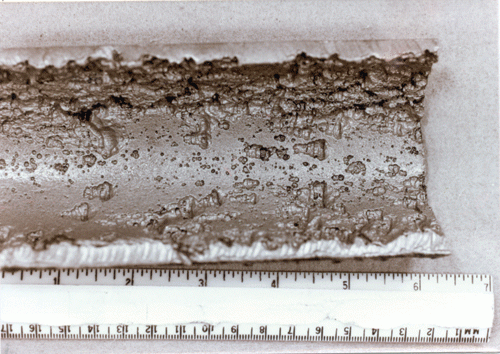 Поэтому при низком содержании меди (до 0,05 %) сплавы 3003 и 3004 имеют сопротивление питтинговой коррозии почти такое же как у чистого алюминия. Повышение содержания меди повышает склонность к питтинговой коррозии в хлоридных растворах и при содержании меди около 0,15 % это влияние становится явным.
Поэтому при низком содержании меди (до 0,05 %) сплавы 3003 и 3004 имеют сопротивление питтинговой коррозии почти такое же как у чистого алюминия. Повышение содержания меди повышает склонность к питтинговой коррозии в хлоридных растворах и при содержании меди около 0,15 % это влияние становится явным.
Медь и железо для питтинговой коррозии алюминия
Медь и железо оказывают наибольшее влияние на склонность к питтинговой коррозии всех алюминиевых сплавов. Хотя сплавы 6ххх (Al-Mg-Si), например, сплав АД31, в целом являются умеренно склонными к питтинговой коррозии, их сопротивление к ней может резко снижаться при повышенном содержании меди и железа, например, сплав АД33 (сплав 6061). Алюминиевые сплавы 7ххх (Al-Zn-Mg) и сплавы 2ххх (Al-Cu-Mg и Al-Cu-Mn), особенно те, что содержат много меди, имеют наименьшее сопротивление питтиниговой коррозии. Поэтому поверхность листов из этих сплавов обычно плакируют – покрывают тонким слоем технического алюминия, например, алюминий марки АД1пл (99,30 %) по ГОСТ 4784-97 или специального алюминиевого сплава с содержанием около 1 % цинка (АЦпл) по тому же стандарту. Сплавы 7ххх без меди (с марганцем или без него) показывают лучшее сопротивление питтинговой коррозии из всех высокопрочных сплавов.
Сплавы 7ххх без меди (с марганцем или без него) показывают лучшее сопротивление питтинговой коррозии из всех высокопрочных сплавов.
Предотвращение питтинговой коррозии алюминия
Типичные подходы к снижению или минимизации питтинговой коррозии основаны на следующих принципах:
- Снижать агрессивность окружающей среды, например, содержание хлоридных ионов, понижать уровень температуры, кислотности и активных окисляющих веществ.
- Тщательно подбирать материалы алюминиевых конструкций. Например, применять по возможности алюминиевые сплавы 5ххх и 3ххх. Высокопрочные алюминиевые сплавы применять только плакированными.
- Тщательно проектировать конструкции: избегать образования щелей, применять циркуляцию и перемешивание жидкостей для предотвращения их застоя, обеспечивать эффективный дренаж жидкостей из конструкций.
Источник: Corrosion of Aluminum and Aluminum Alloys. Edited by J.R. Davis. – ASM International, 1999.
Моделирование питтинговой коррозии в COMSOL Multiphysics®
Когда капля воды попадает на металлическую поверхность, это может привести к возникновению коррозии. При определённых условиях и достаточно длительном времени коррозионного воздействия на металлической поверхности образуется маленькое углубление. Со временем электрохимические условия в таком углублении меняются, вследствие чего нижняя часть поверхности приобретает анодную поляризацию, а удалённая от неё часть — катодную. В результате этого интенсивность коррозии в донной части углубления возрастает, что приводит к увеличению размеров углубления и образованию так называемого питтинга. Моделирование питтинговой коррозии позволяет проанализировать развитие питтингов, возникающих в различных материалах и конструкциях при определённых условиях. В этой статье мы рассмотрим, как построить модель питтинговой коррозии.
При определённых условиях и достаточно длительном времени коррозионного воздействия на металлической поверхности образуется маленькое углубление. Со временем электрохимические условия в таком углублении меняются, вследствие чего нижняя часть поверхности приобретает анодную поляризацию, а удалённая от неё часть — катодную. В результате этого интенсивность коррозии в донной части углубления возрастает, что приводит к увеличению размеров углубления и образованию так называемого питтинга. Моделирование питтинговой коррозии позволяет проанализировать развитие питтингов, возникающих в различных материалах и конструкциях при определённых условиях. В этой статье мы рассмотрим, как построить модель питтинговой коррозии.
Коррозионные процессы. Краткое введение
Гальваническая коррозия возникает при наличии электрического контакта между двумя металлами, атомы которых имеют разные значения энергии сродства к электрону. Если два таких металла поместить в электролит, то на их поверхности образуется двойной электрический слой.
На поверхности благородных металлов (с высоким электрохимическим потенциалом) электроны участвуют в реакции восстановления (катодная реакция). Металлы с меньшим потенциалом отдают электроны и в результате этой анодной реакции растворяются.
Рисунок 1. Схематическое описание гальванической коррозии.
Если позволить электрохимическому процессу, схема которого показана на рис. 1, осуществляться в течение некоторого времени, то металл с меньшим потенциалом (в данном случае это железо) будет растворяться вблизи поверхности контакта с другим металлом (см. рис. 2), потенциал которого выше.
Рисунок 2. В результате гальванической коррозии железо растворяется вблизи области контакта с медью.
Теперь рассмотрим каплю воды на поверхности металла (см. рис. 3). На микроскопическом уровне металл может состоять из разных фаз с отличающимся сродством к электрону. Это означает, что, например, в кристаллитах будут идти катодные реакции, а в межкристаллитных областях — анодные.
рис. 3). На микроскопическом уровне металл может состоять из разных фаз с отличающимся сродством к электрону. Это означает, что, например, в кристаллитах будут идти катодные реакции, а в межкристаллитных областях — анодные.
Рисунок 3. Схема микроструктуры металлической поверхности: показаны кристаллиты и межкристаллитные области.
Согласно схеме, показанной на рис. 2, на той поверхности, где растворяется железо, образуется гидроксид железа. Гидроксид железа — один из компонентов ржавчины. Но если электрохимический процесс идёт по схеме, представленной на рис. 3, тогда ржавчина может появляться на всей поверхности металла, поскольку межкристаллитные области распределены очень равномерно. Такую коррозию обычно называют генерализованной.
Теперь обратимся к рис. 4, на котором показана схема дальнейшего развития генерализованной коррозии, описанной на рис. 3. В центре капли диффузия кислорода к зернам кристаллита занимает больше времени, чем по краям капли, где диффузионный пробег намного короче. На поверхности металла, расположенной под центром капли, концентрация кислорода понижена, что в свою очередь уменьшает электрохимический потенциал в этой части поверхности по отношению к областям по периметру капли. Таким образом, когда потенциал оказывается меньше потенциала пассивации железа, защитный оксидный слой теряет устойчивость. В итоге, кристаллиты, расположенные в центральной части, из-за снижения концентрации кислорода станут анодами. В результате растворения железа в центральной части капли на поверхности металла появляется углубление. Кроме того, ионы железа вступают в реакцию с водой с образованием протонов, из-за чего в углублении снижается водородный показатель pH. Уменьшение pH повышает кислотность среды и, таким образом, ещё сильнее ускоряет коррозию. Описанный процесс получил название эксперимента Эванса с каплей (Evans drop experiment)[1] в честь учёного, который первым объяснил и воспроизвёл этот процесс.
На поверхности металла, расположенной под центром капли, концентрация кислорода понижена, что в свою очередь уменьшает электрохимический потенциал в этой части поверхности по отношению к областям по периметру капли. Таким образом, когда потенциал оказывается меньше потенциала пассивации железа, защитный оксидный слой теряет устойчивость. В итоге, кристаллиты, расположенные в центральной части, из-за снижения концентрации кислорода станут анодами. В результате растворения железа в центральной части капли на поверхности металла появляется углубление. Кроме того, ионы железа вступают в реакцию с водой с образованием протонов, из-за чего в углублении снижается водородный показатель pH. Уменьшение pH повышает кислотность среды и, таким образом, ещё сильнее ускоряет коррозию. Описанный процесс получил название эксперимента Эванса с каплей (Evans drop experiment)[1] в честь учёного, который первым объяснил и воспроизвёл этот процесс.
Концентрацию гидроксильных ионов можно исключить при условии равновесия автопротолиза воды. Концентрацию одного из других ионов, а именно протона, можно исключить, приняв условие электронейтральности. Оба допущения в COMSOL Multiphysics® учитываются автоматически при использовании интерфейса Tertiary Current Distribution, Nernst-Planck
Рисунок 4. Эксперимент Эванса с каплей. Образование углубления приводит к снижению водородного показателя, что дополнительно ускоряет анодную реакцию. –
–
Предположим, что в результате электроосаждения внутри углубления образовался пористый слой, поэтому будем рассматривать углубление как пористую структуру, поры которой заполнены электролитом. Это разумное предположение, поскольку из того металла, на месте которого образовалось углубление, с высокой вероятностью сформируется пористое отложение. Задачу будем решать в двумерной осесимметричной постановке, как показано на рис. 5.
5.
Рисунок 5. Геометрическая модель расчётной области.
Реакция растворения металла моделируется на всей границе, обозначенной на рис. 5 как «Fe electrode surface». Будем считать, что скорость анодной реакции пропорциональна концентрации протонов. Такая зависимость характерна для условий повышенной кислотности в присутствии хлорида [2]. Чтобы связать перемещение границы расчётной области с интенсивностью растворения железа, воспользуемся методом подвижной сетки.
Как мы уже отмечали, реакция восстановления кислорода не моделируется. Мы заменяем моделирование этого процесса на граничное условие постоянного электрического потенциала электролита вдали от углубления на горизонтальной границе, которая обозначена как «Bulk electrolyte boundary». Также на этой границе мы зададим концентрацию ионов натрия, хлорида и железа.
Будем считать, что в области, занятой электролитом, в том числе в углублении, идут реакции автопротолиза воды и образования гидроксида железа. Отметим, что гидроксид расходуется в реакции образования Fe(OH)
Отметим, что гидроксид расходуется в реакции образования Fe(OH)
Начальные значения концентраций и электрического потенциала электролита рассчитываются с помощью решения стационарной задачи для исходной геометрической модели. То есть для получения начальных значений задача решается для неизменяемой геометрической модели с указанными выше граничными условиями с помощью стационарного решателя. В результате получается некоторое распределение концентраций и электрического потенциала электролита для t = 0. Это решение является начальным условием для нестационарной задачи.
Результаты
Использование стационарного решения в качестве начальных условий является разумным подходом, поскольку изменение состава и электрического потенциала электролита сначала, то есть в течение первых суток, происходит довольно медленно.
На рис. 6 показано, как увеличится углубление по истечении 30 дней. Для области внутри углубления характерен большой градиент потенциала электролита. В углублении потенциал электролита изменяется от 0,43 мВ до 16,5 мВ, тогда как за пределами углубления потенциал изменяется от 0 мВ до 0,43 мВ в течение 30 дней. Отметим, что интенсивность процессов переноса в углублении ниже, поскольку эта область представляет собой пористую среду с более низкими по сравнению с электролитом снаружи эффективными свойствами переноса. Качественно такое же распределение потенциала наблюдается в течение всего моделируемого периода времени, при этом донная часть углубления увеличивается в размерах быстрее, чем устье. По этой причине проходное сечение для переноса заряда в устье углубления сужается, что приводит к большим градиентам потенциала электролита. В результате мы действительно наблюдаем коррозию на плоской поверхности. Через 30 дней поверхность сместится примерно на 0,35 мкм, а смещение донной части углубления составит 1,45 мкм.
Для области внутри углубления характерен большой градиент потенциала электролита. В углублении потенциал электролита изменяется от 0,43 мВ до 16,5 мВ, тогда как за пределами углубления потенциал изменяется от 0 мВ до 0,43 мВ в течение 30 дней. Отметим, что интенсивность процессов переноса в углублении ниже, поскольку эта область представляет собой пористую среду с более низкими по сравнению с электролитом снаружи эффективными свойствами переноса. Качественно такое же распределение потенциала наблюдается в течение всего моделируемого периода времени, при этом донная часть углубления увеличивается в размерах быстрее, чем устье. По этой причине проходное сечение для переноса заряда в устье углубления сужается, что приводит к большим градиентам потенциала электролита. В результате мы действительно наблюдаем коррозию на плоской поверхности. Через 30 дней поверхность сместится примерно на 0,35 мкм, а смещение донной части углубления составит 1,45 мкм.
Рисунок 6. Размеры донной части углубления увеличиваются быстрее, чем размеры устья. Это приводит к большему градиенту потенциала электролита вблизи устья.
Это приводит к большему градиенту потенциала электролита вблизи устья.
Изменение водородного показателя в процессе коррозии показано на рис. 7. Значение водородного показателя в донной части через сутки равно 9,48, а через 30 суток — 9,14. Может показаться, что это незначительное изменение, однако оно соответствует увеличению концентрации протонов в 2,2 раза. Константа скорости коррозионного процесса пропорциональна концентрации протонов, а значит и скорость коррозии тоже возрастает.
Рисунок 7. Водородный показатель в углублении в различные моменты времени.
На рис. 8 приведены значения скорости коррозии в мкм/сут для четырех моментов времени, показанных выше. Максимальная скорость коррозии в донной части углубления через 30 дней в 2,3 раза выше по сравнению со скоростью коррозии через 1 день. Соответственно, концентрация протонов через 30 дней в 2,2 раза выше, чем через 1 день.
Рисунок 8. Скорость коррозии на поверхности металла в разные моменты времени.
Распределение концентрации ионов натрия обратно распределению концентрации ионов железа. Причина — условие электронейтральности. По мере того, как ионы железа попадают в электролит, ионы натрия выталкиваются из углубления. В отличие от ионов натрия, ионы хлорида, наоборот, движутся в углубление, вследствие условия электронейтральности (не показаны).
Рисунок 9. Концентрация ионов натрия в различные моменты времени.
Расчётная модель демонстрирует эффект «порочного круга» питтинговой коррозии. Интенсивность процесса растёт с течением времени, пока углубление не станет достаточно глубоким. Тогда омические потери и продукты коррозии ограничивают скорость реакции.
Заключение
Расчётную модель можно усложнить, если добавить учёт материального баланса осажденных продуктов коррозии. Плотность продуктов реакции меньше, чем плотность железа, поэтому они образуются в углублении, но затем вытесняются из него. Этот процесс можно смоделировать, если пористость сделать зависимой переменной и учесть конвективный перенос оксидов.
Ещё одно направление усложнения модели — введение в неё полной геометрической модели капли, что позволит учесть диффузию и восстановление кислорода.
Кроме того, модель можно дополнить более подробным описанием химическим процессов. Например, можно учесть образование различных ионов железа, описать дополнительные окислительно-восстановительные реакции, а также включить в модель больше различных оксидов и гидроксидов железа, образующихся на поверхности металла. Тем не менее, мы можем поэкспериментировать и с исходной моделью, которая сама по себе уже является достаточно комплексной, несмотря на относительную простоту её построения.
Дальнейшие шаги
Узнайте о функциональных возможностях модуля «Коррозия», кликнув по кнопке:
Описание модуля
Источники
- U.R. Evans, “Corrosion and Oxidation of Metals”, Amolds, p. 118., 1960.
- H.C. Kuo and K. Nobe, “Electrodissolution Kinetics of Iron in Chloride Solutions”, J. of Electrochem.
 Soc, vol. 125, no.6, 1978.
Soc, vol. 125, no.6, 1978.
Питтинг Определение и значение — Merriam-Webster
питтинг ˈpi-tiŋ
1
: расположение ям
2
: действие или процесс формирования ям
3
: объединение петухов для борьбы
Примеры предложений
На краске автомобиля было видно, что изрыт из-за летящего гравия.
На ее лице были незначительные изъязвления от ветряной оспы.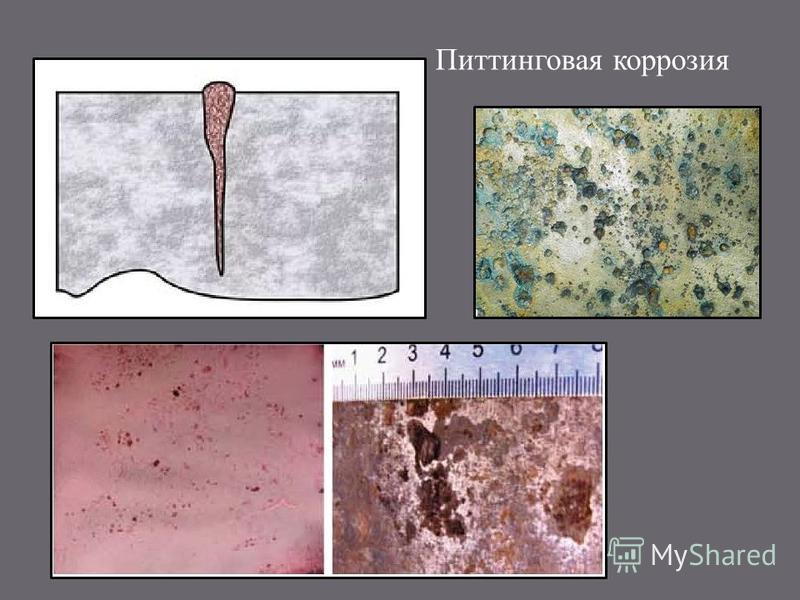
Недавние примеры в Интернете
На последних изображениях New Horizons видны неясные шестиугольные ряби, возможно, из-за циркуляции этих мягких льдов, и широко распространенные ямки , скорее всего, из-за прямого испарения частей твердой поверхности (процесс, известный как сублимация).
— Кори С. Пауэлл, 9 лет.0025 Журнал Discover , 31 декабря 2015 г.
Критики говорят, что Castroville обыграли — фальшивый , противопоставляющий одного недостаточно обслуживаемого сообщества другому.
— Розанна Ксиастафф, писатель, Los Angeles Times , 18 ноября 2022 г.
Чтобы избежать точечной коррозии или других повреждений поверхности, никогда не используйте абразивные инструменты, агрессивные чистящие средства или кислотные ингредиенты, такие как уксус или лимонный сок, для очистки этих раковин.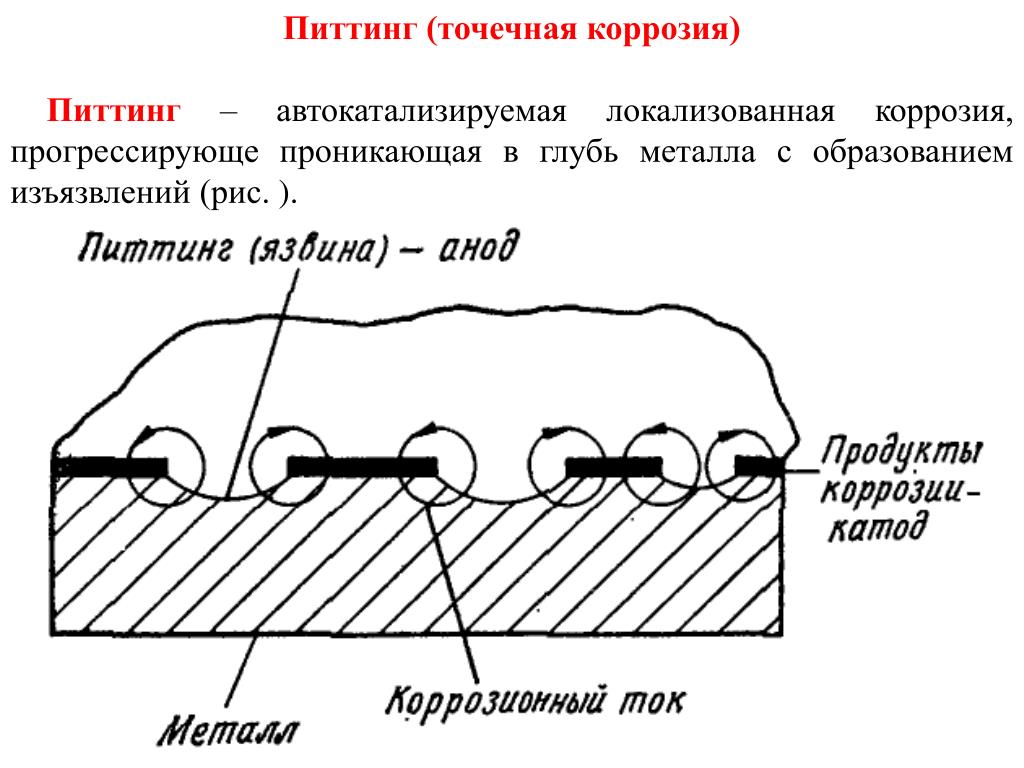 — Джессика Беннетт, 9 лет.0025 Better Homes & Gardens , 8 сентября 2022 г.
Чтобы избежать точечной коррозии или других повреждений поверхности, никогда не используйте абразивные инструменты, агрессивные чистящие средства или кислотные ингредиенты, такие как уксус или лимонный сок, для очистки этих раковин.
— Джессика Беннетт, Better Homes & Gardens , 8 сентября 2022 г.
Чтобы избежать точечной коррозии или других повреждений поверхности, никогда не используйте абразивные инструменты, агрессивные чистящие средства или кислотные ингредиенты, такие как уксус или лимонный сок, для очистки этих раковин.
— Джессика Беннетт, 9 лет.0025 Better Homes & Gardens
— Джессика Беннетт, 9 лет.0025 Better Homes & Gardens , 8 сентября 2022 г.
Чтобы избежать точечной коррозии или других повреждений поверхности, никогда не используйте абразивные инструменты, агрессивные чистящие средства или кислотные ингредиенты, такие как уксус или лимонный сок, для очистки этих раковин.
— Джессика Беннетт, Better Homes & Gardens , 8 сентября 2022 г.
Чтобы избежать точечной коррозии или других повреждений поверхности, никогда не используйте абразивные инструменты, агрессивные чистящие средства или кислотные ингредиенты, такие как уксус или лимонный сок, для очистки этих раковин.
— Джессика Беннетт, 9 лет.0025 Better Homes & Gardens
 — Дэйв Вандерверп, Автомобиль и водитель , 26 августа 2022 г.
Войны советов в Чикаго разразились 2 мая 1983 года, когда 29 олдерменов осознали силу излюбленного сценария профессоров политических наук: противопоставляет слабого мэра сильному городскому совету.
—Chicago Tribune Staff, Chicago Tribune , 19 июня 2022 г.
Но псориатический артрит может вызывать и другие проблемы со здоровьем, в том числе усталость, образование ямок на ногтях и боль в глазах.
— Кэсси Шортслив, Good Housekeeping , 27 августа 2021 г.
Узнать больше
— Дэйв Вандерверп, Автомобиль и водитель , 26 августа 2022 г.
Войны советов в Чикаго разразились 2 мая 1983 года, когда 29 олдерменов осознали силу излюбленного сценария профессоров политических наук: противопоставляет слабого мэра сильному городскому совету.
—Chicago Tribune Staff, Chicago Tribune , 19 июня 2022 г.
Но псориатический артрит может вызывать и другие проблемы со здоровьем, в том числе усталость, образование ямок на ногтях и боль в глазах.
— Кэсси Шортслив, Good Housekeeping , 27 августа 2021 г.
Узнать больше Эти примеры предложений автоматически выбираются из различных онлайн-источников новостей, чтобы отразить текущее использование слова «питтинг». Мнения, выраженные в примерах, не отражают точку зрения Merriam-Webster или ее редакторов. Отправьте нам отзыв.
Мнения, выраженные в примерах, не отражают точку зрения Merriam-Webster или ее редакторов. Отправьте нам отзыв.
История слов
Первое известное использование
1593, в значении, определенном во втором смысле
Путешественник во времени
Первое известное использование питтинг был в 1593 г.
Посмотреть другие слова того же года питтиды
точечная коррозия
зритель последних рядов партера
Посмотреть другие записи поблизости
Процитировать эту запись0003
«Питтинг». Словарь Merriam-Webster.com , Merriam-Webster, https://www. merriam-webster.com/dictionary/pitting. По состоянию на 2 февраля 2023 г.
яма
merriam-webster.com/dictionary/pitting. По состоянию на 2 февраля 2023 г.
яма
Медицинское определение
точечная корка
существительное
1
: действие или процесс образования ямок (например, в угревой коже, зубе или зубной реставрации) при надавливании пальцем или тупым предметом и исчезает лишь медленно после снятия давления при некоторых формах отека
Еще от Merriam-Webster на
точечная коррозияТезаурус: Все синонимы и антонимы слова pitting
Английский: Перевод pitting для говорящих на испанском языке
Последнее обновление: – Обновлены примеры предложений
Подпишитесь на крупнейший словарь Америки и получите тысячи дополнительных определений и расширенный поиск без рекламы!
Merriam-Webster без сокращений
предвещать
См. Определения и примеры »
Определения и примеры »
Получайте ежедневно по электронной почте Слово дня!
Слова, названные в честь людей
- Тёзка купальника Жюль Леотар какую профессию имел?
- Пожарный Врач хирург
- Судья Акробат
Проверьте свой словарный запас с помощью нашей викторины из 10 вопросов!
ПРОЙДИТЕ ТЕСТ
Сможете ли вы составить 12 слов из 7 букв?
ИГРАТЬ
Питтинг Определение и значение | Dictionary.com
- Основные определения
- Викторина
- Связанное содержимое
- Примеры
Показывает уровень оценки в зависимости от сложности слова.
1
[пит-инг]
/ ˈpɪt ɪŋ /
Сохранить это слово!
См. синонимы для: pitting / pittings на Thesaurus.com
Показывает уровень оценки в зависимости от сложности слова.
сущ.
действие или операция по рытью ямы или ям.
действие или операция по размещению в яме или ямах.
организация петушиных боев.
ВИКТОРИНА
ВЫ ПРОЙДЕТЕ ЭТИ ГРАММАТИЧЕСКИЕ ВОПРОСЫ ИЛИ НАТЯНУТСЯ?
Плавно переходите к этим распространенным грамматическим ошибкам, которые ставят многих людей в тупик. Удачи!
Вопрос 1 из 7
Заполните пропуск: Я не могу понять, что _____ подарил мне этот подарок.
Происхождение питтинга
1
Впервые отмечено в 1655–1665 гг.; pit 1 + -ing 1
Слова рядом pitting
лаваш, питакус, pittance, без косточек, pitter-patter, pitting, pittosporum, Pitt-Rivers, Pittsburg, Pittsburgh, Pittsburg Landing
Другие определения для pitting (2 of 2)
pitting 2
[ pit-ing ]
/ ˈpɪt ɪŋ /
действие удаления ямы
3 90
Происхождение питтинга
2
яма 2 + -ing 1
Dictionary. com Unabridged
На основе Random House Unabridged Dictionary, © Random House, Inc., 2023
com Unabridged
На основе Random House Unabridged Dictionary, © Random House, Inc., 2023
Слова, связанные со шурфованием
бурение, бурение, рытье нор, рытье, долбление, разведка, добыча полезных ископаемых, черпание, выемка отверстий, прокладка туннелей, раскопки
Как использовать косточку в предложении
Помимо процесса косточки, разница между ними заключается в том, что плоды без косточек более сочные и немного слаще, что делает их идеальными для консервирования и консервирования.
Путеводитель по косточковым фруктам: как их выбирать, созревать, хранить и готовить с ними|Аарон Хатчерсон|9 июля 2021 г.|Washington Post
Джони Эрнст в Айове.
Крайне правый радиоведущий, который мог передать Сенат Республиканской партии|Бен Джейкобс|6 октября 2014|DAILY BEAST
Ничто так не подвергает ботаников испытанию, как противопоставление одного научно-фантастического/фэнтезийного сериала другому.
Лучшее вирусное видео за апрель|Видео The Daily Beast|30 апреля 2014 г.
 |DAILY BEAST
|DAILY BEASTК 2006 году «Аль-Каида» в Ираке ввергла страну в гражданскую войну, натравливая шиитов на суннитов.
Следующим возвращением «Аль-Каиды» могут стать Афганистан и Пакистан|Брюс Ридель|13 января 2014 г.|DAILY BEAST
Когда официально начинается гонка между президентом Обамой и Миттом Ромни, освещение кампании становится поверхностным и путаным.
10 книг, которые стоит прочитать в преддверии выборов: Цицерон, Видаль и другие|Дэвид Маскиотра|6 сентября 2012 г.|DAILY BEAST
Говард Курц анализирует неприятные истории, противопоставляя мистера Неэффективного мистеру Денежному мешку.
Почему средства массовой информации не любят и Барака Обаму, и Митта Ромни|Говард Курц|23 августа 2012 г.|DAILY BEAST
И снова большие гаубицы возглавили адский оркестр, изрыгая лицо ничейной земли угольно-черными пятнами.
Дневник Галлиполи, Том I|Иан Гамильтон
Большая поклонница принципа «Разделяй, чтобы править», она научилась искусству постоянно противопоставлять одну силу другой.



 Soc, vol. 125, no.6, 1978.
Soc, vol. 125, no.6, 1978. |DAILY BEAST
|DAILY BEAST