Самые теплопроводные металлы: Теплопроводность чистых металлов. Таблица теплопроводности металлов
alexxlab | 29.01.2023 | 0 | Разное
Самый теплопроводный металл: общие характеристики • Люди
Именно серебро лидирует в этом негласном конкурсе, имея теплопроводность в 408 Ватт на метр помноженный на Кельвин, опережая по этому показателю такие элементы с высоким коэффициентом удельной теплопроводности, как медь (384 Вт/(м*К), золото (312 Вт/(м*К) и алюминий (203 Вт/(м*К).
Будучи обладателем пальмы первенства, самый теплопроводный металл имеет наиболее широкое применение в различных сферах производства, причем, список того, где можно использовать серебро, можно продолжать до чуть ли не до бесконечности. Примечательно, что благодаря своим уникальным качествам, наиболее теплопроводный металл в мире использовался с самых давних времен, ведь согласно сохранившихся исторических очерков, еще воины древнего Египта широко использовали серебро для максимального ускорения процесса заживления ран и увечий, полученных в жестоких боях. Так, изготавливая тоненькие пластинки из чистого серебра и прикладывая их к ранам различны типов, они с удивлением отмечали целебные свойства, которыми обладал этот благородный металл.
Нельзя не уделить внимание той огромной роли серебра, которую оно играло для православия, ведь в большинстве русских церквей все сосуды и атрибутику старались изготавливать именно из него и ни для кого не секрет, что посеребренная вода, именуемая святой, способна сохранятся годами в закрытых емкостях, не меняя при этом свой цвет и запах. А все потому, что серебро способно выступать, как своеобразное средство для дезинфекции, применимое не только для воды. Однако, на этом полезные свойства данного металла отнюдь не заканчиваются, ведь помимо высокой теплопроводности, он обладает отличной электропроводностью, а также совершенно не подвержен процессам окисления даже при длительном контакте с влажной средой. Благодаря своим многочисленным уникальным свойствам, серебро широко используется для изготовления мелких комплектующих для различного рода электроприборов, и именно поэтому техника с деталями из этого благородного металла пользуется таким большим спросом.
Рассуждая на тему о сферах применения серебра, невозможно упустить из внимания тот вклад, который продолжает вносить этот металл в ювелирное искусство, ведь оно пользуется не меньшей популярностью, чем золото.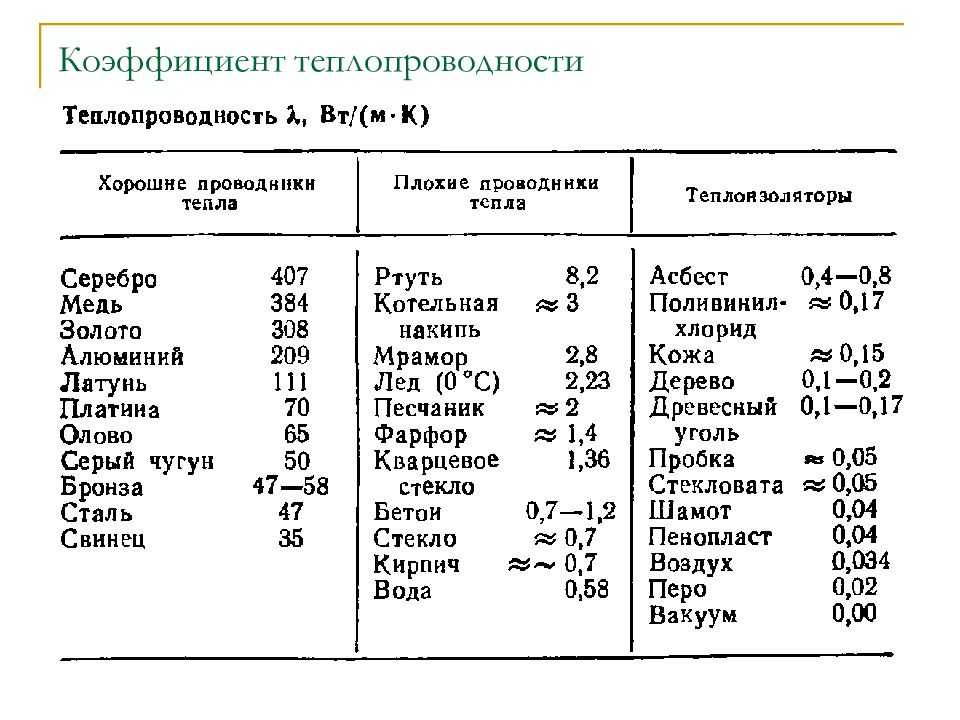 Причем, помимо всевозможных колец, сережек и браслетов, серебро используется для изготовления изысканных столовых приборов и различного рода декоративных элементов, в том числе интерьерных. И речь идет не только о красоте, но и о функциональности. В качестве примера можно привести зеркала, которые вместо традиционного алюминия покрывают тончайшим слоем серебра, чтобы улучшить их отражающую способность. Кроме того, серебро прекрасно подходит для изготовления целого ряда вспомогательных инструментов и довольно сложно придумать лучший материал, с помощью которого можно будет выполнять чеканку монет и орденов. При этом использовать его можно не только в чистом виде, но и во всевозможных сплавах и соединениях.
Причем, помимо всевозможных колец, сережек и браслетов, серебро используется для изготовления изысканных столовых приборов и различного рода декоративных элементов, в том числе интерьерных. И речь идет не только о красоте, но и о функциональности. В качестве примера можно привести зеркала, которые вместо традиционного алюминия покрывают тончайшим слоем серебра, чтобы улучшить их отражающую способность. Кроме того, серебро прекрасно подходит для изготовления целого ряда вспомогательных инструментов и довольно сложно придумать лучший материал, с помощью которого можно будет выполнять чеканку монет и орденов. При этом использовать его можно не только в чистом виде, но и во всевозможных сплавах и соединениях.
Так, определенные химические соединения, в которых принимает непосредственное участие аргентум, активно используются для изготовления зарядных батарей аккумуляторов, которые славятся своей способностью при относительно малом внутреннем сопротивлении генерировать большой ток.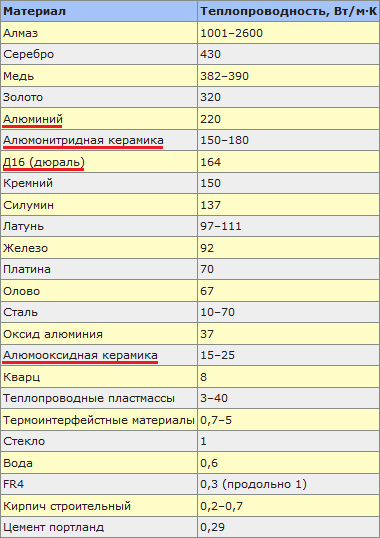
Последние опубликованные
Самая большая свинья в мире: где она живет? Рейтинг детских смесей: самые популярные производители
Тема “Этот удивительный мир металлов”
Тема. Этот удивительный мир металлов.
Цель и задачи:
Ø закрепить знания о свойствах металлов, способах получения, их нахождении в природе, основных областях применения;
Ø акцентировать внимание учащихся на возможности интеграции курсов химии, биологии, литературы, истории…
Ø развивать умения выделять главное, сравнивать и обобщать;
Ø развивать представления о причинно – следственных связях явлений, познаваемости мира.
Оборудование и вещества:
– на столах
учащихся: коллекция
металлов, тигельные щипцы, алюминиевая фольга, железный гвоздь, елочная
игрушка, зеркало, стеклянные пластинки (2шт. ), вода, периодическая таблица и
таблица растворимости;
), вода, периодическая таблица и
таблица растворимости;
– на демонстрационном столе:
– стенд с подборкой фотографий по теме «Твоих оград узор чугунный»
Формы и методы обучения: объяснительно – иллюстративный, демонстрационный, частично – поисковый, эксперимент, беседа, ИКТ.
Ход урока.
Девиз урока: МЕТАЛЛ – ВСЕХ НЕДР ЗЕМНЫХ ВЛАДЫКА. Организационный момент.
( Каждому учащемуся до начала урока учитель выдаёт по 3 кружка бумаги разных цветов).
Изучение новой темы.
Стадия вызова (блиц-опрос).
Ø
Алхимики
считали, что на небе 7 светил и каждое из них имеет своего посланца: «Семь
металлов создал свет по числу семи планет…» Назовите эту семерку.
Ø Какой металл загорается в холодной воде?
Ø Почему свежий разрез яблока на воздухе буреет?
Ø Какой металл плавится от тепла человеческой руки?
Ø Если бы существовал приз «за активность», то атомам какого из металлов вы бы его присудили?
Ø Какой из металлов в глубокой древности называли «небесной медью» и почему?
Ø Какое молоко не пьют?
Ø От соединений каких металлов зависит красный цвет крови и зеленая окраска растений?
Стадия реализации и осмысления.
Что означает слово « металл»? Каков его смысл? (слово « металл» может означать простое вещество и химический элемент.) Составляем с учащимися кластер в тетради и на доске – что мы знаем о металлах (слайд 5)
I – металлы как химические элементы.
1. Положение в ПС (слайд 6).
2. Строение
атома (слайд 7).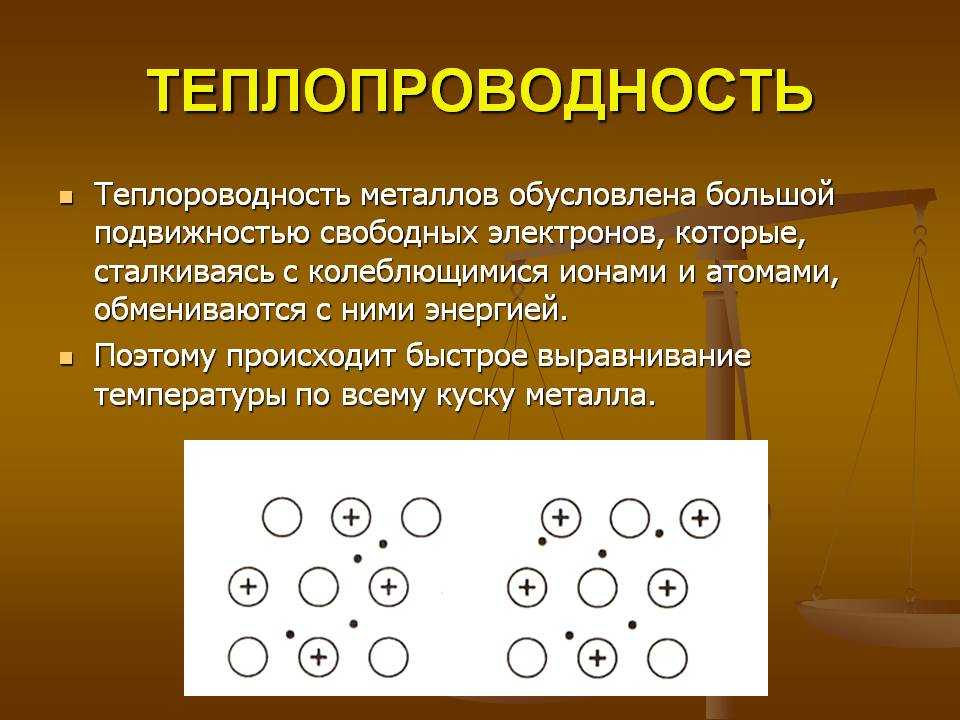
У s– и p-элементов электроны накапливаются на внешнем энергетическом уровне s -и p- подуровнях.
Na +11 (2 8 1 ) 1s22s22p6 3s1
Ga +31 (2 8 18 3) …3s23p63d10 4s24p1
У d – элементов электроны накапливаются на предпоследнем уровне d- подуровне.
Sc+21 (2 8 9 2) …3s23p63d14s2
3. Степень окисления (слайд 8).
Степень окисления:
– в свободном виде – 0;
– высшая, как правило, равна номеру группы:
Na+1, Ca+2, Al+3 …
4. Характер и свойства элемента (слайд 8, 9).
Характер – металлический.
Восстановительные свойства:
– в периоде – уменьшаются: Ra уменьшается
– в группах – возрастают: Ra увеличивается
II – металлы как
простые вещества.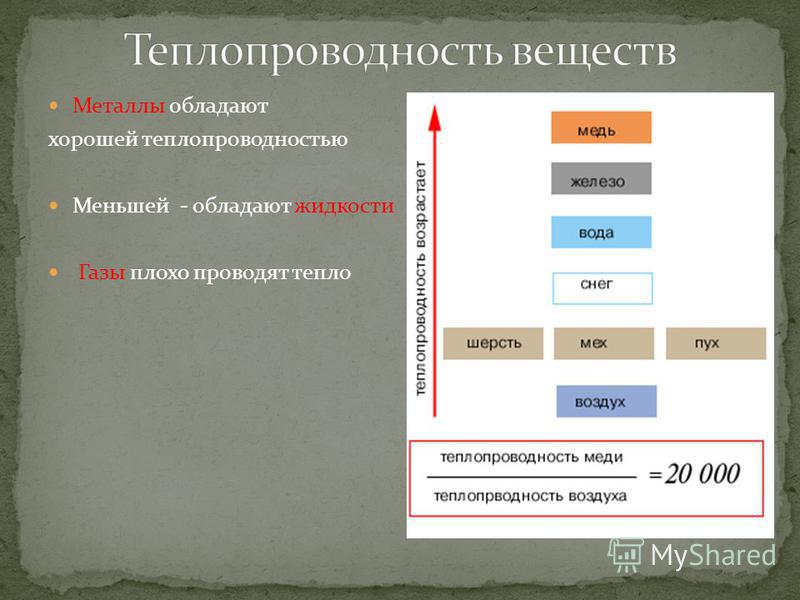
1. Формула простого вещества (слайд 10).
– Mg, Na, Fe…
2. Аллотропные модификации (слайд 10).
Некоторые металлы кристаллизуются в 2 или более кристаллических формах: Fe, Sn.
3.Вид химической связи (слайд 10).
Металлическая связь.
4. Тип кристаллической решетки (слайд 10)
Металлическая кристаллическая
решетка. Металлические
элементы чаще всего кристаллизуются в трех типах
структур:
– объемно-центрированные – тип вольфрама (W,Cr, Fe, K, Li, Mo, Na, V),
– гранецентрированные – тип меди (Cu, Ba, Al, Au, Ph, Pd, Pt, Sr),
– гексагональные – тип магния (Mg, Be, Cd, Ti, Zn).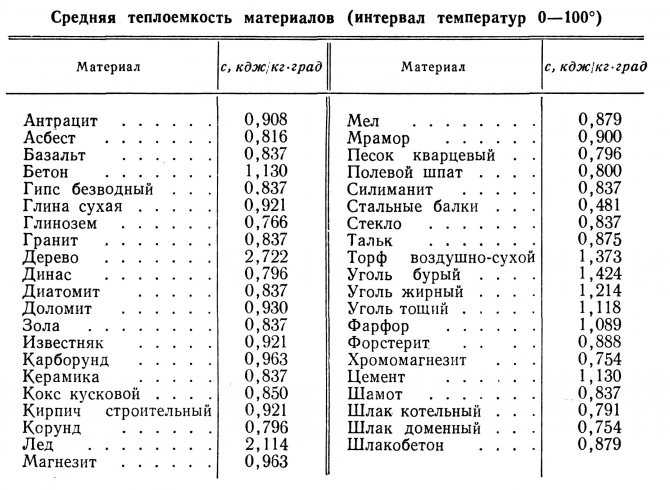
( рассматриваем к.р.)
5. Физические свойства (слайд 11-14).
Великий русский ученый М.В. Ломоносов так говорил о металлах: Металлом называется твердое, непрозрачное и светлое тело, которое на огне плавить и холодное ковать можно». ? О каких физических свойствах металлов идет речь? (учащиеся дают ответ, рассматривают коллекцию)
Характерная черта металлов – способность к пластическим деформациям. Под пластической деформацией металлического кристалла следует понимать изменение его внешней формы под воздействием механических факторов, не приводящих ни к разрушению его на части, ни к изменению объема. Если кристалл ковкого металла подвергается давлению в определенном направлении, то атомы в нем могут перемещаться параллельно одной из атомных плоскостей. Это явление называется скольжением. Чтобы понять это явление учащиеся проводят простой эксперимент.
ЛО 1. Две
стеклянные пластинки накладывают друг на друга. Их легко разъединить. Затем на
поверхность пластин наносят несколько капель воды. Пластинки легко скользят
одна относительно другой, но с трудом отрываются друг от друга.
Пластинки легко скользят
одна относительно другой, но с трудом отрываются друг от друга.
? Какова роль воды? (Прослойка воды – модель «электронного газа»)
Обратите внимание на внешний вид пластин, посмотрите в зеркало. Какое свойство металлов используют при изготовлении зеркал, елочных игрушек? (металлический блеск и непрозрачность) По металлическому блеску на первом месте серебро.
Важное свойство металлов – их температура плавления.
ЛО 2. Учащиеся проводят эксперимент: нагревают гвоздь и алюминиевую фольгу.
? Почему фольга изменяет форму, а гвоздь нет?
Итак, металлы бывают легкоплавкие и тугоплавкие. Самый легкоплавкий металл – ртуть (-390), тугоплавкий – вольфрам (34200)
Плотность металлов различна. Самым легким является литий (0,54 г/см3), а самым тяжелым – осмий (22,6 г/см3).
Следующее свойство –
электропроводность и теплопроводность. Самые электропроводные металлы –
серебро, медь, золото, а самые теплопроводные – серебро, медь, алюминий, железо.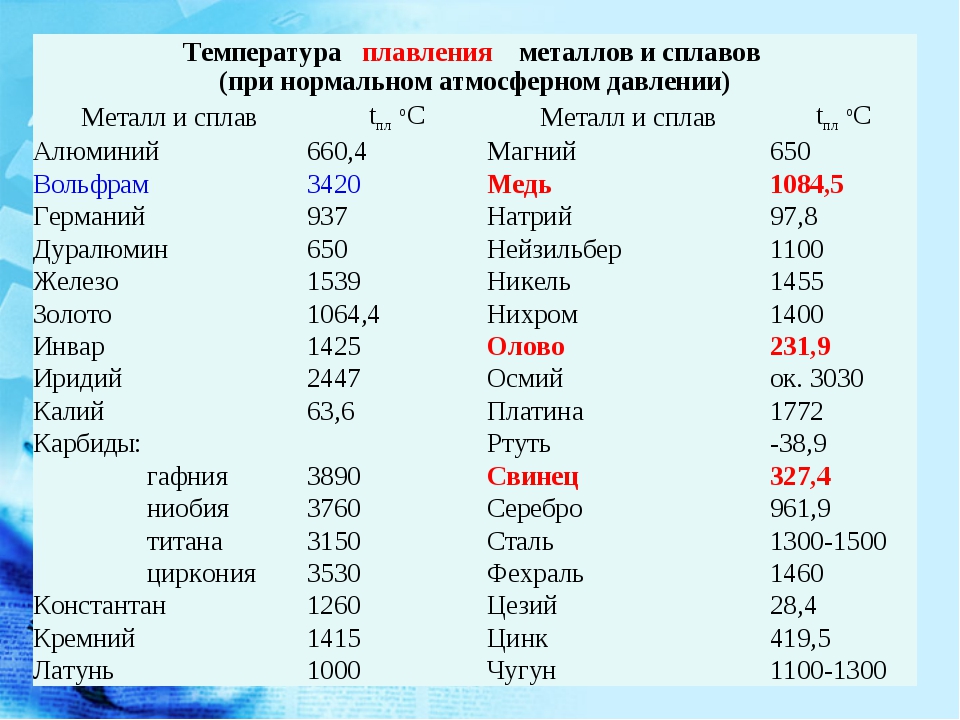 Нагревание металла приводит к росту электрического сопротивления вследствие
увеличения амплитуды колебаний ионов и скорости беспорядочного движения
электронов. При низкой температуре электропроводность металлов возрастает.
Существует группа металлов (около 10), электрическое сопротивление которых при
температурах близких к абсолютному нулю, падает до нуля. Самой высокой
температурой перехода в такое состояние сверхпроводимости обладает ниобий (9К),
а самой низкой – гафний (0,3К).
Нагревание металла приводит к росту электрического сопротивления вследствие
увеличения амплитуды колебаний ионов и скорости беспорядочного движения
электронов. При низкой температуре электропроводность металлов возрастает.
Существует группа металлов (около 10), электрическое сопротивление которых при
температурах близких к абсолютному нулю, падает до нуля. Самой высокой
температурой перехода в такое состояние сверхпроводимости обладает ниобий (9К),
а самой низкой – гафний (0,3К).
Металлы бывают мягкие (калий, натрий можно резать ножом) и твердые (вольфрам и хром – изготавливают режущие и бурильные инструменты)
? Чем обусловлены общие свойства металлов?
? Заполните пропуски нужными словами:
· Радиус атомов металлов …………… радиуса атомов неметаллов.
· Во всех соединениях… ……………….. металлов имеют………………. Степени окисления.
·
При комнатной температуре металлы находятся в …………….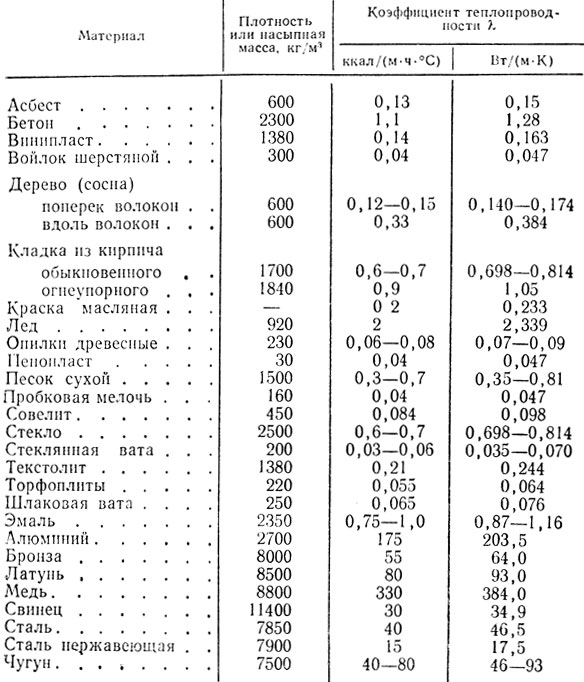 . агрегатном состоянии, за исключением ……………. .
. агрегатном состоянии, за исключением ……………. .
· Они хорошо проводят ……………. И ………………..
Самый тяжелый металл ……………, самый легкий ………………., самый тугоплавкий …………………, самый легкоплавкий …………………… .
6. Химические свойства.
А) взаимодействие с простыми веществами; (слайд 15).
• Ме +H2O = Ме(OH)n +H2
• Ме +H2O = МеnOm + H2↑
• Ме + к-та = соль + H2↑ (иск.HNO3)
• Ме + соль = соль1 + Ме1 (иск. щелочные и щелочноземельные Ме)
ДО 1. Взаимодействие натрия с водой.
Б) взаимодействие со сложными веществами; (слайд 16).
• Ме +H2O = Ме(OH)n +H2↑
• Ме +H2O = МеnOm + H2↑
•
Ме
+ к-та = соль + H2↑ (иск.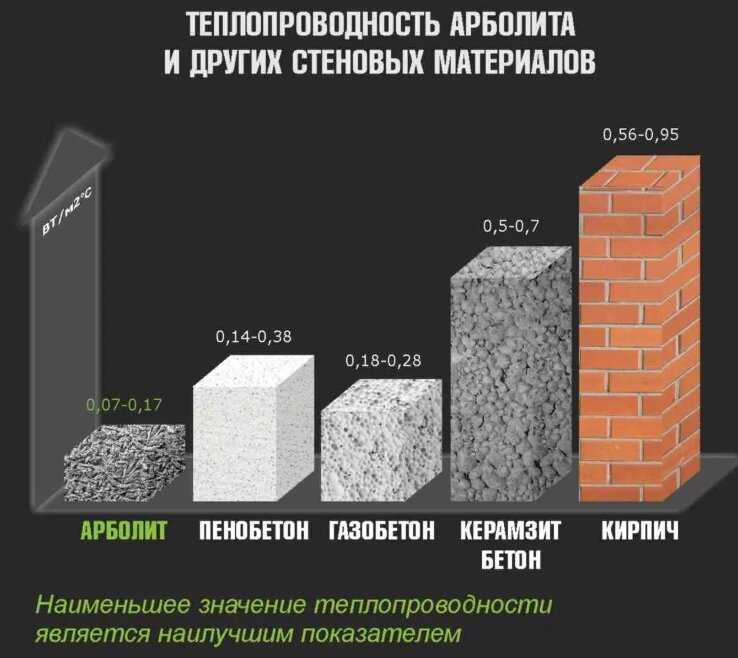 HNO3)
HNO3)
• Ме + соль = соль1 + Ме1 (иск. щелочные и щелочноземельные Ме)
ДО 2. Взаимодействие металлов с растворами солей: цинковую пластинку опускаем в раствор сульфата меди(II)
? Можно ли растворить медный купорос в оцинкованном ведре?
? Будет ли серебро растворяться в растворе хлорида меди?
? Можно ли кипятить в алюминиевой миске раствор соды?
? Закончите уравнения возможных реакций:
Na + H2O = Mg + O2 =
Ag + H2O = Zn + HCl =
Zn + CuSO4 = Na + Cl2 =
Cu + AgNO3 = Al + ZnCl2 =
III. Способы получения металлов (слайд 18).
IV. Применение.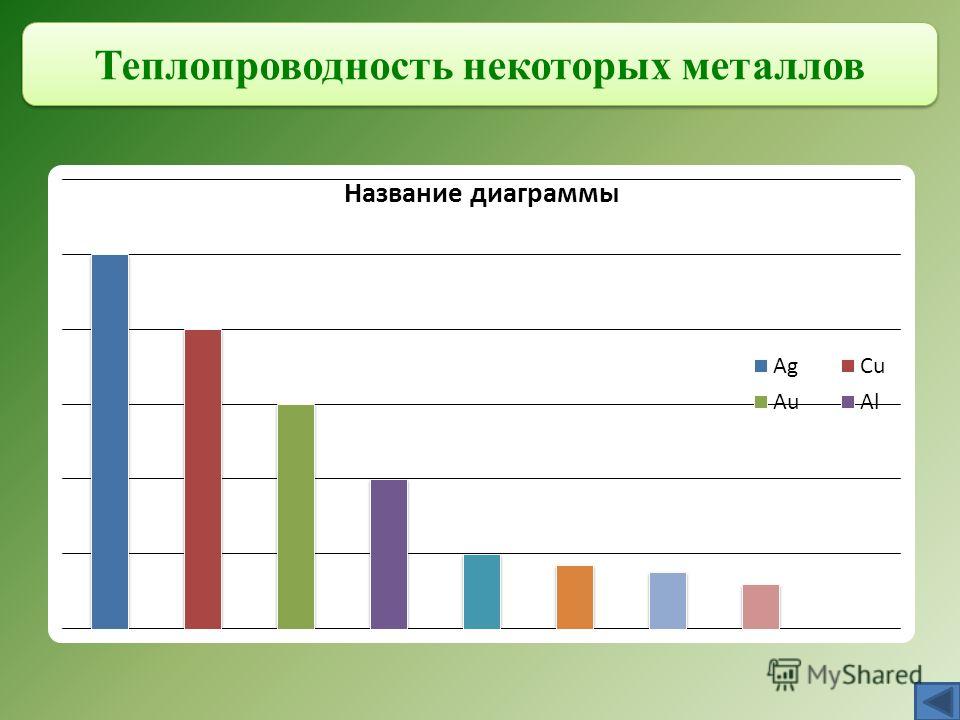
Заслушиваем сообщения учащихся:
– История знакомства человека с металлами.
– Металл в быту человека вчера и сегодня.
– Биологическая роль металлов.
– Металлы в художественном творчестве.
– Роль металлов в производстве.
(Возвращение к ассоциациям). На какие вопросы вы не получили ответа? Что нового вы узнали о металлах? Постарайтесь за 2мин. вспомнить и перечислить все важные сведения о металлах.
Перевертыши:
Ø Разговор – ртуть, крик – платина
Слово – серебро, молчание – золото
Ø Гладь металл, пока холодно
Куй железо, пока горячо
Ø Пролежал холод, сушь и оловянные трубы
Прошел огонь, воду и медные трубы
Ø Не та грязь, что тусклая
Не то золото, что блестит
Ø Звери живут за неметалл
Люди гибнут за металл
Ø В пустыне саксаул коричневый, на нем из меди обручальное кольцо
У Лукоморья дуб зеленый; златая цепь на дубе том.
Подводим итог
урока. Оцениваем работу учащихся, предлагаем домашнее задание.
Оцениваем работу учащихся, предлагаем домашнее задание.
Домашнее задание:
1) Повторить §§ 34-44, подготовиться к контрольной работе.
2) Заполнить таблицу:
Свойство металла | Чем обусловлено данное свойство | Область применения |
|
|
|
2) Найдите дополнительную интересную и полезную информацию по теме (пословицы, поговорки, загадки, стихи, патологическое действие металлов на организм человека, биологические свойства металлов…)
Верните кружки:
– узнал много; интересно; я был очень
активен – красный; – в целом было интересно, но я редко высказывал свое мнение – зелёный;
– ваше личное мнение и пожелание – синий.
Литература
1. Венецкий С. И. Рассказы о металлах. – М.: Металлургия, 1982
2. Еремин В. В., Кузьменко Н. Е., Дроздов А.А., Лунин В.В. Химия. 9 класс. – М.: Дрофа, 2009
3. Рудзитис Г.Е., Фельдман Ф.Г. Химия. 9 класс.- М.: Просвещение,2009
4. Фадеев Г.Н., Сычев А.П. Мир металлов и сплавов. Книга для внеклассного чтения. – М.: Просвещение, 1997
5. Энциклопедический словарь юного химика. – М.: Педагогика, 1992
6. http://all-met.nerod.ru/
7. http://elementy.ru/
Какие металлы являются самыми проводящими?
Проводимость играет жизненно важную роль во многих отраслях промышленности, включая электронику, аэрокосмическую промышленность и телекоммуникации. Однако на самом деле существует несколько видов проводимости. Теплопроводность относится к способности материала передавать тепло, а электропроводность относится к способности материала пропускать электрический ток без сопротивления.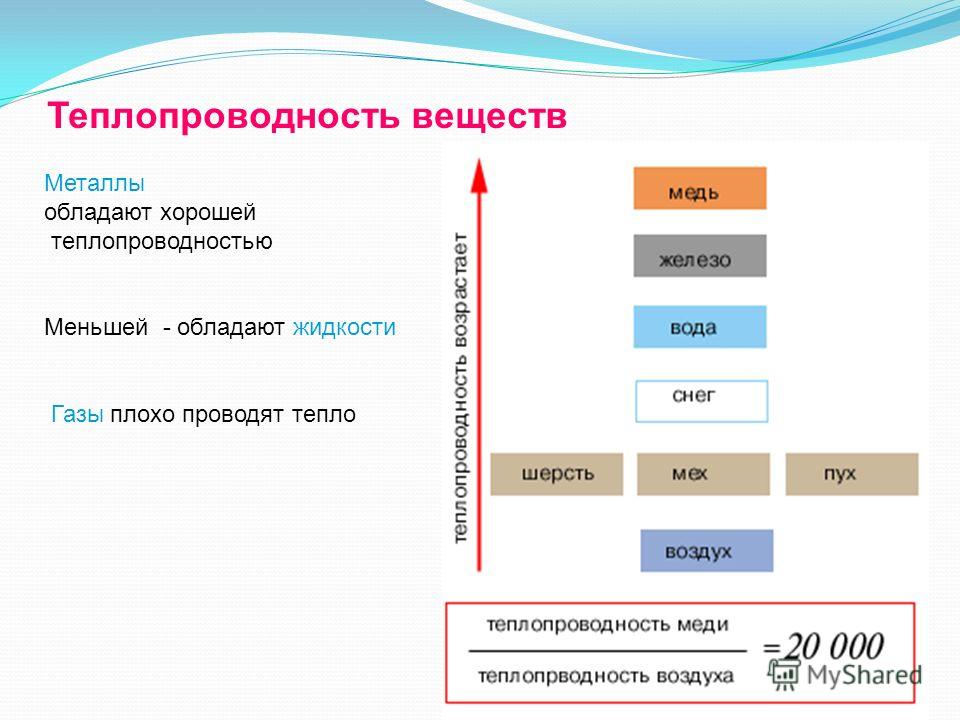 Как правило, материалы с высокой теплопроводностью также обладают высокой электропроводностью.
Как правило, материалы с высокой теплопроводностью также обладают высокой электропроводностью.
Проводимость зависит от различных материалов и внешних условий. Некоторые из факторов, влияющих на проводимость, включают форму, размер, температуру и внешние электромагнитные поля. Примеси в веществе также могут препятствовать потоку электронов и снижать проводимость.
Большинство металлов в той или иной степени проводят тепло и электричество, но некоторые металлы обладают большей проводимостью, чем другие. В результате проводимость является важным фактором, который следует учитывать при гальванике. Если вам нужен конечный продукт, который может хорошо проводить тепло или электричество, вам нужно будет выбрать проводящее металлическое покрытие, которое будет соответствовать уникальным требованиям вашего приложения.
Шесть самых проводящих металлических покрытий
Выбор металла с правильным уровнем электропроводности может обеспечить или сломать функциональный успех продукта или компонента. Чтобы помочь вам оценить ваши варианты, мы создали это руководство по наиболее проводящим металлам, используемым для гальванопокрытий на подложках в промышленных отраслях. Шесть самых проводящих металлов, которые следует учитывать, включают:
Чтобы помочь вам оценить ваши варианты, мы создали это руководство по наиболее проводящим металлам, используемым для гальванопокрытий на подложках в промышленных отраслях. Шесть самых проводящих металлов, которые следует учитывать, включают:
- Серебро: Серебро, самый проводящий металл, эффективно проводит тепло и электричество благодаря своей уникальной кристаллической структуре и единственному валентному электрону. Серебро обеспечивает низкую износостойкость контактов и отличную оптическую отражательную способность, что делает его идеальным для покрытия контактов, зеркал и проводников в телекоммуникационных приложениях. Однако серебряные покрытия также легко тускнеют, поэтому их используют реже, чем покрытия из меди и золота.
- Медь: Как и серебро, один валентный электрон меди делает ее металлом с высокой проводимостью. Он также обеспечивает хорошую коррозионную стойкость. Медные покрытия находят применение в полупроводниках, печатных платах и других устройствах, где важна электропроводность.

- Золото: Высокая проводимость золота в сочетании с его коррозионной стойкостью, износостойкостью и стабильным контактным сопротивлением делает его идеальным для покрытия полупроводников, разъемов, печатных и травленых схем. Если вы готовы согласиться на более высокую цену, золото обычно предлагает наибольшую выгоду для продуктов, требующих проводимости.
- Цинк: Хотя цинк значительно менее электропроводен, чем золото, медь и серебро, он может быть доступной альтернативой этим более дорогим металлам. Цинк обеспечивает хорошую проводимость и большую долговечность.
- Никель: Другой проводящий металл, никель, обычно наносится на поверхность компонента для увеличения толщины и повышения устойчивости к износу и коррозии. Вы можете выбрать никелевые покрытия для сложных промышленных и военных применений.
- Платина: Платина — это драгоценный металл, часто используемый для создания защитного покрытия для других металлов, которые легко подвергаются коррозии.
 Чрезвычайно высокая температура плавления платины также делает ее подходящей для применений, требующих высокой теплопроводности.
Чрезвычайно высокая температура плавления платины также делает ее подходящей для применений, требующих высокой теплопроводности.
Компания SPC может покрывать изделия и компоненты всеми этими высокопроводящими металлами. Если вы не уверены, какой вариант лучше всего соответствует вашим требованиям, наша команда экспертов по отделке поверхностей будет рада помочь вам.
Свяжитесь с SPC, чтобы узнать больше
Sharretts Plating Company – это компания, предоставляющая полный комплекс услуг по отделке, которая занимается инновациями в гальванотехнике уже более 90 лет. Чтобы узнать больше о предлагаемых нами проводящих металлических покрытиях или получить компетентные ответы на другие вопросы, связанные с гальванопокрытием, заполните нашу контактную онлайн-форму сегодня.
Потенциал арсенида бора для охлаждения — ScienceDaily
Маловероятный материал, кубический арсенид бора, может обеспечить необычайно высокую теплопроводность — на уровне отраслевого стандарта, установленного дорогостоящим алмазом — сообщают исследователи в текущем выпуске журнала Письма о физическом обзоре .
Открытие того, что химическое соединение бора и мышьяка может соперничать с алмазом, самым известным теплопроводником, удивило группу физиков-теоретиков из Бостонского колледжа и Военно-морской исследовательской лаборатории. Но новый теоретический подход позволил команде раскрыть секрет потенциально экстраординарной способности арсенида бора проводить тепло.
Меньшие, более быстрые и мощные микроэлектронные устройства создают сложную задачу по отводу выделяемого ими тепла. Хорошие теплопроводники, соприкасающиеся с такими устройствами, быстро отводят тепло от нежелательных «горячих точек», что снижает эффективность этих устройств и может привести к их выходу из строя.
Алмаз — самый ценный из драгоценных камней. Но, помимо своего блеска и ювелирной красоты, он обладает многими другими замечательными свойствами. Наряду со своими углеродными родственниками графитом и графеном алмаз является лучшим проводником тепла при комнатной температуре, имея теплопроводность более 2000 ватт на метр на кельвин, что в пять раз выше, чем у лучших металлов, таких как медь. В настоящее время алмаз широко используется для отвода тепла от компьютерных чипов и других электронных устройств. К сожалению, алмазы редки и дороги, а производство высококачественных синтетических алмазов сложно и дорого. Это подтолкнуло к поиску новых материалов со сверхвысокой теплопроводностью, но в последние годы достигнут незначительный прогресс.
В настоящее время алмаз широко используется для отвода тепла от компьютерных чипов и других электронных устройств. К сожалению, алмазы редки и дороги, а производство высококачественных синтетических алмазов сложно и дорого. Это подтолкнуло к поиску новых материалов со сверхвысокой теплопроводностью, но в последние годы достигнут незначительный прогресс.
По словам соавтора Дэвида Бройдо, профессора физики Бостонского колледжа, хорошо изучена высокая теплопроводность алмаза, обусловленная легкостью составляющих его атомов углерода и жесткими химическими связями между ними. С другой стороны, не предполагалось, что арсенид бора будет особенно хорошим проводником тепла, и фактически было установлено, что с использованием обычных критериев оценки его теплопроводность в 10 раз меньше, чем у алмаза.
Команда обнаружила, что расчетная теплопроводность кубического арсенида бора чрезвычайно высока: более 2000 Вт на метр на кельвин при комнатной температуре и выше, чем у алмаза при более высоких температурах, по словам Бройдо и соавторов Тома Райнеке, старшего научного сотрудника в Лаборатория военно-морских исследований и Лукас Линдсей, научный сотрудник NRL, получивший докторскую степень в Британской Колумбии.
Бройдо сказал, что команда использовала недавно разработанный теоретический подход для расчета теплопроводности, который они ранее протестировали со многими другими хорошо изученными материалами. Уверенные в своем теоретическом подходе, команда более внимательно изучила арсенид бора, теплопроводность которого никогда не измерялась.
В отличие от металлов, где электроны переносят тепло, алмаз и арсенид бора являются электрическими изоляторами. Для них тепло переносится колебательными волнами составляющих атомов, и столкновение этих волн друг с другом создает внутреннее сопротивление тепловому потоку. Команда была удивлена, обнаружив необычное взаимодействие определенных колебательных свойств в арсениде бора, которое выходит за рамки рекомендаций, обычно используемых для оценки теплопроводности электрических изоляторов. Оказывается, ожидаемые столкновения между колебательными волнами гораздо менее вероятны в определенном диапазоне частот. Таким образом, на этих частотах арсенид бора может проводить большое количество тепла.



 Чрезвычайно высокая температура плавления платины также делает ее подходящей для применений, требующих высокой теплопроводности.
Чрезвычайно высокая температура плавления платины также делает ее подходящей для применений, требующих высокой теплопроводности.