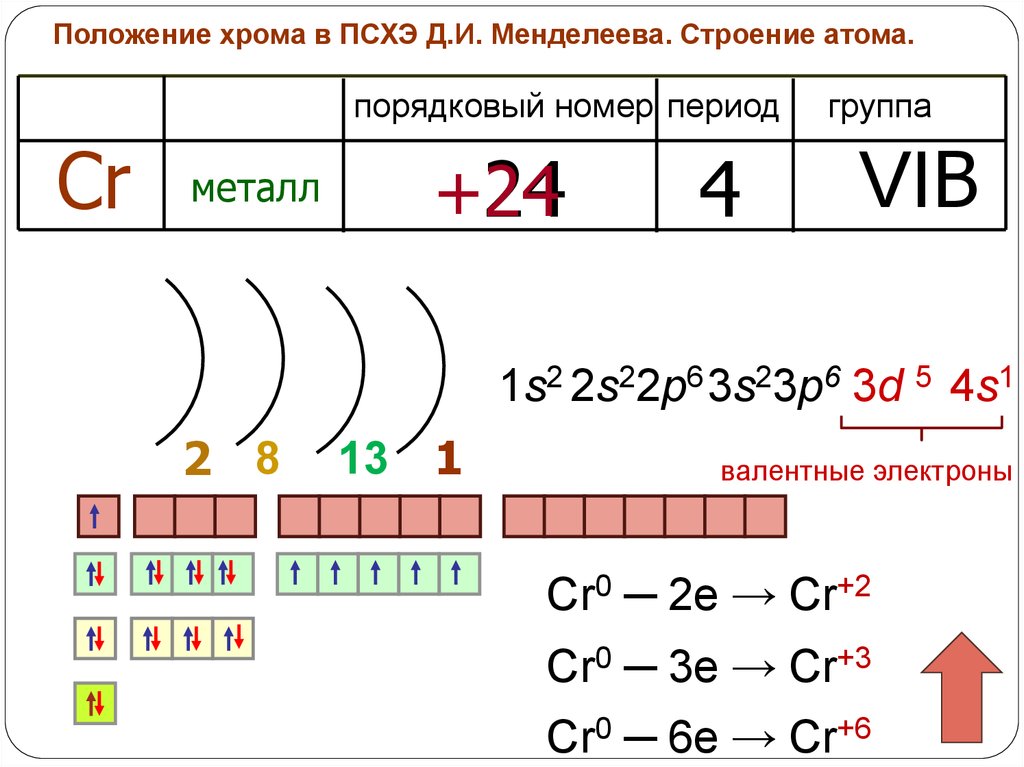
Состав хрома: Хром металлический – ООО “НСплав”
alexxlab | 13.02.2023 | 0 | Разное
Хром металлический Х99
Главная \ Хром \ Хром металлический Х99
Хром Х99 Хром должен изготовляться в соответствии с требованиями настоящего стандарта по технологическому регламенту, утвержденному в установленном порядке. Марки и химический состав-хрома должны соответствовать указанным далее
Упаковка, маркировка, транспортирование и хранение -по ГОСТ 26590-85 с дополнениями:
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Хром в продуктах питания- Администрация СГО
Администрация Сысертского Городского Округа
Официальный сайт
Как ни крути, правильное питание – залог здоровья и долголетия. И дело тут не в подсчете калорий, а в обеспечении организма нужным витаминно-минеральным комплексом.
Человеческий организм гораздо более «химический», чем кажется на первый взгляд. И тут все зависит от того, насколько тщательно вы поддерживаете необходимый состав. Очевидно, что отказ от грамотного, сбалансированного питания может иметь негативные последствия. При этом не менее важно “не перегнуть палку”.
Вот, к примеру, такой важный элемент, как хром, может быть в числе ваших лучших друзей, а может стать самым непримиримым из врагов. Хром в продуктах питания во многом определяет особенности функционирования организма, склонность или устойчивость к различным специфическим заболеваниям и т.д.
В этой статье мы подробно расскажем обо всех аспектах, связанных с содержанием хрома в продуктах.
Продукты, содержащие хром
Среднесуточная норма потребления хрома организмом взрослого человека варьируется от 50 до 70 мкг в зависимости от пола. Мужчинам нужно больше хрома, но в период вынашивания ребенка и лактации женщине требуется 100-120 мкг. Для детей этот показатель находится в диапазоне 11-35 мкг.
При кажущейся незначительности этих показателей, напитать организм хромом вовсе не так просто, как кажется на первый взгляд. Причинами этого являются низкое содержание хрома в продуктах питания, повышенная физическая активность, стрессы, а также другие продукты, употребление в пищу которых понижает концентрацию металла в организме.
В каких продуктах больше хрома?
Превалирующее количество хрома (в мкг/100 г) содержится в пеламиде (100) и тунце (90). Далее следуют: анчоус, карась, карп, горбуша, камбала, зубатка, мойва, треска, сом и некоторые другие рыбы с показателем 55 мкг/100 г. Говяжьи печень, почки и сердце содержат 32, 30 и 30 мкг/100 г хрома соответственно.
Очень много хрома в бразильском орехе, финике, злаках, цельном молоке и молочных продуктах.
Следует знать, что при термической обработке количество хрома будет уменьшаться, поэтому если это возможно, употребляйте продукты в сыром виде.
Последствия недостатка хрома для организма человека
Содержание хрома в крови, тканях и костях постоянно колеблется. Нехватка этого элемента может стать причиной ряда заболеваний. Среди основных последствий нехватки хрома выделяют:
• нарушение темпов роста организма;
• риск развития сахарного диабета из-за повышения концентрации глюкозы в организме;
• ухудшение работы сердечно-сосудистой и мочеполовой систем;
• преждевременное старение, уменьшение продолжительности жизни.
Естественно, важно также не переусердствовать с хромосодержащими продуктами в рационе.

Хром в продуктах питания: польза и вред для организма человека
Данный минерал участвует практически во всех процессах организма. В частности, он способствует лучшему усвоению инсулина, препятствуя таким образом развитию сахарного диабета, поддерживает углеводный и жировой баланс и ускоряет регенерацию поврежденных тканей и органов.
Возможные последствия отравления хромом
В погоне за красотой, здоровьем и долголетием главное — не переусердствовать, поскольку тогда хром преподнесет вам совсем неприятные «сюрпризы» в виде острых аллергических реакций, нервных расстройств, язв, высыпаний, малокровия, сбоев в функционировании печени и почек, общего снижения иммунитета.
Профилактика избытка и дефицита хрома
В случае выявления избытка хрома в организме (достоверным может считаться только итог лабораторных исследований), пациенту назначается специальная диета, которая часто подразумевает прием витаминно-минерального комплекса для снижения его концентрации.

При недостатке хрома также назначается диета, направленная на компенсацию его дефицита и, если врач сочтет нужным, прием медицинских препаратов на основе соединений хрома. В любом случае, стоит контролировать состояние своего организма путем сдачи проверочных анализов с определенной периодичностью.
Ответственное отношение к себе, здоровью, жизни, а значит и способу питания, поможет вам великолепно выглядеть и чувствовать себя отлично на протяжении своей жизни.
Согласовано:
Начальник территориального отдела
Управления Роспотребнадзора по Свердловской
области в Чкаловском районе г. Екатеринбурга,
в г. Полевской и в Сысертском районе. Е.П. Потапкина
Статья подготовлена врачом по гигиене питания отдела
экспертиз за питанием населения Саканян Л.С., т. 269-16-26
- Дата публикации: 20.07.2018
- Дата последнего изменения: 20.07.2018
Хром | Использование, свойства и факты
хром
Посмотреть все СМИ
- Ключевые люди:
- Николя-Луи Воклен
- Похожие темы:
- химический элемент переходный металл обработка хрома
Просмотреть весь соответствующий контент →
Резюме
Прочтите краткий обзор этой темы
хром (Cr) , химический элемент 6-й группы (VIb) периодической таблицы, твердый металл серо-стального цвета, который хорошо полируется и используется в сплавах для повышения прочности и коррозионной стойкости.
| atomic number | 24 |
|---|---|
| atomic weight | 51.9961 |
| melting point | 1,890 °C (3,434 °F) |
| boiling point | 2,482 ° C (4500 °F) |
| удельный вес | 7,20 (28 °C) |
| Состояния окисления | +2, +3, +6 |
| Электронная конфигурация | [AR] 3 D 5 4 S 1 |

Хром является относительно распространенным элементом в земной коре; свободный металл никогда не встречается в природе. Большинство руд состоит из минерала хромита, идеальная формула которого FeCr 2 O 4 . Он широко распространен в природных отложениях, обычно загрязненных кислородом, магнием, алюминием, кремнеземом; содержание хрома в них колеблется от 42 до 56%. Одним из основных применений хрома являются сплавы черных металлов, для которых не требуется чистый металл. Соответственно, хромит часто восстанавливают углеродом в печи с получением сплава феррохрома, который содержит железо и хром в атомном соотношении примерно 1 к 2.
Britannica Викторина
118 Названия и символы периодической таблицы Викторина
Элементарная викторина по фундаментальным вопросам.
Для получения чистого хрома хромит сначала обрабатывают расплавленной щелочью и кислородом, превращая весь хром в щелочной хромат, а последний растворяют в воде и в конечном итоге осаждают в виде дихромата натрия, Na 2 Cr 2 O 7 . Затем дихромат восстанавливают углеродом до полуторного оксида хрома Cr 9.0091 2 O 3 , и этот оксид, в свою очередь, восстанавливается алюминием с образованием металлического хрома.
Затем дихромат восстанавливают углеродом до полуторного оксида хрома Cr 9.0091 2 O 3 , и этот оксид, в свою очередь, восстанавливается алюминием с образованием металлического хрома.
Хром добавляют к железу и никелю в виде феррохрома для получения сплавов, особо отличающихся высокой устойчивостью к коррозии и окислению. Используемый в небольших количествах хром упрочняет сталь. Нержавеющие стали — это сплавы хрома и железа, в которых содержание хрома колеблется от 10 до 26 процентов. Сплавы хрома используются для изготовления таких изделий, как масляные трубки, отделка автомобилей и столовые приборы. Хромит используется как огнеупор и как сырье для производства хромовых химикатов.
Металл белого цвета, твердый, блестящий и хрупкий, чрезвычайно устойчивый к обычным агрессивным реагентам; это сопротивление объясняет его широкое использование в качестве гальванического защитного покрытия. При повышенных температурах Хром соединяется непосредственно с галогенами или с серой, кремнием, бором, азотом, углеродом или кислородом. (Для дополнительной обработки металлического хрома и его получения см. Переработка хрома.)
(Для дополнительной обработки металлического хрома и его получения см. Переработка хрома.)
Хром природный состоит из смеси четырех стабильных изотопов: хром-52 (83,76%), хром-53 (90,55%), хром-50 (4,31%) и хром-54 (2,38%). Металл парамагнитен (слабо притягивается к магниту). Он существует в двух формах: объемно-центрированная кубическая (альфа) и гексагональная плотноупакованная (бета). Хром при комнатной температуре медленно растворяется в соляной и разбавленной серной кислотах. Некоторые окислители образуют на металле тонкий нереакционноспособный оксидный слой, делающий его пассивным также по отношению к разбавленным минеральным кислотам, таким как серная, азотная или холодная царская водка. При обычных температурах металл не реагирует ни на морскую воду, ни на влажный, ни на сухой воздух.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас
Ведущими производителями хрома являются Южная Африка, Индия, Казахстан и Турция.
Основные соединения
Наиболее распространенными степенями окисления хрома являются +6, +3 и +2. Однако известно несколько стабильных соединений в состояниях +5, +4 и +1.
В степени окисления +6 наиболее важными соединениями, образуемыми хромом, являются хромат CrO 4 2– , и дихромат, Cr 2 O 7 2– , ионы. Эти ионы составляют основу ряда промышленно важных солей. Среди них хромат натрия Na 2 CrO 4 и дихромат натрия Na 2 Cr 2 O 7 , которые используются при дублении кожи, при обработке поверхности металлов и в качестве катализаторов в различных промышленных процессах. процессы.
Хром образует несколько коммерчески ценных соединений кислорода, наиболее важным из которых является оксид хрома, обычно называемый триоксидом хрома или хромовой кислотой, CrO 3 , в котором хром находится в степени окисления +6. Оранжево-красное кристаллическое твердое вещество хромовая кислота постепенно разжижается под воздействием влажного воздуха. Обычно его получают обработкой бихромата натрия серной кислотой. Хромовая кислота используется в основном для хромирования, но также используется в качестве красителя в керамике. Это сильный окислитель, который может бурно реагировать с некоторыми органическими материалами, но такие растворы часто используются для контролируемого окисления в органическом синтезе.
Обычно его получают обработкой бихромата натрия серной кислотой. Хромовая кислота используется в основном для хромирования, но также используется в качестве красителя в керамике. Это сильный окислитель, который может бурно реагировать с некоторыми органическими материалами, но такие растворы часто используются для контролируемого окисления в органическом синтезе.
Другим важным соединением кислорода является оксид хрома, также известный как полуторный оксид хрома или оксид хрома, Cr 2 O 3 , в котором хром находится в степени окисления +3. Его получают прокаливанием дихромата натрия в присутствии углерода или серы. Оксид хрома представляет собой зеленый порошок и широко используется в качестве пигмента; его гидратная форма, известная как зеленый Гинье, используется, когда требуется химическая и термостойкость.
Эрик Грегерсен
Ресурсы: Стандарты и свойства – Микроструктуры меди и медного сплава: Хром Медь
Медно-хромистые сплавы представляют собой сплавы с высоким содержанием меди, содержащие от 0,6 до 1,2% Cr. Хромо-медные сплавы используются из-за их высокой прочности, коррозионной стойкости и электропроводности. Сплавы хрома с медью являются дисперсионно-твердеющими, что в данном случае означает изменение свойств при повышенной температуре за счет выделения хрома из твердого раствора. Прочность полностью состаренной хромистой меди почти в два раза выше, чем у чистой меди, а ее проводимость остается высокой на уровне 85% IACS, или 85% от чистой меди. Эти высокопрочные сплавы сохраняют свою прочность при повышенных температурах. Коррозионная стойкость медно-хромовых сплавов лучше, чем у чистой меди, поскольку хром улучшает химические свойства защитной оксидной пленки. Хромистая медь обладает отличной способностью к холодной штамповке и хорошей обрабатываемостью в горячем состоянии. Он используется в таких приложениях, как электроды для контактной сварки, колеса для шовной сварки, переключатели, кабельные соединители, детали автоматических выключателей, формы, наконечники для точечной сварки, а также электрические и тепловые проводники, требующие прочности.
Хромо-медные сплавы используются из-за их высокой прочности, коррозионной стойкости и электропроводности. Сплавы хрома с медью являются дисперсионно-твердеющими, что в данном случае означает изменение свойств при повышенной температуре за счет выделения хрома из твердого раствора. Прочность полностью состаренной хромистой меди почти в два раза выше, чем у чистой меди, а ее проводимость остается высокой на уровне 85% IACS, или 85% от чистой меди. Эти высокопрочные сплавы сохраняют свою прочность при повышенных температурах. Коррозионная стойкость медно-хромовых сплавов лучше, чем у чистой меди, поскольку хром улучшает химические свойства защитной оксидной пленки. Хромистая медь обладает отличной способностью к холодной штамповке и хорошей обрабатываемостью в горячем состоянии. Он используется в таких приложениях, как электроды для контактной сварки, колеса для шовной сварки, переключатели, кабельные соединители, детали автоматических выключателей, формы, наконечники для точечной сварки, а также электрические и тепловые проводники, требующие прочности. Хромо-медные сплавы обозначаются UNS C18050-C18600, литейные сплавы – C81400-C81540.
Хромо-медные сплавы обозначаются UNS C18050-C18600, литейные сплавы – C81400-C81540.
Реакция старения происходит из-за того, что растворимость хрома в твердом состоянии в меди уменьшается при понижении температуры. Структура медленно охлаждаемой хромистой меди представляет собой двухфазную смесь хрома и альфа-меди. Превосходные механические свойства достигаются за счет быстрого охлаждения сплавов хрома с медью от температуры отжига, поэтому хром остается в пересыщенном твердом растворе с медью. Затем следует обработка старением, при которой хром осаждается из твердого раствора, образуя очень мелкую дисперсию осадков в матрице. Микроструктура закаленного или быстро охлажденного хромомедного сплава похожа на структуру нелегированной меди. Быстрое охлаждение предотвращает осаждение хрома из твердого раствора, поэтому полученная литая структура состоит из однофазной структуры альфа-меди. Первым материалом, который затвердевает, является чистая медь, за которой следует эвтектическая смесь альфа-хрома.