Сплавы и их свойства и применение: Сплавы, их классификация и свойства
alexxlab | 22.04.2023 | 0 | Разное
2. Черниченко Р.С. Влияние термомеханической обработки на структуру и механические свойства высокоэнтропийного сплава типа CoCrFeNiMn, содержащего Al и С: Выпускная квалификационная работа … канд. тех. наук. – Белгород: НИУ БелГУ 2018.
3. Юрченко Н.Ю. Разработка и исследование высокоэнтропийных сплавов с высокой удельной прочностью на основе системы Al-Cr-Nb-Ti-V-Zr: Автореф. дис. … канд. тех. наук. – Екатеринбург: УрФУ 2019. – 20 с.
4. Vishwanadh B., Sarkar N., Gangil S. etc. Synthesis and microstructural characterization of a novel multicomponent equiatomic ZrNbAlTiV high entropy alloy // Scripta Materialia. 2016. Vol. 124. P. 146 – 150.
5. Sun X., Zhang H., Lu S. etc. Phase selection rule for Al-doped CrMnFeCoNi high-entropy alloys from first-principles // Acta Materialia. 2017. Vol. 140. P 366 – 374.
6. Zhang Y., Lu Z.P., Ma S.G. etc. Guidelines in predicting phase formation of high-entropy alloys // MRS Communications.
7. Gao M.C., Yeh J.-W., Liaw P.K., Zhang Y. High-Entropy Alloys. – Switzerland: Springer International Publishing, 2016. – 13 p.
8. Yang X., Zhang Y. Prediction of high-entropy stabilized solid-solution in multicomponent alloys // Materials Chemistry and Physics. 2012. Vol. 132. P. 233 – 238.
9. Guo S., Ng C., Lu J., Lu C.T. Effect of valence electron concentration on stability of fcc or bcc phase in high entropy alloys // Journal of Applied Physics. 2011. Vol. 109. Article 103505.
10. Jiang L., Lu Y.P., Jiang H. etc. Formation rules of single phase solid solution in high entropy alloys // Mater. Sci. Technol. 2016. Vol. 32. No. 6. P. 588 – 592.
11. Gao M.C., Alman D.E. Searching for next single-phase high-entropy alloy compositions // Entropy. 2013. Vol. 15. No. 12. P. 4504 – 4519.
12. Singraber A., Morawietz T., Behler J., Dellago C. Parallel multistream training of high-dimensional neural network potentials // Journal of Chemical Theory and Computation.
13. Dębski A., Dębski R., Gąsior W. New features of Entall database: comparison of experimental and model formation enthalpies // Archives of Metallurgy and Materials. 2014. Vol. 59. No. 4. P. 1337 – 1343.
14. The periodic table of the elements [Electronic resource]. URL:https://www.webelements.com (дата обращения 07.09.2019).
15. Информационный ресурс по свойствам материалов [Электронный ресурс]. URL: http://thermalinfo.ru/svojstva-materialov/metally-i-splavy/temperatura-plavleniya-i-kipeniya-metallov-plotnost-i-teploprovodnost.
16. Инженерный справочник DPVA [Электронный ресурс]. URL: https://dpva.ru/Guide/GuidePhysics/Length/AtomicRadius/(дата обращения 21.11.2019).
17. Thermo-Calc Software [Electronic resource]. Sweden, 2019. URL: https://www.thermocalc.com/ (дата обращения 21.11.2019).
18. Жилина Е.М., Красиков С.А., Агафонов С.Н. и др. Термодинамические и кинетические особенности совместного алюмино-термического восстановления титана и циркония из оксидов // Бутлеровские сообщения. 2016. Т. 45. № 1. С. 130 – 135.
2016. Т. 45. № 1. С. 130 – 135.
19. Ведмидь Л.Б., Красиков С.А., Жилина Е.М. и др. Эволюция фазообразования при алюминотермическом восстановлении титана и циркония из оксидов // Расплавы. 2018. № 3. С. 330 – 335.
20. Осинкина Т. В., Красиков С.А., Жилина Е.М. и др. Влияние ниобия и тантала на особенности фазообразования при металлотермическом взаимодействии алюминия с диоксидом титана // Расплавы. 2018. № 5. С. 553 – 56.
21. Allibert M., Gaye H., Geiseler J. etc. Slag Atlas. 2nd edition. – Germany: Verlag Stahleisen GmbH, 1995. – 616 p.
22. Balyakin I.A., Gelchinski B.R., Rempel A.A. Ab initio molecular dynamics study of TiZrNbHfTa and VZrMoHfW liquid alloys // Mater. Today Commun. 2019. Vol. 21. Article 100627.
23. Zhang Y., Guo S., Liu C.T., Yang X. Phase formation rules // High-Entropy Alloys: Fundamentals and Applications. Springer International Publishing, 2016. P. 21 – 49.
Бериллий и его сплавы свойства и применение
КАТАЛОГ ИСКРОБЕЗОПАСНОГО ИНСТРУМЕНТА ИЗ СПЛАВА МЕДЬ-БЕРИЛЛИЙ
БЕРИЛЛИЙ И ЕГО СПЛАВЫ
ОСНОВНЫЕ СВОЙСТВА И ТЕХНОЛОГИИ ПОЛУЧЕНИЯ БЕРИЛЛИЯ
Бериллий — светло-серый металл второй группы Периодической системы элементов Д. И. Менделеева. Порядковый номер бериллия 4, атомная масса 9,01, температура плавления 1284 °С. Бериллий может существовать в двух полиморфных модификациях. Низкотемпературная модификация, существующая до 1250 °С, имеет гексагональную плотноупакованную решетку, высокотемпературная — решетку объемно-центрированного куба. Плотность бериллия 1845 кг/м
И. Менделеева. Порядковый номер бериллия 4, атомная масса 9,01, температура плавления 1284 °С. Бериллий может существовать в двух полиморфных модификациях. Низкотемпературная модификация, существующая до 1250 °С, имеет гексагональную плотноупакованную решетку, высокотемпературная — решетку объемно-центрированного куба. Плотность бериллия 1845 кг/м
Комплекс физических, химических и механических свойств позволяет отнести бериллий к наиболее ценным конструкционным материалам.
Бериллий является редким металлом. Его содержание в земной коре составляет 5 · 10–4 %. Известно около 40 минералов бериллия, из которых наибольшее практическое значение имеет берилл, который после обработки переводят в форму хлорида или фторида. Металлический бериллий получают восстановлением фторида магнием при высокой температуре (900–1300 °С) или электролизом его хлорида в смеси с хлоридом натрия. Дальнейшей вакуумной дистилляцией бериллий очищают до 99,98 %.
Размеры атома бериллия малы (атомный диаметр 0,226 нм). Даже небольшие количества примесей сильно охрупчивают бериллий. Пластичный бериллий, содержащий не более 10 –4 % примесей, получают электролизом хлоридных расплавов с последующей зонной плавкой. Многократное повторение зонной плавки (до 8 проходов) позволяет получать особо чистый бериллий с чрезвычайно высокой пластичностью (δ = 140 %). Введение в очищенный бериллий всего 0,001 % Si приводит к охрупчиванию металла.
Даже небольшие количества примесей сильно охрупчивают бериллий. Пластичный бериллий, содержащий не более 10 –4 % примесей, получают электролизом хлоридных расплавов с последующей зонной плавкой. Многократное повторение зонной плавки (до 8 проходов) позволяет получать особо чистый бериллий с чрезвычайно высокой пластичностью (δ = 140 %). Введение в очищенный бериллий всего 0,001 % Si приводит к охрупчиванию металла.
Для производства компактного бериллия в виде заготовок применяют методы порошковой металлургии. В безокислительной среде бериллий измельчают в порошок и подвергают горячему прессованию в вакууме. Чем мельче зерна порошка, тем выше прочностные и пластические свойства металла. Бериллий и его соединения в виде порошков, пыли и паров остро токсичны, они вызывают расстройство дыхания и дерматиты, поэтому при работе с ними прибегают к специальным методам защиты. Вместе с тем обработанные детали из бериллия вполне безопасны.
Для предотвращения взаимодействия с воздухом горячепрессованные заготовки бериллия помещают в стальные оболочки, нагревают до температуры 800–1100 °С и в таком виде проводят обработку давлением.
Бериллий плохо обрабатывается резанием и требует применения твердосплавного инструмента. Соединения бериллия получают пайкой и дуговой сваркой в аргоне или вакууме.
Механические свойства бериллия зависят от чистоты металла, технологии производства, размера зерна. После горячего прессования при исходной крупности порошка менее 70 мкм σв = 240–300 МПа, δ = 1–2 %. Свойства горячевыдавленного бериллия значительно выше — σ в = 500–700 МПа и δ = 7–10 %. Деформированные полуфабрикаты имеют развитую текстуру деформации, вызывающую сильную анизотропию свойств.
По сравнению с другими легкими материалами бериллий обладает уникальным сочетанием физических и механических свойств. По удельной прочности и жесткости он превосходит все другие металлы (табл. 15.1).
По удельной прочности и жесткости он превосходит все другие металлы (табл. 15.1).
Благодаря высокому значению модуля упругости (Е = 300 ГПа) и низкой плотности, бериллий по удельной жесткости превосходит все известные материалы, сохраняя это преимущество до 500–600 °С (рис. 15.2).
Таблица 15.1
Удельная прочность и жесткость материалов
Материал | σв, МПа | ∙ 10–3 | σв /(γg), км | E /(γg), км |
Магниевый сплав МА10 | 430 | 1,8 | 24 | 2,3 |
Алюминиевый сплав В95 | 700 | 2,9 | 21 | 2,4 |
Титановый сплав ВТ6 | 1500 | 4,5 | 22 | 2,6 |
Сталь 03Н18К9М5Т | 1750 | 7,8 | 23 | 2,6 |
Бериллий | 680 | 1,8 | 38 | 16,1 |
Бериллий отличается высокой электро- и теплопроводностью, приближающейся к теплопроводности алюминия, а по удельной теплоемкости [≈ 2500 Дж/(кг × град)] превосходит все остальные металлы.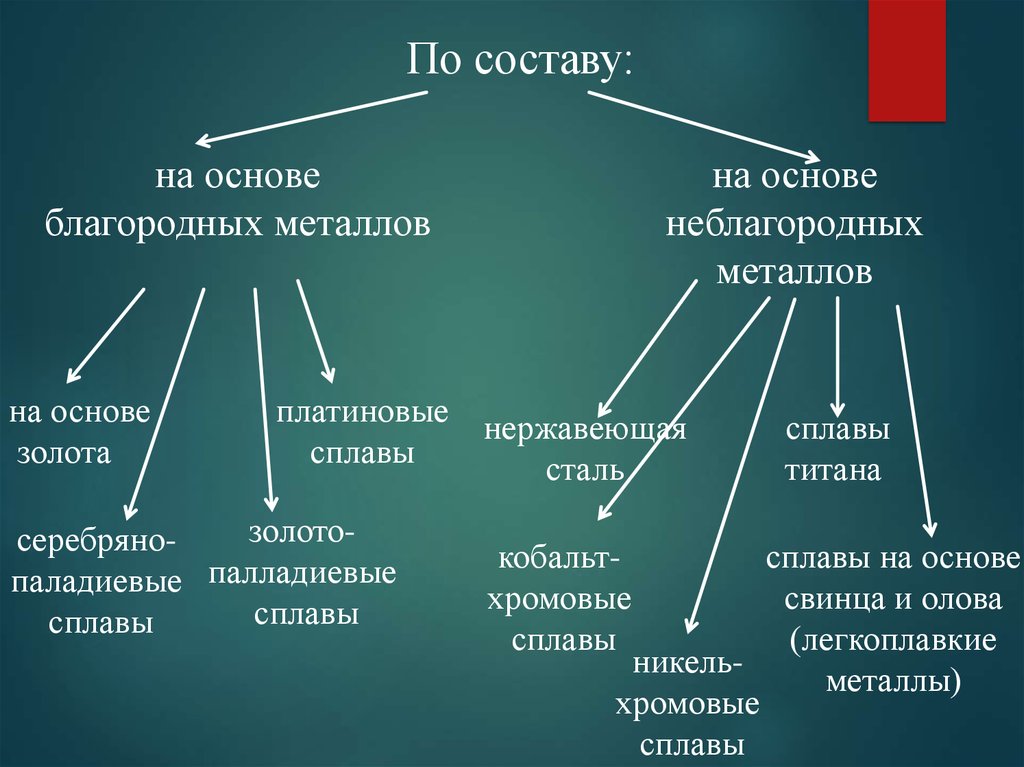 Бериллий стоек к коррозии. Подобно алюминию, при взаимодействии бериллия с воздухом на поверхности его образуется тонкая оксидная пленка, защищающая металл от действия кислорода даже при высокой температуре. Лишь при температуре выше 700 °С обнаруживаются заметные признаки коррозии, а при 1200 °С металлический бериллий сгорает, превращаясь в белый порошок оксида бериллия.
Бериллий стоек к коррозии. Подобно алюминию, при взаимодействии бериллия с воздухом на поверхности его образуется тонкая оксидная пленка, защищающая металл от действия кислорода даже при высокой температуре. Лишь при температуре выше 700 °С обнаруживаются заметные признаки коррозии, а при 1200 °С металлический бериллий сгорает, превращаясь в белый порошок оксида бериллия.
Бериллий имеет высокие ядерные характеристики — самое низкое среди металлов эффективное поперечное сечение захвата тепловых нейтронов и самое высокое поперечное сечение их рассеяния.
Недостатками бериллия является высокая стоимость, обусловленная дефицитностью исходного сырья и сложностью его переработки, а также низкая хладостойкость. Ударная вязкость технического бериллия ниже 5 Дж/см2.
Несмотря на эти недостатки, уникальная совокупность технических преимуществ позволяет относить бериллий к числу выдающихся аэрокосмических материалов.
СПЛАВЫ БЕРИЛЛИЯ
Главная сложность при легировании бериллия состоит в малых размерах его атомов, в результате чего большинство элементов при растворении сильно искажают кристаллическую решетку, сообщая сплаву повышенную хрупкость. Легирование возможно лишь теми элементами, которые образуют с бериллием механические смеси с минимальной взаимной растворимостью.
Легирование возможно лишь теми элементами, которые образуют с бериллием механические смеси с минимальной взаимной растворимостью.
Серьезный недостаток бериллия, заключающийся в низкой ударной вязкости и хладноломкости, может быть преодолен использованием сплавов с алюминием. Из диаграммы состояния Al—Be видно, что эти элементы практически взаимно нерастворимы (рис. 15.3). В таких сплавах эвтектического типа твердые частицы бериллия равномерно распределены в пластичной алюминиевой матрице. Сплавы содержат 24–43 % алюминия, остальное — бериллий. Фирмой «Локхид» (США) разработан сплав, содержащий 62 % бериллия, названный локеллоем. Сплавы Be—Al имеют структуру, состоящую из мягкой пластичной эвтектики и твердых хрупких включений первичного бериллия. Эти сплавы сочетают высокую жесткость, прочность и малую плотность, характерные для бериллия, с пластичностью алюминия (рис. 15.4). Благодаря пластичности матрицы снижается концентрация напряжений у частиц бериллиевой фазы и уменьшается опасность образования трещин, что позволяет использовать сплавы в условиях более сложного напряженного состояния.
Для получения бериллиево-алюминиевых сплавов также используют методы порошковой металлургии. Деформацию осуществляют выдавливанием с последующей ковкой и штамповкой в оболочках. Механические свойства труб из локеллоя (Be + 38 % Al) при комнатной температуре: σв = 600 МПа, σ0,2 = 570 МПа, δ = 1 %.
Для увеличения прочности сплавы Be—Al дополнительно легируют магнием и серебром — элементами, растворимыми в алюминиевой фазе. В этом случае матрица представляет собой более прочный и вязкий сплав Al—Mg или Al—Ag.
Пластичную матрицу можно получить, используя композицию Be—Ag, содержащую до 60 % серебра. Сплавы с серебром дополнительно легируют литием и лантаном.
За исключением сплавов с пластичной матрицей, легирование другими элементами не устраняет хладноломкость бериллия. Максимальную пластичность имеет бериллий высокой чистоты.
Широкое распространение получили сплавы меди с 2–5 % бериллия, так называемые бериллиевые бронзы. В России широко применяется бериллиевая бронза БрБ2 с 2 % Be. Из диаграммы состояния (рис. 15.5) видно, что этот сплав дисперсионно-твердеющий и может упрочняться закалкой с последующим старением. Закалка с 800 °С фиксирует пересыщенный α–твердый раствор, из которого в процессе старения при 300–350 °С выделяются дисперсные частицы CuBe, образуя регулярную, так называемую квазипериодическую структуру (рис. 15.6). После закалки свойства бериллиевой бронзы БрБ2: σв = 500 МПа, δ = 30 %, после старения —
Из диаграммы состояния (рис. 15.5) видно, что этот сплав дисперсионно-твердеющий и может упрочняться закалкой с последующим старением. Закалка с 800 °С фиксирует пересыщенный α–твердый раствор, из которого в процессе старения при 300–350 °С выделяются дисперсные частицы CuBe, образуя регулярную, так называемую квазипериодическую структуру (рис. 15.6). После закалки свойства бериллиевой бронзы БрБ2: σв = 500 МПа, δ = 30 %, после старения —
σв = 1200 МПа, δ = 4 %.
Бериллиевые бронзы обладают высокими упругими свойствами. Их используют для изготовления пружин, сохраняющих упругость в широком интервале температур, в том числе в криогенных условиях. Они хорошо сопротивляются усталости и коррозии.
Бериллиевые бронзы немагнитны и не искрят при ударе. Из них изготавливают инструменты для работы во взрывоопасных средах — шахтах, газовых заводах, где нельзя использовать обычные стали.
Литейные бериллиевые сплавы (ЛБС), состав которых приведен в табл. 15.2, используют для деталей корпусов оснований, рам, кронштейнов и др. Бериллиевые сплавы характеризуются высокими значениями теплоемкости, которые в 1,6 раза выше, чем у сплавов алюминия.
15.2, используют для деталей корпусов оснований, рам, кронштейнов и др. Бериллиевые сплавы характеризуются высокими значениями теплоемкости, которые в 1,6 раза выше, чем у сплавов алюминия.
Теплопроводность и температуропроводность сплавов лишь незначительно уступает литейным алюминиевым сплавам.
Совокупность теплофизических характеристик бериллиевых сплавов в целом выгодно отличает их от других материалов (например, силуминов) и определяет высокую размерную стабильность в условиях возникновения температурных градиентов при эксплуатации изделий.
Коррозионная стойкость бериллиевых сплавов находится на высоком уровне. Анодная оксидированная пленка на поверхности и лакокрасочные покрытия дополнительно обеспечивают надежную защиту сплавов ЛБС от коррозии.
Механические свойства литейных бериллиевых сплавов при комнатной температуре приведены в табл. 15.3, а свойства при различных температурах испытания — в табл. 15.4.
Таблица 15.2
Химические составы (%, остальное — Be) литейных бериллиевых сплавов
Сплав | Al | Ni | Mg | Cu | Zr, Sc, Y, Gd, РЗМ | Примеси, не более | ||||
Si | Fe | Mn | Ti | O2 | ||||||
ЛБС-1 | 24–34 | 3–6 | – | – | 0,06–0,21* | 0,1 | 0,15 | 0,1 | 0,05 | 0,1 |
ЛБС-2 | 36–24 | 3,5–4,5 | 0,6–0,8 | – | 0,03–0,12** | 0,1 | 0,15 | 0,1 | 0,05 | 0,1 |
ЛБС-3 | 30–34 | – | 0,1–0,6 | 6–8 | 0,05–0,1 | 0,1 | 0,15 | – | – | 0,1 |
* Допускается введение только Zr, Sc.
** Допускается введение одного или нескольких элементов Sc, Zr, La, Pr, Nd при содержании: минимальном — 0,01 %, максимальном — 0,08 % любого.
Таблица 15.3
Механические свойства литейных бериллиевых сплавов
Свойство | ЛБС-1 | ЛБС-2 | ЛБС-3 |
σв, МПа | 220–250 | 250–320 | 270–280 |
σ0,2, МПа | 180–220 | 220–270 | 250–270 |
δ, % | 2–3 | 2–3 | 1,1–1,3 |
ψ, % | 2–3 | 2–3,5 | – |
KCU, МДж/м2 | 0,025–0,035 | 0,033–0,040 | 0,025–0,045 |
E, ГПа | 200 | 200 | 200 |
Таблица 15. 4
4
Механические свойства бериллиевых сплавов
при различных температурах
Свойство | Сплав | Температура испытаний, °С | |||||
–100 | 0 | 100 | 200 | 300 | 400 | ||
σв, МПа | ЛБС-1 | 255 | 225 | 186 | 147 | 112 | – |
ЛБС-2 | 274 | 255 | 235 | 176 | 118 | 70 | |
σ0,2, МПа | ЛБС-1 | 235 | 196 | 145 | 120 | 103 | – |
ЛБС-2 | 245 | 216 | 170 | 140 | 108 | 60 | |
δ, % | ЛБС-1 | 2,8 | 2,4 | 2,5 | 2,5 | 1–2,4 | – |
ЛБС-2 | 2,0 | 2,1 | 2,1 | 2,2 | 3,0 | 4,0 | |
Деформированные бериллиевые сплавы обладают высокой жесткостью и низкой плотностью. Эти сплавы являются перспективными для использования в некоторых элементах самолетных двигателей. Для повышения жаропрочных свойств бериллия используется сложное последовательное легирование.
Эти сплавы являются перспективными для использования в некоторых элементах самолетных двигателей. Для повышения жаропрочных свойств бериллия используется сложное последовательное легирование.
На первом этапе выбирают оптимальный бинарный сплав (табл. 15.5).
Таблица 15.5
Механические свойства двойных сплавов
(остальное — Be)
Содержание легирующих элементов, % | Средний размер зерна, мкм | σв, МПа | Hμ при 20 °С | |
20 °С | 500 °С | |||
6,7 Cu | 124 | 256 | 146 | 198 |
2,4 Ag | 186 | 282 | 209 | 215 |
5,8 Ni | 160 | 346 | ||
Сплавы: значение, свойства и примеры
- Автор Аканкша П Джон
- Последнее изменение 25-01-2023
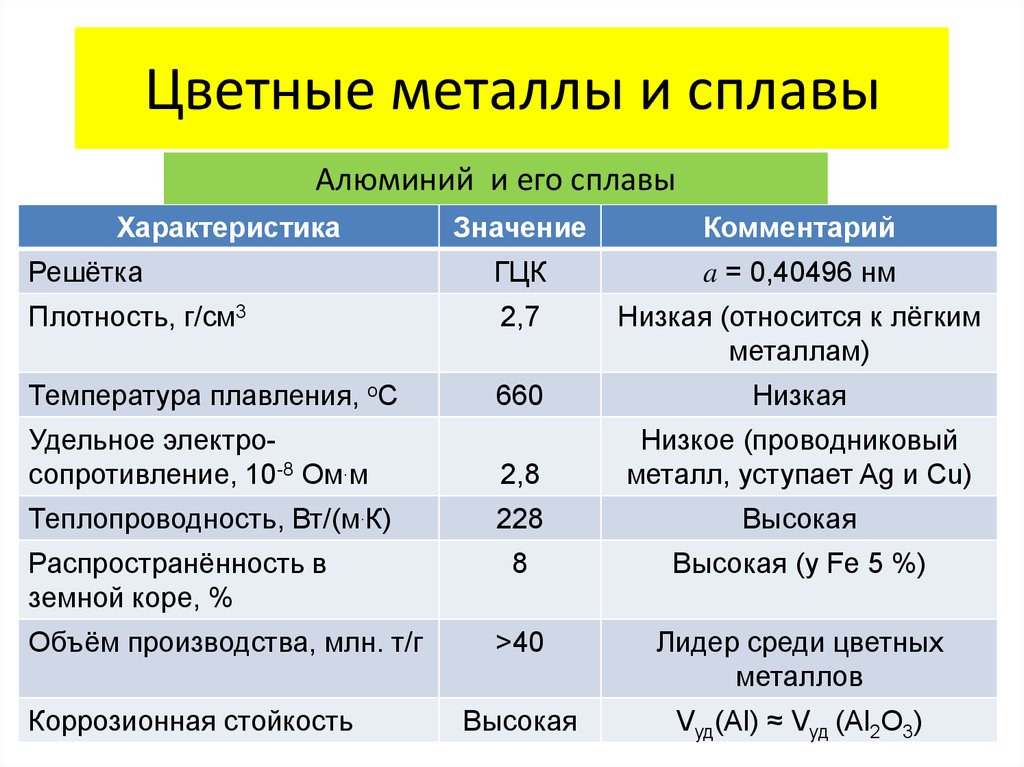
Сплавы: Механические свойства чистых металлов плохие. В результате они не используются в чистом виде в промышленности. Добавление других элементов изменяет их свойства. Сплавы обладают свойствами, которые отличаются от металлов, в которых они содержатся, такими как прочность, твердость, долговечность, пластичность, предел прочности при растяжении и ударная вязкость. В результате они более полезны, чем чистые металлы.
В результате они не используются в чистом виде в промышленности. Добавление других элементов изменяет их свойства. Сплавы обладают свойствами, которые отличаются от металлов, в которых они содержатся, такими как прочность, твердость, долговечность, пластичность, предел прочности при растяжении и ударная вязкость. В результате они более полезны, чем чистые металлы.
Например, бронза (медь и олово) используется для изготовления колоколов, молотков и других предметов. Стали, полученные из сплавов железа, используются для изготовления кузовов автомобилей и железнодорожных путей.
В этой статье мы изучим значение и свойства сплавов, а также некоторые распространенные сплавы, используемые в коммерческих целях.
Что такое сплавы? Сплав представляет собой смесь химических элементов, образующую нечистое вещество (примесь) с металлическими свойствами. Сплав отличается от нечистого металла тем, что добавленные элементы в сплав хорошо контролируются для получения желаемых свойств. Напротив, нечистые металлы, такие как кованое железо, менее контролируемы, но часто считаются полезными. Сплавы создаются путем соединения двух или более элементов, один из которых должен быть металлом. Его обычно называют первичным металлом или основным металлом, и название металла может также быть названием сплава. Другие составляющие могут быть или не быть металлами, но они будут растворимы и растворятся в смеси при смешивании с расплавленной основой. Механические свойства сплавов часто сильно отличаются от свойств составляющих их компонентов.
Напротив, нечистые металлы, такие как кованое железо, менее контролируемы, но часто считаются полезными. Сплавы создаются путем соединения двух или более элементов, один из которых должен быть металлом. Его обычно называют первичным металлом или основным металлом, и название металла может также быть названием сплава. Другие составляющие могут быть или не быть металлами, но они будут растворимы и растворятся в смеси при смешивании с расплавленной основой. Механические свойства сплавов часто сильно отличаются от свойств составляющих их компонентов.
Сплав может быть твердым раствором металлических элементов (одна фаза с одинаковыми металлическими зернами (кристаллами)) или смесью металлических фаз (два или более растворов, образующих микроструктуру различных кристаллов внутри металла). Интерметаллические соединения представляют собой сплавы, имеющие определенную стехиометрию и кристаллическую структуру. Кроме того, в некоторых случаях фазы Zintl (продукты химических реакций между щелочными или щелочноземельными металлами и переходными металлами или металлоидами) могут быть отнесены к сплавам.
Сплавы отличаются своими свойствами металлической связи. В практических приложениях компоненты сплава обычно измеряются в процентах по массе, а в фундаментальных научных исследованиях они измеряются в атомных долях. В зависимости от расположения атомов сплавы обычно классифицируются как замещающие или внедренные. Они также могут быть гомогенными (состоящими из одной фазы), гетерогенными (состоящими из двух и более фаз) или интерметаллическими.
Процесс легированияМеталлы сплавляются путем их соединения с одним или несколькими другими элементами. Самый распространенный и старый процесс легирования включает в себя нагрев основного металла выше его точки плавления, а затем растворение растворенных веществ в расплавленной жидкости, что возможно, даже если температура плавления растворенного вещества намного выше, чем у самого металла.
Некоторые металлы и растворенные вещества, такие как железо и углерод, имеют чрезвычайно высокие температуры плавления и их невозможно расплавить. В результате легирование можно также проводить с одним или несколькими компонентами в газообразном состоянии, например, в доменной печи. Это также может быть сделано с одним, несколькими или всеми компонентами в твердом состоянии, как в древних методах сварки по образцу (сплошной-сплошной), производстве стали для резки (сплошной-сплошной) или производстве тигельной стали (сплошной-сплошной). жидкость), смешивая элементы посредством твердотельной диффузии.
В результате легирование можно также проводить с одним или несколькими компонентами в газообразном состоянии, например, в доменной печи. Это также может быть сделано с одним, несколькими или всеми компонентами в твердом состоянии, как в древних методах сварки по образцу (сплошной-сплошной), производстве стали для резки (сплошной-сплошной) или производстве тигельной стали (сплошной-сплошной). жидкость), смешивая элементы посредством твердотельной диффузии.
Поскольку элементы не просто объединяются в сумму частей, трудно рассчитать точные свойства новых сплавов. Они образуются в результате химических взаимодействий, которые определяются комплектующими и техническими характеристиками.
Отдельные чистые металлы могут обладать такими полезными свойствами, как хорошая электропроводность, высокая прочность и твердость или устойчивость к нагреву и коррозии. Коммерческие металлические сплавы пытаются объединить эти выгодные свойства для получения металлов, которые более полезны для конкретных применений, чем любой из составляющих их элементов.
Сплавы тверже и жестче, чем основные металлы, и они устойчивы к коррозии. Они инертны к обычным химическим веществам, намагничиваемы и пластичны.
Примеры сплавов Металлический баббитМеталлический баббит, также известный как подшипниковый металл, представляет собой сплав, который в основном используется в качестве опорной поверхности в подшипниках скольжения. Исаак Бэббит, американский изобретатель, изобрел этот сплав в \(1839 г.\). Металл Баббит обычно состоит из следующих элементов:0011
Олово \(\left({{\text{Sn}}} \right)\) \({\rm{90\% }}\\) чистое, сурьмяное \(\left({{\text{ Sb}}} \right)\) \({\rm{7\% }}\) чистая, а медь \(\left({{\text{Cu}}} \right)\) \({ \rm{3\% }}\) чисто.
Низкий коэффициент трения этого сплава со сталью является одним из его наиболее желательных свойств.
Металл для колоколов — это сплав, который в основном используется в производстве колоколов и других инструментов (отсюда и название «металл для колоколов»). Это тип бронзы, который содержит относительно большое количество олова в своем составе. Колокольный металл обычно состоит из \(78\%\) меди \(\left({{\text{Cu}}} \right)\) и \(72\%\) олова \(\left({{\ text{Sn}}} \right).\)
Это тип бронзы, который содержит относительно большое количество олова в своем составе. Колокольный металл обычно состоит из \(78\%\) меди \(\left({{\text{Cu}}} \right)\) и \(72\%\) олова \(\left({{\ text{Sn}}} \right).\)
Этот сплав также используется в производстве кухонной и столовой посуды. Он также используется в некоторых видах домашнего декора.
БронзаБронза была первым обнаруженным сплавом и состоит из \(85 – 88\%\) меди, \(12 – 12,5\%\) олова и небольшого количества других металлов, таких как алюминий , марганец, цинк или никель. Целью этой смеси является улучшение свойств меди.
Бронза используется в производстве скульптур, музыкальных инструментов, медалей и в промышленности.
СтальСталь представляет собой сплав железа с примерно \(1\%\) углерода и может содержать другие элементы, такие как марганец. Сталь производится потому, что она прочная, твердая и устойчивая к коррозии.
Сталь как недорогой сплав широко применяется при строительстве автомобильных дорог, железных дорог, аэропортов, мостов, небоскребов и других сооружений, а также при производстве крупной бытовой техники и различных строительных материалов, бытовых изделий и т. п. на.
п. на.
Единственная разница между латунью и бронзой заключается в том, что бронза представляет собой сплав меди и олова. Напротив, латунь представляет собой сплав меди и цинка с другими элементами, такими как мышьяк, свинец, фосфор, алюминий, марганец и кремний. Целью этого сплава является улучшение его электрических и механических свойств.
Латунь используется в производстве декоративных изделий, замков, застежек-молний, шестеренок, дверных ручек, музыкальных инструментов и т.д. Он также используется в сантехнике и электротехнике.
ПрипойПрипой представляет собой легкоплавкий металлический сплав, который используется для неразъемного соединения металлических деталей. Это сплав олова и свинца со следами других металлов.
Этот сплав используется для создания прочного соединения между электрическими компонентами.
Металл Вуда Металл Вуда представляет собой сплав, состоящий из \(50\%\) висмута, \(26,7\%\) свинца, \(13,3\%\) олова и \(10\%\ ) кадмия по массе.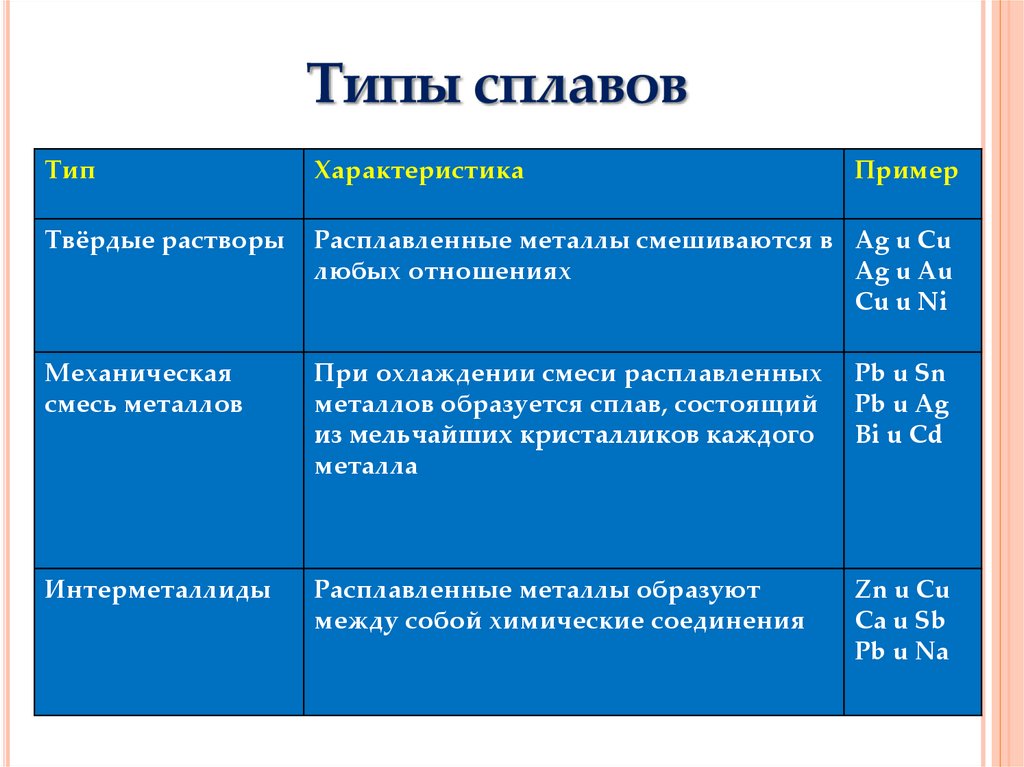 Варнава Вуд создал металлический сплав из дерева.
Варнава Вуд создал металлический сплав из дерева.
Металл Вуда обычно используется в качестве элемента клапана в спринклерных системах пожаротушения, установленных в зданиях. Он также используется в механических мастерских, технических лабораториях, при реставрации антиквариата и так далее.
НихромНихром представляет собой группу сплавов никеля, хрома и железа. Этот сплав обычно используется для изготовления резистивной проволоки. Он имеет высокую температуру плавления, низкую стоимость производства, прочность, пластичность, сопротивление электронному потоку и стойкость к окислению. Благодаря всем этим свойствам нихром широко используется в нагревательных элементах.
Применяется в производстве взрывчатых веществ и фейерверков, а также в производстве нагревательных элементов.
Легированное золото Самая чистая форма золота, \(24\)-каратное золото, очень мягкое и не может использоваться для изготовления украшений, поэтому к нему добавляют медь или серебро, чтобы придать ему твердость и прочность.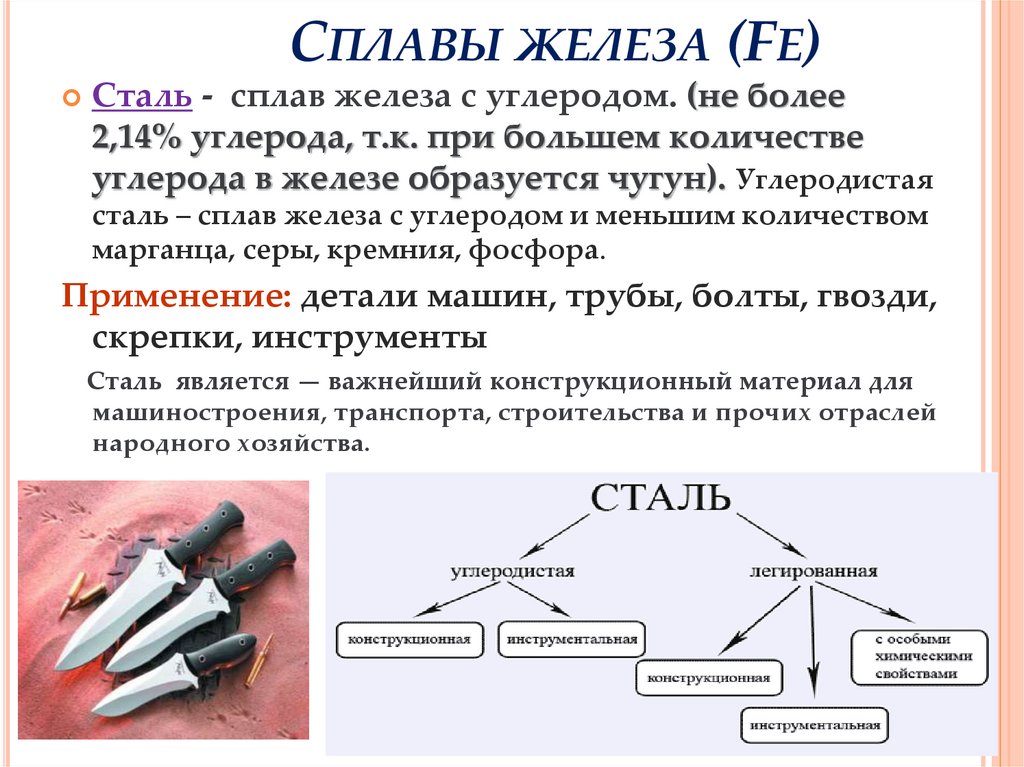
Для преобразования \(24\)-каратного золота в \(22\)-каратное золото с чистотой приблизительно \(91,6\% ,\) примерно \(8,4\% \) добавляется медь или серебро. Большинство украшений изготовлено из 22-каратного золота.
Можно сделать вывод, что сплавы представляют собой гомогенную смесь двух или более растворов металлов. Сплавы тверже и жестче, чем основные металлы, и они устойчивы к коррозии. Они инертны к обычным химическим веществам, намагничиваемы и пластичны. Легирование можно осуществить с помощью одного из самых распространенных и старых процессов, который включает нагрев основного металла выше его точки плавления и затем растворение растворенных веществ в расплавленной жидкости. Мы также изучили некоторые из распространенных сплавов, таких как бронза, сталь, нихром и т. д., а некоторые из распространенных легирующих элементов включают марганец, никель, ванадий, хром и молибден.
Теперь мы знаем некоторые из важных применений сплавов в нашей повседневной жизни, например, при изготовлении кухонной утвари, строительстве железнодорожных путей, деталей транспортных средств и многих других вещах.
Q.1. Что вы имеете в виду под сплавами?
Ответ: Сплавы представляют собой гомогенные смеси двух или более элементов. Можно использовать два металла или металл и неметалл. Чтобы сделать сплав, сначала расплавьте металл, а затем растворите в нем другие элементы. Сталь, например, представляет собой сплав железа с углеродом.
Q.2. Что является примером сплавов?
Ответ: Сплав представляет собой металлический твердый раствор или смесь двух или более элементов. Сплавы включают такие металлы, как латунь, олово, фосфористая бронза, амальгама и сталь.
Q.3. Какие пять сплавов?
Ответ: Некоторые из важных сплавов включают-
1. Сталь
2. Нихром
3. Бронза
4. Латунь
5. Припой
Q.4. Какие элементы обычно используются для легирования?
Ответ: Некоторые распространенные легирующие элементы включают:
1. Марганец
Марганец
2. Никель
3. Ванадий
4. Хром
5. Молибден
8 Как образуются сплавы?
Ответ: Металлы сплавляются путем их соединения с одним или несколькими другими элементами. Самый распространенный и старый процесс легирования включает в себя нагрев основного металла выше его точки плавления, а затем растворение растворенных веществ в расплавленной жидкости, что возможно, даже если температура плавления растворенного вещества намного выше, чем у самого металла.
Q.6. Каковы три свойства сплавов?
Ответ: Сплавы, как правило, прочнее и тверже, менее податливы, менее пластичны и более устойчивы к коррозии, чем основной металл сплава. Смесь сплавов прочнее, потому что она содержит атомы разных размеров из разных элементов.
Изучите химические свойства металлов здесь
Мы надеемся, что эта подробная статья о сплавах поможет вам в подготовке. Если у вас есть какие-либо сомнения, связанные со статьей или вообще с металлами и их сплавами, свяжитесь с нами через раздел комментариев, и мы свяжемся с вами как можно скорее.
Если у вас есть какие-либо сомнения, связанные со статьей или вообще с металлами и их сплавами, свяжитесь с нами через раздел комментариев, и мы свяжемся с вами как можно скорее.
Применение и свойства: различные типы металлов
Будь то бытовая техника или важное промышленное оборудование, металлы всегда были строительными блоками обычных машин и больших конструкций. С эволюцией знаний человечества, постоянное развитие, потому что наука и техника открыли новые двери для материальных открытий и оптимизации их свойств. В связи с чем существует огромное расширение в металлургической промышленности тоже. Здесь мы рассмотрим наиболее распространенные типы металлов, их основные свойства и области применения.
Как мы уже говорили в наших статьях о ЧПУ и сварке, каждый материал уникален. Однако большинство металлов являются пластичными, блестящими (блестящими), ковкими и являются хорошими проводниками тепла и электричества. В этой статье вы найдете все основные свойства и детали металлов, которые вы должны знать как производитель.
Состав
- 1 Железо (феррум)
- 1.1 Известные свойства железа
- 1.2 Применение железа
- 2 Сталь
- 2.1 Properties of Steel
- 2.2 Applications of Steel
- 2.3 Steel Grades by SAE (Society of Automobile Engineers)
- 2.4 Common Steel
- 2.5 Stainless Steel
- 2.6 Other Alloys
- 3 Aluminum
- 3.1 Properties
- 3.2 Применение алюминия
- 4 Медь
- 4.1 Свойства меди
- 4.2 Применение меди
- 5 Никель
- 5.1 Свойства никеля
- 5.2 Применение никеля
- 6 В вольвании
- 6.1.
- 8 Свинец
- 8.1 Свойства свинца
- 8.2 Применение свинца
- 9 Олово
- 9.1 Свойства олова
- 9.2 Applications of Tin
- 10 Zinc
- 10.1 Properties of Zinc
- 10.2 Applications of Zinc
- 11 Cobalt
- 11.
 1 Properties of Cobalt
1 Properties of Cobalt
- 11.
- 12 Bronze
- 12.1 Properties of Bronze
- 12.2 Применение бронзы
- 13 Латунь
- 13.1 Применение латуни
- 14 Заключительные мысли
наша металлургия. Около 5 % земной коры состоит из железа. Он дешев и используется почти во всех отраслях промышленности. Хотя он присутствует не в чистом виде, а в виде соединения, такого как оксид железа, поэтому мы должны извлечь его перед использованием. Традиционный метод – плавка в доменной печи.
Благодаря исследовательской деятельности, мы можем использовать самые лучшие металлы из железа. Говоря о свойствах железа, это мягкое и пластичное вещество. Его температура плавления (1538 градусов по Цельсию) делает его подходящим металлом для использования в особых нагретых средах.
Известные свойства железа
● Плотность: 7,8 г.см-3
● Температура плавления: 1536 °C или 2800 °F
● Теплопроводность: 76,2 Вт/м·К
● Предел текучести: 50 МПа0011
● Предел прочности при растяжении: 540 МПа
Применение железа
● В производстве магнитов
● В производстве стали
● Используется в транспортном оборудовании
● Используется в различном технологическом оборудовании1 Вы уже 9 должен знать о Сталь ; он не нуждается в представлении, поскольку уже является самым распространенным типом металла в мире.

Но все же, мы совершенно уверены, что вы не знаете некоторых интересных фактов о стали, о которых мы вам расскажем. Это сплав Железо, в котором присутствует содержание углерода до 2% , но этот небольшой процент углерода может существенно повлиять на свойства железа, сделав его совершенно новым металлом «Сталь».
Сталь является пластичным материалом, обладает большей прочностью и способностью выдерживать большие напряжения и деформации. Поэтому более полезно и практично использовать сталь во многих промышленных применениях. Из-за высокой теплопроводности в последнее время сталь также входит в состав различной кухонной посуды, наряду с другими видами металлов.
Сталь также используется в производстве балок и конструкций строителями и инженерами-строителями. Это также относительно дешевле по сравнению с другими процедурами заготовки металла. Знаете о знаменитой Эйфелевой башне? Он также сделан из стали, что является причиной его расширения до 6 дюймов в летнее время.

Свойства стали
● Плотность: 7,75 и 8,05 г/см3
● Температура плавления: 1350–1450 °C
● Теплопроводность: 45 Вт/мК
● Предел текучести: 350 МПа
● Предел прочности при растяжении: 420 МПа
Применение стали
● Используется в производстве зубчатых колес
● Используется в строительстве больших конструкций (здания, башни, мосты и т. д.)
1 ● Используется в стальной упаковке (луженой)
● Используется в станочных инструментах и оружии.
Марки стали по SAE (Общество автомобильных инженеров)
Для стандартизации свойств и состава стальных сплавов SAE International ввела систему нумерации для классификации сплавов по определенным категориям. Это четырехзначная система классификации стали, в которой первые две цифры представляют тип стали и концентрацию легирующих элементов, а последние две цифры предназначены для представления концентрации углерода, присутствующего в металле.
Система классификации стали SAE удобна для инженеров и исследователей при проектировании изделий определенной геометрии.
 Кроме того, эта система стандартизирует свойства материалов, обеспечивая общие знания.
Кроме того, эта система стандартизирует свойства материалов, обеспечивая общие знания.Обычная сталь
Первоначально сталь изготавливалась путем соединения только углерода и железа, которая теперь известна как углеродистая сталь. Чем больше углерода мы добавляем в железо, тем тверже оно становится из-за свойств углерода. Однако по мере увеличения прокаливаемости металла его эластичность снижается. Кроме того, сталь с меньшим содержанием углерода легко производить, обрабатывать и перерабатывать.
Углеродистая сталь подразделяется на три категории: низкоуглеродистая, среднеуглеродистая и высокоуглеродистая. Методы термической обработки обычно обеспечивают его. Высокоуглеродистая сталь прочна и отлично противостоит истиранию и может выдерживать большие нагрузки без деформации, но внезапно ломается из-за своей хрупкости. С другой стороны, низкоуглеродистая сталь может сильно деформироваться перед выходом из строя. Углеродистая сталь в настоящее время используется для повседневных и дешевых применений, таких как строительные конструкции и простое механическое оборудование.

Углеродистую сталь легко отличить по ее тусклой структуре с матовым покрытием. Для очень ответственных областей, где коррозия и деформация недопустимы ни в какой степени, не рекомендуется использовать углеродистую сталь из-за ее коррозионной природы и высокой теплопроводности.
Нержавеющая сталь
Это тип стали, который имеет относительно более высокий процент хрома, чем другие типы стали, например, от 10% до 30%. Добавление избыточного количества хрома приводит к отличной устойчивости к коррозии и нагреву. Дополнительные элементы, такие как никель, молибден и титан, также включены для изменения свойств в соответствии с нашими условиями проектирования.
Нержавеющая сталь это тип металла, который сегодня необходим для многих применений, где необходимо использование жаростойких и коррозионно-стойких материалов из-за высоких уровней окисления. Мы можем видеть сталь в ножах, чайниках и другой кухонной утвари.
Скорость коррозии нержавеющей стали намного меньше по сравнению с другими видами стали.
 Таким образом, использование его в суровых условиях не означает, что ржавчина никогда не повлияет на него. Специальные покрытия и правильный уход — лучший способ защитить любой тип стали. Например, в судостроении очень ограничено использование нержавеющей стали. Правильное использование покрытий, антикоррозийных систем и частые проверки гарантируют, что конструкция корабля безопасна без использования более дорогой нержавеющей стали.
Таким образом, использование его в суровых условиях не означает, что ржавчина никогда не повлияет на него. Специальные покрытия и правильный уход — лучший способ защитить любой тип стали. Например, в судостроении очень ограничено использование нержавеющей стали. Правильное использование покрытий, антикоррозийных систем и частые проверки гарантируют, что конструкция корабля безопасна без использования более дорогой нержавеющей стали.Другие сплавы
Желаемые физические и химические свойства могут быть достигнуты путем добавления в сталь различных типов металлов. Эти металлы добавляются преднамеренно, потому что железо и углерод сами по себе не могут обеспечить пластичность, ковкость, формуемость и другие физические свойства.
Марганец, ванадий, хром, никель и вольфрам являются распространенными легирующими материалами для стали. Каждый металл имеет уникальное свойство. Например, вольфрам придает зернистой структуре большую стабильность и прокаливаемость. Кроме того, марганец повышает устойчивость к ударам и нагреву, что делает металл пригодным для использования в производстве шестерен.

Некоторые стальные сплавы дороги для некоторых проектов, и люди используют такие методы, как гальванизация. В каждой задаче вы должны сбалансировать качество и долговечность со стоимостью.
Алюминий — отличная альтернатива стали и железу, а также один из самых важных металлов в производственной отрасли. Столетия назад алюминий был дороже золота. Но в прошлом веке процесс Холла-Эру произвел революцию в извлечении алюминия из оксида алюминия с помощью электролиза, и его стали использовать в различных отраслях промышленности. Хотя добыча алюминия немного дорогая. Таким образом, переработка алюминия всегда имеет решающее значение для сохранения нашей энергии и ресурсов.
Будучи необычайно мягким и пластичным, алюминий стал идеальным металлом для использования в таких технологиях изготовления, как обработка на станках с ЧПУ, сверление, фрезерование и штамповка. Вы можете создавать самые сложные геометрические фигуры с высокой детализацией, используя этот металл в качестве исходного материала.
 Это металл, который весит намного меньше стали, но обладает хорошей прочностью. Вот почему он имеет гораздо более высокое отношение прочности к весу, что делает его правильным выбором для автомобильной и авиационной промышленности, где серьезной проблемой являются перепроектирование и снижение веса.
Это металл, который весит намного меньше стали, но обладает хорошей прочностью. Вот почему он имеет гораздо более высокое отношение прочности к весу, что делает его правильным выбором для автомобильной и авиационной промышленности, где серьезной проблемой являются перепроектирование и снижение веса.Как и любой другой металл, помимо преимуществ, алюминий имеет и недостатки. Некоторые проблемы с алюминием связаны с его высокой теплопроводностью и низкой температурой плавления. Это делает его уязвимым для быстрого возгорания. Поэтому всегда целесообразно очищать поверхность алюминия (который представляет собой оксид алюминия) перед сваркой, так как разница температур плавления будет мешать процессу сварки. Кроме того, сварщик должен быть быстрым, так как медленная сварка может увеличить риск прожога.
Нередко можно встретить алюминий с разными металлами в составе одной и той же конструкции. Особое внимание следует обратить на коррозию алюминия с некоторыми видами стали.
Свойства алюминия
● Плотность: 2,7 г/см³
● Температура плавления: 660,3 °C
● Теплопроводность: 205,0 Вт/м·К (высокая)
● Предел текучести: 310 МПа ● Предел текучести при 100 сек.
 : 700 МПа
: 700 МПаПрименение алюминия
● Используется в алюминиевой фольге
● Кухонная утварь
● Используется в производстве оконных и дверных рам
● Используется в солнечных панелях
● Используется в качестве альтернативы стали в автомобильной промышленности.
Медь является, возможно, одним из старейших металлов, используемых человеческой цивилизацией, и до сих пор остается ценным металлом в производственной промышленности. Сплавы меди достаточно универсальны, чтобы их можно было использовать в качестве основного металла в любой профессиональной отрасли. Вот почему мир потребляет около 18 миллионов тонн меди в год. Еще один удивительный факт заключается в том, что около 40% отходов перерабатывается.
Медь славится своей высокой электропроводностью. Существует довольно много процессов механической обработки, связанных с медью, включая штамповку, формование, полировку, волочение проволоки, прядение и нанесение покрытия.
 Медь похожа на алюминий в том смысле, что конечные продукты мягкие и должны транспортироваться и храниться с особой осторожностью, так как небольшое усилие может разрушить их форму. Эта мягкость также может быть проблемой в процессе обработки, так как немного более высокое усилие резания может сломать кромку металла, что приведет к значительным потерям материала.
Медь похожа на алюминий в том смысле, что конечные продукты мягкие и должны транспортироваться и храниться с особой осторожностью, так как небольшое усилие может разрушить их форму. Эта мягкость также может быть проблемой в процессе обработки, так как немного более высокое усилие резания может сломать кромку металла, что приведет к значительным потерям материала.К медным сплавам можно применять почти любые методы механической обработки, соединения, сварки или деформации благодаря их мягкости. Одним из больших преимуществ использования меди в качестве поверхностного материала является то, что она не требует покраски или покрытия из-за присущих ей свойств сопротивляться коррозии. В некотором смысле металл защищает себя, образуя вокруг себя слой оксидов, карбонатов и других молекул. Этот защитный слой называется патиной. Единственная коррозия, которой подвержена медь, — это гальваническая коррозия из-за контакта металла с металлом. Дуговая сварка, лазерная сварка, сварка в среде защитных газов являются одними из основных методов сварки меди.

Свойства меди
● Плотность: 8,96 г/см³ при комнатной температуре
● Температура плавления: 1085 °C
● Теплопроводность: 385,0 Вт/мК (очень высокая)
● Предел текучести: предел текучести 6 медных сплавов -69 МПа
● Предел прочности при растяжении: 172-220 МПа
Применение меди
● Передача электроэнергии
● Используется в транспортной отрасли
● Широко используется в двигателях электроприборов
● Используется в сантехнике
● Используется в теплообменниках (котлах, нагревателях и т. д.)
Серебристый металл с блестящей текстурой, никель – хорошо известный элемент, присутствующий в большинстве сплавов, таких как монель. , нихром и пермаллой. Процесс скрепления представляет собой современный метод извлечения чистого никеля. Он пользуется наибольшим спросом среди всех типов металлов в лакокрасочной промышленности благодаря своей стойкости к коррозии в воде и воздухе. В настоящее время никель является основным ингредиентом большинства покрытий.
 Однако этот металл можно найти во многих сплавах, и самым известным из них является нержавеющая сталь.
Однако этот металл можно найти во многих сплавах, и самым известным из них является нержавеющая сталь.Никель постоянно используется в пищевой и электронной промышленности для улучшения качества продукции благодаря его коррозионной стойкости к различным щелочам. Как правило, вы не хотели бы использовать никель в чистом виде из-за его неоптимизированных физических и химических свойств, но его сплав может быть очень полезным. Благодаря высокой теплопроводности никелевые сплавы являются лучшим материалом для теплообменников, где различные жидкости делают его очень агрессивной средой.
Никель легко изготовить, поскольку его можно использовать в большинстве процессов. Он имеет очень хорошую свариваемость из-за низкой скорости упрочнения. Проще говоря, это означает, что изгиб или деформация материала не сделает его твердым и хрупким.
Использование никеля постоянно растет, поскольку электромобили и гибридные автомобили постоянно совершенствуются. Спрос на эти автомобили создает идеальные условия для массового производства никель-кадмиевых аккумуляторов.
 По данным Геологической службы США, около 89на сегодняшний день в мире обнаружены запасы никеля.
По данным Геологической службы США, около 89на сегодняшний день в мире обнаружены запасы никеля.Свойства никеля
● Плотность: 8,908 г/см³ при комнатной температуре
● Температура плавления: 1455 °C
● Теплопроводность: 90,9 – 91 Вт/мК (хороший проводник тепла)
● Y Прочность: 110 МПа (отожженный)
● Предел прочности при растяжении: 345 МПа (отожженный)
Применение никеля
● Грунтовка для хромирования
● Компоненты батареи требуют никеля
● Используется в качестве катализатора для различных химических процессов
● Используется в производстве нержавеющей стали
● Используется в производстве литий-ионных батарей.
Вольфрам — это белый металл, обладающий отличной коррозионной стойкостью. Он известен благодаря своей самой высокой температуре плавления среди всех известных чистых металлов. Большинство отраслей промышленности не используют вольфрам в чистом виде. Вместо этого они используют его в виде карбида вольфрама, который обладает отличной прочностью на растяжение и твердостью.
 Его можно получить реакцией вольфрама и углерода при температуре около 1400–2000 ° C.
Его можно получить реакцией вольфрама и углерода при температуре около 1400–2000 ° C.Обладает высокой устойчивостью к истиранию; по этой причине он используется в буровом и обрабатывающем инструментальном оборудовании, легко режющем титан и другие твердые материалы. Его также называют цементированным карбидом. Крупнейший производитель вольфрама в мире в Китае.
Карбид вольфрама используется не только в процессах механической обработки, но также играет важную роль в производстве боеприпасов и горнодобывающей промышленности. Исследователи нашли его применение в хирургическом оборудовании, таком как ножницы, иглодержатели, рукоятки лезвий и т. д. Это важный компонент для создания эффективных режущих инструментов для фрезерования, сверления и токарной обработки. Механическая обработка должна выполняться с большей осторожностью, поскольку мы увеличиваем количество вольфрама в карбиде вольфрама. Также рекомендуется использовать охлаждающую жидкость (с высокой смазывающей способностью) в процессе обработки.
 Таким образом, мы можем получить чрезвычайно точные допуски и чистоту поверхности.
Таким образом, мы можем получить чрезвычайно точные допуски и чистоту поверхности.Одним из наиболее важных применений вольфрама было производство нитей накаливания в лампах, но постепенно его использование постепенно прекращается из-за разработки более энергоэффективных источников света. В любом случае, никто не может отрицать значение вольфрама в промышленности материалов, поскольку он всегда широко использовался в сварке и в качестве нагревательного элемента в печах.
Свойства вольфрама
● Плотность: 19,25 г/см3
● Температура плавления: 3422 °C
● Теплопроводность: 173 Вт/мК (хороший проводник тепла)
● Предел текучести: 750 МПа
● Предел прочности при растяжении: 980 МПа
Применение вольфрама
● Используется в качестве нагревательной нити
● Используется в производстве сплавов тяжелых металлов, например, )
● Используется в электродах для дуговой сварки
● Используется в горнодобывающей и нефтяной промышленности
● Используется в производстве сопел ракет
Титан недавно приобрел популярность в металлургической промышленности после его открытия в 1791.
 Будучи седьмым по распространенности металлом на Земле, титан по-прежнему остается одним из самых дорогих металлов, известных на сегодняшний день, потому что его очень трудно очистить до чистой формы. Хотя стоит извлечь его из его соединений и использовать его преимущества.
Будучи седьмым по распространенности металлом на Земле, титан по-прежнему остается одним из самых дорогих металлов, известных на сегодняшний день, потому что его очень трудно очистить до чистой формы. Хотя стоит извлечь его из его соединений и использовать его преимущества.Титан отлично работает в окисленных средах благодаря наличию оксидной пленки на поверхности. Эта пленка защищает металл так же, как патина защищает медь. В зависимости от толщины слоя металл отражает разные цвета радуги.
Титановые сплавы обеспечивают отличное сопротивление ползучести и относительно более высокую прочность, чем другие обычные металлы. Отдача, которую вы получите в титане, несомненно, будет более значительной, чем у обычных металлов, из-за низкого значения модуля Юнга
Водород атакует титан гораздо сильнее, чем кислород; поэтому титан нельзя помещать в такую среду, где избыточно присутствует водород. Поскольку его теплопроводность низкая, производители используют надлежащие меры для его обработки в виде острых режущих инструментов и большого количества смазки.

Свойства титана
● Плотность: 4,506 г/см³
● Температура плавления: 1668 °C
● Теплопроводность: 17 Вт/мК (плохой проводник тепла)
● Предел текучести Ti-6Al-4 (Класс 5), отожженный: 970 МПа
● Прочность на растяжение с надрезом: 1450 МПа
Применение титана
● Используется в броневой обшивке
● Используется в ракетах и космических кораблях
● Используется в автомобильной промышленности
● Используется в теплообменнике
● Используется в опреснительных трубах
Хотя свинец является одним из наиболее широко используемых металлов в производстве среди всех типов металлов, он по-прежнему редко встречается по сравнению с другими металлами на Земле. . Это голубовато-белый металл со светящимся видом. В чистом виде он реагирует с кислородом воздуха, образуя на своей поверхности оксид свинца, что делает его твердым и хрупким, но в то же время повышает его устойчивость к коррозии.
Этот тип металла очень стабилен, потому что очень кислые растворы, включая соляную и серную кислоты, не могут его растворить.
 Благодаря своей стабильности и высокой плотности свинец является отличным материалом для улавливания или блокирования гамма-излучения. Однако при вдыхании его паров он очень токсичен для здоровья человека. Десятилетия назад он был ингредиентом многих предметов повседневного обихода, включая топливо. В настоящее время использование свинца ограничено.
Благодаря своей стабильности и высокой плотности свинец является отличным материалом для улавливания или блокирования гамма-излучения. Однако при вдыхании его паров он очень токсичен для здоровья человека. Десятилетия назад он был ингредиентом многих предметов повседневного обихода, включая топливо. В настоящее время использование свинца ограничено.Свойства свинца
● Плотность: 11,34 г/см3
● Температура плавления: 327,5 °C
● Теплопроводность: очень низкая
● Предел текучести: 5,5 МПа
● Предел прочности при растяжении: 12 МПа
Применение свинца
производство тетраэтилсвинца
● Используется в амортизаторах вибрации
● Используется в боеприпасах
● Используется в радиационной защите
Возможно, вы слышали о жестяных листах. Это полезный материал для производства листового металла из-за его мягкости и податливости. Это важный элемент для изготовления различных сплавов, в состав которых входит свинец.
 Одним из его распространенных применений является производство бронзы.
Одним из его распространенных применений является производство бронзы.Олово было излюбленным материалом промышленников, поскольку оно доступно по цене по сравнению со сталью и медью. Кроме того, олово является водостойким, что делает его лучшим выбором для упаковки пищевых продуктов. Лужение — это распространенный способ защиты других металлов путем нанесения слоя на их поверхность. Его легко изготовить, так как олово можно легко разрезать и придать ему различные сложные формы, такие как ромбы, конусы или ромбы. Именно поэтому его используют для создания украшений и других декоративных целей в доме. Благодаря своей долговечности и устойчивости он занял свое место во многих роскошных домах. Интерьер выглядит очень хорошо и оригинально из-за олова, использованного в стенах и потолках.
Свойства олова
● Плотность: 7,287 г/см3
● Температура плавления: 231,9 °C
● Теплопроводность: 66,6 Вт/мК при 300K (хороший проводник тепла)
● Предел текучести 4,5 МПа 200 °C
● Предел прочности при растяжении: 200 МПа
Применение олова
● Используется в банках для упаковки пищевых продуктов
● Используется в масляных фильтрах
● Используется в воздуховодах и полках
● Используется в игрушках0011Поговорим еще об одном интересном металле в нашем списке типов металлов.
 Будучи четвертым по популярности металлом, цинк представляет собой бело-голубоватый металл с многочисленными полезными свойствами. Будь то гальванизация стали или наружные применения, такие как крыша, окна или стеновые панели, цинк находит широкое применение в каждом доме и промышленности. Цинк широко используется как антикоррозийный материал.
Будучи четвертым по популярности металлом, цинк представляет собой бело-голубоватый металл с многочисленными полезными свойствами. Будь то гальванизация стали или наружные применения, такие как крыша, окна или стеновые панели, цинк находит широкое применение в каждом доме и промышленности. Цинк широко используется как антикоррозийный материал.ZInc является активным восстановителем и несколько более реакционноспособен, чем большинство металлов, таких как железо и сталь. Большая часть производимого сегодня цинка производится в горнодобывающей промышленности, а некоторые его части перерабатываются. Возможно, вы знакомы с Брассом; Цинк является его обычным компонентом. Это обычный катализатор для многих химических процессов, которые необходимо проводить при оптимальных условиях температуры и реакционной способности.
Свойства цинка
● Плотность: 7,140 г/см3
● Температура плавления: 419,5 °C
● Теплопроводность: 112,2 Вт/м·К (хороший проводник тепла)
● Предел прочности при растяжении: 90 3 MP1011a Применение цинка
● Используется в производстве сплавов, таких как латунь
● Используется в фармацевтике
● Используется в текстильной промышленности
● Используется в косметике
● Используется в батареях
Кобальт — чрезвычайно полезный серебристо-белый металл.
 Это очень важный металл для разработки аккумуляторов. Свойства этого металла зависят от того, как соединены молекулы. Есть два аллотропа кобальта с совершенно разными свойствами; со структурой HCP и структурой FCC, которые являются ферромагнитными и могут лучше всего подходить для магнитных применений, где высока температура. Это умеренно реакционноспособный металл, растворяющийся в разбавленных кислотах. Кислород также реагирует с кобальтом при высоких температурах.
Это очень важный металл для разработки аккумуляторов. Свойства этого металла зависят от того, как соединены молекулы. Есть два аллотропа кобальта с совершенно разными свойствами; со структурой HCP и структурой FCC, которые являются ферромагнитными и могут лучше всего подходить для магнитных применений, где высока температура. Это умеренно реакционноспособный металл, растворяющийся в разбавленных кислотах. Кислород также реагирует с кобальтом при высоких температурах.Как и в любой химической реакции, более мелкие частицы кобальта более реакционноспособны по сравнению с более крупными частицами кобальта. Кобальт обычно не добывается явно; вместо этого он получается как побочный продукт железа, меди и цинка. Если вы хотите узнать о крупнейшем в мире производителе рафинированного кобальта, ответом будет Китай.
Свойства кобальта
● Плотность: 8,86 г/см3
● Температура плавления: 1495 °C
● Теплопроводность: 100 Вт/мК (хороший проводник тепла)
● Предел текучести при растяжении: 100 МПа
● Предел прочности при растяжении: 1250 МПа
Бронза представляет собой сплав, изготовленный из двух ранее обсуждавшихся металлов, олова и меди.
 Есть сотни приложений, где бронза широко используется. Бронза — очень легкоплавкий металл, что делает процесс создания предметов литьем простым. Однако этот факт не делает его мягким, так как он тверже меди.
Есть сотни приложений, где бронза широко используется. Бронза — очень легкоплавкий металл, что делает процесс создания предметов литьем простым. Однако этот факт не делает его мягким, так как он тверже меди.В археологический период самым твердым металлом, известным людям, была бронза, поэтому эту эпоху назвали Бронзовым веком. Позже железный век сменил бронзовый, но бронза продолжала широко использоваться. Бронза была первым сплавом, который когда-либо был сделан, и он был сделан в современной Турции около 5000 лет назад.
Бронза – это не соединение, а смесь элементов, поэтому на бумаге можно составить любые пропорции. Бронза плавится при более низкой температуре, чем чистый металл; следовательно, его легко затачивать, и его можно использовать в машинах и оружии.
Свойства бронзы
● Плотность: 8,8 г/см3
● Температура плавления: от 950 до 1050 °C
● Теплопроводность: 83,0 Вт/мс (умеренный проводник тепла)
019016 Применение бронзы 90 в изготовлении скульптур.
● Используется в производстве инструментов и оружия.
● Широко используется в производстве монет.
● Широко используется в музыкальных инструментах и медалях.
● Благодаря своей устойчивости широко используется в соленой воде. Винты судовых двигателей и другие детали были разработаны с использованием бронзы.
● Одним из применений бронзы является промышленное литье из-за того, что с ней легко работать.
● Из-за отсутствия искр и твердости бронза используется для изготовления строительных инструментов, таких как молоток и отвертки.
Латунь — последний материал, который мы хотели бы добавить в наш список типов металлов. Это другой сплав, состоящий из меди и цинка. Пропорции цинка и меди изменяются с различными вариациями для достижения различных свойств. Латунь чем-то похожа на бронзу; вместо олова в латуни содержится цинк. Мышьяк, свинец, фосфор, алюминий, марганец и кремний можно найти в латуни в крошечных пропорциях.
Свинец добавляется в латунь в количестве около 2%, что улучшает механические свойства латуни.


