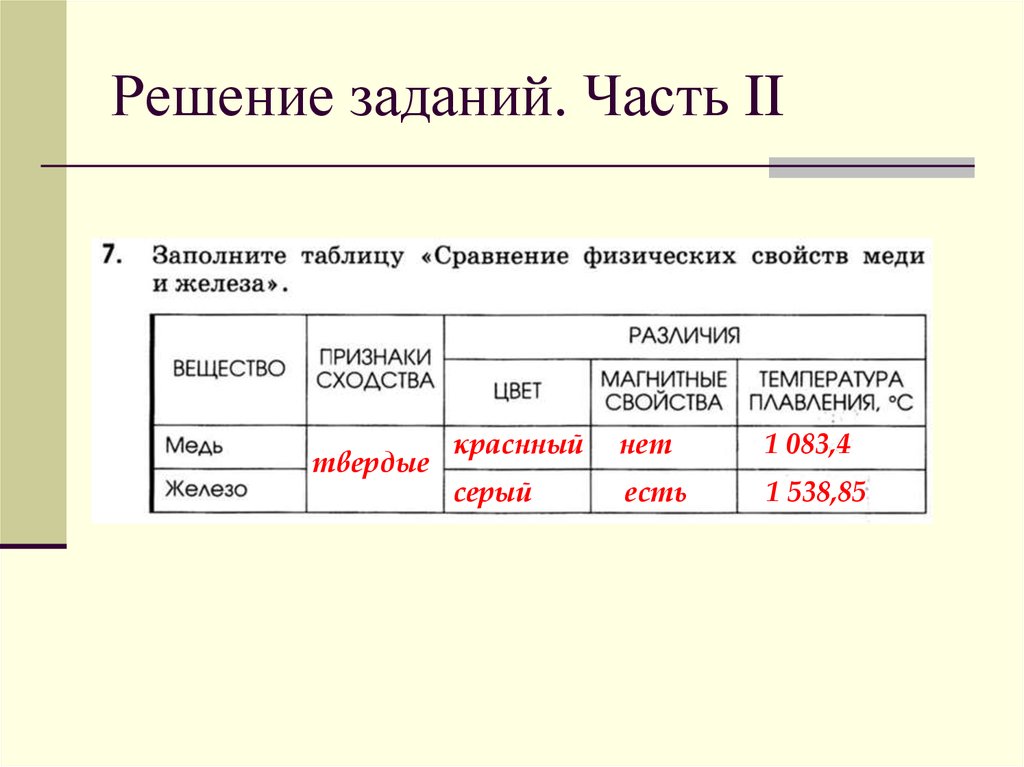
Сравнить серу и медь по физическим свойствам: Сравните физические свойства меди и серы
alexxlab | 20.05.2023 | 0 | Разное
Физические и механические свойства меди
Медь – цветной металл, который применяют в промышленности и в быту. У вещества уникальные особенности, из-за чего элемент остается востребованным в течение тысяч лет. В статье подробно разберем, в чем заключается популярность материала.
Физические свойства – внутренние характеристики, которые есть у медных изделий. Параметры определяют общность или различие с другими элементами. Отличительные черты проявляются как ответная реакция на внешнее воздействие сред и полей.
Медь – пластичный металл розовато-золотого цвета. На открытом воздухе поверхность покрывает оксидная пленка (патина), которая проявляется в виде красновато-желтого отблеска. Оттеночный эффект возникает из-за электронных переходов между третьей заполненной и четвертой полупустой орбиталями атомными, что аналогично длине оранжевого светового луча.
У металлической заготовки высокие характеристики плотности и температуры плавления, кипения. На свойства меди оказывают влияние примеси, добавленные в массу.
- олово;
- железо;
- мышьяк;
- сурьма;
- фосфор.
Cuprum относят к переходным металлам. Величина электроотрицательности по шкале Полинга – 1,9 единиц. У компонента высокие показатели тепло- и электропроводности. По отличительным чертам купрум уступает серебру.
Медные прокат, прутки и проволока устойчивы к химическим и природным влияниям. Элемент не вступает во взаимодействие с солями, щелочами, но медленно растворяется в концентратах азотной или серной кислоты. У материала сильная коррозийная стойкость к влажным условиям и ультрафиолету. Компонент является диамагнетиком, на который не воздействует магнитное поле.
Механические особенности
Механические свойства – способность составляющих сопротивляться внешним нагрузкам. Величина определяет стойкость исходной заготовки к воздействиям напряжений, приводящих к разрушению и деформации. Опции важны как при производстве изделий, так и в период эксплуатации.
Опции важны как при производстве изделий, так и в период эксплуатации.
Купрум плавится при температуре +1083 С, кипит – при +26570 С. В холод (от 0 до -269 С) cuprum сберегает базовые параметры прочности и вязкости, обычные для комнатных условий. При термической обработке (закалке, обжиге) готовую продукцию можно сделать тверже или мягче исходной заготовки.
У меди высокие характеристики устойчивости к сжатию и разрыву. Ее легко обрабатывать, придавая любую форму и изгиб. Материал вытягивают в тонкую проволоку или прокатывают в листы, прутки. При растяжении предел прочности достигает 22 кгс/мм2, модуль упругости по Юнгу – 110 ГПа.
Купрум – уникальный цветной металл с высокой механической прочностью и с устойчивостью к внешним воздействиям. Компонент легко обрабатывать, поэтому его применяют при производстве труб, проката и проволоки любой толщины. Из-за универсальности использования стоимость вещества никогда не была низкой. Актуальную цену меди в Москве можно узнать на нашем сайте, перейдя по ссылке: https://pandorametal.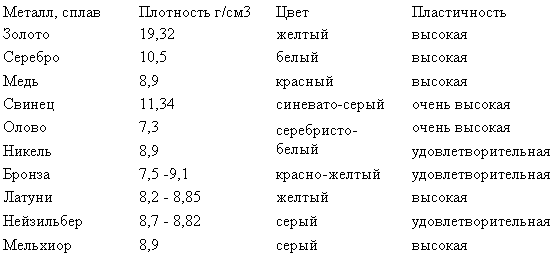 ru/prices
ru/prices
цвет, физические свойства купрум, характеристика, как определить, химический элемент (металл)
Медь что это такое: цвет, физические свойства купрум, характеристика, как определить, химический элемент (металл)!–www.miralinks.ru –>
Перейти к содержанию
Search for:
На чтение 10 мин Просмотров 315 Опубликовано
В нашей статье мы описали все основные физические и химические свойства меди, ее отличия от множества похожих металлов и сплавов. Вы узнаете, как можно отличить медь в домашних условиях от бронзы, латуни и других металлов.
Содержание
- Что представляет собой медь
- Основные свойства меди
- Физические свойства меди
- Химические свойства
- Оптические свойства
- Кристаллографические свойства
- Как идентифицировать медь на глаз
- Как определить медь в домашних условиях
- Проверить цвет
- Тестировать магнитом
- Применить нагрев
- Как отличить медь от других металлов
- Как отличить медь от бронзы
- Как отличить медь от латуни
- Как отличить медь от алюминия
- Медь в природе
- Способы получения
- Пирометаллургический
- Гидрометаллургический
- Интересное о меди
Что представляет собой медь
Хотя она не является ни редким, ни драгоценным металлом ее ценность как химического элемента достаточно высока. В первую очередь это связано с тем, что она широко применяется в медицине, полупроводниковых приборах, фотоэлементах, на производствах и даже оборонной промышленности.
В первую очередь это связано с тем, что она широко применяется в медицине, полупроводниковых приборах, фотоэлементах, на производствах и даже оборонной промышленности.
Цвет меди является основным признаком, по которому можно выделить ее среди похожих металлов. В природе встречается в чистом виде как мягкий материал светловато оранжевого цвета, при контакте с воздухом покрывающийся зеленоватой оксидной пленкой. К характеристикам меди также относится исключительная пластичность.
Основные свойства меди
Все свойства характеризующее медь как ценный для человека химический элемент подразделяются на четыре основные группы – физические, химические, оптические и кристаллографические. Рассмотрим последовательно каждое свойство.
Физические свойства меди
Обладает ярко выраженным красновато оранжевым цветом и хорошо взаимодействует с различными примесями, улучшающими или дополняющими ее физические свойства.
Хорошо проводит тепло и электрический ток (именно благодаря этому свойству получила широкое распространение в электротехнике). Теплопроводные свойства меди нашли применение в системах охлаждения, радиаторах и теплообменниках.
Подробнее о физических свойствах меди в таблице.
Химические свойства
Химический состав меди слабо взаимодействует с неметаллами и практически не реагирует на внешние окислители. В нормальном состоянии, в помещении с сухим воздухом медь не подвержена быстрому окислению. Также слабо реагирует на кислоты и щелочи. Более подробную информацию о химических свойствах этого металла можно узнать из представленной таблицы.
Читать также: Как заварить глушитель электросваркой самостоятельно
Оптические свойства
Спектральный анализ меди показывает, что зависимость преломления оптического показателя под влиянием увеличения длины волны настолько малозначима, что может не приниматься в расчет на производствах. В спектральном диапазоне от 200 нм до 900 нм не наблюдается серьезных изменений коэффициента поглощения.
В спектральном диапазоне от 200 нм до 900 нм не наблюдается серьезных изменений коэффициента поглощения.
Теплоемкость отдельно взятого медного изделия такова, что поглощение энергии светового импульса на единицу площади не приводит к сколько нибудь значимому нагреву при испытаниях в естественных условиях эксплуатации.
Кристаллографические свойства
Основные кристаллографические свойства меди можно узнать из представленной таблицы.
Как идентифицировать медь на глаз
Метод визуальной идентификации самый простой и как ни странно наиболее действенный из доступных. Медные изделия, очищенные от грязи и окислов должны иметь ярко выраженный красноватый или розоватый цвет. При рассмотрении металла в первую очередь стоит вспомнить какие еще химические элементы имеют схожую с медью окраску.
Визуально похожи на медь следующие металлы:
- осмий и металлы на его основе;
- цезий и сплавы, в которых он составляет большую часть процентного соотношения;
- различные сплавы золота.

Очевидно, что если рассматриваемое изделие представляет собой предмет домашнего обихода или деталь электроинструмента, то маловероятно, что для его изготовления использовали большое количество золота или цезия.
Полезная статья: Электрическая дуговая сварка — что это
Как определить медь в домашних условиях
В домашних условиях, где могут попасться медные изделия совершенно различного предназначения, существуют несколько простых, но действенных методов как распознать медь без сложных спектральных анализов и химических лабораторий.
Кроме чистой меди, вполне могут встретиться и сплавы очень похожие по виду, но совершенно отличающиеся по структуре металла и его физико-химическим свойствам. Рассмотренные ниже домашние методы помогут выяснить истинный состав металла даже в таких случаях.
Всего различают три основных способа определения меди.
- Визуальный анализ цвета.
- Тест на магнитные свойства.
- «Тепловой» метод идентификации.

Рассмотрим подробнее каждый из методов.
Проверить цвет
Практически все знают как должна выглядеть медь, но мало кто представляет это цвет визуально. Если есть сомнения в составе представленного металла, то для начала нужно добиться блеска — очистить от следов окислов, пыли, грязи (при наличии).
Если есть возможность и это не повредит самому изделию, то пройтись по видимой части детали мелкозернистой наждачной бумагой.
Полученный результат идентифицируют «на глаз» или же сравнивают с цветом эталонного изделия о котором совершенно точно известно, что это медь. Если такого изделия под рукой не оказалось, то в качестве эталона можно применить токопроводящую жилу от любого силового кабеля.
Как правило, электрические провода изготавливают из чистой меди без примесей.
Тестировать магнитом
Тест на магнитные свойства считается одним из самых надежных методов проверки, но увы не может быть единственным. Чистая медь не магнитится и не намагничивается. Так же не магнитятся и различные медные сплавы. Если смысл только в этом, то на данном этапе тестирование металла можно завершить.
Так же не магнитятся и различные медные сплавы. Если смысл только в этом, то на данном этапе тестирование металла можно завершить.
Если же исследуемое металлическое тело пойдет на вторичную переработку, переплавку или как заготовка для самостоятельного изделия, имеет смысл проверить чистоту металла еще и визуальным методом на срезе торца. Делается это для того, чтобы не спутать чистый металл с например – омедненным алюминием или оловом, которые тоже не реагируют на поднесенное магнитное поле.
Применить нагрев
Кроме всего перечисленного есть и еще один способ проверить медь перед вами или что-то другое. Данный метод применяют только в тех случаях, когда сильный нагрев предположительно медного изделия никак не повлияет на его дальнейшую эксплуатацию.
Исследуемый металл накаляют на открытом огне до температуры в 150 – 200 °C и наблюдают за его состоянием. Чистая медь в процессе нагрева начинает тускнеть и постепенно приобретает буроватый цвет похожий на черные следы окисления.
По мере нагрева вещество не должно выделять резких неприятных запахов, дыма или копоти. Чтобы исключить ошибки, деталь перед нагреванием очищают от внешних загрязнений или моют водой.
Полезная статья: Как выбрать электроды по нержавейке
Как отличить медь от других металлов
Существует ряд металлов со схожими свойствами (цветом, химической реакцией на окислители и магнитными свойствами). Все эти металлы настолько похожи друг на друга, что порой даже специалисты не могут с первого взгляда описать характеристики каждого.
На практике, чаще всего происходит путаница со следующими металлами:
- бронзой;
- латунью;
- алюминием или его сплавами.
Каждый из этих металлов визуально похож, но обладает одним или несколькими свойствами по наличию которых можно однозначно судить о его составе.
Разберем подробнее как отличить медь от бронзы, алюминия или латуни.
Как отличить медь от бронзы
Бронза наиболее часто путаемый металл. По сути это и есть медь, но в сплаве с оловом. В связи с тем, что бронзовые изделия обладают почти тем же набором характеристик, что и медные, отличить их с помощью визуального, магнитного или теплового способа не получится.
По сути это и есть медь, но в сплаве с оловом. В связи с тем, что бронзовые изделия обладают почти тем же набором характеристик, что и медные, отличить их с помощью визуального, магнитного или теплового способа не получится.
Для достижения гарантированного результата проверяемую деталь необходимо слегка деформировать (конечно только в тех случаях, где это допустимо). Медь намного более мягкий и пластичный металл и на изделии из чистой меди однозначно останется вмятина или глубокая царапина. Бронза обладает большей твердостью и останется невредимой.
Второй способ основан на химическом взаимодействии меди с солью. Необходимо приготовить концентрированный раствор обычной поваренной соли, нагреть до температуры 50 – 80 °C и погрузить в него исследуемое изделие (или его часть) на некоторое время (обычно 15-20 минут). Бронзовое изделие не изменит своего первоначального цвета, тогда как медь быстро потемнеет.
Третий способ основан на визуальном восприятии временных изменений. Если перед вами лежит изделие про которое точно известно. Видно, что оно изготовлено достаточно давно и при этом на нем нет ни следа зеленоватого налета, вероятнее всего оно изготовлено не из чистой меди.
Если перед вами лежит изделие про которое точно известно. Видно, что оно изготовлено достаточно давно и при этом на нем нет ни следа зеленоватого налета, вероятнее всего оно изготовлено не из чистой меди.
Полезная статья — Как варить вертикальный шов инвертором
Как отличить медь от латуни
Латунью называется металл, кристаллическая решетка которого состоит из сплава меди с цинком. При высоком содержании в сплаве цинка (от 40% и выше) отличить латунь можно даже визуальным методом – она имеет желтоватый оттенок. В случае, когда примесь цинка не более 10%, на глаз отличия уже не видны. В таких случаях прибегают к «народным» методам.
- Проверка на слух. В связи с тем, что медь более мягкий металл при ударе в него металлическим прутом издает глухой звук похожий на стук упавшего яблока. Латунь звучит более звонче и дольше.
- Если изделие тонкостенное, то можно попробовать его на изгиб. Медь согнется, а латунь будет упругой.

Существуют и другие методы – растворение в соляной кислоте, снятие стружки высокооборотистым фрезером, определение удельной плотности и подобные. Ввиду сложности применения в быту рассматривать их не имеет смысла.
Как отличить медь от алюминия
При наличии двух изделий из чистых металлов различить их не составит труда даже в условиях плохого освещения. Совсем другое дело, когда имеется сплав в непонятном соотношении.
Чаще всего такие сплавы используют для изготовления электрических проводов. Понять из какого металла состоит провод просто, достаточно измерить его сопротивление.
У чистой меди сопротивление всегда меньше чем у алюминия и на сто метров провода не будет превышать 10 Ом. Алюминиевый провод или провод из сплава выдаст гораздо большие показатели.
Алюминиевый провод или провод из сплава выдаст гораздо большие показатели.
Также можно попробовать провод на изгиб – алюминиевый быстро сломается уже после нескольких перегибов, медный выдержит.
Медь в природе
В природе встречается как в соединениях, так и в виде самородков. Большая часть этого металла лежит в поверхностных слоях грунта и добывается открытым способом. Металлургическая руда содержит от 0.25 % до 1.5 % самородной меди на объем грунта.
Полезная статья – Чем заварить нержавейку
Способы получения
Так как даже в «богатой» руде содержание меди не превышает 1.5% плавить такую руду экономически не целесообразно. В целях оптимизации процесса руда предварительно обогащается и далее добывается одним из двух основных методов.
В целях оптимизации процесса руда предварительно обогащается и далее добывается одним из двух основных методов.
Пирометаллургический
Сложный процесс включающий в себя ряд взаимоувязанных этапов:
- обогащение. Суть метода основана на водной флотации, грунт помещается в водяную ванну, где микрочастицы меди увлекаются на поверхность воздушными пузырьками. Данный процесс обогащения позволяет добиться концентрации меди в 35%;
- обжиг. Применяется в основном к руде с большим содержанием серы. После сильного температурного воздействия более половины серы «сгорает», чем также достигается повышение доли меди в руде;
- плавка. Полученную обогащенную руду помещают в плавильные печи и на выходе получают спекшийся медный штейн;
- рафинирование.
 Штейн обрабатывают открытым огнем и электролитом, газовой продувкой удаляются химические примеси. Концентрация чистой меди на этом этапе может достигать 99.97%.
Штейн обрабатывают открытым огнем и электролитом, газовой продувкой удаляются химические примеси. Концентрация чистой меди на этом этапе может достигать 99.97%.
Полезная статья — Поксипол клей двухкомпонентный
Гидрометаллургический
Процесс применяют для руды с критически малым содержанием меди. Суть процесса заключается в химическом растворении руды в концентрате серной кислоты после которой извлекается только медь без содержания других примесей.
Интересное о меди
Медь является неотъемлемым химическим элементом, участвующим в жизненно важных процессах организма. Способствует образованию кровяных телец и замедляет старение организма.
Недостаток меди в организме проявляется в слабой костной структуре и различных патологиях крови. Восполнить недостаток элемента можно употребляя в пищу следующие виды продуктов – любые из видов орехов (лесной, грецкий, миндаль и т.д.), крупы, мясо, говяжья печень, какао и множество других.
Учитывая полезные свойства меди, она очень востребована в медицине, из нее изготавливаются трубопроводы для питательных жидкостей. К примеру, в Японии трубопровод из меди несет в себе сразу две полезные функции – он химически безопасен для организма и сейсмоустойчив, что для острова является важным фактором.
Да
80.72%
Нет
19.28%
Проголосовало: 249
Задавайте свои вопросы в комментариях под статьей. Расскажите, была ли Вам полезна наша статья.
Оцените автора
( 2 оценки, среднее 5 из 5 )
3.5: Различия в материи: физические и химические свойства
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 182627
Цели обучения
Отделить физические свойства от химических.
Все вещества обладают физическими и химическими свойствами. Физические свойства — это характеристики, которые ученые могут измерить без изменения состава исследуемого образца, такие как масса, цвет и объем (объем пространства, занимаемый образцом). Химические свойства описывают характерную способность вещества реагировать с образованием новых веществ; они включают его воспламеняемость и подверженность коррозии. Все образцы чистого вещества обладают одинаковыми химическими и физическими свойствами. Например, чистая медь всегда представляет собой красновато-коричневое твердое вещество (физическое свойство) и всегда растворяется в разбавленной азотной кислоте с образованием синего раствора и коричневого газа (химическое свойство).
Физическое свойство
Физическое свойство — это характеристика вещества, которую можно наблюдать или измерять без изменения идентичности вещества. Серебро — это блестящий металл, который очень хорошо проводит электричество. Из него можно формовать тонкие листы, это свойство называется пластичностью. Соль тусклая и ломкая и проводит электричество, когда она растворена в воде, что она делает довольно легко. К физическим свойствам вещества относятся цвет, твердость, ковкость, растворимость, электропроводность, плотность, температура плавления и температура кипения.
Соль тусклая и ломкая и проводит электричество, когда она растворена в воде, что она делает довольно легко. К физическим свойствам вещества относятся цвет, твердость, ковкость, растворимость, электропроводность, плотность, температура плавления и температура кипения.
Для элементов цвет не сильно отличается от одного элемента к другому. Подавляющее большинство элементов бесцветные, серебристые или серые. Некоторые элементы имеют отличительные цвета: сера и хлор — желтые, медь (разумеется) медного цвета, а элементарный бром — красный. Однако плотность может быть очень полезным параметром для идентификации элемента. Из материалов, существующих в твердом состоянии при комнатной температуре, йод имеет очень низкую плотность по сравнению с цинком, хромом и оловом. Золото имеет очень высокую плотность, как и платина. Чистая вода, например, имеет плотность 0,998 г/см  Это означает, что при добавлении в воду кукурузное масло будет «плавать».
Это означает, что при добавлении в воду кукурузное масло будет «плавать».
| Вещество | Плотность при 25°C (г/см3) |
|---|---|
| кровь | 1,035 |
| жировые отложения | 0,918 |
| цельное молоко | 1,030 |
| масло кукурузное | 0,922 |
| майонез | 0,910 |
| мед |
Твердость помогает определить, как можно использовать элемент (особенно металл). Многие элементы довольно мягкие (например, серебро и золото), в то время как другие (например, титан, вольфрам и хром) намного тверже. Углерод — интересный пример твердости. В графите («грифеле» карандашей) углерод очень мягкий, в то время как углерод в алмазе примерно в семь раз твёрже.
Многие элементы довольно мягкие (например, серебро и золото), в то время как другие (например, титан, вольфрам и хром) намного тверже. Углерод — интересный пример твердости. В графите («грифеле» карандашей) углерод очень мягкий, в то время как углерод в алмазе примерно в семь раз твёрже.
Точки плавления и кипения являются уникальными идентификаторами, особенно для соединений. Помимо получения некоторого представления об идентичности соединения, можно получить важную информацию о чистоте материала.
Химические свойства
Химические свойства вещества описывают его способность подвергаться некоторым химическим изменениям или реакциям в силу своего состава. Присутствующие элементы, электроны и связи придают материи потенциал для химических изменений. Довольно сложно определить химическое свойство, не используя слово «изменение».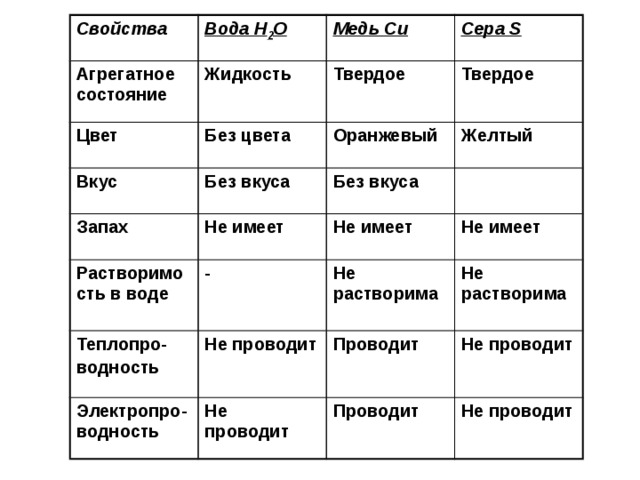
 Химические свойства очень полезны при идентификации веществ. Однако, в отличие от физических свойств, химические свойства можно наблюдать только тогда, когда вещество находится в процессе превращения в другое вещество.
Химические свойства очень полезны при идентификации веществ. Однако, в отличие от физических свойств, химические свойства можно наблюдать только тогда, когда вещество находится в процессе превращения в другое вещество.| Физические свойства | Химические свойства |
|---|---|
| Металлический галлий плавится при 30 o C. | Железный металл ржавеет. |
| Ртуть — очень плотная жидкость. | Зеленый банан при созревании становится желтым. |
| Золото блестит. | Горит сухой лист бумаги. |
Пример \(\PageIndex{1}\)
Какое из следующих химических свойств железа?
- Железо разъедает во влажном воздухе.
- Плотность = 7,874 г/см 3
- Железо в чистом виде мягкое.
- Железо плавится при 1808 К.
Раствор
«Железо разъедает во влажном воздухе» — единственное химическое свойство железа из списка.
Упражнение \(\PageIndex{1A}\)
Какое из перечисленных ниже физических свойств материи?
- коррозионная активность
- рН (кислотность)
- плотность
- воспламеняемость
- Ответить
- с
Упражнение \(\PageIndex{1B}\)
Какое из следующих свойств является химическим?
- воспламеняемость
- температура плавления
- точка кипения
- плотность
- Ответить
- и
Резюме
Физическое свойство – это характеристика вещества, которую можно наблюдать или измерять без изменения свойств вещества. Физические свойства включают цвет, плотность, твердость, температуры плавления и кипения. Химическое свойство описывает способность вещества подвергаться определенному химическому изменению. Чтобы идентифицировать химическое свойство, мы ищем химическое изменение. Химическое изменение всегда производит один или несколько типов материи, которые отличаются от материи, существовавшей до изменения. Образование ржавчины — это химическое изменение, потому что ржавчина — это вещество, отличное от железа, кислорода и воды, существовавших до образования ржавчины.
Физические свойства включают цвет, плотность, твердость, температуры плавления и кипения. Химическое свойство описывает способность вещества подвергаться определенному химическому изменению. Чтобы идентифицировать химическое свойство, мы ищем химическое изменение. Химическое изменение всегда производит один или несколько типов материи, которые отличаются от материи, существовавшей до изменения. Образование ржавчины — это химическое изменение, потому что ржавчина — это вещество, отличное от железа, кислорода и воды, существовавших до образования ржавчины.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.

- Включено
- да
- Теги
- химическое свойство
- физическое имущество
- источник-хим-47458
1.3: Свойства материи — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 21693
↵
Цели обучения
- Отделить физические свойства и изменения от химических
Все материи обладают физическими и химическими свойствами.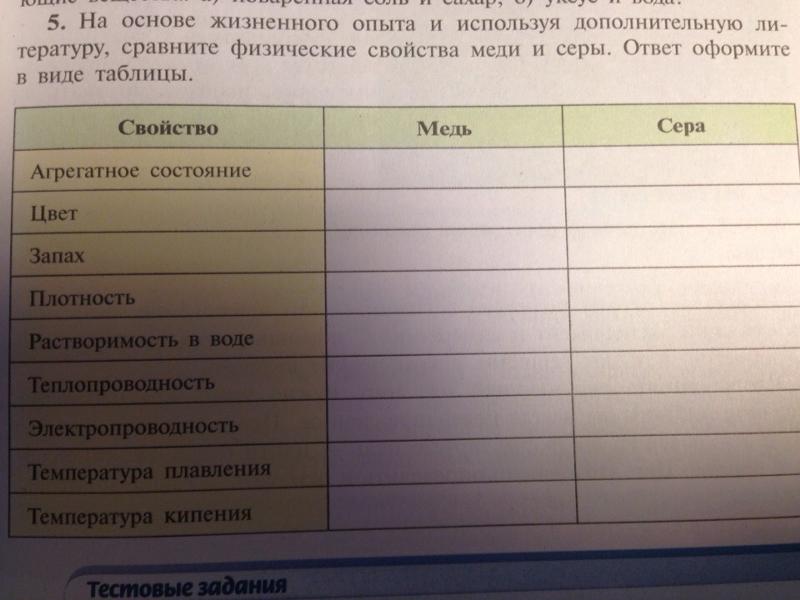 Физические свойства — это характеристики, которые ученые могут измерить без изменения состава исследуемого образца, такие как масса, цвет и объем (объем пространства, занимаемый образцом). Химические свойства описывают характерную способность вещества реагировать с образованием новых веществ; они включают его воспламеняемость и подверженность коррозии. Все образцы чистого вещества обладают одинаковыми химическими и физическими свойствами. Например, чистая медь всегда представляет собой красновато-коричневое твердое вещество (физическое свойство) и всегда растворяется в разбавленной азотной кислоте с образованием синего раствора и коричневого газа (химическое свойство).
Физические свойства — это характеристики, которые ученые могут измерить без изменения состава исследуемого образца, такие как масса, цвет и объем (объем пространства, занимаемый образцом). Химические свойства описывают характерную способность вещества реагировать с образованием новых веществ; они включают его воспламеняемость и подверженность коррозии. Все образцы чистого вещества обладают одинаковыми химическими и физическими свойствами. Например, чистая медь всегда представляет собой красновато-коричневое твердое вещество (физическое свойство) и всегда растворяется в разбавленной азотной кислоте с образованием синего раствора и коричневого газа (химическое свойство).
Физические свойства могут быть экстенсивными или интенсивными. Экстенсивные свойства зависят от количества вещества и включают массу, вес и объем. Интенсивные свойства , напротив, не зависят от количества вещества; они включают цвет, температуру плавления, точку кипения, электрическую проводимость и физическое состояние при данной температуре. Например, элементарная сера представляет собой желтое кристаллическое твердое вещество, которое не проводит электричество и имеет температуру плавления 115,2 °C, независимо от того, какое количество исследуется (рис. \(\PageIndex{1}\)). Ученые обычно измеряют интенсивные свойства для определения идентичности вещества, в то время как экстенсивные свойства передают информацию о количестве вещества в образце.
Например, элементарная сера представляет собой желтое кристаллическое твердое вещество, которое не проводит электричество и имеет температуру плавления 115,2 °C, независимо от того, какое количество исследуется (рис. \(\PageIndex{1}\)). Ученые обычно измеряют интенсивные свойства для определения идентичности вещества, в то время как экстенсивные свойства передают информацию о количестве вещества в образце.
Хотя масса и объем являются экстенсивными свойствами, их соотношение является важным интенсивным свойством, называемым плотностью (\(\rho\)). Плотность определяется как масса на единицу объема и обычно выражается в граммах на кубический сантиметр (г/см 3 ). По мере увеличения массы в данном объеме увеличивается и плотность. Например, свинец с его большей массой имеет гораздо большую плотность, чем тот же объем воздуха, точно так же, как кирпич имеет большую плотность, чем пенополистирол того же объема. При данной температуре и давлении плотность чистого вещества постоянна:
По мере увеличения массы в данном объеме увеличивается и плотность. Например, свинец с его большей массой имеет гораздо большую плотность, чем тот же объем воздуха, точно так же, как кирпич имеет большую плотность, чем пенополистирол того же объема. При данной температуре и давлении плотность чистого вещества постоянна:
\[\begin{align*} \text{плотность} &={\text{масса} \over \text{объем}} \\[4pt] \rho &={m \over V} \label{Eq1} \end{выравнивание*} \]
Чистая вода, например, имеет плотность 0,998 г/см 3 при 25 °C. Средние плотности некоторых распространенных веществ приведены в таблице \(\PageIndex{1}\). Обратите внимание, что кукурузное масло имеет более низкое отношение массы к объему, чем вода. Это означает, что при добавлении в воду кукурузное масло будет «плавать» (рис. \(\PageIndex{2}\)).
| Вещество | Плотность при 25 °C (г/см 3 ) | Вещество | Плотность при 25 °C (г/см 3 ) |
|---|---|---|---|
| кровь | 1,035 | кукурузное масло | 0,922 |
| жировые отложения | 0,918 | майонез | 0,910 |
| цельное молоко | 1,030 | мед | 1,420 |
 Так как плотность масла меньше, чем у воды, оно всплывает на поверхность. (CC-BY SA 3.0; Виктор Блакус).
Так как плотность масла меньше, чем у воды, оно всплывает на поверхность. (CC-BY SA 3.0; Виктор Блакус).Физические свойства и изменение
Физические изменения — это изменения, при которых химические связи не разрываются и не образуются. Это означает, что те же типы соединений или элементов, которые были в начале изменения, остаются и в конце изменения. Поскольку конечные материалы такие же, как и начальные, свойства (такие как цвет, температура кипения и т. д.) также будут одинаковыми. Физические изменения связаны с перемещением молекул, но не с их изменением. Некоторые типы физических изменений включают в себя:
- Изменения состояния (переход из твердого состояния в жидкое или газообразное и наоборот)
- Разделение смеси
- Физическая деформация (порезы, вмятины, растяжения)
- Приготовление растворов (специальных видов смесей) .
Когда кубик льда тает, его форма меняется, поскольку он приобретает способность течь.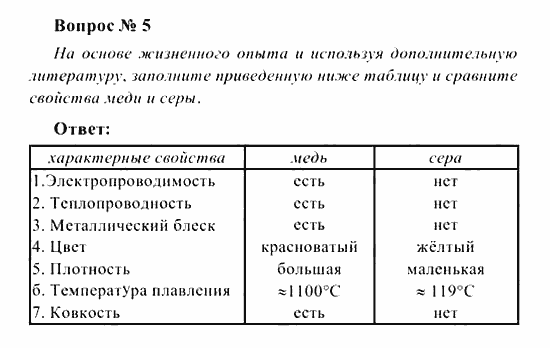 При этом его состав не меняется. Плавление является примером физического изменения (Рисунок \(\PageIndex{3}\)), поскольку изменяются некоторые свойства материала, но не изменяется сущность материи. Физические изменения можно дополнительно классифицировать как обратимые и необратимые. Растаявший кубик льда можно снова заморозить, поэтому таяние является обратимым физическим изменением. Все физические изменения, связанные с изменением состояния, обратимы. Другие изменения состояния включают испарение (жидкость в газ), замерзание (жидкость в твердое) и конденсация (газ в жидкость). Растворение также является обратимым физическим изменением. Когда соль растворяется в воде, говорят, что соль перешла в водное состояние. Соль можно восстановить, выкипятив воду, оставив соль.
При этом его состав не меняется. Плавление является примером физического изменения (Рисунок \(\PageIndex{3}\)), поскольку изменяются некоторые свойства материала, но не изменяется сущность материи. Физические изменения можно дополнительно классифицировать как обратимые и необратимые. Растаявший кубик льда можно снова заморозить, поэтому таяние является обратимым физическим изменением. Все физические изменения, связанные с изменением состояния, обратимы. Другие изменения состояния включают испарение (жидкость в газ), замерзание (жидкость в твердое) и конденсация (газ в жидкость). Растворение также является обратимым физическим изменением. Когда соль растворяется в воде, говорят, что соль перешла в водное состояние. Соль можно восстановить, выкипятив воду, оставив соль.
Рисунок \(\PageIndex{3}\): Таяние льда — это физическое изменение. Когда твердая вода (\(\ce{H_2O}\)) в виде льда превращается в жидкость (воду), она кажется измененной. Однако это изменение носит только физический характер, поскольку состав составляющих молекул остается тем же: 11.19.% водорода и 88,81% кислорода по массе.
Однако это изменение носит только физический характер, поскольку состав составляющих молекул остается тем же: 11.19.% водорода и 88,81% кислорода по массе.
Химические свойства и изменение
Химические изменения происходят при разрыве и/или образовании связей между молекулами или атомами. Это означает, что одно вещество с определенным набором свойств (таким как температура плавления, цвет, вкус и т. д.) превращается в другое вещество с другими свойствами. Химические изменения часто труднее обратить вспять, чем физические изменения.
Одним из хороших примеров химического изменения является сжигание бумаги. В отличие от процесса разрывания бумаги, процесс сжигания бумаги фактически приводит к образованию новых химических веществ (точнее, углекислого газа и воды). Другой пример химического изменения происходит при образовании воды. Каждая молекула содержит два атома водорода и один атом кислорода, химически связанные.
Другим примером химического изменения является то, что происходит, когда в вашей печи сжигается природный газ. На этот раз перед реакцией у нас есть молекула метана, \(\ce{CH_4}\), и две молекулы кислорода, \(\ce{O_2}\), а после реакции у нас есть две молекулы воды, \(\ce{H_2O}\) и одна молекула углекислого газа, \(\ce{CO_2}\). При этом изменился не только внешний вид, но и структура молекул. Новые вещества не обладают такими же химическими свойствами, как исходные. Следовательно, это химическое изменение.
На этот раз перед реакцией у нас есть молекула метана, \(\ce{CH_4}\), и две молекулы кислорода, \(\ce{O_2}\), а после реакции у нас есть две молекулы воды, \(\ce{H_2O}\) и одна молекула углекислого газа, \(\ce{CO_2}\). При этом изменился не только внешний вид, но и структура молекул. Новые вещества не обладают такими же химическими свойствами, как исходные. Следовательно, это химическое изменение.
Горение металлического магния также является химическим изменением (Магний + Кислород → Оксид магния):
\[\ce{2 Mg + O_2 \rightarrow 2 MgO } \nonumber \]
, как и ржавление железа (Железо + Кислород → Оксид железа/ Ржавчина):
\[\ce{4 Fe + 3O_2 \rightarrow 2 Fe_2O_3} \nonumber \]
Используя компоненты состава и свойства, мы имеем возможность отличить один образец вещества от другие.
Различные определения изменений: Различные определения изменений, YouTube(opens in new window) [youtu. be]
be]
Различные определения свойств: Различные определения свойств, YouTube (открывается в новом окне) [youtu.be]
Ссылки
- Петруччи, Биссоннетт, Херринг, Мадура. Общая химия: принципы и современные приложения. Десятое изд. Река Аппер-Сэдл, , штат Нью-Джерси, 07458: Pearson Education Inc., 2011.
- Краколис, Питерс. Основы вводной химии. Активный подход к обучению. Второе изд. Белмонт, CA 94001:Брукс/Коул, 2007.
Авторы и ссылки
- Саманта Ма (Калифорнийский университет в Дэвисе)
1.3: Properties of Matter распространяется по лицензии CC BY-NC-SA 3.0, автором, ремиксом и/или куратором является LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 3,0
- Показать страницу TOC
- № на стр.