Свойства меди алюминия и железа 4 класс: Свойства стали: алюминия, меди, латуни, нержавейки.
alexxlab | 05.02.2023 | 0 | Разное
Контрольно-измерительные материалы по теме “Свойства металлов и сплавов” к разделу “Технология обработки металлов” 6 класс
Контрольно-измерительные материалы
по теме «Свойства металлов и сплавов»
к разделу «Технология обработки металла»
предмета «Технология. Технический труд»
6 класс (мальчики)
Автор: Кабанов Д.Е.
1 вариант
I. Выберите правильный ответ:
1) Все металлы и сплавы делятся на:
а) белые и черные; б) черные и цветные; в) цветные и благородные;
г) белые и цветные.
2) К черным металлам и сплавам относятся:
а) алюминий, сталь, углерод; б) железо, бронза, латунь, в) медь, алюминий, чугун; г) железо, сталь, чугун.
3) В зависимости от свойств стали делятся на:
а) конструкционные и инструментальные; б) механические и технологические; в) черные и цветные; г) чугунные и стальные
4) Металлы и сплавы обладают свойствами:
а) физическими и механическими; б) технологическими и геометрическими; в) механическими и технологическими; г) техническими и физическими.
5) Способность металла или сплава изменять свою форму под действием нагрузок не разрушаясь – это:
а) прочность; б) упругость; в) пластичность; г) твердость
II. Прочитайте следующие высказывания. Если вы согласны с утверждением, поставьте знак «+», если – нет, знак «-».
1) Сталь – это сплав железа с углеродом, в котором углерода содержится менее 2 %.
2) Свойство металла сопротивляться внедрению в него другого, менее твердого материала, называется твердостью.
3) Чугун обладает хрупкостью, поэтому из него изготавливают радиаторы отопления.
4) Высокая коррозионная стойкость латуни используется для производства деталей, работающих в условиях повышенной влажности.
5) Сталь для изготовления пружин должна обладать упругостью.
III. Закончите предложение:
1) Сплавы получают путем смешивания…( двух и более металлов в определенном соотношении). 2) Латунь – это сплав…(меди с цинком).
3) Свойство металлов соединяться в пластичном или расплавленном состоянии называется…(свариваемость). 4) Из меди делают электрические провода, потому что она…(хорошо проводит электрический ток). 5) В авиации требуются легкие и прочные конструкции, поэтому их изготавливают из сплава…(дюралюминия).
4) Из меди делают электрические провода, потому что она…(хорошо проводит электрический ток). 5) В авиации требуются легкие и прочные конструкции, поэтому их изготавливают из сплава…(дюралюминия).
2 вариант
I. Выберите правильный ответ:
1) К цветным металлам и сплавам относятся:
а) медь, бронза, дюралюминий; б) алюминий, железо, чугун; в) сталь, латунь, бронза; г) железо, сталь, чугун.
2) Легкий металл серебристо-белого цвета, самый распространенный на Земле – это:
а) железо; б) алюминий; в) медь; г) дюралюминий
3) Изделия из чугуна нельзя подвергать ударам, потому что чугун:
а) мягкий; б) упругий; в) пластичный; г) хрупкий
4) К технологическим свойствам металлов и сплавов относятся:
а) прочность и твердость; б) упругость и пластичность; в) ковкость и свариваемость; г) прочность и жидкотекучесть.
5) Способность металла или сплава воспринимать действующие нагрузки не разрушаясь – это:
а) прочность; б) упругость; в) пластичность; г) твердость
II. Прочитайте следующие высказывания. Если вы согласны с утверждением, поставьте знак «+», если – нет, знак «-».
Прочитайте следующие высказывания. Если вы согласны с утверждением, поставьте знак «+», если – нет, знак «-».
1) Чугун – это сплав железа с углеродом, в котором углерода содержится менее 2 %.
2) Свойство металла сопротивляться внедрению в него другого, более твердого материала, называется твердостью.
3) Бронза обладает жидкотекучестью, поэтому из нее отливают скульптуры.
4) Из конструкционной стали делают режущие инструменты для обработки металлов.
5) Железо – коррозионно не стойкий металл, во влажной среде оно быстро ржавеет.
III. Закончите предложение:
1) К черным сплавам относят…(сталь и чугун). 2) Свойство металла или сплава получать новую форму под действием удара – это …(ковкость).
3) К механическим свойствам относят:..(прочность, твердость, упругость, пластичность) 4) Из высокотвердой инструментальной стали изготавливают…(режущие инструменты для обработки металлов). 5) Чугун более хрупкий, чем сталь, так как в его составе углерода содержится … (более 2%; от2-6,7% или больше, чем в стали)
Ответы и критерии оценивания представлены в таблице 6.
Ответы и критерии оценивания
1 вариант
2 вариант
№ задания
ответ
№ задания
ответ
I.
I.
1
б
1
а
2
г
2
б
3
а
3
г
4
в
4
в
5
в
5
а
II.
II.
1
+
1
–
2
–
2
+
3
–
3
+
4
+
4
–
5
+
5
+
III.
III.
1
двух и более металлов в определенном соотношении)
1
сталь и чугун
2
меди с цинком
2
ковкость
3
свариваемость
3
прочность, твердость, упругость, пластичность
4
хорошо проводит электрический ток
4
режущие инструменты для обработки металлов
5
дюралюминий
5
более 2%; от2-6,7% или больше, чем в стали
Критерии оценивания
За каждый правильный ответ – 1 балл
5 (отлично) – 14-15 баллов
4 (хорошо) – 11-13 баллов
3 (удовлетворительно) – 8-10 баллов
2 (неудовлетворительно) – 7 и менее баллов
Тестовая работа рассчитана на 15-20 минут урочного времени, пределы зависят от способностей учащихся класса.
Просмотр содержимого документа
«Контрольно-измерительные материалы по теме “Свойства металлов и сплавов” к разделу “Технология обработки металлов” 6 класс »
Контрольно-измерительные материалы
по теме «Свойства металлов и сплавов»
к разделу «Технология обработки металла»
предмета «Технология. Технический труд»
6 класс (мальчики)
Автор: Кабанов Д.Е.
1 вариант
I. Выберите правильный ответ:
1) Все металлы и сплавы делятся на:
а) белые и черные; б) черные и цветные; в) цветные и благородные;
г) белые и цветные.
2) К черным металлам и сплавам относятся:
а) алюминий, сталь, углерод; б) железо, бронза, латунь, в) медь, алюминий, чугун; г) железо, сталь, чугун.
3) В зависимости от свойств стали делятся на:
а) конструкционные и инструментальные; б) механические и технологические; в) черные и цветные; г) чугунные и стальные
4) Металлы и сплавы обладают свойствами:
а) физическими и механическими; б) технологическими и геометрическими; в) механическими и технологическими; г) техническими и физическими.
5) Способность металла или сплава изменять свою форму под действием нагрузок не разрушаясь – это:
а) прочность; б) упругость; в) пластичность; г) твердость
II. Прочитайте следующие высказывания. Если вы согласны с утверждением, поставьте знак «+», если – нет, знак «-».
1) Сталь – это сплав железа с углеродом, в котором углерода содержится менее 2 %.
2) Свойство металла сопротивляться внедрению в него другого, менее твердого материала, называется твердостью.
3) Чугун обладает хрупкостью, поэтому из него изготавливают радиаторы отопления.
4) Высокая коррозионная стойкость латуни используется для производства деталей, работающих в условиях повышенной влажности.
5) Сталь для изготовления пружин должна обладать упругостью.
III. Закончите предложение:
1) Сплавы получают путем смешивания…(двух и более металлов в определенном соотношении). 2) Латунь – это сплав…(меди с цинком).
3) Свойство металлов соединяться в пластичном или расплавленном состоянии называется…(свариваемость). 4) Из меди делают электрические провода, потому что она…(хорошо проводит электрический ток). 5) В авиации требуются легкие и прочные конструкции, поэтому их изготавливают из сплава…(дюралюминия).
2 вариант
I. Выберите правильный ответ:
1) К цветным металлам и сплавам относятся:
а) медь, бронза, дюралюминий; б) алюминий, железо, чугун; в) сталь, латунь, бронза; г) железо, сталь, чугун.
2) Легкий металл серебристо-белого цвета, самый распространенный на Земле – это:
а) железо; б) алюминий; в) медь; г) дюралюминий
3) Изделия из чугуна нельзя подвергать ударам, потому что чугун:
а) мягкий; б) упругий; в) пластичный; г) хрупкий
4) К технологическим свойствам металлов и сплавов относятся:
а) прочность и твердость; б) упругость и пластичность; в) ковкость и свариваемость; г) прочность и жидкотекучесть.
5) Способность металла или сплава воспринимать действующие нагрузки не разрушаясь – это:
а) прочность; б) упругость; в) пластичность; г) твердость
II. Прочитайте следующие высказывания. Если вы согласны с утверждением, поставьте знак «+», если – нет, знак «-».
1) Чугун – это сплав железа с углеродом, в котором углерода содержится менее 2 %.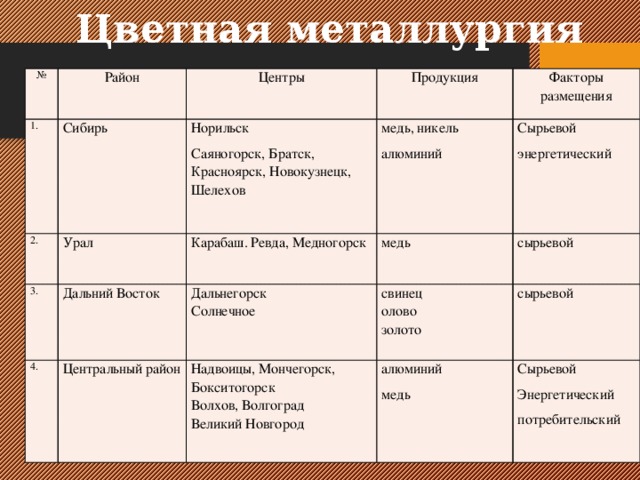
2) Свойство металла сопротивляться внедрению в него другого, более твердого материала, называется твердостью.
3) Бронза обладает жидкотекучестью, поэтому из нее отливают скульптуры.
4) Из конструкционной стали делают режущие инструменты для обработки металлов.
5) Железо – коррозионно не стойкий металл, во влажной среде оно быстро ржавеет.
III. Закончите предложение:
1) К черным сплавам относят…(сталь и чугун). 2) Свойство металла или сплава получать новую форму под действием удара – это …(ковкость).
3) К механическим свойствам относят:..(прочность, твердость, упругость, пластичность) 4) Из высокотвердой инструментальной стали изготавливают…(режущие инструменты для обработки металлов). 5) Чугун более хрупкий, чем сталь, так как в его составе углерода содержится … (более 2%; от2-6,7% или больше, чем в стали)
Ответы и критерии оценивания представлены в таблице 6.
Ответы и критерии оценивания
1 вариант | 2 вариант | ||
№ задания | ответ | № задания | ответ |
I. | I. | ||
1 | б | 1 | а |
2 | г | 2 | б |
3 | а | 3 | г |
4 | в | 4 | в |
5 | в | 5 | а |
II. | II. | ||
1 | + | 1 | – |
2 | – | 2 | + |
3 | – | 3 | + |
4 | + | 4 | – |
5 | + | 5 | + |
III. | III. | ||
1 | двух и более металлов в определенном соотношении) | 1 | сталь и чугун |
2 | меди с цинком | 2 | ковкость |
3 | свариваемость | 3 | прочность, твердость, упругость, пластичность |
4 | хорошо проводит электрический ток | 4 | режущие инструменты для обработки металлов |
5 | дюралюминий | 5 | более 2%; от2-6,7% или больше, чем в стали |
Критерии оценивания | За каждый правильный ответ – 1 балл 5 (отлично) – 14-15 баллов 4 (хорошо) – 11-13 баллов 3 (удовлетворительно) – 8-10 баллов 2 (неудовлетворительно) – 7 и менее баллов | ||
Тестовая работа рассчитана на 15-20 минут урочного времени, пределы зависят от способностей учащихся класса.
Проект “Металлы в жизни человека”
Руководитель:
Кудинова Татьяна Михайловна
Учреждение:
ГБОУ «Трубчевский политехнический техникум»
Детская исследовательская работа по химии “Металлы в жизни человека” рассматривает историю открытия и изучения металлов, а также их положения в периодической таблице Менделеева и использование в быту.
Подробнее о проекте:
В процессе работы над исследовательским проектом по химии об исследовании свойств и особенностей металлов учащийся техникума рассмотрел историю использования алюминия в быту, его положение в периодической системе и особенности строения атома алюминия. В работе перечислены свойства алюминия, рассмотрены основные области применения алюминия и его влияние на организм человека.
Учащийся 1 курса техникума в рамках своего проекта по химии на тему “Металлы в жизни человека” дал определение такого металла, как железо, и рассмотрел историю его использования в быту. В работе можно узнать о положении железа в периодической системе Менделеева и строение атома железа, а также основные области его применения и соединения. В своем проекте ученик рассказал о влиянии железа на организм человека и провел практическую работу по теме исследования.
В работе можно узнать о положении железа в периодической системе Менделеева и строение атома железа, а также основные области его применения и соединения. В своем проекте ученик рассказал о влиянии железа на организм человека и провел практическую работу по теме исследования.
Оглавление
Введение
1. Алюминий.
1.1 История использования алюминия в быту.
1.2 Положение в периодической системе Менделеева и строение атома алюминия.
1.3 Свойства алюминия.
1.4 Основные области применения алюминия.
1.5 Влияние алюминия на организм человека.
2. Железо.
2.1 История использования железа в быту.
2.2 Положение в периодической системе Менделеева. Строение атома железа.
2.3. Основные области применения железа.
2.4.Соединения.
2.5 Влияние железа на организм человека.
5. Практическая часть: алюминий.
6. Практическая часть железо.
Заключение
Список использованной литературы
Приложение
Введение
В настоящее время нельзя представить жизнь человека без металлов. Они играют большую роль. Из металлов изготавливаются посуда, транспорт, украшения, стройматериалы и т.д. Изучая химию, я узнал о свойствах металлов, о которых раньше не подозревал.
Они играют большую роль. Из металлов изготавливаются посуда, транспорт, украшения, стройматериалы и т.д. Изучая химию, я узнал о свойствах металлов, о которых раньше не подозревал.
Мне стало интересно, какие металлы более распространены в быту. Для того, чтобы это узнать, я провёл социологический опрос.
По результатам социологического опроса, мной было выявлено, что наиболее распространёнными металлами являются алюминий и железо. Я решил узнать подробнее об этих металлах:
Алюминий – это достаточно дешевый, легкий и долговечный материал. Он хороший проводник тепла, следовательно, вода и пища в такой посуде нагреваются быстро.
Еще совсем недавно алюминиевая посуда была очень распространена. Но сейчас его популярность сходит на нет, так как в течение многих лет о нем ходят разные слухи. Некоторые люди считают, что алюминий токсичен, другие говорили о связи между алюминиевой посудой и болезнью Альцгеймера. Действительно ли использование алюминиевой посуды опасно для Вашего здоровья?
Об этом сейчас часто спорят. Мы сами дома часто пользуемся алюминиевой посудой и не видим в ней какой – либо опасности. Существуют также другие источники попадания ионов алюминия в организм человека, которые на данный момент изучены гораздо меньше. Считается, что алюминий может попасть в организм человека также через воздух (вдыхание паров), косметические и парфюмерные средства (помада, дезодоранты), лекарственные препараты.
Мы сами дома часто пользуемся алюминиевой посудой и не видим в ней какой – либо опасности. Существуют также другие источники попадания ионов алюминия в организм человека, которые на данный момент изучены гораздо меньше. Считается, что алюминий может попасть в организм человека также через воздух (вдыхание паров), косметические и парфюмерные средства (помада, дезодоранты), лекарственные препараты.
Железо – один из самых распространенных металлов в земной коре. Люди научились извлекать железо из руды и обрабатывать его около 4 тыс. лет назад.
Содержание железа в земной коре составляет 4,65%, а в целом наша планета состоит из железа почти на 35%. В основном оно сосредоточено в земном ядре. Однако железа много не только в земной коре. Этот металл является основным составляющим нашей жизни.
Железо, а точнее его сплавы, в основном используется в строительстве. Из него изготавливают как сложные детали для сборки машин, так и обычные гвозди, которые доступны для всех слоев населения.
Ионы железа являются составляющей частью гемоглобина, который занимается переносом кислорода, необходимого для протекания окислительно-восстановительных процессов в организме. Железо придаёт гемоглобину красный цвет, поэтому кровь животных и человека так же красного цвета. Данный элемент попадает в организм с продуктами питания – печенью, яблоками, творогами, сливами, дынями, хурмой, тыквой, помидорами и абрикосами.
В тоже время мы редко задаёмся вопросом как влияют эти металлы на организм человека ,на повседневную жизнь человека.
Данное исследование актуально, ведь мы встречаемся с этими металлами каждодневно, может быть зная их свойства мы откажемся от их применения или будем применять их с осторожностью?
Предмет исследования: алюминиевая посуда, яблоки.
Проблема исследования: влияние металлов на организм человека и на повседневную жизнь человека.
Гипотеза исследования: металлы могут влиять на организм и на жизнь по- разному.
Цель: исследовать как металлы алюминий и железо влияют на организм человека и на повседневную жизнь человека.
Задачи:
- провести социологический опрос одногруппников
- провести теоретический анализ источников информации по исследуемой проблематике.
- выяснить влияние алюминия на организм человека и пути попадания ионов алюминия в организм человека. Провести лабораторные исследования по данному вопросу.
- выяснить влияние железа на организм человека. Исследовать продукты питания на предмет содержания железа.
- провести сопоставительный анализ практических результатов исследования.
- выработать рекомендации по данным вопросам.
История использования алюминия в быту
В то время как немцы готовили на эмалированной посуде, а британцы использовали эту посуду для дезинфекции домов и больниц. Наполеон Бонапарт во Франции потребовал служащим разносить еду в алюминиевых тарелках, которые стоили дороже, чем золотые. Добытый металл продавался за шестьсот долларов за фунт, и в 1820-х годах Европейское дворянство готово было заменить некоторые золотые и серебряные столовые приборы на алюминиевые.
Однако алюминий быстро терял свой блеск. Добыча металла позволила сбить цену до $ 2,25 фунта в 1890 году. Несмотря на низкую цену, домохозяйки еще не знали о преимуществах приготовления пищи в алюминиевой посуде.
23 февраля 1886 года 22-летний изобретатель Чарльз Мартин Холл, экспериментировал с алюминием в лаборатории в Оберлин, штат Огайо. Записи блокнота Холла говорят, что он усовершенствовал процедуру недорогого производства алюминиевого соединения, которое могло быть использовано в посуде.
Изготовления Холла встретили грозное сопротивление. Домохозяйки не хотели отказываться от своих проверенных жестяных изделий. Крупные универмаги страны отказывались снабжаться новым продуктом, преимущества, которого звучали чересчур фантастическими, чтобы казаться правдой. Поворотный момент наступил весной 1903 года.
Один известный магазин в Филадельфии представил публичную демонстрацию по приготовлению еды в алюминиевой посуде. Сотни женщин с удивлением наблюдали, как профессиональный шеф-повар готовил яблочное повидло. Как только зрителям разрешили сделать шаг вперед и удостовериться в том, что ингредиенты не прилипли к кастрюле, заказы на алюминиевой посуду сразу посыпались.
Как только зрителям разрешили сделать шаг вперед и удостовериться в том, что ингредиенты не прилипли к кастрюле, заказы на алюминиевой посуду сразу посыпались.
К моменту смерти Холла в 1914 году его состоянии оценивалось на сумму 30 млн.долларов, он породил новую кухонную алюминиевую посуду, которая преобразовала американскую кухню.
Положение в периодической системе Менделеева и строение атома алюминия
Название: Алюминий (aluminium)
Порядковый номер: 13
Группа: III
Период: 3
Атомная масса: 26,98154
Электроотрицательность: 1,61
Характерные степени окисления: +3
Атом алюминия состоит из положительно заряженного ядра (+13), внутри которого находится 13 протонов и 14 нейтронов. Ядро окружено тремя оболочками, по которым движутся 13 электронов.
Распределение электронов по орбиталям выглядит следующим образом: 1s22s22p63s23p1.
Свойства алюминия
Физические свойства:
- металл серебристо-белого цвета, лёгкий;
- плотность — 2712 кг/м³;
- температура плавления у технического алюминия — 658 °C, у алюминия высокой чистоты — 660 °C;
- температура кипения — 2518,8 °C;
- высокая пластичность: у технического — 35 %, у чистого — 50 %, прокатывается в тонкий лист и даже фольгу;
- алюминий обладает высокой электропроводностью (37·106 См/м — 65 % от электропроводности меди) и теплопроводностью (203,5 Вт/(м·К)), обладает высокой светоотражательной способностью.
- Алюминий образует сплавы почти со всеми металлами. Наиболее известны сплавы с медью и магнием (дюралюминий) и кремнием (силумин).
Основные области применения алюминия
Данный конструкционный металл имеет широкое распространение. В частности именно с его использования начали свою работу авиастроение, ракетостроение, пищевая промышленность и изготовление посуды. Благодаря своим особенностям алюминий позволяет улучшить маневренность судов за счет меньшей массы.
Благодаря своим особенностям алюминий позволяет улучшить маневренность судов за счет меньшей массы.
Отдельно стоит упомянуть способность металла проводить ток. Такая особенность позволила сделать его главным конкурентом меди. Он активно применяется при производстве микросхем и в целом в области микроэлектроники.
Наиболее популярными сферами использования можно назвать:
- Авиастроение: насосы, двигатели, корпуса и прочие элементы;
- Ракетостроение: как горючий компонент для ракетного топлива;
- Судостроение: корпуса и палубные надстройки;
- Электроника: провода, кабели, выпрямители;
- Оборонное производство: автоматы, танки, самолеты, различные установки;
- Строительство: лестницы, рамы, отделка;
- Область ЖД: цистерны для нефтепродуктов, детали, рамы для вагонов;
- Автомобилестроение: бампера, радиаторы;
- Быт: фольга, посуда, зеркала, мелкие приборы.
Широкое распространение объясняется преимуществами металла, однако есть у него и существенный недостаток – это невысокая прочность. Чтобы минимизировать его, в металл добавляется медь и магний.
Чтобы минимизировать его, в металл добавляется медь и магний.
Влияние алюминия на организм человека
Алюминий в медицине
Несмотря на то, что в больших количествах алюминий вреден для здоровья человека, он находит широкое применение в лечении ряда заболеваний.
На основе алюминия изготавливаются препараты, которые обладают обволакивающим, обезболивающим, адсорбирующим и антацидным действием. Антацидные свойства алюминия используются для снижения кислотности желудочного сока, поскольку он очень активно связывается с соляной кислотой. Показанием в данном случае может быть, например, гастрит с повышенной кислотностью (гиперацидный гастрит). Препараты алюминия находят как внутреннее, так и наружное применение.
Роль алюминия в организме человека.
Алюминий играет очень важную роль – он принимает участие в процессе регенерации (восстановления) эпителиальной и соединительной тканей, поддержания крепости костей, в образовании пептидов и фосфатных комплексов. Алюминий влияет на функцию околощитовидных желез, оказывает как активизирующее, так и тормозящее действие на пищеварительные ферменты. Человек употребляет алюминий с такими продуктами, как: овсяные хлопья, зерна ржи, зерна пшеницы, мука, горох,
Алюминий влияет на функцию околощитовидных желез, оказывает как активизирующее, так и тормозящее действие на пищеварительные ферменты. Человек употребляет алюминий с такими продуктами, как: овсяные хлопья, зерна ржи, зерна пшеницы, мука, горох,
рисовая крупа, картофель, киви, капуста, морковь, яблоки.
Недостаток алюминия в организме человека
Дефицит микроэлемента в организме – это настолько редкое явление, что вероятность его развития сводится к нулю.
С каждым годом количество алюминия в рационе человека стремительно возрастает.
Соединение поступает с продуктами питания, водой, пищевыми добавками (сульфатами), медикаментами, иногда – с воздухом. В медицинской практике за всю историю зафиксировано несколько единичных случаев недостаточности вещества в организме человека. Таким образом, актуальной проблемой XXІ века выступает скорее перенасыщение ежедневного меню элементом, чем развитием его недостаточности.
Несмотря на это, рассмотрим к каким последствиям приводит дефицит алюминия в организме.
- Общая слабость, потеря сил в конечностях.
- Замедление роста, развития детей и подростков.
- Нарушение координации движений.
- Разрушение клеток, тканей и потеря их функциональности.
Данные отклонения возникают, если человек регулярно не получает суточную норму алюминия (30-50 микрограмм). Чем скуднее рацион и меньше потребление соединения, тем интенсивнее проявляются симптомы и последствия нехватки.
Избыток алюминия опасен для здоровья
Излишек микроэлемента токсичен.
Повышенное содержание алюминия опасно для здоровья человека, поскольку снижается иммунитет, а порой возникают необратимые изменения в организме, которые резко сокращают продолжительность жизни.
Характерные признаки излишка микроэлемента: снижение гемоглобина, уменьшение числа эритроцитов в крови, кашель, потеря аппетита, запоры , нервозность, психические расстройства, нарушения речи, ориентации в пространстве, помутнение рассудка. провалы памяти, конвульсии.
Помните, алюминий относится к категории иммунотоксичных микроэлементов, поэтому для сохранения здоровья нужно ежедневно следить за количеством поступающего соединения в организм.
Если алюминий считается имунотоксичным элементом для организма человека, мы решили выяснить пути попадания алюминия в организм человека.
История использования железа в быту
Железо — металл, применение которого в промышленности и быту практически не имеет границ. Доля железа в мировом производстве металлов составляет около 95 %. Применение его, как и любого другого материала, обусловлено определенными свойствами.
Железо сыграло огромную роль в развитии человеческой цивилизации. Первобытный человек начал использовать железные орудия за несколько тысячелетий до нашей эры.
Железо не утратило своего значения и поныне. Это важнейший металл современной техники. Из-за низкой прочности железо практически не используют в чистом виде.
На основе железа создают материалы, способные выдерживать действие высоких и низких температур, вакуума и высоких давлений.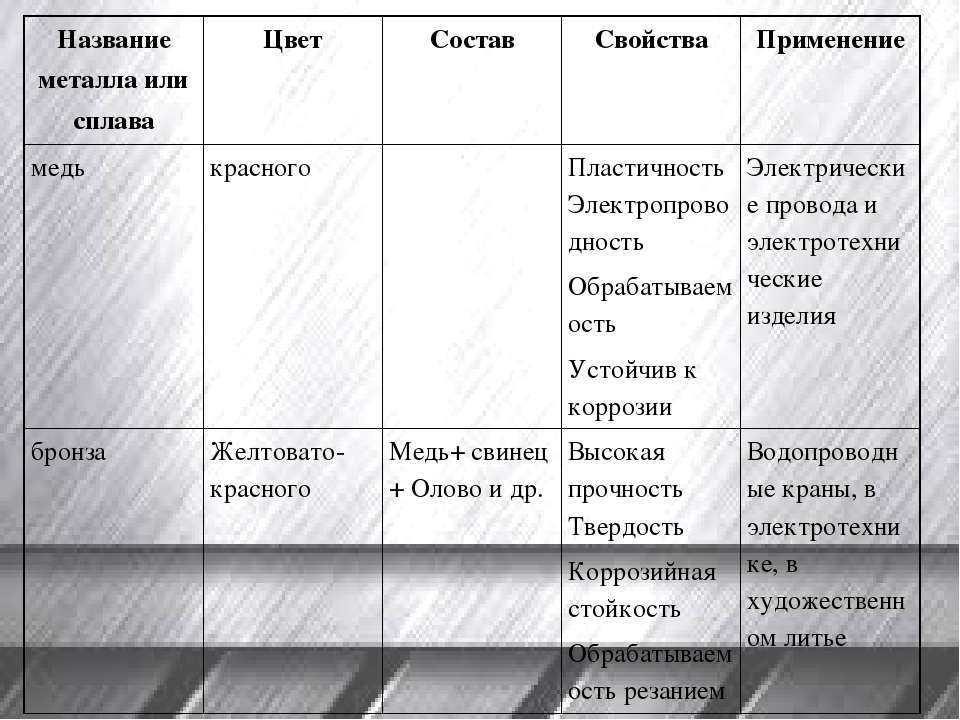 Они успешно противостоят агрессивным средам, переменному напряжению и т. п.
Они успешно противостоят агрессивным средам, переменному напряжению и т. п.
Производство железа и его сплавов постоянно растет. Эти материалы универсальны, технологичны, доступны и в массе — дешевы.
Самыми распространенными сплавами железа являются сталь и чугун.
Нержавеющая сталь – очень популярный материал для предметов домашнего обихода, его использование охватывает все: от котлов до телевизоров. Это очень популярный материал для микроволновых печей, из которого обычно производят двери и внутреннюю панель, а затем покрывают светлой акриловой эмалью, чтобы обеспечить лучшую видимость. В последние годы стало довольно популярным использование кухонной техники из нержавеющей стали, в отличие от простого белого цвета. Речь идет о холодильниках, морозильниках, посудомоечных машинах, духовках, плитах, а также чайниках и тостерах.
Чугун – прочный, но непластичный металл. Из него изготавливают предметы сантехническое оборудование (ванны, трубы, раковины, кухонные мойки), посуду, лестницы, заборы, предметы домашнего интерьера.
Положение в периодической системе Менделеева. Строение атома железа
Название: Железо (ferrum) Порядковый номер: 26 Группа: VIII Период: 4
Атомная масса: 55,847 Электроотрицательность: 1,83 Характерные степени окисления: +2 ,+3
Атом железа состоит из положительно заряженного ядра (+26), внутри которого есть 26 протонов и 30 нейтронов, а вокруг, по четырем орбитам движутся 26 электронов.
Распределение электронов по орбиталям выглядит следующим образом: 1s22s22p63s23p63d64s2.
Основные области применения железа
Под железом зачастую подразумевают вовсе не вещество как таковое, а низкоуглеродистую электротехническую сталь – так называется сплав металла по ГОСТ. Действительно чистое железо получить непросто, и используется оно исключительно для производства магнитных материалов.
Железо является ферромагнетиком, то есть, намагничивается в присутствии магнитного поля. Однако это его свойство сильно зависит от примесей и структуры металла. Магнитные свойства абсолютного чистого железа в 100–200 раз превышают аналогичные показатели технической стали. То же самое можно сказать о величине зерна: чем крупнее зерно, тем лучше магнитные свойства вещества. Имеет значение и механическая обработка, хотя ее влияние и не столь впечатляющее. Только такое железо применяют для получения всех магнитных материалов для электротехники и магнитоприводов.
Соединения
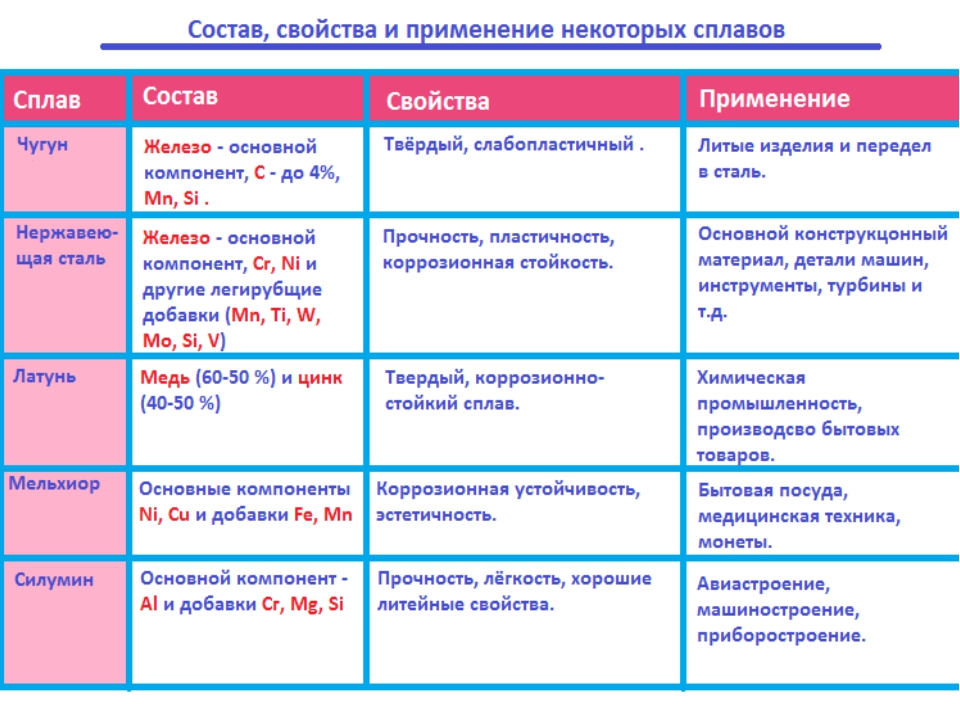
Все металлы, используемые в производстве, делят на цветные и черные. Черные – это сплавы железа, в частности, сталь и чугун, остальные – медные, никелевые, серебряные – относятся к цветным. На долю черной металлургии приходится 95% всех металлургических процессов. Разделяются черные сплавы таким образом:
Сталь – сплав железа с углеродом и другими ингредиентами, чья массовая доля не превышает 2,14%. Углерод придает стали пластичность и твердость. В состав могут входить также марганец, фосфор, сера и так далее; нержавеющая сталь используется в строительстве и машиностроении, где требуется более высокая, чем обычно стойкость к коррозии; жаропрочные сплавы «работают» в условиях высоких температур – турбины, магистрали отопления. Жаростойкие – не окисляются при высоких температурах, что важно для многих рабочих узлов в теплотехнике.
Углерод придает стали пластичность и твердость. В состав могут входить также марганец, фосфор, сера и так далее; нержавеющая сталь используется в строительстве и машиностроении, где требуется более высокая, чем обычно стойкость к коррозии; жаропрочные сплавы «работают» в условиях высоких температур – турбины, магистрали отопления. Жаростойкие – не окисляются при высоких температурах, что важно для многих рабочих узлов в теплотехнике.
Чугун – сплав с углеродом, где допускается большее содержание элемента – до 4,3%. Причем чугуны отличаются по своим свойствам в зависимости от того, в каком виде сплав содержит углерод: если вещество вступило в реакцию с железом, получают белый чугун, если включено в виде графита – серый; износостойкий чугун применяется для изготовления насосных деталей, тормозов, дисков сцепления; жаростойкий применяется при сооружении доменных, мартеновских, термических печей; жаропрочный используется при сооружении газовых печей, при изготовлении компрессорного оборудования, дизельных двигателей.
Злейший враг железа и его сплавов это коррозия. Автомобиль давно перестал быть роскошью , а стал средством передвижения для большинства граждан. Сейчас огромное количество автомобилей разных производителей, разных марок, но все они изготовлены из сплавов на основе железа. Мы решили выяснить автомобили каких производителей меньше подвержены коррозии и тем самым меньше доставляют хлопот своим хозяевам.
Влияние железа на организм человека
Роль железа в организме
У железа очень много функций. Вот основные из них:
Транспортировка кислорода к тканям. Железо входит в состав гемоглобина – белка, из которого состоят красные кровяные тельца (эритроциты). Именно железо отвечает за захват кислорода, после чего эритроциты переносят его ко всем органам и системам организма.
Метаболизм. Железо в организме человека является составной частью многих ферментов и белков, которые необходимы для обменных процессов – разрушения и утилизации токсинов, холестеринового обмена, превращения калорий в энергию. Оно также помогает иммунной системе организма справляться с агрессорами.
Оно также помогает иммунной системе организма справляться с агрессорами.
Человек употребляет железо с такими продуктами, как: печень, креветки, яйца, гречневая крупа, яблоки, орехи, сыр, говядина, утка, пшеница.
Недостаток железа
Нет ничего удивительного в том, что недостаток железа отражается на внешности, здоровье и самочувствии.
При дефиците этого элемента кожа становится бледной и сухой, волосы — тусклыми и слабыми, а ногти — ломкими. В уголках губ возникают незаживающие язвочки, а на кистях рук и ступнях — очень болезненные трещины. По мере снижения количества железа в организме самочувствие ухудшается — пропадает аппетит, многие замечают дискомфорт при глотании. Иногда вкусы меняются самым странным образом, например, человеку очень хочется погрызть мел или пожевать бумагу.
Люди с нехваткой железа испытывают постоянный упадок сил — они даже просыпаются уставшими. Малейшие физические нагрузки вызывают сильную одышку — так сказывается недостаток кислорода. Другие типичные симптомы дефицита железа — головокружения и даже обмороки, сонливость, раздражительность, ухудшение памяти.
Другие типичные симптомы дефицита железа — головокружения и даже обмороки, сонливость, раздражительность, ухудшение памяти.
Для людей, страдающих нехваткой железа, типичны постоянные простуды и кишечные инфекции. Как мы уже говорили, железо принимает непосредственное участие в работе защитной системы организма, и при его дефиците иммунитет не может вовремя отражать атаки болезнетворных бактерий.
Наверняка многим эти симптомы покажутся очень знакомыми. Ничего удивительного: по статистике ВОЗ, примерно у 60% населения планеты отмечается недостаток железа в организме, а у 30% дефицит этого элемента так велик, что речь идет уже о железодефицитной анемии — состоянии, при котором значительно понижается уровень гемоглобина.
Практическая часть: алюминий
Пути попадания алюминия в организм человека:
алюминиевая посуда и препараты, содержащие ионы алюминия
Исследование наличия ионов алюминия в еде, приготовленной в алюминиевой посуде
Цель: Мы часто используем алюминиевую посуду, поэтому мы решили исследовать безопасность алюминевой посуды.
Опыт №1
Алюминий реагирует с водой, при этом выделяется водород и образуется нерастворимый гидроксид алюминия. 2Al + 6h3O = 2 Al(OH)3 ↓ + 3h3↑
В течении 15 минут кипятил воду в алюминиевой кастрюле, затем остудила раствор и проверила его прозрачность.
Наблюдения: Никаких изменений в пробе воды, которая кипятилась в алюминиевой посуде, не наблюдала. Проделывая этот опыт, я убедилась, что оксидная пленка на металле защищает его от взаимодействия с водой, так оксид алюминия в воде не растворяется и не реагирует с ней.
Опыт №2
Алюминий взаимодействует со щелочью, при этом образуется соль и выделяется водород.
2Al + 2NaOH + 6h3O = 2Na[Al(OH)4] + 3h3
Средство для мытья духовок и плит содержит в своём составе каустическую соду, то есть гидроксид натрия. При нанесения этого средства на алюминиевый предмет, достаточно быстро я увидел признаки реакции в виде выделяющегося газа.
Вывод: Если алюминий реагирует со щелочами, и в щелочной среде он переходит в раствор в виде солей, то приготовление и хранение пищи со щелочной реакцией среды приведет к тому, что он в виде иона он так же поступит в пищу.
Практическая часть: железо
Опыт «Исследование содержания железа в яблоках».
Сначала провожу опыт на красном яблоке. Разрезал красное яблоко пополам, рассмотрел поперечный срез красного яблока.
Через некоторое время одна из половинок яблока, не смазанная лимонным соком потемнела, а та, что была «защищена» лимонным соком, осталась белой.
Разрезал лимон. Одну половинку яблока смазал лимонным соком, а вторую половинку красного яблока положил на тарелку срезом вверх. То же самое, в той же последовательности проделал с зелёным яблоком. Положил обе половинки зелёного яблока на тарелку срезом вверх и стал наблюдать за изменениями.
Вывод.
Потемнение происходит из-за окисления железа, которое содержится в яблоках, кислородом воздуха. Кислота, которая содержится в лимонном соке, защищает срез яблока от окисления и замедляет процесс окисления.
Я заметил, что срезы красного яблока почти совсем не потемнели, значит, железа в зелёных яблоках содержится больше и они полезнее.
Заключение
Наша жизнь немыслима без металлов. В нашей творческой работе, посвящённой железу и алюминию, я расширил свои знания об этих элементах, простых веществах металлах их свойствах и применении.
Роль железа и алюминия в развитии и становлении технической культуры человечества исключительно велика. Твёрдость, пластичность, ковкость сделали их незаменимым материалом для изготовления орудий труда и производства. Выглянув на улицу, мы видим сотни автомашин, каждая из которых сделана из железа. Из сплавов железа или алюминия изготавливают тросы, мосты, рельсы, трамваи, поезда, и наконец, самолёты. Везде металлы!… Ну и в нас самих есть эти металлы. Они используются для осуществления различных процессов в организме.
В нашей теоретической части мы охарактеризовали строение и свойства железа и алюминия, применение их в медицине и описали, что бывает при избытке и недостатке ионов этих элементов.
В результате проделанной работы мы сделали выводы:
Ионы железа и алюминия оказывают жизненно важное влияние на организм человека.
Ионы алюминия в большом количестве опасны для здоровья. Поэтому следует в алюминиевой посуде только готовить, а не хранить продукты питания. Не увлекаться употреблением таблеток от изжоги.
Ионы железа благоприятно влияют на организм человека. Поэтому необходимо употреблять продукты питания богатые железом. Такие как, хурма , яблоки, грецкие орехи.
Список использованной литературы
- Горынин И. В. и др. Алюминиевые сплавы. Применение алюминиевых сплавов. Справочное руководство. Москва «Металлургия», 1978 г.
- Хэтч Дж. Е. Алюминий. Свойства и физическое металловедение. Справочник. Москва, «Металлургия», 1989 г.
- Рабинович В. А., Хавин З. Я. Краткий химический справочник.
- Краткая химическая энциклопедия. «Советская энциклопедия», 1963 г.
- Карапетьянц М.Х., Дракин С.И. Общая и неорганическая химия. «Химия», 1981 г.
- Венецкий С. И. Рассказы о металлах
- Беккерт М.. Железо. Факты и легенды.
Приложение.
 Социологический опрос
Социологический опрос- Какие металлы вы знаете?
- С какими металлами встречаетесь в повседневной жизни? Где?
- Как они влияют на организм человека?
Если страница Вам понравилась, поделитесь в социальных сетях:
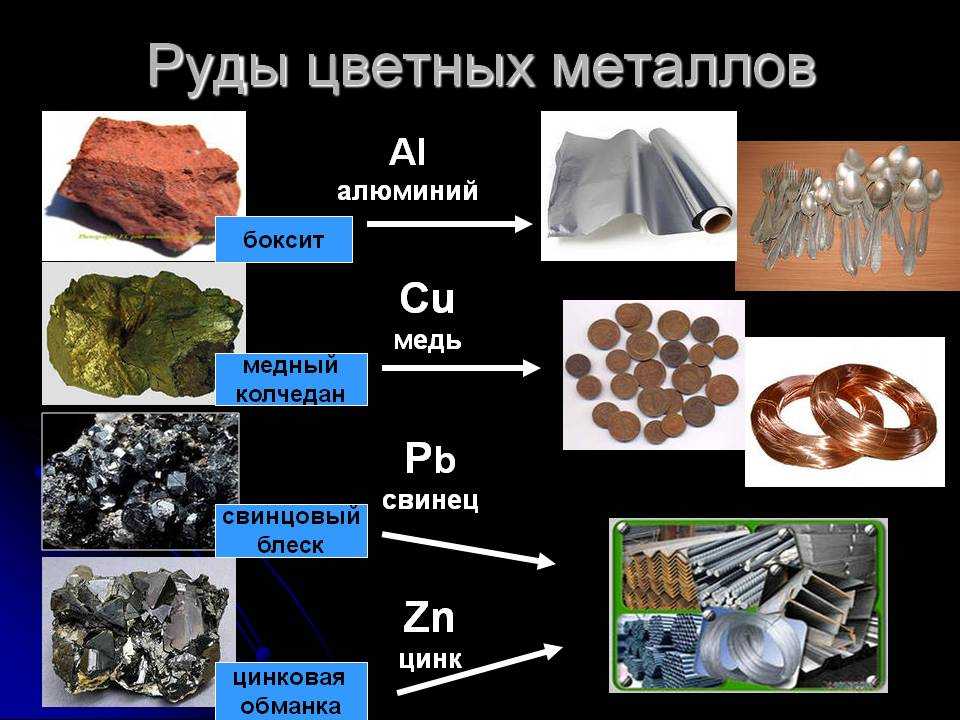
Использование алюминия, меди, цинка и железа
Земная кора богата минералами и рудами. Некоторые руды оказались ценным ресурсом для человечества. Например, железо, полученное из железной руды (гематита), заложило основу промышленной революции. Алюминий, с другой стороны, был важным стратегическим ресурсом для авиации во время Первой и Второй мировых войн. Несмотря на это, металлический алюминий продолжает доминировать на рынке благодаря своим уникальным свойствам, а также быстрой и экономичной добыче. Металлы составляют 70% всех встречающихся в природе элементов. В природе металлы встречаются как в свободном, так и в смешанном виде. Обычно химически активные металлы существуют в смешанных состояниях в виде оксидов, сульфидов, карбонатов и т. д. Металлы в центре ряда реакционной способности, такие как цинк, железо и свинец, умеренно реакционноспособны и встречаются в земной коре в виде оксидов, сульфидов, карбонатов и т. д.
д. Металлы в центре ряда реакционной способности, такие как цинк, железо и свинец, умеренно реакционноспособны и встречаются в земной коре в виде оксидов, сульфидов, карбонатов и т. д.
Алюминий
Алюминий с атомным номером 13 и символом Al является химическим элементом. Алюминий имеет меньшую плотность, чем большинство распространенных металлов, примерно на треть плотности стали. При контакте с воздухом создает на поверхности защитное покрытие из оксида из-за высокого сродства к кислороду. Алюминий имитирует серебро по внешнему виду, как по цвету, так и по способности отражать свет. Он податлив, немагнитен и пластичен.
Свойства алюминия
- Чистый алюминий (99,996%) мягкий и непрочный; технический алюминий (чистота от 99 до 99,6%) со следовыми уровнями кремния и железа является твердым и прочным.
- Алюминий — пластичный и чрезвычайно ковкий металл, из которого можно вытягивать проволоку или сворачивать в тонкую фольгу.
- Металл имеет только одну треть плотности железа или меди.

- Несмотря на свою химическую активность, алюминий обладает высокой коррозионной стойкостью благодаря образованию толстой прочной оксидной пленки на его поверхности на воздухе.
- Алюминий является отличным проводником тепла и электричества.
- Он имеет примерно половину теплопроводности меди и примерно две трети электропроводности.
- Кристаллизуется в гранецентрированной кубической форме.
- Полностью натуральный алюминий содержит стабильный изотоп под названием алюминий-27.
- Металлический алюминий, а также его оксид и гидроксид безвредны.
Использование алюминия
- Алюминий добавляют в умеренных количествах к некоторым металлам для улучшения их свойств для конкретных целей, таких как алюминиевые бронзы и большинство сплавов на основе магния, или значительные количества других металлов и кремния добавляют к алюминию в сплавы на основе алюминия.
- Металл и его сплавы широко используются в производстве самолетов, строительных материалов, товаров длительного пользования (холодильники, кондиционеры, кухонная утварь), электрических проводников, химического и пищевого оборудования.

- Рулоны, банки, фольга и другие упаковочные материалы часто изготавливаются из алюминия в упаковочной промышленности.
- Его также можно найти во многих предметах повседневного обихода, таких как посуда и часы.
- Алюминий используется в строительной промышленности для изготовления дверей, окон, кабелей и кровли.
- Он используется в транспортной отрасли для изготовления велосипедов, космических кораблей, кузовов автомобилей, самолетов и морского оборудования.
- Многие монеты состоят из сплавов, содержащих алюминий.
- Алюминий также используется в производстве красок, отражающих поверхностей и проводов.
Медь
Медь имеет атомный номер 29 и химический символ Cu. Это пластичный, мягкий, ковкий металл с хорошей тепло- и электропроводностью. Цвет свежеобнаженной чистой меди розовато-оранжевый.
Свойства меди
- Медь является одним из самых пластичных металлов, то есть она не очень прочная или твердая.
- Холодная обработка значительно повышает прочность и твердость благодаря получению удлиненных кристаллов с такой же гранецентрированной кубической структурой, как у более мягкой отожженной меди.
- В расплавленной меди кислород, азот, двуокись углерода и двуокись серы растворимы и влияют на механические и электрические свойства затвердевшего металла.
- По тепло- и электропроводности чистый металл уступает только серебру.
- Природная медь состоит из двух стабильных изотопов: меди-63 и меди-65.
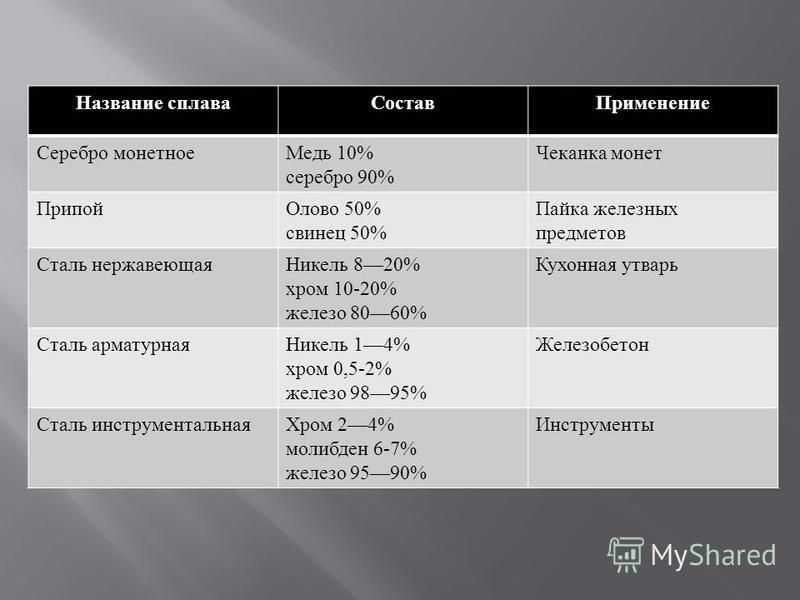
Использование меди
- Медь используется в качестве проводника тепла и электричества, строительного материала и компонента различных металлических сплавов, включая стерлинговое серебро в ювелирных изделиях, мельхиор в морском оборудовании и монетах, константан в тензодатчиках и датчики температуры.
- Большая часть производимой в мире меди используется в электротехнической промышленности, а остальная часть смешивается с другими металлами для образования сплавов.
 (С точки зрения технологии гальваническое покрытие также имеет важное значение.)
(С точки зрения технологии гальваническое покрытие также имеет важное значение.) - Латуни (медь и цинк), бронзы (медь и олово) и нейзильберы представляют собой важные серии сплавов, в которых медь является основным элементом (медь, цинк, и никель, без серебра).
- Существует множество полезных медных и никелевых сплавов, особенно монель; два металла полностью смешиваются.
- Медь также имеет значительную последовательность сплавов с алюминием, известных как алюминиевые бронзы.
- Бериллиевая медь (2% Be) представляет собой уникальный медный сплав, который можно упрочнить путем термической обработки.
- Медь можно найти в различных металлах для чеканки.
Цинк
Цинк — это химический элемент с атомным номером 30 и символом Zn. Цинк является относительно хрупким металлом при нормальной температуре, с серебристо-серым оттенком после удаления окисления. Это первый элемент в группе 12 периодической таблицы (IIB). Цинк в некотором роде химически подобен магнию: оба элемента имеют только одну нормальную степень окисления (+2).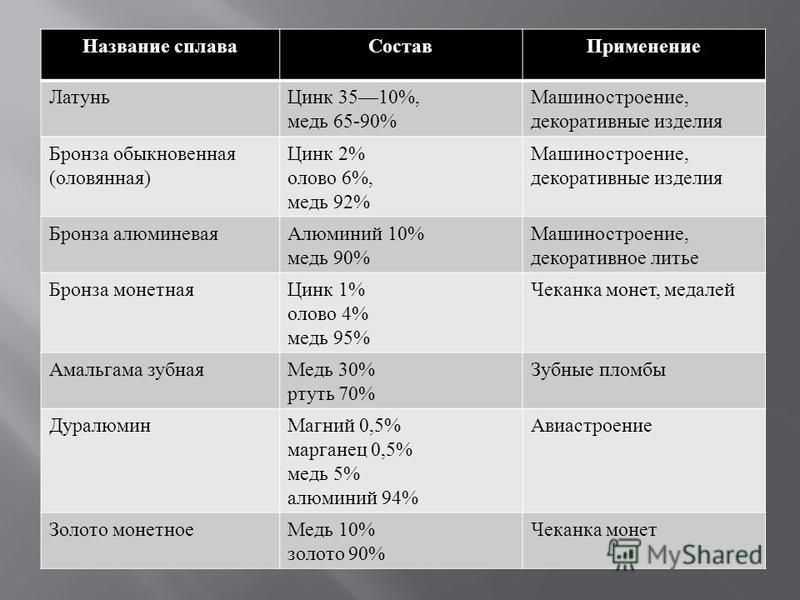 Цинк является двадцать четвертым наиболее распространенным элементом в земной коре с пятью стабильными изотопами.
Цинк является двадцать четвертым наиболее распространенным элементом в земной коре с пятью стабильными изотопами.
Свойства цинка
- Цинк представляет собой голубовато-белый, глянцевый, диамагнитный металл, хотя большинство товарных марок имеют матовую поверхность.
- Он имеет гексагональную кристаллическую структуру с искаженной гексагональной плотной упаковкой, где каждый атом имеет шесть ближайших соседей в своей плоскости (на расстоянии 265,9 пм) и еще шесть на большем расстоянии 290,6 пм.
Использование цинка
- Металлический цинк в основном используется для защиты от коррозии железа и стали, а также в производстве латуни и сплавов для литья под давлением.
- При контакте с воздухом цинк создает непроницаемое покрытие из своего оксида, что делает металл более устойчивым к обычным атмосферным воздействиям, чем железо, и подвержен коррозии с гораздо меньшей скоростью.
- Кроме того, поскольку цинк окисляется быстрее, чем железо, стальная поверхность защищена, даже если часть ее обнажена через трещины.
 Для создания цинкового покрытия используется либо горячее цинкование, либо электроцинкование.
Для создания цинкового покрытия используется либо горячее цинкование, либо электроцинкование. - Поверхность свежеотлитого цинка имеет голубоватый оттенок серебра, который постепенно окисляется на воздухе с образованием сероватого защитного оксидного слоя.
- Так называемый первоклассный западный сорт (чистота 99,8 %) становится хрупким в холодном состоянии, но при температуре 100°C может сворачиваться в гибкие листы. Высокочистый цинк (чистота 99,99%) пластичен.
- Гексагональная плотноупакованная структура цинка кристаллизуется.
- Когда железо и цинк вместе подвергаются воздействию агрессивной жидкости, они образуют электролитическую ячейку, при этом цинк повреждается преимущественно из-за его более высокого электродного потенциала.
- Эта так называемая жертвенная защита, наряду со значительно более высокой коррозионной стойкостью цинка в воздушной среде, служит основой для цинкования.
Железо
Химический символ железа — Fe, атомный номер — 26. Оно принадлежит к первому переходному ряду и группе 8 периодической таблицы. Это самый распространенный элемент на Земле по массе, опережающий кислород (32,1% и 30,1% соответственно), и он составляет большую часть внешнего и внутреннего ядра планеты. Это четвертый по распространенности элемент в земной коре.
Оно принадлежит к первому переходному ряду и группе 8 периодической таблицы. Это самый распространенный элемент на Земле по массе, опережающий кислород (32,1% и 30,1% соответственно), и он составляет большую часть внешнего и внутреннего ядра планеты. Это четвертый по распространенности элемент в земной коре.
Свойства железа
- Во влажном воздухе ржавеет, но не в сухом.
- Легко растворяется в слабых кислотах.
- Этот металл находится в форме феррита или в -форме при комнатной температуре.
- Превращается в гамма-железо при температуре около 910°C, которое по своей природе намного мягче.
- Температура плавления 1536°C и температура кипения 2861°C.
- Поскольку это металл, он обладает магнитными свойствами. Быть металлом магнитно по своей природе.
Использование железа
- Он используется в производстве стали, а также в гражданском строительстве, таком как железобетон, балки и т.д.

- Легированные стали, такие как углеродистые стали, изготавливаются из железа с добавками, такими как никель, хром, ванадий, вольфрам и марганец.
- Из них делают мосты, опоры электропередач, велосипедные цепи, режущие инструменты и стволы винтовок.
- Углерод присутствует в 3–5% чугуна. Он используется в производстве труб, клапанов и насосов.
- Железные катализаторы используются в процессе Габера для получения аммиака.
- Магниты могут быть изготовлены из этого металла, а также его сплавов и соединений.
Концептуальные проблемы
Вопрос 1: Почему железо имеет высокую температуру плавления?
Решение:
Чтобы расплавить или вскипятить металл, необходимо преодолеть притяжение между ионами металла и смещенными электронами. Поскольку такие силы притяжения являются твердыми, металлы имеют высокие температуры плавления и кипения.
Вопрос 2: Каковы свойства железа?
Решение:
Железо — металл серебристо-серого цвета, блестящий, пластичный и ковкий (группа периодической таблицы VIII).
Известно, что он появляется в четырех уникальных кристаллических формах. Железо ржавеет во влажных условиях, но не в сухом воздухе. Быстро растворяется в разбавленных кислотах.
Вопрос 3: Каковы недостатки цинка?
Решение:
Подобно тому, как дефицит цинка может нанести вред здоровью, избыток цинка может иметь противоположные последствия. Наиболее распространенной причиной отравления цинком, которое может вызывать как острые, так и хронические симптомы, является чрезмерное потребление цинка. Тошнота и рвота являются симптомами интоксикации.
Вопрос 4: Как медь влияет на человека?
Решение:
Отравление медью может вызвать воспаление носа, горла и глаз, а также головные боли, боли в животе, головокружение, рвоту и диарею. Чрезмерное поглощение меди может нанести вред печени и почкам, а также привести к смерти. Канцерогенный потенциал меди еще предстоит определить.
Вопрос 5: Каковы три свойства алюминия?
Решение:
Это связано с его отличительными характеристиками. Он имеет низкую плотность, нетоксичен, обладает хорошей теплопроводностью, устойчив к коррозии, его легко отливать, обрабатывать и формовать. Он также немагнитен и не загорится. Это металл со второй по величине ковкостью и шестой по пластичности.
Использование железа, меди, алюминия, цинка. Введение, сходство, свойства и использование, факты и часто задаваемые вопросы
Использование железа Медь Алюминий Цинк
Железо используется в строительстве, автомобилях, инструментах и приборах. Медь используется в строительстве, электропроводке, монетах и ювелирных изделиях. Алюминий используется в строительстве, автомобилях и самолетах. Цинк используется в строительстве, оцинковывании железа для предотвращения ржавчины и в батареях.
Зарегистрируйтесь, чтобы получить бесплатный пробный тест и учебный материал
Класс
— Класс 6Класс 7Класс 8Класс 9Класс 10Класс 11Класс 12
Вы ученик Шри Чайтаньи?
НетДа
+91
Подтвердить OTP-код (обязательно)
Я согласен с условиями и политикой конфиденциальности.
Использование алюминия
Алюминий — это легкий металл, обладающий прочностью и устойчивостью к коррозии. Его часто используют для изготовления банок, фольги и посуды. Алюминий также используется в строительстве, транспорте и электронике.
В чем сходство железа, меди и алюминия
Эти три элемента имеют много общего. Все они металлы, и все они серебристого цвета. Кроме того, все они являются хорошими проводниками электричества.
Свойства и применение алюминия
Алюминий — универсальный металл с широким спектром свойств и областей применения. Он прочный, но легкий, устойчивый к коррозии и нетоксичный. Эти функции делают его полезным для различных приложений, от строительства до транспорта и производства.
Алюминий часто используется в строительстве, потому что он прочный, но легкий. Его можно использовать для изготовления окон, дверей и других строительных элементов. Алюминий также устойчив к коррозии, что означает, что он не подвергается коррозии в присутствии дождя, снега или других погодных условий. Это качество делает его хорошим выбором для строительных материалов, которые подвергаются воздействию элементов.
Это качество делает его хорошим выбором для строительных материалов, которые подвергаются воздействию элементов.
Алюминий также используется в транспорте. Он часто используется в кузовах легковых автомобилей, грузовиков и других транспортных средств. Алюминий легкий, поэтому он помогает уменьшить вес автомобиля и повысить эффективность использования топлива. Он также устойчив к коррозии, поэтому не подвергается коррозии под дождем или снегом.
Алюминий также используется в производстве. Его часто используют для изготовления банок, фольги и других упаковочных материалов. Алюминий легкий и устойчивый к коррозии, что делает его хорошим выбором для упаковочных материалов, которые должны быть легкими и прочными.
Для чего нужен алюминий?
Алюминий — это легкий, прочный, нетоксичный металл, который используется в различных продуктах, включая самолеты, автомобили и консервные банки.
Медь, алюминий и цинк
Медь представляет собой красноватый металл, который широко используется для изготовления электропроводки и других компонентов.




