Температура плавления тантала: Температура плавления тантала
alexxlab | 06.02.2023 | 0 | Разное
Тантал ТАВ 10 – описание
Тантал ТАВ 10 – описание- Сплавы
- Обновлено 10 октября 2020 г.
Современное производство активно использует тантал ТАВ 10. Его применение оправдало себя в решении разного рода задач, начиная от радиоаппаратуры и заканчивая ядерной энергетикой. И это происходит несмотря на высокую стоимость тантала, которая на июнь 2017 года составляет 530 долларов за килограмм.
Так что же послужило причиной такой популярности танталового сплава ТАВ 10? Какие свойства позволили ему сделать это?
Химический состав и расшифровка
Танталовый сплав ТАВ 10 представляет собой тугоплавкое соединение на основе тантала и вольфрама. Последнего в сплаве содержится около 10%, тантала 89%, остальное – это примеси углерода (0,0015%), кислорода (0,0045%) и азота (0,0015%), которые попадают в сплав ввиду несовершенства технологий плавки.
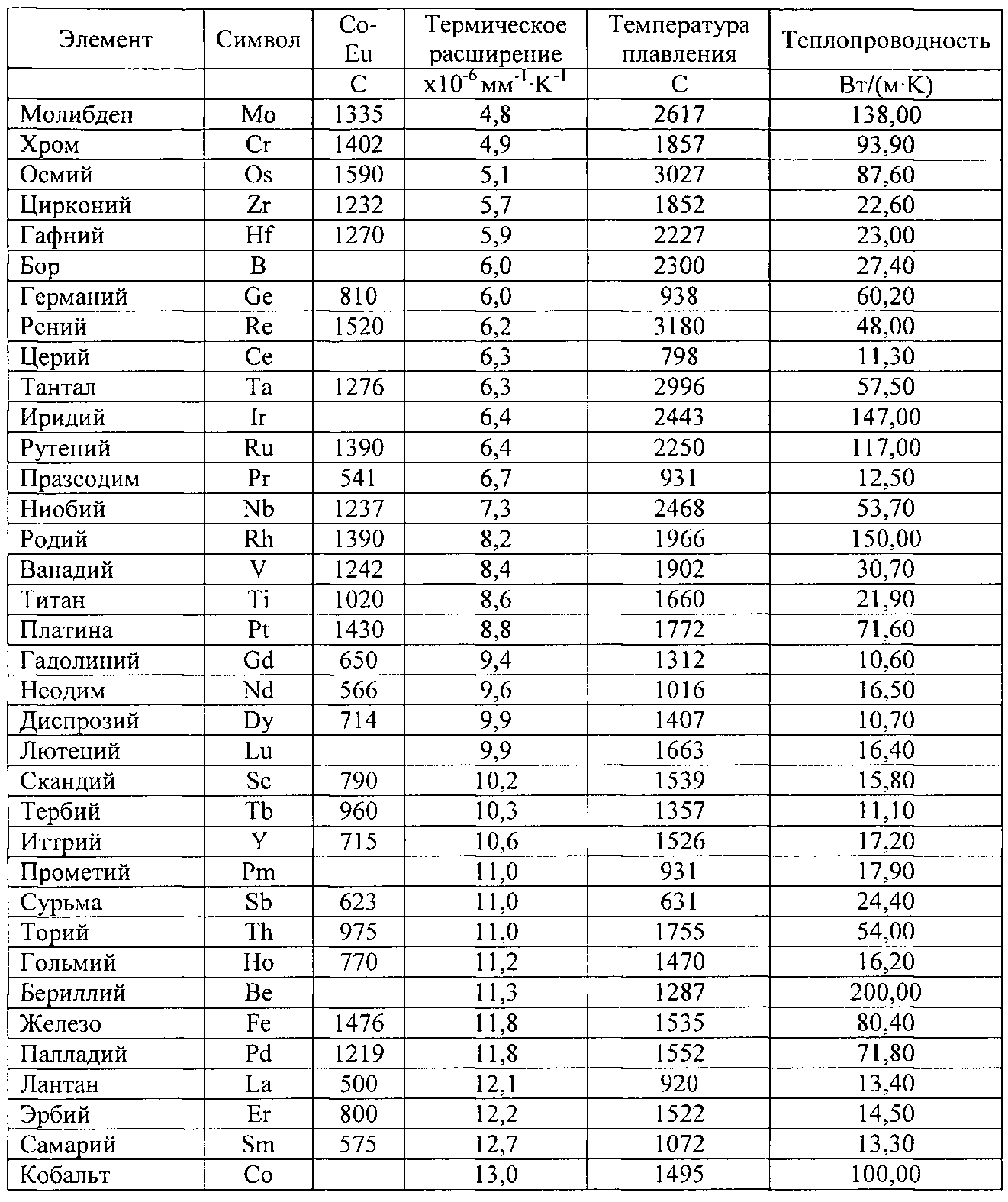
Тантал – серый блестящий металл. Содержание в земной коре порядка 0,0002%. Тантал плавится при температуре 3000 ºС. В природе встречается только в виде соединений с ниобием. Устойчив к воздействию щелочей и кислот, кроме азотной и фтористоводородной.
В природе встречается только в виде соединений с ниобием. Устойчив к воздействию щелочей и кислот, кроме азотной и фтористоводородной.
Вольфрам – серовато-белый металл. Температура плавления 3410 ºС. Распространенность в земной коре 0,0001%. Плотность 19300 кг\м3. В естественных условиях содержится только как соль вольфрамовой кислоты. Не взаимодействует с воздухом и водой. При нагревании активно вступает в реакцию с кислородом, азотом и серой. Растворяется в царской водке, азотной кислоте и расплавленных щелочах.
Физические и механические свойства
Танталовый сплав имеет высокое значение теплопроводности, которое колеблется в зависимости от значения температуры окружающей среды в пределах 0,13-0,20 кал/см с К. Жаропрочен. Сохраняет свои свойства при температурах свыше 2700 ºС.
Механические характеристики ТАВ 10 сильно зависят от типа выплавки. Это связано с тем, что каждый способ по-разному влияет на степень засорения тантала. Существует 2 их основные разновидности:
- Выплавка в электро-лучевой печи.
 Такой сплав обладает твердостью до 190 кг\мм2, пределом прочности 64 МПа и пределом текучести 68 МПа. ТАВ 10 достаточно пластичен: относительное удлинение 27-30%, модуль упругости 16500-18800 кг\мм2.
Такой сплав обладает твердостью до 190 кг\мм2, пределом прочности 64 МПа и пределом текучести 68 МПа. ТАВ 10 достаточно пластичен: относительное удлинение 27-30%, модуль упругости 16500-18800 кг\мм2. - Выплавка в дуговой печи. Танталовый сплав, полученный данным способом, отличается более высоким значением предела прочности (96 МПа) и твердости (230 кг\мм2). Пластичность же его чуть ниже: относительное удлинение 22-25%.
Для уменьшения внутренних напряжений, полученных во время плавки, ТАВ 10 подвергают термической обработке. Как правило, для этого применяют высокотемпературный отжиг (1500 С).
Также танталовые сплавы получают методом порошковой металлургии. Спекание происходит в специальных печах при температуре свыше 3000 С и в инертной среде водорода.
Технологические свойства
Все вышеперечисленные механические характеристики делают танталовый сплав ТАВ 10 хорошим материалом с точки зрения обработки давлением. Из тантала изготавливают различные типы проката: проволока, тонкостенные трубы и прочее. Современные компании имеют возможность производить танталовую фольгу толщиной меньше 0,2 мм.
Современные компании имеют возможность производить танталовую фольгу толщиной меньше 0,2 мм.
ТАВ 10 относится к первой группе свариваемости. Сварные швы получаются плотными и без значительных потерь в прочности. При этом процесс сварки не требует предварительной подготовки: прогрева поверхности сплава и последующей термообработки. Сварка осуществляется аргонно-дуговым способом.
Химические свойства
Танталовый сплав отличается высокой устойчивостью к воздействию агрессивных сред. ТАВ 10 так же, как и чистый тантал, не растворяется в кислотах, не вступает в химические реакции с жидкими щелочными металлами. Окисляется только при температуре свыше 260 ºС.
Танталовый сплав известен своей биологической инертностью по отношению к живым тканям. Не провоцирует отторжение организмом и не создает благоприятные условия для развития бактерий.
Применение
Современные компании использую танталовые сплавы для решения следующих производственных задач:
- Изготовление теплообменников термоядерных реакторов.
 Причина этого – устойчивость к перегретым парам цезия.
Причина этого – устойчивость к перегретым парам цезия. - Компании химической промышленности применяют его при проектировании коррозионно-устойчивой аппаратуры.
- В медицине применяется для изготовления элементов крепежа тканей, костей и нервов, а также материалом для производства имплантантов. Использование сплава в данной отрасли становится все шире и шире. Так, торговая компания «Zimmer», специализировавшаяся на изготовлении танталовых зубных протезов, за последние 10 лет увеличила свой оборот в 2 раза.
- В военной промышленности танталовыми сплавами обогащают облицовку кумулятивных снарядов. По оценке специалистов пробивная способность таких боеприпасов увеличивается на 32%.
- В металлургии из ТАВ 10 изготавливают тигли для плавильных печей редкоземельных металлов, таких как иттрия и скандия.
Оцените статью:
Рейтинг: 0/5 – 0 голосов
Ещё статьи по теме:
Тантал
ТАНТАЛ, Та, химический элемент V группы периодической системы, аналог ванадия и ниобия. Атомный вес 181,4; порядковое число 73. Тантал – металл стально-серого, в отполированном виде белого цвета; удельный вес ~ 16,6, температура плавления 2800°С, температура кипения выше 4400°С, т. о. тантал – третий по плавкости металл [выше плавятся вольфрам (3370 ±50°С) и рений (3167±60°С)]. Сопротивление на разрыв незакаленного тантала около 100 кг/см2; твердость по Бринеллю 45,9. Чистый тантал легко поддается механической обработке: ковке, прокатке, волочению на холоде. Путем термической обработки его твердость м. б. значительно повышена. При нагревании тантал легко поглощает газы и становится хрупким; вследствие этого нагревание предназначенного к механической обработке тантал ведут в вакууме. Поглощенный водород тантал отдает с трудом; при температуре плавления легко поддается сварке. Удельная теплоемкость тантала 0,0365 при 0°С. Термический коэффициент расширения при 20°С – 0,0000065. В химическом отношении тантал чрезвычайно стоек при низких температурах, благодаря чему может заменять во многих случаях платину.
Атомный вес 181,4; порядковое число 73. Тантал – металл стально-серого, в отполированном виде белого цвета; удельный вес ~ 16,6, температура плавления 2800°С, температура кипения выше 4400°С, т. о. тантал – третий по плавкости металл [выше плавятся вольфрам (3370 ±50°С) и рений (3167±60°С)]. Сопротивление на разрыв незакаленного тантала около 100 кг/см2; твердость по Бринеллю 45,9. Чистый тантал легко поддается механической обработке: ковке, прокатке, волочению на холоде. Путем термической обработки его твердость м. б. значительно повышена. При нагревании тантал легко поглощает газы и становится хрупким; вследствие этого нагревание предназначенного к механической обработке тантал ведут в вакууме. Поглощенный водород тантал отдает с трудом; при температуре плавления легко поддается сварке. Удельная теплоемкость тантала 0,0365 при 0°С. Термический коэффициент расширения при 20°С – 0,0000065. В химическом отношении тантал чрезвычайно стоек при низких температурах, благодаря чему может заменять во многих случаях платину. При нагревании на воздухе при температуре около 400°С тантал начинает покрываться синей пленкой окислов, а при температуре красного каления сгорает полностью до пятиокиси тантала (см. ниже).
При нагревании на воздухе при температуре около 400°С тантал начинает покрываться синей пленкой окислов, а при температуре красного каления сгорает полностью до пятиокиси тантала (см. ниже).
Непосредственно соединяется также при высоких температурах с азотом с образованием нитрида, с водородом с образованием гидрида и с углеродом с образованием карбида тантала; при обычной температуре соединяется с фтором. Минеральные кислоты, концентрированные и разбавленные, на него практически не действуют; исключением является плавиковая кислота, особенно в смеси с азотной, в которой тантал растворяется относительно быстро. Элементарный хлор практически на тантал не действует. Относительно быстро разрушается тантал щелочами, особенно горячими концентрированными растворами.
Соединения тантала. Важнейшие соединения производятся от пятивалентного тантала. Соединения низших степеней валентности менее стабильны и не имеют технического значения.
Пятиокись тантала Та2О5 получается путем сильного прокаливания металлического тантала или его соединений с летучими веществами в кислороде или на воздухе. Практически получают ее путем прокаливания танталовой кислоты (см. ниже). Та2О5 – белый порошок, удельный вес 8,70, нерастворимый в воде и кислотах за исключением плавиковой. При сильном прокаливании в вакууме Та2О5 отщепляет кислород и образует металлический тантал. Путем сплавления Та2О5 с едкими или углекислыми щелочами получают соли танталовой кислоты, танталаты: метатанталаты, например, NaTaО3, ортотанталаты, например, Na3TaО4, пиротанталаты, например, минерал иттротанталит, и политанталаты типа Me8Ta6O19. При воздействии минеральных кислот на растворы танталитов выделяется аморфный осадок гидратированной пятиокиси тантала непостоянного состава, т.н. танталовая кислота. Свежеосажденная танталовая кислота слабо растворяется в щелочах и минеральных кислотах; из последних осаждается при разбавлении. Пятифтористый тантал TaF5 получается путем воздействия фтористого водорода на TaCl5 (см.
Практически получают ее путем прокаливания танталовой кислоты (см. ниже). Та2О5 – белый порошок, удельный вес 8,70, нерастворимый в воде и кислотах за исключением плавиковой. При сильном прокаливании в вакууме Та2О5 отщепляет кислород и образует металлический тантал. Путем сплавления Та2О5 с едкими или углекислыми щелочами получают соли танталовой кислоты, танталаты: метатанталаты, например, NaTaО3, ортотанталаты, например, Na3TaО4, пиротанталаты, например, минерал иттротанталит, и политанталаты типа Me8Ta6O19. При воздействии минеральных кислот на растворы танталитов выделяется аморфный осадок гидратированной пятиокиси тантала непостоянного состава, т.н. танталовая кислота. Свежеосажденная танталовая кислота слабо растворяется в щелочах и минеральных кислотах; из последних осаждается при разбавлении. Пятифтористый тантал TaF5 получается путем воздействия фтористого водорода на TaCl5 (см. ниже). Кристаллизуется в виде бесцветных призм, температура плавления 96,8°С, температура кипения 229°С. С водой гидролизуется с образованием танталовой кислоты. ТаF5 обнаруживает большую склонность к образованию комплексных солей, которые получаются при добавлении соответствующих фтористых солей к раствору тантала в плавиковой кислоте. Большинство этих солей соответствует типу 2MeF TaF5, но известны и другие, как 2TaF5 3BaF2; TaF5 3NaF; TaF5·NaF. Флюoтанталат калия TaF5 2KF, или K2TaF7, получают из растворов TaF5 при добавлении солей калия, чем пользуются для отделения тантала от ниобия и титана. В виду большого термического коэффициента растворимости эта соль хорошо перекристаллизовывается из горячей воды. Во избежание гидролиза эту операцию необходимо вести в присутствии небольшого избытка плавиковой кислоты.
ниже). Кристаллизуется в виде бесцветных призм, температура плавления 96,8°С, температура кипения 229°С. С водой гидролизуется с образованием танталовой кислоты. ТаF5 обнаруживает большую склонность к образованию комплексных солей, которые получаются при добавлении соответствующих фтористых солей к раствору тантала в плавиковой кислоте. Большинство этих солей соответствует типу 2MeF TaF5, но известны и другие, как 2TaF5 3BaF2; TaF5 3NaF; TaF5·NaF. Флюoтанталат калия TaF5 2KF, или K2TaF7, получают из растворов TaF5 при добавлении солей калия, чем пользуются для отделения тантала от ниобия и титана. В виду большого термического коэффициента растворимости эта соль хорошо перекристаллизовывается из горячей воды. Во избежание гидролиза эту операцию необходимо вести в присутствии небольшого избытка плавиковой кислоты.
Пятихлористый тантал ТаСl5 – желтое кристаллическое вещество, удельный вес 3,68, температура плавления 211°С и температура кипения 242°С, получается при воздействии хлора на металлический тантал.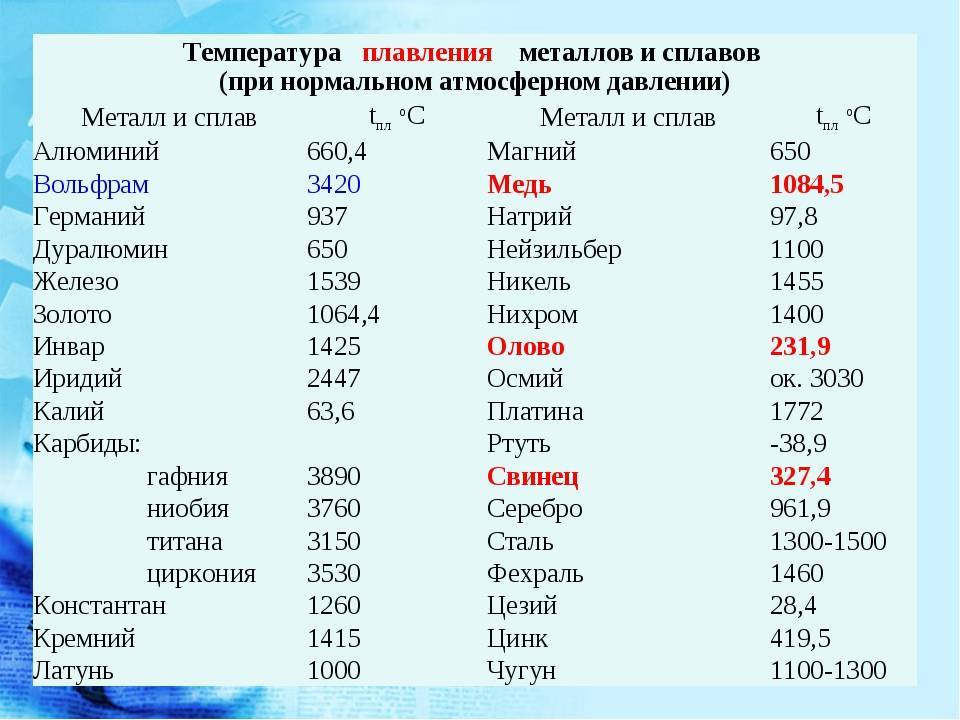 При нагревании на воздухе превращается в Та2О5. Вода разлагает ТаСl5 с образованием хлористого водорода и танталовой кислоты. При нагревании ТаСl5 в вакууме или при осторожном восстановлении его получают кристаллические низшие хлориды тантала зеленого цвета. Треххлористый тантал ТаСl5 растворяется в воде без разложения; из зеленого раствора щелочи осаждается зеленый аморфный осадок гидроокиси тантала Та(ОН)3, обнаруживающей амфотерные свойства и растворимой как в избытке щелочи, так и в кислотах. При кипячении Та(ОН)3 разлагает воду с образованием танталовой кислоты по реакции
При нагревании на воздухе превращается в Та2О5. Вода разлагает ТаСl5 с образованием хлористого водорода и танталовой кислоты. При нагревании ТаСl5 в вакууме или при осторожном восстановлении его получают кристаллические низшие хлориды тантала зеленого цвета. Треххлористый тантал ТаСl5 растворяется в воде без разложения; из зеленого раствора щелочи осаждается зеленый аморфный осадок гидроокиси тантала Та(ОН)3, обнаруживающей амфотерные свойства и растворимой как в избытке щелочи, так и в кислотах. При кипячении Та(ОН)3 разлагает воду с образованием танталовой кислоты по реакции
Та(ОН)3 + 2Н2О=Та(ОН)5 + Н2.
При упаривании растворов ТаСl3 с избытком соляной кислоты образуется своеобразная хлорокись Та3Сl7O·ЗН2O. При сильном нагревании ТаСl3 распадается на ТаСl5 и ТаСl2. Карбид тантала ТаС чрезвычайно твердый, латунно-жёлтого цвета, получается путем нагревания в вакууме смеси порошков металлического тантала или Та2О5 с углем; плавится при температуре около 3900°С.
Карбид тантала ТаС чрезвычайно твердый, латунно-жёлтого цвета, получается путем нагревания в вакууме смеси порошков металлического тантала или Та2О5 с углем; плавится при температуре около 3900°С.
Распространение тантала в земной коре определяется цифрой 2·10-7. В минералах он обычно в виде изоморфной примеси сопровождает ниобий. Важнейшим промышленным минералом является танталит, метатанталат железа Fe(TaО3)2, в котором часть железа м. б. замещена железом, а часть тантала – ниобием (танталитами условно называют минералы изоморфного ряда (Fe, Mn) [(Ta, Nb)О3]2, в которых тантал преобладает над ниобием). Важнейшие месторождения танталитов – Финляндия, Скандинавия и США (Коннектикут и Дакота), месторождения мирового значения в западной и северной Австралии. Во многих минералах тантал связан с редкими землями, как в фергусоните, ортотанталате (и ниобате) иттриевых земель Y [(Ta, Nb)О4], иттротанталите, пиротанталате (и ниобате) тех же оснований Y4[(Ta, Nb)2О7]3 и самарските, сложном ниоботанталате, найденном на Урале, содержащем также и уран. Редко встречающийся микролит представляет собой пиротанталат кальция Са2(Та2О7). Пирохлор, эйксенит и поликраз – сложные титанониобаты, содержащие колеблющиеся количества тантала.
Редко встречающийся микролит представляет собой пиротанталат кальция Са2(Та2О7). Пирохлор, эйксенит и поликраз – сложные титанониобаты, содержащие колеблющиеся количества тантала.
Для извлечения тантала из минералов последние сплавляют обычно с щелочными пиросульфатами в железных сосудах и выщелачивают плав водой. Остающуюся нерастворенной танталовую и ниобиевую кислоты растворяют в плавиковой. Для отделения от ниобиевой кислоты пользуются гл. обр. дробной кристаллизацией солей, чаще всего фторотанталатом калия K2TaF7. Путем восстановления фторотанталата калия металлическими натрием по реакции K2TaF7+5Na = 5NaF+2KF+Ta получают элементарный тантал в виде загрязненного окислами черного порошка. Для очистки его прокаливают в вакуумной электропечи до высоких температур, при которых окислы распадаются; образующийся порошок тантала прессуют и в вакууме же плавят.
Применение тантала довольно разнообразно; оно обусловливается его высокой температурой плавления, механическими свойствами и химической стойкостью. Тантал является первым металлом, из которого изготовляли (с 1903 до 1911 г.) нити для электроламп. Позднее он был вытеснен вольфрамом. В настоящее время из него готовят электроды электронных ламп. Тантал пользуются как материалом для изготовления химической аппаратуры (тиглей, чашек), физических приборов и хирургических, главным образом зубоврачебных инструментов, вечных перьев (самопишущих ручек), а также фильер в производстве искусственного шелка. Благодаря химической стойкости он применяется иногда как материал для электродов, особенно в электроанализе. В серной кислоте катод из тантала покрывается синей пленкой окислов, которая пропускает электрический ток только в одном направлении, благодаря чему тантал применяется в мокрых выпрямителях переменного тока. Сплавы тантала с железом, хромом, ванадием, молибденом и вольфрамом обладают большой твердостью, тугоплавкостью и химической стойкостью, в частности сплав с железом химически весьма стоек. До сих пор эти сплавы вследствие высокой цены тантала производились в относительно небольших масштабах.
Тантал является первым металлом, из которого изготовляли (с 1903 до 1911 г.) нити для электроламп. Позднее он был вытеснен вольфрамом. В настоящее время из него готовят электроды электронных ламп. Тантал пользуются как материалом для изготовления химической аппаратуры (тиглей, чашек), физических приборов и хирургических, главным образом зубоврачебных инструментов, вечных перьев (самопишущих ручек), а также фильер в производстве искусственного шелка. Благодаря химической стойкости он применяется иногда как материал для электродов, особенно в электроанализе. В серной кислоте катод из тантала покрывается синей пленкой окислов, которая пропускает электрический ток только в одном направлении, благодаря чему тантал применяется в мокрых выпрямителях переменного тока. Сплавы тантала с железом, хромом, ванадием, молибденом и вольфрамом обладают большой твердостью, тугоплавкостью и химической стойкостью, в частности сплав с железом химически весьма стоек. До сих пор эти сплавы вследствие высокой цены тантала производились в относительно небольших масштабах. Из соединений тантала практическое значение имеет только карбид – одно из наиболее тугоплавких известных веществ, – обладающий очень большой твердостью. Он начинает находить применение в производстве режущих инструментов и как материал для высокотемпературных печей.
Из соединений тантала практическое значение имеет только карбид – одно из наиболее тугоплавких известных веществ, – обладающий очень большой твердостью. Он начинает находить применение в производстве режущих инструментов и как материал для высокотемпературных печей.
Источник: Мартенс. Техническая энциклопедия. Том 22 – 1933 г.
Периодическая таблица элементов: Лос-Аламосская национальная лаборатория
Вернуться к списку элементов
| Атомный номер: | 73 | Атомный радиус: | 217 часов (Ван-дер-Ваальс) |
| Атомный символ: | Та | Температура плавления: | 3017 °С |
| Атомный вес: | 180,9 | Температура кипения: | 5458 °С |
| Электронная конфигурация: | [Xe]6s 2 4f 14 5d 3 | Степени окисления: | 5 , 4, 3, 2, 1, −1, −3 (слабокислотный оксид) |
История
Назван в честь Танталоса, греческого мифологического персонажа, отца Ниобы. Открыт в 1802 году Экебергом, но многие химики считали ниобий и тантал идентичными элементами, пока Роу в 1844 году и Мариньяк в 1866 году не показали, что ниобиевая и танталовая кислоты – это две разные кислоты. Первые исследователи только изолировали нечистый металл. Первый относительно чистый пластичный тантал был получен фон Болтоном в 1903. Тантал встречается главным образом в минерале колумбит-танталите.
Открыт в 1802 году Экебергом, но многие химики считали ниобий и тантал идентичными элементами, пока Роу в 1844 году и Мариньяк в 1866 году не показали, что ниобиевая и танталовая кислоты – это две разные кислоты. Первые исследователи только изолировали нечистый металл. Первый относительно чистый пластичный тантал был получен фон Болтоном в 1903. Тантал встречается главным образом в минерале колумбит-танталите.
Источники
Танталовые руды находятся в Австралии, Бразилии, Мозамбике, Таиланде, Португалии, Нигерии, Заире и Канаде.
Производство
Отделение тантала от ниобия требует нескольких сложных стадий. Для коммерческого производства элемента используется несколько методов, включая электролиз расплавленного фтортанталата калия, восстановление фтортанталата калия натрием или реакцию карбида тантала с оксидом тантала. Известно, что существует двадцать пять изотопов тантала. Природный тантал содержит два изотопа.
Свойства
Тантал — серый, тяжелый и очень твердый металл. В чистом виде он пластичен и может быть вытянут в тонкую проволоку, которая используется в качестве нити для выпаривания металлов, таких как алюминий. Тантал почти полностью невосприимчив к химическому воздействию при температуре ниже 150°С и подвергается воздействию только плавиковой кислоты, кислых растворов, содержащих ион фтора, и свободного триоксида серы. Щелочи атакуют его очень медленно. При высоких температурах тантал становится гораздо более реакционноспособным. Этот элемент имеет температуру плавления, уступающую только вольфраму и рению. Тантал используется для изготовления различных сплавов с желаемыми свойствами, такими как высокая температура плавления, высокая прочность, хорошая пластичность и т. д. Тантал обладает хорошей «геттерной» способностью при высоких температурах, а пленки оксида тантала стабильны, имеют хорошие выпрямляющие и диэлектрические свойства. характеристики.
В чистом виде он пластичен и может быть вытянут в тонкую проволоку, которая используется в качестве нити для выпаривания металлов, таких как алюминий. Тантал почти полностью невосприимчив к химическому воздействию при температуре ниже 150°С и подвергается воздействию только плавиковой кислоты, кислых растворов, содержащих ион фтора, и свободного триоксида серы. Щелочи атакуют его очень медленно. При высоких температурах тантал становится гораздо более реакционноспособным. Этот элемент имеет температуру плавления, уступающую только вольфраму и рению. Тантал используется для изготовления различных сплавов с желаемыми свойствами, такими как высокая температура плавления, высокая прочность, хорошая пластичность и т. д. Тантал обладает хорошей «геттерной» способностью при высоких температурах, а пленки оксида тантала стабильны, имеют хорошие выпрямляющие и диэлектрические свойства. характеристики.
Использование
Ученые из Лос-Аламоса создали композитный материал из карбида тантала и графита, который считается одним из самых твердых материалов, когда-либо созданных. Соединение имеет температуру плавления 3738°С. Тантал используется для изготовления электролитических конденсаторов и деталей вакуумных печей, на которые приходится около 60% его использования. Металл также широко используется для изготовления химического технологического оборудования, ядерных реакторов, деталей самолетов и ракет. Тантал полностью невосприимчив к жидкостям организма и не вызывает раздражения. Поэтому он нашел широкое применение в изготовлении хирургических приспособлений. Оксид тантала используется для изготовления специального стекла с высоким коэффициентом преломления для объективов фотоаппаратов. Металл имеет много других применений.
Соединение имеет температуру плавления 3738°С. Тантал используется для изготовления электролитических конденсаторов и деталей вакуумных печей, на которые приходится около 60% его использования. Металл также широко используется для изготовления химического технологического оборудования, ядерных реакторов, деталей самолетов и ракет. Тантал полностью невосприимчив к жидкостям организма и не вызывает раздражения. Поэтому он нашел широкое применение в изготовлении хирургических приспособлений. Оксид тантала используется для изготовления специального стекла с высоким коэффициентом преломления для объективов фотоаппаратов. Металл имеет много других применений.
Танталовая проволока и стержень – металлы ESPI
| ТАНТАЛОВАЯ ПРОВОДКА | ТАНТАЛОВЫЙ СТЕРЖЕНЬ |
ТАНТАЛ — ИСТОРИЯ И ПРИМЕНЕНИЕ
Тантал (Ta) — 73-й элемент в периодической таблице. Ранее известный как тантал , это имя происходит от Тантала, мифологического греческого персонажа, известного своим вечным наказанием, в котором он стоял в луже воды, всегда отступая, прежде чем он мог наклониться и сделать глоток, и под фруктовым деревом. с низкими ветвями, с плодами, всегда ускользающими от его рук.
Ранее известный как тантал , это имя происходит от Тантала, мифологического греческого персонажа, известного своим вечным наказанием, в котором он стоял в луже воды, всегда отступая, прежде чем он мог наклониться и сделать глоток, и под фруктовым деревом. с низкими ветвями, с плодами, всегда ускользающими от его рук.
Тантал был открыт в Швеции в 1802 году Андерсом Экебергом, но годом ранее Чарльз Хэтчетт случайно открыл тантал, когда обнаружил еще один элемент колумбий. В 1809 году английский химик Уильям Волластон сравнил оксиды, полученные как из колумбия, так и из колумбита, и пришел к выводу, что эти два оксида идентичны, несмотря на разницу в измеренной плотности, и сохранил название тантал. Другие ученые подтвердили эти результаты, и считалось, что колумбий и тантал — это один и тот же элемент. Оспаривая этот вывод в 1846 году, немецкий химик Генрих Розе утверждал, что в образце танталита было два дополнительных элемента, и назвал их в честь детей Тантала: ниобий (от Ниобы, богини слез), и пелопий (от Пелопса).
В 1866 году швейцарский химик Жан де Мариньяк доказал, что элементов всего два. Де Мариньяк был первым, кто получил металлическую форму тантала в 1864 году, когда он восстановил хлорид тантала, нагревая его в атмосфере водорода. Ранние исследователи могли производить только нечистый тантал, а Вернер фон Болтон был первым, кто произвел относительно чистый пластичный металл в 1903 году. . Теперь его легко изготовить, его характеристики включают в себя очень эффективную тепло- и электропроводность, высокую устойчивость к коррозии и очень высокую температуру плавления 3017 ° C (температура кипения 5458 ° C), которую превосходят только вольфрам, рений и осмий для металлов, а также с углеродом. Плавиковую кислоту можно использовать для растворения материала. Танталовые руды часто содержат значительные количества ниобия, который сам по себе является очень ценным элементом, требующим извлечения обоих металлов для их продажи.
Крупнейшие производства тантала добываются в Австралии. Однако другие страны, такие как Китай, Эфиопия и Мозамбик, добывают руды с более высоким процентным содержанием тантала, поэтому они производят значительный процент мировой добычи. Таиланд и Малайзия также производят тантал как побочный продукт добычи олова. Будущие источники поставок тантала обнаруживаются в Египте, Саудовской Аравии, Канаде, США, Гренландии и Бразилии.
ТАНТАЛОВАЯ ПРОВОЛОКА И ПРУТОК
Тантал входит в группу тугоплавких металлов, которые являются второстепенными компонентами в секторе сплавов. Химическая инертность тантала делает его ценным материалом для лабораторного оборудования и может использоваться вместо платины. Сегодня в основном танталовые конденсаторы используются в электронике.
Благодаря своей пластичности тантал может быть вытянут в тонкую проволоку или нити, которые используются для выпаривания металлов, таких как алюминий. В 1903 г. танталовая проволока, изготовленная из металлического тантала, использовалась для изготовления нитей накаливания ламп, пока вольфрам не заменил ее в широком использовании.
Тантал также используется для производства различных сплавов с высокой температурой плавления, прочностью и хорошей пластичностью. В сплаве с другими металлами он также используется при изготовлении твердосплавных инструментов для металлообрабатывающего оборудования и в производстве суперсплавов для компонентов реактивных двигателей, химического технологического оборудования, ядерных реакторов и деталей ракет.
Тантал инертен по отношению к большинству кислот, кроме плавиковой кислоты и горячей серной кислоты, а также горячие щелочные растворы вызывают коррозию тантала. Это свойство делает его идеальным металлом для сосудов для химических реакций и труб для агрессивных жидкостей. Теплообменные змеевики для парового нагрева соляной кислоты изготовлены из тантала. Тантал широко использовался в производстве электронных ламп сверхвысокой частоты для радиопередатчиков.
Высокая температура плавления и стойкость к окислению обуславливают использование металла в производстве нагревательных элементов (стержней) в вакуумных печах. Тантал чрезвычайно инертен, поэтому из него изготавливают различные коррозионностойкие детали, такие как защитные гильзы, корпуса клапанов и танталовые крепежные детали.
Тантал чрезвычайно инертен, поэтому из него изготавливают различные коррозионностойкие детали, такие как защитные гильзы, корпуса клапанов и танталовые крепежные детали.
Благодаря высокой плотности кумулятивный заряд и вкладыши пенетратора, сформированные взрывом, были изготовлены из тантала. Тантал значительно увеличивает бронепробиваемость кумулятивного заряда благодаря своей высокой плотности и высокой температуре плавления.
Тантал также обладает высокой биоинертностью и используется в качестве ортопедического материала, что делает его полезным для протезов тазобедренных суставов. Поскольку тантал не обладает магнитными свойствами, эти имплантаты считаются приемлемыми для пациентов, проходящих процедуры МРТ.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ О ДОСТУПНЫХ ТАНТАЛОВЫХ ПРОДУКТАХ И ФОРМАХ
ESPI поставляет высокочистую проволоку и прутки во многих различных элементах для распространения в университетах, исследовательских лабораториях и производственных компаниях различной степени чистоты и форм-факторов (например, фольга, лист, лента, дробь, гранулы, куски, порошок, мишени для распыления, диски и детали, изготовленные по индивидуальному заказу). Мы можем изготовить все вышеперечисленное по вашему техническому заданию. Чтобы получить обзор форм по производству проволоки и катанки или дополнительную подробную информацию о других производственных предложениях ESPI, щелкните здесь.
Мы можем изготовить все вышеперечисленное по вашему техническому заданию. Чтобы получить обзор форм по производству проволоки и катанки или дополнительную подробную информацию о других производственных предложениях ESPI, щелкните здесь.
541.488.8311 telephone
800.638.2581 toll-free
541.488.8313 fax
800.488.0060 toll-free fax
This email address is being protected от спам-ботов. У вас должен быть включен JavaScript для просмотра.
ОБЩИЕ ИМУЩЕСТВА
Символ: | Та |
Атомный номер: | 73 |
Атомный вес: | 180.9479 |
Плотность: | 16,654 г/куб. |