Теплопроводность меди и алюминия таблица: Теплопроводность меди и ее сплавов – плюсы и минусы
alexxlab | 09.05.2023 | 0 | Разное
Теплопроводность цветных металлов, теплоемкость и плотность сплавов: таблицы при различных температурах
Теплопроводность цветных металлов и технических сплавов
В таблице представлены значения теплопроводности металлов (цветных), а также химический состав металлов и технических сплавов в интервале температуры от 0 до 600°С.
Цветные металлы и сплавы: никель Ni, монель, нихром; сплавы никеля (по ГОСТ 492-58): мельхиор НМ81, НМ70, константан НММц 58,5-1,54, копель НМ 56,5, монель НМЖМц и К-монель, алюмель, хромель, манганин НММц 85-12, инвар; магниевые сплавы (по ГОСТ 2856-68), электрон, платинородий; мягкие припои (по ГОСТ 1499-70): олово чистое, свинец, ПОС-90, ПОС-40, ПОС-30, сплав Розе, сплав Вуда.
По данным таблицы видно, что высокую теплопроводность (при комнатной температуре) имеют магниевые сплавы и никель. Низкая же теплопроводность свойственна нихрому, инвару и сплаву Вуда.
Коэффициенты теплопроводности алюминиевых, медных и никелевых сплавов
Теплопроводность металлов, алюминиевых, медных и никелевых сплавов в таблице дана в интервале температуры от 0 до 600°С в размерности Вт/(м·град).
Металлы и сплавы: алюминий, алюминиевые сплавы, дюралюминий, латунь, медь, монель, нейзильбер, нихром, нихром железистый, сталь мягкая. Алюминиевые сплавы имеют большую теплопроводность, чем латунь и сплавы никеля.
Коэффициенты теплопроводности сплавов
В таблице даны значения теплопроводности сплавов в интервале температуры от 20 до 200ºС.
Сплавы: алюминиевая бронза, бронза, бронза фосфористая, инвар, константан, манганин, магниевые сплавы, медные сплавы, сплав Розе, сплав Вуда, никелевые сплавы, никелевое серебро, платиноиридий, сплав электрон, платинородий.
Удельное сопротивление и температурный коэффициент расширения (КТР) металлической проволоки (при 18ºС)
В таблице указаны значения удельного электрического сопротивления и КТР металлической проволоки, выполненной из различных металлов и сплавов.
Материал проволоки: алюминий, вольфрам, железо, золото, латунь, манганин, медь, никель, константан, нихром, олово, платина, свинец, серебро, цинк.
Как видно из таблицы, нихромовая проволока имеет высокое удельное электрическое сопротивление и успешно применяется в качестве спиралей накаливания нагревательных элементов множества бытовых и промышленных устройств.
Удельная теплоемкость цветных сплавов
В таблице приведены величины удельной (массовой) теплоемкости двухкомпонентных и многокомпонентных цветных сплавов, не содержащих железа, при температуре от 123 до 1000К. Теплоемкость указана в размерности кДж/(кг·град).
Дана теплоемкость следующих сплавов: сплавы, содержащие алюминий, медь, магний, ванадий, цинк, висмут, золото, свинец, олово, кадмий, никель, иридий, платина, калий, натрий, марганец, титан, сплав висмут — свинец — олово, сплав висмут-свинец, висмут — свинец — кадмий, алюмель, сплав липовица, нихром, сплав розе.
Также существует отдельная таблица, где представлена удельная теплоемкость металлов при различных температурах.
Удельная теплоемкость многокомпонентных специальных сплавов
Удельная (массовая) теплоемкость многокомпонентных специальных сплавов приведена в таблице при температуре от 0 до 1300ºС.
Размерность теплоемкости кал/(г·град).
Теплоемкость специальных сплавов: алюмель, белл-металл, сплав Вуда, инвар, липовица сплав, манганин, монель, сплав Розе, фосфористая бронза, хромель, сплав Na-K, сплав Pb — Bi, Pb — Bi — Sn, Zn — Sn — Ni — Fe — Mn.
Плотность сплавов
Представлена таблица значений плотности сплавов при комнатной температуре.
Приведены следующие сплавы: бронза, оловянистая, фосфористая, дюралюминий, инвар, константан, латунь, магналиум, манганин, монель — металл, платино — иридиевый сплав, сплав Вуда, сталь катаная, литая.
ПРИМЕЧАНИЕ: Будьте внимательны! Плотность сплавов в таблице указана в степени 10-3. Не забудьте умножить на 1000!
Например, плотность катанной стали изменяется в пределах от 7850 до 8000 кг/м3.
Источники:
- Михеев М. А., Михеева И. М. Основы теплопередачи.
- Физические величины. Справочник. А. П. Бабичев, Н. А. Бабушкина, А. М. Братковский и др.
 ; Под ред. И. С. Григорьева, Е. З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
; Под ред. И. С. Григорьева, Е. З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с. - Таблицы физических величин. Справочник. Под ред. акад. И. К. Кикоина. М.: Атомиздат, 1976. — 1008 с.
- Шелудяк Ю. Е., Кашпоров Л. Я. и др. Теплофизические свойства компонентов горючих систем. М.: 1992. — 184 с.
- Казанцев Е. И. Промышленные печи. Справочное руководство для расчетов и проектирования.
Таблица характеристик алюминия
Алюминий относится к минералам, встречающимся в природе в виде небольших мелкозернистых скоплений. Входит в группу парамагнитных металлов. Податливость сплава к обработке обуславливает широкое использование в литье и формовке. Благодаря высоким эксплуатационным характеристикам алюминиевый металлопрокат популярен во всех сферах хозяйства.
Характеристики
Естественный цвет алюминия обладает металлическим серебристо-белым оттенком. В природе чистый элемент отсутствует ввиду активного взаимодействия с другими веществами. Он существует в виде бокситов и минеральных пород – нефелинов, полевого шпата, глиноземов, синего и красного корунда. Минерал корунд известен в ювелирном деле под названиями сапфира и рубина и представляет собой оксид алюминия, формула которого Al2O3.
Минерал корунд известен в ювелирном деле под названиями сапфира и рубина и представляет собой оксид алюминия, формула которого Al2O3.
Физические и химические свойства алюминия приведены в таблице.
|
Физические характеристики |
||||
|
Показатель |
Алюминий |
|||
|
Химическая формула |
Al |
|||
|
Расположение в хим.таблице Менделеева |
3 период, 3 группа, №13 |
|||
|
ГОСТ |
4784-2019 |
|||
|
Расшифровка |
Алюминий и сплавы, получаемые из алюминия |
|||
|
Плотность алюминия, кг/м3 |
2700 |
|||
|
Твердость по Бринеллю |
240 |
|||
|
Температура кипения, °С |
2518 |
|||
|
Температура плавления алюминия, °С |
660 |
|||
|
Параметр удельной теплоемкости, кДж/кг·K |
90 |
|||
|
Теплопроводность при 100°С, кВт/(м·К) |
20 |
|||
|
Электропроводность, см/м |
37·106 |
|||
|
Значение температурного электрического сопротивления, (10−3 K−1) |
4,3 |
|||
|
Коэффициент удельного сопротивления, Ом·мм²/м |
0,026 |
|||
|
Значение линейного теплового расширения, при t=20-200°С (10−6 К−1) |
24 |
|||
|
Ударная вязкость, t = 20°С |
140 |
|||
|
Модуль упругости |
710000 |
|||
|
Показатель предела прочности |
70 |
|||
|
Величина предела текучести |
7-11 |
|||
|
Значение относительного удлинения |
40 |
|||
|
Коэффициент Пуассона |
0,34 |
|||
|
Химические характеристики алюминия и его соединений |
||||
|
Реакции |
Образуемое вещество |
Особенности проведения |
||
|
С простыми элементами: С кислородом С галогенами С фосфором С серой С азотом С углеродом |
оксид алюминия иодид бромид хлорид фосфиды сульфид нитрид метанид или карбид алюминия |
Применяется мелкодисперсный порошок металла Катализатор в реакции с йодом – капля воды Металл смешивается с жидким бромом Применяется нагретая фольга либо мелкий порошок вещества Протекает при температуре в 500-800 градусов Цельсия Нагревание до 200 С Нагревание до 1000 градусов по Цельсию Нагрев до 2000 градусов по Цельсию |
||
|
Со сложными веществами: С водой С оксидами металлов С минеральными кислотами С концентриров. Со щелочами |
гидроксид соли алюминия и газообразный водород сульфат алюминия нитрат алюминия тетрагидроксоалюминат с водородом |
Предварительное удаление оксидной пленки раствором щелочи, солями ртути или хлоридом аммония Смесь поджигается, метод алюмотермии Применяются все кислоты за исключением концентратов серной и азотной Требуется сильный нагрев Взаимодействует с водными щелочными растворами и чистыми щелочами |
||
|
Химические реакции гидроксида алюминия: С растворами кислот С оксидами и карбонатами Со щелочами |
соли соли метаалюминаты комплексные соли |
В условиях сплавления – нагрева до высокой температуры Гидроксид алюминия растворяется в щелочи |
||
|
Процесс алюмотермии – восстановления металлов из оксидов (на примере хрома) |
хром и оксид алюминия |
Сильный экзотермический процесс, требует нагрева |
||
|
Химические свойства солей алюминия |
||||
|
Реакции |
Образуемое вещество |
Особенности проведения |
||
|
Разложение на оксиды: нитрат сульфат |
оксид алюминия, кислород, оксид азота |
Выполняется при нагревании |
||
|
Гидролиз алюминия: растворимых солей сульфида, сульфата, карбоната |
Гидроксид алюминия с белым осадком Нерастворимый гидроксид алюминия |
Двойной обратимый гидролиз, протекает ступенчато Необратимый гидролиз |
||
При соприкосновении с воздухом металл образует устойчивые оксидные пленки.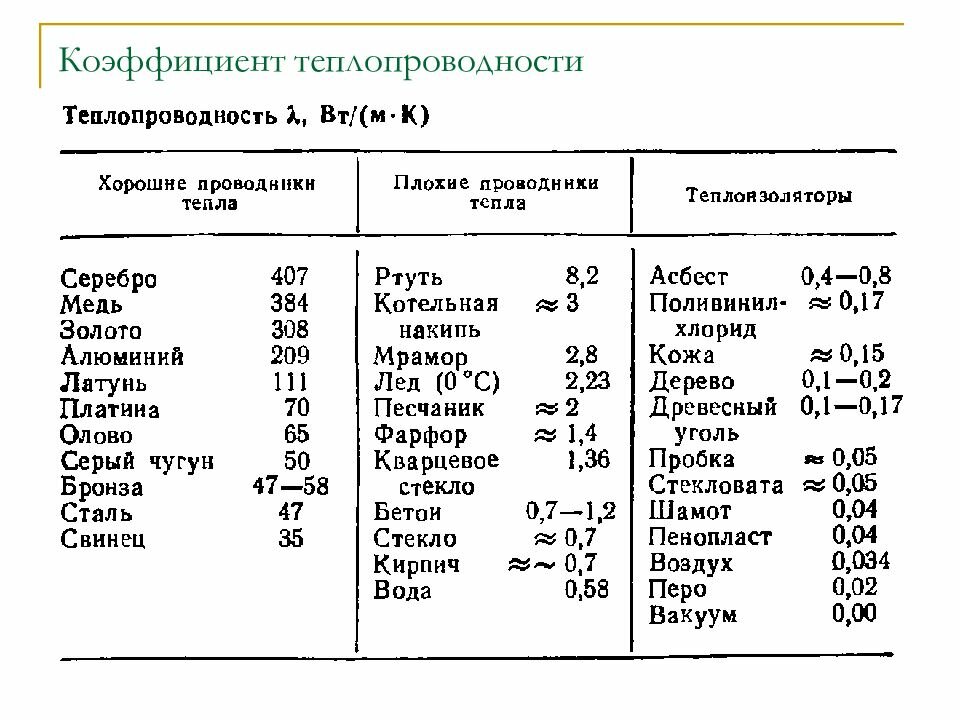 Это обуславливает отличные показатели сопротивляемости сплавов коррозии.
Это обуславливает отличные показатели сопротивляемости сплавов коррозии.
Свойства алюминия:
- прочность;
- малый вес;
- легкоплавкость, податливость резке, штамповке;
- коррозийная стойкость;
- хорошие показатели теплопроводности и электропроводности.
Металл относится к элементам высокой химической активности. Из-за быстрой реакции с воздухом на поверхности формируется оксидная пленка.
Она отличается высокой температурой плавления в 2000 градусов Цельсия, в то время как температура плавления алюминия составляет 660°С. Этим обуславливаются сложные характеристики сварки алюминия – текучесть сплава создает трудности в образовании ровного и прочного шва.
Сварку металлопроката выполняют полуавтоматическим способом в инертной среде либо с помощью вольфрамового электрода и инертного газа. Популярной технологией при отсутствии газов является сварка плавящимися электродами.
Получение
В лабораториях чистый элемент получают, соединяя раствор хлорида алюминия с металлическим калием при нагревании.
Популярным сырьем для промышленности выступает вторичный алюминий. В качестве материала применяются товары и металлопрокат, вышедшие из эксплуатации. Поступающий в переработку лом алюминия отличается большим количеством загрязнителей и примесей, что требует проведения тщательной очистки и сортировки.
Источники металла:
- детали автомобилей, судов, самолетов;
- строительные конструкции;
- стоматологическое оборудование;
- бытовая техника, кухонная утварь, приборы домашнего пользования.
В больших количествах химический элемент содержится в холодильниках, посудомоечных и стиральных машинах, сушилках. Сплавы широко используются в деталях автомобилей – бамперах, элементах рам, крыльях, дверях, капотах, радиаторах. Источниками вторичного алюминия служат и предметы быта – посуда, телевизионные антенны, утюги, светильники, элементы окон и дверей.
Применение
Конструкционный металл востребован в авиастроении, автомобильной и космической отрасли, приборостроении, пищевой промышленности. Легкость сплава обеспечивает маневренность судов при низкой массе. Коррозийная стойкость обуславливает многолетнюю эксплуатацию транспортных средств, оборудования, посуды. Свойства проводника позволяют применять его в производстве микросхем. Для повышения прочности в процессе выплавки в сплав добавляют магний и медь.
Металл применяется в следующих сферах:
- авиастроении – изготовление насосов, элементов корпусов и двигателей;
- судостроении – для палубных комплектующих, трапов, радарных мачт, корпусов судов;
- ракетостроении – в качестве компонента ракетного топлива;
- строительстве – изготовление рам, конструкций, столярных изделий;
- автомобилестроении – производство элементов корпусов, бамперов, радиаторов;
- электронике – для микросхем, проводов и кабелей;
- оборонной промышленности – выпуск автоматов и пистолетов, установок, танков;
- железнодорожной сфере – для рам и деталей вагонов, цистерн.
Металл популярен в производстве бытовых предметов массового потребления – крупной и мелкой техники, зеркал, фольги, посуды. В металлургии элемент задействуется в качестве восстановителя, с его помощью из галогенидов и оксидов получают хром, марганец, калий. Стойкость к агрессивным средам и отсутствие токсичности обуславливают применение вещества в изготовлении емкостей для хранения кислот и щелочей, удобрений, пищевых продуктов. Используется в стекловарении и пиротехнике, изготовлении ювелирной бижутерии, служит пищевой добавкой. Применяется в производстве медикаментов, в сочетании с другими компонентами служит основой для обезболивающих и антацидных препаратов.
Сравнение теплопроводности меди, алюминия и латуни — Сборник экспериментов
Номер эксперимента: 1769
Цель эксперимента
Целью этого эксперимента является использование термочувствительных пленок для визуализации различной динамики теплопроводности в трех различных металлы.

Теория
См. теорию в уже описанном эксперименте: Теплопроводность пластика и металла I., Теория.
Инструменты
Термочувствительная пленка с температурным диапазоном от 25°С до 30°С, три разные металлические пластины одинакового размера, емкость для горячей воды, чайник.
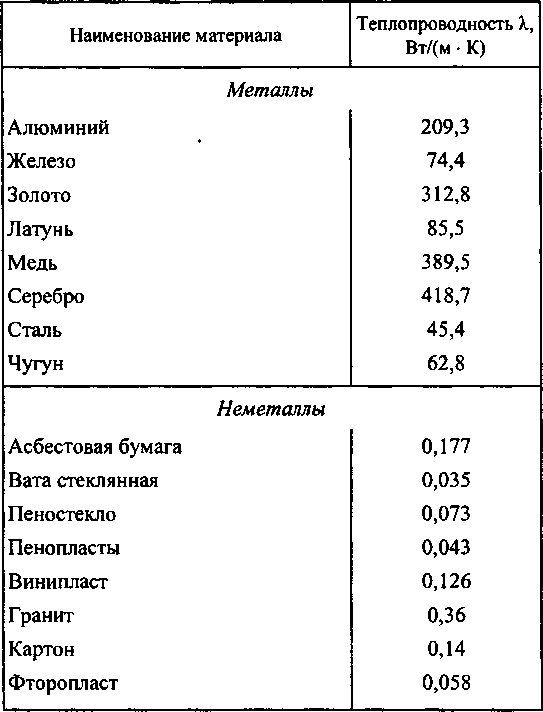
В пробном эксперименте используются медные, алюминиевые и латунные пластины одинаковых размеров; толщина пластин 0,3 мм. (Аналогичные металлические пластины можно приобрести в магазине дизайнерских инструментов). Таблица с теплопроводностями (при 25°C) используемых металлов приведена ниже:
металл λ / Вт·м −1 ·K −1 медь 386 алюминий 237 латунь 120 Термочувствительную пленку можно найти в Интернете под названием двусторонняя температурная этикетка .
 На рисунке 1 показан инструмент, изготовленный специально для этого эксперимента для изучения различной теплопроводности металла — три разные металлические пластины частично покрыты термочувствительной пленкой, что свидетельствует о повышении температуры.
На рисунке 1 показан инструмент, изготовленный специально для этого эксперимента для изучения различной теплопроводности металла — три разные металлические пластины частично покрыты термочувствительной пленкой, что свидетельствует о повышении температуры.
Процедура
Закрепите медный, алюминиевый и латунный лист параллельно друг другу (см., например, рис. 1) с помощью лабораторного стенда так, чтобы концы листов находились на несколько сантиметров выше стола (рис. 2). ). Подставьте под эти концы емкость и налейте в нее горячую воду так, чтобы она покрыла концы листов.
Наблюдайте, как термочувствительные пленки меняют цвет. Температура, представленная цветом, зависит от типа пленки. Пленка, использованная в этом эксперименте, имеет черный цвет при температуре ниже 25 °C. При повышении температуры в интервале от 25°С до 30°С пленка постепенно меняет свой цвет с коричневого, зеленого и синего на темно-синий и, наконец, после превышения 30°С цвет снова меняется на черный.

Целью такого изменения цвета этих пленок является не попытка точного измерения температуры в конкретной точке, а скорее указание и демонстрация распределения температуры поверхности.
Пример результата
Успешно проведенный эксперимент показан на видео ниже. Видео ускорено в 8 раз.
Очевидно, что медный лист нагревается быстрее всего, за ним следуют алюминий и латунь.
Технические примечания
Не наливать в емкость кипяток, использовать воду температурой 60 °C. При более высоких температурах образуется большое количество горячего пара, который течет вверх, что влияет на измерение с помощью термочувствительных пленок и делает его ненадежным.
Указанный выше эффект можно устранить, загнув нижние концы листов под прямым углом. Таким образом, более длинная часть измеряемых металлов может оставаться в горизонтальном положении.

Если вы проводите этот эксперимент летом, рекомендуется убедиться, что температура в классе ниже минимальной температуры, измеренной пленкой (здесь 25 °C). Если температура в классе выше, пленка меняет цвет на соответствующую температуру, делая результат менее заметным.
Нет необходимости использовать горячую воду для нагрева простыней. Однако всегда нужно следить за тем, чтобы простыни прогревались равномерно.
Педагогические заметки
Описание развития этого эксперимента приводит учащихся к выводу, что «медь нагревается быстрее, чем алюминий» и т. д. Более подготовленные ученики могут сообразить, что мы уже обсуждали «готовность ” вещества на изменение температуры в разрезе удельной теплоемкости c вещества . Эта мысль верна и ее следует принять во внимание – готовность материи изменять свою температуру зависит как от удельной теплоемкости, так и от теплопроводности материи.
Аргумент о том, что быстрый нагрев медного листа вызван его низкой теплоемкостью, можно легко опровергнуть с помощью приведенной ниже таблицы:
металл λ / Вт·м −1 ·K −1 с / Дж·кг −1 ·K −1 медь 386 383 алюминий 237 896 латунь 120 384 Следовательно, если бы решающим фактором была удельная теплоемкость металла, то поведение меди и латуни было бы почти одинаковым (они имеют близкие значения c ), но это явно противоречит эксперименту.

Если в классе есть действительно одаренные физики, они могут возразить, что этот аргумент не совсем удовлетворителен — листы имеют разную плотность, а значит, и масса, влияющая на величину теплоты, необходимой для нагрева, тоже разная. К счастью, плотности меди и латуни достаточно близки, так что различное поведение этих двух веществ нельзя объяснить иначе, как на основании разной теплопроводности.
Эффект разной теплопроводности можно продемонстрировать не только при нагреве металлов, но и при их охлаждении. Дайте всем трем металлам прогреться, например, на радиаторе, пока термочувствительные пленки не станут темно-синими. Затем погрузите концы металлических листов в смесь воды и льда. Медь остывает быстрее всех, за ней следуют алюминий и латунь.
При интерпретации продолжения эксперимента следует быть осторожным, чтобы не сложилось впечатление, что щиты «высасывают» холод изо льда – всегда следует интерпретировать понижение температуры как отвод тепла.

Вариант проведения эксперимента
Чтобы продемонстрировать разницу в теплопроводности трех металлов, можно поступить иначе. Положите листы меди, алюминия и латуни на стол и в середину каждого листа поместите кубик льда. Посмотрите, как быстро тают отдельные кубики (видео ускорено в 32 раза):
Очевидно, что быстрее всего лед тает на медном листе, а медленнее всего — на латунном. Медь обладает высокой теплопроводностью и поэтому способна постоянно отдавать тепло от периферийных частей листа к месту, охлаждаемому кубиком льда. Эта способность значительно хуже у латунного листа.
Преимуществом этого эксперимента является возможность обойтись без термочувствительных пленок. Недостатком является то, что это требует больше времени (примерно 15 минут).
Теплопроводность обычных металлов и сплавов
Теплопроводность обычных металлов, сплавов и материалов
Теплопередача Содержание
Свойства металлов – теплопроводность, плотность, удельная теплоемкость 900 типичные значения термических свойств некоторых распространенных коммерческих металлов и сплавов.
Значения относятся к температуре окружающей среды (от 0 до 25°C).
Все значения следует рассматривать как типовые, поскольку эти свойства зависят от конкретного типа сплава, термической обработки и других факторов. Значения для конкретных выделений могут сильно различаться.
Теплопроводность обычных металлов | ||
Имя | Теплопроводность | Теплопроводность |
Слиток железа | 0,7 | |
AISI-SAE 1020 | 0,52 | |
Тип из нержавеющей стали 304 | 0,15 | |
Серый чугун | 0,47 | |
Хастеллой С | 0,12 | |
Инконель | 0,15 | |
| Чистый алюминий | 237 | |
Алюминиевый сплав 3003, катаный | 1,9 | |
Алюминиевый сплав 2014, отожженный | 1,9 | |
Алюминиевый сплав 360 | 9,8 | |
Медь электролитическая (ЭТП) | 3,9 | |
Желтая латунь (высокая латунь) | 22,3 | |
Алюминиевая бронза | 0,7 | |
Бериллий | 218 | |
Бериллиевая медь 25 | 1. | |
Мельхиор 30% | 0,3 | |
Красная латунь, 85% | 1,6 | |
Латунь | 109 | |
| Свинец сурьмы (твердый свинец) | 0,35 | |
Припой 50-50 | 0,5 | |
Магниевый сплав AZ31B | 1,0 | |
Свинец | 35,3 | |
Серебро | 429 | |
Монель | 0,3 | |
Золото | 318 | |
Никель (коммерческий) | 0,9 | |
Мельхиор 55-45 (константан) | 0,2 | |
Титан (коммерческий) | 1,8 | |
Цинк (коммерческий) | 1. | |
Цирконий (технический) | 0,2 | |
| Цемент | 0,29 | |
| Эпоксидная смола (наполненная диоксидом кремния) | 0,30 | |
| Резина | 0,16 | |
| Эпост (незаполненный) | 0,59 | |
| Термопаста | 0,8 – 3 | |
| Термоэпоксидная смола | 1 – 7 | |
| Стекло | 1.1 | |
| Почва | 1,5 | |
| Песчаник | 2,4 | |
| Алмаз | 900-2320 | |
| Асфальт | 0,75 | |
| Бальза | 0,048 | |
| Хромоникелевая сталь | 16,4 | |
| Кориан | 1,06 | |
| Стекловолокно | 0,04 | |
| Гранит | 1,65 – 3,9 | |
| Пенополистирол | 0,032 | |
| Пенополиуретан | 0,02 | |
| Иридиум | 147 | |
Лиственные породы (дуб, клен. ..) ..) | 0,16 | |
Теплопроводность металлов
k = БТЕ/ч · фут · °F
k t = k до – a ( t – t o )
| Вещество | Диапазон температур , °F | к до | и | Вещество | Диапазон температур , °F | к до | и |
Металлы | Олово | 60 – 212 | 36 | 0,0135 | |||
| Алюминий | 70 – 700 | 130 | 0,03 | Титан | 70 – 570 | 9 | 0,001 |
| Сурьма | 70 – 212 | 10,6 | 0,006 | Вольфрам | 70 – 570 | 92 | 0,02 |
| Бериллий | 70 – 700 | 80 | 0,027 | Уран | 70 – 770 | 14 | -0,007 |
| Кадмий | 60 – 212 | 53,7 | 0,01 | Ванадий | 70 | 20 | — |
|---|---|---|---|---|---|---|---|
| Кобальт | 70 | 28 | — | Цинк | 60 – 212 | 65 | 0,007 |
| Медь | 70 – 700 | 232 | 0,032 | Цирконий | 32 | 11 | — |
| Германий | 70 | 34 | — | Сплавы: | |||
| Золото | 60 – 212 | 196 | — | Адмиралтейский металл | 68 – 460 | 58,1 | -0,054 |
| Железо чистое | 70 – 700 | 41,5 | 0,025 | Латунь | -265 – 360 | 61,0 | -0,066 |
| Железо кованое | 60 – 212 | 34,9 | 0,002 | (70 % Cu, 30 % Zn) | 360 – 810 | 84,6 | 0 |
| Сталь (1% С) | 60 – 212 | 26,2 | 0,002 | Бронза, 7,5% Sn | 130 – 460 | 34,4 | -0,042 |
| Свинец | 32 – 500 | 20,3 | 0,006 | 7,7% Алюминий | 68 – 392 | 39,1 | -0,038 |
| Магний | 32 – 370 | 99 | 0,015 | Константан | -350 – 212 | 12,7 | -0,0076 |
| Меркурий | 32 | 4,8 | — | (60 % меди, 40 % никеля) | 212 – 950 | 10,1 | -0,019 |
| Молибден | 32 – 800 | 79 | 0,016 | Дюрал 24С (93,6% Al, 4,4% Cu, | -321 – 550 | 63,8 | -0,083 |
| Никель | 70 – 560 | 36 | 0,0175 | 1,5% Mg, 0,5% Mn) | 550 – 800 | 130. | -0,038 |
| Палладий | 70 | 39 | — | Инконель X (73 % Ni, 15 % Cr, 7 % | 27 – 1 070 | 7,62 | -0,0068 |
| Платина | 70 – 800 | 41 | 0,0014 | Fe, 2,5% Ti) | |||
| Плутоний | 70 | 5 | — | Манганин (84% Cu, 12% Mn, | 1 070 – 1 650 | 3,35 | -0,0111 |
| Родий | 70 | 88 | — | 4% Ni) | -256 – 212 | 11,5 | -0,015 |
| Серебро | 70 – 600 | 242 | 0,058 | Монель (67,1% Ni, 29,2% Cu, 1,7% Fe, 1,0% Mn) | -415 – 1470 | 12,0 | -0,008 |
| Тантал | 212 | 32 | — | ||||
| Таллий | 32 | 29 | — | Нейзильбер (64 % Cu, 17 % Zn, 18 % Ni) | 68 – 390 | 18. | |


 кислотами
кислотами 20.8
20.8 1
1