Тип кристаллической решетки металлов: Типы кристаллических решёток — урок. Химия, 8 класс.
alexxlab | 19.02.2023 | 0 | Разное
Какой тип кристаллической решетки характерен для металлов? § 19-20, вопрос 3. Химия, 11 класс, базовый уровень, Рудзитис Г.Е., Фельдман Ф.Г.
Какой тип кристаллической решетки характерен для металлов? § 19-20, вопрос 3. Химия, 11 класс, базовый уровень, Рудзитис Г.Е., Фельдман Ф.Г. – Рамблер/классИнтересные вопросы
Школа
Подскажите, как бороться с грубым отношением одноклассников к моему ребенку?
Новости
Поделитесь, сколько вы потратили на подготовку ребенка к учебному году?
Школа
Объясните, это правда, что родители теперь будут информироваться о снижении успеваемости в школе?
Школа
Когда в 2018 году намечено проведение основного периода ЕГЭ?
Новости
Будет ли как-то улучшаться система проверки и организации итоговых сочинений?
Вузы
Подскажите, почему закрыли прием в Московский институт телевидения и радиовещания “Останкино”?
Прив, есть вопрос к сделавшим ДЗ.
Лучший ответ
Привет, есть.. Для металлов характерна металлическая кристаллическая решетка. Свойства обусловленные металлической кристаллической решеткой: электропроводность, теплопроводность, металлический блеск, непрозрачность.
еще ответы
ваш ответ
Можно ввести 4000 cимволов
отправить
дежурный
Нажимая кнопку «отправить», вы принимаете условия пользовательского соглашения
похожие темы
Юмор
Олимпиады
ЕГЭ
10 класс
похожие вопросы 5
Всем привет! Решим задачку? химия 10 класс Рудзитис задача 4 параграф 13
Подскажите верное решение) вот условие: Какой объем воздуха (н. у.) потребуется для сжигания 1 м3 бутана-1?
ГДЗ10 классХимияРудзитис Г. Е.
Е.
Здравствуйте.
(Подробнее…)
Химия
Какой был проходной балл в вузы в 2017 году?
Какой был средний балл ЕГЭ поступивших в российские вузы на бюджет в этом году? (Подробнее…)
Поступление11 классЕГЭНовости
16. Расставьте все знаки препинания: укажите цифру(-ы), на месте которой(-ых)… Цыбулько И. П. Русский язык ЕГЭ-2017 ГДЗ. Вариант 13.
16.
Расставьте все знаки препинания: укажите цифру(-ы), на месте которой(-ых)
в предложении должна(-ы) стоять запятая(-ые). (Подробнее…)
ГДЗЕГЭРусский языкЦыбулько И.П.
ЕГЭ-2017 Цыбулько И. П. Русский язык ГДЗ. Вариант 13. 18. Расставьте все знаки препинания: укажите цифру(-ы), на месте которой(-ых)…
18.
Расставьте все знаки препинания: укажите цифру(-ы), на месте которой(-ых)
в предложении должна(-ы) стоять запятая(-ые). (Подробнее…)
ГДЗЕГЭРусский языкЦыбулько И. П.
П.
Основные типы кристаллических решёток металлов
1 Сен
Posted on Author admin 0
Чтобы поделиться, нажимайте
Основные типы кристаллических решёток металлов
Физические свойства металлов определяются их электронным строением и природой кристаллической решётки.
Поскольку металлическая связь ненасыщаема и ненаправлена, для металлов характерны кристаллические структуры с высокими координационными числами (количество атомов, которое окружает один атом). Как правило, металлы кристаллизуются в одном из трёх типов решёток, для двух из них координационное число равно 12, а для третьей – 8.
Строение первых двух кристаллических решёток можно представить следующим образом. Мысленно положим шарообразные атомы металлов на стол и плотно придвинем их друг к другу. Мы заметим, что каждый шар окажется в окружении шести соседних шаров (на рисунке ниже – а).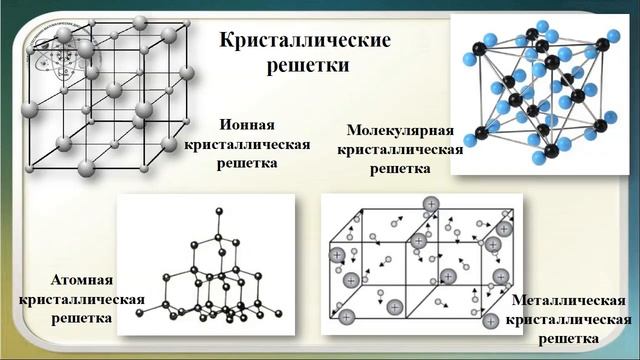
Затем положим сверху на первый слой шаров (А) второй слой (В) так, чтобы шары второго слоя попали в углубления между шарами первого слоя (на рисунке выше – б). Проделаем то же самое, укладывая сверху шары третьего слоя. Укладка шаров третьего слоя возможна двумя различными способами. Однако это не влияет на координационное число, но в результате образуются две неодинаковые структуры.
Первый способ приводит к расположению шаров третьего слоя в точности над шарами первого слоя (на рисунке выше –в). Такая структура называется
Второй способ отличается от первого тем, что расположение шаров третьего слоя С повернуто на 60 градусов вокруг вертикальной оси по отношению к первому слою (на рисунке выше – г). При этом шары третьего слоя оказываются над углублениями между шарами первого слоя. В таком случае только следующий, четвёртый, слой шаров в точности повторяет структуру шаров первого слоя. Такая структура называется кубической плотнейшей упаковкой (КПУ) или гранецентрированной кубической упаковкой (ГЦК) и состоит из чередующихся слоёв атомов металлов АВСАВС.
В таком случае только следующий, четвёртый, слой шаров в точности повторяет структуру шаров первого слоя. Такая структура называется кубической плотнейшей упаковкой (КПУ) или гранецентрированной кубической упаковкой (ГЦК) и состоит из чередующихся слоёв атомов металлов АВСАВС.
Третья кристаллическая структура (координационное число равно 8) может рассматриваться как цент куба, в вершинах которого находятся восемь его ближайших соседей. Такая структура называется объёмно-центрированной кубической упаковкой (ОЦУ).
Элементарные ячейки для всех типов кристаллических решёток металлов показаны на рисунке ниже.
Описанные кристаллические структуры отличаются степенью заполнение пространства: наиболее плотноупакованными (степень заполнения пространства составляет 74%) являются кристаллические решётки ГПУ и КПУ, менее плотноупакована (на 68%) – решётка типа ОЦУ. Пустоты играют важную роль в определении структуры металлических соединений и их сплавов.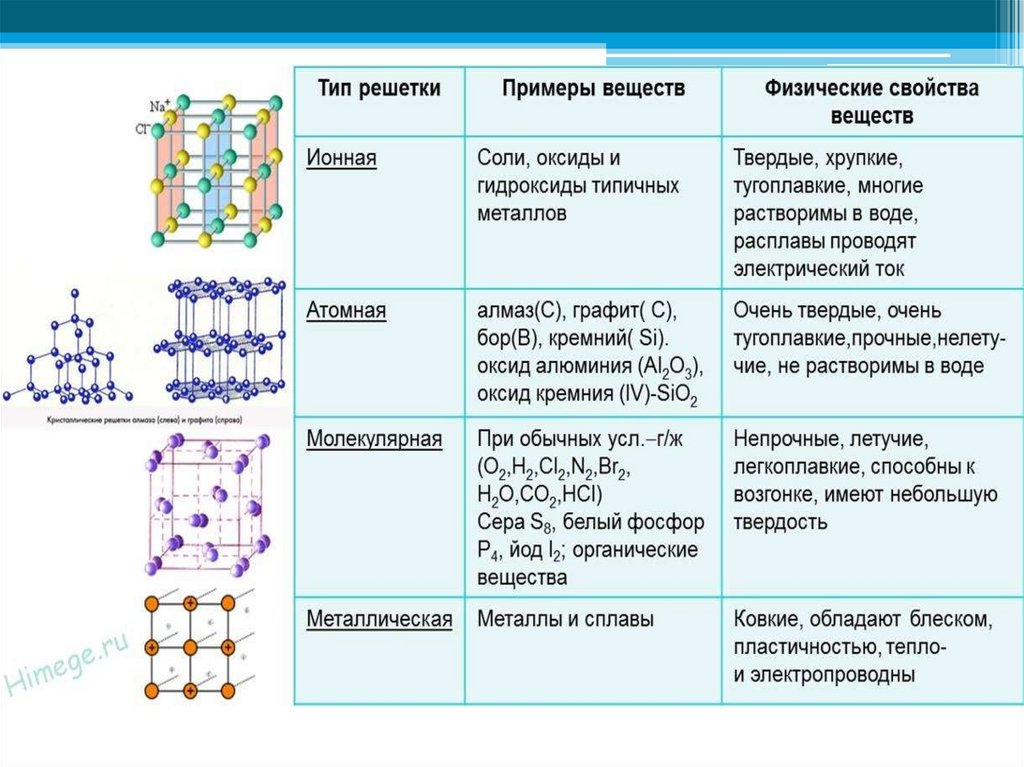
Кристаллические решётки некоторых металлов
Тип решётки | Металл |
| ГПУ | Mg, Zn, Be, Cd, Os, Ru |
| КПУ (ГЦК) | Cu, Ag, Al, Ca, Ni, Au, Pb, Pd, Pt, Co, Sr |
| ОЦУ | Li, Na, K, Rb, Cs, V, Cr, Mo, W, Fe, Ba |
Также важно знать, что ряд металлов в зависимости от температуры может кристаллизоваться в разных типах кристаллических решёток (явление полиморфизма), например белое и серое олово.
Кристаллические структуры благородных металлов и их поведение
Выпуск 036, 23 мая 2022 г.
Меган К. Пуглиа, доктор философии, старший химик-исследователь
Благородные металлы представляют собой кристаллические твердые вещества при комнатной температуре, что означает, что их атомы упорядочены по трехмерному повторяющемуся шаблону, называемому решеткой. Модель твердых сфер описывает поведение этой кристаллографической решетки¹; 1) атомы представляют собой сферы, которые могут соприкасаться друг с другом, но никогда не могут проникать друг в друга, и 2) атомы имеют тенденцию оптимизировать свое расположение, чтобы максимизировать стабильность и плотность упаковки (также известная как плотная упаковка).
Рисунок 1 : Усеченная периодическая таблица элементов, изображающая кристаллическую структуру благородных и неблагородных металлов по определению Дерингера-Ней².
Металлурги представляют бесконечно повторяющуюся решетку с более управляемой «элементарной ячейкой», которая является простейшей повторяющейся единицей, необходимой для воссоздания кристалла. Элементарная ячейка предоставляет обширную информацию о стехиометрии, изотропии и характеристиках³. Пластичность и приспособление к пластической деформации также можно объяснить с помощью кристаллографии.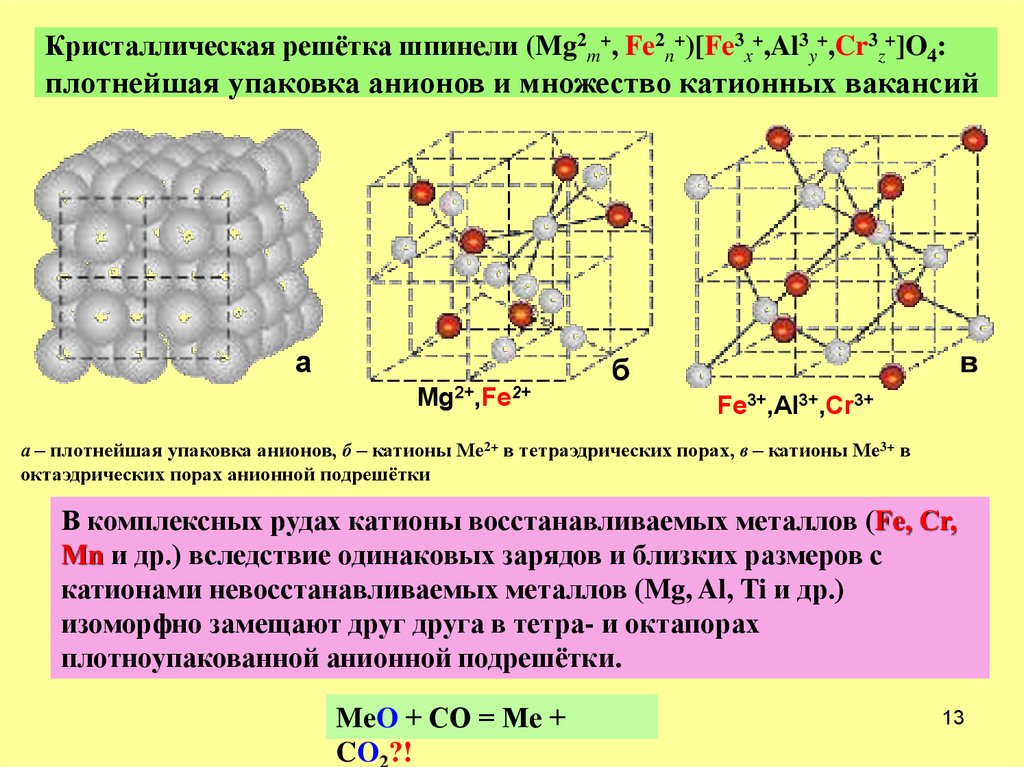
Определенные ориентации элементарной ячейки содержат плотноупакованные плоскости и плотноупакованные направления, которые вместе также известны как системы скольжения. В этих системах скольжения между атомами нет промежутка, и атомы могут легко скользить в соседнее положение. Это способствует легкому способу движения дислокаций, а количество доступных систем скольжения напрямую коррелирует с пластичностью.
Объемно-центрированные кубические: ОЦК-кристаллы имеют кубические элементарные ячейки с атомом в центре и, как показано на рис. 2, имеют плотноупакованные направления, но не имеют истинно плотноупакованных плоскостей. Однако, с учетом самой плотной плоскости, систем скольжения может быть до 48. Металлы ОЦК часто претерпевают пластическое превращение в хрупкое при криогенных температурах; это связано с тем, что этим системам скольжения требуется тепло для активации движения дислокаций. Этот барьер для миграции дислокаций делает ОЦК-металлы менее пластичными, чем ГЦК-металлы, но все же более пластичными, чем ГПУ-металлы.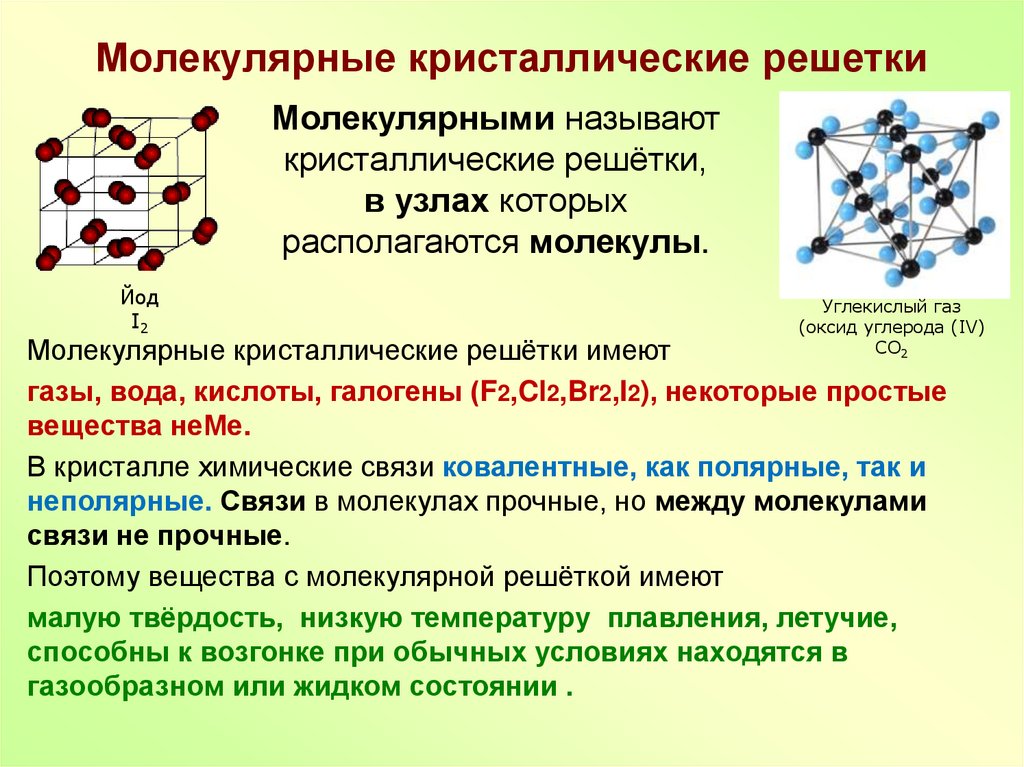
Рисунок 2 : Диаграмма, изображающая а) элементарную ячейку ОЦК и б) наиболее плотно упакованную плоскость, обозначенную зеленой плоскостью и зелеными атомами, которые лежат на этой плоскости.
Гексагональная закрытая упаковка: Всего существует 14 различных систем решетки, и кристаллы не всегда располагаются вдоль кубических решеток³. Структура ГПУ является одним из таких кристаллов и имеет гексагональную элементарную ячейку, рис. 3. На элементарную ячейку приходится только одна плоскость плотной упаковки и только три системы скольжения. Этого недостаточно для облегчения пластической деформации, и кристаллические структуры ГПУ, такие как Re, Ru и Os, известны своей плохой способностью приспосабливаться к пластической деформации. Некоторые кристаллы HCP, такие как Ti, могут использовать дополнительные плотно упакованные плоскости, которые улучшают их пластичность.
Рисунок 3 : Диаграмма, изображающая а) элементарную ячейку ГПУ и б) плоскость плотной упаковки, обозначенную зеленой плоскостью и зелеными атомами, лежащими на этой плоскости.
Гранецентрированный куб: Кристаллы FCC также имеют кубические элементарные ячейки, но с атомом на каждой грани куба. Как показано на рисунке 4, все атомы на этой плоскости касаются своих ближайших соседей. Эта конфигурация имеет как плоскости, так и направления плотной упаковки и порождает в общей сложности 12 систем скольжения. Это обеспечивает легкое движение дислокаций и делает кристаллические структуры FCC, такие как Pd, Pt, Ag, Au и их сплавы замещения, очень пластичными. Движение дислокаций здесь не зависит от температуры и не тормозится криогенными температурами. Сплавы DNI основаны на кристаллической структуре FCC, поэтому они обладают высокой пластичностью и широким диапазоном рабочих температур в дополнение к благородству благодаря своему базовому составу Pd, Pt или Au.
Рисунок 4 : Диаграмма, изображающая а) элементарную ячейку ГЦК и б) плоскость плотной упаковки, обозначенную зеленой плоскостью
, и зеленые атомы, лежащие на этой плоскости.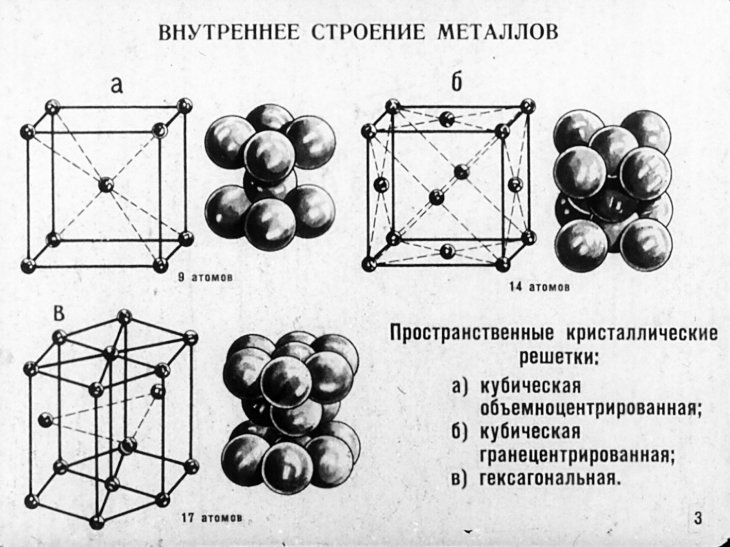
Ссылки:
- В. Каллистер, 3 Структура кристаллических твердых тел, в: Материаловедение и инженерия и введение, 7-е изд., John Wiley and Sons, Inc., 2007: стр. 38–73.
- М. Апулия, Что определяет благородство сплава Дерингер-Ней?, (2020) 1–2.
- Киттель, Чарльз, 1 Кристаллическая структура, в: Введение в физику твердого тела, 8-е изд., John Wiley & Sons, 2005: стр. 1–22.
Важные типы решетчатых структур
Важными решетчатыми структурами являются гранецентрированная кубическая (ГЦК), объемноцентрированная кубическая (ОЦК) и гексагональная плотнейшая упаковка (ГПУ).
- 1 Введение
- 2 Объемно-центрированная кубическая решетка
- 3 Гексагональная плотнейшая решетчатая структура
- 4 Структура гранецентрированной кубической решетки
Введение
В статье о структуре решетки металлов объясняется, почему атомы в металле расположены с определенной регулярностью и, таким образом, образуют структуру решетки.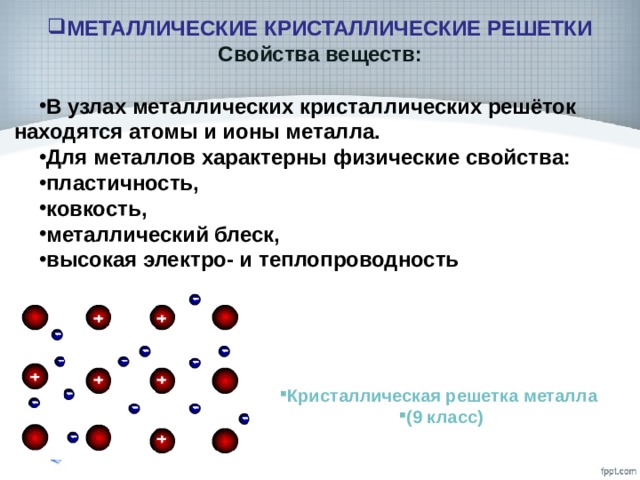 Только в редких случаях появляется простая кубическая кристаллическая структура, как показано на анимации ниже.
Только в редких случаях появляется простая кубическая кристаллическая структура, как показано на анимации ниже.
Гораздо большее техническое значение имеют варианты этой простой структуры кубической решетки. К ним относятся объемно-центрированная кубическая решетка (ОЦК) и гранецентрированная кубическая решетка (ГЦК), а также гексагональная плотноупакованная решетка (ГПУ).
Различия в структуре решетки особенно сильно влияют на пластичность соответствующих металлов! В то время как ГЦК-решетка демонстрирует наибольшую пластичность, а ГПУ-решетка наименьшую деформируемость, ОЦК-решетка обладает пластичностью, которая находится между другими структурами.
Рисунок: Важные решетчатые структуры металлов Чтобы иметь возможность понять эти различия в пластичности, сначала необходимо понять структуру различных типов решетки. По этой причине в этой статье обсуждается реализация трех наиболее важных типов решеток.
Объемно-центрированная кубическая решетка
Разновидностью примитивной кубической решетки является так называемая объемно-центрированная кубическая решетка (ОЦК). В этой атомной структуре отдельные плоскости атомов (плоскость решетки) лежат в промежутках соответствующих нижних плоскостей атомов. Как и в случае с примитивной кубической решеткой, элементарная ячейка также имеет базовую форму куба. В дополнение к угловым атомам, каждый из которых расположен в углах элементарной ячейки кубической формы, теперь есть еще один атом с центром в середине куба («тело»).
Структура объемно-центрированной кубической решетки (ОЦК) содержит еще один атом в середине кубической элементарной ячейки рядом с угловыми атомами!
Рисунок: Структура объемно-центрированной кубической (ОЦК) решетки (элементарная ячейка)Типичными представителями таких объемно-центрированных кубических структур являются металлы железо, хром, молибден, ванадий и вольфрам.
В объемно-центрированном кубическом кристалле один атом находится в непосредственном контакте с восемью окружающими атомами. Это число непосредственных соседних атомов также называют 9.0011 координационный номер . Следовательно, координационное число в ОЦК-решетке равно 8. С другой стороны, в простой кубической решетке получается координационное число 6.
Это число непосредственных соседних атомов также называют 9.0011 координационный номер . Следовательно, координационное число в ОЦК-решетке равно 8. С другой стороны, в простой кубической решетке получается координационное число 6.
Координационное число описывает количество непосредственно соседних атомов!
Для изображения элементарных ячеек имеет смысл изображать атомы в уменьшенном размере, даже если в действительности они «соприкасаются». Для пояснения пространственного расположения атомов также принято указывать основную форму элементарной ячейки штрихами. Обратите внимание, что эти линии не представляют силы связывания!
Рисунок: Объемно-центрированная кубическая элементарная ячейка (ОЦК) Если реально рассматривать атомы как соприкасающиеся сферы, можно определить так называемую плотность упаковки атомной структуры (также называемую коэффициентом упаковки ). Плотность упаковки показывает, какой процент элементарной ячейки заполнен атомами. Таким образом, для объемно-центрированной кубической решетки можно определить плотность упаковки 0,68. Это означает, что 68 % всего объема решетки (или элементарной ячейки) занято атомами. Остальные 32 % приходятся на «щели» между атомами. Вывод этой плотности упаковки показан в отдельном посте.
Таким образом, для объемно-центрированной кубической решетки можно определить плотность упаковки 0,68. Это означает, что 68 % всего объема решетки (или элементарной ячейки) занято атомами. Остальные 32 % приходятся на «щели» между атомами. Вывод этой плотности упаковки показан в отдельном посте.
Плотность упаковки (или коэффициент упаковки) — это отношение атомного объема к общему объему элементарной ячейки!
Рисунок: Получение плотности упаковки объемно-центрированной кубической решетки (ОЦК)Гексагональная плотнейшая решетчатая структура
В объемно-центрированной кубической кристаллической структуре наложенные друг на друга атомные плоскости имеют зазоры, так что соответствующая нижележащая плоскость точно соответствует в щели верхнего. Таким образом, атомные уровни не максимально упакованы. Иначе обстоит дело с гексагональной структурой решетки.
В гексагональной структуре атомы плоскости решетки плотно упакованы вместе. Отдельный атом в этой плоскости решетки A (показанной красным) всегда соприкасается с шестью соседними атомами. Вышележащая атомная плоскость B (показана синим цветом) устроена в принципе идентично. Однако оно сдвинуто настолько, что атомы этой плоскости точно укладываются в углубление нижележащей плоскости. Таким образом, атом верхней плоскости решетки находится в зазоре, образованном тремя атомами нижнего слоя. Эта последовательность плоскостей решетки AB (также называемая последовательность суммирования ) теперь повторяется непрерывно (ABAB …).
Вышележащая атомная плоскость B (показана синим цветом) устроена в принципе идентично. Однако оно сдвинуто настолько, что атомы этой плоскости точно укладываются в углубление нижележащей плоскости. Таким образом, атом верхней плоскости решетки находится в зазоре, образованном тремя атомами нижнего слоя. Эта последовательность плоскостей решетки AB (также называемая последовательность суммирования ) теперь повторяется непрерывно (ABAB …).
Последовательность наложения – это порядок постоянно повторяющихся слоев атомов!
Рисунок: Гексагональная плотно упакованная (ГПУ) структура решетки (элементарная ячейка)Металлы титан, кобальт, цинк и магний обычно встречаются в такой гексагональной структуре решетки с максимальной плотностью упаковки. Атом в гексагональной наиболее плотно упакованной решетке окружен 12 непосредственными соседними атомами. Таким образом, координационное число в решетке этого типа равно 12,9.0007
Элементарная ячейка гексагональной плотно упакованной решетки может быть уменьшена до гексагональной базовой области. В середине элементарной ячейки находятся три других атома, которые располагаются в образующихся атомных промежутках базовой и верхней поверхностей. Поскольку отдельные атомные уровни, составляющие структуру, максимально упакованы, мы также говорим о наиболее плотно упакованных атомных плоскостях. Следовательно, решетка называется гексагональной плотноупакованной решеточной структурой (ГПУ).
В середине элементарной ячейки находятся три других атома, которые располагаются в образующихся атомных промежутках базовой и верхней поверхностей. Поскольку отдельные атомные уровни, составляющие структуру, максимально упакованы, мы также говорим о наиболее плотно упакованных атомных плоскостях. Следовательно, решетка называется гексагональной плотноупакованной решеточной структурой (ГПУ).
В гексагональной плотно упакованной решетке два атомных слоя с гексагональным основанием образуют форму элементарной ячейки. В середине базовых областей находится еще один атом, а также всего три других атома в середине элементарной ячейки!
Рисунок: Гексагональная плотно упакованная элементарная ячейка (ГПУ)Плотность упаковки ГПУ-решетки соответствует максимально возможной плотности упаковки 74 %. Эта максимальная плотность упаковки обычно применима к любому сферическому телу.
Для сферических тел максимальная плотность упаковки может достигать 74 %!
Добавление слова «наиболее плотная упаковка» к названию гексагональной решетки уже подразумевает, что существуют и другие структуры гексагональной решетки. Например, графит также имеет гексагональную структуру решетки (гекс), но она не плотно упакована, как в ГПУ-решетке.
Например, графит также имеет гексагональную структуру решетки (гекс), но она не плотно упакована, как в ГПУ-решетке.
В то время как в атомной плоскости ГПУ-решетки атом непосредственно окружен 6 другими атомами, в гексагональной решетке графита есть только три соседних атома. Отдельные атомные слои расположены со смещением и могут относительно легко смещаться относительно друг друга. Таким образом, сдвинутые атомные плоскости могут быть относительно легко отделены. Например, в этом процессе используется графитный карандаш при рисовании на листе бумаги.
Рисунок: Решетчатая структура графитаГранецентрированная кубическая решетчатая структура
Как и гпу-решетка, гранецентрированная кубическая решетка (ГЦК) имеет максимально упакованные атомные плоскости. Однако порядок укладки другой. Вторая плоскость решетки первоначально укладывается так же, как и в ГПУ-решетке, и располагается в зазорах нижележащего слоя. Однако в отличие от ГПУ-структуры третий атомный слой располагается в «свободных» промежутках. Соответственно, последовательность укладки наиболее плотно упакованных плоскостей приводит к ряду ABCABC …
Соответственно, последовательность укладки наиболее плотно упакованных плоскостей приводит к ряду ABCABC …
Типичными металлами с гранецентрированной кубической структурой решетки являются алюминий, свинец, медь и никель. Как и в ГПУ-решетке, атом в ГЦК-решетке имеет 12 соседних атомов. Координационное число, таким образом, также равно 12.
В гранецентрированной кубической решетке основная форма элементарной ячейки не является гексагональной, как можно предположить по ее структуре, аналогичной гексагональной решетке. Элементарная ячейка на самом деле имеет форму куба и поэтому является одной из кубических кристаллических систем 9.0014 ! Что касается выровненных по горизонтали ближайших упакованных плоскостей, элементарная ячейка стоит на углу куба. Приведенная выше аномалия показывает, что помимо атомов в углу куба, другие атомы сосредоточены на поверхностях куба. Поэтому этот тип решетки называется гранецентрированной .