Твердость особенность строения кристаллической решетки металла: Твёрдость — определение
alexxlab | 02.12.2022 | 0 | Разное
Кристаллическое строение металлов. Кристаллическая решетка металлов
Одним из самых распространенных материалов, с которым всегда предпочитали работать люди, был металл. В каждую эпоху предпочтение отдавалось разным видам этих удивительных веществ. Так, IV-III тысячелетия до нашей эры считаются веком хальколита, или медным. Позже его сменяет бронзовый, а затем в силу вступает тот, что и по сей день является актуальным – железный.
Сегодня вообще сложно представить, что когда-то можно было обходиться без металлических изделий, ведь практически все, начиная от предметов быта, медицинских инструментов и заканчивая тяжелой и легкой техникой, состоит из этого материала или включает в свой состав отдельные части из него. Почему же металлы сумели завоевать такую популярность? В чем проявляются особенности и как это заложено в их строении, попробуем разобраться далее.
Общее понятие о металлах
“Химия. 9 класс” – это учебник, по которому проходят обучение школьники. Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Именно с этого возраста рекомендуют давать детям представление о данных атомах и их свойствах, ведь подростки уже вполне могут оценить значение подобных знаний. Они прекрасно видят, что окружающее их разнообразие предметов, машин и прочих вещей имеет в своей основе как раз металлическую природу.
Что же такое металл? С точки зрения химии, к данным атомам принято относить те, что имеют:
- малое число электронов на внешнем уровне;
- проявляют сильные восстановительные свойства;
- имеют большой атомный радиус;
- как простые вещества обладают рядом специфических физических свойств.
Основу знаний об этих веществах можно получить, если рассмотреть атомно-кристаллическое строение металлов. Именно оно объясняет все особенности и свойства данных соединений.
В периодической системе для металлов отводится большая часть всей таблицы, ведь они образуют все побочные подгруппы и главные с первой по третью группу.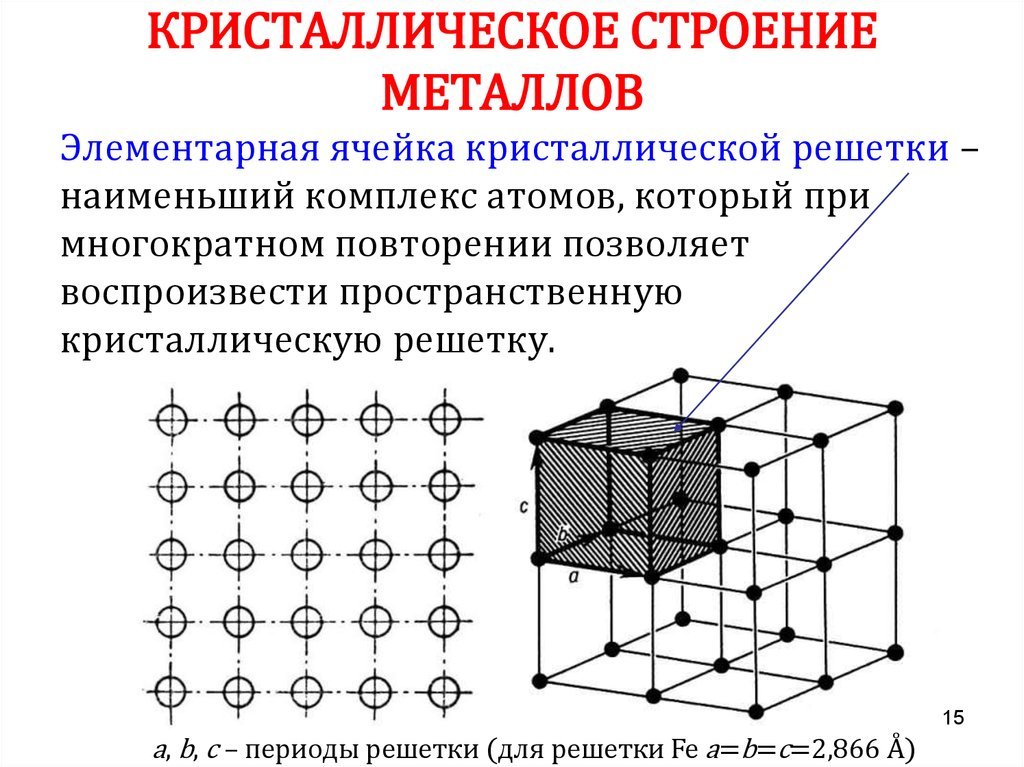 Поэтому их численное превосходство очевидно. Самыми распространенными являются:
Поэтому их численное превосходство очевидно. Самыми распространенными являются:
- кальций;
- натрий;
- титан;
- железо;
- магний;
- алюминий;
- калий.
Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет именно кристаллическое строение металлов.
Свойства металлов
К специфическим свойствам рассматриваемых веществ относят следующие.
- Металлический блеск. Все представители простых веществ им обладают, причем большинство одинаковым серебристо-белым цветом. Лишь некоторые (золото, медь, сплавы) отличаются.
- Ковкость и пластичность – способность деформироваться и восстанавливаться достаточно легко. У разных представителей выражена в неодинаковой мере.
- Электропроводность и теплопроводность – одно из основных свойств, которое определяет области применения металла и его сплавов.
Кристаллическое строение металлов и сплавов объясняет причину каждого из обозначенных свойств и говорит о выраженности их у каждого конкретного представителя.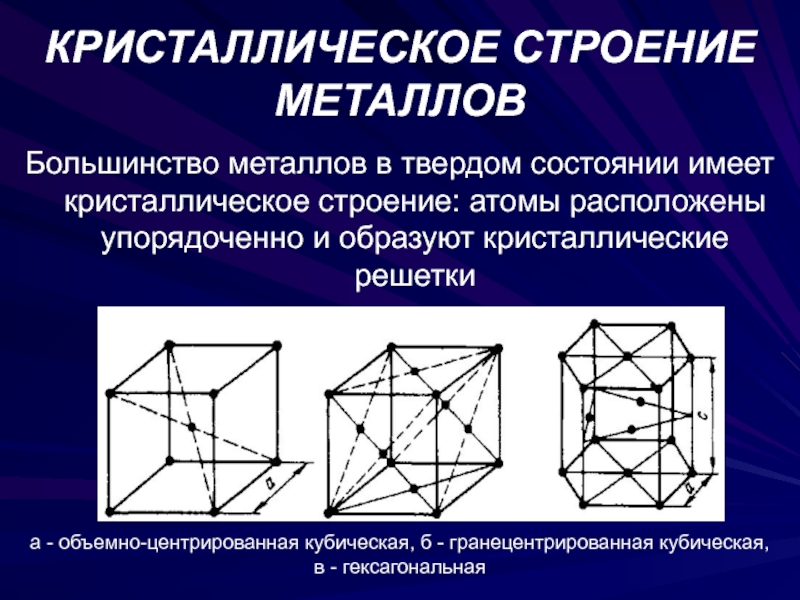 Если знать особенности такого строения, то можно влиять на свойства образца и подстраивать его под нужные параметры, что и делают люди уже многие десятилетия.
Если знать особенности такого строения, то можно влиять на свойства образца и подстраивать его под нужные параметры, что и делают люди уже многие десятилетия.
Атомно-кристаллическое строение металлов
В чем же заключается такое строение, чем характеризуется? Само название говорит о том, что все металлы представляют собой кристаллы в твердом состоянии, то есть при обычных условиях (кроме ртути, которая является жидкостью). А что такое кристалл?
Это условное графическое изображение, построенное путем пересечения воображаемых линий через атомы, которые выстраивают тело. Другими словами, каждый металл состоит из атомов. Они располагаются в нем не хаотично, а очень правильно и последовательно. Так вот, если мысленно соединить все эти частицы в одну структуру, то получится красивое изображение в виде правильного геометрического тела какой-либо формы.
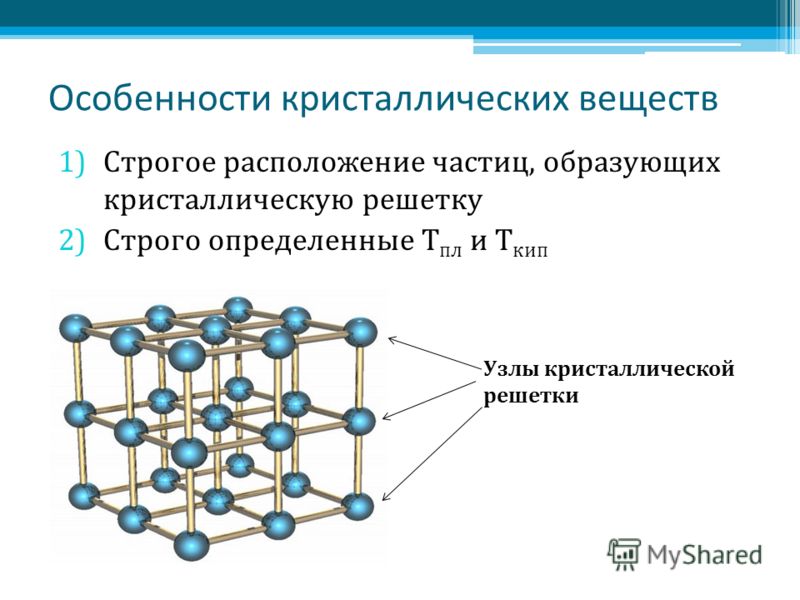
Это и принято называть кристаллической решеткой металла. Она очень сложная и пространственно объемная, поэтому для упрощения показывают не всю ее, а лишь часть, элементарную ячейку.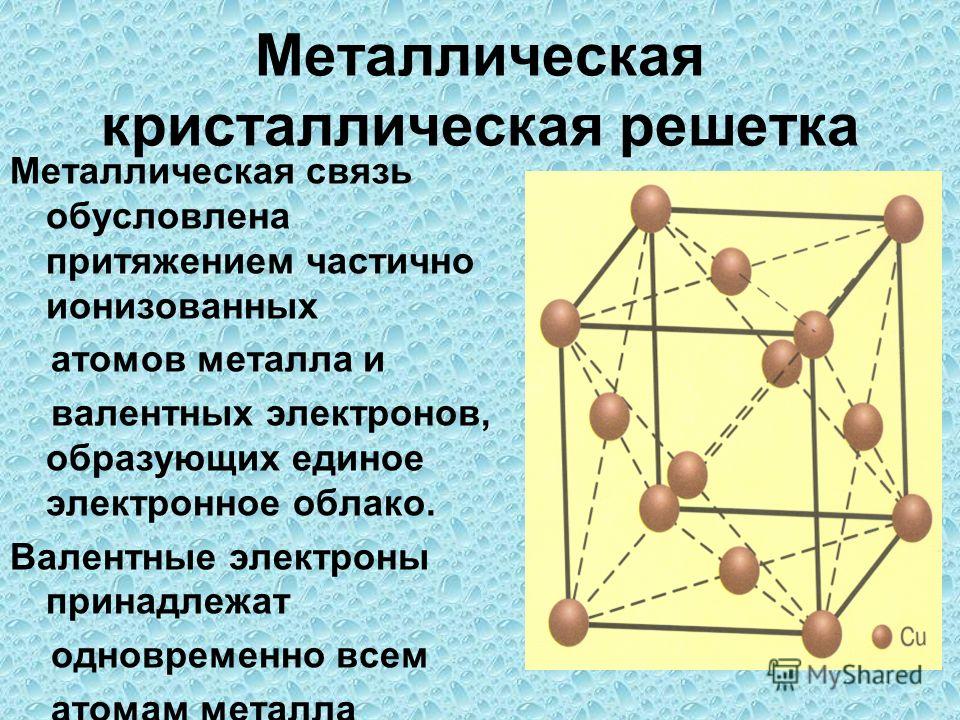 Совокупность таких ячеек, собранная вместе и отраженная в трехмерном пространстве, и образует кристаллические решетки. Химия, физика и металловедение – это науки, которые занимаются изучением особенностей строения таких структур.
Совокупность таких ячеек, собранная вместе и отраженная в трехмерном пространстве, и образует кристаллические решетки. Химия, физика и металловедение – это науки, которые занимаются изучением особенностей строения таких структур.
Сама элементарная ячейка – это набор атомов, которые располагаются на определенном расстоянии друг от друга и координируют вокруг себя строго фиксированное число других частиц. Она характеризуется плотностью упаковки, расстоянием между составными структурами, координационным числом. В целом все эти параметры являются характеристикой и всего кристалла, а значит, отражают и проявляемые металлом свойства.
Существует несколько разновидностей кристаллических решеток. Объединяет их все одна особенность – в узлах находятся атомы, а внутри располагается облако электронного газа, которое формируется путем свободного передвижения электронов внутри кристалла.
Типы кристаллических решеток
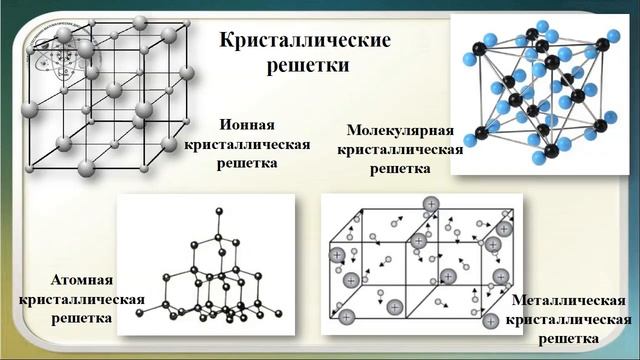
Четырнадцать вариантов строения решетки принято объединять в три основных типа.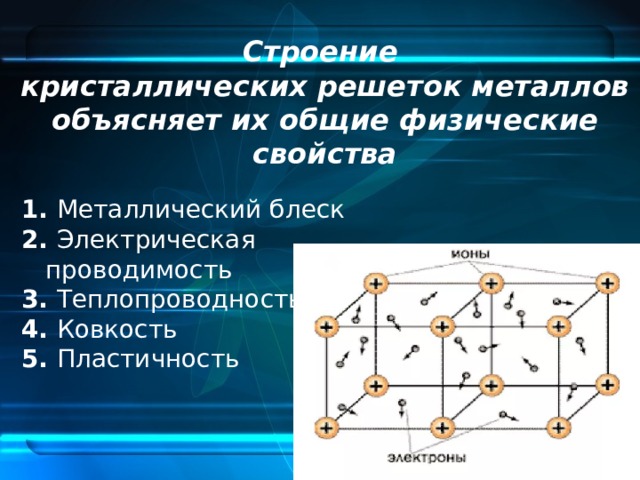 Они следующие:
Они следующие:
- Объемно-центрированная кубическая.
- Гексагональная плотноупакованная.
- Гранецентрированная кубическая.
Кристаллическое строение металлов было изучено только благодаря электронной микроскопии, когда стало возможным получать большие увеличения изображений. А классификацию типов решеток впервые привел французский ученый Браве, по фамилии которого их иногда называют.
Объемно-центрированная решетка
Строение кристаллической решетки металлов данного типа представляет собой следующую структуру. Это куб, в узлах которого находится восемь атомов. Еще один располагается в центре свободного внутреннего пространства ячейки, что и объясняет название “объемно-центрированная”.
Это один из вариантов наиболее простого строения элементарной ячейки, а значит, и всей решетки в целом. Такой тип имеют следующие металлы:
- молибден;
- ванадий;
- хром;
- марганец;
- альфа-железо;
- бетта-железо и другие.

Основные свойства таких представителей – высокая степень ковкости и пластичности, твердость и прочность.
Гранецентрированная решетка
Кристаллическое строение металлов, имеющих гранецентрированную кубическую решетку, представляет собой следующую структуру. Это куб, который включает в свой состав четырнадцать атомов. Восемь из них формируют узлы решетки, а еще шесть расположены по одному на каждой грани.
Подобную структуру имеют:
- алюминий;
- никель;
- свинец;
- гамма-железо;
- медь.
Основные отличительные свойства – блеск разного цвета, легкость, прочность, ковкость, повышенная устойчивость к коррозии.
Гексагональная решетка
Кристаллическое строение металлов, обладающих данным типом решетки, следующее. В основе элементарной ячейки лежит шестигранная призма. В ее узлах располагается 12 атомов, еще два по основаниям и три атома свободно лежат внутри пространства в центре структуры. Всего семнадцать атомов.
Подобную сложную конфигурацию имеют такие металлы, как:
- альфа-титан;
- магний;
- альфа-кобальт;
- цинк.
Основные свойства – высокая степень прочности, сильный серебристый блеск.
Дефекты кристаллического строения металлов
Однако все рассмотренные типы ячеек могут иметь и естественные недостатки, или так называемые дефекты. Это может быть связано с разными причинами: посторонними атомами и примесями в металлах, внешними воздействиями и прочим.
Поэтому существует классификация, отражающая дефекты, которые могут иметь кристаллические решетки. Химия как наука изучает каждый из них с целью выявления причины и способа устранения, чтобы свойства материала не были изменены. Итак, дефекты следующие.
- Точечные. Они бывают трех основных видов: вакансии, примеси или дислоцированные атомы. Приводят к ухудшению магнитных свойств металла, электро- и теплопроводности его.
- Линейные, или дислокационные. Выделяют краевые и винтовые.
 Ухудшают прочность и качество материала.
Ухудшают прочность и качество материала. - Поверхностные дефекты. Влияют на внешний вид и структуру металлов.
В настоящее время разработаны методики устранения дефектов и получения чистых кристаллов. Однако совсем искоренить их не удается, идеальной кристаллической решетки не существует.
Значение знаний о кристаллическом строении металлов
Из вышеизложенного материала очевидно, что знания о тонкой структуре и строении позволяют спрогнозировать свойства материала и повлиять на них. И это позволяет делать наука химия. 9 класс общеобразовательной школы делает в процессе обучения упор на то, чтобы сформировать у учащихся четкое понятие о важном значении основополагающей логической цепочки: состав – строение – свойства – применение.
Сведения о кристаллическом строении металлов очень четко иллюстрирует эту зависимость и позволяет учителю наглядно объяснить и показать детям, насколько важно знать тонкую структуру, чтобы правильно и грамотно использовать все свойства.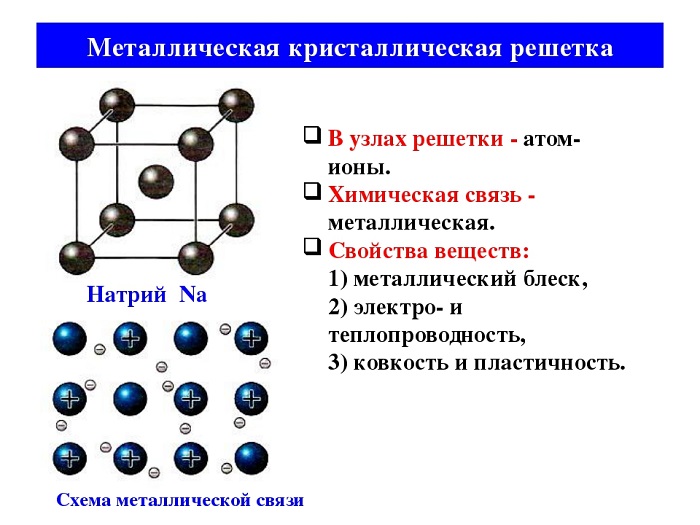
Белорусский государственный университет транспорта – БелГУТ (БИИЖТ)
Регистрация на конференцию ИТЭС
Регистрация на конференцию «Актуальные проблемы теории и практики современной науки»
Регистрация на конференцию «Архитектура и строительство: традиции и инновации»
Как поступить в БелГУТ
Как получить место
в общежитии БелГУТа
Как поступить иностранному гражданину
События
Все события
| Пн | Вт | Ср | Чт | Пт | Сб | Вс |
|---|---|---|---|---|---|---|
1 | 2 | 3 | 4 | 5 Дата : 2022-11-05 | 6 Дата : 2022-11-06 | |
7 | 8 Дата : 2022-11-08 | 9 | 10 | 11 | 12 Дата : 2022-11-12 | 13 |
14 | 15 | 16 Дата : 2022-11-16 | 17 Дата : 2022-11-17 | 18 | 19 Дата : 2022-11-19 | 20 |
21 Дата : 2022-11-21 | 22 | 23 | 24 Дата : 2022-11-24 | 25 Дата : 2022-11-25 | 26 Дата : 2022-11-26 | 27 |
28 Дата : 2022-11-28 | 29 | 30 | ||||
Все анонсы
- Киберспортивный турнир по CS:GO.
 ..
.. - 3 декабря – ДЕНЬ ОТКРЫТЫХ ДВЕРЕЙ ФАКУЛЬТЕТА УПП…
- Экспозиция «85-летний юбилей архитектора МАЛКОВА И…
- Лига брейн-ринга в БелГУТе
- Набор в хор БелГУТа
- V Международная научно-практическая конференция ст…
- I международная научно-техническая конференция сту…
- Набор в Студенческий совет БелГУТа …
- Кастинг видеоблогеров, теле- и радиоведущих…
- Билеты на премьерный спектакль «451° по Фаренгейту…
Анонсы
Университет
Абитуриентам
Студентам
Конференции
Приглашения
Киберспортивный турнир по CS:GO…
3 декабря – ДЕНЬ ОТКРЫТЫХ ДВЕРЕЙ ФАКУЛЬТЕТА УПП…
Экспозиция «85-летний юбилей архитектора МАЛКОВА И…
Лига брейн-ринга в БелГУТе
Новости
Университет
Международные связи
Спорт
Воспитательная работа
Жизнь студентов
Новости подразделений
- Университет
Выставки научно-технической библиотеки в рамках ХII Международной науч. ..
..
29 ноября 2022
- Университет
Победа в Республиканской викторине «Я хочу быть таможенником»…
29 ноября 2022
- Воспитательная работа
Строки, опаленные войной
29 ноября 2022
- Университет
Благодарность за большой вклад в развитие студенческих отрядов…
29 ноября 2022
- Университет
Новый номер газеты «Вести БелГУТа»
29 ноября 2022
- Университет
Секция 9. Работа ХII Международной научно-практической конференции «Пр…
29 ноября 2022
- Университет
Секция 8. Работа ХII Международной научно-практической конференции «Пр…
Работа ХII Международной научно-практической конференции «Пр…
28 ноября 2022
- Университет
БелГУТ среди лучших в лекторском мастерстве!…
28 ноября 2022
- Спорт
Финал соревнований по мини-футболу
28 ноября 2022
Другие новости
- Студенческий совет БелГУТа на I Форуме студенческих советов Гомельской…
- Профориентационная работа в Гомельском и Брестском колледжах…
- 79 лет освобождения Гомеля. Митинг у Вечного огня…
- Молодежь БелГУТа и СамГУПСа – обмен опытом…
- Активисты БРСМ БелГУТа на открытом диалоге «Нам мир завещано беречь»…
- Митинг в Гомельском колледже-филиале БелГУТа…
- Круглый стол «Об изменениях Закона Республики Беларусь «О железнодорож…
- Митинг на «Аллее героев»
- Работа секции № 5 «Безопасность транспортной инфраструктуры».
 ..
.. - Работа секции № 6 «Надежность и безопасность зданий и сооружений»…
- XII Международная научно-практическая конференция «Проблемы безопаснос…
КУДА ПОСТУПАТЬ
Все факультеты
БелГУТ на Доске почета
Достижения университета
Предложения
Все предложения
Видеотека
Все видео
Фотогалерея
Все фото
Кристаллические структуры термообработанной стали | L&L печь
28 июля 2021 г.
Красота и элегантность термообработанной стали не ограничиваются поверхностью металла; их также можно увидеть в сложных кристаллических структурах, которые придают металлу его отличительные характеристики.
В этой статье мы рассмотрим природу кристаллической структуры стали, а также свойства, которые обнаруживаются в различных видах стали после термической обработки.
Понимание кристаллических структур стали В твердом состоянии металлы состоят из кристаллизованных решетчатых структур, которые обычно называют в более общем смысле «кристаллической структурой» металла.
Атомы, составляющие эту особую кристаллическую структуру, могут различаться, хотя нержавеющая сталь преимущественно состоит из атомов железа, а также некоторого количества углерода и небольшого количества других металлов в зависимости от типа.
Стальные кристаллические структуры впервые появляются при затвердевании. В своей жидкой форме железо вообще не является кристаллическим. Однако по мере того, как расплавленный металл начинает остывать, постепенно начинают формироваться кристаллы.
Поскольку металл подвергается нескольким температурным стадиям, образуются различные типы кристаллов. Таким образом, готовая сталь будет содержать следовые количества феррита, аустенита и цементита.
Что делает кристаллические структуры стали такими отличными друг от друга? Эти структуры будут различаться в зависимости от количества углерода, которое они могут поглотить.
Ферритная сталь Ферритные кристаллические структуры содержат лишь небольшое количество углерода, примерно 0,025%. Это делает ферритную сталь чрезвычайно мягкой и пластичной, хотя отсутствие углерода также означает, что ферритная сталь имеет низкую коррозионную стойкость.
Это делает ферритную сталь чрезвычайно мягкой и пластичной, хотя отсутствие углерода также означает, что ферритная сталь имеет низкую коррозионную стойкость.
Кроме того, ферритная сталь имеет среднюю прочность, что означает, что ее не рекомендуется использовать в условиях высоких температур.
Свойства ферритной сталиПричина того, что ферритная сталь поглощает так мало углерода, заключается в ограничениях геометрии ее кристаллической структуры. Кристаллическая структура ферритной стали характеризуется расположением в форме куба, в котором атомы железа размещены в каждом углу и один в центре. Именно такое расположение придает ферритной стали характерные магнитные свойства.
Использование ферритной стали Поскольку это не самая прочная форма стали, ферритная сталь не находит широкого применения. Однако в некоторых случаях ферритную сталь можно комбинировать с другими элементами (например, хромом) для повышения ее долговечности и коррозионной стойкости.
Ферритная сталь нередко используется в следующих областях:
- Автомобильные выхлопные системы
- Пищевое оборудование и приборы
- Теплообменники
- Бытовая техника
В более крупных приложениях используются другие формы стали для большей долговечности.
Аустенитная стальАустенит — это форма железа, которая может поглощать больше углерода, чем феррит. Аустенит можно получить из феррита, подвергая его воздействию экстремальных температур (1000 °C и более), что позволит его объемно-центрированной кубической кристаллической структуре перейти в гранецентрированную структуру.
Свойства аустенитаЭти гранецентрированные кристаллические структуры стали позволяют аустениту поглощать до 2% углерода, что значительно больше, чем ферритная сталь.
К сожалению, при охлаждении аустенит снова принимает свою ферритную форму. Однако сталь можно заставить сохранить свою структуру путем добавления дополнительных металлов, таких как никель и марганец. Это обеспечивает сохранение аустенитом своей структуры и свойств даже при низких температурах.
Это обеспечивает сохранение аустенитом своей структуры и свойств даже при низких температурах.
Аустенитная сталь легче поддается сварке, чем другие виды стали. Это делает аустенит немного более универсальным и доступным, поскольку различные куски стали можно изготавливать отдельно, а затем сваривать вместе.
Использование аустенитаИз-за долговечности аустенита это одна из наиболее часто используемых форм нержавеющей стали.
Металл в ваших винтах из нержавеющей стали или другом оборудовании почти всегда представляет собой форму аустенита. Этот металл используется из-за его относительной прочности и высокой устойчивости к коррозии.
Устойчивость к коррозии также делает аустенит идеальным выбором для пищевой, фармацевтической и нефтехимической промышленности. Некоторые виды мебели также могут быть изготовлены из аустенитной стали. Эту сталь можно использовать даже для некоторых видов металлоконструкций.
Мартенситная сталь При быстрой закалке высокотемпературного аустенита атомы углерода захватываются кристаллическими структурами стали. При этом образуется мартенсит.
При этом образуется мартенсит.
Кристаллическая структура стали в мартенсите содержит относительно большое количество углерода, что делает этот металл чрезвычайно прочным и устойчивым к разрушению. Низкая пластичность (способность изгибаться или скручиваться в проволоку) также делает эту сталь прочной и долговечной.
Кроме того, мартенсит можно выдерживать при относительно низких температурах в течение различных периодов времени в процессе, называемом отпуском. Закалка снижает прочность, повышая ударную вязкость и пластичность. Это позволяет обрабатывать мартенсит и адаптировать его для самых разных применений.
Использование мартенсита Поскольку мартенсит настолько стабилен и прочен, он является идеальным материалом для столовых приборов, ножей и других высококачественных кухонных принадлежностей. Но помимо кухни мартенсит также находит применение в области медицины, а также в аэрокосмической промышленности.
Точное применение мартенситной стали будет зависеть от содержания углерода, полученного в ходе металлургического процесса.
Нержавеющая сталь типа 410 может быть универсальным материалом, который хорошо подходит для изготовления скобяных изделий, деталей оружия, лопаток турбин и деталей машин. Нержавеющая сталь типа 440 обладает большей твердостью, что может быть идеальным для лезвий, поскольку их не придется часто затачивать. Вы можете найти сталь типа 440 в кухонных столовых приборах и медицинских инструментах.
ЗаключениеКонфигурация кристаллических структур стали влияет на способность металла поглощать углерод. Это оказывает большое влияние на общее качество и долговечность готового продукта.
Наиболее распространенные формы кристаллической структуры стали включают ферритную, аустенитную и мартенситную сталь, хотя аустенитная и мартенситная сталь имеют более широкий спектр применения из-за их более высокой прочности и долговечности.
L&L Special Furnace Co. разбирается в химических и механических процессах, связанных с термообработанной сталью. Мы гордимся своей давней репутацией, когда речь идет о промышленных печах, печах, сушильных камерах, закалочных емкостях и других системах термообработки.
Мы стремимся к инновациям и качеству изготовления. Вы можете найти наши предприятия, расположенные к югу от Филадельфии, штат Пенсильвания, хотя мы обеспечиваем продажу и обслуживание оборудования по всему миру.
Свяжитесь с нами для ваших потребностей в термообработке, и мы можем сотрудничать с вами, чтобы предоставить доступное и надежное обслуживание.
Структура и свойства керамики
Как и в любом материале, свойства керамики определяются типами присутствующих атомов, типами связи между атомами и способом упаковки атомов вместе
Два типа связей встречаются в керамике: ионные и ковалентные. Ионная связь возникает между металлом и неметаллом, другими словами, между двумя элементами с очень разной электроотрицательностью. Электроотрицательность — это способность ядра в атоме притягивать и удерживать все электроны внутри самого атома и зависит от количества электронов и расстояния между электронами во внешних оболочках и ядром.
Ионная связь возникает между металлом и неметаллом, другими словами, между двумя элементами с очень разной электроотрицательностью. Электроотрицательность — это способность ядра в атоме притягивать и удерживать все электроны внутри самого атома и зависит от количества электронов и расстояния между электронами во внешних оболочках и ядром.
При ионной связи один из атомов (металл) передает электроны другому атому (неметаллу), становясь таким образом положительно заряженным (катион), тогда как неметалл становится отрицательно заряженным (анион). Два иона с противоположными зарядами притягиваются друг к другу с большой электростатической силой.
Вместо этого ковалентная связь возникает между двумя неметаллами, другими словами, между двумя атомами, которые имеют одинаковую электроотрицательность, и включает в себя общие электронные пары между двумя атомами.
Хотя в керамических материалах между атомами возникают оба типа связей, в большинстве из них (особенно в оксидах) преобладает ионная связь.
Есть еще два типа атомных связей: металлические и ван-дер-ваальсовые. В первом катионы металлов окружены электронами, которые могут свободно перемещаться между атомами. Металлические связи не так прочны, как ионные и ковалентные связи. Металлические связи отвечают за основные свойства металлов, такие как пластичность, когда металл можно легко сгибать или растягивать, не ломая, что позволяет вытягивать его в проволоку. Свободное движение электронов также объясняет, почему металлы имеют тенденцию быть проводниками электричества и тепла.
Связи Ван-дер-Ваальса состоят из слабых электростатических сил между атомами, имеющими постоянную или индуцированную поляризацию. Примером связи Ван-дер-Ваальса является водородная связь между водородом и кислородом, которая отвечает за многие свойства воды.
В полимерах существуют ковалентные связи между атомами полимера, но полимерные макромолекулы (или цепи) удерживаются вместе силами Ван-дер-Ваальса. Из всех четырех типов связей Ван-дер-Ваальса является самой слабой.
Ионные и ковалентные связи керамики обусловливают многие уникальные свойства этих материалов, такие как высокая твердость, высокие температуры плавления, низкое тепловое расширение и хорошая химическая стойкость, а также некоторые нежелательные характеристики, прежде всего хрупкость, которая приводит к трещинам, если только материал не упрочнен армирующими добавками или другими средствами.
Однако свойства керамики также зависят от ее микроструктуры. Керамика по определению является природным или синтетическим неорганическим, неметаллическим, поликристаллическим материалом. Иногда даже монокристаллические материалы, такие как алмаз и сапфир, ошибочно включаются в понятие 9.0147 керамика
. Поликристаллические материалы образуются из нескольких кристаллических зерен, соединенных вместе в процессе производства, тогда как монокристаллические материалы выращиваются как один трехмерный кристалл. Процессы изготовления поликристаллических материалов относительно недороги по сравнению с монокристаллами. Из-за этих различий (например, множественные кристаллы с различной ориентацией, наличие границ зерен, процессы изготовления) поликристаллические материалы действительно не следует путать с монокристаллами, и они должны быть единственными, подпадающими под определение 9.0147 керамика . На свойства и обработку керамики в значительной степени влияют размер и форма ее зерен, а такие характеристики, как плотность, твердость, механическая прочность и оптические свойства, сильно коррелируют с микроструктурой спеченного изделия.
Процессы изготовления поликристаллических материалов относительно недороги по сравнению с монокристаллами. Из-за этих различий (например, множественные кристаллы с различной ориентацией, наличие границ зерен, процессы изготовления) поликристаллические материалы действительно не следует путать с монокристаллами, и они должны быть единственными, подпадающими под определение 9.0147 керамика . На свойства и обработку керамики в значительной степени влияют размер и форма ее зерен, а такие характеристики, как плотность, твердость, механическая прочность и оптические свойства, сильно коррелируют с микроструктурой спеченного изделия. С другой стороны, стекло изготовлено из неорганических, неметаллических материалов с аморфной структурой. Аморфная структура означает, что атомы не организованы в соответствии с хорошо упорядоченным повторяющимся расположением, как в кристаллах. Стеклокерамика состоит из мелких зерен, окруженных стеклообразной фазой, и имеет свойства, промежуточные между стеклом и керамикой.


 Ухудшают прочность и качество материала.
Ухудшают прочность и качество материала.