Углерод железо – – —
alexxlab | 30.11.2019 | 0 | Разное
Диаграмма состояния сплавов железо-углерод — Википедия. Что такое Диаграмма состояния сплавов железо-углерод
Диагра́мма фа́зового равнове́сия (диаграмма состоя́ния) желе́зо—углеро́д (иногда эту диаграмму называют «диаграмма железо—цементит») — графическое отображение фазового состояния сплавов железа с углеродом в зависимости от их химического состава и температуры.
Диаграмма состояния
Железо образует с углеродом химическое соединение Fe3C цементит. Так как на практике применяют металлические сплавы на основе железа с содержанием углерода до 5 %, практически интересна часть диаграммы состояния от чистого железа до цементита[1]. Поскольку цементит — метастабильная фаза, то и соответствующая диаграмма называется метастабильной (сплошные линии на рисунке).
Для серых чугунов и графитизированных сталей рассматривают стабильную часть диаграммы железо—графит (Fe—Гр), поскольку именно графит является в этом случае стабильной фазой. Цементит выделяется из расплава намного быстрее графита и во многих сталях и белых чугунах может существовать достаточно долго, несмотря на метастабильность. В серых чугунах графит существует обязательно.
На рисунке тонкими пунктирными линиями показаны линии стабильного равновесия (то есть с участием графита), там где они отличаются от линий метастабильного равновесия (с участием цементита), а соответствующие точки обозначены штрихом. Обозначения фаз и точек на этой диаграмме приведены согласно неофициальному международному соглашению.
Фазы диаграммы железо-углерод
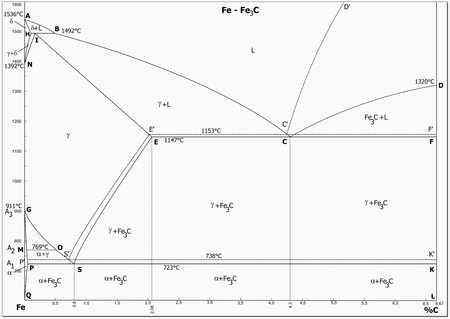 Часть диаграммы состояния сплавов железо-цементит
Часть диаграммы состояния сплавов железо-цементитВ системе железо — углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях[источник не указан 441 день] с образованием однородной жидкой фазы.
Феррит — Твёрдый раствор внедрения углерода в α-железе с объёмно-центрированной кубической решёткой.
Феррит имеет переменную, зависящую от температуры предельную растворимость углерода: минимальную — 0,006 % при комнатной температуре (точка Q), максимальную — 0,02 % при температуре 700 °C (точка P). Атомы углерода располагаются в центре грани или (что кристаллогеометрически эквивалентно) на середине рёбер куба, а также в дефектах решетки [2].
При температуре выше 1392 °C существует высокотемпературный феррит с предельной растворимостью углерода около 0,1 % при температуре около 1500 °C (точка H).
Свойства феррита близки к свойствам чистого железа. Он мягок (твёрдость по Бринеллю — 130 НВ) и пластичен, ферромагнитен (при отсутствии углерода) до точки Кюри — 770 °C.
Аустенит (γ) — твёрдый раствор внедрения углерода в γ-железе с гранецентрированной кубической решёткой.
Атомы углерода занимают место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в аустените — 2,14 % при температуре 1147 °C (точка Е). Аустенит имеет твёрдость 200—250 НВ, пластичен, парамагнитен. При растворении других элементов в аустените или в феррите изменяются свойства и температурные границы их существования
Цементит (Fe3C) — химическое соединение железа с углеродом (карбид железа), со сложной ромбической решёткой, содержит 6,67 % углерода. Он твёрдый (свыше 1000 HВ), и очень хрупкий. Цементит — метастабильная фаза и при длительным нагреве самопроизвольно разлагается с выделением графита.
В железоуглеродистых сплавах цементит как фаза может выделяться при различных условиях:
- цементит первичный (выделяется из жидкости),
- цементит вторичный (выделяется из аустенита),
- цементит третичный (из феррита),
- цементит эвтектический и
- эвтектоидный цементит.
Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зёрен аустенита (после эвтектоидного превращения они станут зёрнами перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зёрен [4].
Эвтектический цементит наблюдается лишь в белых чугунах. Эвтектоидный цементит имеет пластинчатую форму и является составной частью перлита. Цементит может при специальном сфероидизируюшем отжиге или закалке с высоким отпуском выделяться в виде мелких сфер. Влияние на механические свойства сплавов оказывает форма, размер, количество и расположение включений цементита, что позволяет на практике для каждого конкретного применения сплава добиваться оптимального сочетания твёрдости, прочности, стойкости к хрупкому разрушению и т. п.[5]
Графит — фаза состоящая только из углерода со слоистой гексагональной решёткой. Плотность графита (2,3 г/см3) много меньше плотности всех остальных фаз (около 7,5—7,8 г/см3) и это затрудняет и замедляет его образование, что и приводит к выделению цементита при более быстром охлаждении. Образование графита уменьшает усадку при кристаллизации, графит выполняет роль смазки при трении, уменьшая износ, способствует рассеянию энергии вибраций.
Графит имеет форму крупных крабовидных (изогнутых пластинчатых) включений (обычный серый чугун) или сфер (высокопрочный чугун).
Графит обязательно присутствует в серых чугунах и их разновидности — высокопрочных чугунах. Графит присутствует также и в некоторых марках стали — в так называемых графитизированных сталях.
Фазовые переходы
Линия ACD — это линия ликвидуса, показывающая температуры начала затвердевания (конца плавления) сталей и белых чугунов. При температурах выше линии ACD — жидкий сплав. Линия AECF — это линия солидуса, показывающая температуры конца затвердевания (начала плавления).
По линии ликвидуса АС (при температурах, отвечающих линии АС) из жидкого сплава кристаллизуется аустенит, а по линии ликвидуса CD — цементит, называемый первичным цементитом. В точке С при 1147 °С и содержании 4,3 % углерода из жидкого сплава одновременно кристаллизуется аустенит и цементит первичный, образуя эвтектику, называемую ледебуритом. При температурах, соответствующих линии солидуса AE, сплавы с содержанием углерода до 2,14 % окончательно затвердевают с образованием структуры аустенита. На линии солидуса EC (1147° С) сплавы с содержанием углерода от 2,14 до 4,3 % окончательно затвердевают с образованием эвтектики ледебурита. Так как при более высоких температурах из жидкого сплава выделялся аустенит, следовательно, такие сплавы после затвердевания будут иметь структуру аустенит + ледебурит.
На линии солидуса CF (1147 °С) сплавы с содержанием углерода от 4,3 до 6,67 % окончательно затвердевают также с образованием эвтектики ледебурита. Так как при более высоких температурах из жидкого сплава выделялся цементит (первичный), следовательно, такие сплавы после затвердевания будут иметь структуру — первичный цементит + ледебурит
В области ACEA, между линией ликвидуса AC и солидуса AEC, будет жидкий сплав + кристаллы аустенита. В области CDF, между линией ликвидуса CD и солидуса CF, будет жидкий сплав + кристаллы цементита (первичного). Превращения, протекающие при затвердевании сплавов, называют первичной кристаллизацией. В результате первичной кристаллизации во всех сплавах с содержанием углерода до 2,14 % образуется однофазная структура — аустенит. Сплавы железа с углеродом, в которых в результате первичной кристаллизации в равновесных условиях получается аустенитная структура, называют сталями.
Сплавы с содержанием углерода более 2,14 %, в которых при кристаллизации образуется эвтектика ледебурит, называют чугунами. В рассматриваемой системе практически весь углерод находится в связанном состоянии, в виде цементита. Излом таких чугунов светлый, блестящий (белый излом), поэтому такие чугуны называют белыми[4].
В железоуглеродистых сплавах превращения происходят также и в твердом состоянии, называемые вторичной кристаллизацией и характеризуемые линиями GSE, PSK, PQ. Линия GS показывает начало превращения аустенита в феррит (при охлаждении). Следовательно, в области GSP будет структура аустенит + феррит.
Линия SE показывает, что с понижением температуры растворимость углерода в аустените уменьшается. Так, при 1147 °С в аустените может раствориться углерода 2,14 %, а при 727°С — 0,8 %. С понижением температуры в сталях с содержанием углерода от 0,8 до 2,14 % из аустенита выделяется избыточный углерод в виде цементита, называемого вторичным. Следовательно, ниже линии SE (до температуры 727°С) сталь имеет структуру: аустенит + цементит (вторичный). В чугунах с содержанием углерода от 2,14 до 4,3 % при 1147 °С, кроме ледебурита, есть аустенит, из которого при понижении температуры тоже будет выделяться вторичный цементит. Следовательно, ниже линии EC (до температуры 727 °С) белый чугун имеет структуру: ледебурит + аустенит + цементит вторичный.
Линия PSK (727° С) — это линия эвтектоидного превращения. На этой линии во всех железоуглеродистых сплавах аустенит распадается, образуя структуру, представляющую собой механическую смесь феррита и цементита и называемую перлитом. Ниже 727°С железоуглеродистые сплавы имеют следующие структуры.
- Стали, содержащие углерода менее 0,8 %, имеют структуру феррит + перлит и называются доэвтектоидными сталями.
- Сталь с содержанием углерода 0,8 % имеет структуру перлита и называется эвтектоидной сталью.
- Стали с содержанием углерода от 0,8 до 2,14 % имеют структуру цементит + перлит и называются заэвтектоидными сталями.
- Белые чугуны с содержанием углерода от 2,14 до 4,3 % имеют структуру перлит + вторичный цементит + ледебурит и называются доэвтектическими чугунами.
- Белый чугун с содержанием углерода 4,3 % имеет структуру ледебурита и называется эвтектическим чугуном.
- Белые чугуны с содержанием углерода от 4,3 до 6,67 % имеют структуру цементит первичный + ледебурит и называются заэвтектическими чугунами [5].
Линия PQ показывает, что с понижением температуры растворимость углерода в феррите уменьшается от 0,02 % при 727 °С до 0,006 % при комнатной температуре. При охлаждении ниже температуры 727° С из феррита выделяется избыточный углерод в виде цементита, называемого третичным. В большинстве сплавов железа с углеродом третичный цементит в структуре можно не учитывать из-за весьма малых его количеств. Однако в низкоуглеродистых сталях в условиях медленного охлаждения третичный цементит выделяется по границам зерен феррита (рис. 76). Эти выделения уменьшают пластические свойства стали, особенно способность к холодной штамповке[5].
См. также
Примечания
- ↑ Кузьмин, 1971, с. 91.
- ↑ Циммерман, 1982, с. 31.
- ↑ Циммерман, 1982, с. 33.
- ↑ 1 2 Кузьмин, 1971, с. 93.
- ↑ 1
- ↑ Кузьмин, 1971, с. 92.
Литература
- Кузьмин Б. А., Самохоцкий А. И., Кузнецова Т. Н. Металлургия, металловедение и конструкционные материалы. — Москва: Высшая школа, 1971. — 352 с.
- Циммерман Р., Гюнтер К. Металлургия и материаловедение. — Справ. издание. Пер. с нем.. — Москва: Металлургия, 1982. — 480 с.
wiki.sc
Диаграмма состояния сплавов железо-углерод — Википедия
Диаграмма фазового равновесия (диаграмма состояния) железо-углерод (иногда говорят железо-цементит) — графическое отображение фазового состояния сплавов железа с углеродом в зависимости от их химического состава и температуры.
Диаграмма состояния[править]
Железо образует с углеродом химическое соединение Fe3C цементит. Так как на практике применяют металлические сплавы с содержанием углерода до 6,67 %, то рассматриваем часть диаграммы состояния от железа до цементита. Поскольку цементит – фаза метастабильная, то и соответствующая диаграмма называется метастабильной (сплошные линии на рисунке).
Для серых чугунов и графитизированных сталей необходимо рассматривать стабильную диаграмму железо-графит (Fe-Гр), поскольку именно графит является стабильной фазой. Цементит образуется намного быстрее графита и во многих сталях и белых чугунах может существовать достаточно долго. В серых чугунах графит существует обязательно.
На рисунке тонкими пунктирными линиями показаны линии стабильного равновесия (то есть с участием графита), там где они отличаются от линий метастабильного равновесия (с участием цементита), а соответствующие точки обозначены штрихом. (Отметим, что обозначения фаз и точек на этой диаграмме подчиняются неофициальному международному соглашению.)
Фазы диаграммы железо — цементит[править]
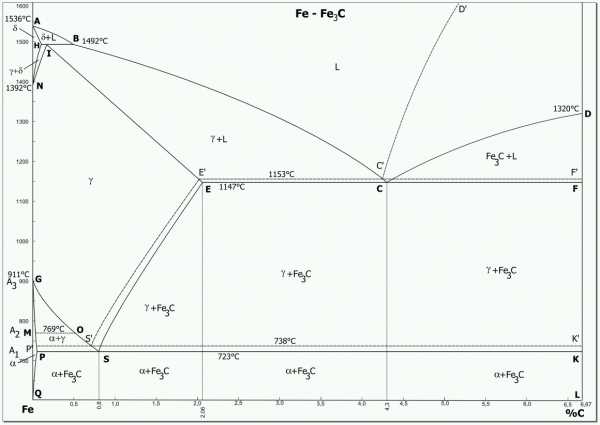 Часть диаграммы состояния сплавов железо-цементит
Часть диаграммы состояния сплавов железо-цементит
В системе железо — углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
1. Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
2. Феррит — Твёрдый раствор внедрения углерода в α-железе с ОЦК (объёмно-центрированной кубической) решёткой.
Феррит имеет переменную предельную растворимость углерода: минимальную — 0,006 % при комнатной температуре (точка Q), максимальную — 0,02 % при температуре 700 °C (точка P). Атомы углерода располагаются в центре грани или (что кристаллогеометрически эквивалентно) на середине рёбер куба, а также в дефектах решетки.
При температуре выше 1392 °C существует высокотемпературный феррит, с предельной растворимостью углерода около 0,1 % при температуре около 1500 °C (точка I)
Свойства феррита близки к свойствам чистого железа. Он мягок (твердость — 130 НВ) и пластичен, магнитен (при отсутствии углерода) до 770 °C.
3. Аустенит (γ) — твёрдый раствор внедрения углерода в γ-железе с ГЦК (гране-центрированной кубической) решёткой.
Атомы углерода занимают место в центре гранецентрированной кубической ячейки.
Предельная растворимость углерода в аустените — 2,14 % при температуре 1147 °C (точка Е).
Аустенит имеет твёрдость 200—250 НВ, пластичен, парамагнитен.
При растворении других элементов в аустените или в феррите изменяются свойства и температурные границы их существования.
4. Цементит (Fe3C) — химическое соединение железа с углеродом (карбид железа), со сложной ромбической решёткой, содержит 6,67 % углерода. Он твёрдый (свыше 1000 HВ), и очень хрупкий. Цементит фаза метастабильная и при длительным нагреве самопроизвольно разлагается с выделением графита.
В железоуглеродистых сплавах цементит как фаза может выделяться при различных условиях:
- — цементит первичный (выделяется из жидкости),
- — цементит вторичный (выделяется из аустенита),
- — цементит третичный (из феррита),
- — цементит эвтектический и
- — эвтектоидный цементит.
Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зёрен аустенита (после эвтектоидного превращения они станут зёрнами перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зёрен.
Эвтектический цементит наблюдается лишь в белых чугунах. Эвтектоидный цементит имеет пластинчатую форму и является составной частью перлита.
Цементит может при специальном сфероидизируюшем отжиге или закалке с высоким отпуском выделяться в виде мелких сфероидов.
Влияние на механические свойства сплавов оказывает форма, размер, количество и расположение включений цементита, что позволяет на практике для каждого конкретного применения сплава добиваться оптимального сочетания твёрдости, прочности, стойкости к хрупкому разрушению и т. п.
5. Графит — фаза состоящая только из углерода со слоистой гексагональной решёткой. Плотность графита (2,3) много меньше плотности всех остальных фаз (около 7,5 — 7,8) и это затрудняет и замедляет его образование, что и приводит к выделению цементита при более быстром охлаждении. Образование графита уменьшает усадку при кристаллизации, графит выполняет роль смазки при трении, уменьшая износ, способствует рассеянию энергии вибраций.
Графит имеет форму крупных крабовидных (изогнутых пластинчатых) включений (обычный серый чугун) или сфероидов (высокопрочный чугун).
Графит обязательно присутствует в серых чугунах и их разновидности — высокопрочных чугунах. Графит присутствует также и в некоторых марках стали — в графитизированных сталях.
wp.wiki-wiki.ru
Углерод и железо – Популярная химия
Углерод в железе при различных условиях вызывает разные структурные состояния, определяемые количеством углерода и температурой среды.
Внедренный в железо углерод в различных соотношениях и при различной концентрации с условиями внедрения определяет массу различных свойств соединения. Это свойство нашло обширное практическое применение на производствах и в металлургической промышленности.
Различные состояния соединения железо-углерод имеют разные названия: стабильная твердая фаза – графит, затем по убыванию степени твердости цементит, аустенит, феррит и жидкая фаза.
Диаграмма железо-углерод
Начало изучению диаграммы железо-углерод положено в 1868 году инженером Обуховского металлургического завода Дмитрием Константиновичем Черновым. Ученый заметил, что у стали имеются критические точки, в которых степень сродства с углеродом резко меняется при проявляемой стабильности в другом температурном диапазоне. При этом критическая точка была вариабельна в зависимости от концентрации углерода, что обуславливало физические свойства конечного продукта.

В настоящее время диаграмма имеет диапазон температур до 1536 градусов по Цельсию. При более высокой температуре железо имеет жидкое агрегатное состояние и свободно растворяет любые количества углерода, образуя гомогенную массу. Соединения с углеродом находят практическое применение при пропорциях от 0,006% до 6,67% содержания углерода (цементит). Соединения при более высоких концентрациях нестабильны и не нашли практического применения, по этой причине шкала диаграммы ограничены концентрацией 6,67.
.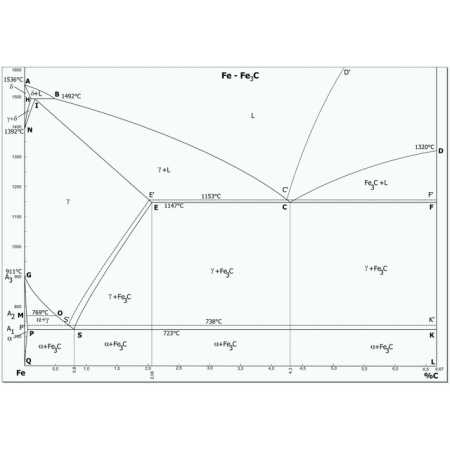
5 фаз диаграммы железо-углерод
Жидкая фаза – в этом состоянии железо растворяет углерод в любых соотношениях.
Феррит – образуется при температуре до 727 градусов. Концентрация углерода по мере увеличения температуры может возрастать от 0,006% до 0,02%. Его свойства близки к железу – мягкий, пластичный, магнитен при малом количестве углерода.
Аустенит – твердый раствор углерода в железе с кубической решеткой, где атомы углерода занимают центральное положение в решетке. Соединение обладает большей твердостью, нежели феррит. Проявляет парамагнитные свойства – то есть может быть намагниченным от внешнего магнитного поля. На практике его используют в составе сталей для придания сплаву устойчивости как к литью, так и закалке. Открытие аустенита позволило в разы ускорить процесс литья стали и ее закалки за счет повышения температурных режимов производства.
Цементит – очень твердое, но хрупкое соединение, магнитных свойств не имеет. Является результатом добавления углерода до 6,67% при темпере до 1536 градусов. Излишек углерода свыше 6,67% выделится в виде графита. Соединения считается условно стабильным, так как при длительном нагревании начинает выделять графит и уровень углерода снижается. В зависимости от условий получения, цементит может иметь различную форму – пластин, равноосные зерна, сетка и т.д. Цементин входит в различных концентрациях в состав железоуглеродистых сплавов. В промышленности цементит является основным сырьем для изготовления бетона и железобетона, которые являются самыми распространенными строительными материалами на сегодняшний день. Его уникальность заключается в его практически нулевой пластичности – он либо остается неизменной формы, либо ломается. Это объясняется сложностью строения его кристаллической решетки.
Графит – чистый углерод, не содержащий железа. Графит самый низкий по плотности из всех перечисленных фаз. Графит присутствует в соединениях чугуна и некоторых марках высокопрочной стали.
Графит находит особо широкое применение из-за его физических свойств: из него производят электроды и нагревательные элементы за счет его высокой электропроводимости и особой устойчивости к водным растворам, несвойственной ряду металлов. Его применяют также для получения синтетических алмазов, высокопроводящих клеев, наполнителя пластмасс и еще во множестве специфических сфер.

Заключение
Углерод, вступая в реакцию с железом в различных условиях, делает из железа совершенно уникальные соединения, придавая ему свойства, которые изначально и не подозревались. А доступность обоих материалов делает их ведущей основой для производства самой различной направленности
ximik.biz
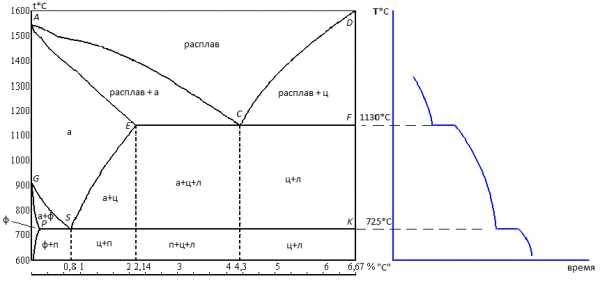
Уже много веков железо и его сплавы играют ключевую роль в научно-техническом прогрессе, являясь основным конструкционным и инструментальным материалом. Но, все начиналось около трех тысяч лет назад с первых кузнечных поковок из низкоуглеродистой стали весьма сомнительного качества. Эту нашу беседу мы посвятим углеродистым сталям, в прошлый раз мы неплохо рассмотрели получение углеродистых сталей, теперь очередь за строением и свойствами. До температуры в 768оС железо имеет объемно-центрированную кубическую кристаллическую решетку с длинной грани 2,87 ангстрема или 0,287 нм. Эта аллотропная модификация железа называется α-железом, и обладает магнитными свойствами. При температуре от 768 до 910оС существует следующая аллотропная модификация железа β-железо, с длинной грани 0,290 нм, за счет размыва дендритной структуры железа, при этой и более высоких температурах железо становится немагнитным. При температуре от 910 до 1390оС существует гранецентрированная кубическая решетка γ-железа, с длинной грани 0,365 нм. В каждой восьмигранной кристаллической ячейке находится уже не один, а 6 атомов железа. При температурах от 1390 до 1535оС существует δ-железо с объемно-центрированной кубической кристаллической решеткой с длинной грани 0,293 нм. При более высоких температурах существует только жидкий расплав железа. Иногда, для упрощений выделяют только α-железо и γ-железо, отличая их по магнитным свойствам. Для нас очень важно, что γ-железо способно хорошо растворять углерод, за счет большего свободного объема в кристаллической решетке. Если учесть выше приведенные сведения при построении графической зависимости, рассматривающей фазовые превращения в системе железо-углерод при различных температурах, то получим знаменитую диаграмму, несколько упрощенный вид которой представлен на рисунке 1.
Рисунок 1. В левой части находится прямоугольная диаграмма состояния системы железо-углерод, по горизонтали отложено содержание углерода в процентах, от 0 до 6,67%, что соответствует максимальной растворимости углерода в расплавленном железе. По вертикали отложена температура от 600 (при более низких температурах ни каких существенных изменений в системе не происходит) до 1600оС (при более высоких температурах существует только расплав). В правой части, синим цветом показана температурная кривая остывания системы железо-углерод. По горизонтали отложено время (так как зависимость, усредненная для всех содержаний углерода, то значений не указанно), по вертикали температура (в тех же пределах, что и для левой диаграммы). “Ступеньки” на линии графика означают временные промежутки остывания расплава при начале процесса кристаллизации новой фазы. Это происходит из-за выделения тепла при построении более плотной кристаллической решетки из расплава под действием структурно-ориентирующих сил на поверхности первых зародившихся кристаллов. По закону сохранения энергии, избыток энергии выделяется в виде тепла, в зависимости от скорости отвода тепла от системы (скорость охлаждения расплава), эти ступеньки могут быть различны по протяженности и даже пологости. Перейдем к составу системы, для начала оговоримся, что растворимость углерода в железе при комнатной температуре составляет не более 0,006%. Такая структура железа называется феррит (от латинского “феррум” – железо). Феррит (ф) имеет низкую твердость (НВ 80-100), так как углерод заполняет небольшой объем его кристаллической решетки и практически не мешает послойным перемещениям кристаллов. Феррит имеет хорошие пластические и магнитные свойства, прекрасно обрабатывается ковкой, штамповкой, волочением, глубокой вытяжкой и др. Максимальное количество углерода содержит цементит (ц), он представляет собой нестехиометрический карбид железа. Иначе говоря, наиболее химически и термически устойчивый раствор карбида железа в феррите, данная структура весьма устойчива. Цементит получил свое название от процесса цементации – насыщения поверхности стальных изделий углеродом в струе горящего газа или раскаленных углях при небольшом доступе воздуха. Цементация применялась еще в средние века и составляла тайну мастеров, передававшуюся от отца к сыну. В промышленном масштабе цементацию начали применять во второй половине 19-го века, в начале для упрочнения режущего инструмента и усиления брони кораблей, затем более широко. Цементит имеет наибольшую твердость среди всех соединений железа (НВ 750-800), но, он также имеет и наибольшую хрупкость (относительное удлинение при растяжении (δ) =0%), то есть, цементит хрупкий как стекло. Промежуточное место между ферритом и цементитом занимает перлит (п). Перлит (твердость НВ 200-250, δ=40-50%, содержание углерода около 0,83%) представляет собой ферритную матрицу в которую вкраплены частицы цементита, либо пластинчатой, либо овальной формы (зернистый перлит). Зернистый перлит получается при долгом томлении стали в печи, желательно с периодическими проковками с целью измельчения и “полировки” зерна. Примерно так и выглядела технология ковки холодного оружия из сталей посредственного качества в античности и средних веках. Зернистый перлит имеет более высокую пластичность и ударную вязкость при той же твердости, но, сложности процесса его получения не принесли ему широкого распространений, хотя, к процессам измельчения и сфероидизации структуры низко и среднеуглеродистых сталей мы вернемся в другой раз, уже в разделе легирующих добавок. При температурах выше 725оС появляется другая структура аустенит (а), главное отличие этой структуры от остальных состоит в высокой растворимости углерода, до 2%. Этот предел стал отличительной чертой сталей от чугунов. При содержании углерода от 2 до 4,3% мы имеем дело с так называемыми доэвтектическими (или “серыми”) чугунами, при содержании углерода от 4,3 до 6,67% – заэвтектические чугуны (или “белые”). Белые чугуны имеют высокие твердость и хрупкость, поэтому не находят применения в промышленности, их перерабатывают в кислородных конвертерах в сталь. Серые чугуны используют для изготовления массивных деталей литьем. Серый чугун имеет более низкую удельную себестоимость, чем любая сталь, но он более хрупок и его расход на аналогичную деталь больше. Для повышения ковкости и ударной вязкости, серый чугун также подвергают томлению (не менее 10-20 часов), что приводит к сфероидизации углерода и повышению пластических свойств. Томленый, или “ковкий” чугун имеет относительное удлинение на разрыв 3-6%, что меньше, чем у сталей, но больше, чем у обычного чугуна. Классические примеры использования ковкого чугуна: зубчатые колеса, кронштейны крепления деталей в подъемных машинах, корпуса минометных мин большого калибра и др. Кроме того, существует еще одна структура – ледебурит (л), названная в честь ученого А. Ледебура. Ледебурит представляет собой эвтектический сплав цементита и аустенита, свойственный системам с высоким содержанием углерода. Ледебурит и является той линией, разделяющей доэвтектические чугуны от заэвтектических чугунов. На рисунке 1, ледебуриту соответствует пунктирная линия, опущенная из точки С. Также, на рисунке 1, линия АЕСF – линия солидус (от латинского слова “солидус” – твердый), ниже которой только твердая фаза, и линия ACD – ликвидус (от слова “ликвидус” – жидкий), выше которой только жидкий расплав. Линия AESG ограничивает область аустенитного состояния, в этой области производится большинство операций термообработки углеродистых сталей. Треугольная область в левом нижнем углу диаграммы, соответствующая ферритному состоянию, описывает стали, которые практически не подвергаются закалке, так как в них нет лишнего углерода для его перевода из одного состояния в другое. Закалкой таких сталей можно добиться лишь накопления внутренних напряжений кристаллической решетки, что незначительно повысит твердость, но сильно снизит усталостную прочность материала. Температура 725оС соответствует и на графике и на диаграмме переходу α-железа в γ-железо, сопровождающиеся выделением небольшого количества энергии из-за уплотнения кристаллической решетки (длинна грани от 0,290 до 0,287 нм). Подавляющее большинство из применяемых в промышленности углеродистых сталей находятся левее пунктирной линии, опущенной из точки S. Стали и чугуны, лежащие между пунктирными линиями из точек S и Е, почти не используются, так как имеют высокую хрупкость при не особенно выдающейся твердости, и значительную себестоимость производства. При повышении содержания углерода в сталях, влияние вредных примесей (главным образом: сера, мышьяк, азот, фосфор, селен и др.) усиливается пропорционально повышению твердости изделий. Причем, как собственной твердости сырой (не подвергнутой термической обработке) стали, так и приобретенной в процессе закалки. Поэтому, к конструкционным сталям с низким содержанием углерода предъявляются менее жесткие требования по чистоте, чем к инструментальным углеродистым сталям. Но, об этом в следующий раз. |
www.chemfive.info
Железа углерода – Справочник химика 21
Диаграмма состояния системы железо — углерод [c.414] Чему равна стандартная теплота реакции восстановления оксида трехвалентного железа углеродом до железа и моноксида углерода, протекающей в доменной [c.94]
Современный вид диаграммы состояния железо—углерод представлен на рис. XIV, 14. В ее создании принимали участие многие отечественные и зарубежные исследователи. Диаграмма охватывает область составов от О до 6—7% углерода. Буквы, отмечающие различные точки диаграммы, приняты в качестве стандартных обозначений во всей научной литературе. [c.415]
Диаграмма железо—углерод является первой фазовой диаграммой, использованной в металлургии. После того как было начато систематическое изучение фазовых диаграмм, развитие металлургии стало па прочную научную основу. [c.417]
Ре 1К[1ии D твердом фазе протекают обычно при температурах выше 20°С. Теплоемкость же твердых тел (за исключением железа, углерода и некоторых других) выше 20° С меняется с температурой незначительно. [c.115]
При доменной плавке прямое восстановление оксидов железа углеродом кокса играет незначительную роль и возможно лишь при высоких температурах. В доменной печи преобладает процесс косвенного восстановления их оксидом углерода (II) и водородом, описываемый уравнениями [c.62]
Добавка к Ре, Со, N1 даже в небольших количествах других элементов приводит к значительному изменению механических и физико-химических свойств этих металлов. Причем на свойства сплавов оказывает сильное влияние термическая и механическая обработка. Кратко рассмотрим эти закономерности на примере наиболее важной системы железо — углерод. [c.557]
Диаграмма состояния системы железо — углерод. В 1868 г. Д. К. Чернов впервые указал на существование определенных температур ( критических точек ), зависящих от содержания углерода в стали и характеризующих превращения одной микроструктуры стали в другую. Этим было положено начало изучению диаграммы состояния Ге—С, а 1868 г. стал годом возникновения металловедения — науки о строении и свойствах металлов и сплавов. Позже Ф. Осмонд уточнил значения критических точек и описал характер микроструктурных изменений, наблюдаемых при переходе через эти точки. Он дал названия важнейшим структурам железоуглеродистых сплавов эти названия употребляются до сих пор. [c.617]
Рис, 173 Часть диаграммы состояния систсмы железо —углерод. [c.683]
Какие превращения происходят в системе железо—углерод при затвердевании расплава и последующем охлаждении [c.53]
Природа не приготовила для людей ни простых, ни сложных веществ в особо чистом состоянии. Хотя ряд веществ, таких, как алмаз, кварц, самородное золото и т. д., и встречается в природе на первый взгляд в чистом виде, но и эти вещества содержат разнообразные примеси — одних больше, других меньше. Если мы, например, имеем дело с серой самородной, то уже визуально заметно, что она загрязнена примесями в ней кроме атомов серы, составляющих основную массу вещества, находятся атомы селена, мышьяка, железа, углерода и других элементов. Любое простое или сложное вещество —это смесь многих веществ, и задача получения индивидуального вещества состоит в выделении из этой смеси основного вещества. При получении того или иного вещества с помощью химической реакции примеси, содержащиеся в реагентах, частично переходят в продукты реакции. Кроме того, при этом всегда образуются побочные соединения, загрязняющие получаемое вещество. Таким образом, получение простых и сложных веществ в высокочистом состоянии заключается в глубокой их очистке и освобождении от примесей. Отличие от обычного разделения здесь состоит в том, что при получении вещества высокой чистоты глубина разделения должна быть значительно большей, а материал стенок аппаратуры не должен в сколько-нибудь заметной степени загрязнять очищаемое вещество. [c.9]
На рис. 3.124 представлена диаграмма состояния системы железо — углерод. Твердые фазы и их смеси в этой системе имеют специальные названия. [c.558]
Изменения фазового состава и структуры железоуглеродистых сплавов, то есть системы железо—углерод в зависимости от температуры при различном содержании компонентов в ней представлены на упрощенной (не учитывающей существование р – и 5-форм железа) диаграмме состояния этой системы (рис. 3.1). Буквенные
www.chem21.info
Формула сплава железа с углеродом
Сплавы железа . Деление железоуглеродистых сплавов на стали и чугуны Сплавляя железо с углеродом и варьируя содержание компонентов, получают сплавы с различными структурой и свойствами. Сплавы, в которых углерода менее 0,02%, называются технически чистым железом (армко-железо). Техническое железо имеет высокую магнитную проницаемость ( m= 4500 Гс/Э). Оно является электротехническим магнитно-мягким материалом (марки Э, ЭА, ЭАА) и применяется для сердечников, полюсных наконечников, электромагнитов, пластин аккумуляторов. Железоуглеродистые сплавы – сплавы железа Fe (основной компонент) с углеродом С. Различают чистые железоуглеродистые сплавы (со следами примесей), получаемые в небольших количествах для исследовательских целей, и технические железоуглеродистые сплавы, содержащие примеси, легирующие элементы и специальные добавки. В зависимости от содержания углерода эти славы делятся на стали и чугуны. Сталь — железоуглеродистый сплав, в котором углерода содержится до 2%. Сталь обладает высокой прочностью и твердостью, хорошо сопротивляется ударным нагрузкам. Сталь можно ковать, прокатывать, легко обрабатывать на металлорежущих станках. Стальные изделия хорошо свариваются. Чугун — железоуглеродистый сплав с содержанием углерода свыше 2%. В технике наибольшее применение получили чугуны, имеющие от 2,4 до 3,8% углерода . Чугун более хрупок, чем сталь, он хуже сваривается, но обладает лучшими литейными свойствами. Поэтому изделия из чугуна получают исключительно литьем. Большая часть чугуна идет на переплавку в сталь. Структурные составляющие железоуглеродистых сплавов и их свойства. Компонентами железоуглеродистых сплавов являются железо, углерод и цементит. Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (предел прочностиσВ=250 МПа) и высокими характеристиками пластичности (относительное удлинение δ=50%). Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500 °С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000 °С). В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах). Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа ), содержит 6,67 % углерода . Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность. Такие свойства являются следствием сложного строения кристаллической решетки. В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит. Жидкая фаза . В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы. Феррит (Ф) Feα (C) – твердый раствор внедрения углерода в α-железо. Свойства феррита близки к свойствам железа . Он мягок (твердость – 130 НВ, предел прочностиσВ=300 МПа) и пластичен (относительное удлинение δ=30%), магнитен до 768oС. Аустенит (А) Feγ (С) – твердый раствор внедрения углерода в γ-железо. Аустенит имеет твердость 200…250 НВ, пластичен (относительное удлинение δ=40…50%), парамагнитен. С ростом содержания углерода в структуре стали увеличивается количество цементита, при одновременном снижении доли феррита. Изменение соотношения между составляющими приводит к уменьшению пластичности, а также к повышению прочности и твердости.
touch.otvet.mail.ru
Система железо-углерод – Справочник химика 21
Диаграмма состояния системы железо — углерод [c.414] Добавка к Ре, Со, N1 даже в небольших количествах других элементов приводит к значительному изменению механических и физико-химических свойств этих металлов. Причем на свойства сплавов оказывает сильное влияние термическая и механическая обработка. Кратко рассмотрим эти закономерности на примере наиболее важной системы железо — углерод. [c.557]
Диаграмма состояния системы железо — углерод. В 1868 г. Д. К. Чернов впервые указал на существование определенных температур ( критических точек ), зависящих от содержания углерода в стали и характеризующих превращения одной микроструктуры стали в другую. Этим было положено начало изучению диаграммы состояния Ге—С, а 1868 г. стал годом возникновения металловедения — науки о строении и свойствах металлов и сплавов. Позже Ф. Осмонд уточнил значения критических точек и описал характер микроструктурных изменений, наблюдаемых при переходе через эти точки. Он дал названия важнейшим структурам железоуглеродистых сплавов эти названия употребляются до сих пор. [c.617]
Какие превращения происходят в системе железо—углерод при затвердевании расплава и последующем охлаждении [c.53]
На рис. 3.124 представлена диаграмма состояния системы железо — углерод. Твердые фазы и их смеси в этой системе имеют специальные названия. [c.558]
Изменения фазового состава и структуры железоуглеродистых сплавов, то есть системы железо—углерод в зависимости от температуры при различном содержании компонентов в ней представлены на упрощенной (не учитывающей существование р – и 5-форм железа) диаграмме состояния этой системы (рис. 3.1). Буквенные [c.40]
Хорошо известная диаграмма равновесия системы железо— углерод исключительно сложна. Она позволяет судить о том, как широк диапазон режимов термообработки и закалки. Сплавы цветных металлов имеют несколько иную кристаллическую структуру, поэтому для них используют ограниченный диапазон режимов термической обработки. Некоторые сплавы меди, алюминия и никеля можно подвергать различным методам термообработки. [c.316]
Кратко рассмотрим закономерности изменения свойств металла на примере наиболее важной системы железо – углерод. [c.531]
Превращения при образовании твердых растворов в системе железо — углерод имеют огромное значение в производстве углеродистых сталей. [c.199]
Твердые растворы часто образуются металлами только на небольшом протяжении диаграмм плавкости, т. е. два компонента в твердом состоянии смешиваются между собой не во всех отношениях (ограниченные твердые растворы). Если при этом кривые температуры начала кристаллизации пересекаются ниже температур плавления обоих компонентов, то получается кривая плавкости. Такая кривая изучена для системы железо — углерод [c.226]
Расплавы железо — углерод. Изучение строения расплавов системы железо — углерод представляет интерес как для выяснения характера межатомного взаимодействия в этой системе, так и для понимания процессов, происходящих при производстве промышленных сплавов на основе железа. [c.195]
Исключительное по важности значение в металлохимии самого железа имеют взаимодействия в системе железо — углерод, поскольку сплавы железа с углеродом составляют основу черной металлургии. При карботермическом восстановлении железа из оксидных руд (доменный процесс) образуется не чистое железо, а чугун. Особенности взаимодействия в системе Fe—С наглядно отражаются диаграммой состояния (рис. 61). Геометрический строй диаграммы со стороны железа определяется тремя полиморфными модификациями a-Fe, 7-Fe и б-Fe, поскольку переход aT не связан с наличием тепловых эффектов и не отражается на диаграмме. Углерод в железе образует твердые растворы внедрения, области которых на диаграмме обозначены как а, 7, б. Самая большая растворимость углерода — в y-Fe. Этот твердый раствор называется аустенитом. Области твердых растворов углерода в а- и б-Fe, называемые -и б-фер-ритами, значительно меньше. [c.413]
Представление о формировании структуры и фазовых превращениях, протекающих в чугуне при охлаждении и нагревании можно составить ио диаграмме состояния системы железо — цементит и железо — графит (см. рис. 1), а также по диаграмме состояния системы железо — углерод — кремний (рнс. 52). [c.120]
Процессы закалки и отпуска можно понять, если рассмотреть фазы, образующиеся в системе железо—углерод. Углерод растворим в гамма-железе, причем такая форма устойчива вы
www.chem21.info