В промышленности ацетилен получают из: №4. Как получают ацетилен в лаборатории и в промышленности? Напишите уравнения соответствующих реакций.
alexxlab | 30.04.2023 | 0 | Разное
Урок №18. Получение и применение ацетилена.
Урок №18. Получение и применение ацетилена.Получение 1. Термическое разложение алканов (электрокрекинг)
2CH4 t=1500→ HC≡CH + 3H2 (пиролиз метана)
C2H6t,kat → C2H2 + 2H2 (t=1200)
2C3H8t,kat → 3C2H2 + 5H2 (t=1200)
2. Гидролиз карбида кальция (получение ацетилена)
В лаборатории и в промышленности ацетилен получают взаимодействием карбида кальция с водой (карбидный способ): CaC2 + 2H2O → Ca(OH)2 + C2H2
Карбид кальция получают в электропечах при нагревании кокса с негашеной известью:
3.
CH3-CH-CH2 + 2KOH спирт.р–р → CH3– C≡CH +2KCl +2H2O │ │ пропин Cl Cl 1,2-дихлорпропан
4. Из ацетиленидов
HC≡CNa + CH3-Cl → HC≡C-CH3 + NaCl моноацетиленид хлорпропан пропин натрия
AgC≡CAg + 2CH3-I → CH3-C≡C-CH3 + 2AgI↓ ацетиленид серебра йодметан бутин-2
Применение Ацетилен широко применяют в органическом
синтезе. Примеры промышленного использования ацетилена: ЦОР: Образование молекулы ацетилена Образование названий алкинов по номенклатуре ИЮПАК Получение ацетилена, его химические свойства ТРЕНАЖЁРЫ: Алкины: строение, номенклатура, получение и физические свойства Алкины: строение, номенклатура, получение и физические свойства (расчетные задачи) Гомологический ряд ацетиленаТипы химических реакций, характерные для алкинов Уравнения реакций, характеризующие химические свойства ацетилена Химические свойства алкинов Химические свойства алкинов (расчетные задачи) |
Ацетилен
Для газопламенных работ необходимо осуществить передачу тепла из пламени в металл в количестве, достаточном для конкретных условий работ. Горючие газы сгорают, как правило, в смеси с кислородом. Наибольшей температурой обладает ацетилено-кислородное пламя (3200°С), что позволяет использовать ацетилен при любых видах газопламенной обработки металлов. Интенсивность горения пламени определяется произведением нормальной скорости горения на теплоту сгорания смеси. Ацетилен обладает наивысшей «интенсивностью горения», которая для смеси стехиометрического состава составляет 27 700 ккал/(м
Горючие газы сгорают, как правило, в смеси с кислородом. Наибольшей температурой обладает ацетилено-кислородное пламя (3200°С), что позволяет использовать ацетилен при любых видах газопламенной обработки металлов. Интенсивность горения пламени определяется произведением нормальной скорости горения на теплоту сгорания смеси. Ацетилен обладает наивысшей «интенсивностью горения», которая для смеси стехиометрического состава составляет 27 700 ккал/(м
Ацетилен относится к группе непредельных углеводородов ряда СnН2n-2.. Это бесцветный горючий газ со специфическим запахом; благодаря наличию в нем примесей – фосфористого водорода, сероводорода и пр. плотность ацетилена при 20°С и 760 мм рт. ст. равна 1,091 кг/м3; при 0°С и 760 мм рт. ст. – – плотность 1,171 кг/м3. Ацетилен легче воздуха; плотность по сравнению с плотностью воздуха 0,9; молекулярная масса 26,038. Критическая точка для ацетилена характеризуется давлением насыщенного пара, равным 61,65 кгс/см2, и температурой 35,54°С. При 760 мм рт. ст. и температуре –84°С ацетилен переходит в жидкое состояние, при температуре –85°С – затвердевает.
При 760 мм рт. ст. и температуре –84°С ацетилен переходит в жидкое состояние, при температуре –85°С – затвердевает.

Взрывчатый распад ацетилена, как правило, начинается при интенсивном нагреве со скоростью 100 – 500°С/с. При медленном нагреве происходит реакция полимеризации ацетилена, идущая с выделением тепла, которая, как правило, при температуре свыше 530°С влечет за собой взрывчатый распад ацетилена. Нижнее предельное давление, при котором возможно разложение ацетилена, равно 0,65 кгс/см2. Пределы взрываемости для ацетилена широки (табл. 2). Наиболее опасными являются смеси ацетилена с кислородом стехиометрического состава (~30%). Скорости распространения пламени и детонации достигают наибольшего значения при соотношении ацетилена и кислорода 1:2,5 и соответственно равны 13,5 и 2400 м/с при нормальных условиях. Давление, образующееся при взрыве ацетилена, зависит от начальных параметров и характера взрыва. Оно может возрасти примерно в 10 – 12 раз по сравнению с начальным при взрыве в небольших сосудах и может быть увеличено в 22 раза при детонации чистого ацетилена и в 50 раз при детонации ацетилено-кислородной смеси.
При газопламенной обработке металлов ацетилен используют либо в газообразном состоянии при получении его в переносных или стационарных ацетиленовых генераторах, либо в растворенном состоянии. Растворенный ацетилен представляет собой раствор ацетилена в ацетоне, распределенный равномерно в пористом наполнителе под давлением. Растворимость ацетилена зависит от температуры и давления. Пористая масса в баллоне обеспечивает рассосредоточение ацетилена по всему объему и локализацию взрывчатого распада ацетилена. При отсутствии пористой массы в баллоне инициированный взрывной распад ацетилена, растворенного в ацетоне, происходит при давлении ниже 5 кгс/см
Физико-химические показатели газообразного и растворенного технического ацетилена оговорены ГОСТ 5457 – 75. По содержанию допустимого количества примесей различают ацетилен растворенный, растворенный и газообразный; допустимое содержание примесей (в объемных долях) соответственно равно:
- воздуха и других малорастворимых в воде газов – не более 0,9, 1,0, 1,5;
- фосфористого водорода – 0,01; 0,04; 0,08;
- сероводорода – 0,005; 0,05; 0,15;
- водяных паров при 20°С и 760 мм рт.
 ст. – 0,5; 0,6.
ст. – 0,5; 0,6.
Технический растворенный ацетилен транспортируют в стальных баллонах. Допустимое максимальное давление в баллонах не должно вревышать 13,4 кгс/см 2 при температуре –5°С и давлении 760 мм рт. ст. и 30 кгс/см2 при температуре+40°С и давлении 760 мм рт. ст. Остаточное давление в баллоне при тех же параметрах не должно быть меньше соответственно 0,5 и З,0 кгс/см2.
Для газопламенной обработки металлов, наряду с ацетиленом, полученным из карбида кальция, применяют пиролизный ацетилен, получаемый из природного газа термоокислительным пиролизом метана с кислородом. Пиролизный ацетилен также хранят и транспортируют в баллонах в растворенном виде. Наполнитель и растворитель для пиролизного ацетилена тот же, что и для ацетилена из карбида кальция.
При применении растворенного ацетилена по сравнению с газообразным обеспечиваются наибольший коэффициент использования карбида, чистота рабочего места сварщика, устойчивая работа аппаратуры и безопасность в работе.
Содержание фосфористого водорода в ацетилене по объему не более 0,08%, содержание сульфидной серы не более 1,2%. В ГОСТ 1460 оговаривается также допустимое количество кусков карбида кальция других размеров в партиях указанной грануляции. Большой тепловой эффект реакции разложения карбида создает опасность сильного перегрева. Без отвода тепла при взаимодействии стехиометрического количества карбида кальция и воды реакционная масса разогревается до 700 – 800°С. Разложение карбида при недостаточном охлаждении и особенно в присутствии воздуха может привести к взрыву, поэтому необходимо процесс осуществлять при значительном избытке воды. Для разложения 1 кг карбида необходимо 5 – 20 л воды. Особое внимание необходимо обращать на наличие карбидной пыли в карбиде. Пыль разлагается почти мгновенно; за счет мгновенного разогрева может возникнуть взрыв ацетилена. Поэтому переработка пыли в обычных генераторах, не приспособленных для использования пыли, не допускается. Если содержание пыли значительно, карбид кальция перед загрузкой в генератор просеивают через сито с ячейками диаметром 2 мм. Накопившуюся пыль следует разложить на открытом воздухе в специальном сосуде вместимостью не менее 800 – 1000 л при интенсивном помешивании, одновременно высыпая не более 250 г карбидной пыли.
Большой тепловой эффект реакции разложения карбида создает опасность сильного перегрева. Без отвода тепла при взаимодействии стехиометрического количества карбида кальция и воды реакционная масса разогревается до 700 – 800°С. Разложение карбида при недостаточном охлаждении и особенно в присутствии воздуха может привести к взрыву, поэтому необходимо процесс осуществлять при значительном избытке воды. Для разложения 1 кг карбида необходимо 5 – 20 л воды. Особое внимание необходимо обращать на наличие карбидной пыли в карбиде. Пыль разлагается почти мгновенно; за счет мгновенного разогрева может возникнуть взрыв ацетилена. Поэтому переработка пыли в обычных генераторах, не приспособленных для использования пыли, не допускается. Если содержание пыли значительно, карбид кальция перед загрузкой в генератор просеивают через сито с ячейками диаметром 2 мм. Накопившуюся пыль следует разложить на открытом воздухе в специальном сосуде вместимостью не менее 800 – 1000 л при интенсивном помешивании, одновременно высыпая не более 250 г карбидной пыли. Воду следует менять после разложения пыли в количестве до 100 кг.
Воду следует менять после разложения пыли в количестве до 100 кг.
Карбид кальция транспортируют и хранят в железных барабанах с толщиной стенки не менее 0,51 мм и массой 50 – 130 кг. Боковую поверхность барабанов делают гофрированной для большей жесткости. Карбид кальция интенсивно поглощает влагу даже из воздуха, поэтому при плохой герметичности тары возможно образование ацетилена непосредственно в барабане. Герметичность барабанов следует тщательно проверять; при перевозке барабанов на открытых машинах необходимо покрывать барабаны брезентом. При обнаружении повреждения барабана, карбид должен быть пересыпан в другую герметичную тару.
При обслуживании стационарных генераторов карбид из барабанов пересыпают в специальные приемники-бункеры. Вскрытие барабанов на станции, как правило, механизировано. Для этих целей применяют станки, в которых верхняя крышка вырезается специальным режущим роликом или клиновыми ножами. Ножи и ролик изготовляют из неискрящегося материала. Кроме того, к месту реза подается масло или азот.
Кроме того, к месту реза подается масло или азот.
Транспортировка карбида кальция в барабанах для стационарных генераторов производительностью свыше 20 м3/ч экономически не оправдана, так как раскупорка барабанов занимает значительное время; накапливается большое количество порожней тары, которая вторично не может быть использована; потери карбида за счет его дробления при перекатывании барабанов и последующего отсева от пыли значительны. Поэтому можно считать наиболее перспективным контейнерный способ перевозки и хранения карбида для стационарных установок. При газопламенной обработке алюминия, латуни, свинца и других металлов, имеющих температуру плавления ниже температуры плавления стали, в качестве горючего газа целесообразно применять не ацетилен, а газы – заменители ацетилена или жидкие горючие. Основные физические и тепловые свойства горючих газов приведены в табл. 2.
Таблица 1. Физико-химические показатели карбида кальция
Размеры кусков, мм | Обозначение | «Литраж», л/кг, не менее | |
Первый сорт | Второй сорт | ||
25 – 80 | 25/80 | 285 | 265 |
15 – 25 | 15/25 | 275 | 255 |
8 – 15 | 8/15 | 265 | 250 |
2 – 8 | 2/8 | 255 | 240 |
Для кусков смешанного размера |
| 275 | 255 |
Таблица 2. Основные физические и тепловые свойства горючих газов
Основные физические и тепловые свойства горючих газов
Наименование горючего газа и химическая формула | Низшая теплота сгорания при 20°С и 760 мм рт. ст., ккал/мз | Температура пламени смеси с кислородом, °С | Коэффициент замены ацетилена | Плотность при 20°С и 760 мм рт. ст., кг/м3 | Критическое давление, кгс/см2 | Температура,°С | Пределы взрываемости, % содержания горючего в смеси | Оптимальное соотношение между кислородом и другим горючим в смеси | Относительная скорость распространения пламени с воздухом | |||
критическая*1 | плавления | кипения | с воздухом | с кислородом | ||||||||
Ацетилен С2Н2 | 12000 | 3100-3200 | 1,0 | 1,09 | 61,65 | +35,54 | -81,0 | -83,6 | 2,1-100 | 2,3-100 | 1,7 | 1,0 |
Водород Н2 | 2400 | 2100-2500 | 5,2 | 0,084 | 12,8 | -239,8 | -259,2 | -252,8 | 3,3-81,5 | 2,6-95 | 0,4 | 1,2 |
Метан СН4 | 8000 | 2000-2200 | 1,6 | 0,67 | 45,7 | -82,5 | -182,5 | -161,7 | 4,8-16,7 | 5-59, | 2,0 | – |
Этан С2Н6 | 14400 | 2200 | 1,27 | – | – | – | -172,1 | -88,5 | 3,1-15,0 | 4,1-50,1 | – | – |
Пропан С3Н8 | 20800 | 2600-2750 | 0,65 | 1,88 | 42 | +96,8 | -189,9 | -42,6 | 2,0-11 | 2,0-48 | 3,5-4,0 | 0,3 |
Бутан С4Н10 | 27800 | 2400-2500 | 0,45 | 2,54 | 36 | -152 | -139 | -0,6 | 1,5-8,5 | 3,0-45 | 3,5-4,0 | – |
Пропан-бутан | 20600 | 2000-2100 | 0,6 | 1,867 | – | – | – | – | 2,17-9,5 | – | 3,5-4,0 | – |
Этилен С2Н4 | 14200 | 2900 | 0,9 | 1,17 | – | – | – | – | 2,7-36 | 2,6-80 | – | – |
Окись углерода СО | 2800 | 2600-2800 | 4,5 | 1,16 | 34,5 | -140,2 | -205 | -191,5 | 11,4-77,5 | 15,5-93,9 | – | – |
Сланцевый газ *2 | 3000–3400 | 1500-2000 | 4,0 | 0,74-1,0 | – | – | – | – | – | – | 0,7 | 0,5 |
Коксовый газ *2 | 3500–4400 | 2000-2200 | 3,2 | 0,4-0,55 | – | – | – | – | 7-21 | – | 0,8-0,9 | 0,7 |
Природный газ*2 (метан 98%) | 7500 – 9000 | 2000-2200 | 1,8 | 0,68-0,9 | – | – | – | – | 4,8-14,0 | – | 1,7-2,1 | 0,4 |
Нефтяной (попутный) газ | 8700–14800 | 2000-2400 | 1,2 | 0,87-1,37 | – | – | – | – | 3,5-16,3 | — | 1,9-2,9 | 0,5 |
Городской газ*2 | 4100–9000 | 2000-2300 | 3,0 | 0,84-1,05 | – | – | – | – | 3,8-40 | 8,5-73,6 | 1,2 | 0,5 |
Пиролизный газ | 7500 – 9000 | 2000-2400 | 1,8 | 0,65-0,85 | – | – | – | – | – | – | – | – |
МАПП или МАФ | 21 200 | 2800-2900 | 0,55 | 1,76 | – | – | – | – | 3,4-108 | 2,5-60 | – | – |
Пары бензина (~С7Н15) | 10 тыс. | 2400 | – | 0,7-0,74 кг/л | – | – | – | – | 0,7-6,0 | 2,1-28,4 | – | – |
Пары керосина (~С7Н14) | 10 тыс. ккал/кг | 2300 | – | 0,79-0,82 кг/л | – | – | – | – | 1,4-5,5 | – | – | – |
*1 Критической температурой называется такая температура, выше которой газ не переходит в жидкое состояние ни при каком давлении.
*2 Для горючих газовых смесей приводимые данные относятся к средним составам этих газов.
Широкие пределы изменения плотности, температуры пламени и теплоты сгорания объясняются изменяющимся химическим составом указанных газов, зависящим от месторождения или места производства.
Метилацетилен-пропадиен МАПП (широко применяемый в США) – смесь горючих газов; по физическим свойствам близок к пропану. Пределы взрываемости МАПП в смеси с воздухом 3,4 – 10,8%, в смеси с кислородом 2,5 – 60%. Смеси метилацетилена и пропадиена термодинамически нестойки, поэтому в состав МАППа вводят стабилизатор. Распад метилацетилена, аналогично ацетилену, происходит с большим выделением тепла. Температура пламени МАПП (2900°С) близка к температуре ацетилена. МАПП используют для кислородной резки и сварки и других газопламенных процессов.
Горючее МАФ – метилацетиленовая пропадиеновая фракция является отходом олифинового производства, а также отходом производства этилена и моновинилацетилена.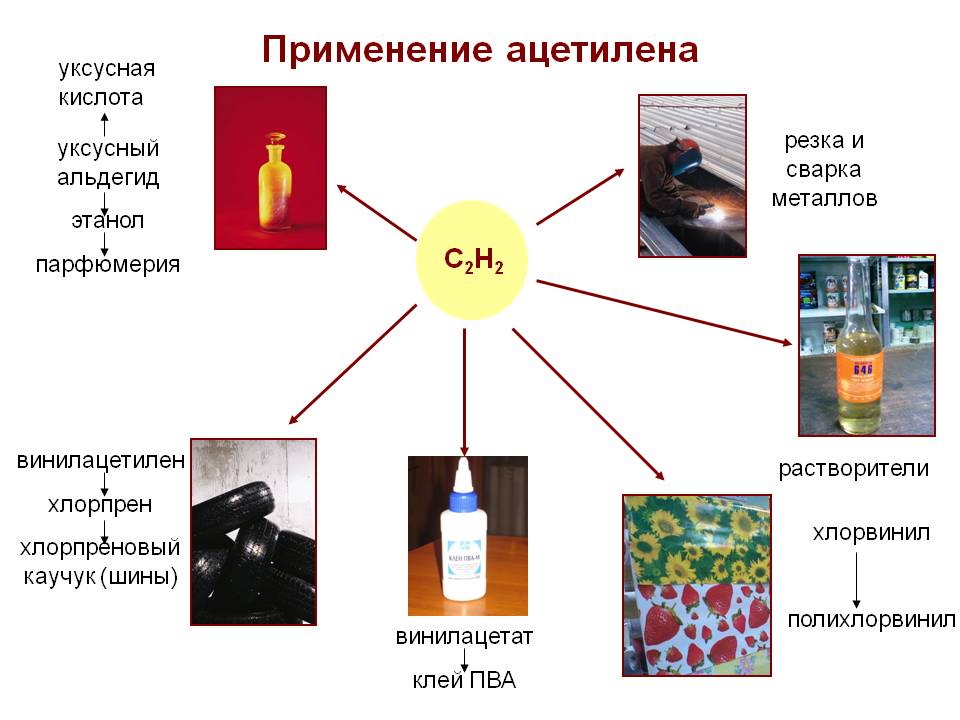 Эта фракция содержит 48 – 75% смеси метилацетилена и пропадиена и стабилизаторы: 3% пропилена, 15% пропана, 7% других углеводородов. Пределы взрываемости для МАФа те же, что и для МАППа. МАФ нечувствителен к удару. Баллоны с МАФом не взрываются, находясь рядом с горящим баллоном. Смесь инертна при температуре до 215°С и давлении до 20 кгс/см2. При соприкосновении с медью образуются взрывоопасные соединения – ацетилениды меди. Скорость распространения пламени МАФ равна 470 см/с. Вместимость баллонов для сжиженных газов 40 или 55 дм3; толщина стенки 3 мм. Предельное рабочее давление (кгс/см2)в баллонах для сжиженных газов различно: для пропана не более 16, для пропилена 20, для бутана и бутилена 3,8. Коэффициент наполнения баллонов сжиженными газами (в кгс/м3) соответственно будет равен: 425 для пропана, 445 – пропилена, 448 – бутана и 526 – бутилена. Коэффициент наполнения обозначает массу газа в кг на 1 м3 вместимости баллона и не должен превышать значений, указанных для каждого газа.
Эта фракция содержит 48 – 75% смеси метилацетилена и пропадиена и стабилизаторы: 3% пропилена, 15% пропана, 7% других углеводородов. Пределы взрываемости для МАФа те же, что и для МАППа. МАФ нечувствителен к удару. Баллоны с МАФом не взрываются, находясь рядом с горящим баллоном. Смесь инертна при температуре до 215°С и давлении до 20 кгс/см2. При соприкосновении с медью образуются взрывоопасные соединения – ацетилениды меди. Скорость распространения пламени МАФ равна 470 см/с. Вместимость баллонов для сжиженных газов 40 или 55 дм3; толщина стенки 3 мм. Предельное рабочее давление (кгс/см2)в баллонах для сжиженных газов различно: для пропана не более 16, для пропилена 20, для бутана и бутилена 3,8. Коэффициент наполнения баллонов сжиженными газами (в кгс/м3) соответственно будет равен: 425 для пропана, 445 – пропилена, 448 – бутана и 526 – бутилена. Коэффициент наполнения обозначает массу газа в кг на 1 м3 вместимости баллона и не должен превышать значений, указанных для каждого газа.
Ацетилен на основе карбида Vs. Химический ацетилен
Перейти к основному содержанию
Роб МойерРоб Мойер
генеральный директор Rexarc | Промоутер и стратегическое развитие | Поколения превосходства стальных резервуаров | Изготовление пользовательских сосудов ASME с быстрой доставкой | Ценить…
Опубликовано 10 февраля 2016 г.
+ Подписаться
Ацетилен представляет собой бесцветный легковоспламеняющийся газ, который находит множество применений в критически важных приложениях и процессах. Тем не менее, этот газ до сих пор остается загадкой, поскольку еще не все его возможные применения были использованы.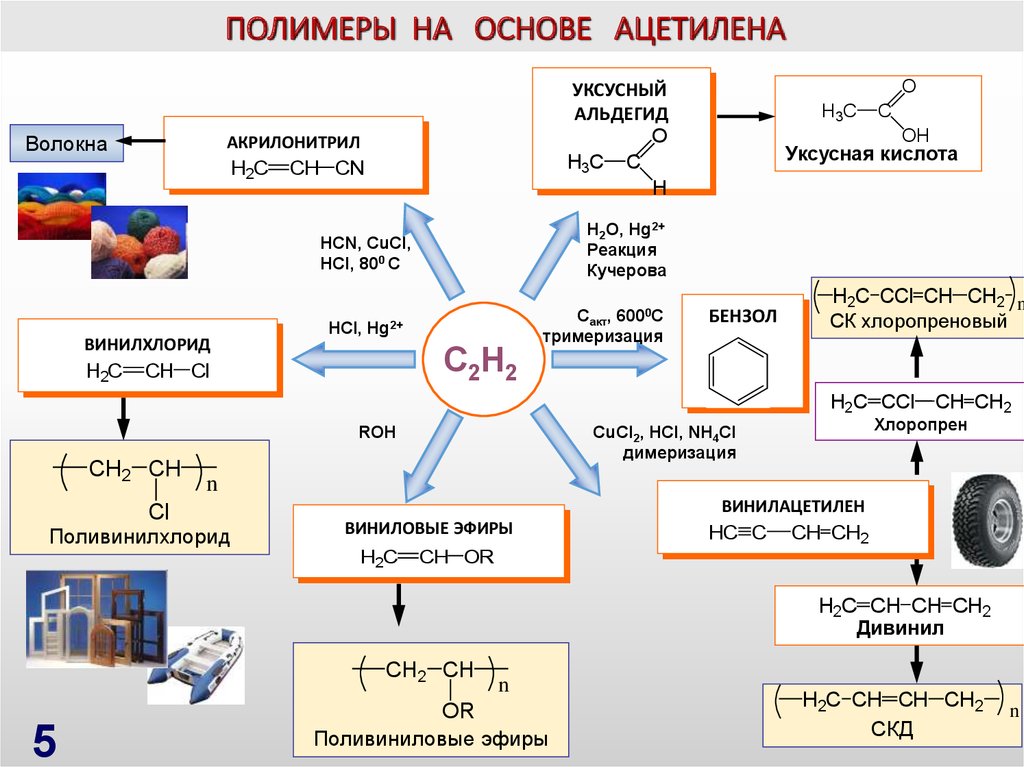 В этой сфере проводится много исследований. Поскольку этот газ легко вступает в реакцию с другими газами, элементами и материалами с образованием важных продуктов, таких как пластик, этилен и т. д., он пользуется большим спросом. Для большинства применений требуется, чтобы ацетилен был в чистом виде. Это связано с тем, что ацетилен реагирует с загрязнителями и влагой с образованием других продуктов и побочных продуктов, которые могут мешать протеканию химических реакций. Давайте рассмотрим два процесса, используемых для производства ацетилена.
В этой сфере проводится много исследований. Поскольку этот газ легко вступает в реакцию с другими газами, элементами и материалами с образованием важных продуктов, таких как пластик, этилен и т. д., он пользуется большим спросом. Для большинства применений требуется, чтобы ацетилен был в чистом виде. Это связано с тем, что ацетилен реагирует с загрязнителями и влагой с образованием других продуктов и побочных продуктов, которые могут мешать протеканию химических реакций. Давайте рассмотрим два процесса, используемых для производства ацетилена.
Два основных процесса производства ацетилена
1. Производство ацетилена из карбида кальция
Производство ацетилена с использованием карбида кальция является наиболее распространенным процессом, используемым в нескольких странах, таких как США, Япония, Ближний Восток и т. д. Это двухчастный процесс. В первой части карбид кальция получают путем смешивания кокса (углерода) с известняком при очень высоких температурах.
Химическая формула для производства карбида кальция: CaO + 3C → CaC + CO
На втором этапе процесса карбид кальция смешивают с водой для получения ацетилена и гидроксида кальция. Известковая суспензия представляет собой не что иное, как взвешенный в воде гидроксид кальция. Известковая суспензия — это больше, чем просто побочный продукт. Он может быть использован для различных других целей и в нескольких отраслях промышленности.
Химическая формула для производства ацетилена: CaC + 2H O → C H + Ca (OH)
После получения карбида кальция вторая часть процесса проводится на месте производителями ацетилена. через оборудование для производства ацетилена.
2. Ацетилен, синтезированный из природного газа
Этот процесс также известен как метод сухого крекинга или просто метод крекинга. В этом процессе природный газ нагревается до очень высоких температур, что приводит к разрушению углеводородов. В зависимости от используемого природного газа может использоваться электрическая дуга, печь или камера сгорания. Как только углеводороды распадаются, их заставляют воссоединяться с образованием ацетилена.
В зависимости от используемого природного газа может использоваться электрическая дуга, печь или камера сгорания. Как только углеводороды распадаются, их заставляют воссоединяться с образованием ацетилена.
Химический ацетилен также может быть получен в качестве побочного продукта при производстве этилена. Здесь также используется метод сухого крекинга. Для этого процесса можно использовать многие природные газы. Обычно для производства этилена используют этан или лигроин. Отдельная установка гидрирования расположена рядом с производством этилена. Эта камера гидрирования используется для обработки ацетилена.
Ацетилен, полученный с использованием этого метода, растворяется в диметилформамиде (ДМФ), в отличие от его растворения в ацетоне при производстве и распределении с использованием других методов.
Многие заводы по производству ацетилена, использующие химический ацетилен в качестве основного источника, все еще используют генератор карбида кальция на полурегулярной основе, поэтому их заводы остаются в рабочем состоянии во время остановов химических заводов, которые происходят в течение нескольких недель в году.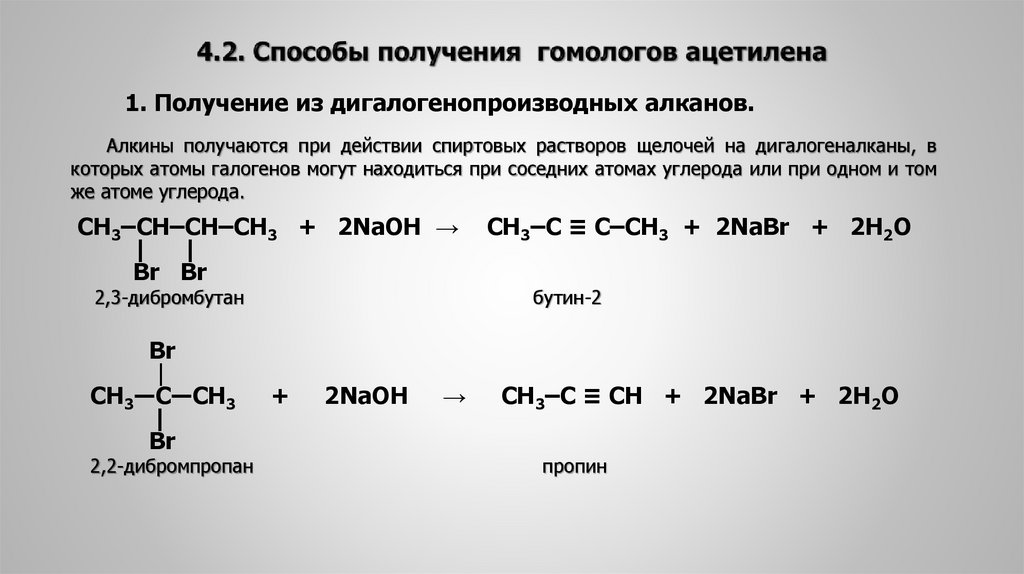 Другой проблемой широкого использования химического ацетилена является локализованность продукта. Поскольку он чаще всего является побочным продуктом процесса производства этилена, крекинг-заводы часто находятся слишком далеко от рынков, чтобы сделать экономически целесообразной транспортировку этилена. Однако, если доступен химический ацетилен, он является экономичной альтернативой ацетилену, полученному из карбида. Из-за проблем с химическим обеспечением ацетилена наиболее распространенным методом производства ацетилена по-прежнему является процесс с использованием карбида кальция, на который приходится большая часть ацетилена, производимого во всем мире.
Другой проблемой широкого использования химического ацетилена является локализованность продукта. Поскольку он чаще всего является побочным продуктом процесса производства этилена, крекинг-заводы часто находятся слишком далеко от рынков, чтобы сделать экономически целесообразной транспортировку этилена. Однако, если доступен химический ацетилен, он является экономичной альтернативой ацетилену, полученному из карбида. Из-за проблем с химическим обеспечением ацетилена наиболее распространенным методом производства ацетилена по-прежнему является процесс с использованием карбида кальция, на который приходится большая часть ацетилена, производимого во всем мире.
Знать о различных топливных газах и температурах их пламени
14 мая 2019 г.
Рекомендации по безопасному обращению с баллонами с растворенным ацетиленом
15 марта 2019 г.

CGA и безопасность в отрасли сжатого газа
23 октября 2017 г.
Rexarc на конференции MENA Industrial Gas Conference 2017
14 сентября 2017 г.
Краткая история коммерциализации ацетилена и карбида кальция
20 сентября 2016 г.
Основные усовершенствования технологических процессов для максимального повышения эффективности ацетиленовых заводов, часть II
7 декабря 2015 г.

Основные усовершенствования технологических процессов для максимального повышения эффективности ацетиленовых заводов, часть I
4 ноября 2015 г.
10 процедур безопасности на заводах по производству ацетилена
30 сентября 2015 г.
Топ-4 коммерческого использования газообразного ацетилена
Установки по производству ацетилена производят ацетилен для различных промышленных и коммерческих целей.
Газообразный ацетилен обладает свойствами, которые делают его чрезвычайно полезным газом в различных областях применения и отраслях промышленности. Ацетилен в основном производится для химического синтеза. Вторым наиболее распространенным применением ацетилена является сварка и резка.
Ацетилен в основном производится для химического синтеза. Вторым наиболее распространенным применением ацетилена является сварка и резка.
Ацетилен является важной частью многих важных процессов в промышленности. Хотя в настоящее время использование ацетилена немногочисленно, область его применения не ограничена. В связи с этим проводятся углубленные исследования, чтобы обеспечить максимально выгодное использование этого ресурса. Ацетилен является важным природным газом, который используется в различных целях, включая:
1. Использование ацетилена в портативном освещении:
В конце 1800-х годов ацетилен впервые был использован для освещения переносной лампы, известной как карбидная или ацетиленовая газовая лампа. Эти лампы устанавливались на автомобили, в домах, на велосипедах и т. д. Они также широко использовались шахтерами.
В некоторых случаях ацетилен использовался для освещения некоторых городов и поселков. В лампах для получения ацетилена используется карбид кальция и вода.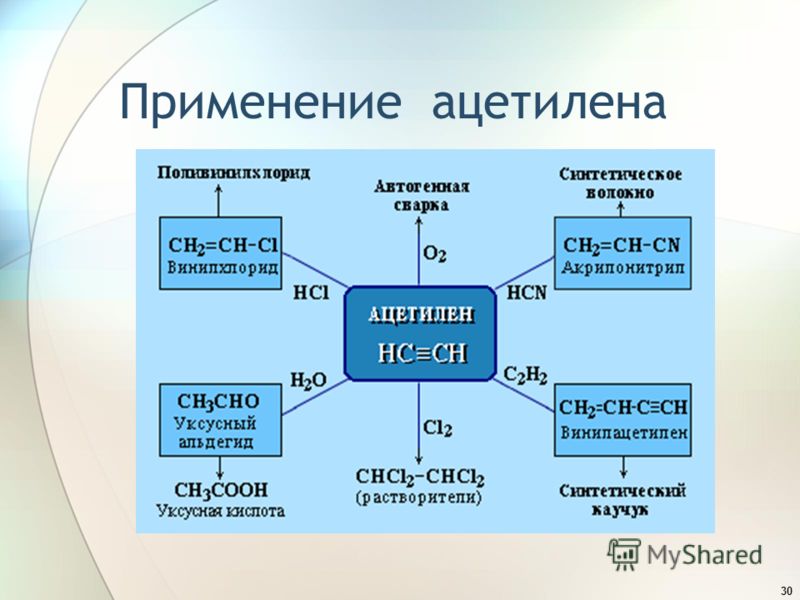 Поток ацетилена тщательно контролируется, чтобы контролировать количество используемого ацетилена. Количество используемого ацетилена напрямую влияет на интенсивность света. Многие охотники или спелеологи до сих пор используют эти лампы для занятий на местности.
Поток ацетилена тщательно контролируется, чтобы контролировать количество используемого ацетилена. Количество используемого ацетилена напрямую влияет на интенсивность света. Многие охотники или спелеологи до сих пор используют эти лампы для занятий на местности.
2. Использование газообразного ацетилена при сварке, резке и термической обработке:
Ацетилен используется для сварки и резки. Сварочный процесс, в котором используется ацетилен, известен как газокислородная резка или газовая резка. Этот метод используется для резки или сварки материалов, требующих температуры до 3500 ° C (6330 ° F).
Среди всех других газов ацетилен способен производить самое горячее пламя. По этой причине ацетилен служит важной средой для термообработки металлов и других материалов. Ацетилен используется в производстве автомобильных деталей, а также при изготовлении других металлических деталей, где точность имеет решающее значение.
3. Использование ацетилена в производстве химикатов:
Основным применением ацетилена является химический синтез. Ацетилен используется для производства нескольких неорганических соединений. Он используется в синтезе некоторых витаминов, таких как витамин А и Е.
Ацетилен используется для производства нескольких неорганических соединений. Он используется в синтезе некоторых витаминов, таких как витамин А и Е.
Его также можно использовать для производства некоторых компонентов духов, растворителей и т. д. Он используется для производства уксусной кислоты, 1,4-бутандиола (БДО), несколько ацетиленовых спиртов и т. д. При производстве этих химикатов и витаминов необходимо строго соблюдать уровень чистоты ацетилена.
4. Использование ацетилена в производстве полиэтиленовых пластмасс:
Полиэтиленовые пластмассы, ПВХ и ПВДФ производятся из этилена или метана, которые, в свою очередь, получают из ацетилена. Другой производственный процесс включает смешивание ацетилена с другими химическими веществами или элементами, такими как хлор, соляная кислота и т. д., для производства различных вариантов пластика, таких как ПВХ, ПВДФ и т. д. Эти пластики обычно используются для изготовления ряда бытовых и коммерческих товаров.
Важность чистоты газообразного ацетилена
Ацетилен может реагировать с кислородом или примесями, вызывая мощные взрывы. Следовательно, производственный процесс должен быть безупречным. В процессе производства, если ацетилен не совсем чистый, конечный продукт может сильно измениться. Поддержание чистоты производимого ацетилена имеет жизненно важное значение. В зависимости от процесса могут быть сделаны некоторые допуски в отношении качества получаемого ацетилена.
Например, ацетилен, используемый в химическом синтезе, не должен содержать более 0,5% примесей. Этот ацетилен известен как ацетилен класса А. Для процессов газокислородной резки или термообработки используется ацетилен более низкого качества. Ацетилен марки Б может содержать до 2% примесей. Эти газы могут быть дополнительно обработаны и очищены для получения чрезвычайно чистого газа. Ацетилен в любой форме, твердой или жидкой, чрезвычайно взрывоопасен.
Следовательно, при производстве ацетилена или его использовании для производства химикатов или других продуктов следует соблюдать крайнюю осторожность.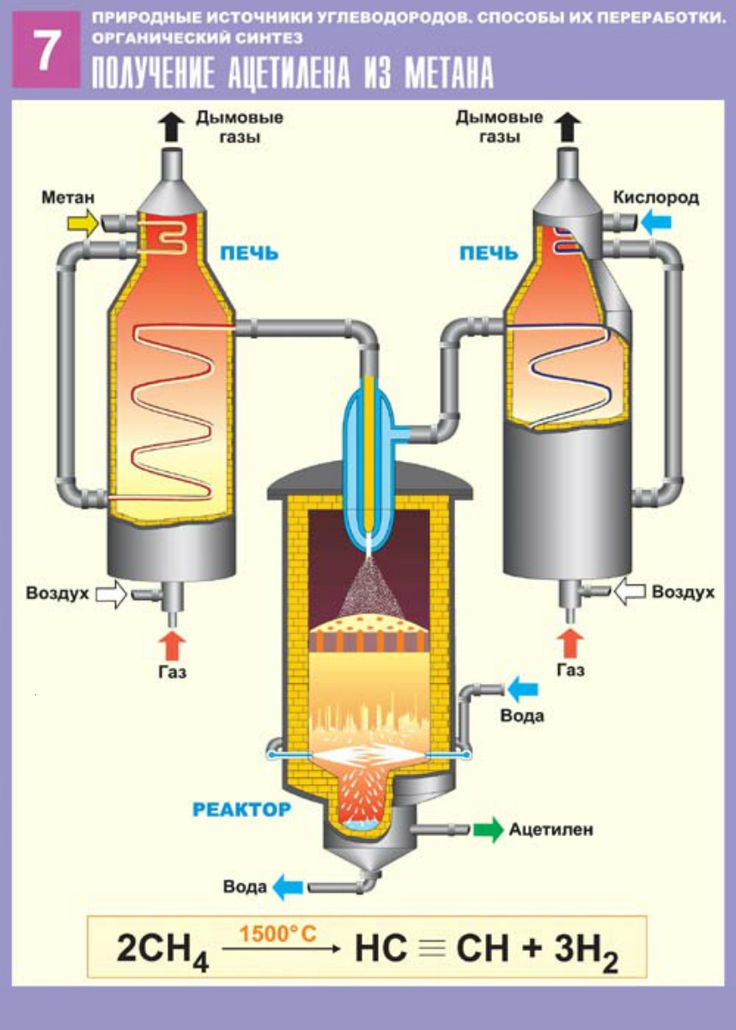


 Дегидрогалогенирование дигалогеналканов:
Дегидрогалогенирование дигалогеналканов:
 ккал/кг
ккал/кг