Аргон газ формула – Формула аргона в химии
alexxlab | 08.10.2019 | 0 | Вопросы и ответы
| Таблица ^ =>> v
| История открытия:Первый вклад в открытие аргона внес английский физик и химик Генри Кавендиш. Изучая в 1785 году окисление атмосферного азота кислородом под действием электрического разряда, он обнаружил, что остается небольшой объем газа, не подвергающегося окислению. Однако он не нашел объяснения этому факту. В 1892 году английский физик Дж. Рэлей обнаружил небольшое (всего на 0,13%) превышение плотности азота, выделяемого из воздуха, над плотностью азота, получаемого химическим путем. Английский физик У. Рамзаем предположил, что причиной этого может быть примесь еще неизвестного более тяжелого газа и предложил выделить его. Ему и Дж. Рэлею в 1894 году удалось выделить этот газ и спектральным анализом доказать, что это новый химический элемент. Дальнейшие исследования показали полную химическую инертность этого вещества. Благодаря своей химической инертности (а это был первый из открытых инертных газов), новый элемент и получил свое название Аргон (греч. аrgos – неактивный, ленивый). Нахождение в природе и получение:В атмосферном воздухе содержится 0,93% аргона по объему (9,34 л в 1м3), его запасы в атмосфере оцениваются в 4·1014 т. Среди других изотопов преобладает aргон-40, постоянно образующийся в ходе ядерной реакции (“электронный захват”) из природного изотопа калия: 40K + e = 40Ar + ne Физические свойства:Бесцветный, без запаха газ. Температура кипения аргона (при нормальном давлении) -185,9°C, температура плавления -189,4°C. Плотность при нормальных условиях 1,784 кг/м3. В 100 мл воды при 20°C растворяется около 3,3 мл аргона. в некоторых органических растворителях аргон растворяется значительно лучше, чем в воде. При пропускании электрического разряда через стеклянную трубку, заполненную аргоном, наблюдается сине-голубое свечение. Химические свойства: Аргон химически инертен, при обычных условиях химических соединений не образует. Однако со многими веществами, между молекулами которых действуют водородные связи (водой, фенолом, гидрохиноном и другими), образует соединения включения (клатраты), где атом аргона, как своего рода “гость”, находится в полости, образованной в кристаллической решетке молекулами вещества-хозяина. Установлено существование так называемых эксимерных молекул, содержащих аргон. На переходах этих молекул из метастабильного состояния в несвязанное генерируется лазерное излучение. Важнейшие соединения:Клатрат Ar*6H2O – соединение включения, температура разложения Аr·6Н2О при 101325 Па 42,0°С. Гидрофторид аргона HArF – первое открытое, и пока единственное известное на 2013 г. химическое соединение аргона с электронейтральной молекулой. Получен при УФ-облучении смеси аргона и фтороводорода при 8K. Нестоек и распадается уже при 17 К на фтороводород и аргон. CU(Ar)O – образование такого соединение при 3 К предполагается на основании спектральных данных. В этой молекуле уран должен быть связан с тремя другими атомами – углеродом, аргоном и кислородом. Применение:Аргон широко используют для создания инертной и защитной атмосферы, прежде всего при термической обработке легко окисляющихся металлов (аргоновая плавка, аргоновая сварка и другие). В атмосфере аргона получают кристаллы полупроводников и многие другие сверхчистые материалы. Аргоном часто заполняют электрические лампочки (для замедления испарения вольфрама со спирали). Это же его свойство используется в аргоновой сварке, которая позволяет соединять алюминиевые и дюралевые детали. Аргон (в смеси с неоном, парами ртути) применяют для наполнения газоразрядных трубок (сине-голубое свечение), что используется в светящейся рекламе. Также аргон используется в аргоновых лазерах. В геохронологии по определению соотношения изотопов 40Ar/40К устанавливают возраст минералов. Мавлянова Н.Х., Жудин С.М. Источники: Аргон /WebElements.narod.ru/ URL: http://webelements.narod.ru/elements/Ar.htm (дата обращения: 8.07.13). |
www.kontren.narod.ru
Аргон (Ar2) по ТУ 6-21-12-94, ГОСТ 10157-70
Данное оборудование указано в следующих разделах каталога:
Газообразный и жидкий аргон получают из воздуха и остаточных газов аммиачных производств.
Газообразный и жидкий аргон используется в качестве защитной среды при сварке, резке и плавке активных и редких металлов и сплавов на их основе, алюминия, алюминиевых и магниевых сплавов, нержавеющих хромоникелевых жаропрочных сплавов и легированных сталей различных марок, а также при рафинировании металлов в металлургии. В аналитической химии чистый аргон используется в качестве газа-носителя в эмиссионной спектрометрии, ICP-спектрометрии, масс-спектрометрии и т.д.
Аргон – жидкость при температуре -185,9 °С, при нормальных условиях – газ.
Не оказывает опасного воздействия на окружающую среду. Газообразный аргон тяжелее воздуха и может накапливаться в слабо проветриваемых помещениях у пола. При этом снижается содержание кислорода в воздухе, что вызывает кислородную недостаточность и удушье.
Жидкий аргон – низкокипящая жидкость, которая может вызвать обморожение кожи и поражение слизистой оболочки глаз.
Технические характеристики
| Техническое наименование | Аргон газообразный |
| Химическая формула | Ar |
| Номер по списку OOН | 1006 |
| Класс опасности при перевозках | 2.1 |
Физические свойства
| Физическое состояние при нормальных условиях | газ |
| Плотность, при нормальных условиях (101,3 кПа, 20 °C), кг/м³ | 1,66 |
| Температура кипения, °С при 101,3 кПа | -185,8 |
| Температура тройной точки и равновесное ей давление °С, мПА | -189,2 (0,688) |
| Растворимость в воде | незначительна |
| Пожаро- и взрывоопасность | пожаро-взрывобезопасен |
| Стабильность и химическая активность | Стабильность | стабильный |
| Реакционная способность | инертный газ | |
| Температура воспламенения, °С | с воздухом | – |
| с кислородом | – | |
| Пределы воспламенения, объемные доли, % газа | с воздухом | – |
| с кислородом | – | |
| Опасность для человека | ПДК, мг/м³ | – |
| Токсическое воздействие | не токсичен | |
| Экологическая опасность | не оказывает влияния на окружающую среду | |
| Средства пожаротушения | применимы любые огнетушащие средства |
Технические требования
Аргон газообразный. Сорт высший ГОСТ 10157-79 с изм. 1, 2, 3
| Объемная доля аргона | не менее 99,993% |
| Объемная доля кислорода | не более 0,0007% |
| Объемная доля азота | не более 0,005% |
| Содержание влаги при норм. усл. | не более 0,0009% |
| Углеродосодержащие | не более 0,0005% |
| Давление при стандартных условиях | не менее 15,0 МПа |
Аргон газообразный высокой чистоты ТУ 6-21-12-94
| Объемная доля аргона | не менее 99,998% |
| Объемная доля кислорода | не более 0,0002% |
| Объемная доля азота | не более 0,001% |
| Объемная доля водяного пара | не более 0,0003% |
| Объемная доля СO2 | не более 0,00002% |
| Объемная доля метана | не более 0,0001% |
| Объемная доля водорода | не более 0,0002% |
| Давление при стандартных условиях | не менее 15,0 МПа |
Аргон жидкий Сорт высший ГОСТ 10157-79 с изм. 1, 2, 3
| Объемная доля азота | не более 0,005% |
| Объемная доля кислорода | не более 0,0007% |
| Содержание влаги при норм. усл. | |
| Углеродосодержащие | не норм. |
Газообразный аргон транспортируется в стальных баллонах (ГОСТ 949-73) серого или черного цвета под давлением 150 кгс/см². Для перевозок автомобильным транспортом баллоны среднего объема помещают в металлические специальные контейнеры (поддоны).
Жидкий аргон заливают в специальные цистерны с порошковой, вакуумно-порошковой или вакуумно-многослойной изоляцией, предназначенной для перевозок жидкого аргона.
granat-e.ru
Плотность аргона (Ar), значение и примеры
Плотность аргона и другие его физические свойства
Молекулы аргона одноатомные и взаимодействуют друг с другом лишь за счет слабых лондоновских сил.
Аргон образует клараты на основе воды и гидрохинона, например, состава 8Ar×46Н2О. Плохо растворяется в воде (растворимость понижается в присутствии сильных электролитов), лучше — в органических растворителях.
Важнейшие константы аргона приведены в таблице ниже.
Таблица 1. Физические свойства и плотность аргона.
|
Плотность, г/см3 |
1,784×10-3 |
|
Температура плавления, oС |
-248,6 |
|
Температура кипения, oС |
-246,1 |
|
Стандартная энтальпия испарения, кДж/моль (20 oС) |
1,74 |
|
Растворимость в воде при 20oС, мл/л |
10,5 |
Распространенность аргона в природе
Аргон содержится, главным образом, в воздухе (его содержание составляет 0,932% (об.), 1,28% (масс.)), являясь сырьем для его промышленного получения.
Краткая характеристика химических свойств и плотность аргона
Аргон не реагирует со всеми другими веществами (простыми и сложными).
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Аргон: факты и фактики
А. Мотыляев
«Химия и жизнь» №7, 2015
Как аргон поставил в тупик Д. И. Менделеева и других именитых химиков? Первым аргон открыл Генри Кавендиш в 1795 году: он несколько недель пропускал электрический разряд сквозь воздух, при этом кислород реагировал с азотом (их тогда называли «дефлогистонный воздух» и «флогистонный воздух» соответственно) и давал азотистую кислоту, которую поглощал поташ. Объем газа в сосуде уменьшался, однако газ не исчезал полностью: оставалось что-то, не вступающее в реакцию. Никто на открытие Кавендиша особого внимания не обратил. Но вот в 1882 году лорд Рэлей начал серию нудных опытов по измерению плотности газов. И все время у него получалось, что соотношение веса водорода и изучаемого газа немного меньше целочисленного. Физикам же, еще не подозревавшим о существовании изотопов, очень хотелось, чтобы оно было целочисленным. Желая найти источник ошибки, Рэлей решил получить чистый, не атмосферный, азот. Для этого он прогнал над раскаленной медью смесь аммиака с кислородом: аммиак разлагался, давая азот и воду. Такой азот оказался на полпроцента легче, нежели атмосферный. А в 1894 году Уильям Рамзай обнаружил, что азот поглощается раскаленным магнием. Он-то и решил выделить обнаруженную Рэлеем тяжелую примесь к азоту. Вскоре в руках Рамзая оказалось 40 мл газа, который не поглощался магнием. Измерения показали, что его молекулярный вес равен 40. Поскольку все известные на тот момент газы были двухатомными, получался атомный вес 20, что выглядело странно — тяжелее фтора, легче натрия. Одноатомный же газ был бы слишком тяжелым и никак не вписывался в Периодическую таблицу — такой элемент следовало поставить между двумя металлами — калием и кальцием. Поэтому возникла гипотеза, что Рамзай обнаружил трехатомный азот, благо 40 примерно в три раза больше, чем 14. Вот как Менделеев пишет об этом в «Дополнении к 5-й главе» шестого издания «Основ химии»: «Гипотеза А=40 вовсе не дает места аргону в периодической системе… Мне кажется более простым предположение, что аргон содержит N3, особенно потому, что аргон содержится в азоте…» Рэлей, огорченный неприятием его нового газа, больше химией не занимался и Нобелевскую премию получил в 1904 году по физике за исследование плотностей газов и открытие в связи с этим аргона. А Рамзай за открытие и исследование элементов нулевой группы получил в том же году премию по химии.
Почему аргон с весом 39,9 стоит в таблице перед калием, вес которого 39,1? У аргона есть три устойчивых изотопа с весами 36, 38 и 40. Во Вселенной больше легких изотопов, а аргона-40 очень мало. При этом аргона в планетарных туманностях и в веществе звезд много, он преобладает над такими распространенными на Земле элементами, как калий, кальций, фтор и хлор. А вот на нашей планете и самого-то аргона немного, и его легких изотопов ничтожно мало — видимо, они улетели на периферию Солнечной системы. Аргон-40 мы не унаследовали из протопланетного облака; он образуется здесь и сейчас — в результате радиоактивного превращения калия-40. Обычно у этого изотопа, обеспечивающего основную часть природного фона излучений, нейтрон становится протоном с испусканием позитрона, и получается следующий элемент — кальций-40. Но в каждом пятом случае происходит так называемый К-захват: электрон с нижней орбитали падает в ядро, один из протонов становится нейтроном с испусканием нейтрино, атом же уходит на предыдущую клетку Периодической системы. Именно из-за недостатка легких изотопов аргона на Земле его вес, измеренный химиками, оказался больше, чем у следующего за ним калия, представленного всеми изотопами.
Есть ли на Земле радиоактивный аргон? В природе радиоактивного аргона почти нет, поскольку самый долгоживущий — аргон-39 — имеет период полураспада 269 лет. Однако высокоактивный аргон-41 с периодом полураспада 1,85 часа непрерывно образуется в атомном реакторе, а при неисправностях в системе вентиляции может попасть и за его пределы. После запуска термоядерного реактора проблема усложнится. Согласно расчету Владимира Хрипунова из Курчатовского института (Fusion Engineering and Design, 2015, DOI:10.1016/j.fusengdes.2015.02.058), при массированной нейтронной бомбардировке — напомним, что именно за счет торможения нейтронов стенками токамака планируется снимать тепло, выделяющееся при термоядерном синтезе, — начнет образовываться аргон-39 в достаточном количестве, чтобы вызвать беспокойство за здоровье работников термоядерной станции.
Как аргоном измеряют время? Калий — один из самых распространенных элементов на Земле и других каменистых планетах, а период полураспад калия-40 — 1,3 млрд лет. Постоянно образующийся аргон-40 оказывается заключенным в любую горную породу, и его количество растет начиная со времени ее затвердевания. Соответственно по соотношению аргона-40 и калия-40 можно узнать, когда эта порода (как правило, речь идет о базальте) была извержена из недр планеты. Измерения проводят, бомбардируя аргон-40 потоком нейтронов: получается короткоживущий аргон-41, его распад легко заметить. Аргоном удается мерить время в масштабе от сотен миллионов до десятков тысяч лет, то есть когда углеродный метод работает уже неточно. За разработку метода профессор Э. К. Герлинг получил в 1963 году Ленинскую премию. В частности, аргоновым методом по возрасту окружающих камешков были датированы первые, найденные в Олдувейском ущелье в Кении, останки человека умелого Homo habilis, его возраст оказался 1,7 млн лет (см. «Химию и жизнь», 1967, №6). В числе последних достижений — новая датировка Деканских траппов (Journal of Asian Earth Sciences, 2014, 84, 9–23, DOI:10.1016/j.jseaes.2013.08.021), крупнейшего разлива лавы, занимающего треть Индостана с западной его стороны. Как оказалось, возраст наиболее объемных разливов статистически неотличим от даты катастрофы, погубившей динозавров. Падение же метеорита в районе Юкатана, создавшее кратер Чиксулуб, по новейшим данным произошло на 300 тысяч лет раньше массового вымирания. Вообще, деканская гипотеза давно конкурирует с чиксулубской.
В какие реакции вступает аргон? Не имея свободных электронов и потому будучи химически инертным, аргон образует химические соединения неохотно и в весьма экзотических условиях. Однако он формирует так называемые клатратные соединения: атом аргона может оказаться заключенным в полость, образованную какой-то молекулой, либо в кристаллической решетке другого вещества. Подобно ксенону, аргон способен образовывать и соединения с белками; в результате при повышенном давлении аргон-кислородная смесь вызывает потерю сознания — аргоновый наркоз.
Чем опасен аргон? При работе с установками, заполненными аргоном, следует соблюдать меры предосторожности: аргон — тяжелый газ, он скапливается во всевозможных углублениях, например колодцах, вытесняя оттуда кислород, то есть может создать атмосферу, непригодную для дыхания. Если рабочий, потеряв сознание, упадет в такое углубление, он задохнется. Материаловеды, работающие с аргоном, говорят: «Аргон дырочку найдет», а изготовители оборудования это обстоятельство учитывают. Рассказывают такой случай. На одном предприятии ставили новый шведский газостат. Это огромная установка высотой с пятиэтажный дом, в которой можно подвергать детали нагреву и высокому давлению для устранения внутренних полостей в металле, образующихся при изготовлении. Чтобы избежать окисления детали, газостат заполняют инертным газом — аргоном. Поскольку копать вниз проще, чем строить вверх, газостат хотели заглубить, но изготовители категорически это запретили именно потому, что вытекающий из установки аргон нигде не должен скапливаться. А вот на растения аргон влияет хорошо: в атмосфере из 98% аргона и 2% кислорода семена лука, моркови и салата прорастают вполне успешно.
Зачем заполняют аргоном стеклопакет? Для повышения звукоизоляции и снижения теплопроводности — у аргона выше модуль упругости и ниже теплопроводность, чем у воздуха. Правда, с учетом правила «аргон дырочку найдет», не ясно, как долго этот газ будет находиться внутри стеклопакета.
Как получают аргон? При разделении воздуха на кислород и азот в колоннах высокого давления. Летучесть аргона больше, чем у кислорода, и меньше, чем у азота, — его и забирают из верхней трети колонны. Отделяют аргон также из отхода производства аммиака — того азота, что не израсходовался на реакцию с водородом; он сам собой оказывается обогащенным аргоном.
Как аргон применяют в технике? Будучи самым распространенным инертным газом — все-таки третий по значимости компонент атмосферы Земли после азота и кислорода, — аргон очень востребован, прежде всего в качестве вещества, не способного к химическим реакциям. Заполнив установку или весь цех аргоном, можно не бояться, что нагретая металлическая деталь или заготовка окислится либо насытится азотом с последующим выделением нитридов. Склонны к окислению, например, молибден и вольфрам: многие могли наблюдать мгновенное превращение спирали лампы накаливания в синеватый порошок при попадании в нее воздуха. В среде аргона обрабатывают титан, тантал, ниобий, бериллий, гафний, цирконий, а также уран, торий и плутоний. Продувая аргон через сталь в конвертере, из нее удаляют газовые включения. Революцию в технике совершил метод аргонно-дуговой сварки: поток аргона, подаваемый в то место, где горит электрическая дуга, вытесняет воздух и не дает металлу окисляться — оксиды снижают прочность шва, а то и вовсе делают сварку материалов невозможной. Таким методом сваривают легированные стали и цветные металлы, режут их толстые листы. Еще одно серьезное направление — распыление всевозможных материалов для получения чистого от оксидов порошка.

Что такое аргоновые кластеры? Пучки ионизированных кластеров — новый метод обработки поверхности до атомной гладкости. Его суть — бомбардировка не отдельными ионами (это называется «ионное травление»), а гораздо более тяжелыми частицами, состоящими из десятков, а то и тысяч атомов. Пучки аргоновых кластеров получили широкое распространение из-за инертности газа и его относительной дешевизны. Кластеры формируют, подавая газ под высоким давлением через узкое сопло. Проходя сквозь него, газовый поток резко расширяется и охлаждается; атомы аргона слипаются в твердое вещество, где их удерживают силы Ван-дер-Ваальса. Когда поверхность бомбардируют кластерами с высокой энергией, образуются кратеры размером в нанометры; такой будет и гладкость всей поверхности. Повторяя сканирование пучком менее энергичных кластеров, гладкость увеличивают. Таким методом обрабатывают полупроводники, тонкие пленки, поверхность дисков для компьютеров и многое другое. Кластерными пучками можно и создавать наноузоры на поверхностях. Они же позволяют, не нагревая образец, проводить послойное изучение его состава, постепенно забираясь все глубже и глубже; этот метод применяют для анализа строения органических веществ.
Как аргон работает в нанотехнологиях? Аргоновая плазма либо добавка аргона к плазме другого газа — важнейший метод получения всяческих наноструктур: сферических наночастиц, нанолезвий, наноигл. Суть плазменного метода состоит в том, что разделенное на ионы и электроны вещество обладает способностью активировать химические реакции и даже делает возможными те, что в нормальных условиях запрещены термодинамически. Аргон — прекрасный активатор: сам в реакцию не вмешивается, а продукты реакции либо конденсируются в равноосные частицы, либо оседают на поверхности, давая неравноосные структуры. Он же может служить разбавителем плазмы другого, реакционного газа — таким способом меняют параметры процесса. Наконец, высокотемпературную плазму аргона применяют для распыления металлической мишени и получения из нее нанопорошков с частицами заданного размера. Другие инертные газы — неон, ксенон — дают свои размеры. Применяют аргон и как охладитель: он выдувает порошок из зоны плазмы, что опять же позволяет регулировать размер частиц, поскольку тот зависит от времени нахождения материала в зоне плазмы.
Кому нужна пена с аргоном? С помощью аргона можно делать пористые шаблоны из желатина для последующего их заселения клетками при выращивании искусственных органов. Преимущество аргона здесь очевидно — его химическая инертность.
Что такое аргоновый лазер? В этом лазере, изобретенном в 1964 году, генератором света служит трубка, заполненная аргоном. Электроды создают в ней плазму с большой плотностью ионов аргона, а катушка, обмотанная вокруг трубки, формирует магнитное поле, еще больше увеличивающее плотность плазмы. Этот лазер дешевле твердотельных аналогов, дает мощное — 20–30 ватт — излучение в сине-зеленой части спектра, причем его цвет можно переключать между 14-ю спектральными линиями. Такие лазеры применяют для накачки других лазеров, для световых шоу, а также для стимулирования флуоресценции при химическом анализе сложных органических веществ. С его помощью, например, находят следы РНК в количестве пикограмм, то есть столько, сколько есть в одной клетке (Electrophoresis, 2015, DOI:10.1002/elps.201500117). Применяют аргоновый лазер и при лечении слепоты, вызванной диабетом, — она появляется из-за чрезмерного развития кровеносных сосудов в глазу, а лазером их можно безболезненно проредить.
Как аргоном проводят стерилизацию? Для уничтожения бактерий используют холодную аргоновую плазму. В такой плазме есть горячие электроны, а температура ионов равна комнатной, то есть она не может обжечь, но сохраняет способность активировать реакции. Реакции же эти зависят и от способа получения плазмы (от температуры ее электронов), и от добавок других газов. Например, облучение клеток млекопитающих в физиологическом растворе чистым или влажным аргоном давало прежде всего гидроксил-радикал, который угнетал развитие клеток. А вот плазма из аргона с добавками 1% кислорода или 1% воздуха давала, скорее всего, атомарный кислород. Реагируя с хлорид-ионом, он порождал радикалы Cl2– или ClO–, убийственно действующие на клетки, причем никакие ферменты-антиоксиданты вроде супероксиддисмутазы с ними справиться не могли. Время жизни таких радикалов оказалось на уровне получаса (Biointerphases, 2015, 10, 2: 029518; DOI:10.1116/1.4919710). Итог понятен: аргоновой плазмой можно проводить «холодную» дезинфекцию. Так, кишечную палочку на образце удается извести за 10 минут (Applied Biochemistry & Biotechnology, 2013, 171, 7; DOI:10.1007/s12010-013-0430-9), а с добавкой 0,5% кислорода — уже за 30 секунд (International Journal of Radiation Biology, 2009, 85, 4; DOI:10.1080/09553000902781105). Вообще, холодная плазма из различных газов очищает поверхность мяса, птицы, овощей, фруктов от таких микробов, как кишечная палочка, листерия, сальмонелла, золотистый стафилококк, за считаные секунды. И никакой антимикробной «химии», пугающей потребителя. Однако технология эта новая, оборудование не стандартизировано, каждый генератор дает свою плазму, и результаты опытов сравнивать трудно. Также неизвестно, как такая обработка повлияет на качество пищи при ее массовой обработке (Annual Review of Food Science & Technology. 2012, 3, 125-42; DOI:10.1146/annurev-food-022811-101132).
Как аргон применяют в медицине? Разными способами. Например, плазма может пригодиться для той же дезинфекции ран, хотя в случае с трофическими язвами результаты вышли неоднозначными: вроде бы число бактерий уменьшалось не так быстро, как при применении лекарства, однако язвы заживали с той же скоростью. Возможно, дело в том, что плазмой можно обрабатывать язвы меньшего размера и они заживают быстрее (Journal of Wound Care, 201, 24, 5; DOI:10.12968/jowc.2015.24.5.196). Плазменное лечение не вызывает таких побочных действий, как лекарственные средства, поэтому авторы рекомендуют продолжить исследования с разными источниками плазмы, тем более что устойчивости к ней не может развиться по определению, чего о лекарствах не скажешь.
С помощью специально придуманной плазменной щетки удается уничтожать и бактерии, вызывающие кариес. Но здесь есть нюансы. Так, основными вредителями зубов считаются Streptococcus mutans и Lactobacillus acidophilus, которые образуют на эмали бактериальные маты и выделяют много кислоты. У стрептококка клетки маленькие, и они разрушаются всего за 13 секунд. А у лактобактерии — большие, образующие толстые слои, и, чтобы избавиться от них, нужны уже минуты (Journal of Dentistry, 2011, 39, 1; DOI:10.1016/j.jdent.2010.10.002). Вряд ли такая щетка появится в быту, а вот стоматологу для дезинфекции свежеобработанного дупла пригодится. К тому же плазма изменяет поверхность вещества зуба, что увеличивает прочность ее соединения с пломбой на 60%. Тут главное — не перестараться: эффект дает обработка в течение 30 секунд, а несколько минут, наоборот, ухудшают сцепление (European Journal of Oral Science. 2010, 118, 5; DOI:10.1111/j.1600-0722.2010.00761). Аргоновой плазмой можно быстро остановить кровь при внутреннем кровотечении. Вдыхание аргона защищает нейроны, пострадавшие от ишемического удара или вследствие травмы (PLoS One, 2014, 9, 12:e115984, DOI:10.1371/journal.pone.0115984).

Как работает аргоновая криохирургия? Криохирургия — это уничтожение больных тканей в результате их быстрого замораживания. Ее применяют по самым разным показаниям, от сведения бородавок и сглаживания шрамов до удаления опухолей. Если бородавки замораживают снаружи ваткой, смоченной в жидком азоте, то шрамы и опухоли — изнутри, вводя в них полую иглу — криозонд, через которую прокачивают холодное вещество. Используют еще и криоаппликаторы — их на замораживаемый объект накладывают. Установка с жидким азотом — гораздо проще и дешевле, но в ней применяют толстые, диаметром 6 мм, зонды. Аргоновая же устроена гораздо сложнее, требует высокой квалификации персонала, в частности специальных знаний по работе с высоким давлением, но позволяет очень точно замораживать ткань: диаметр иглы может быть величиной с миллиметр, такая игла легко проходит сквозь кожу. Заморозку проводят газообразным аргоном. Газ хранят под давлением 400 атмосфер, а, проходя через узкое сопло и затем резко расширяясь, он вследствие эффекта Джоуля—Томсона охлаждает до –140°С. Если термодатчики, воткнутые рядом с местом заморозки, показывают, что температура слишком упала и могут пострадать здоровые ткани, в зонд подают гелий, который отогревает замерзшую ткань. Так можно проводить циклы контролируемого замораживания-размораживания, что увеличивает эффективность процедуры, да и примерзший криозонд проще извлекать.
Как аргоновый резак используют хирурги? С помощью аргонового плазменного резака можно проводить удивительные по виртуозности операции — подрезать стенты, вставленные в кишечник, или тонкие протоки пищеварительной системы, например те, что доставляют желчь и секрет поджелудочной железы. В силу разных причин (опухоль, камни и подобное) проток может перекрыться. Для лечения туда вставляют трубочку — стент, например, из интерметаллида NiTi — нитинола. Изначально ее диаметр невелик, а попав на место и нагревшись, изделие, в силу эффекта памяти формы нитинола, увеличивается в размере и расширяет просвет сосуда. Однако может получиться так, что размер стента выбран неверно либо со временем из-за изменений в организме становится неподходящим. Кроме того, стент может зарасти или сдвинуться с места и так перекрыть канал, что к нему не подберешься с тем эндоскопом, которым этот стент размещали. Тогда вводят плазменный резак мощностью в несколько десятков ватт и подрезают стент. Во многих случаях эта операция проходит вполне успешно, никаких повреждений сосудов и кровотечения не вызывает (а если и вызовет, той же плазмой можно остановить кровь), но для самочувствия пациента она гораздо лучше, нежели изъятие старого стента и установка нового (Endoscopy, 2005, 37, 5,434–438). Это важно, поскольку возраст пациента может быть преклонным.
elementy.ru
Способы получения аргона | Сварка и сварщик
Как уже говорилось в статье «Аргон – самый ленивый газ», содержание аргона в воздухе довольно значительно, поэтому его добывают как побочный продукт, при получении кислорода и азота из воздуха методом низкотемпературной ректификации в специальных аппаратах.
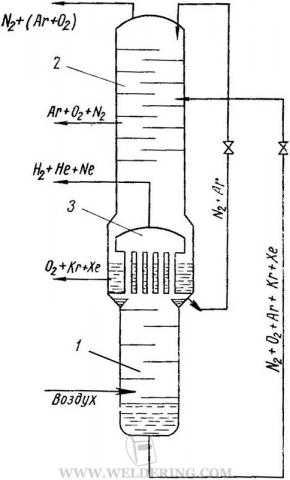
1 – колонна высокого давления;
2 – колонна низкого давления
3 – промежуточный койденсатор-испаритель
Схема аппарата двойной ректификации воздуха
Аргон по летучести занимает промежуточное положение между азотом и кислородом – основными компонентами воздуха. Этим и объясняется специфическое поведение аргона при ректификации жидкого воздуха. Окончательное разделение жидкого воздуха на азот и кислород производится в колонне низкого давления воздухоразделительного аппарата. Дистиллятом этой колонны является газообразный азот, а нижним продуктом – газообразный или жидкий кислород.
В верхней части колонны низкого давления аргон выступает в роли тяжелолетучего (по сравнению с азотом) компонента, а в нижней части – легколетучего (по сравнению с кислородом). Этим объясняется существование в колонне низкого давления зон повышенной концентрации аргона в обеих секциях колонны – концентрационной (выше ввода жидкости из куба колонны высокого давления) и отгонной (ниже ввода). На распределение аргона по тарелкам ректификационной колонны низкого давления сильно влияет сопутствующий ему третий компонент – кислород. Содержание аргона в зоне повышенной концентрации верхней секции колонны возрастает по мере уменьшения содержания кислорода в дистилляте при неизменном составе продукционного кислорода (этого можно достичь увеличением числа тарелок в колонне).
Схематично процесс добычи аргона описывается следующим образом. Вначале воздух очищается от пыли и сжимается до сжижения. Жидкий воздух подвергается ректификации с целью разделения его на составные части. Получающаяся аргоно-азотно-кислородная смесь (сырой аргон) затем очищается от кислорода и азота. Разделение воздуха и попутное извлечение из него аргона в промышленном масштабе осуществляется путем сжижения и ректификации при низкой температуре. Жидкий кислород под давлением 101 кПа кипит при температуре -182,9°С, а жидкий азот – при температуре -195,8°С. Поэтому пары жидкого воздуха при кипении обогащаются легкокипящим азотом, температура кипения которого почти на 13°С ниже, чем у кислорода. Одновременно происходит обогащение кипящей жидкости кислородом. Благодаря этому, в ректификационной разделительной колонке, где непрерывно кипит жидкий воздух и конденсируются его пары, удается получить одновременно кислород (в нижней части) и азот – (в верхней части). Большая часть жидкого аргона, температура кипения которого -185,3°С, скапливается в средней части колонки, откуда в смеси с кислородом и азотом отводится (так называемая аргонная фракция) в специальную аргонную колонну, смонтированную вместе с воздухораспределительным аппаратом. Здесь аргонная фракция (содержащая 8-12% аргона, 0,2-0,3% азота, остальное – кислород) подвергается дополнительной ректификации и обогащается аргоном до 85-95% (остальные 15-5% составляет смесь азота и кислорода). Этот продукт называют сырым аргоном, из него на последующих этапах очистки получают чистый аргон.
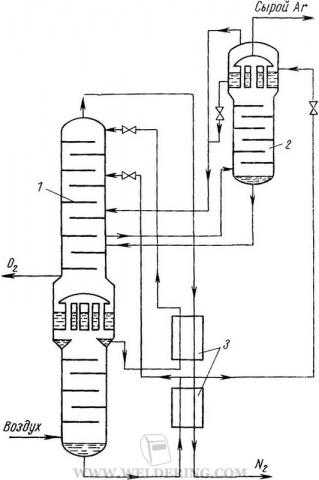
1 – воздухоразделительный аппарат
2 – аргонная колонка
3 – переохладитель
Присоединение аргонной колонны к аппарату двойной ректификации воздуха
Сырой аргон от кислорода можно очищать несколькими способами. Один из них основан на каталитическом окислении водорода, содержащегося в сыром аргоне, при температуре 400-500° С. Вследствие тоге, что при этом способе продукты реакции смешиваются с очищенным аргоном, необходимо, чтобы они легко отделялись от него. Для этой цели применяется только электролитический водород, не содержащий примесей, загрязняющих аргон. Так как при этом способе очистки содержание кислорода не должно быть более 2-2,5%, в схеме предусмотрена циркуляция газа для разбавления сырого аргона очищенным газом, не содержащим кислорода. Циркуляция газа осуществляется с помощью газодувки.
Водяной пар, полученный в результате соединения водорода с кислородом в контактном аппарате, конденсируют в холодильнике и удаляют через влагоотделитель, после чего газ осушают. Полученная смесь аргона с азотом подвергается ректификации по схеме, которая аналогична применяемой при ректификации воздуха. При этом используется насос для жидкого аргона, что позволяет избежать загрязнения чистого аргона при его сжатии и заполнении баллонов. При помощи компрессора смесь аргона и азота сжимается и через ресивер подается в блок адсорбционной осушки, где из нее удаляются остатки влаги. После этою через теплообменник смесь поступает в ректификационную колонку, где охлаждается до температуры сжижения выходящими из колонки продуктами разделения – азотом и аргоном.
Для обеспечения условий ректификации и восполнения потерь холода в ректификационную колонку подают жидкий азот и парообразную кислородно-азотную смесь из основного воздухоразделительного аппарата. Чистый аргон собирается в нижней части колонки, а «отбросный» азот отводится в атмосферу из верхней части колонки через теплообменник.
Существуют и другие способы получения аргона, например при производстве синтетического аммиака. Его получают при синтезе азотно-водородной смеси в колонках. В продувочном газе содержится 10-19% аргона, и именно из этого газа его и извлекают. Считается, что аргон, выделенный при производстве аммиака, имеет более низкую себестоимость.
В любом случае качество газа зависит от совершенства систем очистки и от точности определения малых примесей азота, кислорода, водорода и паров воды в аргоне.
weldering.com
Где применяют газ аргон?
Аргон представляет собой одноатомный инертный газ, он не имеет вкуса, запаха и цвета. А в периодической таблице Менделеева порядковый номер аргона восемнадцатый. Стоит сказать, что этот газ в природных условиях распространен не в соединениях химического характера, а в свободном виде. Воздух нашей планеты содержит в себе 0,95 % аргона. Кстати, этот газ есть в морской воде и земной коре.

Аргон впервые был открыт в 1882 году Джоном Рэлеем, знаменитым английским физиком. Благодаря опытам и научным экспериментам Рэлей обнаружил, что переработанный литр азота более увесист, чем тот же литр вещества, полученного после распада азотистого соединения.
Опубликованное открытие позволило выдвинуть гипотезы о том, что имеются существенные разницы о величинах плотности газа, полученного двумя совершенно разными способами. Физики предположили что азот, выделившийся из воздуха, имеет в себе неизвестный газ с более высокой плотностью. Опыты продолжились, и позже был выделен аргон. Это самый инертный из газов, известных в девятнадцатом веке. В 1894 году учеными был сделан официальный доклад об аргоне и его свойствах.
Свойства аргона
Аргон является одноатомным газом. Он не имеет запаха, лишен цвета и вкуса. В стандартных атмосферных условиях плотность аргона составляет 1, 7839 кг/ м3. Примерно в ста миллилитрах обычной воды может раствориться около трех миллилитров аргона.
Температура кипения газа составляет минус 185 градусов по Цельсию, а температура плавления равна 189 градусам. У аргона имеется два химических соединения (HArF и CU(Ar)O). Эти соединения получаются при низкой минусовой температуре. Синтезируют аргон при помощи процедуры разделения воздуха на азот и кислород.
Применение газа
Аргон стоит довольно дешево и при этом он очень востребован в разнообразных промышленных сферах. Например, этот газ имеется в обычных лампах накаливания. Когда-то давно для этих целей использовался азот. Этот газ используется также в металлургической промышленности и в подобных смежных отраслях.
Плюс использования данного газа заключается в том, что он помогает не допустить вредный контакт металла с воздухом. Аргон используется в медицине. Он инертен, и это позволяет очищать инструменты, им также обрабатывают гидрокостюмы и используют как пропеллент для обычных аэрозольных упаковок.
В нашей компании вы можете купить аргон в баллонах с доставкой или самовывозом.
Меры безопасности
Аргон не взрывоопасен и не токсичен для человека. Но его высокая концентрация в воздухе может нанести вред человеку, так как может начаться кислородное голодание мозга, сопровождающееся потерей сознания и резкими головокружениями. Хоть аргон и не горючее вещество, но обращаться с ним надо аккуратно, так как при его нагревании повышается и его давление.

Контакт с жидкостью, содержащий аргон может вызвать серьезное обморожение конечностей. А при попадании аргона в глаза наступает потеря зрения, и появляются ожоги сетчатки. Поэтому при работе с аргоном следует обязательно носить защитную спецодежду и респираторы.
Следует помнить и о том, что аргон тяжелее воздуха в своем газообразном состоянии. И утечка газа из баллона может серьезно повлиять на физическое состояние человека. Обычно в промышленности при работе с аргоном используется шланговый противогаз или изолирующий прибор. Внимательно отслеживается уровень аргона в окружающем воздухе. По всем нормативам кислорода в помещении должно быть не менее девятнадцати процентов.
kriogenservis.ru
гелий, неон, аргон, криптон, ксенон и радон
Общая характеристика инертных газов
Каждый период Периодической системы заканчивается инертным газом, кроме гелия, все они имеют на внешнем энергетическом уровне по 8 электронов, образующих очень устойчивую систему, в связи с чем эти элементы получили название инертных. Несмотря на то, что электронная оболочка гелия состоит из двух электронов, она также очень устойчива. В связи с этим явлением атомы инертных газов обладают высокими значениями энергий ионизации и, как правило, отрицательными значениями энергии сродства к электрону.
Электронная конфигурация внешнего энергетического уровня инертных газов – 1s2 (He) и ns2np6 для других инертных газов.
Изначально предполагали, что атомы инертных газов не способны к образованию химических связей с другими элементами. Были известны лишь несколько нестойких соединений благородных газов – гидраты аргона, криптона и ксенона (Ar×6H2O, Kr×6H2O, Xe×6H2O), которые получались при действии инертных газов на кристаллизующуюся переохлажденную воду.
Позже, было установлено, что Kr, Xe и Rn вступают в реакции взаимодействия с другими веществами, например, с фтором, при нагревании или электрическом разряде. Для ксенона известны оксид – XeO3 и гидроксид- Xe(OH)6.
Наибольшее практическое применение среди всех благородных газов находят аргон, неон и гелий.
Гелий
По физическим свойствам гелий наиболее близок к молекулярному водороду. В связи с малой поляризуемостью атома гелия, у него самые низкие температуры кипения и плавления, по сравнению с другими элементами VIIIA группы. Однако, он хуже, чем другие инертные газы растворим в воде.
В обычных условиях гелий химически инертен, но в возбужденном состоянии он способен образовывать неустойчивые молекулярные ионы He2+ или ионизированные молекулы HeH+.
Гелий – наиболее распространенный из элементов космоса, после водорода и состоит из двух изотопов — 4He и 3He. Доказано присутствие гелия в атмосфере Солнца, звезд и в метеоритах.
Гелий получают из некоторых природных газов методом глубокого охлаждения, при этом гелий остается в газообразном состоянии, в то время как другие газы конденсируются.
Гелий нашел применение в атомной энергетике, при автогенной сварке металлов, в физических лабораториях в качестве хладоносителя. Изотоп гелия 3 He – единственное вещество, пригодное для измерения температур ниже 1К.
Неон. Аргон
Основное отличие неона от гелия – большая поляризуемость атома, склонность к образованию межмолекулярных связей, несколько большая растворимость и способность адсорбироваться.
Агрон, как и неон, имеет 8 электронов на внешнем энергетическом уровне и, вследствие высокой устойчивости электронной структуры атома неона, он не способен к образованию соединений валентного типа. Аргон образует молекулярные соединения включения – клатраты – с водой, фенолом, толуолом и другими веществами. С сединениями H2S, SO2, CO2, HCl аргон дает двойные гидраты, т.е. смешанные клатраты.
Неон и аргон получают из воздуха путем его разделения при глубоком охлаждении. Аргон, в связи с его сравнительно высоким содержанием в воздухе, получают в значительных количествах, неон – в меньших.
Неон и аргон применяют в качестве наполнителей ламп накаливания, газосветных трубок (для неона характерно красное свечение, для аргона – сине-голубое). Аргон, как наиболее доступный из инертных газов, используют в металлургии, в частности при аргонно-дуговой сварке алюминиевых и алюминиевомагниевых сплавов.
Подгруппа криптона
Энергия ионизации элементов подгруппы криптона (Kr, Xe, Rn) характеризуются меньшими значениями энергии ионизации, чем типические элементы VIIIA группы, поэтому могут образовывать соединения обычного типа. Так, ксенон может проявлять степени окисления «+2», «+4», «+6», «+8».
Криптон применяют в электровакуумной технике, в смеси с ксеноном его используют в качестве наполнителя для различного вида осветительных ламп и трубок. Радиоактивный радон используют в медицине.
Примеры решения задач
ru.solverbook.com

