Из оксида кальция получить карбид кальция – Как получить карбид кальция (CaC2) из оксида кальция (CaO)
alexxlab | 26.02.2017 | 0 | Вопросы и ответы
CaO -> CaC2 уравнение реакции
Оксид кальция (негашеная / жженая известь) представляет собой белый гигроскопичный порошок. Тугоплавкий, термически устойчивый, летучий при очень высоких температурах. Энергично реагирует с водой (образуется щелочной раствор). Проявляет основные свойства, реагирует с кислотами. Поглощает углекислый газ из воздуха.
В результате взаимодействия оксида кальция с коксом происходит образование карбида кальция и выделение угарного газа (CaO -> CaC2). Реакцию проводят в температурном диапазоне . Молекулярное уравнение реакции имеет вид:
Для получения оксида кальция в промышленности наиболее часто принято использовать следующие реакции:
ru.solverbook.com
Как получить карбид кальция
Как получить карбид кальция
Наверное, каждый человек помнит свои веселые школьные дни. А особенное веселье приходилось на момент проведения ремонтных работ в здании школы, когда рабочие, помимо всего прочего оборудования, приносили с собой генератор ацетилена и бочку карбида кальция. Такие дни были страшным сном для работников всех школ, начиная с директора и заканчивая уборщицей потому, что карбид кальция – это любимое развлечение школяров. Нет счету испорченным унитазам в школьных туалетах. Вот такой он карбид кальция. 
- Тигель (желательно графитовый), графитовый электрод, оксид кальция (негашеная известь), кокс, источник тока.

- Карбонат кальция в виде известняка или мела. Керамический тигель для отжига. Пропановая или ацетиленовая горелка.
- Запишите уравнения реакций, с помощью которых можно

- Азотная кислота. Карбонат кальция. Стеклянная реторта. Посуда для выпаривания соляного раствора. Газовая горелка или спиртовка.
www.kakprosto.ru
Карбид кальция
Что такое «карбид», знает любой мальчишка. Если бросить кусочек карбида в лужу, то кроме дикого шипения получается еще дичайшая вонь. А как получается сам карбид?
Вообще карбидов существует множество, как и применений ему. Но нас пока интересует карбид кальция CaC2 — то есть тот, который используют для получения ацетилена при соединении карбида с водой.
Слишком сложного в получении карбида кальция нет. Сейчас для этого в электропечах пережигают негашеную известь с коксом. При всей этой простоте — впервые карбид кальция был получен в лаборатории в 1836-м году, а промышленно его начали получать в 1892 году. Для попаданца — широчайшее поле для внедрения!
Все реакция — CaO + 3C = CaC2 + CO Негашеная известь соединяется с углеродом. Негашеную известь получали с древних времен, пережигая известняк, ну и древесный уголь тоже дефицитом не был никогда. Полученный попутно угарный газ (СО) окисляется до углекислого газа прямо при выходе из печи, хотя сейчас часто печи делают закрытыми для сбора угарного газа. На 100 весовых частей негашеной извести нужно 70-80 весовых частей углерода. При производстве лучше иметь избыток угля, чем извести — такой карбид отдает больше ацетилена. Готовый карбид кальция технического качества почти на 80% состоит из самого карбида кальция, 17% — известь, остальное примеси.
Карбид выходит в виде расплава, который после затвердевания измельчают.
Но, несмотря на простоту реакции получения, есть некоторые неприятные нюансы. Главное — процесс этот эндотермический, он поглощает дикое количество тепла в процессе производства — 3000 кВт на тонну продукта. Именно из-за этого его делают электродуговым способом. При этом сам процесс идет в жидкой фазе — то есть расплавленная известь постепенно реагирует с кусками углерода. При этом нужна температура примерно 2000°С, что совсем немало. И что совсем неприятно — при перегреве до 2200-2400°С карбид кальция распадается на составляющие.
Поэтому, если нам не доступно электричество в больших объемах, у нас есть два выхода.
Первый — это плавить в тигле. Проблема в том, что тигель должен выдержать эти самые 2000°С, а в древние времена ни графитовый, ни вольфрамовый тигель нам будут недоступны.
Второй — построить небольшую доменную печь. Требуемое тепло даст избыточное количество угля. Уголь и известь насыпаются туда слоями и печь поддувается большим количеством воздуха. Такие печи пытались строить и главная проблема — поддержка точных условий реакции, что регулируется силой поддува. С одной стороны — такую печь можно построить только когда уже работают доменные печи для железа. А с другой стороны — а нам точно нужен карбид, если нет даже железа?
Трудность вызовет хранение карбида. Он должен быть абсолютно изолирован от воды — много лучше, чем порох. Потому что если порох намокнет, то он не взорвется, а если намокнет карбид — то взрыв обеспечено. И что хуже всего — при хранении не должна использоваться медь, серебро или золото.
Проблем с производством карбида будет немало. Но при каком производстве их будет мало? Зато все проблемы — решаемые чуть ли не с технологиями Древнего Египта.
А пользы от карбида будет много…
И последнее — ацетилен, который получается после контакта карбида с водой — ничем не пахнет, человек просто не имеет обонятельных рецепторов для него. Та вонь, по которой мы безошибочно определяем карбид — это примеси, которых в техническом карбиде несколько процентов.
www.popadancev.net
Карбид кальция – это… Что такое Карбид кальция?
Карби́д ка́льция (углеро́дистый ка́льций, ацетилени́д кальция) — CaC2 — в чистом виде белое кристаллическое вещество. Соединение кальция с углеродом.
История получения
Впервые получен в 1862 г. Ф. Вёлером нагреванием сплава цинка и кальция с углём.
Получение
В настоящее время получают прокаливанием в электрических печах (температура 1900—1950 °C) смеси оксида кальция с коксом.
Полученный таким образом технический продукт имеет грязную окраску вследствие загрязнения углём и другими красящими примесями. Он содержит также примеси фосфида и сульфида кальция, вследствие чего такой карбид кальция и полученный из него ацетилен имеют неприятный запах.
Свойства
При соединении с водой разлагается, образуя ацетилен и гидроксид кальция (гашеную известь).
CaC2 + 2h4O → C2h4 + Ca(OH)2Применение
Карбид кальция широко применяют в технике для производства ацетилена, цианамида кальция (при нагревании с азотом), а также для восстановления щелочных металлов.
См. также
| В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 31 мая 2011. |
dic.academic.ru
Как получить ацетилен из карбида кальция
Ацетилен – самый простой представитель класса алкинов, имеет химическую формулу С2Н2. Бесцветный газ, горюч, в смеси с воздухом взрывоопасен. Благодаря наличию тройной связи в своей молекуле, весьма активен с химической точки зрения, легко вступает в реакции присоединения. При сгорании выделяет большое количество тепла, что может быть использовано, например, многим известная «ацетиленовая горелка». Как же его синтезировать? При хранении ацетилена следует учитывать его особенности. Например, его нельзя держать в баллонах, имеющих бронзовый вентиль, поскольку газ реагирует с медью, входящей в состав бронзы, образуя чрезвычайно взрывоопасное вещество – ацетиленид меди. Самый старый, проверенный временем метод получения ацетилена – реакция карбида кальция с водой. Наверное, многие мальчишки в детстве развлекались, бросая кусочки карбида в лужу, тут же начиналось яростное шипение, карбид буквально «бурлил», исчезая на глазах, и в воздухе отчетливо пахло чем-то резким, «острым». Эта реакция протекает таким образом: СаС2 + 2Н2О = С2Н2 + Са(ОН)2 Для того чтобы она протекала не слишком бурно, можно использовать не простую воду, а насыщенный раствор хлорида натрия, например. Если этот опыт планируется показать на уроке химии, следует подобрать реакционную колбу подходящего размера. Если она будет слишком маленькой, то образующая при растворении карбида пена может быть «выброшена» давлением ацетилена в отводную трубку, и дальше – в приемный сосуд. В случае же с чересчур большой колбой, придется долго ждать, пока образующийся ацетилен не вытеснит весь воздух из прибора. Воду, а лучше насыщенный раствор хлорида натрия, следует добавлять в колбу с кусочками карбида медленно, по каплям, регулируя скорость реакции, не допуская, чтобы она протекала чересчур бурно. Используется ацетилен в самых разных областях. Например, как сырье для получения целого ряда химических веществ (уксусной кислоты, пластмасс, некоторых ароматических углеводородов, некоторых видов синтетического каучука, этилового спирта и т.д.). На его основе синтезируют некоторые очень сильные взрывчатые вещества, используемые в качестве инициаторов, т.е. для детонации. Повсеместно применяется при резке и сварке металлов, при получении яркого света в автономных светильниках. Как получить ацетилен из карбида кальция
www.kakprosto.ru
www.moscow-vitaminp.ru
Карбид кальция | khimie.ru
Карбид кальция — собственно ацетилид кальция (ибо его можно производить от ацетилена), обычно называемый просто карбидом, образует в чистом виде бесцветную кристаллическую массу удельного веса 2,22, Он нерастворим ни в одном из обычных растворителей. Водой разлагается с образованием ацетилена. Из оксидов металлов он выделяет при высокой температуре свободные металлы или взаимодействует с ними с образованием карбидов соответствующих металлов и оксида кальция. С азотом карбид кальция при нагревании переходит в цианамид кальция СаСN2.
Технически карбид получают нагреванием жженой извести с коксом; или древесным углем в электрических почах. Электроды состоят из больших угольных брусков, через которые пропускают ток до 50000 А.
При получении в технических масштабах на каждый килограмм 85% -ного карбида расходуется около 1 кг едкой извести, 0,7 кг кокса и 2,8-3,5 квт-ч электроэнергии.
Для получения карбида в небольших количествах лучше всего поступать следующим образом в плавильном тигле средней величины стачивают наждачным кругом дно, так что образуется отверстие, через которое вставляется уголь дуговой лампы толщипой 13-15 мм.
Верхнюю часть угля вдвигают приблизительно на 2 мм в тигль, укрепляют его в этом положении при помощи глины и соединяют через сопротивление и амперметр с отрицательным полюсом электрической сети. Анодом служит твердый заостренный уголь длиной 10-15 см, толщиной 7 мм, укрепленный зажимом на стеклянном штативе, который для удобства передвижения угля вверх и вниз целесообразно снабдить зубчатым механизмом. Реакционную смесь приготовляют, тщательно перемешивая 15 г тонко измельченного порошка оксида кальция с 20 г порошка древесного угля. Сначала насыпают очень немного этой смеси и включают ток силой примерно 12-14 А. Вместо постоянного тока можно пользоваться и переменным. Во время опыта, продолжающегося около 10-15 мин, понемногу подсыпают смесь. Кроме того, тигель следует закрыть асбестовым листом с проделанным в нем отверстием. Расстояние между углями, равное вначале 1 см, во время опыта доводят до 5-6 см. Количество карбида, получаемого при помощи такого простого устройства, достаточно для приготовления нескольких литров ацетилена.
Помимо получения ацетилена, карбид кальция. расходуется прежде всего для получения цианамида кальция. Кроме того, его используют в качестве восстановителя в металлургии.
Чистый СаС2 обладает, как показал Франк, решеткой иной структуры, чем загрязненный примесями и технический карбид. Последний кристаллизуется, образуя тетрагональную гранецентрированную решетку, так же как чистый SrС2 и ВаС2. Карбид кальция, содержащий СаСN2, образует иную решетку. Чистый СаС2 легко, а технический с большим трудом превращается в СаСN2.
Ваш отзыв
Вы должны войти, чтобы оставлять комментарии.
khimie.ru
Способ получения карбида кальция
Изобретение может быть использовано в химической промышленности и охране окружающей среды. Твердые бытовые отходы, например бумагу, картон, дерево, кожу, пластмассу, текстиль, подвергают пиролизу. Продукты пиролиза с содержанием летучих 4-10 масс.% и зольностью не выше 6 масс.% используют в качестве углеродистого восстановителя при плавлении извести в электротермической печи. Плавление ведут в режиме печи сопротивления при удельной плотности тока на электроде 1,5-2,0 А/см2 с использованием полых электродов. Расплав охлаждают в печи и извлекают. Содержание СаС2 – 85 масс.%, литраж – до 316 л/кг. Изобретение позволяет улучшить экологию путем утилизации твердых бытовых отходов и исключения образования в процессе плавления хлорорганических соединений. Сокращается продолжительность процесса. 1 з.п. ф-лы.
Изобретение относится к химической технологии, в частности к получению карбида кальция.
Известен способ получения карбида кальция, включающий плавление шихты, состоящей из оксида кальция (извести) и углеродистого восстановителя (кокса, антрацита) (Кузнецов Л.А. Производство карбида кальция. М.: 1954, с.77-78).
Недостатком способа является использование дорогостоящих и дефицитных углеродистых материалов (металлургического кокса и антрацита), а также длительность процесса из-за незначительной поверхности контакта реагирующих элементов.
Известен способ получения карбида кальция (патент РФ № 2129093, кл. С 01 В 31/32, заявл. 1,1.03.97), согласно которому коксозольный остаток термической переработки окисленных бурых углей состава, масс.%: СаО – 4.75, С – 34.5, Fe2О3 – 6.6, SiO2 – 5.0, Mg – 3.3, Al2О3 – 1.6, S – 0.1, остальное 0,5, смешивают с 12,9-28,3% от массы смеси карбоната кальция в виде известняка, подвергают высокотемпературной плавке при 2000-2100°С, охлаждают, разделяют СаС2 и ферросилиций, получают СаС2 с литражом 275-285 л/кг и содержанием ферросилиция 0,1-0,2 масс.%. Использование отходов угледобычи позволяет снизить себестоимость карбида кальция на 30%.
Недостатками способа являются технологические сложности при эксплуатации производства и ухудшение технико-экономических и экологических показателей процесса, обусловленные значительным содержанием примесей (железа, кремния, магния).
Известен также способ получения карбида кальция (а.с. № 350753, Кл. С 01 В 31/30, заявл. 15.06.70) путем взаимодействия извести с углеводородами (с коксом или без него), согласно которому в качестве углеводородов используют жидкие или твердые парафиновые, ароматические, высокомолекулярные соединения гибридного или гетероциклического строения, а также их технические смеси, например, мазут или сырой антрацит. Углеводородное сырье подают в реакционное пространство электродуговой печи через полые электроды. При взаимодействии углеводородов с накаленной до 2000-2500°C поверхностью расплава последние расщепляются с выделением углерода, что позволяет интенсифицировать процесс по сравнению, например, с использованием в качестве углеродистого восстановителя антрацита или кокса.
Недостатком способа являются большие энергетические затраты, обусловленные высокотемпературным расщеплением углеводородов (2500°С), а также невозможность использования побочных продуктов технологического процесса (смесь сажи, водорода, ацетилена), что ухудшает экологию процесса.
Кроме того, в процессе используется плавление карбида кальция в дуговом режиме работы карбидной печи, что определяет удельную плотность электрического тока в электроде 5-7 А/см2 (Электротермические процессы химической технологии. Л.: Химия, Ленинградское отделение, 1984, с.212) Это ведет к значительным возгонам карбонатной составляющей шихтовых материалов, что также ухудшает экономические и экологические показатели процесса.
Наиболее близким к заявляемому способу получения карбида кальция (прототипом) является способ производства карбида кальция, описанный в заявке DE № 4241245 (кл. С 01 В 31/32, 1994), заключающийся в использовании при получении карбида кальция реакции обмена содержащего углерод соединения с оксидом кальция в электродуговой печи. В качестве содержащего углерод соединения используют измельченные отходы пластмасс, которые в присутствии тонкодисперсного оксида кальция (массовое соотношение оксида кальция к отходам пластмасс составляет 1:0,5-3) обрабатывают во вращающейся трубчатой печи. Процесс получения исходного материала (шихты) для производства карбида кальция идет в две стадии: сначала проводят пиролиз при 400-800°С, а затем кальцинирование при 1000-1300°С образовавшегося на первой стадии продукта, представляющего собой смесь оксида кальция и пиролизного кокса. После охлаждения до 500°С мелкие фракции (менее 3 мм) смеси карбида кальция с коксом отделяют, а крупные (более 3 мм) подают в закрытую карбидную печь как исходный материал для получения карбида кальция. Полученный карбид кальция содержит 82% СаС2.
Известный способ дает возможность утилизации пластмассовых отходов и открывает малозатратный углеродистый компонент для процесса производства карбида кальция, однако он малоэффективен применительно к технологии получения карбида кальция, так как осуществляется в несколько стадий, что существенно влияет на продолжительность технологического процесса и качество целевого продукта. Кроме того, в среде, создаваемой в трубчатой печи, будет в качестве восстановителя образовываться сажа – вещество с пониженной активностью как восстановитель в системе взаимодействия СаО:С, а на второй стадии – прокаливание смеси оксида кальция и пиролизного кокса при температуре 1000-1300°С – будет происходить графитизация углерода, то есть снижение его восстановительной активности в процессе получения карбида кальция, что отрицательно скажется на интенсивности процесса. В заявке DE № 4241245 не указана температура, при которой проводился процесс плавления карбида кальция, но известно, что получение даже самого низкоплавкого карбида кальция не может быть осуществлено при температуре ниже 1750°С. Карбид кальция, полученный по известному способу и содержащий 82% СаС2, плавится при температуре не ниже 1900°С (см. рис. XIV.8 “Диаграмма плавкости системы СаО-СаС2 / Электротермические процессы химической технологии”. Химия, Ленинградское отделение, 1984 г., с.327). Приведенный в заявке DE № 4241245 диапазон температур 1000-1300°С относится к температуре кальцинации (просто прокалки) смеси оксида кальция и пиролизного кокса с целью получения более качественной шихты для производства карбида кальция. Следует также отметить, что значительное содержание в шихте углеродистых материалов (в способе-прототипе массовое соотношение оксида кальция к отходам пластмасс составляет 1:0,5-3,0) кроме необоснованного расхода сырья и энергии на его переработку, ведет к значительным газопылевым выбросам в системе, что негативно сказывается на экологии окружающей среды.
Задачей предлагаемого изобретения является повышение эффективности способа за счет сокращения продолжительности процесса, увеличения выхода целевого продукта высокого качества и расширения сырьевой базы, а также его экологичности.
Поставленная задача достигается тем, что в способе получения карбида кальция путем плавления в электротермической печи извести и углеродистого восстановителя, в качестве которого используют продукты пиролиза твердых бытовых отходов, согласно изобретению берут продукты пиролиза с содержанием летучих 4-10 масс.% и зольностью не выше 6 масс.% и плавление ведут в режиме печи сопротивления при удельной плотности тока на электроде 1,5-2,0 А/см2 с использованием полых электродов, при этом берут отходы бумаги, картона, дерева, кожи, пластмасс, текстиля.
Заявляемый способ получения карбида кальция является эффективным и экологичным, так как пиролиз некомпостируемых твердых бытовых отходов (ТБО) проводится в закрытой емкости с косвенным обогревом при температуре до 800°С с получением активного углеродистого восстановителя, который содержит летучих 4-10 масс.%, разлагаемых при нагреве в результате непосредственного контакта с расплавом карбида кальция (температура 1800-2000°С) и насыщающих оксид кальция молекулярным углеродом в зоне твердофазных процессов в ванне карбидной печи, что приводит к возрастанию интенсивности процесса в зоне плавления, исключает разбавление пиролизного газа и определяет незначительные (по сравнению с процессом сжигания) объемы газопылевых выбросов. Кроме того, в предлагаемом способе используется двухкомпонентная шихта: оксид кальция и углеродистый восстановитель подаются в карбидную печь раздельно и это позволяет строго выдерживать оптимальное соотношение оксида кальция к углеродистому восстановителю в пределах 1:0,65-0,85, что значительно улучшает качество получаемого карбида кальция.
Углеродистый восстановитель получают следующим образом. Готовят шихту из следующих фракций ТБО в соотношениях компонентов в соответствии с морфологическим составом ТБО (мас.%): бумага, картон – 58; дерево – 6,5; кожа – 4,3; пластические массы – 19,6; текстиль – 11. Шихту подвергают термическому нагреву в закрытой емкости до температуры 800°C и выдерживают при этой температуре 2 часа. Выделяющуюся в процессе термообработки шихты газопаровую фазу или сжигают «на свечу» или утилизируют как теплоноситель. Коксовый остаток, используемый далее в процессе получения карбида кальция в качестве углеродистого восстановителя, охлаждают и анализируют. Получаемый углеродистый восстановитель имеет состав (мас.%): углерод – Собщий – 90-94, в том числе летучие – 4-10; содержание металлов СаО – 0,28-0,6; Al – 0,1-0,96; Mg – 0,05-0,096; Fe – 0,09-0,91; Si – 0,13-2,94; Cr – 0,003-0,038; Ti – 0,01-0,025; Cu – 0,0001-0,015; Zn – 0,001-0,003; Ni – 0,002; Cd<0,001; Pb – 0,003; P<0,03; Mn – 0,001.
Выход продукта – 35-38%. Продукт различной грануляции, легко размалываемый.
Поскольку углеродистый восстановитель, полученный в процессе пиролиза ТБО, имеет малую прочность, легко истирается в транспортных системах при подаче его в ванну карбидной печи, наиболее рационально его использование по следующей технологии.
Первое – раздельная подача компонентов шихты для выплавки карбида кальция в ванну печи. Известковый компонент шихты грануляцией 12-25 мм подают в ванну, мелкодисперсный углеродистый восстановитель, размолотый до грануляции минус 3 мм, подают непосредственно в зону расплава карбида кальция через полый электрод.
Второе – режим плавки с учетом возможности выноса мелкодисперсного компонента шихты мягкий, при малой плотности тока на электроде в пределах 1,5-2,0 А/см2 и при низком рабочем напряжении 45-50 вольт, т.е бездуговой режим плавления в режиме печи сопротивления.
Пример
Готовят шихту из 960 г извести грануляцией 10-15 мм, загружают ее в ванну лабораторной карбидной печи мощностью 40 кВт. Печь работает при следующих электрических характеристиках: напряжение – 40 вольт, плотность тока в электроде 1,5-2 А/см2. Для запуска печи на под насыпают низколитражную мелочь карбида кальция. После разогрева печи (через 15 минут) через отверстие по центру полого угольного электрода подают в расплав углеродистый восстановитель в количестве 650 г грануляцией минус 3 мм, при этом между жидкой фазой, представляющей расплав СаС2-СаО, и твердым углеродом происходит реакция карбидообразования при температурах 1800-2200°C. Известь растворяется в расплаве и взаимодействует с углеродистым восстановителем. Реакционные газы, проходя через слой извести, насыщают ее углеродом и это способствует более активному растворению извести в расплаве СаС2-СаО. Взаимодействие расплава СаС2-СаО с углеродистым восстановителем приводит к обогащению жидкой ванны карбидом до соотношения, отвечающего температуре и давлению СО в печи. Остаточное содержание летучих пиролизуется в зоне высоких температур при подаче восстановителя непосредственно в зону расплава, продукт пиролиза дополнительно насыщает известковую составляющую углеродом.
Срабатывание шихтовых материалов постоянно компенсируют раздельной подачей компонентов: извести в объем ванны, углеродистого восстановителя в зону расплава через отверстие в электроде. По конструктивным особенностям используемой лабораторной карбидной печи плавку ведут «на блок». Расплав охлаждают в печи, извлекают, анализируют. Вес выплавленного карбида кальция – 1,2 кг. Получают продукт с содержанием СаС2 – 85% (литраж 316 л/кг).
Удельный расход сырья (на 1 кг условного карбида кальция):
известь – 960 г,
углеродистый восстановитель – 650 г.
Содержание примесей в карбиде кальция: РН3 – менее 0,003%;
Н2S – менее 0,015%.
Остаточное содержание летучих в углеродистом восстановителе свыше 10% ухудшает процесс получения карбида кальция, т.к. при плавлении карбида кальция возрастает интенсивность выделения летучих, нарушается работоспособность элементов конструкции печи, реакционные газы процесса засоряются непрореагировавшими сажистыми включениями, что осложняет работу элементов печи (снижается электрическое сопротивление изоляции и возникают пробои в электроизоляции) и осложняет работу узла газоочистки реакционных газов.
Снижение содержания летучих в углеродистом восстановителе менее 4% массовых нежелательно, т.к. резко снижается интенсивность плавления карбида кальция за счет сокращения зоны твердофазных процессов в ванне печи, где имеет место нагрев шихты и насыщение окиси кальция углеродом, что определяет интенсивность процесса в зоне плавления.
Низкая зольность, не выше 6 масс.%, углеродистого восстановителя исключает необходимость дополнительных затрат энергии и сырья, расходуемых при производстве карбида кальция, на побочные нецелевые реакции, снижает величину возгонов в процессе плавления соединений элементов, содержащихся в золе, имеющих более низкие температуры плавления и разложения, чем карбид кальция.
Предлагаемый способ позволяет исключить образование больших объемов реакционных газов (водорода, ацетилена), смешанных с сажей, не подлежащих использованию и тем самым улучшить экологичность процесса. Остатки хлора, которые в основной массе отогнаны из углеродистого восстановителя при пиролизе твердых бытовых отходов, связываются в прочное соединение CaCl2, которое имеет температуру плавления ниже температуры плавления СаС2 и поэтому выводится из процесса без разложения, что исключает образование в процессе плавления карбида кальция опасных хлорорганических соединений (диоксинов, фуранов).
Таким образом, заявляемый способ получения карбида кальция является более эффективным и экологичным по сравнению со способом-прототипом, так как проходит в одну стадию, позволяет получать карбид кальция более высокого качества с содержанием СаС2 85 масс.% (литраж до 316 л/кг) и при этом вовлечь в переработку продукты пиролиза твердых бытовых отходов (бумаги, картона, дерева, кожи, пластмасс, текстиля), которые в настоящее время практически не утилизируются, что значительно улучшает общую экологическую обстановку окружающей среды.
1. Способ получения карбида кальция путем плавления в электротермической печи извести и углеродистого восстановителя, в качестве которого используют продукты пиролиза твердых бытовых отходов, отличающийся тем, что берут продукты пиролиза с содержанием летучих 4-10 мас.% и зольностью не выше 6 мас.% и плавление ведут в режиме печи сопротивления при удельной плотности тока на электроде 1,5-2,0 А/см2 с использованием полых электродов.
2. Способ по п.1, отличающийся тем, что используют отходы бумаги, картона, дерева, кожи, пластмасс, текстиля.
www.findpatent.ru
Карбид кальция и ацетилен – друзья не разлей вода!
- Карбид кальция
- химическое соединение кальция с углеродом, в чистом виде представляющее собой белое кристаллическое вещество. Химическая формула – СаС2

- Технический карбид кальция
- твердый кускообразный материал, цвет излома которого меняется в зависимости от содержания карбида кальция. При содержании 60-75% СаС2 – имеет излом серого цвета, переходящий в фиолетовый при более высоком содержании CaC2. Высокопроцентный (80% СаС2 и выше) – имеет окраску от светло-коричневого до голубовато-черного.

Карбид кальция имеет резкий чесночный запах и сильно поглощает воду. Его плотность повышается с увеличением количества примесей и изменяется в пределах 2,22-2,8 г/см3. Молекулярная масса – 64,102. Технический карбид кальция выпускают по ГОСТ 1460.
Карбид кальция является основным сырьем для получения ацетилена – горючего газа применяемого при газовой сварке и газовой резке.
Карбид кальция был получен случайно в 1862 г. Немецкий химик Фридрих Вёлер (Friedrich Wöhler) при попытке выделения металлического кальция из извести (карбоната кальция СаСО3) путем длительного прокаливания смеси, состоящей из извести и угля получил массу сероватого цвета, в которой не обнаружил признаков металла. Как результат неудавшегося эксперимента он выбросил эту массу на свалку во дворе. Во время дождя лаборант заметил выделение какого-то газа из выброшенной массы. Это заинтересовало Фридриха Вёлера, он провел анализ газа и установил, что это ацетилен (С2Н2), ранее открытый Эдмундом Дэви (Edmund Davy), в 1836 г.
Однако имя этому газу присвоил французский химик Пьер Эжен Марселен Бертло (Marcellin Berthelot), после того, как в 1863 году получил ацетилен, пропуская водород над раскалёнными электрической дугой графитовыми электродами.
Томас Уилсон (Thomas Leopold “Carbide” Willson) в 1888 году и Фердинанд Фредерик Анри Муассан (Ferdinand Frederic Henri Moissan) в 1892 независимо друг от друга открыли метод получения карбида кальция в дуговой электропечи, что послужило толчком для дальнейшего развития промышленного получения технического карбида кальция.
В России первые заводы по изготовлению карбида кальция были построены акционерным обществом «Перун» в 1908 г. в Земковицах, а в 1910 г. в Петербурге. В 1914 г. на этом заводе работали две карбидные печи мощностью по 500 кВт и две печи по 900 кВт.
В 1917 г. при Макеевском металлургическом заводе была построена установка с электропечью мощностью 1800 кВт. Почти одновременно на заводе в Баку для нужд нефтепромышленности и на Аллавердском медеплавильном заводе также были пущены карбидные печи.
В 1930 г. был построен и пущен первый большой карбидный завод в Растяпино (ныне г. Дзержинск Нижегородской области). На этом заводе карбид кальция впервые стал выпускаться не только как товарный продукт, но и для получения цианамида кальция.
Получение карбида кальция
Технический карбид кальция получают в результате взаимодействия обожженной извести (СаО) с коксом (3С) или антрацитом в электрических печах при температуре 1900-2300оС. Шихту, состоящую из смеси кокса или антрацита и извести в определенной пропорции, загружают в электропечь, шихта расплавляется, при этом происходит эндотермическая химическая реакция (т. е. с поглощением тепла) по формуле:
СаО+3С = СаС2+СО -108 ккал/моль
Таким образом, для получения 1 т карбида кальция требуется:
- 4000 кг извести
- 600 кг кокса
- 1965 кВт·ч электроэнергии
Однако вследствие значительных потерь энергии в карбидных печах практически для получения 1 т технического карбида кальция расходуется от 2800 до 3700 кВт·ч в зависимости от мощности печи. Если мощность печи меньше 1000 кВт, то расход электроэнергии может достичь 4000 кВт·ч/т и более.
Расплавленный карбид кальция сливают из печи в специальные изложницы, в которых он остывает и затвердевает. После затвердевания его дробят в щековых дробилках и сортируют в решетчатых барабанах на куски различной величины от 2 до 80 мм.
Выход кусков различных размеров при дроблении приведен ниже:
Грануляция карбида кальция, мм | 25-80 | 15-25 | 8-15 | 2-8 | до 2 |
|---|---|---|---|---|---|
Выход, % | 66-80 | 8-10 | 6-14 | 4,5-6,5 | 1,5-3,0 |
Товарным карбидом кальция считается грануляцией от 2 до 100 мм. Карбидная пыль, получающаяся при дроблении, непригодна для нормальных ацетиленовых генераторов из-за слишком энергичного разложения водой, перегрева и опасности взрыва.
Зависимость удельного веса технического карбида кальция от содержания в нем СаС2, приведена в таблице ниже:
Содержание СаС2 в техническом карбиде, % | 80 | 75 | 70 | 65 | 60 | 55 |
|---|---|---|---|---|---|---|
Удельный вес технического карбида | 2,32 | 2,37 | 2,41 | 2.45 | 2,49 | 2,53 |
Технический карбид кальция, получаемый в электропечах, содержит ряд примесей, попадающих в него из исходных материалов, которыми пользуются при его производстве. Средний химический состав технического карбида кальция применяемого для сварки:
Компонент | Содержание, % (по массе) |
|---|---|
Карбид кальция (СаС2) | 72,5 |
Известь (СаО) | 17,3 |
Окись магния (MgO) | 0,4 |
Окись железа (Fe2O3) и окись алюминия (Al2O3) | 2,5 |
Окись кремния (SiO2) | 2,0 |
Сера (S) | 0,3 |
Углерод (С) | 1,0 |
Другие примеси | 4,0 |
Как видно из приведенного состава, основной примесью является известь.
Примеси, содержащиеся в исходных материалах, применяемых для производства, ухудшают его качество. Особенно вредными примесями являются фосфор и сера, которые переходят в карбид кальция в виде фосфористых и сернистых соединений кальция, а при разложении карбида попадают в ацетилен в виде фосфористого водорода и сероводорода.
При температуре 1000°С карбид кальция, взаимодействуя с азотом, образует цианамид кальция:
CaC2+N2=CaCN2+C
Эта реакция используется для промышленного производства цианамида кальция. Цианамид кальция применяется в качестве удобрения и как исходный продукт для получения цианидов.
С водородом карбид кальция вступает в реакцию при температуре выше 2200°С с образованием ацетилена и металлического кальция. При высокой температуре карбид кальция восстанавливает большинство окислов металлов.
Одним из промышленных способом получения ацетилена для газовой сварки и газовой резки является гидролиз карбида кальция т.е. разложение в воде.
При взаимодействии карбида кальция (CaC2) с водой (H2O) образовывается газ – ацетилен (C2H2) и гашеная известь (Ca(OH)2), являющуюся отходом. Химическая активность карбида кальция по отношению к воде столь велика, что он разлагается даже кристаллизационной водой, содержащейся в солях.
Экзотермическая реакция (т.е. с выделением тепла) взаимодействия карбида кальция с водой протекает бурно по уравнению:
CaC2+2H2O=C2H2+Ca(OH)2 +30,4 ккал/моль
Тепловой эффект разложения технического карбида кальция слагается из тепла, выделяемого при взаимодействии с водой карбида кальция и негашеной извести (содержащейся в карбиде кальция). Взаимодействие извести с водой протекает по уравнению:
СаО+H2O = Ca(OH)2 +15,2 ккал/моль
- Выход ацетилена
- объем ацетилена в литрах, выделяемый при разложении 1 кг карбида, приведенный к 20° и 760 мм рт. ст.
Для разложения 1 кг химически чистого карбида кальция теоретически необходимо 0,562 кг воды, при этом получается 0,406 кг ацетилена (285 л) и 1,156 кг гашеной извести.
Значительный тепловой эффект реакции разложения карбида кальция и опасность перегрева ацетилена заставляют вести процесс разложения карбида с большим избытком воды для охлаждения. Это делает процесс более безопасным. Температура выходящего из генератора ацетилена при этом превышает температуру окружающей среды всего на 10-15°С.
Минимальное количество воды, необходимое для охлаждения при разложении 1 кг карбида кальция, может быть рассчитано следующим образом.
При разложении 1 кг 70%-го карбида кальция образуется 0,284 кг ацетилена и 1,127 кг гидрата окиси кальци т.е. гашеной извести (принимая содержание окиси кальция в карбиде кальция равным 24%).
Принимаем, что начальная температура воды равна 15° С, а температура в генераторе во время работы равна 60° С. Уравнение теплового баланса для 1 кг карбида кальция выражается следующим образом:
q=q1+q2+q3+q4+q5
где q – количество тепла, выделяющееся при разложении 1 кг 70%-го карбида кальция, равное 397 ккал/кг
q1 – количество тепла, затрачиваемое на нагревание получаемой гашеной извести с 15 до 60°С:
q1= 1,127×(60-15)-0,23= 11,7 ккал
0,23 – средняя теплоемкость гидрата окиси кальция в ккал/кг
q2 – количество тепла, затрачиваемое на нагревание получаемого ацетилена с 15 до 60° С:
q2=0,284×(60-15)-0,336 = 4,3 ккал
0,336 – средняя теплоемкость 1 кг ацетилена в ккал в указанном интервале температур
q3 – тепло, затрачиваемое на испарение воды в количестве 0,034 кг (при 60° С содержание водяных паров, насыщающих ацетилен, полученный из 1 кг карбида кальция, равно 34 г) скрытая теплота парообразования воды – 539 ккал/кг
q3 = 0,034×539+0,034×1×(60-15) -19,9 ккал
q4 – потеря тепла в окружающую среду и на нагревание стенок генератора, она составляет примерно 7% от общего количества выделяющегося тепла:
q4=397×7/100=27,8 ккал
q5 – количество тепла, расходуемое на нагревание воды до температуры 60° С:
q5=q×(q1+q2+q3+q4)=397×(11,7+4,3+19,9+27,8) = 336,3 ккал
Искомый минимальный безопасный объем воды равен:
V=q5/(60-15)×1=336,3/45≈7,5 л
Так как 1 м3 ацетилена при абсолютном давлении 1 кгс/мм2 и 20°С весит 1,09 кг, следовательно, из 1 кг химически чистого карбида кальция теоретически можно получить 0,406/1,09 = 0,3725 м3, или 372,5 л ацетилена.
Как уже говорилось выше, технический карбид кальция обычно содержит не более 70-80% CaC2. Поэтому из 1 кг технического карбида кальция можно получить от 230 до 280 л ацетилена.
Если учесть потери ацетилена на растворение в воде и продувку ацетиленового генератора, то для получения 1 м3 (1000 дм3) ацетилена практически приходится расходовать 4,3-4,5 кг карбида кальция. Более точные данные о фактическом выходе ацетилена из технического карбида кальция в зависимости от количества примесей (сорта) и размеров “кусков” (грануляции) указаны в ГОСТ 1460.
Для Получение ацетилена из карбида кальция осуществляется в аппаратах, называемых ацетиленовыми генераторами.
Чем меньше размеры кусков карбида кальция, тем быстрее происходит его разложение.
Например: Карбид кальция размером 50×80 мм разлагается полностью в течение 13 мин, а размером 8×15 мм – в течение 6,5 мин.
При величине кусков менее 2 мм карбид кальция считается отходом и называется карбидной пылью. Карбидная пыль разлагается практически мгновенно. При взаимодействии с водой разложение карбидной пыли происходит на поверхности воды и выделяемое тепло не может быть быстро отведено. Это приводит к повышению температуры в зоне реакции и перегреву частиц карбида и выделяющегося ацетилена. При этом особенно опасно присутствие воздуха, так как быстро достигается температура воспламенения ацетилено-воздушной смеси. Поэтому карбидную пыль нельзя применять в обычных ацетиленовых генераторах, рассчитанных для работы на кусковом карбиде кальция, так как это может вызвать взрыв ацетилена в генераторе. Для разложения карбидной пыли применяют генераторы специальной конструкции.
Чем выше температура воды, тем быстрее идет разложение карбида кальция. Если вода сильно загрязнена гашеной известью, образующейся при разложении карбида кальция, то реакция разложения замедляется.
При разложении неподвижного карбида кальция в недостаточном количестве воды куски его могут покрываться коркой гашеной извести и сильно перегреваться, при этом может иметь место реакция:
СаС2+Ca(ОН)2 = C2H2+2СаО
В этом случае разложение карбида кальция происходит за счет отнятия влаги, содержащейся в гашеной извести. В результате повышается плотность корки, что приводит к еще большему перегреву. Поэтому непрерывное удаление извести из зоны реакции имеет большое значение, так как перегрев карбида кальция может привести к взрыву ацетилено-воздушной смеси или вызвать взрывчатый распад ацетилена.
Если производить разложение одинаковых количеств карбида кальция различными постепенно уменьшающимися количествами воды, то температура получаемой смеси ацетилен – водяной пар будет соответственно повышаться. При температуре около 90°С почти все тепло (за исключением тепла, затрачиваемого на нагревание ацетилена и карбидного ила) расходуется на образование водяного пара. Эти условия разложения соответствуют процессу, при котором получается сухой гидрат окиси кальция, поскольку вся вводимая в реакцию вода расходуется на разложение карбида и образование водяного пара.
При погружении карбида кальция в воду процесс разложения протекает также весьма неравномерно: вначале реакция идет очень активно с бурным выделением ацетилена, а затем скорость реакции уменьшается. Это объясняется уменьшением поверхности кусков и тем, что они покрываются коркой извести, препятствующей свободному доступу воды.
При перемешивании воды с находящимся в ней карбидом кальция разложение происходит быстрее и равномернее.
Скорость разложения карбида кальция в воде зависит от чистоты карбида кальция и поверхности соприкосновения кусков карбида кальция с водой.
Скорость разложения карбида кальция в воде является весьма важным элементом, характеризующим качество карбида кальция. Для практических целей пользуются понятием продолжительности разложения.
Продолжительностью разложения карбида кальция считают время, в течение которого выделяется 98% от всего количества ацетилена, который может быть выделенным из карбида кальция, так как остаток разлагается очень медленно и не характеризует процесс разложения применительно к условиям работы ацетиленовых генераторов.
В таблице ниже приведены экспериментальные данные о продолжительности разложения карбида кальция в зависимости от размеров его кусков.
Размеры кусков, мм | Пыль | 2/4 | 5/8 | 8/15 | 15/25 | 25/50 | 50/80 |
|---|---|---|---|---|---|---|---|
Продолжительность разложения, мин. | Несколько секунд | 1,17 | 1,65 | 1,82 | 4,23 | 13,5 | 16,6 |
Следует, оговорить, что данные таблицы характеризуют лишь те образцы карбида кальция, с которыми были проведены опыты. Практически могут иметь место значительные отклонения, главным образом в сторону уменьшения скорости разложения.
Скорость разложения карбида кальция в значительной степени зависит от выхода ацетилена из карбида кальция. Чем ниже выход, тем меньше скорость разложения.
На диаграмме ниже показаны изменения в скорости разложения карбида кальция двух сортов с одинаковыми размерами кусков (25/50).
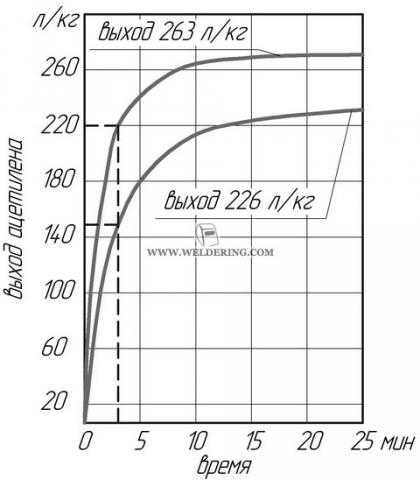
Например: При разложении 1 кг карбида кальция с выходом ацетилена 263 л/кг за первые 3 мин. выделяется 220 л ацетилена, а соответственно при выходе 226 л/кг – только 150 л.
weldering.com
Карбид кальция
В результате взаимодействия углерода с металлами при высоких температурахполучаются карбиды. Например, карбид кальция: Ca + 2C → CaC2. Из всех карбидов он имеет наибольшее практическое значение. Чистый CaC2 — хорошо кристаллизующееся твердое вещество, бесцветные кристаллы образованы ионами Ca2+ и C2-. Другие его названия — ацетиленид кальция или углеродистый кальций. Молярная масса равняется 64,1 г/моль. Он не летуч и не растворим ни в одном из известных растворителей, а под действием воды разлагается. Плотность его составляет 2,22 г/см³. Температура плавления равняется 2160°С, а кипения — 2300°С. По степени воздействия на организм относится к веществам чрезвычайно опасным (1-й класс опасности).
Впервые ацетиленид кальция был получен в 1862 году немецким химиком Фридрихом Велером при нагревании с углем сплава из цинка и кальция. Им же была описана реакция углеродистого кальция с h3O. Даже с ее следами (например, с атмосферной влагой) карбид кальция реагирует энергично, с выделением большого количества тепла. Но в случае недостатка воды может произойти самовоспламенение образующегося ацетилена. Карбид кальция бурно взаимодействует с разбавленными неорганическими кислотами и водными растворами щелочей. При этом также происходит выделение ацетилена. Являясь сильным восстановителем, CaC2 способен восстанавливать все оксиды металлов до карбидов или чистых металлов.
Получение карбида кальция удобнее не из самого кальция, а его окисла. При высокой температуре (от 2000 до 2300°С) происходит его восстановление. При этом металл и углерод соединяются: CaO + 3C → CO↑ + CaC2. Процесс протекает в электродуговой печи, где накаливают смесь негашеной извести и кокса или антрацита. Технический продукт окрашен, имеет сероватый цвет, так как содержит примеси в виде свободного углерода, окиси, а также сульфида, фосфида кальция и других химических соединений. Массовая доля CaC2 в нем составляет 80—85%.
При взаимодействии карбидов с водой выделяется или металл, или ацетилен. По второму варианту с водой реагирует карбид кальция. Ацетилен, полученный в результате реакции, которая имеет промышленное значение: 2h3O + CaC2 → C2h3 + Ca(OH)2, является техническим и имеет неприятный запах, так как содержит ряд примесей (Nh4, h3S, Ph4 и другие). Хотя в чистом виде он является бесцветным газом с характерным слабоватым запахом, и он довольно хорошо растворяется в воде. Имеет большое значение для получения цианамида кальция (является сырьем в производстве цианистых соединений или применяется в качестве удобрения) из карбида взаимодействием его с азотом по уравнению реакции: N2 + CaC2 → CaCN2 + C.
В прошлом CaC2 широко использовался в карбидных лампах, где служил источником ацетиленового пламени. В настоящее время применение такого источника света ограничивается в основном спелеологией, его используют также в бакенах и маяках. Другие важные направления применения CaC2 — это химические технологии, где он является сырьем. Например, в производстве продуктов органического синтеза, главным из них является каучук синтетический. Также из углеродистого кальция получают ацетиленовую сажу, винилхлорид, уксусную кислоту, акрилонитрил, этилен, ацетон, искусственные смолы, стирол. В металлургии служит для раскисления металлов и десульфурации (снижение содержания кислорода и серы соответственно). Карбид кальция используют для изготовления регулятора роста растений, порошкового карбидного реагента (ацетиленовая сварка).
Получение каждой тонны CaC2 требует примерно 3 тысячи квт/час электроэнергии. Поэтому оно оправдано при наличии низких цен на нее. Однако в целом мировое производство углеродистого кальция растет. Если в 70-х годах предшествующего столетия ежегодно вырабатывалось до 5 миллионов тонн, то в нашем веке это количество выросло примерно вдвое. Так, в Китае производство ацетилена на основе карбида кальция является основным источником сырья для химической промышленности, в частности, для производства поливинилхлорида. Получение ацетилена из своего сырья экономичнее, чем при использовании импортной нефти. Поэтому производство его в Китае растет. В 2005 году оно достигало 8,94 миллионов тонн, и была реальная возможность выпускать 17 миллион тонн.
В отличие от Китая, в США, Европе и Японии потребление углеродистого кальция, как правило, снижается. Уровень его производства в США в 90-х годах составлял всего 236 тысяч тонн в год. В нашей стране карбид кальция выпускают по техническим условиям, изложенным в ГОСТ 1460-81. Основные его потребители — это Украина, Узбекистан, Румыния и Словакия. Из-за высокой энергоемкости продукта и в связи с ростом цен на электроэнергию потребление ацетиленида кальция в России и странах-экспортерах снизилось вдвое.
fb.ru
Карбид кальция: хранение, получение, реакция
При щелочной реакции углерода с металлами могут получится различные карбиды. За счет соединения определенных химических элементов получаются соединения, которые характеризуются высокой прочностью. Довольно большое распространение получил вариант исполнения, который получил название карбид кальция. Его стали применять в самых различных областях промышленности.
 Карбид кальция
Карбид кальцияВнешний вид и характеристики технического карбида кальция
Впервые рассматриваемый состав был получен в 1862 году. Проводимая процедура касалась отделения кальция от извести, в результате чего получился бледно-серый состав без признаков, свойственных металлам. В результате опыта был получен карбид, который в последствии стал активно использоваться при выпуске различной продукции.
В начале 20 века карбид кальция стали использовать для производства ацетилена в больших объемах. Именно поэтому стали вести активные исследования для выявления более производительной технологии.
Технические характеристики материала определяют его широкое распространение. Внешний вид вещества характеризуется светло-серым цветом, выпускаются карбиды в виде камня или порошка.
Физические свойства
При выборе практически любого материала следует уделять больше всего внимания физическим свойствам. У рассматриваемого они следующие:
- Соединение имеет кристаллическую структуру.
- Показатель температуры плавления составляет 2300 °С. Стоит учитывать, что подобная цифра свойственна только чистому составу. Добавление в состав различных примесей приводит к тому, что температура плавления существенно падает.

Чистый карбид кальция
Стоит учитывать, что карбид кальция в большинстве случаев находится в твердом состоянии. Кроме этого, цвет может варьироваться от серого до коричневого цвета. Физические свойства карбида кальция определяют его широкое применение в самых различных отраслях промышленности.
Химические свойства
Немаловажное значение имеют и химические свойства. Они также учитываются при применении материала. К основным характеристикам можно отнести следующие качества:
- Карбид кальция характеризуется тем, что хорошо впитывает влагу. Стоит учитывать, подобная процедура проявляется яркой химической реакцией, связанной с разложением вещества.
- При работе с рассматриваемым материалом стоит учитывать, что образующаяся пыль оказывает раздражительный эффект на слизистые органы. Кроме этого, подобная реакция может проявится при попадании кристаллов или пыли на поверхность кожи. Именно поэтому при работе с рассматриваемым соединением следует использовать респиратор и некоторые другие средства защиты.
- Кристаллы активное реагируют на воздействие других веществ зачастую только при нагреве. При этом может образоваться карбонат кальция.
- В некоторых случаях проводится соединение кристаллического вещества с азотом, в результате чего получается цианамид кальция.
- При нагреве может проходить реакция с мышьяком и хлором, а также фосфором.

Карбонат кальция
Считается, что наиболее важным химическим качеством является податливость к разложению при воздействии воды.
Получение
Как ранее было отмечено, карбид кальция активно применяется при получении самых различных материалов. Именно поэтому процесс получения карбида кальция постоянно совершенствовался. К особенностям применяемых технологий можно отнести нижеприведенные моменты:
- В качестве сырья применяется негашеная известь. В большинстве случаев вещество получается из извести, но в домашних условиях провести подобную процедуру сложно.
- Известь смешивается с измельченном коксом для получения однородной массы.
- В промышленности карбид кальция получают по схеме, которая предусматривает нагрев вещества до высокой температуры. Для этого применяются электронные печи. Рекомендуемая температура плавления составляет 1900 ⁰С.
- После нагрева вещества до столь высокой температуры оно переходит в жидкое состояние. Для работы подготавливаются специальные формы.
При рассмотрении того, как из углерода получить карбид кальция отметим, что по установленным стандартам в состав должно входить не менее 80% основного вещества. На долю примесей должно приходится не более 25%, в число которых также входит углерод. Производство оксида кальция также приводит к выделению тепловой энергии, что стоит учитывать.
Транспортировка и хранение
Порошок карбида кальция при воздействии влаги практически моментально разлагается. При этом образуется ацетилен, который при большой концентрации горюч и взрывоопасный. Именно поэтому нужно уделять довольно много внимания хранению карбида кальция, для чего часто применяют бидоны и специальные барабаны. К другим особенностям хранения отнесем следующие моменты:
- Выделяющийся ацетилен легче воздуха, поэтому скапливается вверху. Стоит учитывать, что он обладает наркотическими действиями, может самовоспламеняться.
- При производстве большого объема вещества особое внимание уделяется технике безопасности. Для фасовки применяются специальные упаковки.
- Для открытия упаковки следует использовать инструменты, которые не становятся причиной образования искр.
- Если вещество попадает на кожу или слизистую оболочку, то его нужно сразу удалить. При этом пострадавшая поверхность обрабатывается специальным кремом или другим защитно-заживляющим веществом.
- По установленным правилам, транспортировка может проводится исключительно при применении крытого транспортного средства. При этом проводить доставку по воздуху запрещается.

Контейнер для транспортировки
Установленные правила также запрещают хранить карбид кальция вместе с другими химическими веществами и источниками тепла. Это связано с тем, что образующиеся газы могут вступать в химическую реакцию с другими химическими веществами и возгораться.
Применение карбида кальция
Как ранее было отмечено, карбид кальция встречается в самых различных областях промышленности, зачастую поставляют для проведения промышленного синтеза. Свойства карбида кальция и реакция, протекающая при его соединении с различными веществами, определяют использование вещества в нижеприведенных случаях:
- Многие синтетически компоненты, входящих в состав современных материалов, производят на основе рассматриваемого компонента.
- Применяется для получения цианамида кальция. Подобный компонент используется для получения различных химических удобрений. Именно поэтому сырье применяется для регулирования скорости роста растений.
- Цианамид кальция также получают при соединении вещества с азотом.
- В некоторых случаях проводится восстановление металлов щелочной группы.
- Можно использовать рассматриваемое соединение в процессе газовой сварки.
При рассмотрении карбида кальция и области применения стоит учитывать, что подобное вещество чаще всего применяют для получения ацетилена. Подобный синтез карбида кальция разработал немецкий ученый. Среди особенностей подобного способа применения отметим следующие моменты:
- Ацетилен из карбида получают при оказании воздействия водой на используемое сырье.
- В результате прохождения химической реакции образуется требующийся газ, гашеная известь выпадает в осадок.
- Стоит учитывать, что при смешивании компонентов выделяется большое количество тепла. Поэтому работа должна проводится с учетом техники безопасности.
- В зависимости от вида применяемой технологии переработки сырья с 1 килограмма выходит около 290 литров газа.
- Скорость протекания процедуры зависит от чистоты применяемого сырья, температуры и количества воды.

Получение ацетилена из карбида кальция
Как показывает практика, при использовании чистого карбида на протекание химической реакции отводится около 20 литров волы на 1 килограмм сырья. Подобное количество воды требуется для того чтобы снизить температуру реакции, за счет чего обеспечиваются оптимальные условия для работы.
Техника безопасности
При проведении различных химических реакций для производства материалов должна соблюдаться техника безопасности. Как ранее было отмечено, выделяемые вещества могут быть взрывоопасными. Техника безопасности при взаимодействии с различными химическими веществами заключается в следующем:
- Для хранения и обработки требуется герметичное место. В обычном гараже проводить работы не рекомендуется.
- Нельзя допускать огонь к самому сырью, а также образующимся газам.
- Даже мелкие частицы могут привести к поражению кожных покровов. Именно поэтому работа должна проводится в респираторе и защитной одежде.
- Генераторы ацетилена размещают исключительно в хорошо изолированных помещениях.
- Если сырье применялось при проведении сварочных работ, то следует образующийся шлак утилизировать в специальных местах.
- При перемещении металлических и иных емкостей они должны быть надежно закреплены, столкновение и падение не допускается. Это может привести к появлению искр, которые станут причиной взрыва вещества.

Горение карбида кальция
Вышеприведенная информация определяет то, что работы с рассматриваемым сырьем не рекомендуется проводить в гараже или домашней мастерской. Несоблюдении технологии, отсутствии требующего оснащения и многие другие причины могут привести к возникновению искры и воспламенению веществ.
Карбид кальция реакция с водой
Рассматриваемое сырье чаще всего применяется для соединения с водой, в результате чего получается ацетилен. Взаимодействие карбида кальция с водой становится причиной появления газа с неприятным запахом и достаточно большим количеством различных примесей. В чистом виде получить подобное вещество можно только при его многоэтапной очистке.
Реакция карбида кальция с водой может быть проведена опытным путем. К особенностям подобной процедуры отнесем следующие моменты:
- В качестве емкости применяется 1,5-литровая бутылка.
- После ее заполнения водой добавляется несколько кусочков кристаллического материала.
- Протекание реакции приводит к появлению избыточного давления.
- После того как карбид кальция больше не вступает в реакцию, на бутылку помещается горящая бумага. В результате взаимодействия между карбидом кальция и водой образуется газ, который взрывается. При рассматриваемом опыте образуется огненное облако.
Подобный опыт довольно опасен и должен быть проведен с соблюдением техники безопасности.
В заключение отметим, что рассматриваемый компонент в последнее время часто применяется для проведения самых различных опытов. Соединение обладает большим количеством свойств, которые должны учитываться. Выделение тепла и газов становится причиной, по которой проводить опыты рекомендуется только в промышленности.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
stankiexpert.ru

