Описание меди по химии 8 класс – Презентация на тему “Медь” по химии для 8 класса
alexxlab | 07.04.2020 | 0 | Вопросы и ответы
Химия 8 класс. Все формулы и определения. Кратко, таблицы, схемы.
«Химия 8 класс. Все формулы и определения»
Ключевые слова: Химия 8 класс. Все формулы и определения, условные обозначения физических величин, единицы измерения, приставки для обозначения единиц измерения, соотношения между единицами, химические формулы, основные определения, кратко, таблицы, схемы.
1. Условные обозначения, названия и единицы измерения
некоторых физических величин, используемых в химии
| Физическая величина | Обозначение | Единица измерения |
| Время | t | с |
| Давление | p | Па, кПа |
| Количество вещества | ν | моль |
| Масса вещества | m | кг, г |
| Массовая доля | ω | Безразмерная |
| Молярная масса | кг/моль, г/моль | |
| Молярный объем | Vn | м3/моль, л/моль |
| Объем вещества | V | м3, л |
| Объемная доля | Безразмерная | |
| Относительная атомная масса | Ar | Безразмерная |
| Относительная молекулярная масса | Mr | Безразмерная |
| Относительная плотность газа А по газу Б | DБ(А) | Безразмерная |
| Плотность вещества | р | кг/м3, г/см3, г/мл |
| Постоянная Авогадро | NA | 1/моль |
| Температура абсолютная | Т | К (Кельвин) |
| Температура по шкале Цельсия | t | °С (градус Цельсия) |
| Тепловой эффект химической реакции | Q | кДж/моль
|

2. Соотношения между единицами физических величин

3. Химические формулы в 8 классе
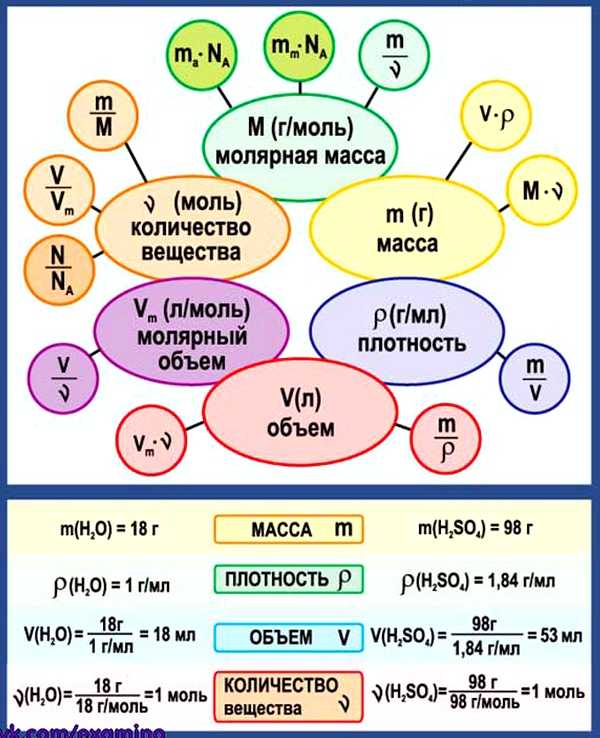
Схема. Химические формулы в 8 классе
4. Основные определения в 8 классе
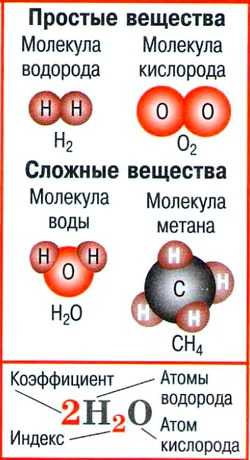
- Атом — мельчайшая химически неделимая частица вещества.
- Химический элемент — определённый вид атомов.
- Молекула — мельчайшая частица вещества, сохраняющая его состав и химические свойства и состоящая из атомов.
- Простые вещества
- Сложные вещества — вещества, молекулы которых состоят из атомов разного вида.
- Качественный состав вещества показывает, из атомов каких элементов оно состоит.
- Количественный состав вещества показывает число атомов каждого элемента в его составе.
- Химическая формула — условная запись качественного и количественного состава вещества посредством химических символов и индексов.
- Атомная единица массы (а.е.м.) — единица измерения массы атома, равная массы 1/12 атома углерода 12С.
- Моль — количество вещества, в котором содержится число частиц, равное числу атомов в 0,012 кг углерода 12С.
- Постоянная Авогадро (Na = 6*1023 моль-1) — число частиц, содержащихся в одном моле.
- Молярная масса вещества (М) — масса вещества, взятого в количестве 1 моль.
- Относительная атомная масса элемента Аr — отношение массы атома данного элемента m0 к 1/12 массы атома углерода 12С.
- Относительная молекулярная масса вещества Мr — отношение массы молекулы данного вещества к 1/12 массы атома углерода 12С. Относительная молекулярная масса равна сумме относительных атомных масс химических элементов, образующих соединение, с учётом числа атомов данного элемента.
- Массовая доля химического элемента ω(Х) показывает, какая часть относительной молекулярной массы вещества X приходится на данный элемент.
АТОМНО-МОЛЕКУЛЯРНОЕ УЧЕНИЕ
1. Существуют вещества с молекулярным и немолекулярным строением.
3. Молекулы находятся в непрерывном движении.
4. Молекулы состоят из атомов.
6. Атомы характеризуются определённой массой и размерами.
При физических явлениях молекулы сохраняются, при химических, как правило, разрушаются. Атомы при химических явлениях перегруппировываются, образуя молекулы новых веществ.
ЗАКОН ПОСТОЯНСТВА СОСТАВА ВЕЩЕСТВА
Каждое химически чистое вещество молекулярного строения независимо от способа получения имеет постоянный качественный и количественный состав.
ВАЛЕНТНОСТЬ
Валентность — свойство атома химического элемента присоединять или замещать определённое число атомов другого элемента.

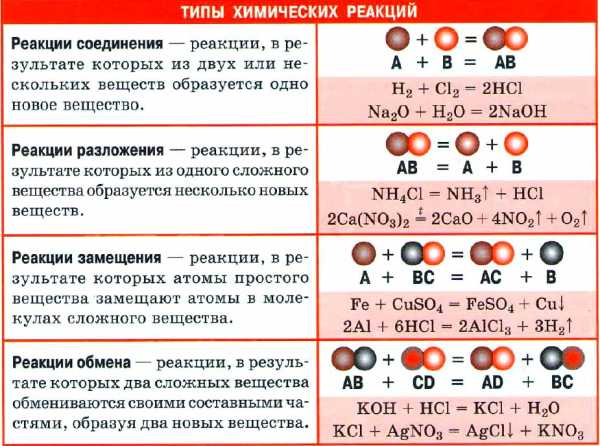
ХИМИЧЕСКАЯ РЕАКЦИЯ
Химическая реакция — явление, в результате которого из одних веществ образуются другие. Реагенты — вещества, вступающие в химическую реакцию. Продукты реакции — вещества, образующиеся в результате реакции.
1. Выделение теплоты (света).
2. Изменение окраски.
3. Появление запаха.
4. Образование осадка.
5. Выделение газа.
- Химическое уравнение — запись химической реакции с помощью химических формул. Показывает, какие вещества и в каком количестве вступают в реакцию и получаются в результате реакции.
ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ
Масса веществ, вступивших в химическую реакцию, равна массе веществ, образовавшихся в результате реакции. В результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка.
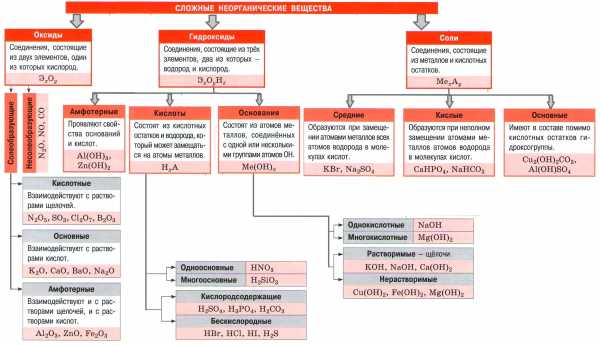
Важнейшие классы неорганических веществ
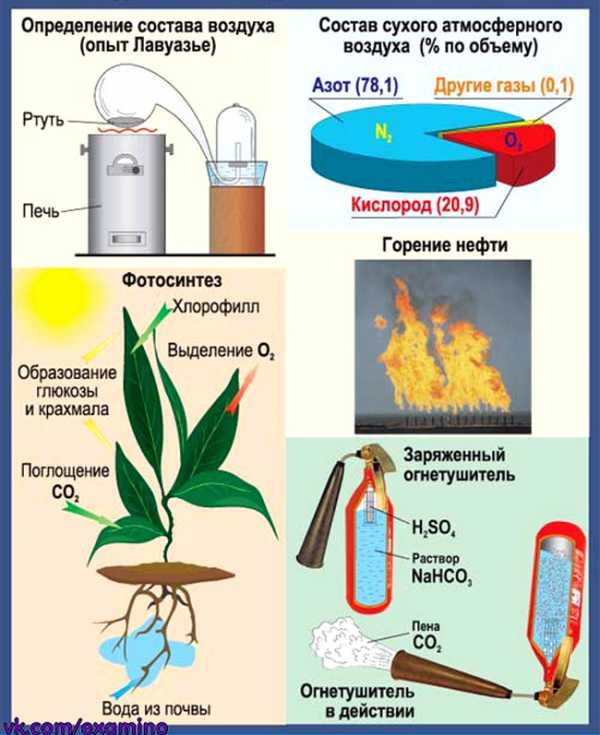
Воздух. Кислород. Горение
Конспект урока «Химия 8 класс. Все формулы и определения».
Следующая тема: «».
Химия 8 класс. Все формулы и определения
4.5 (90.43%) 23 votesuchitel.pro
Химия 8 класс | Социальная сеть работников образования
Урок1
Тема урока: Предмет химии. Ее истоки.
Чему бы жизнь нас не учила,
Но сердце верит в чудеса…
Ф. Тютчев
Цель урока: дать представление о химии, как о науке, ее задачах, целях, рассказать об истории возникновения химии. Урок-лекция, коллективная форма работы.
1.Организационный момент
-знакомство,
– учебник, задачник
-тетради ( 96листов, 2тетради по 12 листов,1 половинку)
-требования
(оценка, правила выживания в химической лаборатории)
2.Изучение нового материала
1) А)Что же такое химия?
Химия – наука, изучающая формы, структуру. Свойства веществ, а также законы, по которым происходят превращения одних веществ в другие, вероятность, энергетику,скорость и механизмы этих прцессов. Таким образом, объектом изучения химии становится вся вселенная, а равно и новые вещества, получаемые искусственным путем.
Б)Давно ли появилось слово «химия»?
Слово “химия” возникло, видимо, еще за 3000 лет до новой эры, если судить по тексту клинописных таблиц, найденных при раскопках древних городов Египта и Малой Азии. Установить происхождение этого слова очень трудно. Алхимик 4в. н. Э. Зосима из Панополиса в Греции считал, что слово “химия” произошло от слова “Хемес”- сокращенного имени Гермеса Трисмегиста- лнгендарного мудреца, получившего знания в виде божественного откровения. По преданию, воины Александра Македонского нашли могилу Гермеса Трисмегиста с каменной плитой , названной “Изумрудной Скрижалью Гермеса”. На ней была надпись, в которой будто 6ы сообщалось о способе получения удивительного вещества-“философского камня”. Некоторые историки считают, что слово “химия” связано с древнегреческим “хима”, означающим искусство выплавки металлов. Свида, византийский лексикограф, живший в 10-11в, понимал под химией искусственное приготовление золота и серебра. На древнекитайском языке “ким” означало “золото”.
Чаще всего слово “химия” связывают с названием Древнего Египта- “Хеми”,так как жрецы этой страны были выдающимися химиками. Поэтому по смыслу слово “химия” является тождественным выражению “египетская наука”. В 3в. до н.э. в Александрии уже была основана Академия наук , и священному искусству- химии- было отведено даже особое здание, храм Сераписа. Современное название “химия” производится от позднелатинскогослова Chimia и является интернациональным словом: немецкое chemie, французское chimie, английское chemistry
В)Алхимия- древнейший прообраз химии.
Понятие «алхимия» было введено арабами, которые прибавили к греко-египетскому названию «химия» арабскую приставку «ал». Алхимия- древнейший прообраз химии. Алхимия была связана со всеми областями химических ремесел. Людей, занимавшихся алхимией называли алхимиками. Многие алхимики в течение более тысячи лет с поразительным упорством пытались получить золото или серебро из неблагородных металлов с помощью «философского камня»- гипотетического вещества, либо «алкагеста»- никем никогда неполученного универсального растворителя. Занимались «алхимики» и поисками «эликсира жизни»- жидкости, которая должна дать людям возможность сохранять вечную молодость. Алхимией занимались не только ученые, но и всякого рода мошенники и неудачливые пророки. В 18 веке в ходу было такое четверостишие:
Алхимию постигнуть каждый рад:
Безмозглый идиот, старик и юный фат,
Портной, старуха, юркий адвокат,
Монах плешивый, пастырь и солдат.
Постепенно алхимия все более приобретала облик практической химии.Так знаменитый таджикский врач и философ Абу Али ал-Хусейн ибн Абдаллах ибн Сина(980-1037), известный под именем Авиценна, умел получать хлороводородную кислоту, азотную, серную. В15в. Парацельс ставил задачу алхимии получение лекарств для лечения больных. Алхимия как область человеческой деятельности перестала существовать после18века.
2).Нас окружают тела, а тела состоят из веществ. Вещества имеют определенные свойства: физические (температуру плавления, кипения, агрегатное состояние, цвет, запах, плотностьэлектропроводность и теплопроводность) и химические. Тела имеют форму и размер.
Свойства веществ – признаки по которым можно отличить одни вещества от других или установить сходство между ними.
Задание: определить тела и вещества: капля росы, медь, золото, электрический провод, медный колокол, снежинка, алюминий, кастрюля, химическая колба, кусочек мела, уксусная кислота, стекло, пробирка, капрон, тетрадь, бумага, фарфоровая чашка, вода.
Вещества делятся на простые и сложные, простые вещества делятся на металлы и неметаллы
.
Какими сходными и отличительными свойствами обладают следующие вещества
А)поваренная соль и сахар Б)уксусная кислота и вода?
Д/з: $1,2,3, тетради Дать характеристику меди и сере( цвет, запах, электро- и теплопроводность, плотность, температура плавления
СОЛЬ | ВОДА |
САХАР | Уксусная кислота |
nsportal.ru
ФОРМУЛА РЕАГЕНТА | |||
А) | AlCl3 → Al(OH)3 | 1) | Cl2 |
Б) | Fе → FeCl3 | 2) | HCl |
В) | Fе → FeCl2 | 3) | NaOHизбыток |
4) | NaOH | ФОРМУЛА РЕАГЕНТА | |
А) | AlCl3 → Al(OH)3 | 1) | H2SO4 разб. |
Б) | Al → Al(OH)3 | 2) | H2SO4 конц. холодная |
В) | Al → Al2(SO4)3 | 3) | Н2О |
4) | NaOHпо каплям | ||
СХЕМА ПРЕВРАЩЕНИЯ | ФОРМУЛА РЕАГЕНТА | ||
А) | FeCl3 → Fe(OH)3 | 1) | Cl2 |
Б) | Fe(OH)3 → Na3[Fe(OH)6] | 2) | HCl |
В) | Fe(OH)3 → FeCl3 | 3) | NaOH конц. избыток |
4) | NaOHпо каплям | ||
doc4web.ru
ГДЗ по химии для 8 класса О.С. Габриелян
автор: О.С. Габриелян.
Химия – это довольно увлекательная и обширная наука. Именно она помогла людям научиться получать различные материалы и превращать одно вещество в совершенно иное. Умело пользоваться дарами природы, применяя их в современной промышленности, научила нас химия. И яркий пример тому, это производство различных лекарств, которые постоянно спасают жизни громадному количеству людей.
И в 8 классе школьникам предстоит познакомиться с этим увлекательным предметом и заготовить прочную базу, на которой будут строиться знания в будущем. А верным помощником и надежным товарищем в этом вопросе для восьмиклассников станет О.С. Габриелян. Заслуженный педагог и специалист своего дела он написал решебник к школьному учебнику по химии 8 класса.
Сборник ГДЗ является неотъемлемой частью учебно-методического комплекса по химии, разработанного для учеников общеобразовательной школы. Готовые ответы призваны помочь восьмикласснику разобраться со сложными терминами и понятиями , ответить на все вопросы из сорока пяти параграфов и научить правильно оформлять лабораторные и практические работы.
Вначале ГДЗ по химии за 8 класс Габриелян предоставят основные химические понятия. И с первой главы уже начнется изучение атомов всех химических элементов. Далее пойдут темы о простых веществах и о соединениях химических элементов. Четвертая глава расскажет про изменения, происходящие с некоторыми веществами. И самая обширная последняя глава включает информацию про растворение, растворы и про реакции ионного обмена и окислительно-восстановительных реакциях.
Включили в сборник авторы и готовые ответы к химическим практикумам № 1 и 2 . Первый представляет алгоритмы решения практических работ, в основе которых лежат простейшие операции с веществом. А именно, школьникам предстоит наблюдать за изменениями, происходящими с горящей свечей, они должны будут проанализировать свойства почвы и воды. Расписать признаки химических реакций и рассчитать массовую долю сахара в растворе также предстоит восьмиклассникам при заполнении первого практикума.
Второй практикум посвящен свойствам электролитов. Поэтому его работы будут заключаться в определении ионной реакции; реакций между растворами электролитов; свойств кислот, оснований, оксидов и солей, а также необходимо будет решить экспериментальные задачи. В конце пособия представлены ответы к лабораторным опытам.
ГДЗ к рабочей тетради по химии за 8 класс Габриелян О.С. можно скачать здесь.
ГДЗ к тетради для оценки качества знаний по химии за 8 класс Габриелян О.С. можно скачать здесь.
gdzputina.ru
ГДЗ по химии для 8 класса Г.Е. Рудзитис
- ГДЗ
- 1 Класс
- Математика
- Английский язык
- Русский язык
- Немецкий язык
- Информатика
- Природоведение
- Основы здоровья
- Музыка
- Литература
- Окружающий мир
- Человек и мир
- 2 Класс
- Математика
- Английский язык
- Русский язык
- Немецкий язык
- Белорусский язык
- Украинский язык
- Информатика
- Природоведение
- Основы здоровья
- Музыка
- Литература
- Окружающий мир
- Человек и мир
- Технология
- 3 Класс
- Математика
- Английский язык
- Русский язык
- Немецкий язык
- Белорусский язык
- Украинский язык
- Информатика
- Музыка
- Литература
- Окружающий мир
- Человек и мир
- Испанский язык
- 4 Класс
- Математика
- Английский язык
- Русский язык
- Немецкий язык
- Белорусский язык
- Украинский язык
- Информатика
- Основы здоровья
- Музыка
resheba.me
ГДЗ по химии для 8 класса Г.Е. Рудзитис
- ГДЗ
- 1 Класс
- Математика
- Английский язык
- Русский язык
- Немецкий язык
- Информатика
- Природоведение
- Основы здоровья
- Музыка
- Литература
- Окружающий мир
- Человек и мир
- 2 Класс
- Математика
- Английский язык
- Русский язык
- Немецкий язык
- Белорусский язык
- Украинский язык
- Информатика
- Природоведение
- Основы здоровья
- Музыка
- Литература
- Окружающий мир
- Человек и мир
- Технология
- 3 Класс
- Математика
- Английский язык
- Русский язык
- Немецкий язык
- Белорусский язык
- Украинский язык
- Информатика
- Музыка
- Литература
- Окружающий мир
- Человек и мир
- Испанский язык
- 4 Класс
- Математика
- Английский язык
- Русский язык
- Немецкий язык
- Белорусский язык
- Украинский язык
- Информатика
- Основы здоровья
- Музыка
resheba.me
ГДЗ по химии для 8 класса на 5.fun
ГДЗ по химии для 8 класса на 5.fun ГДЗ 8 класс Химия- Химия 8 класс
- авторы: И.И. Новошинский, Н.С. Новошинская
- издательство: Русское слово
- Химия 8 класс
- авторы: Кузнецова Н.Е., Титова И.М., Гара Н.Н.
- издательство: Вентана-граф
-

- Химия 8 класс рабочая тетрадь
- автор: Габрусева Н.И.
- издательство: Просвещение
- Химия 8 класс тетрадь для оценки качества знаний
- авторы: О.С. Габриелян, А.В. Купцова
- издательство: Дрофа
- Химия 8 класс
- авторы: Оржековский П. А., Мещерякова Л. М.
- издательство: Аст/Астрель
- Химия 8 класс
- авторы: Ерёмин В.В., Кузьменко Н.Е., Дроздов А.А.
- издательство: Дрофа
- Химия 8 класс
- авторы: Минченков Е.Е., Журин А.А., Оржековский П.А.
- издательство: Мнемозина
- Химия 8 класс рабочая тетрадь
- авторы: Гара Н.Н., Ахметов М.А.
- издательство: Вентана-граф
-

- Химия 8 класс
- автор: Журин А.А.
- издательство: Просвещение
-

- Химия 8 класс тетрадь-тренажёр
- автор: Гара Н.Н.
- издательство: Просвещение
-

- Химия 8 класс тетрадь-практикум
- автор: Журин А.А,
- издательство: Просвещение
-

- Химия 8 класс тетрадь-экзаменатор
- авторы: Бобылёва О.Л., Бирюлина Е.В., Дмитриева Е.Н.
- издательство: Просвещение
- Химия 8 класс
- авторы: Шиманович И.Е., Красицкий В.А., Сечко О.И., Хвалюк В.Н.
- издательство: Народная асвета
- Химия 8 класс сборник контрольных и самостоятельных работ
- авторы: Масловская Т.Н., Пашуто Е.Н., Власовец Е.Н.
- издательство: Аверсэв
- Химия 8 класс сборник задач
- автор: Рябов М.А.
- издательство: Экзамен
-

- Химия 8 класс
- авторы: Габриелян О.С., Остроумов И.Г., Сладков С.А.
- издательство: Просвещение
- Химия 8 класс контрольно-измерительные материалы
- авторы: Троегубова Н.П., Стрельникова Е.Н.
- издательство: ВАКО
- Химия 8 класс рабочая тетрадь
- автор: Габриелян О.С.
- издательство: Дрофа
Часто ищут
-

- Геометрия 8 класс
- автор: А.В. Погорелов
- издательство: Просвещение
-

- Русский язык 8 класс
- авторы: Рыбченкова Л.М., Александрова О.М., Загоровская О.В.
- издательство: Просвещение
-

- Геометрия 8 класс
- авторы: Л.С. Атанасян, В.Ф. Бутузов, С.Б. Кадомцев
- издательство: Просвещение
-

- Русский язык 8 класс рабочая тетрадь
- авторы: Л. М. Рыбченкова, О. М. Александрова
- издательство: Просвещение
-

- География 8 класс тетрадь-тренажер
- автор: Николина В. В.
- издательство: Просвещение
-

- Биология 8 класс
- авторы: В. В. Пасечник, А. А. Каменский, Г. Г. Швецов
- издательство: Просвещение
-

- Физика 8 класс
- авторы: С.В. Громов, Н.А. Родина
- издательство: Просвещение
-

- Русский язык 8 класс
- авторы: Л.А. Тростенцова, Т.А. Ладыженская, А.Д. Дейкина, О.М. Александрова
- издательство: Просвещение
- История 8 класс
- автор: Н. В. Загладин
- издательство: Русское слово
na5.fun

