Определение плотность металлов – Определение плотности металлов и сплавов
alexxlab | 29.03.2020 | 0 | Вопросы и ответы
Определение плотности металлов и сплавов
Химическая лаборатория ИЦ “Композит-Тест” проводит определение плотности металлических образцов и других твердых непористых веществ.
Плотность является одной из важнейших физических величин, характеризующих свойства вещества.
Плотностью вещества называется отношение массы тела к его объему и выражается в г/см3. Плотность является постоянной величиной для каждого химически однородного вещества при данной температуре.
Для определения плотности металлических, пластмассовых образцов нами применяется гидростатический метод, который обеспечивает наиболее точное измерение плотности.
Гидростатический метод определения плотности в твердых образцах описан в:
- ГОСТ 20018-74 “Сплавы твердые спеченые”;
- ГОСТ 25281-82 “Металлургия порошковая. Метод определения плотности формовок”;
- ГОСТ 15139-69 “Пластмассы. Методы определения плотности (объемной массы)”;
- ТУ 48-19-76-90 “Вольфрам металлический для металлургических целей. Технические условия”
Для определения плотности применяются жидкости, хорошо смачивающие материалы, которые не должны растворять и пропитывать образец или вступать с ним в реакцию, а также не должны улетучиваться во время определения (например, этиловый спирт, ацетон и другие).
В качестве жидкости для взвешивания мы применяем дистиллированную воду.
Гидростатический метод определения плотности материала состоит во взвешивании образца в воздухе, а затем в воде и вычислении его плотности. Метод предназначен для определения плотности формованных изделий (стержни, бруски, трубки, твердые спеченые сплавы, штабики и пластины металлического вольфрама и молибдена).
При взвешивании температура испытуемого образца, жидкости и окружающего воздуха должна быть одинаковой. Температуру дистиллированной воды, в которую помещаем образец, поддерживаем постоянной, или, если это невозможно, измеряем температуру до и после каждого взвешивания, принимая в расчет среднее из полученных значений.
Значения плотности дистиллированной воды в зависимости от температуры воздуха приводятся в нормативных документах на испытуемый материал.
Имеются и другие методы определения плотности веществ, которые приводятся в ГОСТ 15139-69 “Пластмассы. Методы определения плотности (объемной массы)”.
Пикнометрический метод заключается в сравнении масс одинаковых объемов испытуемого вещества и жидкости известной плотности. Жидкость должна смачивать испытуемое вещество и стенки пикнометра, а ее плотность не должна быть выше плотности исследуемого вещества. В качестве такой жидкости применяют бензин, толуол, ксилол и другие органические жидкости. Метод применяется для определения плотности формованных изделий, порошков, гранул, хлопьев.
Метод обмера и взвешивания заключается в определении плотности вещества по отношению массы к его объему, определяемым непосредственно взвешиванием и обмером.
Допускается измерять объем другими методами, например по вытесненному объему жидкости для образцов неправильной или трудно измеряемой формы. Метод применяется для определения плотности изделий, полуфабрикатов (стержни, бруски, трубы, отливки).
Заявку на выполнение работ по определению плотности различных металлов и сплавов можно сделать по телефону (495) 513-20-71
kompozit-test.ru
9. Определение плотности металла
Предлагается единый метод определения плотности сталей, из которых изготовлены детали и узлы теплоэнергетического оборудования.
Методика относится к элементам, которые эксплуатируются при рабочих напряжениях и повышенных температурах:
для углеродистой стали tраб –больше или равна 400°С;
для перлитной и ферритной стали tраб больше или равна 470°С;
для аустенитной, мартенситной и мартенсито-ферритной стали tраббольше или равна 525°С.
Методика определения плотности стали в исходном состоянии и после эксплуатации позволяет выявить динамику ее изменения на разных этапах работы теплоэнергетического оборудования. Плотность стали на каждом этапе эксплуатации оборудования определяется структурным и фазовым составом материала, а также уровнем его поврежденности.
9.1. Сведения о методе
9.1.1. Прецизионный метод определения плотности основан на гидростатическом взвешивании и заключается в последовательном взвешивании образца на воздухе и в жидкости, плотности которых известны. Метод позволяет определять плотность материала без фиксации его объема, что дает возможность оценить плотность образцов любой геометрической формы с заданной относительной погрешностью, не превышающей ±0,01%.
9.1.2. Схема установки для прецизионного определения плотности металлов представлена на рис. 6.
9.1.3. Установка включает в себя:
аналитические весы с погрешностью не более ±10-7кг;
ультратермостат, поддерживающий температуру рабочей среды с точностью не ниже ±0,05°С.
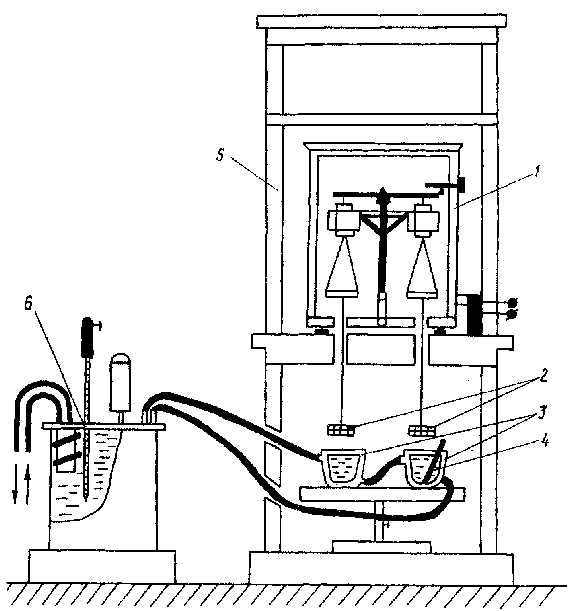
Рис. 6. Установка для прецизионного измерения плотности:
1 – аналитические весы; 2 – система подвесок образцов; 3 – сосуды с рабочей жидкостью;
4 – термометр для контроля температуры рабочей жидкости;
5 – вытяжной шкаф; 6 – ультратермостат
9.1.4. Рабочая среда, в которой производится взвешивание, должна обладать стабильной во времени плотностью; в течение 6 мес. плотность не должна изменяться более чем на ±0,1 кг/м3. При большем изменении плотности жидкость должна быть заменена.
9.1.5. Контроль плотности рабочей среды следует проводить не реже одного раза в месяц. В температурном интервале производства измерений должен соблюдаться линейный закон зависимости плотности от температуры.
9.1.6. Температура кристаллизации рабочей жидкости должна быть меньше 10 °С. Температура кипения рабочей жидкости должна значительно превышать температуру окружающего пространства при проведении взвешивания.
9.1.7. Рабочая жидкость должна обладать вязкостью менее 0,5 Па/с.
9.1.8. Система подвесок, состоящая из капроновых нитей, крепится к нижней поверхности чашек весов. На концах капроновых нитей закрепляются корзинки из платиновой проволоки. Масса подвесок правой и левой чашек весов не должна отличаться более чем на 10-5кг. Корзинки, погруженные в сосуды с рабочей жидкостью, не должны касаться дна сосудов, их стенок или выступать над поверхностью жидкости.
9.1.9. Сосуды с рабочей жидкостью представляют собой стеклянные цилиндры с двойными стенками, между которыми циркулирует вода.
9.1.10. Постоянство температуры жидкости в ультратермостате обеспечивается с точностью ±0,05 °С. Ультратермостат поддерживает температуру рабочей жидкости в сосудах за счет циркуляции воды между стенками цилиндров.
9.1.11. Контроль температуры воды и рабочей жидкости осуществляется термометрами с точностью ±0,05 ° С.
studfiles.net
Металлы определение плотности – Справочник химика 21
Марганец — серебристо-белый твердый хрупкий металл. Его плотность 7,44 г/см , температура плавления 1245 °С. Известны четыре кристаллические модификации марганца, каждая из которых термодинамически устойчива в определенном интервале температур. Ниже 707 °С устойчив а-марганец, имеющий сложную структуру — в его элементарную ячейку входят 58 атомов. Сложность структуры марганца при температурах ниже 707° С обусловливает его хрупкость. Хрупкость — следствие того, что в структуре марганца при [c.518]В лаборатории имеются металлы в следующем виде цинк — гранулы, медь — стружки, железо — опилки, алюминий— тонкая фольга и т. п. Предложите методику определения плотности металла, размеры куска которого измерением линейкой найти невозможно. Для изученных металлов рассчитайте межъядерные расстояния, как об этом говорилось выше, и сформулируйте выводы об изменении их по периоду и подгруппе периодической системы. [c.443]
Образование окисных или солевых слоев влияет не только на анодное растворение металлов, но приводит и к ингибированию многих других электродных процессов. Так, при адсорбции кислорода на платине замедляется скорость ионизации молекулярного водорода в сернокислых растворах. Такое же влияние оказывает адсорбированный кислород и на электроокисление различных органических веществ (метанола, этанола, этилена и др.). На рис. 198 представлены тафелевские зависимости для анодного выделения кислорода на платиновом электроде из растворов хлорной кислоты. При достижении определенной плотности тока происходит резкий рост перенапряжения и выход о Т Г
Выпрямители для процессов гальванопластики должны регулировать силу тока в пределах О—-500 А (до любого технологически заданного значения). Конструируют специальные выпрямители с декадным регулированием напряжения от О до 36 В и, следовательно, силы тока. Выпрямители снабжают счетчиком, контролирующим количество электричества Q, и после достижения заданного значения Q (достижения нужной толщины, массы) электроосаждение металла прекращается отключением выпрямителя. Выпрямительные агрегаты оборудуют также таймерами, и программными устройствами, позволяющими вести процесс осаждения металла по программе (например, заданное время при определенной плотности тока) 12]. Толстые слои металла можно получать реверсом тока, изменением отношения катодного и анодного периода или наложением переменного тока на постоянный. Схемы таких устройств описаны в работе [18]. [c.230]
НИИ сплавов возможны процессы одновременного образования ионов различных металлов. Компоненты, составляющие материал анода, могут образовывать разные фазы, твердые растворы или химические соединения. Если же составляющие сплавы не образуют ни твердых растворов, ни химических соединений и находятся в разных фазах, то при электролизе потенциал анода будет определяться наиболее электроотрицательным компонентом, который и растворяется в то же время более положительные компоненты растворяться не будут. Это приведет к тому, что частицы нерастворившихся включений выпадут в шлам. Если электрорастворение электроотрицательного металла протекает со значительной поляризацией, то при определенных плотностях тока начнется растворение и более электроположительного компонента. Для перехода в раствор при анодном растворении двух компонентов такого сплава необходимо, чтобы их электродные потенциалы были равны, т. е.
При разложении амальгамы в короткозамкнутом элементе э.д. с. расходуется на создание определенной плотности тока разложения. На рис. 3.33 представлен элемент разлагателя амальгамы, в котором графитовая насадка находится в растворе гидроксида щелочного металла. Сила тока, протекающая в таком элементе по контуру, показанному стрелками, равна [c.88]
Не потеряли своего значения и электрохимические методы измерения адсорбции. Хемосорбированный на металле кислород, равно как и возникающие при окислении слои оксидов, могут быть электрохимически восстановлены в электролитах при соответствующих потенциалах электродов [39]. Процесс восстановления кислородсодержащих поверхностных соединений металла осуществляется при пропускании тока определенной плотности через электрохимическую ячейку, в которой исследуемый образец является катодом. При фиксируемой плотности тока исследуется изменение потенциала электрода во времени, причем потенциал отсчитывается по отношению к потенциалу одного из стандартных [c.32]
Часто ставится вопрос сколько времени требуется для проведения полного анализа породы . Это зависит, конечно, от минералогической сложности анализируемой породы и от того, как работает выполняющий анализ аналитик. Если в лаборатории имеется препаратор, который проводит измельчение, и если не требуется определения плотности, то после долгой практики можно научиться так экономить каждую минуту рабочего дня, чтобы при обилии платиновой посуды и возможности непрерывного пользования, днем ]i ночью, воздушными и водяными или паровыми банями и при условии отсутствия случайных задержек, — через каждые три дня после выполнения первого анализа заканчивать по одному анализу из серии образцов горных пород сходного характера, содержащих каждый от 18 до 20 определяемых количественно компонентов. В число последних не входят фтор, углерод, азот, металлы сероводородной группы п кобальт. [c.888]
Для установления степени загрязнения более чистого металла использовали физические методы определение плотности [273, 274], удельного электрического сопротивления [1406, 1444], температурного коэффициента электрического сопротивления [1406] и т. д. Из физических методов наиболее пригодным считался рентгенографический метод Дебая — Шерера, который позднее был подвергнут критике [2051]. [c.220]
Примерами необходимых отливок из металлов являются тела одинакового объема для определения плотности вещества, [c.90]
При контроле стыковых и угловых швов, для определения непроваров, трещин, крупных шлаковых включений Для определения плотности сварных швов для жидкостей и газов Для выявления внутренних дефектов в сварных соединениях стальных конструкций и из других тяжелых металлов толщиной от 30 до 250 мм [c.746]
Пассивации металлов сопутствует сдвиг их потенциалов в положительную сторону. Пассивность железа, стали и других металлов можно вызвать электрохимическим путем с помощью анодной поляризации (например, в разбавленной серной кислоте при наложении постоянного тока определенной плотности). Указанное явление положено в основу анодной защиты. [c.48]
При увеличении плотности тока возрастает число возникающих в единицу времени кристаллических новообразований. Распределение тока по поверхности выделяющегося металла становится более равномерным и получающийся осадок более мелкокристаллическим. Однако увеличение плотности тока сопровождается более значительным обеднением ионами выделяющегося металла прилегающего к электроду слоя раствора. Это ведет к увеличению скорости роста некоторых наиболее крупных кристаллических образований, крайние точки которых находятся в более отдаленных от поверхности и более богатых ионами данного металла слоях электролита. При этом образуются дендриты — хрупкие веточки кристаллов, что опять приводит к механическим потерям. Следовательно, при электровесовых определениях плотность тока должна соответствовать некоторому среднему оптимальному значению (обычно порядка 10 2—а/см ). Если выделение металла сопровождается выделением водорода, то образуются очень непрочные порошкообразные или губчатые осадки. При этом защелачивание приэлектродного слоя может привести к образованию и включению в осадок металла его гидроокиси или основных солей. [c.295]
Для определения потенциалов разряда металлов на висмуте были сняты поляризационные кривые катодного осаждения (рис. 2) и кривые потенциал — время (рис. 3) в начальный момент электролиза (первые 0,01—0,2 мин.) при определенной плотности тока. Из [c.217]
Процесс электролиза может быть использован для так называемой электрополировки металлов, заключающейся в анодном растворении поверхностного слоя металла. В литературе есть указания на возможность электрополировки изделий из вольфрама [192] при погружении металлического вольфрама в раствор едкого натра соответствующей концентрации и анодной поляризации металла подбирая для данной концентрации едкого натра определенную плотность тока и температуру получают гладкую, как бы полированную поверхность. [c.87]
Таким образом, методы, основанные на применении переменных токов, пригодны для определения плотностей тока обмена в интервале от мка-см до а-см . Для определения малых плотностей тока обмена в особенности подходит метод с использованием постоянного тока. Методы включения здесь тоже применимы, однако они из-за громоздкости аппаратуры только тогда с успехом применяются, когда можно ожидать быстрого изменения поверхности, как, например, при поляризации электродов металл/ионы металла. [c.462]
При электролитическом полировании погруженный в электролит предмет работает как анод. Постоянный ток определенной плотности растворяет металл с поверхности и одновременно сглаживает ее. Ход процесса зависит от состава электролита, температуры, плотности тока и времени его пропускания. [c.139]
На рис. 190 представлена зависимость количества возникающих на поверхности точечных анодов и их глубины от плотности анодного тока. Эта зависимость в логарифмических координатах описывается уравнением прямой с показателем степени п = , что указывает на наличие прямой пропорциональности между числом возникающих питтингов и плотностью тока. Средняя глубина питтингов при анодной поляризации возрастает с плотностью тока очень медленно, а начиная с определенной плотности тока (5-10 а/см ) она падает (рис. 190, кривая 2). С увеличением плотности поляризующего тока на поверхности металла возникает все больше мелких питтингов (табл. 55). Это является результатом того, что металл в большинстве питтингов пассивируется и они со временем перестают функционировать. Проявляется двойственная роль анодной поляризации в одних центрах она способствует активному растворению металла, в других — пассивированию поверхности. В активном состоянии остается лишь небольшое число активных центров, в которых, очевидно, не был достигнут ток пассивации. В этих центрах скорость растворения металла возрастает непрерывно с плотностью тока вследствие того, что поляризующий ток распределяется на малое число активных центров (рис. 190, кривая 3). [c.356]
СТОЯНИЯ металла и способа определения плотности. Так, некоторые авторы (891] считают наиболее точной цифру 19,050, установленную рентгенографическим методом при 20° С на чистом уране. То же следует сказать и о температурах плавления и кипения цифры. колеблются для температуры плавления от 1105 до 1850° С. Одиако температуры выше 1150° С в настоящее время считаются завышенными, и наиболее правильной принимается величина 1133° С. Температура кипения 3500° С а по новейшим данным (917] 3927° С. Сиборг и Кац [624] приводят несколько меньшую величину (3818°С). [c.350]
Характеристика металла и методы определения Плотность г/см> Год Литератур- ный источник [c.281]
Не во всех комплексных растворах осадки металлов на катоде получаются мелкозернистыми и однородными по структуре. Так, при электролизе станнитных и плюмбитных растворов, протекающем при очень малой поляризации, а также в некоторых -аммиачных растворах в отсутствие поверхностно-активных веществ осадки на катоде по структуре мало отличаются от осадков тех же металлов из растворов простых солей. Возможно, что в таких растворах, по крайней мере до некоторого значения потенциала или до определенной плотности тока, разряжаются гидратированные ионы или комплексы с меньшим числом аддендов, для разряда которых требуется меньшая энергия активации процесса и концентрация которых в растворе, не слишком мала. [c.245]
Поляризационные кривые позволяют изучить кинетику электродных процессов, величину защитного тока при электрохимической. чащите, явление пассивности и др. Существует два способа снятия поляризационных кривых гальваностатический и потенциостатический. Гальваностатический метод заключается в измерении стационарного потенциала металла при пропускании через него тока определенной плотности. По ряду значений потенциалов при соответствующих плотностях поляризующего тока строят кривые катодной или анодной поляризации, т. е. зависимости Е = /(г к) или Е = /(/,г). [c.342]
Совместное осаждение 5п и N1 на катоде достигается ири добавлении фторидов к. члоридам олова и никеля, которые образуют с оловом прочные комплексные анионы 5пр4 и ЗпРгС . При этом равновесный и катодные потенциалы олова приобретают более электроотрицательные значения. Благодаря этому при определенных плотностях тока достигается сближение потенциалов выделения эти.к. металлов на катоде. Совместному осаждению 5п и N1 способствует также неодинаковая деполяризация при разряде ионов обои.х металлов вследствие образования химического соединения Ы18п. [c.53]
О, адсорбированные анионы, адатомы металлов и др.) а/ и ttj/i — соответствующие значения адсорбционных коэффициентов. Уравнение отвечает аддитивному влиянию различных адсорбированных частиц на энергию активации процесса хемосорбции органического вещества. В случае собственной неоднородности поверхности уравнение (3.57) выполняется при условии, что адсорбция различных компонентов происходит на одних и тех же адсорбционных центрах и энергии адсорбции на i-x местах компонентов А, В, С… связаны между собой простой связью (ЛО°а) =а (ДО°в) = a”( AG° ). .., т. е. вид функции распределения для различных компоненто.в сохраняется неизменным. Одновременное выполнение названных условий при адсорбции веществ, сильно отличающихся по своей химической природе, представляется маловероятным. Возможна некоррелируемость или сложная связь свободных энергий и энергий активации процессов хемосорбции различных частиц. Соответственно уравнения, выражающие зависимость Уа от 0i, могут отличаться от уравнения (3.57) и быть значительно более сложными. Аддитивность в большей мере соответствует модели наведенной неоднородности, когда частицы различных сортов одновременно участвуют в соз-.дапии общего дипольного потенциала на поверхности или определенной плотности электронного газа. [c.111]
Оказалось, что потенциалы выделения большинства металлов почти равны равновесным потенциалам на границе данного металла с раствором соли того же металла определенной концентрации, т. е. величины перенапряжения металлов незначительны. Исключение составляют металлы Ре, Со, N1, у которых перенапряжение при значительной скорости выделения составляет 0,2—0,3 в (при комнатной температуре). Потенциалы выделения газов намного превышают равновесные потенциалы. Особенно большое перенапряжение водорода на ртути. Так, например, при плотности тока 10 ма/см в I н. растворе Н2504 оно составляет 1,16 в по отношению к теоретическому равновесному водородному электроду. [c.321]
Поляризационные кривые дают возможность определить скорость электрохимических реакций, протекающих на металле в данной среде. Этот метод нашел применение не только для теоретических исследований, но и для практических задач по выбору подходящих материалов для данных условий. Снятие поляризационных кривых можно проводить гальваностатическим или потенцпостатнческим методом. В первом случае через ячейку пропускают ток определенной плотности и изучают изменение потенциала, во втором — исследуемому электроду задают определенный потенциал и измеряют силу тока, устанавливающуюся в системе при данном потенциале, [c.31]
И. орг. соединений проводят обычно по след, схеме в) исследование внешнего вида, определение осн. физ. юнстант (плотности, Пп, iпл, IKun), регистрация спектров поглощения, испускания и ЯМР, проба на горение и зольность, качеств, обнаружение нек-рых элем. (N, S, Hal, Si, металлов), определение р-римости в воде, в водных р-рах К Т и щелочей, орг. р-рителях б) качеств, функцнональ- анализ в) получение твердых производных (не менее двух) идентифицируемого в-ва и определение их а также ( л их смесей с соответствующими производными швестного соед. отсутствие депрессии г.л смеси — важное доказательство тождества сравниваемых в-в г) сопоставление всех полученных результатов с литературными данны- КЯ для предполагаемого соединения. [c.207]
Плотность тока обмена железа. Определению плотности тока обмена и параметров кинетических уравнений для металлов группы железа посвящено большое количестве исследований. Однако определение ис тинных токов обмена на этих металлах затруднено из-за сложности экспериментального измерения равновесного потенциала. Но косвенные метода – радиохимический [134], экстраполяция тафелевских зависимостей до перенапряжения, равного нуло, или пересечение кривых анодной и катодной поляризаций [135], осциллогра-фический метод [13б] показывают,что величина тока обмена для железа очень мала по сравненш с “нормальными” металлами. Плотность тока обмена железа, по данным [13б], в I М растворе Ь еЗО равна 2 х 10″ А/см , а в работе [137] определенный методом стационарных поляризационных кривых ток обмена в 0,06 М 1 еБ0 при pH 5 составляет [c.44]
Аналогичная картина наблюдалась [102] при катодной поляризации стали в ОЛМ h3SO4. В начале поляризации при повышении плотности тока, по-видимому, увеличивается концентрация адсорбированного на поверхности катода водорода, что вызывает увеличение скорости наводороживания и соответственно уменьшение времени до начала образования трещин. После достижения определенной плотности тока рекомби-пационнып механизм выделения водорода на стали (при низких плотностях тока) заменяется электрохимической эвакуацией водорода. Это приводит к уменьше1 ию концентрации адсорбированного водорода [141 снижается скорость наводороживания катода и увеличивается время до появления трещин в металле. [c.254]
В своем сочинении Конспект курса химической философии Канниццаро обосновал необходимость изменений атомных 1асс ряда металлов, не только-базируясь на результатах определений плотностей пара металлоорганических соединений, но и [ривлекая данные о валентности металлов, их способности да- ать соединения со спиртовыми радикалами. При этом выясни-[ось, что вывод А. Кекуле и некоторых других химиков о посто-[нной валентности металлов неверен. Оказалось, что многие [c.137]
Например, если опустить в раствор Сс1504 пластинку из металлического кадмия, то, возможно, в раствор с металлической пластинки начнут переходить ионы 0(1 +, в результате чего поверхность пластинки зарядится отрицательно за счет избытка электронов. В дальнейшем этот переход начнет уменьшаться, и наконец на границе металл — раствор установится равновесие, которому будет отвечать определенная плотность заряда повёрх-ности электрода и равные скорости перехода ионов металла с электрода в раствор и из раствора на электрод. [c.30]
Менделеев систематически занимался изучением растворов и изоморфных смесей. Сконструировал (1859) пикнометр — прибор для определения плотности жидкости. Создал (1865—1887) гидратную теорию растворов. Развил идеи о существовании соединений переменного состава. Исследуя газы, нашел (1874) общее уравнение состояния идеального газа, включающее как частность зависимость состояния газа от температуры, обнаруженную (1834) физиком Б. П. Э. Клапейроном (уравнение Клапейрона — Менделеева). Выдвинул (1877) гипотезу происхождения нефти из карбидов тяжелых металлов предложил принцип дробной перегонки при переработке нефтей. Выдвинул (1880) идею подземной газификации углей. Занимался вопросами химизации сельского хозяйства. Совместно с И. М. Чельцовым принимал участие (1890—1892) в разработке бездымного пороха. Создал физическую теорию весов, разработал конструкции коромысла, точнейшие методы взвещнвания. [c.334]
Гидриды щелочных металлов кристаллизуются по типу каменной соли (см. стр. 238). Длины ребер а элементарного куба и рентгенометрически определенные плотности d сортавляют (Zintl, 1931) [c.200]
chem21.info
* Плотность этих элементов (газов) измеряется не в г/см3, а в г/л (г/дм3). |
www.sdelaysam.info
Методы определения плотности металлов и сплавов
Министерство образования Российской Федерации
Южно-Уральский государственный университет
Кафедра физического металловедения и физики твёрдого тела
Реферат
На тему: Методы определения плотности металлов и сплавов
Выполнил: Студент группы ФМ-425
Коновалов И.В.
Проверил: Ильин
Челябинск 2010
Плотностью называют массу единицы объема вещества. Массу определяют путем взвешивания. Напомним, что численное значение плотности, выраженное в г/см3, совпадает с численным значением удельного веса, выраженным в гс/см3. Это позволяет при измерениях массы оперировать результатами взвешивания. Поэтому плотность вещества γ можно выразить как отношение веса в вакууме P 0 к его объему V
γ = P 0 /V (1)
Используя закон Архимеда, взвешивание в вакууме можно заменить
взвешиванием в воздухе
P 0 =P1 + V γ1 (2)
Здесь P 1 – вес образца в воздухе, γ 1 – плотность воздуха. Из уравнений
(1) и (2) находим
γ = P1 + V γ1 / V = P1 / V + γ1 (3)
Определение объема образца путем вычисления по результатам измерения его размеров обычно не обеспечивает необходимой точности. По-этому объем образца находят косвенным путем, заменяя измерение размеров взвешиванием. Ниже рассмотрены два метода, в которых используется этот прием.
1.1. Определение плотности методом трехкратного взвешивания
Определяют вес образца в воздухе P 1 , вес пикнометра[1] с жидкостью P 2 и вес пикнометра с жидкостью и образцом, погруженным в жидкость, P 3 .
В двух последних случаях уровень жидкости в пикнометре устанавливают по метке на горловине сосуда. Очевидно, что
P 3 =P 1 +P 2 −V (γ2 −γ1 ) . (4)
В этом уравнении γ2 – плотность жидкости, заливаемой в пикнометр, V (γ2 −γ1 ) – вес жидкости, вытесненной образцом. Из последнего уравнения
V= P 1 +P 2 – P 3 / γ2 −γ1 (5)
Подставив найденное значение V в уравнение (3), получим
γ = P 1 (γ2 −γ1 ) / P 1 +P 2 – P 3 (6)
Жидкость, заливаемая в пикнометр, должна хорошо смачивать его стенки и поверхность образа, чтобы не оставалось пузырьков воздуха, которые могли бы уменьшить величины P 2 и P 3 .
1.2. Метод гидростатического взвешивания
Как и в предыдущем случае, исходным соотношением для определения плотности служит уравнение (3). Для нахождения объема образца его взвешивают в воздухе и в жидкости (P 1 и P 2 соответственно). Вес образца в вакууме можно выразить через его вес в жидкости аналогично соотношению (2). Используя те же соотношения, что и в разделе 1.1, находим
P 0 =P 2 + γ2V . (7)
Так как правые части уравнений (2) и (7) равны, то
V = P 1 – P 2 / γ2 −γ1 (8)
Подставив найденное значение V в уравнение (3), получим
γ = (P 1 (γ2 −γ1 ) / P 1 – P 2 ) + γ1 (9)
Для взвешивания образца в жидкости его привязывают тонкой проволочкой к чаше аналитических весов и погружают в сосуд с жидкостью. Далее взвешивание производится обычным образом. При этом определяют суммарный вес Р3 образца, находящегося в жидкости, и проволочки, частично погруженной в жидкость. Затем определяют вес ( P 4 ) без образца проволочки, опущенной в жидкость на ту же глубину, что и при взвешивании образца. Очевидно, что P 2 =P 3 −P 4 .
[1] Пикнометр – прибор для измерения плотности
mirznanii.com
Плотность металлов (Met), значения и примеры задач
Плотность металлов и другие их физические свойства
Особое строение кристаллических решеток металлов придает им ряд общих свойств.
К одним из наиболее важных физических свойств металлов относятся плотность, твердость и температура плавления. Эти свойства у металлов весьма различны.
Например, наименьшую плотность имеют щелочные металлы, а наибольшую – осмий. Металлы, плотность которых меньше пяти, условно принято называть легкими металлами, а металлы с плотностью больше пяти – тяжелыми.
По твердости металлы сравнивают с алмазом, твердость которого принята за 10. Самыми мягкими являются щелочные металлы, а самым твердым – хром.
Все металлы обладают металлическим блеском. Это свойство объясняется тем, что металлы хорошо отражают от своей поверхности световые лучи. Металлы отражают также радиоволны, что используется в радиотелескопах, улавливающих радиоизлучения искусственных спутников Земли, и в радиолокаторах, обнаруживающих самолеты на больших расстояниях.
Металлы – хорошие проводники электричества и теплоты. Это зависит от наличия в металлических решетках свободных электронов, которые в электрическом поле перемещаются от отрицательного к положительному полюсу. Электрическая проводимость и теплопроводность металлов неодинакова. Она увеличивается от ртути к серебру.
Из наиболее доступных металлов хорошей электрической проводимостью обладают медь и алюминий, поэтому они используются в качестве проводников электрического тока.
Многие металлы пластичны и обладают хорошей ковкостью, что также объясняется особенностью металлической связи. Так как ионы в металлической решетке друг с другом непосредственно не связаны, отдельные слои их могут свободно перемещаться один относительно другого. Самые хрупкие металлы находятся в V, VI и VII группах Периодической системы Д.И. Менделеева.
Распространенность металлов в природе
Самым распространенным металлом в земной коре является алюминий. За ним следуют железо, кальций, натрий, калий, магний и титан. Содержание остальных металлов незначительно. Так, например, хрома в земной коре всего лишь 0,3, никеля – 0,2, а меди – 0,01%.
Металлы встречаются в природе как в свободном, так и в виде различных соединений.
Краткая характеристика химических свойств и плотность металлов
Наиболее общими химическими свойствами металлов является способность их атомов при химических реакциях отдавать валентные электроны и превращаться в положительно заряженные ионы.
Наиболее энергично металлы реагируют с кислородом и серой, электроотрицательность которых велика:
Ca + Cl2 = CaCl2;
2Mg + O2 = 2MgO;
2Na + S = Na2S.
В этих реакциях окислителем является соответствующий неметалл.
Металлы могут окисляться также ионами водорода и ионами других металлов. Например, в ходе реакций взаимодействия металлов с водой, с кислотами и растворами солей:
2Na + 2H2O = 2NaOH + H2;
Zn + 2HCl = Zn + H2;
Fe + CuSO4 = FeSO4 + Cu.
Примеры решения задач
ru.solverbook.com
Металлы Плотность — Определение – Энциклопедия по машиностроению XXL
Напряжения, вызывающие смещение атомов в новые положения равновесия, могут уравновешиваться только силами межатомных взаимодействий. Поэтому под нагрузкой при пластическом деформировании деформация состоит из упругой и пластической составляющих, причем упругая составляющая исчезает при разгрузке (при снятии деформирующих сил), а пластическая составляющая приводит к остаточному изменению формы и размеров тела. В новые положения равновесия атомы могут переходить в результате смещения в определенных параллельных плоскостях, без существенного изменения расстояний между этими плоскостями. При этом атомы не выходят из зоны силового взаимодействия и деформация происходит без нарушения сплошности металла, плотность которого практически [c.53]Результаты экспериментов [44], проведенных на слитках диаметра 30 и высотой 70 мм и закристаллизованных под поршневым давлением, показали, что при увеличении давления плотность дислокаций, определенная методом ямок травления, возрастает (рис. 12). При этом наибольшее изменение плотности дислокаций наблюдается при приложении давления до 200 МН/м . В этом же интервале давлений наиболее существенно измельчается структура сплавов и металлов, а также происходит изменение и других структурных характеристик [c.30]
Даже хорошо отожженные металлы содержат большую плотность дислокаций, оцениваемую приблизительно 10 —10 см 2. При пластических деформациях металлов плотность дислокаций значительно возрастает и может достигать 10 —10 см- и выше. Однако плотность дислокаций увеличивается не только при пластических деформациях статического нагружения. Большинство экспериментальных работ, посвященных исследованию дислокационной структуры при усталости и ультразвуковых колебаниях, показывает, что, несмотря на относительно малые амплитуды напряжений (деформаций), плотность дислокаций возрастает в процессе циклического нагружения. После некоторого числа циклов нагружения она достигает определенной величины насыщения и в дальнейшем остается практически постоянной. Большей амплитуде напряжения (деформации) циклического нагружения соответствует и большая величина насыщения плотности дислокаций. Полученная при этом дислокационная структура зависит не только от величины амплитуды напряжения (деформации) циклического нагружения, но и от кристаллического строения материала и температуры, при которой проводится эксперимент. [c.176]
Уравнение Тафеля выводится с учетом процессов активации, управляющих растворением чистого металла. При точном выдерживании условий эксперимента константа Тафеля Ь может быть определена по величине наклона прямолинейного участка экспериментальной поляризационной кривой, а плотность тока обмена to — экстраполированием прямой линии до — О, что соответствует величине стандартного электродного потенциала металла. Если для определения констант Тафеля и получения сопутствующей информации используются экспериментальные данные, то необходимо обеспечить отсутствие посторонних факторов, способных исказить результаты. Это весьма сложная задача. Имеются два основных фактора, препятствующие экспериментальному определению наклона Тафеля, а именно концентрационная и омическая поляризации. Рассмотрим их ниже. [c.78]
Компоненты сплава или название сплава Химическая формула Плотность Опытно определенное процентное содержание компонентов Модули упругости (кгс/мм ) Отношение скорости звука в металле к скорости звука в воздухе из опытов на s s E > 1 a С Ф s s 1 о 0 s Л 4 Q z s S3 1 = 5 a u u i s a С [c.308]
При температуре 7 , составляющей около 40 / абсолютной температуры плавления и дальнейшем ее повышении в деформированном металле происходит с определенной скоростью явление рекристаллизации. Оно состоит в том, что искаженная за счет деформации кристаллическая решетка восстанавливается, исчезают микродефекты металла, возрастает его плотность. Происходит это за счет избыточной энергии деформации искаженной структуры и вследствие того, что при высокой температуре значительно облегчается диффузия атомов. Пластичность в результате рекристаллизации заметно увеличивается, т. е. при прочих равных условиях металл имеет повышенную способность деформироваться без разрушения, сопротивление (предел текучести, прочности) уменьшается. [c.192]
При определении массы наплавленного металла плотность р принята для сталей 7,8 г/сж (табл. 30—32 39—42) для алюминиевых сплавов 2,7 г/с,и (табл. 43) для титановых сплавов 4,5 г/с.и (табл. 45). [c.36]
Уже более осторожно можно сказать об уменьшении размера зерна с увеличением перенапряжения (или плотности тока) при получении металла из вполне определенного электролита. Здесь при изменении плотности тока в результате изменения ситуации в приэлектродном слое и условий кристаллизации структура может изменяться не столь простым образом. Итак, общая тенденция уменьшения размера зерна с ростом поляризации при выделении металла не всегда оказывается справедливой. [c.41]
При механизированной сварке под флюсом глубина проплавления основного металла в определенных пределах не зависит от формы подготовки кромок и величины зазора, что объясняется высокой плотностью тока и концентрированностью теплового действия дуги при этом способе сварки, [c.13]
При разности потенциалов на электродах происходит ионизация межэлектродного промежутка. Когда напряжение достигнет определенного значения, в среде между электродами образуется канал проводимости, по которому устремляется электрическая энергия в виде импульсного искрового или дугового разряда. При высокой концентрации энергии, расходуемой за 10″ —10 с, мгновенная плотность тока в канале проводимости достигает 8000—10 ООО А/мм , в результате чего температура на поверхности обрабатываемой заготовки-электрода возрастает до 10 ООО—12 ООО °С. При этой температуре мгновенно оплавляется и испаряется элементарный объем металла и на обрабатываемой поверхности заготовки образуется лунка. Удаленный металл застывает в диэлектрической жидкости в виде гранул диаметром 0,01—0,005 мм. [c.401]
Очень большая замедленность анодной реакции ионизации металла имеет место при возникновении анодной пассивности (см. с. 305). Анодная поляризация металлов в определенных условиях может облегчать переход металлов в пассивное состояние (образование на металле первичных фазовых или адсорбционных защитных пленок), что сопровождается резким торможением анодного процесса с соответствующим самопроизвольным падением плотности тока и значительным смещением потенциала электрода в положительную сторону (участок BE на рис. 137) до значений, достаточных для протекания нового анодного процесса, обычно выделения кислорода [участок EF кривой (Ко,)обр DEF на рис. 137]. Значение этого вида анодной поляризации рассчитать нельзя и его берут обычно из опытных данных. [c.197]
В экспериментальной установке для определения теплоотдачи жидких металлов по трубке диаметром d=l2 мм и длиной / = = 1 м течет висмут. Трубка обогревается электрическим нагревателем плотность теплового потока на стенке постоянна по длине трубки и равна 9с = 6-10 Бт/м1 [c.102]
Представление о том, что коррозия порождается разностью потенциалов между анодными и катодными участками и ее скорость пропорциональна этой разности, лежит в основе так называемой теории микрогальванических элементов Определенный вклад в суммарную скорость коррозии этот фактор действительно вносит. Однако вклад этот весьма невелик, обычно меньше 1—2 %, и исчезающе мал для чистых металлов. В первом приближении поверхность корродирующего металла можно считать изопотенциальной. Скорость коррозии определяется значением анодной плотности тока при коррозионном потенциале. Сказанное относится к микрогальваническим элементам, но не к полиметаллическим системам, где коррозия происходит при контакте разнородных металлических частей значительных размеров. Количественный анализ этих явлений приведен в [2а и 2Ь]. — Примеч. ред. [c.24]
Обычно поляризуются как катодные, так и анодные участки. Это явление называется сл(е-шанным контролем. Следует заметить, что степень поляризации зависит не только от природы металла и электролита, но и от истинной площади корродирующего электрода. Если площадь поверхности анодных участков корродирующего металла очень мала, например из-за пористых поверхностных пленок, коррозия может сопровождаться значительной анодной поляризацией, даже если измерения показывают, что при данной плотности тока незащищенные участки анода поляризуются незначительно. Следовательно, отношение площадей поверхности анода и катода также является важным фактором в определении скорости коррозии. Если на график вместо суммарного коррозионного тока нанести плотность тока, например для случая, когда площадь анода составляет половину площади катода, мы получим поляризационные кривые, представленные на рис 4.9. [c.63]
Разрушение пассивности ионами С1 чаще происходит локально, на тех участках поверхности, где структура или толщина пассивной пленки изменены. Образуются мельчайшие анодные участки активного металла, окруженные большими катодными площадями пассивного металла. Разность потенциалов между подобными участками 0,5 В или более, и эти элементы называют активно-пассивными элементами. Высокие плотности тока на аноде обусловливают высокую скорость разрушения металла, что создает катодную защиту областей металла, непосредственно окружающих анод. Фиксирование анода на определенных участках приводит к образованию питтингов. Чем больше ток и катодная защита около питтинга, тем меньше вероятность образования другого питтинга по соседству. Поэтому плотность расположения глубоких питтингов обычно меньше, чем мелких. Исходя из вероятности образования активно-пассивного элемента очевидно, [c.84]
Как уже говорилось, исходный металл, не подвергавшийся еще никаким нагрузкам, содержит в себе начальную плотность дислокаций, которая возрастает при нагружении. На границе перехода металла из упругого в пластическое состояние достигается критическое значение плотности дислокаций, но сами дислокации в металле располагаются хаотически (рис. 70, а). Один из механизмов диссипации подводимой энергии – преобразование ее в энергию образования дислокаций. За счет этого каждая вновь возникающая одиночная дислокация запасает определенную порцию энергии Е (см. рис 69, а). Следующий механизм диссипации позволяет избавляться от части энергии, запасенной одиночными дислокациями, за счет их перемещения и объединения (см. рис. 69, б). Оба этих механизма действуют на всех масштабных уровнях. Но если в масштабе отдельных дислокаций они приводят к формированию дисклинаций (см. рис. 69, в), то в больших масштабах в действие вступают коллективные эффекты. Они позволяют целым коллективам дислокаций действовать как единое целое и формировать более крупные и сложные структуры. [c.109]
До определенного момента дисклинации имеют возможность перемещаться лишь параллельно самим себе (трансляционный характер перемещения). Это обусловлено относительно низкой плотностью дислокаций, которая недостаточна, чтобы обеспечить возможность какого-либо еще вида движения внутри металла, ведь дислокации делают структуру металла более разряженной и внутренне напряженной. Металл становится более текучим и по ряду свойств приближается к жидкому состоянию. Некоторые авторы предлагают рассматривать пластически деформированное состояние металла как особое сильно возбужденное состояние кристалла, к которому принципиально неприменима теория возмущений идеального кристалла. [c.109]
Согласно второй точке зрения, металлы, пассивные по определению 1, покрыты хемосорбционной пленкой, например, кислородной. Такой слой вытесняет адсорбированные молекулы HjO и уменьшает скорость анодного растворения, затрудняя гидратацию ионов металла. Другими словами-, адсорбированный кислород снижает плотность тока обмена (повышает анодное перенапряжение), соответствующую суммарной реакции М -f гё. Даже доли монослоя на поверхности обладают пассивирующим действием [16, 17]. Отсюда следует предположение, что на начальных этапах пассивации пленка не является диффузионно-барьерным слоем. Эту вторую точку зрения называют адсорбционной теорией пассивности. Вне всякого сомнения, образованием диффузионно-барьерной пленки объясняется пассивность многих металлов, пассивных по определению 2. Визуально наблюдаемая пленка сульфата свинца на свинце, погруженном в h3SO4, или пленка фторида железа на стали в растворе HF являются примерами защитных пленок, эффективно изолирующих металл от среды. Но на металлах, подчиняющихся определению 1, основанному на анодной поляризации, пленки обычно невидимы, а иногда настолько тонки (например, на хроме или нержавеющей стали), что не обнаруживаются методом дифракции быстрых электронов . Природа пассивности металлов и сплавов этой группы служит предметом споров и дискуссий вот уже 125 лет. Представление, что причиной пассивности всегда является пленка продуктов реакции, основано на результатах опытов по отделению и исследованию тонких оксидных пленок с пассивного железа путем его обработки в водном растворе KI + I2 или в ме-танольных растворах иода [18, 19]. Анализ электроно рамм пле- [c.80]
Дислокации формируются естественным образом при кристаллизации металла, когда в качестве зародышей твердой фазы выступают фуллереновые комплексы (см. раздел 3.4,2), Дислокации являются неотъемлемой частью реальных металлов и несут определенные функции. Исследования показали, что металлические материалы достигают энергетически наиболее выгодного состояния лишь в том случае, когда в них присутствует определенная равновесная плотность дислокаций – р. Под плотностью дислокаций понимают суммарную длину дислокаций в см, приходящуюся на единицу объема Vкристалла, выраженную в см1 Таким образом, размерность р – см При производстве металлических материалов начальная плотностью дислокаций составляет обычно менее 10 см . [c.105]
Определение электродных потенциалов позволяет судить о коррозионной стойкости различных зон сварного соединения, обнаружить их наиболее уязвимые участки. Изменением потенциалов можно воспользоваться для выбора наиболее безопасного в коррозионном отношении метода и режима сварки. Особенно опасным является случай, когда шов или ЗТВ являются анодом, а основной металл – катодом макрогальванического элемента. Из-за их малой площади по сравнению с основным металлом плотность коррозионного тока будет весьма высокой, а следовательно, будет высокэй и скорость растворения. [c.44]
Сущность метода гидростатического взвешивания заключается в измерении массы отделенного от основного металла покрытия на воздухе и в жидкости с известной плотностью. При определении общей пористости по ГОСТу 18898—73 покрытие сначала взвешивают на воздухе с точностью 0,005 г. После этого поверхностные поры покрытия закрывают путем пропитки в расплавленном парафине или тонким слоем вазелина или лака. Покрытие пропитывают, полностью цогружая его в расплавленный парафин и выдерживая в нем до прекращения выделения пузырьков воздуха. Если на покрытие наносится лак, то после погружения излишки лака удаляют, а покрытие помещают в сушильный шкаф и выдерживают при температуре 50—60 С 10—15 мин. Вазелин наносят на поверхность покрытия, намазывая его тонким слоем с последующим втиранием. [c.78]
Удельное электрическое сопротивление сухого отвала определенное по четырехэлектродной схеме [19,30,51] составляет 20 Ом-м, pH водной вытяжки 3.5-4.5. При влажности 25% и более удельное сопротивление отвала резко снижается и не привышает 1.0 Ом- м. Химический состав отвала включает в себя до 30% сернистых соединений, а также в небольшом количествах медь, цинк, вольфрам, молибден, свинец, кобальт, кадмий, и некоторые другие металлы. Плотность отвала Башкирского медно-серного комбината (БМСК) составляет 1.9 г/см . [c.79]
Важным признаком электрохимических реакций является эквивалентность их скорости плотности токаг. Такая эквивалентность следует из закона Фарадея. Сущность этого закона состоит в том, что, например, для реакции растворения металла величина потери массы металла в течение определенного времени позволяет рассчитать скорость его растворения, а из нее — плотность анодного тока [c.78]
При наличии в системе эффективного катодного процесса фк2 токовая анодная кривая уже заметно отличается от истинной, т. е. коррозионной. Она приобретает вид кривой фазЛ”В”С, на которой появляется катодная ветвь, несмотря на то что металл поляризуется анодно. Такое аномальное поведение электрода свидетельствует о том, что окислительно-восстановительные реакции, протекающие в системе, создают высокие плотности тока, которые намного выше анодных токов, необходимых для пассивации электрода. В таких условиях металл может в определенной области потенциалов перейти в пассивное состояние и без внешнего анодного тока. Аналогичным образом, просуммировав катодную кривую ф2з М с анодной токовой кривой EF, можно получить истинную анодную кривую DE и на участке перепассивации. Более подробный анализ поведения подобных систем сделан в работе Томашова и Черновой [2, с. 13]. [c.30]
Несовершенства кристаллической решетки металла должны оказывать определенное влияние на проницаемость металлических мембран для водорода, так как возможными путями диффузии водорода через металл являются 1) междоузлия кристаллической решетки 2) границы зерен в поликристалличе-ских образцах 3) несовершенства кристаллической решетки внутри зерен. Соотношение между этими видами диффузии устанавливается, очевидно, в каждом конкретном случае в зависимости от состояния металла и условий (температура, давление газообразного водорода вне металла или плотность тока, состав электролита и т. д.). Роль междоузлий и границ зерен в диффузии водорода через железо и сталь обсуждалась ранее (раздел 2.6). Нарушения кристаллической решетки (вакансии, дефекты упаковки, дислокации, малоугольные границы в блоках мозаики и т. д.), вызванные механической или термической обработкой (Металла, могут служить ловушками , коллекторами, для водорода. Это приводит к сильному торможению процесса диффузии водорода через металл [268—270]. Имеющиеся в настоящее время экспериментальные данные недостаточны для того, чтобы надежно разделить влияние на диффузию водорода внутренних напряжений, границ блоков мозаики, дислокаций, вакансий и других нарушений кристаллической решетки [259]. Решение этой задачи осложняется тем, 1что один тип дефектов непрерывным образом может трансформироваться (за счет количественных изменений) в другой. [c.84]
Основной метод исследования пассивности — съемка потенцио-статических анодных поляризационных кривых. При этом методе съемки кривых с помощью по-тенциостата на исследуемый металл подаются строго определенные значения потенциала и регистрируется скорость анодного процесса (анодная плотность тока). [c.55]
Температура рекристаллизации некоторых сплавов алюминия с марганцем, хромом, никелем, цирконием, титаном и другими, переходными металлами, подвергнутых по определенным режимам горячей, а в некоторых случаях и холодной обработке давлением, превышает обычно назначаемую температуру нагрева под деформацию или закалку. Поэтому после закалки и старения таких сплавов в них сохраняется нерекристаллизованная (поли-гонизованная) структура, с высокой плотностью дислокаций,что значительно повышает прочность по сравнению с рекристаллизо-ванной структурой. Это явление получило название структурного упрочнения. [c.368]
Успешное деййтвие зашиты в оптимальных случаях, как уже указывалось выше, достигает 100%, т. е. наблюдается полное прекрашение коррозии, однако условия, при которых наиболее полно подавляется коррозия, должны быть обязательно проверены. Условия, при которых достигается максимальная защита, могут быть установлены различными методами. Наилучшим является постоянный контроль веса защищаемой металлической конструкции. Однако такой контроль на практике не всегда можно осуи ествить, поэтому определяют потери в весе контрольных образцов, включенных в общую защиту сооружения. При всех своих преимуществах (наглядность и надежность) этот метод имеет тот недостаток, что требует для проверки действия защиты достаточно длительного срока, в то время как очень часто необходимо сразу после пуска защиты в действие определить, все ли сооружение находится под достаточной и максимальной защитой. Поэтому приходится прибегат , и к другим критериям защиты, отвечающим требованиям конкретного случая. Такими методами являются измерение величины защитного потенциала поляризации (иначе потенциала трубопровод — земля, металл — земля) или определение защитной плотности тока на защищаемой поверхности. В связи с тем, что защитная плотность тока может быть определена только косвенным путем, наибольшее и повсеместное распространение при осуществлении катодной защиты получил метод измерения защитного потенциала. Необходимо [c.190]
При исследовании указанным методом чистых кристаллов германия [41, 43] было установлено, что дислокации образуют совершен1ю определенную границу, на линии которой направление кристаллографических плоскостей металла изменяется на определенный малый угол, величина которого зависит от плотности дислокаций. Данные измерений подтвердили теоретическое выражение для величины этого угла. Далее была найдена основная причина возникновения дислокаций в твердом кристалле, в котором при охлаждении в процессе изготовления возникали значительные температурные градиенты. [c.78]
Режим электролиза — плотность тока, температура, переме, шивание — влияет не только на структуру и внешний вид электроосажденных сплавов, но и на их химический состав. В общем можно сказать, что повышение плотности тока, понижение температуры, отсутствие перемешивания способствуют повышению процентного содержания в сплаве металла с более электроотрицательным потенциалом. Такое положение, однако, справедливо только в том случае, когда поляризационные кривые для отдельных металлов расположены примерно параллельно друг другу. Если же с повышением плотности тока разряд ионов более благородного металла сопровождается большей катодной поляризацией, чем разряд ионов менее благородного металла, то до определенной плотности тока будет повышаться процентное содержание в сплаве менее благородного металла, а при дальнейшем повышении плотности тока его содержание в сплаве будет падать (см. рис. 33). [c.120]
К фи.зическим свойствам шлака относятся теилофизические характеристики — температура плавления, температурный интервал затвердевания, теплоемкость, теплосодержание и т. п. вязкость способность растворять окислы, сульфиды и т. п. определенная плотность определенная газопроницаемость достаточное различие в коэффициентах линейного и объемного расширения по сравнению с металлом, что необходимо для легкой очистки металла шва. [c.98]
Все эти изменения приводят к тому, что с увеличением деформации уменьшается плотность металла. На рис. 66 приведены результаты о пытов по определению плотности разорванного образца чистого железа. После разрыва в месте шейки (участок 9) деформация была максимальной, а у головки (участ0 К /) почти отсутствовала. По мере приближения к более деформированным участкам плотность уменьшается. [c.85]
После расплавления шихты в сталеплавильной печи образуются две несмешивающиеся среды жидкий металл и шлак. Металл и шлак разделяются из-за различных плотностей. В соответствии с законами распределения закон Нернста), если какое-либо вещество растворяется в двух соприкасающихся, но несмешивающихся жидкостях, то распределение вещества между этими жидкостями происходит до установления определенного соотношения (константы распределения) постоянного для данной температуры. Поэтому большинство компонентов (Мп, Si, Р, S) и их соединения, растворимые в жндкovf металле и шлаке, будут распределяться между металлом и шлаком в определенном соотношении, характерном для данной температуры. [c.29]
На рис. 187 приведена полученная автором и Т. К. Атанасян зависимость скорости растворения алюминия, определенная по количеству металла, перешедшего в раствор, и выраженная в единицах плотности тока t, от потенциала V в растворах уксусной кислоты разных концентраций при 22° С. Как следует из приведенных на рис. 187, а графиков, коррозия алюминия в 2,75 3 и 7-н. растворах СН3СООН протекает при близких стационар- [c.279]
К количественным показателям коррозии помимо перечисленных ранее показателя склонности к коррозии / t, очагового показателя коррозии Кп, глубинного показателя коррозии Кп, показателя изменения массы Кт, объемного показателя коррозии Кобъемн, токового показателя коррозии i (плотность коррозионного тока), механического показателя коррозии Ка, показателя изменения электрического сопротивления относится также отражательный (или оптический) показатель коррозиы — выраженное в процентах изменение отражательной способности поверхности металла за определенное время коррозионного процесса. [c.428]
Поляризационные кривые позволяют изучить кинетику электродных процессов, величину защитного тока при электрохимической защите, явление пассивности и др. Существует два способа снятия поляризационных кривых гальваностатический и потен-циостатический. Гальваностатический метод заключается в измерении стационариого потенциала металла при пропускании через него тока определенной плотности. По ряду значений потенциалов при соответствующих плотностях поляризующего тока строят кривые катодной или анодной поляризации, т. е. зависимости Е = /(г к) или Е = /(/-г). [c.342]
Влияние несимметричности реакций фарадеевское выпрямление) наблюдается особенно часто при вызываемой переменным током коррозии пассивных металлов (в основном, по определению 1 в гл. 5). Показано, что нержавеющие стали корродируют под действием переменного тока [4], алюминий в разбавленных растворах соли разрушается при 15 А/м на 5 %, а при 100 А/м на 31 % по отношению к разрушениям, вызванным при 100 А/м постоянным током той же силы. Феллер и Рукерт [4] изучали воздействие наложения переменного тока (1 В, 54 Гц) на постоянный на никель в 1 и. h3SO4. Оказалось, что на потенцио-статических поляризационных кривых полностью исчезла пассивная область, а высокая плотность анодного тока сохранялась во всей области положительных потенциалов. Чин и Фу [5] отметили аналогичное поведение мягкой стали в 0,5т N82804 при pH = 7. Плотность пассивирующего тока возрастала с повышением плотности наложенного переменного тока, достигая при плотности тока 2000 А/м и частоте 60 Гц критического значения (отсутствие пассивной области). Они нашли также, что при плотности переменного тока 500 А/м потенциал коррозии снижался на несколько десятых вольта, одновременно в отрицательную сторону сдвигалась и область Фладе-потенциала, но [c.209]
В холоднодеформированном металле при нагреве миграция границ зерен и изменение их размера и формы имеет свои специфические особенности. В этом случае получает развитие процесс рекристаллизации обработки или первичной рекристаллизации. Движущей силой процесса служит накопленная при пластической деформации энергия, связанная в основном с образованием дислокаций, имеющих высокую плотность (до 10″…10 см ). Рекристаллизация обработки приводит к образованию новых равноносных зерен с обновленной кристаллической решеткой. При этом свободная энергия рекристаллизованного металла становится меньше, чем деформированного вследствие уменьшения плотности дислокаций (до 10. ..10 см ). Процесс состоит из образования зародышей новых зерен и их роста. Имеется определенная аналогия с фазовыми превращениями диффузионного типа. Накопленная в объеме зерен энергия деформации примерно в 100 раз выше поверхностной энергии их границ, поэтому рекристаллизация на первых этапах может привести к образованию мелких зерен и увеличению их числа (по сравнению с деформированным металлом). [c.507]
mash-xxl.info

