Сообщение о сплавах – Сплавы, их классификация и свойства
alexxlab | 19.05.2020 | 0 | Вопросы и ответы
ОСНОВНЫЕ СВЕДЕНИЯ О МЕТАЛЛАХ И СПЛАВАХ — Студопедия.Нет
Раздел первый ОСНОВЫ МЕТАЛЛОВЕДЕНИЯ
Глава I ОСНОВНЫЕ СВЕДЕНИЯ
О МЕТАЛЛАХ И ИХ СПЛАВАХ
Общие сведения о металлах и их сплавах
В настоящее время известно 107 химических элементов (см. Периодическую систему элементов Д. И. Менделеева), которые делятся на две основные группы: металлы и неметаллы (металлоиды). Большинство элементов (83) — металлы, отличительными признаками которых являются непрозрачность, специфический блеск, высокая теплопроводность и электропроводность, ковкость и др. При обычной температуре все металлы, кроме ртути, находятся в твердом состоянии. Металлоиды не имеют таких свойств.
Перечисленными выше свойствами металлы обладают в различной степени, что и определяет их различное практическое использование. Наиболее широкое применение в промышленности получили железо, медь, алюминий, магний, свинец, цинк и олово.
В земной коре металлы занимают небольшое место (около 15% по массе), остальную часть составляют кислород (49%), кремний (26%) и другие металлоиды. Самыми распространенными металлами являются алюминий (7%) и железо (5%), реже встречаются кальций, натрий, магний и калий. Содержание урана, золота, платины и других редких металлов определяется миллионными и миллиардными долями процента.
В технике слово «металлы» объединяет чистые металлы и сплавы. Чистыми металлами называют химические элементы обычно с небольшими добавками других элементов (примесей). Например, техническая медь содержит примеси свинца, висмута, сурьмы, железа, мышьяка, олова и других элементов.
Сплавы — это сложные материалы, образующиеся путем соединения двух и более элементов (в том числе и неметаллов).
Чистые металлы имеют заданные природой свойства. Сплавам можно придать необходимые свойства, поэтому они и получили наибольшее распространение.
В промышленности металлы обычно делят на две группы: черные и цветные. Черные металлы — это железо и его сплавы с углеродом (сталь и чугун). Цветные металлы — это медь, алюминий, магний, никель, цинк, олово, свинец и др. и их сплавы. Наиболее распространены черные металлы (на их долю приходится более 90% общей массы металлов). Из металлоидов широко применяют углерод и кремний.
Металлы получают из металлических руд, которые представляют собой скопление химических элементов в виде простых веществ или соединений. Добычей руд из недр земли занимается горнодобывающая промышленность, получением металлов и сплавов из руд — металлургическая. В соответствии с делением металлов на черные и цветные металлургия делится также на черную и цветную.
В настоящее время выплавляют около 75 металлов и огромное количество сплавов.
§ 2. Внутреннее строение металлов и их сплавов
Все вещества состоят из атомов, а атом — из положительно заряженного ядра и вращающихся вокруг него отрицательно заряженных электронов (рис. 1). В ядре находятся положительно заряженные частицы — протоны. Количество протонов при обычном состоянии атома равно количеству электронов, т. е. атом электрически нейтрален. Число электронов, обозначенное порядковым номером в периодической системе элементов Д. И. Менделеева, для каждого элемента различно. Атом при определенных условиях может терять и приобретать электроны. Если электронов станет больше, чем протонов, то он будет заряжен отрицательно, а если меньше, то положительно. Такой электрически заряженный атом называется попом.
Электроны вращаются вокруг ядра по орбитам, число которых определяется номером периода элемента в периодической, системе.
У металлов на внешней орбите находятся один, два или три электрона, слабо связанных с ядром, поэтому под воздействием положительно заряженных атомов они могут отрываться от своего атома, превращая его в положительно заряженный ион. Электроны, свободно переходящие от одного атома к другому, называются свободными.
Атомы металлоидов при определенных условиях стремятся заполнить внешнюю оболочку, т. е. присоединить электроны и превратиться в отрицательно заряженные ноны.
ОСНОВНЫЕ СВЕДЕНИЯ О МЕТАЛЛАХ И СПЛАВАХ
Используемые в технике металлические материалы разделяют на простые и сложные металлы (сплавы).
Простые металлы состоят из одного основного элемента и незначительного количества примесей других элементов. Например, технически чистая медь содержит от 0,1 до 1 % примесей свинца, висмута, сурьмы и других элементов.
Сплавы — это сложные металлы, представляющие сочетание какого-либо простого металла (основы сплава) с другими металлами или неметаллами. Например, латунь — сплав меди с цинком. Здесь основу сплава составляет медь.
Химический элемент, входящий в состав металла или сплава, называется компонентом. По числу компонентов сплавы делятся на двухкомпонентные (двойные), трех-компонентные (тройные) и т. д.
Большинство сплавов получают сплавлением компонентов в жидком состоянии.
Сплавы превосходят простые металлы по прочности, твердости, обрабатываемости и т. д. Вот почему они применяются в технике значительно шире простых металлов. Например, железо — мягкий металл, почти не применяющийся в чистом виде. Зато самое широкое применение в технике имеют сплавы железа с углеродом — стали и чугуны.
Все применяемые в технике металлы и сплавы делят ся на черные и цветные.
К черным металлам относятся железо и его сплавь (сталь и чугун). Все остальные металлы и сплавы состав представляют группу цветных металлов.
Наибольшее распространение в технике получили черные металлы. Это обусловлено большими запасами железных руд в земной коре, сравнительной простотой технологии выплавки черных металлов, их высокой прочностью.
Цветные металлы применяются в технике реже, чем черные. Это объясняется незначительным содержанием многих цветных металлов в земной коре, сложностью процесса их выплавки из руд, недостаточной прочностью. Цветные металлы дороже черных. Во всех случаях, когда это возможно, их заменяют черными металлами, пластмассами и другими материалами.
Из большого числа цветных металлов и сплавов в сельскохозяйственной технике наибольшее распространение получили сплавы алюминия, меди, а также подшипниковые сплавы.
Все металлы и сплавы в твердом состоянии имеют
кристаллическое строение, т. е. их атомы (ионы) расположены в строго определенном порядке. Этим кристаллические тела отличаются от аморфных тел, у которых атомы расположены хаотично. Аморфными телами являются стекло, клей, воск и др.
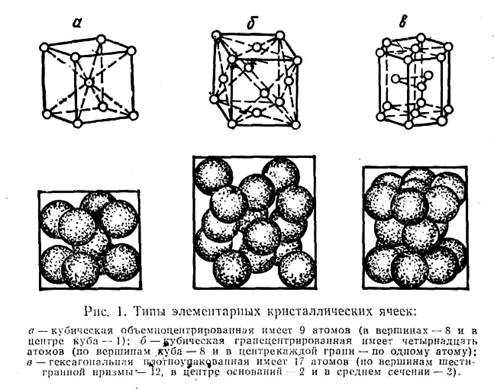 |
Если атомы металла мысленно соединить прямыми линиями, то получится правильная геометрическая система, называемая
В узлах кристаллических решеток металлов расположены положительно заряженные ионы, удерживаемые на определенном расстоянии друг от друга свободными электронами. Такое внутреннее строение обусловливает характерные признаки металлов, такие, как высокая электро- и теплопроводность, пластичность (ковкость) и др.
Свойства металлов и сплавов зависят от природы их атомов, типа кристаллической решетки и от расстояния между атомами в решетке.
Все свойства металлов делятся на физические, химические, механические и технологические.
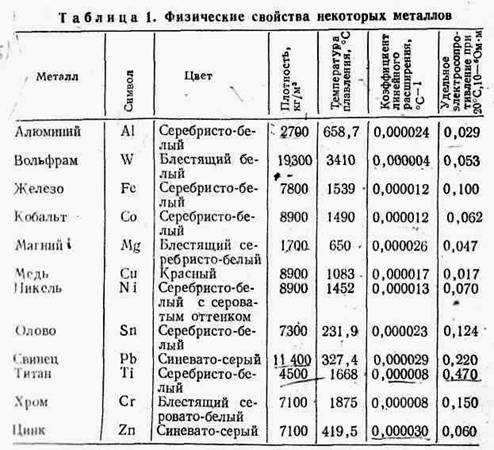
Физические свойстваметаллов и сплавов определяются цветом, плотностью, температурой плавления, тепловым расширением, тепло- и электропроводностью, а также магнитными свойствами (табл. 1). Плотность металла — величина, определяемая отношением массы металла к занимаемому им объему. Она измеряется в кг/м3. Для снижения массы изделия необходимо использовать материалы с небольшой плотностью (сплавы магния, алюминия и титана).
Температура плавления — температура, при которой металл переходит из твердого состояния в жидкое. Знание температуры плавления металлов и сплавов необходимо в металлургии, в литейном производстве, при горячей обработке металлов давлением, при сварке, пайке и других процессах, сопровождающихся нагреванием металлических материалов.
 |
Тепловое расширение – изменение линейных размеров иобъема металлического материала при нагревани. Неодинаковость величины теплового линейного расширения материалов характеризуется коэффициентом линейного расширения а, который показывает, на какую долю первоначальной длины при 0 °С удлинилось тело вследствие нагревания его на 1 °С. Тепловое расширение металлов необходимо учитывать при изготовлении и эксплуатации точных, сложностью приборов и инструментов, изготовлении литейных форм, Прокладке железнодорожных рельс и т. д.
Теплопроводность — способность металлов передавать’ Теплоту от более нагретых частей тела к менее нагретым. Среди металлических материалов лучшей теплопроводностью обладают серебро, медь, алюминий.
Электропроводность — способность металлов провопить электрический ток. Она оценивается на практике Величиной удельного электросопротивления р. Чем меньше электросопротивление, тем более электропроводен металлический материал. Высокой электропроводностью Обладают те металлы, которые хорошо проводят электрический ток (серебро, медь, алюминий).
Способность металлов намагничиваться под действием магнитного поля/называют магнитной проницаемостью. Сильно выраженными магнитными свойствами обладают железо, никель, кобальт и их сплавы. Эти металлы называют ферромагнитными
Механическими свойствамиметаллов называется совокупность свойств, характеризующих способность металлических материалов сопротивляться воздействию внешних усилий (нагрузок).
К механическим свойствам металлов. относятся:
прочность — способность материала сопротивляться действий внешних сил без разрушения; упругость — способность материала восстанавливать свою первоначальную форму и размеры после прекращения действия внешних сил, вызвавших деформацию;
пластичность — способность материала изменять свою форму и размеры под действием внешних сил, не разрушаясь, и сохранять полученные деформации после прекращения действия внешних сил;
твердость — способность материала оказывать сопротивление проникновению в него другого, более твердого тела;
вязкость — способность, металлических материалов оказывать сопротивление быстро возрастающим (ударным) нагрузкам; хрупкость — свойство, обратное вязкости;
1 ползучесть — свойство металлических материалов медленно и непрерывно пластически деформироваться при длительной нагрузке и высоких температурах; усталость — процесс постепенного накопления повреждений материала под действием повторно-переменных напряжений, приводящих к уменьшению долговечности, образованию трещин и разрушению. Способность металлических материалов противостоять усталости называется выносливостью.
Механические свойства являются основной характеристикой металлов и сплавов, поэтому на заводах созданы специальные лаборатории, где производятся различные испытания с целью определения этих свойств.
Механические испытания можно разделить на:
статические, при которых нагрузка, действующая на металлический образец или деталь, остается постоянной или возрастает крайне медленно;
динамические (ударные), при которых нагрузка возрастает быстро и действует в течение незначительного времени;
испытание при повторных или знакопеременных нагрузках — нагрузках, изменяющихся многократно по величине или по величине и направлению.
Рассмотрим основные виды испытаний металлов с целью определения их механических свойств.
Технологические свойства характеризуют способность металлов поддаваться различным видам технологической обработки для получения определенной формы, размеров и свойств: Они имеют большое значение при выборе металлических материалов для изготовления деталей машин и конструкций. Из технологических свойств наибольшее значение имеют обрабатываемость резанием, свариваемость, ковкость, прокаливаемость, литейные свойства.
Обрабатываемостью резанием называется способность металлов подвергаться обработке режущими инструментами для придания деталям определенной формы, размеров (с необходимой точностью) и чистоты поверхности. Обрабатываемость резанием определяется по скорости резания, усилию резания и по шероховатости обрабатываемой поверхности. При разных методах обработки (точении, сверлении, фрезеровании и т. д.) обрабатываемость одного и того же металла может быть различной. Для улучшения обрабатываемости сталей в них допускается повышенное содержание серы, а также вводятся свинец, селен и другие элементы.
Свариваемостью называется свойство металла или сплава образовывать при установленной технологии сварки соединения, отвечающие требованиям, обусловленным конструкцией и эксплуатацией изделия. Свариваемость углеродистых сталей ухудшается с по-вышением содержания в них углерода. Ковкостью называется способность металла без разрушения поддаваться обработке давлением (ковке, штамповке, прокатке и т. д.). Ковкость металла зависит от его пластичности. Чем металл более пластичен, тем лучше он поддается обработке давлением.
Металлы обладают ковкостью как в холодном, так и в нагретом состоянии. В холодном состоянии хорошо куются латуни и сплавы алюминия, сталь — в нагретом • состоянии. Чугун из-за повышенной хрупкости обработке давлением не подвергается.
Прокаливаемость— способность стали воспринимать закалку на определенную глубину от поверхности. Прокаливаемость стали определяется по виду излома, по измерению твердости в различных точках сечения образца, а также методом торцовой закалки.
Литейные свойства металлов определяются жидкоте-кучестью, усадкой и склонностью к ликвации. Жидкоте кучесть — это способность расплавленного металла заполнять форму и давать плотные отливки с точной конфигурацией. Усадка — сокращение объема расплавленного металла при затвердении и последующем охлаждении. Ликвация — неоднородность химического состава твердого металла в разных частях отливки. .
При выборе литейных материалов учитывают, что чугун обладает высокими литейными свойствами: хорошей жидкотекучестью, небольшой усадкой и незначительной склонностью к ликвации. Литейные свойства стали хуже, чем чугуна.
Химические свойства металлов
Химическим свойством называется способность металлов под действием окружающей среды превращаться в другие вещества и изменять свои свойства.
К химическим свойствам относится способность металлов корродировать, т. е. окисляться под действием кислорода воздуха и воды, разрушаться под действием кислот и щелочей, образовывать окалину при нагреве в окислительной среде.
Коррозии(лат. corrosia — разъедание) подвергаются почти все металлы. Например, железо на воздухе ржавеет, медь покрывается зеленым слоем окиси, алюминий — белым слоем окиси и т. д.
Металлы, не поддающиеся коррозии, называются благородными. К ним относятся золото и платина. Они разрушаются только в смеси соляной и азотной кислот, называемой «царской водкой».
Высокой коррозионной стойкостью обладают хром, никель и их сплавы, а титан и его сплавы по коррозионной стойкости приближаются к благородным металлам.
[Химическая коррозия возникает вследствие химического взаимодействия металла со средами, не являющимися проводниками электрического тока (сухие газы, нефть, бензин, керо-син, масла). При этом металлы вступают в химическое взаимодействие с активными веществами внешней среды, обычно с кислородом, в результате чего на поверхности металлов появляются окисные пленки и изделие начинает разрушаться.
Типичным примером химической коррозии является газовая коррозия, которая наблюдается при нагреве заготовок для ковки и термической обработки, деталей топок и дымоходов котлов, проточных частей газовых турбин, выхлопных труб двигателей и т. д. На судах химической коррозии подвергаются внутренние поверхности цистерн с керосином или бензином, танки с нефтью и другими подобными продуктами.
Электрохимическая коррозия возникает при взаимодействии металла с электролитом, т. е. со средами, проводящими электрический ток (щелочи, растворы солей и кислот, вода и воздух). Коррозию металлов в атмосфере воздуха обычно называют ржавлением.
Явления при электрохимической коррозии по своей природе не отличаются от тех, которые происходят в гальванических элементах. Известно, что при работе гальванического элемента положительно заряженные ионы анода переходят в раствор.” При этом анод заряжается отрицательно, а раствор (электролит), приобретая эти ионы, заряжается положительно. Таким образом, возникает разность потенциалов. Чем она больше, тем быстрее переходят ионы с анода в раствор и, следовательно, тем быстрее анод разрушается.
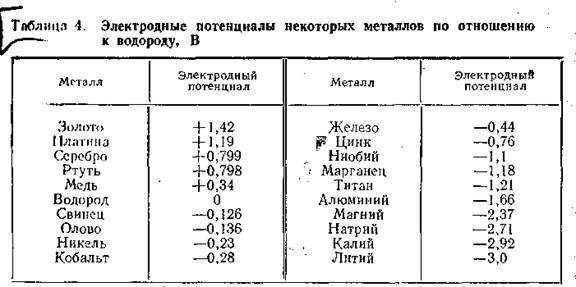
Разность потенциалов, возникающая на поверхности металла, соприкасающегося с электролитом, называется электродным потенциалом. Значения электродных потенциалов элементов измеряют по отношению к водороду, потенциал которого принят равным нулю (табл. 4). Металлы, расположенные выше водорода, электроположительны, а ниже — электроотрицательны.
Если построить гальванический элемент из двух разнородных металлов, то разрушаться будет тот, который в таблице расположен ниже. Так, если в электролит поместить пластинки цинка и железа, то разрушаться будет цинк. Каждый металл будет анодом по отношению к металлу, расположенному выше него в таблице, и катодом — ко всем нижерасположенным. Поэтому нельзя допускать в конструкциях, работающих в коррозионных средах, соединения металлов, разных по активности, например железа с алюминием или медью, меди с алюминием. Возникновению коррозии на металле способствует неоднородность их строения, наличие загрязнений и примесей.
Металлические изделия подвергаются коррозии как в процессе эксплуатации, так и хранения.
 |
По характеру воздействия на металл коррозию можно разделить на сплошную (равномерную), местную и межкристаллитиую.
Сплошная (равномерная) коррозия равномерно распространяется по всей поверхности металла.
Местная коррозия вызывает разрушение отдельных участков поверхности металла в виде язв, пятен и точек. Поэтому ее иногда называют язвенной, пятнистой, точечной. Она возникает обычно в местах дефектов металла: царапин, рисок, забоин, следов обработки и т. д.
Межкристалли тная коррозия развивается (возникает) по границам кристаллов, не вызывая заметных изменений поверхности металла. Этот вид коррозии наиболее опасный. Он приводит к мгновенной поломке деталей при эксплуатации
Интенсивность (скорость) коррозии зависит от химического состава и структуры металла, состояния его поверхности, наличия внутренних и наружных дефектов, окружающей среды (ее состава, температуры, скорости движения) и т. д. Металл с дефектами имеет более высокий электродный потенциал, чем чистый. Дефекты способствуют образованию гальванических микроэлементов и, следовательно, разрушению основного металла. Чем меньше металл имеет дефектов, тем выше его коррозионная стойкость, и наоборот.Химический состав металла значительно влияет на его коррозионную стойкость. При увеличении содержания углерода сопротивляемость металла коррозии уменьшается, и наоборот. Содержание в металлах таких элементов, как хром, никель, титан, медь, повышает их коррозионную стойкость. Ниобий и титан повышают стойкость металлов к межкристаллитной коррозии. Коррозия стали усиливается в кислых растворах и уменьшается в щелочных средах.
Часто одновременно с коррозией металлов происходит эрозия. Эрозией называется механическое разрушение поверхности металла ударами частиц твердых тел, воды, газа, пара, воздуха и т. д. Совместная коррозия и эрозия значительно быстрее разрушают металл.
Около 10 % всех наплавленных металлов, воплощенных в различные изделия, конструкции и машины, ежегодно разрушается от коррозии. Поэтому борьба с коррозией является важнейшей народнохозяйственной задачей. Знание химических свойств металлов позволяет правильно выбрать нужный для изготовления изделий или конструкций, работающих в коррозионных средах.
Коррозия судовых конструкций
Судовые конструкции работают в чрезвычайно неблагоприятных условиях. Детали двигателей внутреннего сгорания и газовых турбин, топки и дымоходы паровых котлов, нагреваемые при обработке судостроительные заготовки подвергаются газовой коррозии, судовые конструкции, соприкасающиеся с нефтью, бензином, керосином, маслами,— химической коррозии, судовые конструкции, находящиеся в воде и влажной атмосфере,— электрохимической коррозии. Многие судовые конструкции (корпус судна, гребные винты, рули, вращающиеся детали турбин и насосов, трубы большинства судовых систем и т. д.) подвергаются также эрозии. В результате потери металла от коррозии в судостроении довольно высоки.
Основной коррозионной средой судовых конструкций является морская вода, в которой содержатся растворы различных солей. Соленость океанов составляет примерно 35 промилле, морей — не более 25, рек и озер — не более 0,3 промилле. Чем выше концентрация солей в воде, тем выше электропроводность и, следовательно, тем выше ее коррозионная активность. Растворенные в морской воде кислород, йод, бром также способствуют ее коррозионной активности.
Наиболее подвержены коррозии в морской воде углеродистая сталь и чугун. Чем больше примесей (серы и фосфора) содержит металл, тем ниже его коррозионная стойкость. Нержавеющие стали и особенно сплавы на основе титана, циркония и тантала устойчивы против коррозии.
Коррозионная стойкость цветных металлов колеблется в широких пределах. Высокую коррозионную стойкость имеет медь и ее сплавы (латунь и бронза). Но простые латуни подвержены в морской воде обесцинкованию. Обесцинкование — это вид избирательной коррозии, при которой цинк растворяется, а медь выделяется на поверхности в виде рыхлых образований.
Алюминий и его сплавы устойчивы против коррозии в пресной воде, а сплавы алюминия с магнием устойчивы и в морской воде, если они имеют дополнительную защиту. Магний и его сплавы мало устойчивы против коррозии в морской воде, а титан и его сплавы — практически абсолютно устойчивы против коррозии, поэтому являются ценным материалом для изготов-ления судовых конструкций.
Увеличение скорости движения воды повышает электрохимическую коррозию, а при определенных условиях вызывает коррозионную эрозию, прежде всего судовых конструкций в кормовой части корпуса судна: гребных винтов, внутренних поверхностей судовых трубопроводов и др.
Коррозионная стойкость судовых конструкций зависит в значительной степени от чистоты их обработки. Бугорчатая поверхность сварных швов, выступающие головки заклепок и других крепежных деталей могут быть причинами интенсивной местной коррозии. Ускоряет коррозию наличие окалины на поверхности судовых конструкций, даже находящейся под слоем краски.
Особенно интенсивно происходит электрохимическая коррозия конструкций, в которых сочетаются различные металлы, например сталь с алюминиевыми или медными сплавами. Однако при постройке судов без таких материалов невозможно обойтись.
Подводная часть судов (обычно до грузовой ватерлинии) во время плавания и особенно стоянки обрастает различными животными или растительными организмами, которые повреждают покрытие корпуса судна, что способствует возникновению местной коррозии. В процессе жизнедеятельности эти организмы выделяют вредные химические соединения: сернистый водород, углекислый газ, различные кислоты и кислород, что также способствует повышению скорости коррозии.
При очистке подводной части крупнотоннажных судов в доках снимают до 200 т продуктов обрастания, которое не только способствует возникновению коррозии, но и снижению скорости движения судов, увеличению расхода топлива, ускорению сроков докования.
studopedia.net
Общие сведения о сплавах
Количество просмотров публикации Общие сведения о сплавах – 1419
Металлы — кристаллические вещества, характеризующиеся высокими электро- и теплопроводностью, ковкостью, способностью хорошо отражать электромагнитные волны и другими специфическими свойствами. Свойства металлов обусловлены их строением: в их кристаллической решетке есть не связанные с атомами электроны, которые могут свободно перемещаться.
В технике обычно применяют не чистые металлы, а сплавы, что связано с трудностью получения чистых веществ, а также с крайне важно стью придания металлам требуемых свойств.
Сплавы — это системы, состоящие из нескольких металлов или металлов и неметаллов. Сплавы обладают всеми характерными свойствами металлов. В строительстве применяют сплавы железа с углеродом (сталь, чугун), меди и олова (бронза) и меди и цинка (латунь) и др.
Размещено на реф.рф
На практике термин ʼʼметаллыʼʼ распространяют и на сплавы, в связи с этим далее он относится и к металлическим сплавам.
Применяемые в строительстве металлы делят на две группы: черные и цветные.
К черным металлам относятся железо и сплавы на его базе (чугун и сталь).
Сталь — сплав железа с углеродом (до 2,14%) и другими элементами. По химическому составу различают стали
углеродистые и легированные, а по назначению — конструкционные, инструментальные и специальные.
Чугун — сплав железа с углеродом (более 2,14%), некоторым количеством марганца (до 2%), кремния (до 5%), а иногда и других элементов. Учитывая зависимость отстроения и состава чугун бывает белый, серый и ковкий.
К цветным металлам относятся все металлы и сплавы на базе алюминия, меди, цинка, титана и др.
Широкое использование металлов в строительстве и других отраслях экономики объясняется сочетанием у них высоких физико-механических свойств с технологичностью.
Металлы обладают высокой прочностью, причем прочность на изгиб и растяжение у них практически такая же, как и на сжатие (у каменных материалов прочность на изгиб и растяжение в 10… 15 раз ниже прочности на сжатие). Так, прочность стали более чем в 10 раз превышает прочность бетона на сжатие и в 100…200 раз прочность на изгиб и растяжение; в связи с этим, несмотря на то, что плотность стали (7850 кг/м) в 3 раза выше плотности конструкционного бетона (2400 + 50 кг/м), металлические конструкции при той же несущей способности значительно легче и компактнее бетонных. Этому способствует также высокий модуль упругости стали (в 10 раз выше, чем у бетона и других каменных материалов). Еще более эффективны конструкции из легких сплавов.
Металлы очень технологичны: во-первых, изделия из них можно получать различными индустриальными методами (прокатом, волочением, штамповкой и т.п.), во-вторых, металлические изделия и конструкции легко соединяются друг с другом с помощью болтов, заклепок и сварки.
При этом с точки зрения строителя металлы имеют и недостатки. Высокая теплопроводность металлов требует устройства тепловой изоляции металлоконструкций зданий. Хотя металлы негорючи, но металлические конструкции зданий крайне важно специально защищать от действия огня. Это объясняется тем, что при нагревании прочность металлов резко снижается, и металлоконструкции теряют устойчивость и деформируются. Большой ущерб экономике наносит коррозия металлов. Металлы широко применяют в других отраслях промышленности, в связи с этим их использование в строительстве должно быть обосновано экономически.
Организация рабочего места слесаря
Рабочим местом принято называть определенный участок производственной площади цеха, мастерской, закрепленный за данным рабочим (или бригадой рабочих), предназначенный для выполнения определенной работы и оснащенный в соответствии с характером этой работы оборудованием, приспособлениями и материалом.
Организацией рабочего места является важнейшее звено организации труда. Правильный выбор и размещение оборудования, инструментов и материалов на рабочем месте создают наиболее благоприятные условия работы.
В целях экономии движения на рабочем месте предметы делят на предметы постоянного и временного пользования, за которым постоянно закреплены места хранения и расположения. На рабочем месте должны находиться только те предметы, которые необходимы для выполнения донного задания. Предметы, которыми рабочие пользуются чаще, кладут ближе на площади. Предметы, которыми рабочие пользуются реже, кладут дальше, но не дальше чем в пределах площади. По возможности избегают такого размещения предметов, которые при выполнении работ поворотов и особенно колебания корпуса, а также перекладывания предметов из одной руки в другую. Приспособления, материалы и готовые детали располагают в специальные ящики (тару), находящиеся на отведенных для них местах. Измерительные инструменты хранят в специальных футлярах или в деревянных коробках. Режущие инструменты (напильники, метчики, сверло, отвертки и многое другое), хранят на деревянных подставках. После окончания работы, использованные инструменты и приспособления очищают от грязи и масла и протирают. Поверхность верстака очищают от стружки и мусора. Рабочие места должны иметь хорошее индивидуальное освещение. Свет должен падать на обрабатываемые предметы, а не на лицо рабочего. Свет должен быть рассеянным и не создавать бликов, мешающих работать.
Слесарный верстак является основным видом оборудования рабочего места для выполнения трудных работ и представляет собой специальный стол, для выполнения слесарных работ. Он должен быть прочным и устойчивым, каркас верстака сварной конструкции из чугунных и стальных труб, стального профиля. Крышку верстаков изготовляют из досок толщиной 50-60 мм. Столешницу покрывают листовым железом толщиной 1-2 мм, линолеумом или фанерой. Кругом окантовывают бортиком, чтобы не скатывались детали. Под столешницей верстака находятся выдвижные ящики, разделённые на ряд ячеек для хранения в определённом порядке инструментов, мелких деталей и документаций. При малом росте рабочего используют специальные регулируемые по высоте подставки под ноги. Для выполнения работ механизированным инструментом к верстаку подводится силовая электрическая линия. Одноместные слесарные верстаки имеют длину 1200-1500 мм, ширину 700-800 мм, высоту 800-900 мм, а многоместные длину 2400-3600 мм или 3000-4500 мм, ширину ту же, что и одноместные верстаки. Когда слесарю приходится перемещаться, он пользуется переносным инструментным ящиком или сумкой.
referatwork.ru
Понятие о сплавах.
Характерной особенностью металлов является их способность образовывать друг с другом или с неметаллами сплавы. Чтобы получить сплав, смесь металлов обычно подвергают плавлению, а затем охлаждают с различной скоростью, которая определяется природой компонентов и изменением характера их взаимодействия в зависимости от температуры. Иногда сплавы получают спеканием тонких порошков металлов, не прибегая к плавлению (порошковая металлургия). Итак сплавы – это продукты химического взаимодействия металлов.
Кристаллическая структура сплавов во многом подобна чистым металлам, которые, взаимодействуя друг с другом при плавлении и последующей кристаллизации, образуют: а) химические соединения, называемые интерметаллидами; б) твердые растворы; в) механическую смесь кристаллов компонентов.
Современная техника использует огромное число сплавов, причем в подавляющем большинстве случаев они состоят не из двух, а из трех, четырех и большего числа металлов. Интересно, что свойства сплавов часто резко отличаются от свойств индивидуальных металлов, которыми они образованы. Так, сплав, содержащий 50% висмута, 25% свинца, 12,5% олова и 12,5% кадмия, плавится всего при 60,5 градусах Цельсия, в то время как компоненты сплава имеют соответственно температуры плавления 271, 327, 232 и 321 градус Цельсия. Твердость оловянной бронзы (90% меди и 10% олова) втрое больше, чем у чистой меди, а коэффициент линейного расширения сплавов железа и никеля в 10 раз меньше, чем у чистых компонентов.
Однако некоторые примеси ухудшают качество металлов и сплавов. Известно, например, что чугун (сплав железа и углерода) не обладает той прочностью и твердостью, которые характерны для стали. Помимо углерода, на свойства стали влияют добавки серы и фосфора, увеличивающие ее хрупкость.
Среди свойств сплавов наиболее важными для практического применения являются жаропрочность, коррозионная стойкость, механическая прочность и др. Для авиации большое значение имеют легкие сплавы на основе магния, титана или алюминия, для металлообрабатывающей промышленности – специальные сплавы, содержащие вольфрам, кобальт, никель. В электронной технике применяют сплавы, основным компонентом которых является медь. Сверхмощные магниты удалось получить, используя продукты взаимодействия кобальта, самария и других редкоземельных элементов, а сверхпроводящие при низких температурах сплавы – на основе интерметаллидов, образуемых ниобием с оловом и др.
Задания для закрепления и проверки знаний Контрольные вопросы:
Как определить степени окисления металлов побочных подгрупп?
Какие степени окисления наиболее характерны для железа?
Назовите формулы оксидов и соответствующих им гидроксидов железа.
Охарактеризуйте кислотно-основные свойства гидроксидов железа (II) и железа
(III)?
Какие степени окисления характерны для хрома? Какие из них наиболее устойчивы?
Назовите формулы оксидов и гидроксидов хрома и охарактеризуйте их кислотно-основные свойства.
Как меняются окислительно-восстановительные свойства соединений хрома с
увеличением степени его окисления?
Напишите формулы хромовой и дихромовой кислот.
Какие степени окисления проявляет марганец в соединениях? Какие из них наиболее устойчивы?
Напишите формулы оксидов и гидроксидов хрома и охарактеризуйте их кислотно-основные свойства и окислительно-восстановительные свойства.
Как меняются окислительно-восстановительные свойства соединений марганца с увеличением степени его окисления?
studfiles.net
ОСНОВНЫЕ СВЕДЕНИЯ О СПЛАВАХ
Чистые металлы характеризуются низким пределом прочности, поэтому в технике применяют главным образом их сплавы. Металлическим сплавом называют сложное вещество, полученное сплавлением (или спеканием) нескольких металлов или металлов с неметаллами. Например, мягкая медь с добавлением олова превращается в более твердую бронзу. При этом улучшаются эксплуатационные и технологические свойства металлического материала.
Для изучения процессов, происходящих в сплавах при их превращениях, а также для описания строения сплавов в металловедении используют понятия: компонент, фаза, система.
Компонентами называют вещества, образующие систему. Чистый металл представляет собой однокомпонентную систему, сплав двух металлов – двухкомпонентную систему и т.д. Компонентами могут быть металлы и неметаллы, а также устойчивые, т.е. не диссоциирующие на составные части в рассматриваемых интервалах температур вещества — химические соединения. Так, для цветных металлических сплавов компонентами могут быть металлы (например, медь с цинком образует латунь), а для черных— металлы с небольшим содержанием неметаллов (железо с углеродом — чугун, сталь).
Фазой называют однородную часть системы, имеющую одинаковый состав, одно и то же агрегатное состояние и отделенную от остальных частей системы поверхностью раздела, при переходе через которую химический состав или структура вещества изменяются скачкообразно.
Совокупность фаз, находящихся в равновесии при определенных внешних условиях (давлении, температуре), называют системой. Например, однородная жидкость (расплавленный металл) является однофазной системой, при кристаллизации чистого металла система состоит из двух фаз: жидкой (расплавленный металл) и твердой (зерна закристаллизовавшегося металла). Другой пример: механическая смесь двух видов кристаллов образует двухфазную систему, так как каждый кристалл отличен по составу или строению и отделен один от другого поверхностью раздела. Сплав называют однородным (гомогенным), если его структура однофазна, и разнородным (гетерогенным), если его структура состоит из нескольких фаз. Под структурой сплава понимают видимое в микроскоп взаимное расположение фаз, их форму и размеры Компоненты в сплавах могут составлять (рис. 13) жидкие и твердые растворы, химические соединения и механические смеси.
Однородные жидкие растворы (рис. 13, а) характерны почти для всех металлов, растворяющихся друг в друге в жидком состоянии в любых соотношениях. В однородном жидком растворе атомы 1 растворимого металла (компонента) А равномерно распределены среди атомов металла В – растворителя. Лишь немногие металлы растворяются в жидком состоянии ограниченно. И только очень немногие металлы из-за большой разницы в размерах своих атомов не растворяются друг в друге в жидком состоянии. В процессе кристаллизации и затвердевания сплавов взаимодействие компонентов может быть различным.
Твердые растворы образуются в результате перехода в твердое состояние однородных жидких растворов. В твердом растворе одно из веществ, входящих в состав сплава, сохраняет присущую ему кристаллическую решетку, а другое в виде отдельных атомов распределяется в кристаллической решетке первого вещества. Твердые растворы бывают двух типов:
твердые растворы замещения и твердые растворы внедрения. Независимо от типа твердые растворы однофазны.
. 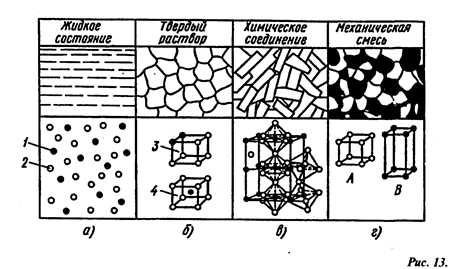 Структура и строение элементарной ячейки различных сплавов из двух металлов А и В: 1- атомы металла А, 2- атомы металла В, 3 – твердый раствор замещения, 4 — твердый раствор внедрения
Структура и строение элементарной ячейки различных сплавов из двух металлов А и В: 1- атомы металла А, 2- атомы металла В, 3 – твердый раствор замещения, 4 — твердый раствор внедрения
В твердых растворах замещения часть атомов в кристаллической решетке одного из компонентов замещена атомами другого(рис. 13, б). Твердые растворы замещения образуются, например, в сплавах железа с хромом, никелем и с другими элементами. Твердые растворы замещения называют неупорядоченными твердыми растворами, поскольку атомы растворимого элемента могут замещать атомы растворителя в любых узлах решетки.
В твердых растворах внедрения атомы растворенного компонента внедряются в межатомное пространство кристаллической решетки другого компонента-растворителя(см. рис. 13, б). Твердые растворы внедрения образуются, например, в сплавах железа с водородом, азотом, бором.
Химические соединения (рис. 13, в) образуются при сплавлении различных металлов или металла с неметаллом. Соотношение чисел атомов элементов химического соединения может быть выражено формулой вида АnBm. Химическое соединение — однородное кристаллическое тело, имеет кристаллическую решетку с упорядоченным расположением атомов, которая отлична от решеток элементов, образующих это соединение. Химические соединения, как и чистые металлы, имеют постоянную температуру плавления и, как правило, обладают большой твердостью и значительной хрупкостью.
Механическая смесь(рис. 13, г) двух компонентов А и В образуется тогда, когда при кристаллизации компоненты сплава не способны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединения. Механическая смесь может состоять из зерен двух насыщенных твердых растворов или зерен твердого раствора и химического соединения. В этом случае сплав состоит из кристаллов А иВ, которые, если они достаточно крупны, отчетливо выявляются на микроструктуре. Рентгенограмма сплава отчетливо показывает наличие двух решеток компонентов А и В.
Температуры, при которых изменяется строение металлов и сплавов, называют критическими точками. При плавлении и затвердевании чистые металлы имеют одну критическую точку, а сплавы — две. В интервале между этими точками в сплавах существуют две фазы — жидкий сплав и кристаллы.
Похожие статьи:
poznayka.org
Помогите найти сообщение по химии на тему ” Сплавы” ? Нужно выбрать самое главное!
Сплавы, макроскопические однородные системы, состоящие из двух или более металлов (реже – металлов и неметаллов) с характерными металлическими свойствами. В более широком смысле сплавы – любые однородные системы, полученные сплавлением металлов, неметаллов, неорганических соединений и т. д. Многие сплавы (например, бронза, сталь, чугун) были известны в глубокой древности и уже тогда имели обширное практическое применение. Техническое значение металлических сплавов объясняется тем, что многие их свойства (прочность, твердость, электрич. сопротивление) гораздо выше, чем у составляющих их чистых металлов. Называют сплавы исходя из названия элемента, содержащегося в них в наибольшем количестве (основной элемент, основа) , например сплавы железа, сплавы алюминия. Элементы, вводимые в сплавы для улучшения их свойств, называют легирующими, а сам процесс -легированием. По характеру металла – основы различают черные сплавы (основа – Fe), цветные сплавы (основа – цветные металлы) , сплавы редких металлов, сплавы радиоактивных металлов. По числу компонентов сплавы делят на двойные, тройные и т. д. ; по структуре – на гомогенные (однородные) и гетерогенные (смеси) , состоящие из нескольких фаз (последние могут быть стабильными и метастабильными) ; по характерным свойствам – на тугоплавкие, легкоплавкие, высокопрочные, жаропрочные, твердые, антифрикционные, коррозионностойкие, сплавы со специальными свойствами и другие. По технологии производства выделяют литейные (для изготовления деталей методом литья) и деформируемые (подвергаемые ковке, штамповке, прокатке, прессованию и другим видам обработки давлением) . Структура и получение. Физико-химической основой создания сплавов являются диаграмма состав-свойства и диаграмма состояния соответствующих систем, позволяющие определять свойства сплавы в условиях их термической обработки. Диаграммы состояния строят на основании экспериментальных данных или расчетным путем с использованием различных термодинамических моделей. В настоящее время в той или иной степени диаграммы состояния известны для большинства имеющих практических значение двойных и тройных систем… <a rel=”nofollow” href=”http://www.chemport.ru/data/chemipedia/article_3531.html” target=”_blank” >Далее… </a> и вот еще есть -> <a rel=”nofollow” href=”http://works.tarefer.ru/94/100194/index.html” target=”_blank” >Реферат: СПЛАВЫ</a> надеюсь самое главное, выберите уже сами )
дохуя писать сука (((
Доброго времени суток!) Качественно и не дорого делают работы на заказ здесь: <a rel=”nofollow” href=”https://vsesdal.com/promo/?ref=35090″ target=”_blank”>VSESDAL</a> Если что то не понравилось, то можно вернуть деньги за работу. Исполнителя выбираешь сам. Делают рефераты, дипломные, контрольные, эссе, курсовые, переводы, практические и многое другое! Пользуюсь уже 3 год! Недорого!!! Удачи!
touch.otvet.mail.ru

