Травление нержавейки соляной кислотой – Травление нержавейки в домашних условиях
alexxlab | 20.09.2020 | 0 | Вопросы и ответы
Обработка нержавейки после сварки: рекомендации
Как ни странно, но и на качественной, хорошей нержавеющей стали со временем могут появиться следы ржавчины. Это происходит, как правило, в так называемой «агрессивной среде», при повышенной влажности и температуре. Чтобы этого не случилось, не следует допускать соприкосновения стали с пылью и стружкой металла.
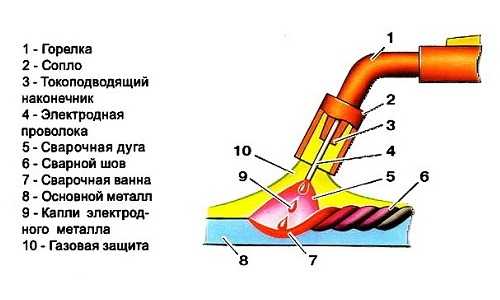
Сварка нержавейки.
При последующей обработке не подвергайте изделие вредному и разрушительному воздействию щелочи и кислот. После сварки на поверхности изделия образуется тонкий оксидный слой. Он ослабляет сопротивление соединения к коррозии. Коррозия разделяется на электрохимическую и химическую.
- Электрохимическая — это развал металла в электролитах.
- Химическая — это разрушение металла от воздействия окружающей среды.
Способы обработки нержавеющей стали после сварки
Для этого вам потребуется специальный защитный костюм и маска. Как правило, при травлении используются серная, соляная, плавиковая или азотная кислоты в виде гелей, паст, аэрозолей, спреев. Для травления швов лучше применять пасты с очень густой консистенцией. Пасту необходимо наносить кистью, очень ровным слоем.
Первый способ — травление кислотами.
- Разъедание окалины при помощи соляной и серной кислоты. Необходимо соблюдать строжайший контроль насыщенности раствора и температуры.
- Промывание водой.
- Погружение в ванну со смесью плавиковой и азотной кислоты.
- Тщательная промывка.
Процесс травления нержавеющей стали кислотами.
В воздухе образуются пары кислот, это требует серьезного подхода к защите кожи и органов дыхания. Данный процесс имеет множество различных вариаций с концентрацией состава, временем и последовательностью действий.
Электролитическое травление является одним из способов кислотного травления. В ванну пропускается электрический ток, либо постоянный, либо переменный, он оказывает механическое воздействие. Вышеописанные способы очень сложны и требуют крупных финансовых вложений.
Второй способ — травление уже готовыми смесями кислот после сварки.
- Сначала производится очистка от всех следов грязи, ржавчины, а также жирных пятен. Состав наносится на полчаса.
- Заключительная обработка пассиватором.
Это легкодоступный метод очистки. Что касается мер предосторожности, то пасту нельзя нагревать, подвергать воздействию прямых солнечных лучей. В помещении должна быть хорошая вентиляция, эти составы обладают едким, неприятным запахом. Если паста попадет на кожу, немедленно промойте это место водой.
Вернуться к оглавлению
Механические способы и термообработка после сварки
Минимальная обработка — это удаление шлака и окалины методом шлифовки шва щеткой из нержавеющей стали. В некоторых случаях этого недостаточно, и необходима дополнительная химическая обработка. Очень распространена шлифовка мелкозернистой наждачной бумагой.
Травление изделия из нержавейки с помощью кислоты.
Механические способы — это обдувание песком, жидко-абразивная и гидропескоструйная очистка. Обязательное условие — минимум содержания железа в песке. После такой очистки идет пассирование поверхности.
Термообработка нержавейки подразделяется на несколько видов: закалка (максимальная температура и быстрое охлаждение), отжиг (нагревание металла и медленное охлаждение), нормализация (похожа на отжиг, разница в том, что охлаждение происходит на свежем воздухе, а не в печи), отпуск (проводится после закалки).
От правильного нагрева заготовки зависит итоговый результат и качество изделия. Под воздействием жара металл меняет свою структуру и свойства. При перегреве приобретает нежелательную крупнозернистую структуру. Следить за температурой нагрева необходимо очень внимательно. Например, пережог является браком, который уже не подлежит исправлению.
Химико-термическая обработка нержавейки — термическая обработка с нанесением различных элементов на поверхность (хром, алюминий, азот и др.)
Вернуться к оглавлению
Особенности пассивации нержавеющей стали
Такой способ очистки поможет устранить все загрязнения с поверхности металла, а также создаст необходимую устойчивость к коррозии, поспособствует улучшению внешнего вида изделия, сохранит от возможного загрязнения в дальнейшем. Пассивация — это защитная пленка, которая образуется на поверхности металла и надежно защищает его от повреждений и разрушения. Пассиватор нужно наносить на полчаса, можно и на влажную поверхность.
Методом распыления средство равномерно распределяется по всей поверхности.
После того как необходимое время выдержано, пассиватор удаляется с изделия. Для этого, как правило, используется водный компрессор.
Вернуться к оглавлению
Полировка сварных швов
Для того чтобы изделие после сварки обрело законченный вид сварочные швы необходимо обработать шлифовальным станком.
После сварки нужно привести изделие в должный, законченный вид, придать ему блеск, лоск и сияние. Благодаря применению новых технологий в полировке время на проведение этой работы значительно сократилось, а качество возросло.
Полировка — это использование специального шлифовального станка. Режим необходимо выбирать тот, который порекомендовал производитель. Особенности полированных труб заключаются в том, что они имеют безупречный внешний вид, отличаются износостойкостью и долговечностью. Полировка может быть ручной, ультразвуковой и машинной. В домашних условиях может подойти обычная наждачная бумага, шлифовальные абразивные материалы, напильники.
Первый шаг — избавиться от грубого шва, сделать поверхность гладкой и однородной. Для выполнения этой задачи вам потребуется доводочный круг. Он с легкостью снимет грубый шов, удалит окалину. Теперь поверхность подготовлена к дальнейшим действиям.
Второй шаг — выведение рисок от первой обработки. Поверхность доводится до состояния, близкого к конечному. Иногда на этом этапе можно остановиться. Поверхность уже сейчас хорошо выглядит.
Третий шаг — финальная полировка. Доведение металла до зеркального блеска. При этом при полировке нержавейки с поверхности удаляются микроскопические дефекты, а при шлифовке — грубые.
Вернуться к оглавлению
Шлифовка: практические рекомендации
Классификация сварных швов по положению в пространстве.
При выполнении такой работы не забудьте хорошо подготовиться. Следует надеть маску во избежание попадания пыли в глаза. Шлифовке подлежат изделия, которые имеют явно заметные дефекты: потертости, царапины и так далее. Вам потребуются шлифовальные головки, которые имеют абразивные ленты.
Для получения желаемого результата шлифуют сталь в несколько заходов. Запомните, что правильно подобранные материалы и инструменты позволят вам снизить время работы и повысить ее качество, это гарантия отличного результата.
Шлифовка готовых изделий выполняется с помощью абразивной шкурки. Этот материал имеет бумажную или тканевую основ с покрытием самой различной зернистости. Мокрая шлифовка делается при помощи водостойких шкурок. Покрытия могут выполняться из стекла, а также кремния. Шлифовка является заключительным этапом процесса обработки нержавейки после сварки. Она равномерно снимает все верхние слои.
Материалы, которые вам потребуются:
- болгарка;
- шлифовальные круги с разной зернистостью;
- столярный клей;
- наждачная бумага;
- полировальная паста.
Для шлифовки сварочных швов на изделиях из нержавейки понадобится болгарка.
Первым делом нужно убрать наплывы металла со сварного шва. Сделать это можно болгаркой. Если поверхность в достаточной степени гладкая и ровная, то можете сразу приступать ко второму этапу. Приготовьте войлочный круг, с помощью обычного шпателя наносите на поверхность обрабатываемого изделия столярный клей. Аккуратно и осторожно пройдитесь по абразивной крошке, которую можно получить из наждачной шкурки.
Затем отшлифуйте поверхность еще три-четыре раза. При этом размер абразива должен уменьшаться. Поверхность нержавейки требуется промывать после каждой шлифовки.
Она должна быть идеальной, абсолютно гладкой и ровной, без шероховатостей. Иначе придется переделывать все заново. На следующем этапе вам понадобится войлочный круг и полировальная паста. Лучше найти алмазную, со степенью зернистости, соответствующей вашему металлу. Это финишная полировка, убирающая видимые риски. Вы увидите, как поверхность преображается и становится более гладкой.
Вернуться к оглавлению
Несколько слов в заключение
Итак, о плюсах стали известно уже очень давно. Материал «нержавейка» плотно вошел в жизнь каждого человека. Ему есть место практически повсюду, даже на современной кухне многие предметы выполнены из качественной нержавеющей стали. Такая популярность обусловлена хорошими характеристиками и свойствами данного чудесного металла.
После должной обработки он выглядит безупречно красиво, в его зеркальной поверхности можно разглядеть собственное отражение. Данный материал является одним из самых прочных, крепких и долговечных. Устойчивость этого материала просто поражает. Но для того чтобы все было именно так, придется немного повозиться.
Обработка стали после сварки — довольно трудоемкая, сложная и кропотливая задача. Она требует настоящего мастерства, профессионализма и абсолютной точности исполнения. Начинающему домашнему мастеру будет непросто освоить эту замысловатую науку, но при правильном и ответственном подходе результат труда вас, несомненно, порадует.
Самое главное, не забывайте об опасности, с которой можете столкнуться при выполнении такой работы, очень важно соблюдать все меры предосторожности. А потом придет необходимый опыт, навыки и сноровка.
moiinstrumenty.ru
Обработка нержавейки после сварки
Нержавеющие стали активно используются в промышленности для изготовления емкостей и трубопроводов под агрессивные жидкости. В быту из этого металла изготавливают кухонные принадлежности и красивые полотенцесушители. Зеркальная поверхность имеет привлекательный вид, а изделие способно служить очень долго. Но чтобы добиться такого эффекта на готовой конструкции требуется правильно обработать сварные швы нержавейки. Если этого не сделать, то места сварки будут иметь желтый и черный цвет, или они могут даже поржаветь. Почему это происходит? Какие существуют механические и химические способы обработки?

Причины обработки
При изготовлении разнообразных конструкций из нержавеющей стали применяются методы сваривания металлов электрической дугой в среде инертных газов. Для этого используют вольфрамовый неплавящийся электрод и подачу чистого аргона для защиты сварочной ванны от взаимодействия с окружающей средой. Создавать шов можно и полуавтоматами, где дуга горит между кончиком проволоки и изделием. Из сопла горелки подается смесь аргона и углекислоты. Проволоку толкает специальный механизм, скорость которого регулируется в зависимости от толщины металла и силы тока.
Хоты швы получаются крепкими и ровными, они имеют непривлекательный вид, и поэтому их необходимо обрабатывать. Само место соединения может быть синевато-зеркального оттенка. Околошовная зона часто желтого цвета. При чешуйчатом рисунке в бороздках могут прослеживаться черные риски. А со временем, такие места даже ржавеют.
Все это происходит из-за перегрева в зоне сварки. Высокие температуры от электрической дуги содействуют выгоранию легирующих элементов и обедняют данный участок. Вследствие чего он меняет цвет и становится более уязвимым для внешнего воздействия. Образовавшаяся на поверхности пленка имеет малую сопротивляемость к агрессивной среде, поэтому, при соприкосновении с рабочими жидкостями на химических предприятиях, становится слабым местом, и покрывается коррозией.
Полотенцесушители иногда ржавеют в местах сварки из-за наличия небольшого электрического напряжения в трубах, которое взаимодействует с материалом изделия, и продолжает ослаблять сварочный шов. Еще такое случается из-за неверного выбора нержавеющей стали под конкретный вид продукции. Например, вместо марки 304, которая богата хромом, производители применяют нержавейку 201, стоящую дешевле, но в чьем составе хром заменен марганцем. Их сложно отличить визуально, но при длительной работе в контакте с жидкостями, это проявится рыжими пятнами. Поэтому правильный выбор марки стали и последующая обработка нержавейки — залог долгого привлекательного вида изделия.
Механическая шлифовка
Хорошие коррозийные свойства нержавеющей стали способствуют ее активному применению в среде, где используются жидкости. Такие изделия служат дольше, чем малоуглеродистая сталь. А блеск и зеркальный вид поверхности позволяют устанавливать конструкции на видных местах, улучшая общий дизайн помещения или фасада. Из нержавейки производят наружные перила и пандус, парковочные стойки, разнообразные полотенцесушители. Несмотря на соприкосновение с водой, и проведение сварочных работ на изделиях, все эти элементы сохраняют красивый вид. Достигается это за счет нескольких видов обработки.
Одним из них является механическая шлифовка, при которой убирается верхний оксидный слой на сварке, являющийся слабым местом конструкции, а также устраняются цветовые переходы и неровности в сварочном соединении. Этот процесс происходит в следующей последовательности:
- При помощи болгарки и толстого шлифовального круга стираются волны металлического шва и его выпуклости, выступающие за общую плоскость поверхности. Так можно быстро сравнять шов, но после болгарки остаются грубые борозды от абразива, и перегретые участки с темными пятнами.
- Чтобы снять эти дефекты более бережно, можно применить лепестковые круги для болгарки. Процесс будет длиться немного дольше, и потратится больше расходных материалов, при крупном объеме работ, но риски останутся мельче.
- Далее используются шлифовальную машину, называемую Rebir. Он имеет прямую форму, электромотор и рукоятку для удержания. На конец надеваются лепестковые круги (КШЛ), но их расположение отличается от кругов на болгарке. Благодаря широкой структуре кусочков наждачной бумаги можно производить больший нажим на обрабатываемое изделие, и захватывать широкую площадь. КШЛ бывают разного калибра по величине применяемого абразива. Для обработки нержавейки после сварки применяют сначала «40-ку», а затем «нулевку». Так устраняются все борозды от предыдущих инструментов. Покрытие становится одноцветным и матовым.
Работы следует проводить в респираторе, поскольку пыль от абразива и частицы снятого металла парят в воздухе. Шлифовщик должен защищать и глаза, для чего надеваются прозрачные очки. Нержавейка нагревается от трения шлифовальными кругами, поэтому на руках рабочего должны быть перчатки для избежания ожогов. В качестве аналога ручного шлифования применяются пескоструйные установки, где под даванием воздуха подаются гранулы песка, счищающие верхний оксид с металла. Это используется на предприятиях с большим оборотом продукции. В домашних условиях устанавливать такое оборудование нецелесообразно.
Полировка
Следующим этапом обработки нержавеющей стали является полировка сварочного участка, и всего изделия, для придания окончательного блеска. Это еще больше зачищает поверхность, делая ее ровной и цельной, что мешает воздействию агрессивных жидкостей извне.
Вначале, сварочные швы обрабатываются диском с вулканитом. Это резиноподобный материал, круг которого насаживается на дрель. Вулканитом возможно придать шву нужную глубину и форму, «запилить» его создав вогнутую структуру. Материал действует мягко на сталь. После этого, на уже отшлифованную поверхность, наносится паста для полировки. Это может иметь алмазный состав. Подойдет обычная паста ГОИ. На дрель одевается войлочный круг и производятся продольные движения по всей поверхности. Чтобы хорошо отполировать места сварки используются маленькие круги, которыми удобно доставать участки в угловых соединениях. Работа ведется до получения зеркальной поверхности и отсутствия матовых пятен.
Кислоты и гели
Чтобы удалить все цветовые переходы после сварки, и устранить оксидный слой содействующий коррозии, используют травление нержавеющей стали. Это относится к кислотному виду обработки материала. Можно использовать серную или соляную кислоту. Подойдут и аналоги, такие как: плавиковая или азотная. Они выпускаются в виде гелей и паст. Существуют и специальные аэрозоли. Процедура происходит так:
- После сварки с поверхности удаляются окалины и мусор. Для этого используется металлическая щетка.
- Изделию дают время остыть до температуры 50 градусов.
- Состав наносится сверху или конструкция погружается в емкость с кислотным средством.
- После 30 минут кислоту смывают большим количеством воды.
Рабочему важно быть в респираторе, поскольку в воздухе будет большое количество паров, опасных для органов дыхания. Защищать требуется и кожу на руках, для чего надеваются резиновые перчатки. При попадании кислоты на открытый участок кожи необходимо быстро и тщательно промыть место большим количеством воды.
Еще одним способом обработки является электрохимическое травление. Для этого используют емкость с кислотой. От источника тока исходит два провода, которые через сопротивление помещаются в жидкость. К «плюсу», который состоит из свинцовой пластины, крепится изделие. «Минус» свинцовой пластины свободно опускается в кислоту. Замыкание напряжения в составе содействует отделению окислов с поверхности нержавейки, но предотвращает перенасыщением водорода. Процедура длится до 8 минут.
Благодаря разнообразным способам обрабатывания нержавеющей стали можно получить красивый вид в месте ведения сварки. Это кропотливый процесс, требующий усердия и настойчивости, но благодаря таким мерам создается зеркальная поверхность изделия, которая не будет ржаветь в будущем из-за слабого оксидного слоя.
Поделись с друзьями
0
0
0
0
svarkalegko.com
Травление металла в домашних условиях — этапы гравировки металла

Травлением называют процесс обработки металла, в результате которого с поверхности удаляется слой определенной толщины под воздействием активных химических веществ (кислот или солей с кислой реакцией), а также постоянного тока в ванне с электролитом.
Травление металла может преследовать различные цели и применяться в промышленности и домашних условиях. Поверхность изделия, подвергаемого травлению, получает целый ряд технологических и декоративных свойств и позволяет рассмотреть его микроструктуру в металлографический микроскоп, удалить окалину и другие неметаллические включения с поверхности, получить необходимый ювелирный орнамент или подготовить к пайке.

К травлению, называемому также электрохимической гравировкой, в домашних условиях или в гараже прибегают чаще всего для получения рельефных изображений на различных предметах с декоративными функциями. Чаще всего ему подвергают стали с высокой твердостью, обработка которых обычным гравировальным инструментом требует больших усилий. Этот процесс не представляет высокой сложности даже при отсутствии художественных навыков, если соблюдать его технологию.
Подготовка поверхности металла
Для того, чтобы процесс травления протекал с высокой скоростью, а толщина удаляемого слоя была одинаковой, с поверхности изделия следует удалить все загрязнения и следы масел. Для этого подойдут обычные моющие и чистящие средства, используемые для мытья посуды, и тёплая вода. После мытья и просушки поверхность следует протереть фиброй, смоченной в растворителе, который, кроме обезжиривания, способствует удалению остатков влаги.
Отдельно стоит сказать о качестве обработки поверхности. Полировка в зеркало впоследствии гарантированно даст хороший контрастный рисунок даже при небольшой глубине травления. Но если ее выполнение невозможно по каким-либо причинам, поверхность можно обработать наждачной бумагой так, чтобы риски от нее шли в одном направлении. Это также даст хороший оптический эффект.
Нанесение рисунка
Для нанесения рисунка на металл можно использовать массу различных способов, работающих по одному и тому же механизму: участки, не подвергающиеся травлению, защищаются от воздействия агрессивной среды или электролита.
Способ №1
Самым доступным способом считается нанесение на защищаемые участки обычного лака для ногтей. Однако, он обладает рядом существенных недостатков:
- Вязкость лака не позволяет сделать линии достаточно тонкими для получения узоров высокой сложности;
- Необходимы хорошие способности в изобразительном искусстве;
- Исправление неточных линий затруднительно.

Способ №2
Для начала необходимо нанести защитный слой на всю поверхность изделия. Для этого можно использовать грунтовки ГФ-021, ХВ-062 или битумный лак, доступные в магазинах автозапчастей и хозтоваров. После полного высыхания покрытия при помощи гелевой ручки или тонкого маркера можно нанести контуры будущего изображения. Для этой задачи можно привлечь опытного художника.
Далее из медной (можно латунной) проволоки или прутка, диаметр которых выбирается исходя из удобства удержания в руке, необходимо сделать иглу с заострённым концом и процарапать грунтовку по линиям изображения до металла. Более твердый материал иглы может повредить полировку поверхности изделия.

Уже на этом этапе можно оценить рельефность будущего орнамента. Для получения участков с разной глубиной травления металла, например, контуров и полутеней, этот процесс можно проводить в два и более цикла.
Важно! В процессе грунтовка не должна откалываться. Перед нанесением рисунка стоит поэкспериментировать и убедиться в том, что она пригодна для работы.
Способ №3
Понадобится лазерный принтер, глянцевая бумага, программа для обработки изображений и утюг. Выбранную картинку необходимо отформатировать (подогнать под размер, сделать зеркальной) и распечатать. Самый доступный источник глянцевой бумаги – женские журналы.
Распечатанное изображение прикладывается к поверхности, накрывается сверху обычным альбомным листом (для защиты утюга) и проглаживается. После остывания бумага смывается под струёй воды, а слой тонера остается на поверхности металла.

Таким способом часто пользуются для травления печатных плат. Основной его недостаток – рисунок наносится только на прямолинейную поверхность.
Важно! Глянец под водой плохо виден. После высыхания необходимо убедиться в том, что он не остался на изделии.
Необходимо позаботиться о защите всех поверхностей изделия. Для этого можно использовать различные вещества. Закрыть тыльную поверхность можно обычным пластилином: он является хорошим диэлектриком.
Способы травления металла
Выбор конкретного способа зависит от многих факторов: химической активности металла, доступности химических реактивов и соображений безопасности.
Химическое травление
Выполняется в емкости с активным веществом. Для углеродистых сталей могут подойти растворы слабых кислот: лимонной, уксусной. Хорошо работает соляная кислота. К травлению в аккумуляторном электролите, азотной кислоте и преобразователе ржавчины следует относиться очень осторожно: в процессе могут выделяться ядовитые газообразные вещества, поэтому с такими реактивами лучше не работать при отсутствии вытяжного шкафа и хорошей вентиляции.
Одним из самых безопасных веществ считается насыщенный раствор хлорного железа. Его можно купить в магазинах, торгующих радиодеталями. Преимуществами раствора являются практически неограниченный срок его службы (при работе со сплавами железа) и окрашивание протравленной поверхности в ровный серый цвет.

Время протекания процесса подбирается экспериментально в зависимости от концентрации используемого реактива и активности металла.
Электрохимическое травление
Многие нержавеющие и кислотостойкие стали, например, 40Х13, 95Х18, 08Х10Н18, 03Х12Н14М2, не реагируют на воздействие кислот, поэтому для их травления используется электрохимический способ.
Для него понадобятся ванна для электролита из пластмассы или стекла, провода, клеммы и источник постоянного тока.В качестве электролита вполне сойдет насыщенный раствор поваренной соли. При выборе емкости для него следует помнить, что процесс может протекать достаточно бурно, этому ее объём должен быть в 2 раза больше, чем у электролита.
В качестве источника тока можно использовать аккумуляторные батареи, но лучше применять зарядное устройство (3 – 10А) с амперметром и возможностью регулировки параметров тока для выбора их оптимального значения. Обрабатываемая деталь при помощи клемм и проводника присоединяется к аноду (плюсовому контакту), в качестве катода можно использовать любую нержавеющую пластину, размещаемую в ванне параллельно к лицевой поверхности детали. После этого прибор включается в сеть.
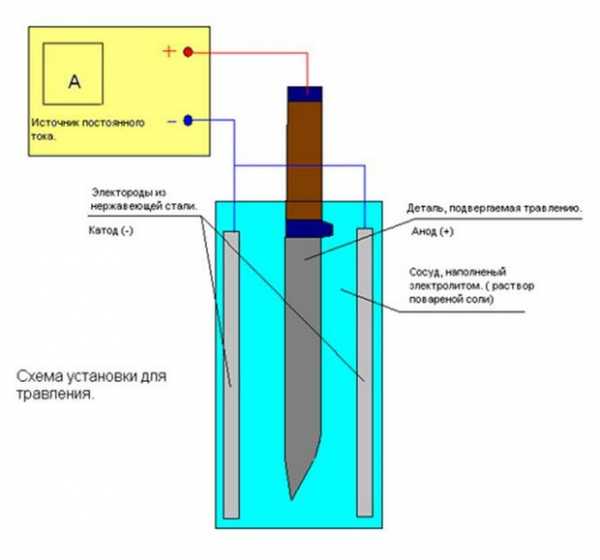
Весь процесс может занимать от двух минут до получаса в зависимости от силы тока и площади рисунка. Глубину травления следует контролировать, периодически вынимая деталь из ванны. При этом не забываем отключать питание.

По окончании процесса защитное покрытие можно удалить подходящим растворителем и оценить результаты работы. Благодаря хорошей адгезии протравленной поверхности возможно создание цветного рисунка.

Для этого вся поверхность изделия задувается из баллона нитроэмалью, а после ее высыхания протирается куском чистой кожи, войлоком или другим безабразивным материалом. С полированной поверхности краска удаляется, оставаясь только во впадинах.
Уважаемые читатели, если у вас остались вопросы, задавайте их, используя форму ниже. Мы будем рады общению с вами 😉
Рекомендуем другие статьи по теме
stroi-specialist.ru
раствор и способ травления нержавеющей стали – патент РФ 2072397
Изобретение относится к области химической обработки металлов, в частности, к растворам и способам травления нержавеющей стали и может быть использовано в металлургической промышленности и других отраслях. Раствор содержит ионы железа (II), ионы железа (III), источник перекиси водорода, не окисляющую железо органическую кислоту для поддержания соотношения ионов железа (II) к ионам железа (III), равного 10/90-40/60. В качестве органической кислоты используют соединение формулы R-(СООН)n, где n = 1-3, R – водород, алкильная или гидроксиалкильная группа с С1-C4, арильная, аралкильная или алкиларильная группа с С6-C14, незамещенная или замещенная С1-C4-алкильной группой или галогеном, например, муравьиную, уксусную, пропионовую, бутановую, молочную, бензойную, фталевую, нафтойную. В качестве источника перекиси водорода используют надкислоту, например, надуксусную, надборную, надбензойную, надсерную, надфосфорную, иодную, надфталевую или кислоту, гомологичную органической кислоте; соль надкислоты, например, пероксикарбонат натрия или пероксиборат магния; органическую перекись, например, перекись мочевины. Способ травления нержавеющей стали включает обработку кислым раствором, содержащим ионы железа (III), ионы железа (III) и источник перекиси водорода, при 10-90oС. 2 с и 7 з.п. ф-лы. Изобретение относится к способу декапирования (очистки поверхности) металлических материалов из стали, особенно из нержавеющей стали. Способ декапирования может быть осуществлен на металлических материалах из стали, особенно из нержавеющей стали, в промышленной среде, перед выпуском с завода, например, для удаления окалины, но также непрофессионалами в металлургии для зачистки элементов из нержавеющей стали. Согласно известному способу операция травления нержавеющих сталей заключается в погружении материалов в травящие ванны, содержащие 6-16% азотной кислоты и фтористоводородную кислоту в соотношении 6-16% HNO3 на литр и 1-5% HF на литр, причем температуре использования ванны составляет величину в интервале 40-60oС. Однако азотная кислота ведет к выделению особенно токсичных паров оксида и диоксида азота, и выделению азотистых соединений, таких, как нитриты и нитраты, в эфлюенты. Если допустимое максимальное предельное содержание нитратов относительно высокое, то эта же норма в отношении нитратов намного более жесткая, т.к. нитриты приводят к образованию вредных нитрозаминов. В патенте Франции А-2 587 369, кроме того, описывается способ декапирования материалов из нержавеющей стали, в котором используют декапирующую ванну, образованную плавиковой кислотой, железом в виде растворенного трехвалентного железа, причем остальное составляет вода. Ванну используют при температуре 15-70oС. Во время операции или операций декапирования поддерживают содержание трехвалентного железа в ванне с помощью инжекции воздуха или за счет циркуляции со свободным воздухом. Такой способ обработки на основе плавиковой кислоты имеет недостаток, связанный с тем, что плавиковая кислота опасна при работе с ней, поэтому она не подходит для любых операций очистки методом пульверизации или опрыскивания металлических элементов таких, как резервуар или цистерна. Также известен из патента Японии А-7547826 способ декапирования металлических материалов из нержавеющей стали, заключающийся в использовании ванны: образованной смесью галогенсодержащих кислот, содержащей в определенном количестве соляную кислоту. В этом способе декапирования основным агентом, вступающим в химическую реакцию, является соляная кислота, которая реагирует с декапируемым материалом с получением хлорида железа (П) и выделением водорода, согласно реакции:2HCl + Fe _ FeCl2+H2
Такой способ, использующий окисляющее воздействие соляной кислоты на декапируемый металл, приводит к большому расходу соляной кислоты, что делает способ дорогостоящим; к сильному выделению водорода, который вызывает опасность взрыва во время использования способа в закрытой среде;к хрупкости обработанной стали из-за промежуточной диффузии атомов водорода в кристаллическую решетку стали. Целью изобретения является снижение загрязнения окружающей среды. Эта цель достигается тем, что декапирование металлических материалов из стали, особенно из нержавеющей стали, может быть осуществлено без необходимости использования корродирующей окисляющей кислоты, такой, как HF или HCl, при условии окисления смесью Fe2+ + Fe3+, в которой поддерживают окислительновосстановительный потенциал между определенными значениями, причем ионы Fe2+ и Fe3+ поддерживаются в водном растворе за счет органической кислоты, не представляющей опасности для человека во время ее использования. Таким образом, предметом изобретения является способ декапирования материалов из стали, особенно из нержавеющей стали, отличающийся тем, что материалы обрабатывают водным раствором, содержащим ионы двухи трехвалентного железа, а также не окисляющую железо органическую кислоту, в количестве, достаточном для поддерживания в растворе ионов Fe2+ и Fe3+, причем ионы двух- и трехвалентного железа находятся в растворе в соотношении Fe2+/Fe3+, равным 10/90-40/60 и тем, что поддерживают соотношение Fe2+/Fe3+ в определенном интервале за счет добавления перекиси водорода. Кислота, содержащаяся в растворе и вступающая во вторичные реакции во время декапирования, приводит к образованию либо легко рециркулируемой в промышленную среду соли, либо нетоксичной соли, что делает способ более простым и безопасным. Органической кислотой является предпочтительно соединение, обозначенное общей формулой: R(COOH)n, в которой R обозначает водород, алкильную группу С1-C4, оксиалкильную группу С1-C4 или арильную группу, аралкильную группу или алкиларильную группу С6-C14, в известных случаях замещенную одним или несколькими заместителями, выбираемыми среди C1-C4-алкильных групп и атомов галогена, и n обозначает 1, 2 или 3. Из предпочтительных органических кислот можно назвать муравьиную, уксусную, пропионовую, бутановую, молочную, бензойную, фталевую и нафтойную кислоту. Предпочтительно, соотношение Fe2+/Fe3+ составляет величину от 10/90 до 40/60, предпочтительно от 10/90 до 25/75, и еще лучше около 20/80. Соотношение и, следовательно, кинетика реакции поддерживаются за счет регенерации иона Fe3+ путем добавления перекиси водорода. Для того, чтобы генерировать перекись водорода в ванне для декапирования, вводят перекись водорода в ванну или добавляют соединение, выбираемое среди надкислоты, соли надкислоты или органической перекиси. Надкислота предпочтительно выбирается среди надборной, надуксусной, надугольной, надбензойной, надсерной, надфосфорной, надфталевой и иодной кислот. Соль надкислоты предпочтительно выбирается среди пероксокарбоната натрия и пероксобората магния, а органической перекисью предпочтительно является пероксид мочевины. Температура осуществления способа предпочтительно составляет 10-90oC. Предметом изобретения является также декапирующее средство для обработки материалов из стали, особенно, из нержавеющей стали, отличающееся тем, что оно включает с одной стороны раствор, содержащий ионы двух- и трехвалентного железа, причем соотношение Fe2+/Fe3+ составляет 10/90-40/60, а также достаточное для поддержания в растворе ионов Fe2+ и Fe3+ количество не окисляющей железо органической кислоты и, с другой стороны, источник перекиси водорода, предназначенный для добавления в раствор для поддержания соотношения Fe2+/Fe3+ в определенном интервале. Органическая кислота и источник перекиси водорода такие, как определенные выше. Декапирующее средство согласно изобретению может транспортироваться без особой упаковки на место его использования, и может быть использовано без особых мер предосторожности везде, включая декапирования закрытых резервуаров, таких, как цистерны, фиксированные или подвижные резервуары, или контейнеры. Способ согласно изобретению используется для декапирования металлических материалов из стали, особенно, из нержавеющей стали и особенно для удаления окалины, полировки и очистки вышеуказанных материалов, причем обработка может быть реализована в ванне, путем опрыскивания или пульверизации. Интерес к органическим кислотам вызван тем, что они разлагаются на СO2, H2O и H2, т.е. на такие остатки от разложения, которые безвредны для среды с точки зрения экологии, когда их выбрасывают в атмосферу, в эфлюенты или даже в море. Другой интерес вызван тем, что органическая среда позволяет образовывать пассивирующую пленку, снижающую коррозию металла. Кроме того, декапирующий раствор, используемый в изобретении, позволяет избегать повторного осаждения некоторых металлов, таких, как медь, никель, хром, олово, цинк в процессе декапирования благодаря повышенному значению окислительно-восстановительного потенциала раствора. В промышленном плане, образование иона Fe3+ контролируется путем измерения окислительно-восстановительного потенциала декапирующей ванны. Окислительно-восстановительный потенциал или РЕДОКС представляет собой разницу потенциалов, измеряемую между некорродирующим электродом (например, из платины) и стандартным электродом (например, Hg (HgCl) или насыщенный каломель), причем эти оба электрода погружены в декапирующий раствор. Измеренная величина позволяет с одной стороны характеризовать окисляющую способность декапирующей ванны и с другой стороны регулировать ванну путем введения перекиси водорода или способного давать H2O2 соединения. В предпочтительном варианте реализации способа изобретения источником перекиси водорода, вводимым в основной декапирующий раствор может быть надкислота, гомологичная кислоте раствора, преимуществом которой является то, что она не изменяет начального состава раствора. Например, пары: органическая кислота (надкислоты, используемые для осуществления способа, могут быть следующими: уксусная кислота (надуксусная кислота; бензойная кислота (надбензойная кислота; фталевая кислота) надфталевая кислота. Другим методом поддержания подобного состава основного раствора является использование в качестве источника перекиси водорода органического окислителя, такого, как надугольная кислота H4(CO3)23H2O2 или пероксид мочевины СО(NH2)2 H2O2, который разлагается на СО2, H2O и N2. Существенным преимуществом способа, в котором используется раствор органической кислоты, является то, что получают оксид трехвалентного железа (Fe2O3), остаток, используемый в области электротехники для изготовления ферритов. Преимущества способа также заключаются в том, что окислитель образуется “in situ” без добавления токсических или загрязняющих веществ, и используемые кислые эфлюенты и растворы безвредны для человека. Так, продукт согласно изобретению, включающий кислый раствор и окисляющую его жидкость или твердое вещество, может быть использован в любых средах, даже в закрытой среде. Способ декапирования, согласно изобретению, следовательно, обладает следующими преимуществами:
он не загрязняет окружающую среду и безопасен во время его использования;
он позволяет использовать кислый раствор без заметной химической модификации во время его осуществления, и
он позволяет рекуперировать и рециркулировать использованные продукты в промышленную среду. Пример 1
Листовую аустенитную дробленую сталь подвергают травлению способом по изобретению в следующих условиях:
концентрация муравьиной кислоты 25% в/в
концентрация Fe общая 21,8 г/л
концентрация ионов Fe2+ 2,5 г/л
концентрация ионов Fe3+ 19,3 г/л
соотношение Fe2+/Fe3+ 0,12
температура 64 2oС
продолжительность 8 мин. потенциал Редокс системы (электрод с насыщенной каломелью) 150-300 мВ
Потенциал Редокс поддерживают в заданном интервале путем введения перекиси водорода. Стальной лист промывают водой при 80oС. Пример 2
Ферритную листовую сталь подвергают травлению в следующих условиях:
концентрация муравьиной кислоты 18% в/в
концентрация Fe общая 15,3 г/л
концентрация ионов Fe2+ 5,7 г/л
концентрация ионов Fe3+ 9,6 г/л
соотношение Fe2+/Fe3+ 0,59
температура 68 2oC
продолжительность 8 мин. потенциал Редокс (электрод с насыщенной каломелью) 150-320 мВ
Потенциал Редокс поддерживают в заданном интервале добавлением перекиси водорода. Сталь промывают водой при 80oС. Пример 3
Дробленую аустенитную сталь подвергают травлению в следующих условиях:
концентрация уксусной кислоты 25% в/в
концентрация Fe общая 21,8 г/л
концентрация ионов Fe2+ 2,5 г/л
концентрация ионов Fe3+ 19,3 г/л
соотношение Fe2+/Fe3+ 0,12
температура 64 2oC
продолжительность 8 мин. потенциал Редокс (электрод с насыщенной каломелью) 150-300 мВ
Потенциал Редокс поддерживают в заданном интервале добавлением перуксусной кислоты. Сталь промывают водой при 80 o С. Пример 4
Ферритную сталь подвергают травлению в следующих условиях:
концентрация щавелевой кислоты 18% в/в
концентрация Fe общая 15,3 г/л
концентрация ионов Fe2+ 5,7 г/л
концентрация ионов Fe3+ 9,6 г/л
соотношение Fe2+/Fe3+ 0,59
температура 68 2oC
продолжительность 8 мин. потенциал Редокс (электрод с насыщенной каломелью) 150-320 мВ
Потенциал Редокс поддерживают в определенном интервале добавлением перекиси мочевины. Сталь промывают водой при 80oС. Пример 5
Дробленую аустенитную сталь подвергают травлению в следующих условиях:
концентрация молочной кислоты 25% в/в
концентрация Fe общая 21,8 г/л
концентрация ионов Fe2+ 2,5 г/л
концентрация ионов Fe3+ 19,3 г/л
соотношение Fe2+/Fe3+ 0,12
температура 64 2oС
продолжительность 8 мин. потенциал Редокс (электрод с насыщенной каломелью) 150-300 мВ
Потенциал Редокс поддерживают в определенном интервале добавлением периодной кислоты. Сталь промывают водой при 80oС. Пример 6
Ферритную сталь подвергают травлению в следующих условиях:
концентрация лимонной кислоты 18% в/в
концентрация Fe общая 15,3 г/л
концентрация ионов Fe2+ 5,7 г/л
концентрация ионов Fe3+ 9,6 г/л
отношение Fe2+/Fe3+ 0,59
температура 68 2oC
продолжительность 8 мин. потенциал Редокс (электрод с насыщенной каломелью) 150-320 мВ
Потенциал Редокс поддерживают в определенном интервале добавлением пероксида периодной кислоты. Сталь промывают водой при 80oС. Пример 7
Ферритную сталь подвергают травлению в следующих условиях:
концентрация бензойной кислоты 18% в/в
концентрация Fe общая 15,5 г/л
концентрация ионов Fe2+ 5,7 г/л
концентрация ионов Fe3+ г/л
отношение Fe2+/Fe3+ 0,59
температура 68 2oС
продолжительность 8 мин. потенциал Редокс (электрод с насыщенной каломелью) 150-320 мВ
Потенциал Редокс поддерживается в определенном интервале добавлением пербензойной кислоты. Сталь промывают водой при 80oС.
ФОРМУЛА ИЗОБРЕТЕНИЯ
1. Раствор для травления нержавеющей стали, содержащий кислоту, ионы железа (II) и ионы железа (III), отличающийся тем, что он дополнительно содержит источник перекиси водорода, а в качестве кислоты не окисляющую железо органическую кислоту для поддержания соотношения ионов железа (II) к ионам железа (III), равного 10:90-40:60. 2. Раствор по п.1, отличающийся тем, что в качестве органической кислоты он содержит соединение формулы R-(COOH)n, где n 1 3, R водород, алкильная или гидроксиалкильная группа с С1-С4, арильная, аралкильная или алкиларильная группа с С6-С14, незамещенная или замещенная С1-С4 -алкильной группой или галогеном. 3. Раствор по п.2, отличающийся тем, что в качестве органической кислоты он содержит муравьиную, уксусную, пропионовую, бутановую, молочную, бензойную, фталевую или нафтойную кислоты. 4. Раствор по п.1, отличающийся тем, что в качестве источника перекиси водорода он содержит надкислоту, ее соль или органическую перекись. 5. Раствор по п.4, отличающийся тем, что в качестве надкислоты он содержит надуксусную, надборную, надбензойную, надсерную, надфосфорную, надиодную или надфталевую кислоты. 6. Раствор по п.4, отличающийся тем, что в качестве надкислоты он содержит надкислоту, гомологичную органической кислоте. 7. Раствор по п.4, отличающийся тем, что в качестве соли надкислоты он содержит пероксикарбонат натрия или пероксиборат магния. 8. Раствор по п.4, отличающийся тем, что в качестве органической перекиси он содержит перекись мочевины. 9. Способ травления нержавеющей стали, включающий обработку кислым раствором, содержащим ионы железа (II) и ионы железа (III), при измерении окислительно-восстановительного потенциала ионов железа (II) и ионов железа (III), отличающийся тем, что обработку ведут раствором по любому из пп.1 8 при температуре 10 90oС.www.freepatent.ru
Вопрос о травлении нержавейки.
vadim79 27-04-2009 10:20уважаемые форумчане, подскажите кто чем может, у вас опыта всяко больше, чем а точнее как протравить нержу(марку не знаю)и в поиск плиз не шлите (весь выкурил)
нужна собсна матовость поверхности(типа как при травлении углеродки или подобие того), из химии есть много ХЖ и соляной кислоты.
заранее спасибо всем неравнодушным
с уважением вадим
Попробуйте в тёплой воде развести ХЖ и добавить соли, процесс лучше непрерывно контролировать.
Graaver 27-04-2009 10:59На сколько мне известно, то в “царской водке”..
vadim79 27-04-2009 13:20похожа неравнодушных более нету….
kU 27-04-2009 13:24ножевые нержавейки (которые не самые коррозионностойкие) обычно получается протравить горячим хлорным железом.
“кастрюльные” царской водкой либо электрохимией либо вообще подумать о пескоструке
пытался в ХЖ холодном-ноль результата(держал минут 15)
SiDiS 27-04-2009 13:34Теплое ХЖ и немного соляной кислоты в нем – именно то, что надо для протравы нержи
napalm 27-04-2009 13:35Травил 420 сталь в ХЖ, при комнатной температуре, протравилось нормально… Слышал такую вещь, что старый раствор ХЖ иногда теряет травящие свойства. Может, просто надо свежий взять?
hunter1957 27-04-2009 16:11Вариант травить соляной кислотой с добавкой перекиси водорода, или горячим ХЖ с добавкой небольшого количества соляной кислоты и перекиси водорода.
AlexAD 27-04-2009 17:02Добрый день, уважаемые Форумчане!
Вчера удалось протравить нож из нержавейки (марку не знаю, нож называется “Путник” с каким-то номером) в ГОРЯЧЕМ хж. Узор проявился интересный, но слабо. Раствор старый, травил где-то часа 2 -2 с половиной постоянно помешивая и наблюдая за процессом. До этого пытался в холодном растворе – ничего путного не вышло. Только грязь развел..
——————
С уважением, AlexAD
quote:
протравить нержу
нагреть электролит (который в автомагазинах для аккумуляторов продают) на водяной бане, и туда эту железяку. только вентиляцию обязательно, а еще лучше на открытом воздухе, испарения зверски едкие.Babaiko 27-04-2009 19:54
Нержа отлично травится составом для зачистки сварных швов на нержавейке.
В состав входят две кислоты правда состав на итальянском доберусь до работы отпишусь.
Результат получается такой

hПросто разбавить водой для ускорения процесса горячей водой.
Можно использовать повторно разогрев в ведре с горячей водой.
нержа травиться царской водкой оч легко причем не нужно конц кислот 5мл азотной кислоты и 10мл соляной все это на пол литра дистилированой воды теплой потемнеет на глазах покрайней мкре 95х18
нержа травиться царской водкой оч легко причем не нужно конц кислот 5мл азотной кислоты и 10мл соляной все это на пол литра дистилированой воды теплой потемнеет на глазах покрайней мере 95х18
Посмотрел Состав содержит Nitric Acid и Hydrochloric acid.
кстати замечательно очищает медь и латунь.
Применение такое. Поскольку состав представляет из себя гель его нужно разводить горячей водой из под крана вполне подойдёт. Где-то 1-4, 1-5. До получения жидкости что-то между молоком и кефиром. Травится минут пять максимум.
В отличии от царской водки при попадании на кожу катастрофического эффекта не вызывает, достаточно просто помыть с мылом.
guns.allzip.org
Травление нержавеющей стали в окислительной электролитической ванне с кислотой
Изобретение относится к электролитическим способам обработки металлов и может быть использовано для травления полосы из нержавеющей стали. Способ включает травление полосы из нержавеющей ферритной стали в ванне смесью, содержащей H2SO4 и избыток по меньшей мере одного окислителя, при этом на сталь подают электрический ток, а указанная смесь не содержит HF. Второй вариант способа включает обработку указанной стали в ванне смесью, содержащей H2SO4 и избыток по меньшей мере одного окислителя, обеспечивающего превращение всего количества сульфата железа (II) в сульфат железа (III) (Fe2(SO4)3), и подачу тока на сталь, причем концентрация H2SO4 составляет от 10 г/л до 200 г/л. Технический результат: снижение общего количества химических реагентов, содержащихся в электролите травления. 2 н. и 23 з.п. ф-лы, 6 табл., 4 пр., 3 ил.
[0001] Настоящая заявка испрашивает приоритет по предварительной заявке на патент США №61/539239, поданной 26 сентября 2011 года под названием «ТРАВЛЕНИЕ НЕРЖАВЕЮЩЕЙ СТАЛИ В ОКИСЛИТЕЛЬНОЙ ЭЛЕКТРОЛИТИЧЕСКОЙ ВАННЕ С КИСЛОТОЙ» («STAINLESS STEEL PICKLING IN AN OXIDIZING, ELECTROLYTIC ACID BATH»), описание которой приводится в настоящем документе посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
[0002] Отжиг полосы металла, такой как полоса нержавеющей стали, может привести к образованию оксидов на поверхности полосы металла. Эти оксиды включают, например, оксиды железа, хрома, никеля и других оксидов родственных металлов, и удаляются или раскисляются перед использованием полосы. Оксиды нержавеющей стали, тем не менее, могут быть устойчивы к традиционным видам обработки кислотой. Кроме того, эти оксиды имеют большое сродство к основному металлу, и поэтому может потребоваться механическое расщепление окалины, такое как дробеструйная обработка, гибка в вальцах или правка полосы стали или обработка в ванне с электролитом и/или расплавом соли перед травлением (удалением оксидов с поверхности полосы) для уменьшения содержания этих оксидов или для придания поверхности из оксидов большей пористости перед травлением полосы.
[0003] Традиционно, оксиды на поверхности нержавеющей стали удаляются, или “стравливаются”, с использованием азотной кислоты в комбинации с плавиковой кислотой; или с использованием комбинации пероксида водорода, серной кислоты, и плавиковой кислоты, как было описано в патенте США 6,645,306 под названием «Схема травления марок нержавеющей стали с помощью перекиси водорода», выданного 11 ноября 2003 года, приведенного здесь в качестве ссылки. Такие кислоты, в особенности плавиковая кислота, являются дорогими. В свою очередь, азотная кислота считается экологически небезопасной.
[0004] Настоящее изобретение описывает способ травления нержавеющей стали путем получения смеси кислоты, такой как серная кислота (H2SO4), избытка пероксида водорода (H2O2), и по меньшей мере одного комплекта электродов, содержащего по меньшей мере один из катода или анода, и подачи тока на полосу металла (такую как нержавеющая полоса стали), проходящую через раствор. Благодаря избыточному содержанию H2O2, весь сульфат железа (II) превращается в сульфат железа (III) (Fe2(SO4)3), который и выступает в роли окислителя. Способ позволяет снизить общее количество используемых химических реагентов для способа травления по сравнению с известными способами травления и, в частности, уменьшить использование азотной кислоты (HNO3) и/или плавиковой кислоты (HF) по сравнению с известными способами травления. Более того, определенные ферритные нержавеющие стали могут подвергаться травлению без использования HF в способе травления, с помощью вышеупомянутой смеси кислоты, такой как серная кислота (H2SO4), избытка пероксида водорода (H2O2), и по меньшей мере комплекта электродов.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0005] В то время как описание завершается формулой изобретения, в которой охарактеризовано настоящее изобретение, полагают, что настоящее изобретение будет более понятным из следующего описания конкретных примеров совместно с прилагаемыми чертежами, в которых одинаковые номера позиций определяют одинаковые элементы и в которых:
[0006] ФИГ. 1 изображает схему установки трех ванн для травления нержавеющей полосы стали, известного из уровня техники;
[0007] ФИГ. 2 изображает схему установки трех ванн для травления стальной полосы, где первая ванна включает комплект электродов катод-анод-катод; и
[0008] ФИГ. 3 изображает схему электролитической установки из одной ванны для травления нержавеющей полосы стали.
[0009] Чертежи не предполагают какого-либо ограничения объема притязаний, и предполагается, что различные варианты реализации изобретения могут быть осуществлены множеством других путей, включая те, что не отражены на чертежах. Прилагаемые чертежи, включенные в описание и являющиеся его частью, иллюстрируют несколько аспектов настоящего изобретения, и вместе с описанием служат для объяснения принципов изобретения; следует понимать, однако, что настоящее описание не ограничено лишь приведенными вариантами установок.
ПОДРОБНОЕ ОПИСАНИЕ
[00010] Следующее описание конкретных примеров не следует рассматривать как ограничение объема настоящего изобретения. Другие примеры, признаки, аспекты, варианты реализации и преимущества нового способа травления станут очевидны для специалистов в данной области техники из нижеследующего описания. Как станет понятно, изобретение допускает и другие различные и очевидные аспекты без отступления от настоящего изобретения. Соответственно, чертежи и описание следует рассматривать как носящие иллюстративный характер и не ограничивающие.
[00011] Настоящее изобретение относится к способу травления металла, и, в частности к травлению горячекатаной, горячекатаной и подвергнутой отжигу, холоднокатаной и подвергнутой отжигу нержавеющей полосы стали, которое осуществляется непрерывно. Способ включает по меньшей мере один резервуар для травления и необязательно может включать по меньшей мере один резервуар для предварительного травления, резервуар для очистки щетками, резервуар для очистки от загрязнений, установку фильтрации или теплообменник. Например, способ может включать серию стадий предварительного травления механическим и/или химическим способом, один или более резервуаров для травления и стадию последующей обработки, заключающуюся в промывке и сушке обработанного материала, при этом все из указанного хорошо известно в данной области техники. Стадия предварительной обработки может включать, например, дробеструйную обработку, выравнивание растяжением, обработку в ванне с расплавом или стадию любой подходящей предварительной обработки, которая будет известна специалисту в данной области техники с учетом сущности изобретения согласно настоящему описанию. На таких стадиях предварительной обработки механически разбивают и/или удаляют окалину и/или химически уменьшают слой пленки на полосе металла, что подготавливает полосу металла для более эффективного травления.
[00012] Природа оксидов и виды обработки для их удаления с основного металла зависят от состава сплава основного металла. Нержавеющая сталь в большом количестве содержит хром (Cr), и при ее нагреве образуются оксиды с большим содержанием Cr. Оксиды с большим содержанием Cr относительно устойчивы/пассивны к воздействию большинства кислот. Как правило, в случае таких оксидов требуется применение комбинации кислот, таких как азотная кислота (HNO3) и фтороводородная кислота (HF) для полного их удаления. Действие HF состоит в проникновении сквозь защитный оксид с большим содержанием хрома с последующим обеспечением возможности растворения основного металла, обедненного хромом, под действием окисляющих кислот, таких как HNO3 и предотвращением преждевременной пассивации основного металла до полного удаления слоя оксидов. HF является дорогим химическим реагентом, а HNO3 стараются не использовать по экологическим соображениям.
[00013] Описанный способ обеспечивает снижение требуемой концентрации кислот, в частности HNO3 и HF, без негативного влияния на производительность благодаря использованию дополнительного устройства для травления из по меньшей мере одной электродной установки, имеющей по меньшей мере один катод и по меньшей мере один анод, избыток окислителя, такого как H2O2. Избыток окислителя создает другой окислитель, и мощность другого окислителя, такого как Fe2(SO4)3, способствует агрессивному воздействию на оксид с большим содержанием и, таким образом освобождает/очищает основной металл от оксида. Данный способ позволяет уменьшить количество химических реагентов, используемых в способе травления в отличие от известных способов травления, и снизить количество азотной кислоты (HNO3) и/или фтороводородной кислоты (HF) по сравнению с известными способами травления.
[00014] В известных способах травления горячекатаный металлический материал, горячекатаный и подвергнутый отжигу металлический материал и/или холоднокатаный и подвергнутый отжигу металлический материал, такой как полоса нержавеющей стали, обрабатываются комбинацией смеси кислот и подвергаются серии операций в травильных резервуарах или ваннах. В одном известном способе, первый резервуар может содержать серную кислоту (H2SO4) и HF. Второй резервуар может содержать HNO3 и HF. Последний резервуар может содержать HNO3 для пассивации поверхности полосы металла, которая потом подвергается промывке и сушке. На ФИГ. 1 показан известный из уровня техники способ травления, включающий три резервуара. Первый резервуар 10 содержит H2SO4 и может дополнительно содержать HF. Второй резервуар 12 содержит HNO3 и HF. Третий резервуар 14 содержит HNO3. Полоса 16 нержавеющей стали непрерывно проходит через каждый из первого резервуара 10, второго резервуара 12 и третьего резервуара 14 в направлении стрелки А.
[00015] Описанный способ позволяет уменьшить или исключить необходимость использования ванны с HNO3 и HF во втором резервуаре для ферритной нержавеющей стали и обеспечивает снижение концентраций, необходимых в такой ванне с HNO3 и HF для травления аустенитных и мартенситных нержавеющих сталей.
[00016] Описанный способ следует за стадией (стадиями) предварительной обработки, описанных выше в п. [00011]. После стадии (стадий) предварительной обработки, полосу металла погружают в первую ванну для электролитического травления, содержащую смесь кислот и окислитель. Кислотная среда может содержать, например, H2SO4, и дополнительно может содержать HF. Определенные марки ферритных нержавеющих сталей не требуют присутствия HF на данной стадии способа. Одним из окислителей может быть, например, сульфат железа (III) (Fe2(SO4)3), который может быть получен путем непрерывной подачи другого окислителя, такого как пероксид водорода (H2O2), и содержание H2O2 можно поддерживать в избытке по отношению к растворенным металлам так, что концентрация H2O2 будет превышать ту, что необходима для превращения всего металла железа (II) до металла железа (III). Например, как только пленка оксидов на полосе стали растворяется в результате способа травления, металл железа (II) растворяется в смеси для травления в виде сульфата железа (II). Сульфат железа (II) замедляет химическую реакцию, связанную со скоростью травления. Сульфат железа (II) способен превращаться в сульфат железа (III) под действием окислителя, такого как H2O2 или HNO3, например. Преимуществом является то, что сульфат железа (III) выступает в качестве катализатора для скорости реакции химического травления. Избыточное количество H2O2 обеспечивает превращение сульфата железа (II) полностью в сульфат железа (III).
[00016] Электроды служат для подачи тока на полосу металла, когда полоса погружена в ванну. Комплект электродов может включать по меньшей мере один из катода или анода, в то время как полоса металла может выступать в роли другого из катода или анода для пропускания тока. Например, в периодическом способе травления, витки стальной проволоки или стальные детали погружают в ванну, содержащую смесь для травления, как отдельные элементы, а не как непрерывную полосу. В таком случае, катод может присутствовать в смеси, а стальная деталь может выполнять роль анода. Дополнительно, или альтернативно, в периодическом способе травления или непрерывном способе, может быть использован комплект электродов из по меньшей мере одного катода и по меньшей мере одного анода, например. Схема электродов может быть представлена в виде схемы комплекта электродов катод-анод-катод, хотя специалисту в данной области техники будет очевидна альтернативная или дополнительная возможность использования другой схемы с учетом сущности изобретения, описанного в настоящем документе. Например, может быть использована одинарная схема электродов, включающая один катод и один анод. При использовании ванны для электролитического травления, описанной выше, контроль отношения ионов трехвалентного железа к ионам двухвалентного железа не требуется.
[00018] Применение такого решения как первая ванна для травления преимущественно удаляет окалину с большинства ферритных нержавеющих сталей и значительно уменьшает слой окалины для аустенитных нержавеющих сталей, для которых затем может потребоваться вторая ванна для травления, содержащая пониженные концентрации кислот, таких как HNO3 и/или HF, для полного удаления каких-либо остаточных слоев оксида/окалины. В то время как описанный способ не требует использования третьей ванны с HNO3 для получения очищенной и травленой полосы металла в случае ферритных нержавеющих сталей, такая третья ванна может применяться для пассивации поверхности полосы металла, подвергнутой обработке.
[00019] На ФИГ. 2 показан пример описанного способа, в котором применяют ванну для электролитического травления после отжига и обработки расплавом соли стальной полосы 16. Первый резервуар включает ванну с H2SO4 и HF, в которой находятся комплекты электродов 22, 24 и 26, расположенных согласно схеме 28, через которую полоса нержавеющей стали 16 проходит непрерывно и в направлении стрелки А. Первый резервуар 20 может содержать, например, от примерно 10 г/л до примерно 200 г/л H2SO4, или от примерно 30 г/л до примерно 120 г/л H2SO4, или от примерно 25 г/л до примерно 35 г/л H2SO4; от примерно 0 г/л до примерно 100 г/л HF, от примерно 0,01 г/л до примерно 100 г/л H2O2, или от примерно 1 г/л до примерно 100 г/л H2O2, или от примерно 5 г/л до примерно 100 г/л H2O2, и по меньшей мере комплект электродов из одного катода и одного анода. Включение HF в электролитическую ванну потребует использование специального совместимого материала, устойчивого к химическому воздействию, но при этом сохраняющего электропроводность. Комплект электродов 22 является катодным комплектом электродов, комплект электродов 24 является анодным комплектом электродов, и комплект электродов 26 является катодным комплектом электродов. Полоса стали 16 проходит через установку 28, и с помощью каждого из электродов 22, 24, 26 на полосу стали 16 подается ток. Например, можно подавать ток в диапазоне от примерно 10 до примерно 200 Кл/дм2 и плотностью тока от примерно 1 до примерно 100 А/дм2 или от примерно 1 до примерно 10 А/дм2. Температуру раствора можно поддерживать от примерно 21°C (70°F) до примерно 82°C (180°F) или от примерно 26°C (80°F) до примерно 24°F (130°F) для контроля распада H2O2 при его введении в систему. Количество растворенных металлов может быть равно либо меньше 80 г/л, в диапазоне от примерно 0 до 80 г/л или в диапазоне от примерно 5 до примерно 40 г/л.
[00020] Второй резервуар 30 может содержать, например, HNO3 для использования при обработке ферритных нержавеющих сталей. Второй резервуар 30 может содержать, например, от примерно 10 г/л до примерно 130 г/л HNO3. Использование второго резервуара для обработки ферритных нержавеющих сталей является необязательным, если нет необходимости осветления и пассивации полосы стали в способе травления, а не при последующей естественной реакции с воздухом, при которой применение второго резервуара будет необходимым. Для марок аустенитных нержавеющих сталей общее количество HNO3 и HF, содержащееся во втором резервуаре, может быть снижено по сравнению с известными способами травления. Например, как будет описано ниже относительно Примера 1, количество HF может быть снижено на примерно 50% по сравнению с известным способом таким образом, что общий расход HNO3 и HF во втором резервуаре снижается. HF может содержаться в концентрации от, например, примерно 1 г/л до примерно 100 г/л или от примерно 5 г/л до примерно 30 г/л или от примерно 5 г/л до примерно 25 г/л. В резервуаре 32 может содержаться HNO3 для применения, например, при обработке ферритной нержавеющей стали, либо может быть использована HF для применения, например, при обработке аустенитной нержавеющей стали. Резервуар 32 может содержать от примерно 10 г/л до примерно 130 г/л HNO3. HF в третьем резервуаре 32 может содержаться в концентрации, например, от примерно 1 г/л до примерно 100 г/л или от примерно 5 г/л до примерно 30 г/л или от примерно 5 г/л до примерно 25 г/л. Или в третьем резервуаре 32 HF может вообще отсутствовать, и количество HNO3 может быть снижено на примерно 20% по сравнению с известным способом таким образом, что общий расход кислот в третьем резервуаре снижен по отношению к способам, известным из уровня техники.
[00021] В способе, описанном в данной заявке, альтернативно может использоваться один резервуар, показанный на ФИГ. 3, как единственный резервуар 40. Такой способ с использованием одного резервуара может применяться, в частности, для полосы стали 16, которая является ферритной нержавеющей сталью. Резервуар 40 включает раствор ванны, описанный выше для первого резервуара 20 на ФИГ. 2. После выхода из резервуара 40, как будет понятно специалисту в данной области техники с учетом излагаемой в настоящем описании сущности изобретения, полоса стали 16 поступает в секцию для обработки, заключающейся в промывке и сушке.
[00022] ПРИМЕРЫ
[00023] В приведенных ниже примерах полярность электролита изменили по меньшей мере один раз способом, известным специалисту в данной области техники с учетом излагаемых в настоящем описании сведений.
[00025] В первом примере, в котором показаны фактические данные, было обнаружено, что в способе электролитического травления (“ЭТ”) в настоящем изобретении общий расход химических соединений ниже, и проводят способ при более низкой температуре, что позволило получить лучшие результаты, по сравнению с известным из уровня техники способом травления (называемый ниже «Базовым способом»)
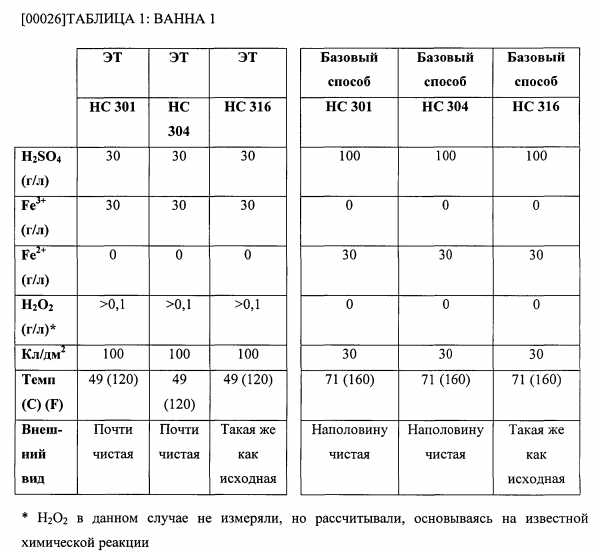
[00027] Нержавеющие стали по классификации ASTM марок 301, 304 и 316, при этом марки и химический состав таких сталей хорошо известны в данной области, испытывали по базовому способу и способу электролитического травления. По результатам базового способа получили остаточное количество ионов Fe2+ 30 г/л, что свидетельствует о том, что H2O2 присутствовал не в избытке (что также соответствует 0 г/л H2O2). По результатам электролитического травления получили количество ионов Fe2+ 0 г/л, что свидетельствует об избыточном количестве H2O2 (что также подтверждается количеством H2O2 5 г/л). По базовому способу для нержавеющей стали марки 301 использовали первую ванну, содержащую 100 г/л H2SO4 и 30 Кл/дм2 при температуре 71°C (160°F), что привело к частичному очищению поверхности стали. Для способа электролитического травления использовали первую ванну, содержащую сниженное количество H2SO4 30 г/л, 30 г/л Fe3+ и характеризующуюся повышенным значением 100 Кл/дм2 при пониженной температуре 49°C (120°F), что позволило получить по существу полностью очищенную поверхность стали. Аналогичные результаты получили для нержавеющей стали марки 304 при тех же значениях. Для нержавеющей стали марки 316 поверхность стали после травления при таких же технологических режимах осталась такой же, как и до проведения обработки, что свидетельствует о неудовлетворительной очистке. Материалы, используемые в данном первом примере, могут быть затем полностью очищены в одной или более последующих ваннах, которые содержали меньшее количество HNO3 и HF, по сравнению с последующими ваннами, используемыми в известных способах травления. “Общее количество HF” описано в следующих примерах и является комбинацией “свободного HF” и части, связанной с растворенными металлами. В зависимости от метода анализа, можно измерить “общее количество HF” и “свободный HF”.
[00028] Для полной очистки материала следующий способ травления проводили при нижеуказанных концентрациях для каждой из ванн 2 и 3. Условия очистки в целом свидетельствовали о приемлемом внешнем виде с точки зрения производства, что будет очевидно специалисту в данной области техники.
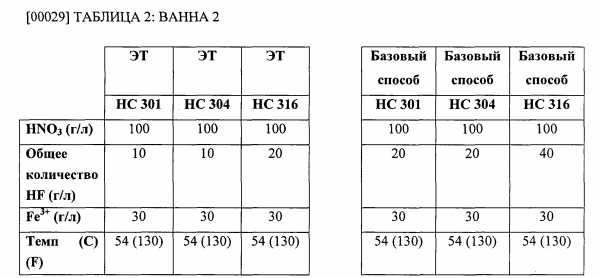
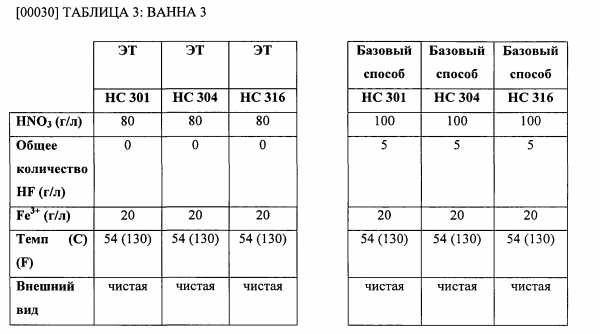
[00031] В способе электролитического травления, раскрытого в первом примере, потребляемое количество HF снизилось более чем в половину, по сравнению с количеством, потребляемым по базовому способу во второй ванне, и HF полностью отсутствовал в смеси в третьей ванне. Концентрацию HNO3 можно было снизить на примерно 20% во второй ванне.
[00032] ПРИМЕР 2
[00033] В следующем втором примере предложен случай, когда для электродов использовали совместимый материал. Во втором примере показан способ электролитического травления с двумя ваннами, при котором вторая ванна содержит только HNO3, что привело к существенному очищению поверхности нержавеющей стали. Поскольку во второй ванне HF не использовали, наблюдалось снижение общего расхода кислот по сравнению с известным способом, в котором во второй ванне применяли обе кислоты – HNO3 и HF. Поскольку травление нержавеющей стали марки 316 является более трудным, добавление HF во вторую ванну является необязательным.
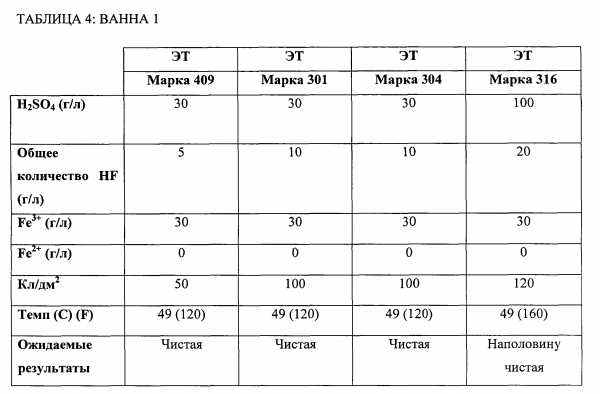
[00035] Для каждой марки стали (301, 304, 316 и 409), используемой для эксперимента, использовали 30 г/л H2SO4 и 30 г/л Fe3+ при температуре раствора 49°C (120°F). Для трудно травящейся нержавеющей стали марки 316 использовали 20 г/л HF и 120 Кл/дм2. Для нержавеющих сталей марок 301 и 304 использовали 10 г/л HF и 100 Кл/дм2. Для нержавеющей стали марки 409, которая значительно легче травится, использовали 5 г/л HF и 50 Кл/дм2. Для существенного и дополнительного полного очищения полос стали по второму примеру, вторая и/или третья ванны могут содержть меньшее по сравнению с известными способами травления количество HF. Например, можно не использовать HF в одной или более последующих ваннах при травлении нержавеющей стали марки 409. Для травления нержавеющей стали марки 301 и 304 можно использовать от примерно 0 г/л до примерно 10 г/л HF, и для нержавеющей стали марки 316 можно использовать от примерно 10 г/л до примерно 30 г/л HF. Эта концентрация могла представлять собой снижение на величину от примерно 20% до примерно 50% для данных марок нержавеющей стали по сравнению с известными способами травления.
[00037] Третий пример, приведенный ниже и основанный на фактических данных, подчеркивает, что способ электролитического травления способствует снижению общего количества потребляемых химических реагентов. Так, в базовом способе использовали сульфат натрия (Na2SO4), и нержавеющую сталь марок 304 и 409 подвергали испытаниям по базовому способу и по способу электролитического травления.
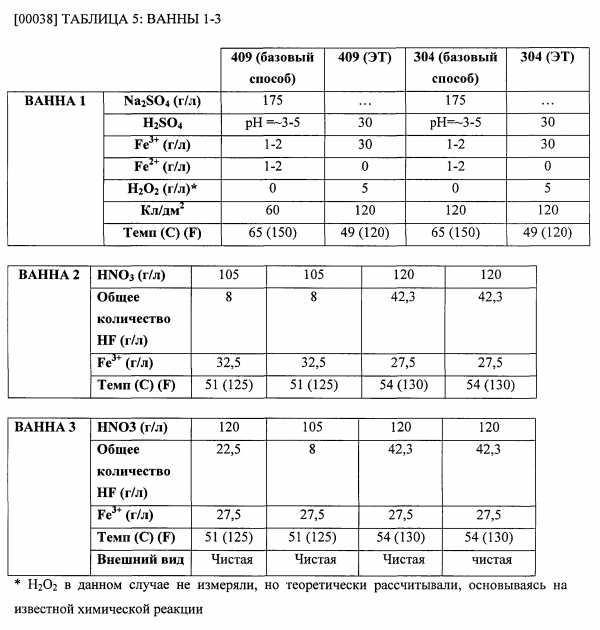
[00039] Для ванны 2 и 3 примечательно, что HNO3 ведет себя как окислитель, что способствует полному превращению ионов двухвалентного железа в ионы трехвалентного железа. Для нержавеющей стали марки 304 по базовому способу в первой ванне использовали 175 г/л Na2SO4, 1-2 г/л Fe3+, 1-2 г/л Fe2+, 0 г/л H2O2, 120 Кл/дм2 и температуру поддерживали 65°C (150°F). Во второй и третьей ваннах в каждой содержалось по 120 г/л HNO3, 42,3 г/л HF, 27,5 г/л Fe3+ при температуре 54°C (130°F). В результате получили визуально чистую поверхность.
[00041] Для нержавеющей стали марки 409 по базовому способу в первой ванне использовали 175 г/л Na2SO4, 1-2 г/л Fe3+, 1-2 г/л Fe2+, 0 г/л H2O2, 60 Кл/дм2 и температуру поддерживали 65°C (150°F). Во второй ванне содержалось 105 г/л HNO3, 8 г/л HF, 32,5 г/л Fe3+ при температуре 51°C (125°F). В третьей ванне содержалось 120 г/л HNO3, 22,5 г/л HF, 27,5 г/л Fe3+ при температуре 51°C (125°F). В результате получили визуально чистую поверхность.
[00041] Для нержавеющей стали марки 409 по базовому способу в первой ванне использовали 175 г/л Na2SO4, 1-2 г/л Fe3+, 1-2 г/л Fe2+, 0 г/л H2O2, 60 Кл/дм2 и температуру поддерживали 65°C (150°F). Во второй ванне содержалось 105 г/л HNO3, 8 г/л HF, 32,5 г/л Fe3+ при температуре раствора 51°C (125°F). В третьей ванне содержалось 120 г/л HNO3, 22,5 г/л HF, 27,5 г/л Fe3+ при температуре раствора 51°C (125°F). В результате получили визуально чистую поверхность.
[00042] Для нержавеющей стали марки 409 по электролитическому способу в первой ванне использовали 30 г/л H2SO4, 30 г/л Fe3+, 0 г/л Fe2+, 5 г/л H2O2 и 60 Кл/дм2 и поддерживали пониженную температуру 51°C (120°F). Во второй ванне содержалось 105 г/л HNO3, 8 г/л HF, 32,5 г/л Fe3+ при температуре 51°C (125°F). В третьей ванне при температуре раствора 51°C (125°F) содержалось 27,5 г/л Fe3+ при пониженном содержании HNO3 105 г/л и 8 г/л HF. В способе электролитического травления было израсходовано меньшее общее количество кислот по сравнению в базовым способом. Например, в третьей ванне в способе электролитического травления концентрация HNO3 была снижена на 15 г/л по сравнению с концентрацией, использованной в третьей ванне в базовом способе, и концентрация HF была снижена на 14,5 г/л по сравнению с концентрацией, использованной в третьей ванне в базовом способе. Это привело к снижению общей концентрации используемых кислот на 29,5 г/л в третьей ванне по электролитическому способу травления, по сравнению с общей концентрацией кислот, использованных в базовом способе. Более того, в результате была получена визуально чистая поверхность.
[00044] Четвертый пример, приведенный ниже, свидетельствует о том, что способ электролитического травления позволяет снизить предполагаемые концентрации используемых химических реагентов. В базовом способе использовали сульфат натрия (Na2SO4), и нержавеющую сталь марок 304 и 409 подвергали испытаниям по базовому способу и по электролитическому способу травления.
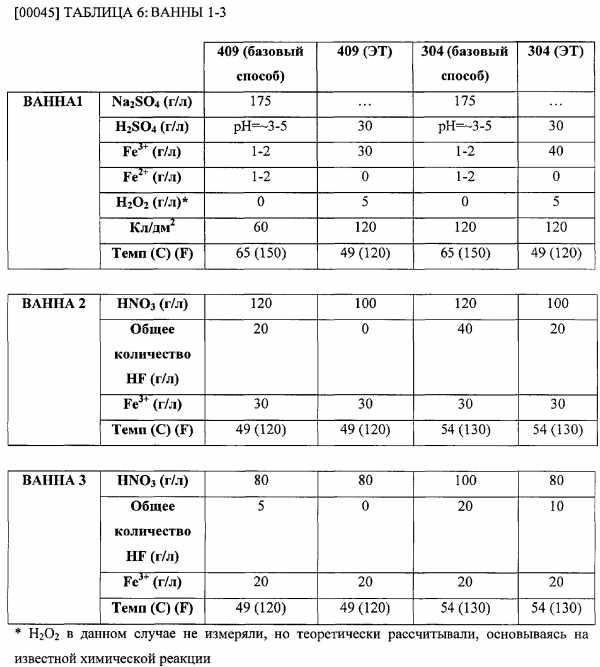
[00046] Для нержавеющей стали марки 304 по базовому способу в первой ванне использовали 175 г/л Na2SO4, 1-2 г/л Fe3+, 1-2 г/л Fe2+, 0 г/л H2O2, 120 Кл/дм2 и температуру поддерживали 65°C (150°F). Во второй ванне содержалось 120 г/л HNO3, 40 г/л HF, 30 г/л Fe3+ при температуре 54°F (130°F) и в третьей ванне содержалось 100 г/л HNO3, 20 г/л HF, 20 г/л Fe3+ при температуре 54°C (130°F). В результате предполагается получение визуально чистой поверхности.
[00047] Для нержавеющей стали марки 304 по электролитическому способу в первой ванне использовали 30 г/л H2SO4, 40 г/л Fe3+, 0 г/л Fe2+, избыток H2O2 (>0,1 г/л), 120 Кл/дм2 и поддерживали пониженную температуру 49°C (120°F). Во второй ванне содержалось 100 г/л HNO3, 20 г/л HF, 30 г/л Fe3+ при температуре 54°C (130°F) и в третьей ванне содержалось 80 г/л HNO3, 10 г/л HF, 20 г/л Fe3+ при температуре 54°C (130°F). В способе электролитического травления количество используемых химических реагентов снизили по сравнению с базовым способом, в том числе каждого из компонентов HNO3 и HF во второй и в третьей ваннах. Например, во второй ванне в способе электролитического травления концентрацию HNO3 снизили на 20 г/л по сравнению с концентрацией, использованной во второй ванне в базовом способе, и концентрация HF была снижена на 10 г/л по сравнению с концентрацией, использованной во второй ванне в базовом способе. Это привело к снижению общей концентрации используемых кислот на 30 г/л во второй ванне по электролитическому способу травления, по сравнению с общей концентрацией кислот, использованных в базовом способе. Кроме того, в третьей ванне в способе электролитического травления концентрация HNO3 снижена на 20 г/л по сравнению с концентрацией, использованной в третьей ванне в базовом способе, и концентрация HF была снижена на 5 г/л по сравнению с концентрацией, использованной в третьей ванне в базовом способе. Это привело к общему снижению концентрации используемых кислот на 25 г/л в третьей ванне по электролитическому способу травления, по сравнению с общей концентрацией кислот, использованных в базовом способе. В результате предполагается получение визуально чистой поверхности.
[00048] Для нержавеющей стали марки 409 по базовому способу в первой ванне использовали 175 г/л Na2SO4, 0 г/л Fe3+, 40 г/л Fe2+, 0 г/л H2O2, 60 Кл/дм2 и поддерживали температуру 65°C (150°F). Во второй ванне содержалось 120 г/л HNO3, 20 г/л HF, 30 г/л Fe3+ при температуре раствора 49°C (120°F). В третьей ванне содержалось 80 г/л HNO3, 5 г/л HF, 20 г/л Fe3+ при температуре 49°C (120°F). В результате предполагается получение визуально чистой поверхности.
[00049] Для нержавеющей стали марки 409 по электролитическому способу в первой ванне использовали 30 г/л H2SO4, 30 г/л Fe3+, 0 г/л Fe2+, 5 г/л H2O2 и 120 Кл/дм2 и поддерживали пониженную температуру 49°C (120°F). Во второй ванне содержалось 100 г/л HNO3, 0 г/л HF, 30 г/л Fe3+ при температуре 49°C (120°F). В третьей ванне при температуре раствора 49°C (120°F) содержалось 20 г/л Fe3+ и пониженные количества HNO3 80 г/л и 0 г/л HF. В способе электролитического травления общее количество используемых химических реагентов снизили по сравнению с базовым способом, в том числе снизили использование каждого из компонентов HNO3 и HF во второй ванне и использование HF в третьей ванне. Например, во второй ванне в способе электролитического травления концентрацию HNO3 снизили на 20 г/л по сравнению с концентрацией, использованной во второй ванне в базовом способе, и концентрация HF была снижена на 20 г/л (до 0 г/л) по сравнению с концентрацией, использованной во второй ванне в базовом способе. Это привело к общему снижению концентрации потребляемых кислот на 40 г/л во второй ванне по электролитическому способу травления, по сравнению с общей концентрацией кислот, использованных в базовом способе. Кроме того, концентрация HF в третьей ванне по электролитическому способу травления была снижена на 5 г/л по сравнению с концентрацией, использованной в третьей ванне в базовом способе. Это привело к общему снижению концентрации потребляемых кислот до 5 г/л в третьей ванне по электролитическому способу травления, по сравнению с общей концентрацией кислот, использованных в базовом способе. В результате предполагается получение визуально чистой поверхности.
[00050] Таким образом, для нержавеющей стали марки 409 при электролитическом способе травления можно исключить использование HF на 100%. Для остальных марок ферритных сталей и низколегированных марок аустенитных сталей, таких как нержавеющая сталь марки 301 и нержавеющая сталь марки 304, концентрацию HF можно снизить на 20% или более по сравнению с базовыми способами. Для аустенитной нержавеющей стали марки 316 существенное снижение концентрации может не наблюдаться. В некоторых случаях концентрацию HNO3 могли снизить для способа электролитического травления на 10-20% по сравнению с базовым способом.
[00051] Основываясь на раскрытых и описанных различных вариантах реализации настоящего изобретения, дополнительные варианты воплощения описанных здесь способов и систем могут быть выполнены специалистом в данной области техники путем внесения подходящих изменений, не отклоняясь при этом от объема настоящего изобретения. Некоторые из таких возможных изменений были упомянуты, и остальные будут очевидны специалистам в данной области техники. Например, рассмотренные выше примеры, варианты реализации, параметры, материалы, размеры, соотношения, стадии и т.п. являются иллюстративными. Таким образом, объем настоящего изобретения следует рассматривать в пределах пунктов формулы изобретения, приведенной ниже, и не ограничивать показанными и описанными в описании и чертежах особенностями структуры и осуществления способов.
1. Способ электролитического травления полосы из нержавеющей ферритной стали, характеризующийся тем, что при травлении указанную полосу подвергают обработке в ванне смесью, находящейся в указанной ванне, при этом указанная смесь содержит H2SO4 и избыток по меньшей мере одного окислителя, при этом на сталь подают электрический ток, а указанная смесь не содержит HF.
2. Способ по п.1, отличающийся тем, что указанный по меньшей мере один окислитель обеспечивает превращение всего количества сульфата железа (II) в сульфат железа (III) (Fe2(SO4)3).
3. Способ по п.2, отличающийся тем, что концентрация Fe2(SO4)3 составляет от 5 г/л до 100 г/л.
4. Способ по п. 1, отличающийся тем, что указанный по меньшей мере один окислитель представляет собой Н2О2.
5. Способ по п. 1, отличающийся тем, что концентрация H2SO4 составляет от 10 г/л до 200 г/л.
6. Способ по п. 1, отличающийся тем, что используют для травления единственную ванну.
7. Способ по п. 1, отличающийся тем, что травление стали проводят непрерывно.
8. Способ по п. 1, отличающийся тем, что стадия подачи тока на сталь включает подачу тока посредством по меньшей мере одного из катода или анода.
9. Способ по п. 8, отличающийся тем, что сталь используют в качестве катода или анода.
10. Способ электролитического травления полосы из нержавеющей стали, включающий обработку указанной стали первой смесью, находящейся в первой ванне, при этом указанная первая смесь содержит H2SO4, избыток по меньшей мере одного окислителя, при этом указанный по меньшей мере один окислитель обеспечивает превращение всего количества сульфата железа (II) в сульфат железа (III) (Fe2(SO4)3), и подачу тока на сталь, причем концентрация H2SO4 составляет от 10 г/л до 200 г/л.
11. Способ по п. 10, отличающийся тем, что концентрация Fe2(SO4)3 составляет от 5 г/л до 100 г/л.
12. Способ по п. 10, отличающийся тем, что указанный по меньшей мере один окислитель представляет собой Н2О2.
13. Способ по п. 10, отличающийся тем, что первая смесь дополнительно содержит HF.
14. Способ по п. 13, отличающийся тем, что концентрация H2SO4 составляет от 25 г/л до 35 г/л и при этом концентрация HF составляет от 0 г/л до 100 г/л.
15. Способ по п. 10, отличающийся тем, что стадия подачи тока на сталь включает подачу тока посредством по меньшей мере одного из катода или анода.
16. Способ по п. 15, отличающийся тем, что сталь используют в качестве катода или анода.
17. Способ по п. 10, дополнительно включающий обработку стали второй смесью, находящейся во второй ванне, причем вторая смесь содержит по меньшей мере один из HNO3 и HF, при этом концентрация HNO3 составляет от 10 г/л до 130 г/л и при этом концентрация HF составляет от 0 г/л до 30 г/л.
18. Способ по п. 17, отличающийся тем, что первая смесь дополнительно содержит HF.
19. Способ по п. 17, отличающийся тем, что нержавеющая сталь представляет собой ферритную нержавеющую сталь, и вторая смесь содержит HNO3.
20. Способ по п. 17, отличающийся тем, что нержавеющая сталь представляет собой аустенитную нержавеющей сталь, и вторая смесь содержит HNO3 и HF, и при этом концентрация HF во второй смеси находится в диапазоне от 5 г/л до 25 г/л.
21. Способ по п. 17, дополнительно включающий обработку стали третьей смесью, находящейся в третьей ванне, причем указанная третья смесь содержит HNO3 и при этом концентрация HNO3 составляет от 10 г/л до 130 г/л.
22. Способ по п. 10, отличающийся тем, что травление стали проводят непрерывно.
23. Способ по п. 10, при котором температура первой смеси находится в диапазоне от 21°C (70°F) до 82°C (180°F) или в диапазоне от 26°C (80°F) до 54°C (130°F).
24. Способ по п. 10, отличающийся тем, что после обработки указанной полосы первой смесью количество полностью растворенных металлов в первой смеси равно или меньше 80 г/л.
25. Способ по п. 10, отличающийся тем, что стадия подачи тока на сталь включает подачу тока посредством электродов, которые включают схему катод-анод-катод и выполнены с возможностью подачи тока в диапазоне от 10 Кл/дм2 до 200 Кл/дм2 с плотностью тока в диапазоне от 1 А/дм2 до 100 А/дм2.
www.findpatent.ru
Травление – сталь – Большая Энциклопедия Нефти и Газа, статья, страница 1
Травление – сталь
Cтраница 1
Травление стали в растворах соляной кислоты происходит преимущественно путем растворения окисной пленки. В растворах серной кислоты растворимость окислов железа мала. Проникая сквозь поры и трещины в окалине к слою вюстита, серная кислота растворяет как его, так и контактирующее с ним металлическое железо. Выделяющийся при этой реакции газообразный водород механически отщепляет наружный слой окалины, удаляя вместе с ним и другие загрязнения случайного характера. [1]
Травление стали в растворах соляной кислоты протекает преимущественно путем растворения окисной пленки. В растворах серной кислоты растворимость окислов железа меньше. Проникая сквозь поры и трещины в окалине к слою вюстита, серная кислота растворяет как его, так и контактирующее с ним металлическое железо. Выделяющийся при этой реакции газообразный водород механически отщепляет наружный слой окалины, удаляя вместе с ним и другие загрязнения случайного характера. [2]
Травление сталей сопровождается выделением на их поверхности шлама – порошкообразного налета карбидов железа, которые не растворяются в соляной и серной кислотах. [3]
Травление сталей азотной кислотой имеет определенную специфику. Азотную кислоту используют для высоколегированных сталей; окалина на поверхности состоит из окиси железа, хрома, никеля и других легирующих элементов. Как правило, водород при травлении не выделяется. В табл. 2 приведены вредные вещества в виде N203, половину из которых составляет окись азота и половину – двуокись азота. [4]
Травление стали в смеси серной и соляной кислот. [5]
Травление стали соляной кислотой получило широкое распространение, когда были разработаны технологические схемы, в которых процессы выделения и разложения хлорида железа были совмещены в одном аппарате. Из зарубежных публикаций известны пять вариантов осуществления этого процесса, отличающихся друг от друга в основном типом реактора для окисления дихлорида железа. Основной принцип процесса для всех вариантов является общим. Он заключается в следующем. Травильный раствор, подлежащий регенерации, распыляется в реакторе при температуре 500 – 800 С. При этих условиях и в присутствии кислорода воздуха происходят испарение воды и разложение дихлорида железа на оксид железа и хлорид водорода. Образующийся оксид железа осаждается или в самом реакторе или в последующем пылеотделителе и извлекается как побочный продукт. Из газовой смеси, содержащей хлорид водорода, пары воды и газообразные продукты горения, хлорид водорода выделяют поглощением водой и в виде соляной кислоты возвращают на травление. Как уже сказано выше, в зависимости от типа реактора для окисления дихлорида железа установки делятся на пять вариантов. [6]
Травление стали ЭИ811 в 10 % HNO3 4 % NaF при 20 и 40 не вызывает образования металлической пленки. [7]
Травление сталей Bethnamel и Zerocarbon осуществляют иногда в 10 – 15-процентном растворе лимонной кислоты при 80 – 90 С в течение 8 – 10 мин. [8]
Травление сталей аустенитного класса типа 12Х18Н10Т и 12Х21Н5Т происходит при температуре 15 – 35 С в растворе, г / л: 220 – 240 HNO3; 20 – 25 NaF; 20 – 35 NaCl. Продолжительность травления 30 – 60 мин, глубина съема основного металла до 2 мкм. [9]
Для травления стали применяется соляная или серная кислота. В соляной кислоте происходит растворение окалины, в то время как серная кислота подтравливает окалину, ослабляя ее адгезию со сталью. Обычные стали, уже обезжиренные, травят в 30 % – ной соляной кислоте при комнатной температуре вплоть до полного удаления окалины и ржавчины. После промывки применяют анодное обезжиривание с целью удаления протравленного шлама при / 5 – МО А / дм2 в течение 1 – 2 мин. После промывки производят – 10-с активацию поверхности в 10 % – ном растворе серной кислоты при комнатной температуре. [10]
После травления стали подвергают пассивированию в 3 – 5 % – ном растворе азотной кислоты при 40 – 50 С в течение 3 – 5 мин. Для пассивирования хромистых сталей применяют тот же раствор, но рекомендуется вводить в него дополнительно 1 – 2 % бихромата натрия. После пассивирования поверхность полуфабрикатов и деталей становится серебристо-матовой, чистой, в результате значительно повышается коррозионная стойкость металла. [11]
После травления стали подвергают пассивированию в 3 – 5 % – ном растворе азотной кислоты при 40 – 50 С в течение 3 – 5 мин. Для пассивирования хромистых сталей применяют тот же раствор, но рекомендуют вводить в него дополнительно 1 – 2 % бихромата натрия. После пассивирования поверхность полуфабрикатов и деталей становится серебристо-матовой, чистой, в результате значительно повышается коррозионная стойкость металла. [12]
Для травления стали в соляной кислоте рекомендуется [ 98, с. [13]
Для травления стали обычных марок употребляется серная кислота, для травления нержавеющей и жароупорных марок сталей – соляная или азотная кислоты. [14]
Механизм травления стали Х18Н10Т в акустическом поле отличается от травления углеродистой стали отсутствием газообразных продуктов реакции и высокой коррозионной стойкостью окисной пленки. Химическое травление стали Х18Н10Т обычно производится в два этапа. На первом этапе осуществляется обработка металла при 400 С в расплаве щелочи, содержащем 65 % NaOH, 30 % NaNO3 и 5 % NaCl. В результате обработки в щелочи окалина становится рыхлой и пористой. На втором этапе производится химическое травление окалины при 20 – 30 С в водных растворах, содержащих азотную и плавиковую кислоты. [15]
Страницы: 1 2 3 4
www.ngpedia.ru

