Какова температура плавления: Какова температура плавления и температура кипения фосфора???
alexxlab | 30.10.2018 | 0 | Разное
таблица по возрастанию в градусах, самая высокая температура плавления
plazmen.ru » Сварка » Какова температура плавления железа
Металлы и сплавы — это незаменимая основа для литейного и ювелирного производства, ковки и многих других сфер. Что бы ни делал человек из металла (какой бы это ни был процесс), для правильной работы ему нужно знать, при какой температуре плавится тот или иной металл. Мы подробно рассмотрим процесс плавления, его отличие от кипения, а также сравним температуры в таблицах.
Процесс плавления металлов.
Что такое температура плавления
Каждый металл имеет неповторимые свойства, и в этот список входит температура плавления. При плавке металл уходит из одного состояния в другое, а именно из твёрдого превращается в жидкое. Чтобы сплавить металл, нужно приблизить к нему тепло и нагреть до необходимой температуры – этот процесс и называется температурой плавления. В момент, когда температура доходит до нужной отметки, он ещё может пребывать в твёрдом состоянии. Если продолжать воздействие – металл или сплав начнет плавиться.
Плавление и кипение – это не одно и то же. Точкой перехода вещества из твердого состояния в жидкое, зачастую называют температуру плавления металла. В расплавленном состоянии у молекул нет определенного расположения, но притяжение сдерживает их рядом, в жидком виде кристаллическое тело оставляет объем, но форма теряется.
При кипении объем теряется, молекулы между собой очень слабо взаимодействуют, движутся хаотично в разных направлениях, совершают отрыв от поверхности. Температура кипения – это процесс, при котором давление металлического пара приравнивается к давлению внешней среды.
Для того, чтобы упростить разницу между критическими точками нагрева мы подготовили для вас простую таблицу:
| Свойство | Температура плавки | Температура кипения |
|---|---|---|
| Физическое состояние | Сплав переходит в расплав, разрушается кристаллическая структура, проходит зернистость | Переходит в состояние газа, некоторые молекулы могут улетать за пределы расплава |
| Фазовый переход | Равновесие между твердым состоянием и жидким | Равновесие давления между парами металла и воздухом |
| Влияние внешнего давления | Нет изменений | Изменения есть, температура уменьшается при разряжении |
При какой температуре плавится
Металлические элементы, какими бы они ни были — плавятся почти один в один. Этот процесс происходит при нагреве. Оно может быть, как внешнее, так и внутреннее. Первое проходит в печи, а для второго используют резистивный нагрев, пропуская электричество либо индукционный нагрев. Воздействие выходит практически схожее. При нагреве, увеличивается амплитуда колебаний молекул. Образуются структурные дефекты решётки, которые сопровождаются обрывом межатомных связей. Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
Этот процесс происходит при нагреве. Оно может быть, как внешнее, так и внутреннее. Первое проходит в печи, а для второго используют резистивный нагрев, пропуская электричество либо индукционный нагрев. Воздействие выходит практически схожее. При нагреве, увеличивается амплитуда колебаний молекул. Образуются структурные дефекты решётки, которые сопровождаются обрывом межатомных связей. Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
У разных веществ разные температуры плавления. Теоретически, металлы делят на:
- Легкоплавкие – достаточно температуры до 600 градусов Цельсия, для получения жидкого вещества.
- Среднеплавкие – необходима температура от 600 до 1600 ⁰С.
- Тугоплавкие – это металлы, для плавления которых требуется температура выше 1600 ⁰С.
Плавление железа
Температура плавления железа достаточно высока. Для технически чистого элемента требуется температура +1539 °C. В этом веществе имеется примесь — сера, а извлечь ее допустимо лишь в жидком виде.
Без примесей чистый материал можно получить при электролизе солей металла.
Плавление чугуна
Чугун – это лучший металл для плавки. Высокий показатель жидкотекучести и низкий показатель усадки дают возможность эффективнее пользоваться им при литье. Далее рассмотрим показатели температуры кипения чугуна в градусах Цельсия:
- Серый — температурный режим может достигать отметки 1260 градусов. При заливке в формы температура может подниматься до 1400.
- Белый — температура достигает отметки 1350 градусов. В формы заливается при показателе 1450.
Важно! Показатели плавления такого металла, как чугун – на 400 градусов ниже, по сравнению со сталью. Это значительно снижает затраты энергии при обработке.
Плавление стали
Плавления стали при температуре 1400 °C
Сталь — это сплав железа с примесью углерода. Её главная польза — прочность, поскольку это вещество способно на протяжении длительного времени сохранять свой объем и форму. Связано это с тем, что частицы находятся в положении равновесия. Таким образом силы притяжения и отталкивания между частицами равны.
Связано это с тем, что частицы находятся в положении равновесия. Таким образом силы притяжения и отталкивания между частицами равны.
Справка! Сталь плавится при 1400 градусах по Цельсию.
Плавление алюминия и меди
Температура плавления алюминия равна 660 градусам, это означает то, что расплавить его можно в домашних условиях.
Чистой меди – 1083 градусов, а для медных сплавов составляет от 930 до 1140 градусов.
От чего зависит температура плавления
Для разных веществ температура, при которой полностью перестраивается структура до жидкого состояния – разная. Если взять во внимание металлы и сплавы, то стоит подметить такие моменты:
- В чистом виде не часто можно встретить металлы. Температура напрямую зависит от его состава. В качестве примера укажем олово, к которому могут добавлять другие вещества (например, серебро). Примеси позволяют делать материал более либо менее устойчивым к нагреву.
- Бывают сплавы, которые благодаря своему химическому составу могут переходить в жидкое состояние при температуре свыше ста пятидесяти градусов. Также бывают сплавы, которые могут «держаться» при нагреве до трех тысяч градусов и выше. С учетом того, что при изменении кристаллической решетки меняются физические и механические качества, а условия эксплуатации могут определяться температурой нагрева. Стоит отметить, что точка плавления металла — важное свойство вещества. Пример этому – авиационное оборудование.
Термообработка, в большинстве случаев, почти не изменяет устойчивость к нагреву. Единственно верным способом увеличения устойчивости к нагреванию можно назвать внесение изменений в химический состав, для этого и проводят легирование стали.
Таблица температур плавления
Узнать какая нужна температура для плавления металлов, поможет таблица по возрастанию температурных показателей.
| Элемент или соединение | Необходимый температурный режим |
|---|---|
| Литий | +18°С |
| Калий | +63,6°С |
| Индий | +156,6°С |
| Олово | +232°С |
| Таллий | +304°С |
| Кадмий | +321°С |
| Свинец | +327°С |
| Цинк | +420°С |
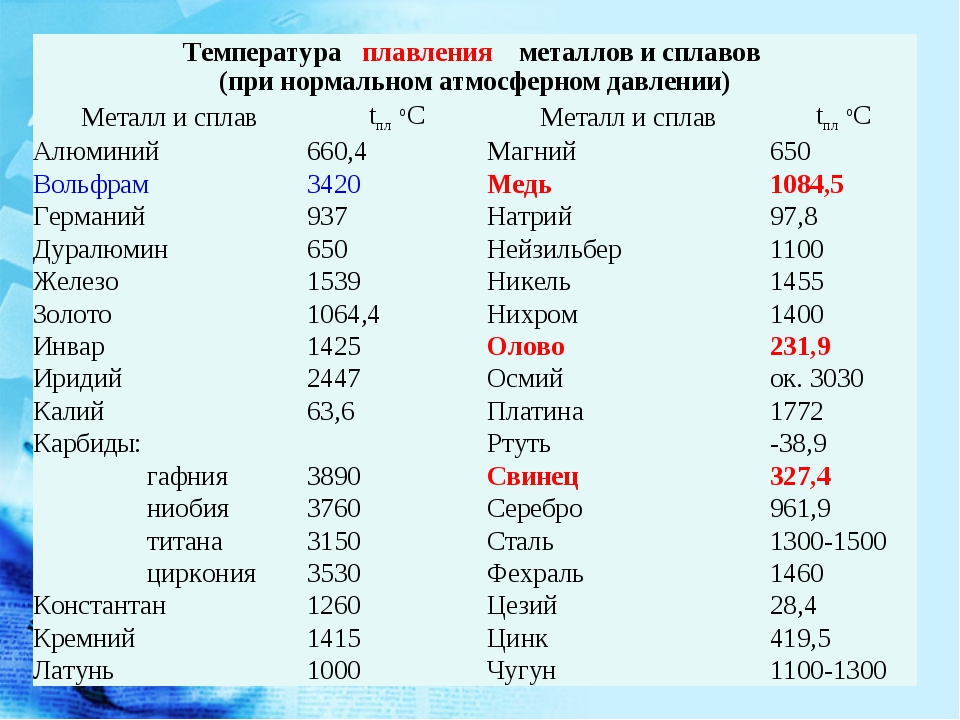
Таблица плавления среднеплавких металлов и сплавов.
| Элемент либо сплав | Температурный режим |
|---|---|
| Магний | +650°С |
| Алюминий | +660°С |
| Барий | +727°С |
| Серебро | +960°С |
| Золото | +1063°С |
| Марганец | +1246°С |
| Медь | +1083°С |
| Никель | +1455°С |
| Кобальт | +1495°С |
| Железо | +1539°С |
| Дюрали | +650°С |
| Латуни | +950…1050°С |
| Чугун | +1100…1300°С |
| Углеродистые стали | +1300…1500°С |
| Нихром | +1400°С |
Таблица плавления тугоплавких металлов и сплавов.
| Наименование элемента | Температурный режим |
|---|---|
| Титан | +1680°С |
| Платина | +1769,3°С |
| Хром | +1907°С |
| Цирконий | +1855°С |
| Ванадий | +1910°С |
| Иридий | +2447°С |
| Молибден | +2623°С |
| Тантал | +3017°С |
| Вольфрам | +3420°С |
У какого металла самая высокая температура плавления
Вольфрам – самый тугоплавкий металл, 3422 °C (6170 °F).
Твердый, тугоплавкий, достаточно тяжелый материал светло-серого цвета, который имеет металлический блеск. Механической обработке поддается с трудом. При комнатной температуре достаточно хрупок и ломается. Ломкость металла связана с загрязнением примесями углерода и кислорода.
Примечание! Технически, чистый металл при температуре выше четырехсот градусов по Цельсию становится очень пластичным. Демонстрирует химическую инертность, неохотно вступает в реакции с другими элементами. В природе встречается в виде таких сложных минералов, как: гюбнерит, шеелит, ферберит и вольфрамит.
Вольфрам можно получить из руды, благодаря сложным химическим переработкам, в качестве порошка. Используя прессование и спекание, из него создают детали обычной формы и бруски.
Вольфрам — крайне стойкий элемент к любым температурным воздействиям. По этой причине размягчить вольфрам не могли более сотни лет. Не существовало такой печи, которая смогла бы нагреться до нескольких тысяч градусов по Цельсию. Ученым удалось доказать, что это самый тугоплавкий металл. Хотя бытует мнение, что сиборгий, по некоторым теоретическим данным, имеет большую тугоплавкость, но это лишь предположение, поскольку он является радиоактивным элементом и у него небольшой срок существования.
Температура плавления меди – при какой температуре плавится медь
Благодаря тому, что температура плавления меди достаточно невысокая, этот металл стал одним из первых, которые древние люди начали использовать для изготовления различных инструментов, посуды, украшений и оружия. Самородки меди или медную руду можно было расплавить на костре, что, собственно, и делали наши далекие предки.
Этап плавления меди
Несмотря на активное применение человечеством с древних времен, медь не является самым распространенным природным металлом. В этом отношении она значительно уступает остальным элементам и занимает в их ряду только 23-е место.
Как плавили медь наши предки
Благодаря невысокой температуре плавления меди, составляющей 1083 градуса Цельсия, наши далекие предки не только успешно получали из руды чистый металл, но и изготавливали различные сплавы на его основе. Чтобы получить такие сплавы, медь нагревали и доводили до жидкого расплавленного состояния. Затем в такой расплав просто добавляли олово или выполняли его восстановление на поверхности расплавленной меди, для чего использовалась оловосодержащая руда (касситерит). По такой технологии получали бронзу – сплав, обладающий высокой прочностью, который использовали для изготовления оружия.
Какие процессы происходят при плавлении меди
Что характерно, температуры плавления меди и сплавов, полученных на ее основе, отличаются. При добавлении в медь олова, имеющего меньшую температуру плавления, получают бронзу с температурой плавления 930–1140 градусов Цельсия. А сплав меди с цинком (латунь) плавится при 900–10500 Цельсия.
Во всех металлах в процессе плавления происходят одинаковые процессы. При получении достаточного количества теплоты при нагревании кристаллическая решетка металла начинает разрушаться. В тот момент, когда он переходит в расплавленное состояние, его температура не повышается, хотя процесс передачи ему теплоты при помощи нагрева не прекращается. Температура металла начинает вновь повышаться только тогда, когда он весь перейдет в расплавленное состояние.
Диаграмма состояния системы хром-медь
При охлаждении происходит противоположный процесс: сначала температура резко снижается, затем на некоторое время останавливается на постоянной отметке. После того, как весь металл перейдет в твердую фазу, температура снова начинает снижаться до полного его остывания.
Как плавление, так и обратная кристаллизация меди, связаны с параметром удельной теплоты. Данный параметр характеризует удельное количество теплоты, которая требуется для того, чтобы перевести металл из твердого состояния в жидкое. При кристаллизации металла такой параметр характеризует количество теплоты, которое он отдает при остывании.
Более подробно узнать о плавлении меди помогает фазовая диаграмма, показывающая зависимость состояния металла от температуры. Такие диаграммы, которые можно составить для любых металлов, помогают изучать их свойства, определять температуры, при которых они кардинально меняют свои свойства и текущее состояние.
Кроме температуры плавления, у меди есть и температура кипения, при которой расплавленный металл начинает выделять пузырьки, наполненные газом. На самом деле никакого кипения меди не происходит, просто этот процесс внешне очень его напоминает. Довести до такого состояния ее можно, если нагреть до температуры 2560 градусов.
Довести до такого состояния ее можно, если нагреть до температуры 2560 градусов.
Как понятно из всего вышесказанного, именно невысокую температуру плавления меди можно назвать одной из основных причин того, что сегодня мы можем использовать этот металл, обладающий многими уникальными характеристиками.
Какова температура плавления меди и сплавов?
Сфера применения меди очень широка. Поэтому многие задаются вопросами: как правильно плавить медь и какова температура ее плавления? У меди температура плавки довольно низкая,это же касается и ее сплавов, однако условия варьируются в зависимости от количества примесей.
Медь и ее использование
По предположениям ученых, первобытные предки современного человека находили самородки меди, которые иногда были огромных размеров. На латинице имеет название Cuprum. Древние греки занимались ее добычей на Кипре – отсюда такое имя.
Стоит отметить, что экологи обеспокоены последствиями добычи металла. При открытом способе добычи карьер превращается в источник токсичных веществ. Самое токсичное озеро в мире — Беркли Пит (штат Монтана, США) — зародилось из кратера медного рудника.
Ввиду того, что температура плавления довольно невысокая (1083 °С), медную руду или же самородки не составляло трудности расплавить прямо на костре. Эта легкость плавления позволяла повсеместно использовать данный металл, чтобы изготовлять предметы быта, орудия труда, оружие, украшения.
Инструменты, изготовленные из этого металла и его сплавов, не создают искр. Этим обуславливается их широкое применение в тех сферах, где существуют повышенные требования к безопасности (на огнеопасных и взрывоопасных производствах).
Еще издавна люди применяли медь регулярно, сфера ее использования была довольно обширна, однако Cuprum занимает всего лишь двадцать третье место среди прочих химических компонентов по количеству нахождения под землей. Наиболее часто можно встретить ее природе в виде различных соединений, компонентов сульфидных руд. Самые популярные – это медный блеск, медный колчедан. Есть несколько методик добывания чистого металла из руды.
Наиболее часто можно встретить ее природе в виде различных соединений, компонентов сульфидных руд. Самые популярные – это медный блеск, медный колчедан. Есть несколько методик добывания чистого металла из руды.
Как плавили медь раньше
Выше мы уже писали следующую информацию: Cuprum легко плавится, так как температура для плавки низкая. Данный факт давал возможность обработки металла еще на этапах зарождения цивилизации. Стоит сказать: мы в долгу у древнейших металлургов. Они нашли способы добывания, плавления как чистого металла, так и сплавов.
Плавлением называют процесс перехода из твердого состояния в жидкость. Это делали методом простого нагрева, что удавалось благодаря низкой температуре плавления. Далее добавляли олово. Таким образом получалась бронза. Медь уступала бронзе по своей прочности, именно поэтому из сплава делали оружие.
к меню ↑Медь, её сплавы
к меню ↑ МедьМедь, употребляемая сегодня промышленностью, не представляет собой чистый металл Cuprum. Состав содержит огромное количество других компонентов: железо, никель, сурьма, мышьяк. Качество, соответственно и марка, определяется процентным соотношением примесей (их содержание до 1%). Этот металл является чистым с технической точки зрения. Очень важные качества этого металла — высокие показатели электропроводности, теплопроводности. Этим обуславливается невысокая температура для плавки. Температура плавления меди — 1084°С.
Сам по себе – это достаточно гибкий пластичный металл, поэтому его очень широко используют в различных технических отраслях, промышленности. Как расплавить медь? Идеальный метод плавления красной меди — ацетилено-кислородным пламенем, еще угольной дугой или контактной сваркой.
к меню ↑ ЛатуньЛатунь – смесь меди с цинком, процентное соотношение может доходить до равноценного: 50 на 50. Температурные условие для плавки латуни: плавится при 800-950 градусах Цельсия, температура плавления изменяется от процентного соотношения двух металлов. Закономерность такова: чем меньше цинка, тем ниже температура плавления.
Закономерность такова: чем меньше цинка, тем ниже температура плавления.
Какова сфера использования данного сплава? Его часто используют как литейный материал, а также листовой, сортовой металл.
Помимо цинка в различных марках можно увидеть содержание алюминия, свинца, олова, марганца, железа. Содержание прочих компонентов будет оказывать влияние на процесс плавки.
Латунь хорошо сваривать ацетилено-кислородным пламенем. Остальные виды не так предпочтительны, так как цинк интенсивно будет испаряться.
к меню ↑ БронзаСплав Cuprum и Stannum (олово) называют бронзой. Встречаются также безоловянные — в них нет олова. Например, с некоторым процентом алюминия или железа и марганца.
Сфера применения бронзы не так широка. Чаще всего ее используют как литейный материал в производстве подшипников, работающих на трение, также иногда для изготовления украшений, предметов интерьера.
Что же касается плавки, то температура зависит от наличия, количества и состава примесей. В общем, чаще всего температура такова: оловянистые виды бронзы — 900—950°, безоловянистые с наличием алюминия и прочих элементов — 950—1080°С. Их можно сваривать ацетилено-кислородным пламенем, также возможно электродуговой сваркой.
▷ Какова температура плавления алюминия? 🥇 cultmir.ru
Алюминий – это металл, который находится во втором ряду, а группа 13 – в таблице Менделеева. Это третий самый распространенный элемент после кислорода и кремния, который можно найти в земной коре. Алюминий встречается в природе в соединениях, но никогда не в виде чистого металла. Процесс извлечения алюминия из его соединений сложный и довольно сложный. Алюминий является полезным и распространенным металлом, который известен своим легким весом, пластичностью и устойчивостью к коррозии. Алюминий легче утилизировать, чем очищать от руд. Это также достаточно безопасно, когда он вступает в контакт с кожей и используется вокруг пищи.
Это также достаточно безопасно, когда он вступает в контакт с кожей и используется вокруг пищи.
Какова температура плавления алюминия?
Точка плавления вещества определяется как температура, при которой вещество изменяется от твердого до жидкого состояния, но при определенном атмосферном давлении. Именно в точке плавления жидкое и твердое состояния вещества находятся в равновесии. Однако температура плавления вещества в основном зависит от давления; он часто специфичен при стандартном давлении в стандартных материалах. Точка плавления вещества также называется ликвидусом, температурой сжижения или солидусом. Температура плавления алюминия составляет 659 градусов по Цельсию или 1218 по Фаренгейту.
Какова цель определения температуры плавления вещества?
Температура плавления вещества является существенным физическим свойством. Основная цель определения температур кипения и плавления веществ во время лабораторного эксперимента состоит в том, чтобы использовать результаты, чтобы помочь идентифицировать примеси в этих веществах или неизвестных веществах. Точку плавления неизвестного твердого вещества можно использовать для его идентификации, сравнивая его с множеством других потенциальных твердых веществ и их температур плавления, таким образом, подбирая соответствие для идентификации твердого тела. Кроме того, цель определения температуры плавления вещества состоит в том, чтобы использовать диапазон его температур плавления, чтобы помочь определить его общую чистоту. В связи с этим, чем больше диапазон плавления вещества, тем менее чистым является вещество, в то время как чем больше диапазон температур плавления уменьшается, тем чище вещество.
Факторы, влияющие на температуру плавления веществ
Температура плавления вещества варьируется от одного вещества к другому. Например, в то время как кислород тает при температуре 218 градусов по Цельсию, лед тает при температуре 0 градусов по Цельсию, а алюминий – 219 градусов по Цельсию. Поэтому определенные вещи влияют на температуры плавления разных веществ. Факторы, влияющие на температуру плавления веществ, включают межмолекулярные силы, изменения температуры плавления ионных связей, форму молекул и размер молекул. Чистое соединение, которое является кристаллическим, обычно имеет более точную температуру плавления, поэтому полностью плавится в небольшом диапазоне температур, не превышающем 0,5-1 градуса Цельсия. Если такое вещество содержит даже малейшее количество примесей, в точках замерзания обычно образуется углубление, показывающее увеличение ширины диапазона температур плавления. Если диапазон температур плавления превышает пять градусов, то это означает, что вещество является нечистым ,
Поэтому определенные вещи влияют на температуры плавления разных веществ. Факторы, влияющие на температуру плавления веществ, включают межмолекулярные силы, изменения температуры плавления ионных связей, форму молекул и размер молекул. Чистое соединение, которое является кристаллическим, обычно имеет более точную температуру плавления, поэтому полностью плавится в небольшом диапазоне температур, не превышающем 0,5-1 градуса Цельсия. Если такое вещество содержит даже малейшее количество примесей, в точках замерзания обычно образуется углубление, показывающее увеличение ширины диапазона температур плавления. Если диапазон температур плавления превышает пять градусов, то это означает, что вещество является нечистым ,
Использование алюминия
Алюминий – один из самых полезных металлов в мире. В чистом виде алюминий в основном используется в электронной промышленности для изготовления жестких дисков, проводниковых дорожек на кремниевых чипах и конденсаторной фольги. Когда металл легируется другими металлами, такими как кремний, цинк, медь и магний, он становится еще прочнее. Еще одним важным применением алюминия является производство банок для напитков и фольги, используемой для защиты продуктов питания и различных кухонных принадлежностей.
Какова температура плавления железа
Железо – первый по значимости и распространенности конструкционный материал. Известен он с глубокой древности, а свойства его таковы, что когда железо научились выплавлять в значимом количестве, металл вытеснил все остальные сплавы. Наступил век железа и, судя по области его применения, время это закончится нескоро. Данная статья расскажет вам, какова удельная плотность железа, какая у него температура плавления в чистом виде.
Состав и структура железа
Железо – типичный металл, причем химически активный. Вещество вступает в реакцию при нормальной температуре, а нагрев или повышение влажности значительно увеличивают его реакционноспособность. Железо корродирует на воздухе, горит в атмосфере чистого кислорода, а в виде мелкой пыли способно воспламениться и на воздухе.
Железо корродирует на воздухе, горит в атмосфере чистого кислорода, а в виде мелкой пыли способно воспламениться и на воздухе.
Чистому железу присуща ковкость, однако в таком виде металл встречается очень редко. На деле под железом подразумевают сплав с небольшими долями примесей – до 0,8%, которому присущи мягкость и ковкость чистого вещества. Значение для народного хозяйства имеет сплавы с углеродом – сталь, чугун, нержавеющая сталь.
Железу присущ полиморфизм: выделяют целых 4 модификации, отличающиеся структурой и параметрами решетки:
- α-Fe – существует от нуля до +769 С. Имеет объемно-центрированную кубическую решетку и является ферромагнетиком, то есть, сохраняет намагниченность в отсутствие внешнего магнитного поля. +769 С – точки Кюри для металла;
- от +769 до +917 С появляется β-Fe. От α-фазы она отличается лишь параметрами решетки. Практически все физические свойства при этом сохраняются за исключением магнитных: железо становится парамагнетиком, то есть, способность намагничиваться оно утрачивает и втягивается в магнитное поле. Металловедение β-фазу как отдельную модификацию не рассматривает. Поскольку переход не влияет на значимые физические характеристики;
- в диапазоне от 917 до 1394 С существует γ-модификация, которой присуща гранецентрированная кубическая решетка;
- при температуре выше +1394 С появляется δ-фаза, для которой характерна объемно-центрированная кубическая решетка.
Температура фазовых переходов заметно изменяется при легировании тем же углеродом. Собственно, сама способность железа образовать столько модификаций служит основой обработки стали в разных температурных режимах. Без таких переходов металл не получил бы столь широкого распространения.
Теперь настал черед свойств металла железа.
О структуре железа рассказывает этот видеосюжет:
Железо – достаточно легкий, умеренно тугоплавкий металл, серебристо-серого цвета. Легко реагирует с разбавленными кислотами и поэтому считается элементом средней активности. На воздухе – сухом, металл постепенно покрывается пленкой оксида, которая препятствует дальнейшей реакции.
Легко реагирует с разбавленными кислотами и поэтому считается элементом средней активности. На воздухе – сухом, металл постепенно покрывается пленкой оксида, которая препятствует дальнейшей реакции.
Но при самой небольшой влажности вместо пленки появляется ржавчина – рыхлая и неоднородная по составу. Ржавчина дальнейшей коррозии железа не препятствует. Однако физические свойства металла, а, главное, его сплавов с углеродом таковы, что, несмотря на низкую коррозийную стойкость, использование железа более чем оправдано.
Далее вы узнаете, чему равна плотность железа (в кг на м3) в сравнении, например, с медью или алюминием.
Масса и плотность
Молекулярная масса железа составляет 55,8, что указывает на относительную легкость вещества. А какая же у железа плотность? Такой показатель определяется фазовой модификацией:
- α-Fe – 7,87 г/куб. см при 20 С, и 7,67 г/куб. см при 600 С;
- γ-фаза отличается еще более низкой плотностью – 7,59 г/куб см при 1000С;
- плотность δ-фазы составляет 7,409 г/куб см.
С повышением температуры плотность железа закономерно падает.
А теперь давайте узнаем, какова температура плавления железа по Цельсию, сравнивая ее, например, с медью или чугуном.
Температурный диапазон
Металл относится к умеренно тугоплавким, что означает сравнительно невысокую температуру изменения агрегатного состояния:
Благодаря тому, что температура плавления меди достаточно невысокая, этот металл стал одним из первых, которые древние люди начали использовать для изготовления различных инструментов, посуды, украшений и оружия. Самородки меди или медную руду можно было расплавить на костре, что, собственно, и делали наши далекие предки.
Несмотря на активное применение человечеством с древних времен, медь не является самым распространенным природным металлом. В этом отношении она значительно уступает остальным элементам и занимает в их ряду только 23-е место.
Как плавили медь наши предки
Благодаря невысокой температуре , составляющей 1083 градуса Цельсия, наши далекие предки не только успешно получали из руды чистый металл, но и изготавливали различные сплавы на его основе. Чтобы получить такие сплавы, медь нагревали и доводили до жидкого расплавленного состояния. Затем в такой расплав просто добавляли олово или выполняли его восстановление на поверхности расплавленной меди, для чего использовалась оловосодержащая руда (касситерит). По такой технологии получали бронзу – сплав, обладающий высокой прочностью, который использовали для изготовления оружия.
Чтобы получить такие сплавы, медь нагревали и доводили до жидкого расплавленного состояния. Затем в такой расплав просто добавляли олово или выполняли его восстановление на поверхности расплавленной меди, для чего использовалась оловосодержащая руда (касситерит). По такой технологии получали бронзу – сплав, обладающий высокой прочностью, который использовали для изготовления оружия.
Какие процессы происходят при плавлении меди
Что характерно, температуры плавления меди и сплавов, полученных на ее основе, отличаются. При , имеющего меньшую температуру плавления, получают бронзу с температурой плавления 930–1140 градусов Цельсия. А сплав меди с цинком (латунь) плавится при 900–10500 Цельсия.
Во всех металлах в процессе плавления происходят одинаковые процессы. При получении достаточного количества теплоты при нагревании кристаллическая решетка металла начинает разрушаться. В тот момент, когда он переходит в расплавленное состояние, его температура не повышается, хотя процесс передачи ему теплоты при помощи нагрева не прекращается. Температура металла начинает вновь повышаться только тогда, когда он весь перейдет в расплавленное состояние.
При охлаждении происходит противоположный процесс: сначала температура резко снижается, затем на некоторое время останавливается на постоянной отметке. После того, как весь металл перейдет в твердую фазу, температура снова начинает снижаться до полного его остывания.
Как плавление, так и обратная кристаллизация меди, связаны с параметром удельной теплоты. Данный параметр характеризует удельное количество теплоты, которая требуется для того, чтобы перевести металл из твердого состояния в жидкое. При кристаллизации металла такой параметр характеризует количество теплоты, которое он отдает при остывании.
Более подробно узнать о плавлении меди помогает фазовая диаграмма, показывающая зависимость состояния металла от температуры. Такие диаграммы, которые можно составить для любых металлов, помогают изучать их свойства, определять температуры, при которых они кардинально меняют свои свойства и текущее состояние.
Кроме температуры плавления, у меди есть и температура кипения, при которой расплавленный металл начинает выделять пузырьки, наполненные газом. На самом деле никакого кипения меди не происходит, просто этот процесс внешне очень его напоминает. Довести до такого состояния ее можно, если нагреть до температуры 2560 градусов.
Как понятно из всего вышесказанного, именно невысокую температуру плавления меди можно назвать одной из основных причин того, что сегодня мы можем использовать этот металл, обладающий многими уникальными характеристиками.
Сегодня медь является одним из самых востребованных металлов. Высокий спрос объясняется отличительными характеристиками, присущими этому металлу. Медь проводит электроток лучше любых других металлов, кроме серебра, благодаря этому ее используют в производстве кабелей и электропроводов. Температура плавления меди не высокая, металл пластичный и легко поддается обработке, благодаря этому качеству стало возможным ее применение в строительстве в качестве водопроводных тр. Этот металл имеет высокое сопротивление к внешним раздражающим факторам, поэтому долговечен и может быть использован несколько раз, после переплавки. Это качество меди высоко ценят экологи, поскольку при повторной обработке металла тратится значительно меньшее количество энергии, чем при добыче и обработки руды, к тому же сохраняются земные недра. Добыча медной руды не проходит бесследно, на месте отработанных рудников появляются токсичные озера, наиболее известное во всем мире такое озеро – Беркли-Пит в штате Монтана в США.
Необходимая температура для плавления меди
Медь не является легкоплавким металлом
Люди нашли применение меди еще в древние времена, тогда ее добывали в виде самородков. Ввиду низкой температуры, необходимой для осуществления процесса плавления ее стали широко применять для изготовления орудий труда и охоты, самородки можно плавить на костре. В наши дни технология получения металла мало чем отличается от придуманной в древние времена, совершенствуются лишь печи, увеличена скорость обжига и объемы обработки. Здесь возникает уместный вопрос — какая температура плавления меди? Ответ на него можно найти в любом учебнике по физике и химии – медь начинает плавиться при температуре нагрева до 1083 о С.
Здесь возникает уместный вопрос — какая температура плавления меди? Ответ на него можно найти в любом учебнике по физике и химии – медь начинает плавиться при температуре нагрева до 1083 о С.
Кипение меди уменьшает ее прочность
В процессе термического воздействия на металл происходит разрушение его кристаллической решетки, это достигается при определенной температуре, которая в течение некоторого времени остается постоянной. В этот момент и происходит плавка металла. Когда процесс разрушения кристаллов полностью завершен, температура металла снова начинает подниматься, и он переходит в жидкую форму и начинает кипеть. Температура плавления меди значительно ниже, чем та, при которой металл кипит. Процесс кипения начинается с появлением пузырьков, по аналогии с водой. На этом этапе любой металл, в том числе и медь, начинает терять свои характеристики, в основном это отражается на прочности и упругости. Температура кипения меди составляет 2560 о С. Во время остывания металла происходит похожая картина, как и при нагреве – сначала температура опускается до определенного градуса, в этот момент происходит затвердевание, которое длится некоторое время, затем продолжается остывание до обычного состояния.
Любой нагрев меди влечет за собой изменение ее характеристик, наиболее значимой является величина ее удельного сопротивления. Медь является проводником электрического тока, при этом металл оказывает сопротивление движению носителям заряда. Отношение площади сечения проводника к оказываемому движению и называется удельным сопротивлением.
Так вот, эта величина для чистой меди составляет 0,0172 ОМ мм 2 /м при 20 о С. Этот показатель может измениться после термической обработки, а также вследствие добавления в состав различных примесей и добавок. Здесь наблюдается обратная зависимость сопротивления меди от температуры – чем выше была температура обработки металла, тем ниже будет ее сопротивление электрическому току. Для обеспечения наилучших электролитических характеристик медной проволоки, ее обрабатывают при 500 о С.
Во время термической обработки можно не только придавать металлу нужную форму и размер, но и создавать различные сплавы. Самыми распространёнными медными сплавами является бронза и латунь. Бронза получается путем смешивания меди с оловом, а латунь – с цинком. Добавление алюминия и стали увеличивает прочность материала, а добавление никеля повышает антикоррозийные свойства. Но стоит заметить, что любая примесь снижает главное свойство – электропроводность, поэтому для изготовления жил электрокабеля используют чистый состав металла.
Отжиг меди
Под отжигом меди следует понимать процесс ее нагрева с целью дальнейшей обработки и приданию необходимых форм изделию. В ходе отжига металл становится более пластичным и мягким, поддающимся различным трансформациям. При отжиге меди температура достигает 550 о С, она приобретает темно-красный оттенок. После нагрева желательно быстро производить ковку и оправлять изделие на охлаждение.
Если подвергать материал медленному, естественному охлаждению, то возможно образование наклепа, поэтому чаще применяют мгновенное охлаждение путем помещения заготовки в холодную воду. Если превысить допустимую величину нагрева, металл может стать более хрупким и ломким.
Во время отжига осуществляется процесс рекристаллизации меди, в ходе которого образуются новые зерна или кристаллы металла, которые не искажены решеткой и отделены от прежних зерен угловыми границами. Новые зерна по размеру могут сильно отличаться от предшественников, при их образовании высвобождается большое количество энергии, увеличивается плотность и появляется наклеп. Рекристаллизация осуществляется только после деформации изделия, и только после достижения ее определенного уровня. Для меди критический уровень деформации составляет 5%, если он не достигнут процесс формирования новых зерен не начнется. Температура рекристаллизации меди составляет 270 о С. Следует отметить, что при этой температуре процесс роста кристаллов только начинается, но он достаточно медленный, поэтому для достижения необходимого результата медь необходимо нагреть до 500 о С, тогда времени для остывания хватит для завершения процесса рекристаллизации.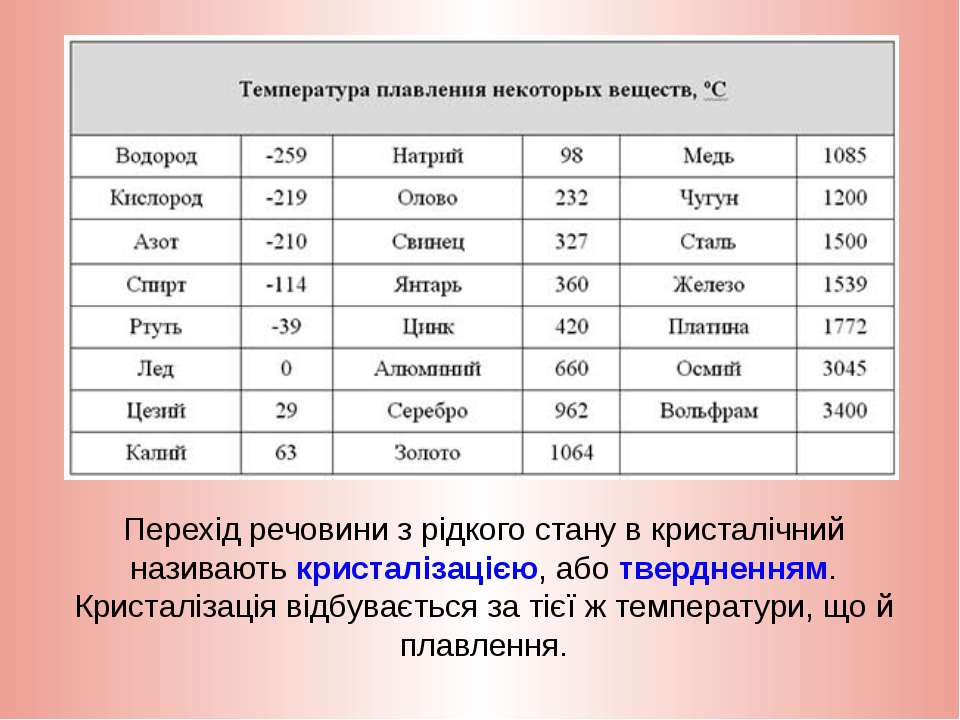
Видео: Плавление меди в микроволновке
Предметы из меди, а также различные изделия, в состав которых она входит, получили широкое распространение в бытовых условиях. Поэтому многие задаются вполне стандартным вопросом: «Как расплавить медь самостоятельно?»
Имея представление о такой технологии, люди научились изготавливать разные предметы из чистого металла, а также получаемых из него сплавов – бронзы и латуни.
Плавление – это процесс, характеризующий постепенный переход металла из стандартного твердого состояния в жидкую консистенцию. Каждому металлическому соединению или металлу в чистом виде свойственная своя температура, под воздействием которой он начинает плавиться.
Немаловажным фактором в данном случае является то, какие примеси входят в состав расплавляемого соединения.
Так, медь начинает плавиться при температуре 1083 градусов по Цельсию. Если к ней добавить олово, то температура плавления снизится и составит примерно 930-1140 градусов по Цельсию.
В данном случае такое колебание обусловлено количеством олова, входящего в сплав. Соединение из меди и цинка плавится при еще более низкой температуре – 900-1050 градусов. Нагревание любых металлов связано с постепенным разрушением решетки, образованной из множества кристаллов.
С нагреванием температура плавления поднимается до максимально необходимой отметки, затем ее рост останавливается и сохраняется на достигнутом уровне до того момента, пока не расплавится весь металл, после чего начинает снижаться.
Остывание – обратный процесс изменения температуры. По мере охлаждения она падает и «замирает» на определенном уровне до тех пор, пока металл полностью не затвердеет.
Медь, разогретая до максимально возможной отметки, закипает при температуре, достигшей отметки в 2560 градусов. По внешнему виду ее кипение схоже с кипением любых жидких веществ, на поверхности которых по мере нагревания появляются пузырьки, и выделяется газ. Так, из меди в процессе кипения выходит углерод, образовавшийся в результате окисления и ее тесного контакта с воздухом.
Технология плавления меди получила широкое применение с древних времен, когда люди с помощью костра расплавляли металл для изготовления стрел, наконечников и другого оружия, и предметов быта.
Плавка меди в домашних условиях также возможна. Для этого понадобятся:
- Тигель, где будет плавиться медь, и щипцы, необходимые для того, чтобы извлечь тигель из печи или снять его с огня.
- Древесный уголь.
- Муфельная печь (лучше, если в ней будет регулироваться температура нагрева).
- Горн.
- Обычный пылесос.
- Форма, в которую выливается расплавленная жидкость.
- Крюк, изготовленный из стальной проволоки.
- Газовая горелка, если нет муфельной печи.
Алгоритм плавления включает несколько поэтапных шагов:
- Металл измельчить и пересыпать в тигель . Причем чем более мелкие фрагменты будут, тем скорее он достигнет расплавленного состояния. Тигель поставить в печь, раскаленную до максимально высокой температуры, необходимой для начала процесса плавления (здесь кстати придется регулятор температур). Во многих муфельных печах на двери вырезано окошко. Через него можно безопасно осуществлять наблюдение за процессом.
- По достижении медью жидкого окончательно расплавленного состояния, тигель с помощью щипцов нужно постараться как можно аккуратнее и скорее вынуть из печи . На поверхности жидкого вещества будет образована пленка, ее подвинуть к краю тигля, используя крюк из проволоки. Очищенный от пленки металл максимально быстро перелить в заранее подготовленную форму.
- Если муфельная печь отсутствует, осуществить плавку меди можно с применением обычной газовой горелки . Но тогда медь будет находиться в тесном контакте с воздухом, а сам процесс окисления пройдет значительно быстрее. Поэтому для предотвращения образования толстой пленки на поверхности металла, медь, когда она достигнет жидкого состояния, присыпают растолченным древесным углем.
- Расплавить медь и ее сплавы можно также с помощью горна . Для этого древесный уголь нужно хорошо раскалить и поместить на него тигель с металлом (предварительно измельчить медь). Для ускорения нагревательного процесса на уголь направить пылесос, включенный на режиме выдувания. Особое внимание стоит уделить наконечнику трубы. Она должна быть металлической, поскольку пластик расплавится под воздействием высокой температуры.
У чистой меди, в состав которой не входят другие соединения, достаточно плохая текучесть. Поэтому делать из нее сложное литье или мелкие детали не рекомендуется.
Тогда стоит использовать сплавы. Например, латунь, оттенок которой светлее остальных. Это говорит о том, что для ее плавления нужны менее высокие температуры.
Температура плавления латуни, бронзы и меди примерно одинаковая. Во всяком случае значения этой характеристики для всех трех данных цветных металлов находятся в одном узком диапазоне температур. Это обусловлено тем, что бронза и латунь являются сплавами меди, свойства которой в значительной степени влияют на их физические характеристики.
Для твердых кристаллических материалов, к коим относятся и металлы, состоящие из чистого (без примесей) вещества, температурой плавления является такой показатель их нагревания, при котором они переходят в другое состояние – жидкое. Причем при этой же температуре чистые вещества (металлы) и застывают. То есть для них такой показатель нагрева является температурой одновременно и плавления, и кристаллизации. А сами металлы, нагретые до температуры их плавления, могут находиться не только в жидком, но и твердом состоянии. Это зависит от того, продолжить подводить к ним дополнительное тепло или дать начать остывать.
Вообще, по достижении температуры плавления чистое вещество сначала все еще остается твердым. Если продолжить нагрев, то оно станет жидким. Но температура вещества не будет повышаться (меняться) до тех пор, пока оно все полностью не расплавится в рассматриваемой системе (изделии, теле). А когда расплавленное вещество остывает до температуры кристаллизации (плавления), то оно сначала все еще остается жидким. И только если начать дополнительное отведение от него тепла, тогда оно станет переходить в кристаллическое твердое состояние (застывать). Но температура вещества, опять же, не будет меняться (понижаться), пока оно полностью не затвердеет.
У смесей веществ (в том числе и у различных сплавов металлов) нет температуры плавления/кристаллизации. Они совершают переход из одного состояния в другое (из твердого в жидкое и обратно) в некотором определенном интервале степени своего нагрева, граничные значения диапазона которого имеют соответствующее название. Температуру, при которой смеси веществ и сплавы металлов начинают переходить в жидкую фазу (или полностью затвердевают), называют “точкой солидуса”. Степень нагрева, при котором происходит полное расплавление (или начинается кристаллизация при остывании), называют “точкой ликвидуса”. Но в обиходе чаще говорят: температура солидуса и ликвидуса.
Точно замерить эти температуры как для смесей веществ, так и для сплавов металлов невозможно. Их определяют по специальным расчетным методикам, в которых учитывается точное процентное соотношение в смеси каждого элемента и ряд других параметров.
То есть относительно рассматриваемых металлов можно сделать следующие выводы. Температура плавления есть . Причем, только у чистой. У всех остальных металлов (латуни, бронзы и различных марок меди) ее нет, а есть температуры солидус и ликвидус. Для латуни и бронзы это так, потому что они являются сплавами меди, в которых в зависимости от марки добавлены различные легирующие добавки (другие металлы или иные вещества) и еще есть какие-то примеси. А производимые металлургической промышленностью для различных нужд имеют такие характеристики плавления, так как они тоже производятся легированными и с примесями. Чистую медь изготавливать нецелесообразно, и она уступает по своим характеристикам, требуемым для народного и промышленного ее использования, свойствам выпускаемых из нее марок.
Температура плавления металлов
Очевидно, что величина температуры ликвидус рассматриваемых металлов будет зависеть от их химического состава. В первую очередь от процентного содержания меди, так как ее в них всегда больше 50 %. И, соответственно, точка ликвидус марок этих металлов будет тем ближе к температуре плавления самой меди, чем ее больше в сплаве. А легирующие металлы или другие вещества и примеси, в зависимости от своего процентного содержания и температуры плавления, будут вносить соответствующую корректировку в сторону понижения либо повышения точки ликвидус у марок меди, бронзы и латуни. Понижать, если своя температура плавления ниже, чем у меди, и повышать, когда выше.
Так, ознакомившись, можно самому догадаться, в какую сторону будет отличаться у них точка ликвидус от температуры плавления чистой меди. Сам подскажет его влияние на эту и другие характеристики данного сплава. А даст возможность судить об отклонениях ее точки ликвидус от температуры плавления меди. С марками меди то же самое, но влияние легирующих добавок и примесей на их точку ликвидус будет рассмотрено отдельно ниже.
Температура плавления чистой меди – 1084,5 °C. А выпускаемые марки меди содержат ничтожно малое по отношению к самому этому металлу количество других веществ. Такое, что даже легирующие элементы, как, например, серебро и никель, наравне с прочими “случайными” веществами, относят в составе марок меди к примесям. Самого этого металла – от 99,93 до 99,99 %. И поэтому точки солидус и ликвидус выпускаемых марок меди очень близки к температуре плавления самого этого металла. Температуры полного расплавления в зависимости от марки: меди – 1083–1084 °C, латуни – 880–1050 °C, а бронзы – 900–1140 °C.
Изделия из меди
Температурные главным образом зависят от содержания меди и гораздо менее тугоплавкого цинка, являющегося в латунных сплавах основным легирующим элементом. А относительно бронзы следует отметить, что ее так называемые оловянные марки, с легированием оловом, полностью плавятся при температуре 900–950 °C, а не содержащие этот металл, безоловянные – при 950–1140 °C.
Прям совсем уж в домашних условиях плавить эти металлы, да еще потом и отливать из них какие-то заготовки, а тем более изделия, не получится. Надо будет сначала предварительно соответствующим образом подготовить подходящее помещение, обзавестись необходимым оборудованием и инструментом или смастерить самому что-то из требуемого для плавки и литья оснащения. И, разумеется, желательно поточнее выяснить характеристики сплава, с которым предполагается работать. А именно, его состав и температуру ликвидус.
Плавление в домашних условиях
А какие именно необходимо создать условия для работы, подготовить оборудование, оснащение и инструменты, а также технология плавки и литья перечислены и описаны в одной из публикаций сайта. Это статья: . Так как у этого сплава и у марок меди с латунью точки ликвидус близки по своим значениям, а другие свойства, влияющие на процессы плавки и литья, относительно сопоставимы, то и вся технология в кустарных условий для этих металлов идентична. То есть для меди и латуни можно воспользоваться инструкциями-рекомендациями по плавке бронзы из этой статьи.
Железом человек начал владеть (ковать, плавить) спустя несколько тысячелетий после освоения работ с медью. Первое самородное железо в виде комков было найдено на Ближнем Востоке в 3000 году до нашей эры. А металлургия железа, по мнению специалистов, возникла в нескольких местах планеты, разные народы осваивали этот процесс в разное время. Благодаря этому железо как материал для изготовления орудий труда, охоты и войны вытеснило камень и бронзу.
Первые процессы изготовления железа назывались сыродутными. Суть заключалась в том, что в яму засыпалась железная руда с древесным углем, который разжигали и плотно закупоривали, оставляя дутьевое отверстие, через которое подавался свежий воздух для дутья. В процессе такого нагрева температура плавления железа, конечно, не могла быть достигнута, получалась размягченная масса (крица), в которой находился шлак (зола от топлива, окислы руды и породы).
Далее полученную крицу несколько раз проковывали, удаляя шлак и другие не нужные включения, этот трудоемкий процесс производился по несколько раз, в результате чего из общей массы до финишной операции доходила пятая часть. С изобретением водяного колеса появилась возможность подавать значительное количество воздуха. Благодаря такому дутью температура плавления железа стала достижимой, появился металл в жидком виде.
Этим металлом был чугун, который не ковался, но было замечено, что он хорошо заполняет форму. Это были первые опыты по чугунному литью, которое с некоторыми усовершенствованиями и изменениями дошло до наших дней. Со временем был найден способ переработки чугуна в сварочное железо. Куски чугуна загружались с древесным углем, в ходе этого процесса чугун размягчался, происходило окисление примесей, в том числе углерода. В результате чего металл становился густым, температура плавления железа повышалась, т.е. получалось сварочное железо.
Таким образом, металлурги того времени смогли разделить единый процесс на две ступени. Этот двухступенчатый процесс в самой идее сохранился до настоящего времени, изменения в большей степени касаются появлению процессов, происходящих на втором этапе. Чистое железо или металл, имеющий минимум примесей, практического применения почти не имеет. Температура плавления железа по диаграмме железо – углерод находится в точке А, что соответствует 1535 градусам.
Температура кипения железа наступает при достижении отметки 3200 градусов.
На открытом воздухе железо со временем покрывается оксидной пленкой, во влажной среде появляется рыхлый слой ржавчины. Железо с момента его появления и по сегодняшний день является одним из главных металлов. Используется железо, главным образом, в виде сплавов, которые различаются по свойствам и составу.
При какой температуре плавится железо, зависит от содержания углерода и других компонентов, входящих в состав сплава. Наибольшее применение имеют углеродистые сплавы – чугун и сталь. Сплавы, содержащие углерод более 2%, называют чугуном, менее 2% относятся к стали. Чугун получают в доменных печах, путем переплава обогащенных на аглофабрике руд.
Сталь выплавляют в мартеновских, электрических и индукционных печах, в конвертерах.
В качестве шихты применяется металлический лом и чугун. Путем окислительных процессов из шихты удаляется лишний углерод и вредные примеси, а добавки легирующих материалов позволяют получить нужную марку стали. Для получения стали и других сплавов современные металлургия использует технологии электрошлакового переплава, вакуумные, электронно-лучевые и плазменные плавки.
В разработке находятся новые методы плавления стали, предусматривающие автоматизацию процесса и обеспечивающие получение высококачественного металла.
Научные разработки достигли такого уровня, когда можно получать материалы, выдерживающие вакуум и большое давление, большие температурные перепады, агрессивную среду, радиационные излучения и т.п.
Цены и новости на рынке химии
Новости и события
Австрийские ученые впервые экспериментально доказали существование новой экзотической формы льда и описали его кристаллическую структуру. До сих пор было известно 18 кристаллических форм льда, ко…
Претендент на Нобелевскую премию, профессор Университета Южной Калифорнии Валерий Фокин недавно стал действительным членом Американского института медицинской и биологической инженерии (AIMBE) и …
Российские ученые из РХТУ, НГТУ и ННГУ предложили проводить синтез аммиака с помощью гибридной технологии, сочетающей возможности мембранной очистки и современных абсорбентов. Они доказали, что т…
Компании обрабатывающей промышленности Казахстана обеспокоены. Материал, который они используют для выпуска упаковки, может подорожать. Обсуждается введение пошлины на ввоз в РК полимерного сырья…
АО “ВНИИХТ” (входит в научный дивизион “Росатома”) запущена линия по производству безгалогенных композиционных материалов. Производство налажено в рамках инвестиционного проекта “Производство пож…
Завод “Сибур-ПЭТФ” (г.Тверь, входит в СИБУР Холинг) по итогам работы в 2019 году продемонстрировал высокую эффективность и устойчивую динамику роста, наработав полиэтилентерефталат (ПЭТФ) в объем…
Информация
Новая экзотическая форма льда
О Голливуде, удаче, химии памяти и «микрофотографиях» клеток
Российские ученые предложили проводить синтез аммиака с помощью гибридной технологии
Новая экзотическая форма льда
О Голливуде, удаче, химии памяти и «микрофотографиях» клеток
Российские ученые предложили проводить синтез аммиака с помощью гибридной технологии
Каталог организаций и предприятий
Производство ртути. Директор: Устюгин Юрий Евгеньевич…
ООО “Мерком” специализируется на производстве ртути и ее соединений, оксида вольфрама, ферровольфрама, оксида сурьмы. Перерабатывает отходы металлического вольфрама. Принимает на утилизацию ртутьсодер…
ООО «Комплектсервис Групп» – Предприятие по переработке и утилизации ртутьсодержащих отходов предоставляет полный цикл услуг, начиная со сбора, транспортировкt, утилизации, заканчивая ликвидацией посл…
Фирма КОРЕФ предлагает изоляционные, облегченные, кислотоупорные, жаропрочные и огнеупорные бетоны готовые к эксплуатации. Мы изготавливаем бетоны на базе шамота, муллита, андалузита, шпинели, боксита…
КОМПЛЕКСНОЕ ОСНАЩЕНИЕ ПРОИЗВОДСТВЕННЫХ ЛАБОРАТОРИЙ предприятий металлургической, машиностроительной и др. отраслей промышленности. Анализаторы сырья и материалов (анализ металлов и сплавов, рудничного…
Уважаемые господа! Производственная компания ООО «ПАЛЬМИРА» предлагаем вам стабильные поставки высококачественной масло-жировой продукции. Маргарины (ГОСТ 32188-20013). Предназначены для использов…
Предложения на покупку и продажу продукции
Продаем новый танк-контейнер (контейнер-цистерна) Т14, футерованный полиэтиленом, для перевозки и хранения агрессивных химических веществ, кислот (кислота хлористоводородная ООН1789, кислота серная ОО…
Красная ртуть (Hg207Sb2), она же RM-20/20, она же Многофункциональный катализатор или Compound-20/20. Красная Ртуть , Оксистибат ртути (Sb2O7Hg2). КАС: 129-16-8 Химическая формула: Hg207Sb2 Молекул…
Безасбестовые уплотнительные листы серии GAMBIT AF – это совpеменные материалы, предназначенные для изготовления технических уплотнений (расcчитанных на широкий диапазон давлений и температур) при вза…
ООО Андалус реализует собственные объемы печного топлива темного, жидкое топливо для котельных отопления. Используется как топливо для дизельных котлов, а так же для любых котлов работающих на жидком …
ООО Андалус реализует собственные объемы печного топлива темного, жидкое топливо для котельных отопления. Используется как топливо для дизельных котлов, а так же для любых котлов работающих на жидком …
Продаем новый танк-контейнер (контейнер-цистерна) Т11 для химических грузов. Танк-контейнер имеет рамную конструкцию, оснащен устройствами верхнего налива и нижнего слива, предохранительным клапаном п…
Плотность, температура плавления и кипения простых веществ: таблицы для элементов
В таблице приводятся основные физические свойства простых веществ: плотность при температуре 20°С (в случае, если плотность измерена при другой температуре, последняя указана в скобках), температура плавления и температура кипения веществ в градусах Цельсия.
Указаны плотность и температуры плавления и кипения следующих простых веществ: азот N2, актиний Ac, алюминий Al, америций Am, аргон Ar, астат At, барий Ba, бериллий Be, бор B, бром Br, ванадий V, висмут Bi, водород H2, вольфрам W, гадолиний Gd, галлий Ga, гафний Hf, гелий He, германий Ge, гольмий Ho, диспрозий Dy, европий Eu, железо Fe, золото Au, индий In, йод (иод) J, иридий Ir, иттербий Yb, иттрий Y, кадмий Cd, калий K, кальций Ca, кислород O2, озон O3, кобальт Co, кремний Si, криптон Kr, ксенон Xe, кюрий Cm, лантан La, литий Li, лютеций Lu, магний Mg, марганец Mn, медь Cu, молибден Mo, мышьяк As, натрий Na, неодим Nd, неон Ne, нептуний Np, никель Ni, ниобий Nb, олово Sn, осмий Os, палладий Pd, платина Pt, плутоний Pu, полоний Po, празеодим Pr, прометий Pm, протактиний Pa, радий Ra, радон Rn, рений Re, родий Rh, ртуть Hg, рубидий Rb, рутений Ru, самарий Sm, свинец Pb, селен Se, сера S, серебро Ag, скандий Sc, стронций Sr, сурьма Sb, таллий Tl, тантал Ta, теллур Te, тербий Tb, технеций Tc, титан Ti, торий Th, тулий Tu, углерод C (алмаз, графит), уран U, фосфор P (белый, красный), франций Fr, фтор F, хлор Cl, хром Cr, цезий Cs, церий Ce, цинк Zn, цирконий Zr, эрбий Er.
Следует отметить, что плотность веществ в таблице выражена в размерности кг/м3 со множителем 103. В таблице можно выделить вещества (химические элементы) с минимальной и максимальной плотностью. Наименьшей плотностью из химических элементов обладают газы — например, плотность водорода равна всего 0,089 кг/м3 — это самый легкий газ на планете. Из тяжелых элементов высокой плотностью отличаются вольфрам — его плотность 19,3·103 кг/м3, уран, нептуний, осмий и другие металлы.
Цифры в скобках означают, что вещество при данной температуре разлагается. Сокращения: г. — газ, ж. — жидкость, тв. — твердое вещество, возг. — возгоняется, ромб. — ромбическая структура.
По данным таблицы можно выделить вещества, обладающие минимальной и максимальной температурой плавления и кипения. Самую низкую температуру плавления имеет химический элемент гелий — его температура плавления равна минус 272,2 °С. Гелий также обладает и самой низкой температурой кипения.
Самую высокую температуру плавления среди простых веществ имеет такой химический элемент, как углерод в виде графита. Он начинает плавиться при температуре 3600°С. Другая модификация углерода — алмаз также относится к тугоплавким веществам с температурой плавления 3500°С.
Самую высокую температуру кипения имеет элемент кадмий, он кипит при температуре не ниже 7670°С, хотя начинает плавиться всего лишь при 321°С.
Атомная масса и плотность простых веществ
В таблице приведена атомная масса и плотность следующих химических элементов: азот ,актиний, алюминий, америций, аргон, астат, барий, бериллий, берклий, бор, бром, ванадий, висмут, водород, вольфрам, гадолиний, галлий, гафний, гелий, германий, гольмий, диспрозий, европий, железо, золото, индий, йод, иридий, иттербий, иттрий, кадмий, калий, калифорний, кальций, кислород, кобальт, кремний, криптон, ксенон, кюрий, лантан, литий, лютеций, магний, марганец, медь, менделевий, молибден, мышьяк, натрий, неодим, неон, нептуний, никель, ниобий, олово, осмий, палладий, платина, плутоний, полоний, празеодим, прометий, протактиний, радий, радон, рений, родий, ртуть, рубидий, рутений, самарий, свинец, селен, сера, серебро, скандий, стронций, сурьма, таллий, тантал, теллур, тербий, технеций, титан, торий, тулий, углерод (графит, алмаз), уран, фермий, фосфор, франций, фтор, хлор, хром, цезий, церий, цинк, цирконий, эйнштейний, эрбий.
Указанные значения плотности соответствуют плотности веществ при температуре 20°С и атмосферном давлении, за исключением тех случаев, когда в скобках указана другая температура.
Плотность элементов дана в размерности тонна на кубометр. Например, плотность жидкого азота при температуре -195,8°С равна 0,808 т/м3 или 808 кг/м3; плотность хлора в газообразном состоянии равна 3,214 кг/м3, жидкого — 1557 кг/м3. Значения плотности веществ приведены для их естественного молекулярного и агрегатного состояний при указанной температуре.
Источники:
1. Писаренко В.В. Справочник лаборанта-химика. Справ. пособие для проф.-техн. учебн. заведений. М., «Высшая школа», 1970. — 192 стр. с илл.
2. Физические величины. Справочник. А.П. Бабичев, Н.А. Бабушкина, А.М. Братковский и др.; Под ред. И.С. Григорьева, Е.З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
Точка плавления, точка замерзания, точка кипения
Точка плавления, точка замерзания, Температура кипения
Температура плавления и замерзания Путевая точка
Чистые кристаллические твердые вещества имеют характеристическую температуру плавления , температура, при которой твердое вещество плавится и превращается в жидкость. Переход между твердым телом а жидкость настолько острая для небольших образцов чистого вещества, что точки плавления могут быть измеренным до 0.1 o C. Температура плавления, например, твердого кислорода составляет -218,4 o С.
Жидкости имеют характерную температуру, при которой они превращаются в твердые вещества, известную как их точка замерзания . Теоретически температура плавления твердого тела должна быть то же, что и точка замерзания жидкости. На практике небольшие различия между этими количества можно наблюдать.
Трудно, если не невозможно, нагреть твердое тело выше его точки плавления, потому что тепло, которое входит в твердое тело при его температуре плавления, используется для преобразования твердого вещества в жидкость.Однако возможно охлаждение некоторых жидкостей до температур ниже их точки замерзания. точки, не образуя твердого тела. Когда это сделано, жидкость называется переохлажденной .
Пример переохлажденной жидкости может быть получен путем нагревания твердого ацетата натрия. тригидрат (NaCH 3 CO 2 3 H 2 O). Когда это твердое вещество тает, ацетат натрия растворяется в воде, которая была захвачена кристаллом, с образованием раствора. Когда раствор остынет до комнатной температуры, он должен затвердеть.Но часто этого не происходит. Если в жидкость добавляется небольшой кристалл тригидрата ацетата натрия, однако содержимое колбы затвердевают в течение нескольких секунд.
Жидкость может переохлаждаться из-за того, что частицы твердого тела упакованы в регулярная структура, характерная для данного вещества. Что-нибудь из этого твердые вещества образуются очень легко; другие нет. Некоторым нужна частица пыли или затравочный кристалл, действовать как место, на котором кристалл может расти. Для образования кристаллов натрия тригидрат ацетата, ионы Na + , ионы CH 3 CO 2 – , и молекулы воды должны собраться вместе в правильной ориентации.Это сложно для эти частицы организуются, но затравочный кристалл может обеспечить основу для что правильное расположение ионов и молекул воды может расти.
Потому что трудно нагреть твердые тела до температур выше их точек плавления, и поскольку чистые твердые вещества имеют тенденцию плавиться в очень небольшом диапазоне температур, точки плавления часто используется для идентификации соединений. Мы можем различать три известных сахара как глюкоза ( MP = 150 o C), фруктоза ( MP = 103-105 o C) и сахарозы ( MP = 185-186 o C), для например, путем определения точки плавления небольшого образца.
Измерения температуры плавления твердого тела также могут предоставить информацию о чистота вещества. Чистые кристаллические твердые вещества плавятся в очень узком диапазоне температуры, тогда как смеси плавятся в широком диапазоне температур. Смеси также склонны к плавятся при температурах ниже точек плавления чистых твердых веществ.
Точка кипения
Когда жидкость нагревается, она в конечном итоге достигает температуры, при которой пар давление достаточно велико, чтобы внутри тела жидкости образовывались пузырьки.Эта температура называется точкой кипения . Как только жидкость закипит, температура остается постоянной до тех пор, пока вся жидкость не превратится в газ.
Нормальная температура кипения воды составляет 100 o C. Но если вы попытаетесь приготовить яйцо в кипящей воды во время кемпинга в Скалистых горах на высоте 10 000 футов, вы обнаружит, что яйцо готовится дольше, потому что вода кипит только при температуре 90 o C на этой высоте.
Теоретически нельзя нагревать жидкость до температуры выше нормальной. точка кипения. Однако до того, как микроволновые печи стали популярными, использовались скороварки. чтобы сократить время приготовления пищи. В обычной скороварке вода может оставаться жидкостью при температурах до 120 o C, а пища готовится в меньше одной трети обычного времени.
Чтобы объяснить, почему вода закипает при температуре 90 o C в горах и 120 o C в скороварку, даже если нормальная температура кипения воды составляет 100 o C, мы надо понимать, почему закипает жидкость.По определению жидкость закипает, когда пар давление газа, выходящего из жидкости, равно давлению, оказываемому на жидкость в окружающей среде, как показано на рисунке ниже.
| Жидкости кипят, когда давление их паров равно давлению, оказываемому на жидкость своим окружением. |
Нормальная температура кипения воды составляет 100 o C, потому что это температура при котором давление пара воды составляет 760 мм рт. ст., или 1 атм.В нормальных условиях, когда давление атмосферы примерно 760 мм рт. ст., вода закипает при температуре 100 o C. На высоте 10 000 футов над уровнем моря атмосферное давление составляет всего 526 мм рт. На этих над уровнем моря вода закипает, когда давление ее паров составляет 526 мм рт. ст., что происходит при температуре из 90 o C.
Скороварки оснащены клапаном, который позволяет выходить газу при повышении давления. внутри банка превышает некоторую фиксированную стоимость. Этот клапан часто устанавливается на 15 фунтов на квадратный дюйм, что означает что водяной пар внутри горшка должен достичь давления 2 атм, прежде чем он сможет уйти.Поскольку вода не достигает давления пара 2 атм, пока температура не достигнет 120 o C, он кипит в этом контейнере при 120 o C.
Жидкости часто закипают неравномерно, или поднимает . Они имеют тенденцию натыкаться, когда есть нет ли царапин на стенках емкости, где могут образоваться пузыри. Натыкаясь легко предотвратить, добавив в жидкость несколько кипящих стружек, которые обеспечивают грубую поверхность, на которой могут образовываться пузырьки. При варке чипсов практически все на поверхности этих стружек образуются пузыри, которые поднимаются сквозь раствор.
Точка плавления | Химия для неосновных
Цели обучения
- Определите точку плавления.
- Опишите процесс движения частиц при плавлении.
- Опишите силы, влияющие на температуру плавления материала.
Примеры
Вы когда-нибудь катались на коньках?
Зимой многие люди считают снег и лед прекрасными.Им нравится кататься на лыжах или коньках. Другие не считают это время года таким веселым. Когда тает снег, дороги становятся очень неряшливыми и грязными. Эти люди с нетерпением ждут весны, когда уже не будет снега и льда, а погода станет теплее.
Точка плавления
Твердые тела похожи на жидкости в том, что оба являются конденсированными состояниями с частицами, которые расположены гораздо ближе друг к другу, чем частицы газа. Однако, в то время как жидкости жидкие, твердые тела – нет. Частицы большинства твердых веществ плотно упакованы и упорядочены.Движение отдельных атомов, ионов или молекул в твердом теле ограничено колебательным движением вокруг фиксированной точки. Твердые тела почти полностью несжимаемы и являются наиболее плотными из трех состояний материи.
Когда твердое тело нагревается, его частицы вибрируют быстрее, поскольку твердое тело поглощает кинетическую энергию. В конце концов, организация частиц внутри твердой структуры начинает разрушаться, и твердое тело начинает плавиться. Температура плавления – это температура, при которой твердое вещество превращается в жидкость.В точке плавления разрушительные колебания частиц твердого тела преодолевают силы притяжения, действующие внутри твердого тела. Как и в случае с температурами кипения, температура плавления твердого вещества зависит от силы этих сил притяжения. Хлорид натрия (NaCl) – это ионное соединение, состоящее из множества сильных ионных связей. Хлорид натрия плавится при 801 ° C. Лед (твердый H 2 O) представляет собой молекулярное соединение, молекулы которого удерживаются вместе водородными связями. Хотя водородные связи являются самыми сильными из межмолекулярных сил, прочность водородных связей намного меньше, чем у ионных.Температура плавления льда 0 ° C.
Точка плавления твердого вещества такая же, как точка замерзания жидкости. При этой температуре твердое и жидкое состояния вещества находятся в равновесии. Для воды это равновесие происходит при 0 ° C.
Мы склонны думать о твердых телах как о материалах, которые тверды при комнатной температуре. Однако все материалы имеют ту или иную температуру плавления. Газы становятся твердыми при очень низких температурах, а жидкости также становятся твердыми, если температура достаточно низкая.В таблице , приведенной ниже, приведены температуры плавления некоторых распространенных материалов.
| Материал | Точка плавления (° C) |
| водород | -259 |
| кислород | -219 |
| диэтиловый эфир | -116 |
| этанол | -114 |
| вода | 0 |
| чистое серебро | 961 |
| чистое золото | 1063 |
| утюг | 1538 |
Основные выводы
Резюме
- Точка плавления – это температура, при которой твердое вещество превращается в жидкость.
- Межмолекулярные силы оказывают сильное влияние на температуру плавления.
Упражнения
Практика
Вопросы
Воспользуйтесь ссылкой ниже, чтобы ответить на следующие вопросы
http://chemwiki.ucdavis.edu/Organic_Chemistry/Organic_Chemistry_With_a_Biological_Emphasis/Chapter__2%3a_Introduction_to_organic_structure_and_bonding_II/Section_2.4%3a_Solubility%2c_Point_points_points
- С какой степенью точности можно измерить температуру плавления?
- Как мы можем использовать данные о температуре плавления, чтобы идентифицировать соединение?
- Как мы можем использовать точки плавления для оценки чистоты соединения?
Упражнения
Обзор
Вопросы
- Определите точку плавления.
- Что происходит, когда материал плавится?
- Ожидаете ли вы, что этан (C 2 H 6 ) будет иметь более высокую или более низкую температуру плавления, чем вода? Поясните свой ответ.
Глоссарий
- несжимаемый: Невозможно сжать.
- точка плавления: Температура, при которой твердое вещество превращается в жидкость.
- колебательное движение: Возвратно-поступательное движение.
Точки плавления металлов | Металл Супермаркеты
Металлы известны своей способностью противостоять экстремальным условиям. Тяжелые нагрузки, непрерывная езда на велосипеде, сильные удары, едкая среда и даже высокие температуры. Печи, двигатели внутреннего сгорания, реактивные двигатели, форсунки зажигания, высокоскоростное оборудование и выхлопные системы постоянно подвергаются воздействию температур, которые могут вызвать плавление некоторых типов металлов. При выборе металла для высокотемпературного применения необходимо оценить несколько различных температурных точек, и одна из наиболее важных температур, которую необходимо знать, – это температура плавления металла.
Что такое температура плавления металлов?
Температура плавления металла, более известная с научной точки зрения как точка плавления, – это температура, при которой металл начинает превращаться из твердой фазы в жидкую фазу. При температуре плавления твердая фаза и жидкая фаза металла находятся в равновесии. Как только эта температура будет достигнута, к металлу можно будет непрерывно подводить тепло, однако это не приведет к повышению общей температуры. Когда металл полностью перейдет в жидкую фазу, дополнительное тепло снова продолжит повышать температуру металла.
Почему важна температура плавления металла?
Есть много важных температур, которых достигает металл, когда он нагревается либо в процессе обработки металла, либо в результате нанесения, но температура плавления металла является одной из самых важных.
Одна из причин, по которой температура плавления так важна, заключается в отказе компонентов, который может произойти, когда металл достигнет своей температуры плавления. Разрушение металла может произойти до точки плавления, но когда металл достигает температуры плавления и становится жидкостью, он больше не будет служить своему назначению.Например, если компонент печи начинает плавиться, печь больше не будет работать, если компонент достаточно важен. Если топливная форсунка реактивного двигателя расплавится, отверстия засорятся, и двигатель станет бесполезным. Важно отметить, что другие типы разрушения металла, такие как трещины, вызванные ползучестью, могут произойти задолго до достижения температуры плавления, и необходимо заранее изучить влияние различных температур, которым будет подвергаться металл.
Другая причина, по которой температура плавления металла так важна, заключается в том, что металлы наиболее пластичны, когда они находятся в жидком состоянии.Металлы нагреваются до температуры плавления для многих различных производственных процессов. Плавка, сварка плавлением и литье требуют, чтобы металлы были жидкими. При выполнении производственного процесса, в котором металл будет плавиться, важно знать температуру, при которой это произойдет, чтобы можно было выбрать подходящие материалы для используемого оборудования. Например, сварочный пистолет должен выдерживать внешнее тепло от электрической дуги и расплавленного металла.Оборудование для литья, такое как штампы, должно иметь более высокую температуру плавления, чем отливаемый металл.
Температуры плавления обычных металлов
Это температуры плавления обычных металлов:
- Алюминий: 660 ° C (1220 ° F)
- Латунь: 930 ° C (1710 ° F)
- Алюминиевая бронза *: 1027-1038 ° C (1881-1900 ° F)
- Хром: 1860 ° C (3380 ° F)
- Медь: 1084 ° C (1983 ° F)
- Золото: 1063 ° C (1945 ° F)
- Инконель *: 1390-1425 ° C (2540-2600 ° F)
- Чугун: 1204 ° C (2200 ° F)
- Свинец: 328 ° C (622 ° F)
- Молибден: 2620 ° C (4748 ° F)
- Никель: 1453 ° C (2647 ° F)
- Платина: 1770 ° C (3218 ° F)
- Серебро: 961 ° C (1762 ° F)
- Углеродистая сталь *: 1425-1540 ° C (2597-2800 ° F)
- Нержавеющая сталь *: 1375-1530 ° C (2500-2785 ° F)
- Титан: 1670 ° C (3038 ° F)
- Вольфрам: 3400 ° C (6152 ° F)
- Цинк: 420 ° C (787 ° F)
* Сплавы содержат более одного элемента, поэтому их температура плавления – это диапазон, который зависит от состава сплава.
Metal Supermarkets – крупнейший в мире поставщик мелкосерийного металла с более чем 90 обычными магазинами в США, Канаде и Великобритании. Мы эксперты по металлу и обеспечиваем качественное обслуживание клиентов и продукцию с 1985 года.
В Metal Supermarkets мы поставляем широкий ассортимент металлов для различных областей применения. В нашем ассортименте: нержавеющая сталь, легированная сталь, оцинкованная сталь, инструментальная сталь, алюминий, латунь, бронза и медь.
Наша горячекатаная и холоднокатаная сталь доступна в широком диапазоне форм, включая пруток, трубы, листы и пластины.Мы можем разрезать металл в точном соответствии с вашими требованиями.
Посетите одно из наших 90+ офисов в Северной Америке сегодня.
Точка плавления – обзор
Экологическая судьба и перенос
HMX, более мощное взрывчатое вещество, чем тринитротолуол (TNT), использовалось как часть спускового механизма для атомного (делительного) оружия, как компонент в пластических взрывчатых веществах и в ракетном топливе [2,3]. Производство соединения ограничено одним местом в Соединенных Штатах (Армейский завод боеприпасов Холстона (AAP) в Кингспорте, штат Теннесси), где, как сообщалось, до 45 фунтов в день выбрасывалось в окружающую среду. водные объекты в сбрасываемых сточных водах производства и переработки.Концентрации октогена до 3,36 миллиграммов на литр (мг / л) были обнаружены в стоках с установки Холстона [4]. Выбросы октогена также имели место на объектах, где собираются, хранятся или испытываются боеприпасы. Например, на некоторых армейских объектах в почве сообщалось о концентрациях до 5700 миллиграммов на килограмм (мг / кг) [4].
Физико-химические свойства октогена, влияющие на судьбу и перенос соединения в окружающей среде, перечислены в таблице 5.1.
Таблица 5.1. Краткое изложение физико-химических свойств HMX
| Номер CAS | 2691-41-0 | |||
| Молекулярный вес | 296,16 | |||
| Цвет | Бесцветный | |||
| Кристаллическое твердое вещество | ||||
| Точка плавления | 276 – 280 ° C | |||
| Точка кипения | Нет данных | |||
| Запах | Нет данных | |||
| Растворимость в воде 5 – Растворимость в воде 5 -63 мг / л при 20-25 ° C; растворим в ацетоне, циклогексаноне, уксусном ангидриде, диметилсульфоксиде | ||||
| Коэффициенты распределения: | ||||
| Log K ow | 0,06, 0,26 | |||
| Log K 8 | Log K 8 | давление при 25 ° C | 3,33 × 10 – 14 мм рт. ст. | |
| Константа закона Генри при 25 ° C | 2,60 × 10 -15 атм. | 1 частей на миллион = 12.11 мг / м 3 | ||
| 1 мг / м 3 = 0,083 частей на миллион |
Источники: ATSDR [2], Агентство по охране окружающей среды США [3], Talmage et al . [4].
Давление пара и константа закона Генри достаточно низкие (3,33 × 10 –14 мм рт. Ст. И 2,60 × 10 –15 атм. 3 / моль, соответственно), что указывает на маловероятность попадания октогена в воздух. как пар. Однако воздушное рассеивание соединения при прилипании к почве, частицам пыли или некоторым альтернативным средствам аэрозолизации является вероятным механизмом, с помощью которого соединение может быть выброшено в атмосферу [2].HMX имеет низкий коэффициент распределения органического углерода почвы в бревнах, равный 0,54, и обладает потенциалом высокой подвижности в почве, которая может вымываться в грунтовые воды. Например, октоген был обнаружен в грунтовых водах на территории Луизианской AAP в концентрациях до 4,2 мг / л [4].
Фотолиз, по-видимому, является доминирующим процессом разложения октогена в окружающей среде, при этом константа скорости фотолиза первого порядка, по сообщениям, составляет 0,15 дня – 1 [3]. Это говорит о том, что концентрация водного октогена 0.Период полувыведения 5 мг / л при воздействии естественного солнечного света составляет от 4 до 5 дней. Основные продукты этого процесса включают нитрат, нитрит и формальдегид. Напротив, процессы биодеградации / биотрансформации с участием бактерий или другой микрофлоры происходят чрезвычайно медленно, хотя образование 1,1-диметилгидразина было продемонстрировано в результате анаэробной деградации [3].
Точки плавления | Протокол
Точки плавления в органической химии
Точка плавления соединения – это температура, при которой твердая фаза переходит в жидкую фазу при стандартном давлении в 1 атмосферу.Температура плавления соединения – это физическое свойство, такое как растворимость, плотность, цвет и электроотрицательность, которые могут использоваться для идентификации соединения. Определение точной температуры, при которой соединение начинает плавиться, является сложной задачей; по этой причине температура плавления соединений указывается в виде диапазона. Нижний предел диапазона температур плавления – это температура, при которой наблюдаются первые капли жидкости. Верхний предел диапазона – это температура, при которой вся твердая фаза переходит в жидкую фазу.В литературе существуют справочные руководства с принятыми значениями, которые используются для идентификации соединений.
Влияние межмолекулярных сил на точки плавления
Одним из основных факторов, влияющих на точку плавления соединения, является тип межмолекулярных сил, существующих внутри соединения. Межмолекулярные силы являются либо притягивающими, либо отталкивающими между молекулами соединения. В твердой фазе молекулы соединения образуют организованную решетчатую структуру, поскольку молекулы упакованы близко друг к другу.Существует три основных типа межмолекулярных сил:
- Водородная связь – Водородная связь – это тип межмолекулярной силы, которая возникает из-за сил притяжения между электроотрицательным кислородом и атомом водорода. Следовательно, для существования такого типа межмолекулярной силы соединение должно содержать кислород и водород. Следовательно, соединения, содержащие гидроксильные группы, такие как спирты, легко образуют водородные связи. Внутри гидроксильной группы образуется диполь, поскольку более электроотрицательный кислород притягивает к себе электронную плотность, заставляя кислород иметь частичный отрицательный заряд.Это также оставляет водород с частичным положительным зарядом. Близлежащие электроотрицательные атомы кислорода притягиваются к частичному положительному заряду, образуя водородную связь. Из трех типов межмолекулярных сил водородная связь является самой сильной.
- Диполь-дипольные взаимодействия – второй по силе тип межмолекулярных сил, диполь-дипольные взаимодействия образуются в молекулах, которые содержат электроотрицательные атомы, такие как кислород, азот, и любые галогениды, такие как хлор и фтор. Например, молекула углеводорода, содержащая фтор, будет образовывать диполь-дипольные взаимодействия.Как? Электроотрицательный атом фтора притягивает к себе электронную плотность, заставляя его иметь частичный отрицательный заряд. Связующий атом, углерод, теряет часть этой электронной плотности и, таким образом, приобретает частичный отрицательный заряд. Это образует временный диполь на связи фтор-углерод. По мере притяжения противоположных зарядов частично отрицательный фтор притягивается к частично положительному углероду другой соседней молекулы, образуя диполь-дипольное взаимодействие.
- Лондонские дисперсионные силы – Этот тип взаимодействия является формой сил Ван-дер-Ваальса и присутствует во всех соединениях.Лондонские дисперсионные силы – самый слабый тип межмолекулярных сил. Подобно диполь-дипольным взаимодействиям, происходит перераспределение электронной плотности вокруг молекулы, вызывающее образование временных зарядов. В отличие от диполь-дипольных взаимодействий диполи, образованные лондонскими дисперсионными силами, очень слабые и минимальные. Например, неполярные соединения, такие как метан, этан, пентан и октан, взаимодействуют посредством лондонских дисперсионных сил. Площадь поверхности и длина молекулы определяют силу сил притяжения, так что соединения с большей площадью поверхности имеют большие силы лондонской дисперсии, чем соединения меньшего размера.Следовательно, октан будет иметь более сильные силы лондонской дисперсии, чем метан.
Каждый тип межмолекулярной силы имеет разную силу притяжения. Следовательно, соединениям, содержащим водородные связи, требуется больше энергии для разрыва притяжения между молекулами, чем неполярным соединениям, которые имеют только силы дисперсии Лондона. Таким образом, наличие водородных связей увеличивает температуру плавления соединения.
Влияние примесей на температуру плавления
Приведенные в литературе значения температур плавления предполагают, что у вас есть чистый образец рассматриваемого соединения.Часто в лаборатории или в неизвестных образцах исследуемые образцы не являются чистыми соединениями. Примеси вызывают наблюдаемую температуру плавления смеси ниже, чем фактическая температура плавления чистого соединения. Наблюдаемый диапазон больше, чем у чистого вещества.
В чистом соединении твердое вещество состоит из однородной и упорядоченной структуры, и для перехода соединения в жидкую фазу требуется определенная температура, чтобы разрушить структуру. В смеси, содержащей примеси, твердая фаза имеет неорганизованную структуру.Это требует гораздо меньше энергии для перехода в жидкую фазу, что снижает температуру плавления. Это явление известно как понижение температуры плавления. Чем больше примесей в образце, тем шире диапазон температур плавления и тем ниже температура плавления.
Справочник по точкам плавления элементов – Angstrom Sciences
Справочник по точкам плавления элементов – Angstrom SciencesПерейти к навигации
| Символы | Точка плавления | Имя | # | ||
|---|---|---|---|---|---|
| 0.95 К | -272,05 ° С | -458 ° F | Гелий | He | 2 |
| 14.025 К | -258,975 ° С | -434 ° F | Водород | H | 1 |
| 24,553 К | -248,447 ° С | -415,205 ° F | Неон | Ne | 10 |
| 50,35 К | -222,65 ° С | -368,77 ° F | Кислород | O | 8 |
| 53.48 К | – 219,52 ° С | -363,14 ° F | Фтор | F | 9 |
| 63,14 К | -209,86 ° С | -345,75 ° F | Азот | N | 7 |
| 83,81 К | -189,19 ° С | -308,54 ° F | Аргон | Ar | 18 |
| 115,78 К | -157,22 ° С | -251 ° F | Криптон | Кр | 36 |
| 161.3 К | -111,7 ° С | -169,1 ° F | Ксенон | Xe | 54 |
| 172,16 К | -100,84 ° С | -149,51 ° F | Хлор | Класс | 17 |
| 202 К | -71 ° С | -96 ° F | Радон | Rn | 86 |
| 234,28 К | -38,72 ° С | -37,7 ° F | Меркурий | Hg | 80 |
| 265.9 К | -7,1 ° С | 19,2 ° F | Бром | Br | 35 |
| 300 К | 27 ° С | 81 ° F | Франций | Fr | 87 |
| 301,55 К | 28,55 ° С | 83,39 ° F | Цезий | CS | 55 |
| 302,9 К | 29,9 ° С | 85,8 ° F | Галлий | Ga | 31 |
| 312.64 К | 39,64 ° С | 103,35 ° F | Рубидий | руб. | 37 |
| 317,3 К | 44,3 ° С | 111,7 ° F | фосфор | -П | 15 |
| 336,35 К | 63,35 ° С | 146,03 ° F | Калий | К | 19 |
| 371 К | 98 ° С | 208 ° F | Натрий | Na | 11 |
| 386.7 К | 113,5 ° С | 236,3 ° F | Йод | I | 53 |
| 388,36 К | 115,36 ° С | 239,65 ° F | Сера | S | 16 |
| 429,76 К | 156,76 ° С | 314,17 ° F | Индий | В | 49 |
| 453,7 К | 180,7 ° С | 357,3 ° F | Литий | Li | 3 |
| 494 К | 221 ° С | 430 ° F | Селен | SE | 34 |
| 505.06 К | 232,06 ° С | 449,71 ° F | Олово | Sn | 50 |
| 527 К | 254 ° С | 489 ° F | Полоний | Po | 84 |
| 544,52 К | 271,52 ° С | 520,74 ° F | висмут | Bi | 83 |
| 575 К | 302 ° С | 576 ° F | Астатин | в | 85 |
| 577 К | 304 ° С | 579 ° F | Таллий | Tl | 81 |
| 594.18 К | 321,18 ° С | 610,12 ° F | Кадмий | Cd | 48 |
| 600,6 К | 327,6 ° С | 621,7 ° F | Свинец | Пб | 82 |
| 692,73 К | 419,73 ° С | 787,51 ° F | Цинк | Zn | 30 |
| 722,65 К | 449,65 ° С | 841,37 ° F | Теллур | Te | 52 |
| 903.9 К | 630,9 ° С | 1167,6 ° F | Сурьма | Сб | 51 |
| 913 К | 640 ° С | 1184 ° F | Плутоний | Pu | 94 |
| 913 К | 640 ° С | 1184 ° F | Нептуний | Np | 93 |
| 922 К | 649 ° С | 1200 ° F | Магний | мг | 12 |
| 933.25 К | 660,25 ° С | 1220,45 ° F | Алюминий | Al | 13 |
| 973 К | 700 ° С | 1292 ° F | Радий | Ra | 88 |
| 1002 К | 729 ° С | 1344 ° F | Барий | Ba | 56 |
| 1042 К | 769 ° С | 1416 ° F | Стронций | Sr | 38 |
| 1071 К | 798 ° С | 1468 ° F | Церий | CE | 58 |
| 1081 К | 808 ° С | 1486 ° F | Мышьяк | как | 33 |
| 1095 К | 822 ° С | 1512 ° F | Европий | Eu | 63 |
| 1097 К | 824 ° С | 1515 ° F | Иттербий | УБ | 70 |
| 1112 К | 839 ° С | 1542 ° F | Кальций | Ca | 20 |
| 1133 К | 860 ° С | 1580 ° F | Эйнштейний | Es | 99 |
| 1173 К | 900 ° С | 1652 ° F | Калифорний | Cf | 98 |
| 1193 К | 920 ° С | 1688 ° F | Лантан | La | 57 |
| 1204 К | 931 ° С | 1708 ° F | Прометий | мкм | 61 |
| 1204 К | 931 ° С | 1708 ° F | Празеодим | Pr | 59 |
| 1210.4 К | 937,4 ° С | 1719,3 ° F | Германий | Ge | 32 |
| 1234 К | 961 ° С | 1762 ° F | Серебро | Ag | 47 |
| 1259 К | 986 ° С | 1807 ° F | Берклий | B K | 97 |
| 1267 К | 994 ° С | 1821 ° F | Америций | Am | 95 |
| 1289 К | 1016 ° С | 1861 ° F | Неодим | Nd | 60 |
| 1323 К | 1050 ° С | 1922 ° F | Актиний | Ac | 89 |
| 1337.58 К | 1064,58 ° С | 1948,24 ° F | Золото | Au | 79 |
| 1340 К | 1067 ° С | 1953 ° F | Кюрий | см | 96 |
| 1345 К | 1072 ° С | 1962 ° F | Самарий | см | 62 |
| 1357,6 К | 1084,6 ° С | 1984,3 ° F | Медь | Cu | 29 |
| 1405 К | 1132 ° С | 2070 ° F | Уран | U | 92 |
| 1517 К | 1244 ° С | 2271 ° F | Марганец | Mn | 25 |
| 1551 К | 1278 ° С | 2332 ° F | Бериллий | Be | 4 |
| 1585 К | 1312 ° С | 2394 ° F | Гадолиний | Gd | 64 |
| 1630 К | 1357 ° С | 2475 ° F | Тербий | Тб | 65 |
| 1683 К | 1410 ° С | 2570 ° F | Кремний | Si | 14 |
| 1685 К | 1412 ° С | 2574 ° F | Диспрозий | Ду | 66 |
| 1726 К | 1453 ° С | 2647 ° F | Никель | Ni | 28 |
| 1743 К | 1470 ° С | 2678 ° F | Гольмий | Ho | 67 |
| 1768 К | 1495 ° С | 2723 ° F | Кобальт | Co | 27 |
| 1795 К | 1522 ° С | 2772 ° F | Эрбий | Er | 68 |
| 1799 К | 1526 ° С | 2779 ° F | Иттрий | Y | 39 |
| 1808 К | 1535 ° С | 2795 ° F | Утюг | Fe | 26 |
| 1812 К | 1539 ° С | 2802 ° F | Скандий | Sc | 21 |
| 1818 К | 1545 ° С | 2813 ° F | Тулий | ТМ | 69 |
| 1825 К | 1552 ° С | 2826 ° F | Палладий | Pd | 46 |
| 1933 К | 1660 ° С | 3020 ° F | Титан | Ti | 22 |
| 1936 К | 1663 ° С | 3025 ° F | Лютеций | Лю | 71 |
| 2028 К | 1755 ° С | 3191 ° F | Торий | Чт | 90 |
| 2045 К | 1772 ° С | 3222 ° F | Платина | Pt | 78 |
| 2113 К | 1600 ° С | 2912 ° F | Протактиний | Па | 91 |
| 2125 К | 1852 ° С | 3366 ° F | Цирконий | Zr | 40 |
| 2130 К | 1857 ° С | 3375 ° F | Хром | Cr | 24 |
| 2175 К | 1902 ° С | 3456 ° F | Ванадий | В | 23 |
| 2239 К | 1966 ° С | 3571 ° F | Родий | Rh | 45 |
| 2473 К | 2200 ° С | 3992 ° F | Технеций | TC | 43 |
| 2500 К | 2227 ° С | 4041 ° F | Гафний | HF | 72 |
| 2523 К | 2250 ° С | 4082 ° F | Рутений | Ру | 44 |
| 2573 К | 2300 ° С | 4172 ° F | Бор | B | 5 |
| 2716 К | 2443 ° С | 4429 ° F | Иридий | Ir | 77 |
| 2741 К | 2468 ° С | 4474 ° F | Ниобий | Nb | 41 |
| 2890 К | 2617 ° С | 4743 ° F | молибден | Пн | 42 |
| 3269 К | 2996 ° С | 5425 ° F | Тантал | Ta | 73 |
| 3300 К | 3027 ° С | 5481 ° F | Осмий | Ос | 76 |
| 3453 К | 3180 ° С | 5756 ° F | Рений | Re | 75 |
| 3680 К | 3407 ° С | 6165 ° F | Вольфрам | Вт | 74 |
| 3773 К | 3500 ° С | 6332 ° F | Углерод | С | 6 |
Какие факторы влияют на температуру плавления?
Точка плавления – это температура, при которой твердое вещество превращается в жидкость.Теоретически точка плавления твердого вещества такая же, как точка замерзания жидкости – точка, при которой она превращается в твердое тело. Например, лед – это твердая форма воды, которая тает при 0 градусах Цельсия / 32 градусах Фаренгейта и переходит в жидкую форму. Вода при той же температуре замерзает и превращается в лед. Трудно нагреть твердые вещества до температур выше их точек плавления, поэтому определение точки плавления – хороший способ идентифицировать вещество.
TL; DR (слишком долго; не читал)
Молекулярный состав, сила притяжения и наличие примесей могут влиять на температуру плавления веществ.
Состав молекул
Когда молекулы плотно упакованы вместе, вещество имеет более высокую температуру плавления, чем вещество, молекулы которого плохо упаковываются. Например, симметричные молекулы неопентана имеют более высокую температуру плавления, чем изопентан, в котором молекулы плохо упаковываются. Размер молекулы также влияет на температуру плавления. Когда другие факторы равны, молекулы меньшего размера плавятся при более низких температурах, чем молекулы большего размера. Например, температура плавления этанола составляет -114.1 градус Цельсия / -173,4 градуса по Фаренгейту, а температура плавления более крупной молекулы этилцеллюлозы составляет 151 градус Цельсия / 303,8 градуса по Фаренгейту.
Макромолекулы имеют гигантские структуры, состоящие из множества атомов неметаллов, соединенных с соседними атомами ковалентными связями. Вещества с гигантской ковалентной структурой, такие как алмаз, графит и диоксид кремния, имеют чрезвычайно высокие температуры плавления, потому что несколько прочных ковалентных связей должны быть разорваны, прежде чем они смогут расплавиться.
Сила притяжения
Сильное притяжение между молекулами приводит к более высокой температуре плавления.Как правило, ионные соединения имеют высокие температуры плавления, потому что электростатические силы, связывающие ионы, – ион-ионное взаимодействие – являются сильными.